-
PM2.5 (空气动力当量直径小于或等于2.5 μm的颗粒物)是发生雾霾事件的主要原因[1 − 2],是各种潜在污染源如汽车尾气、工业生产和煤炭燃烧等排放污染物的混合物[3 − 4]. PM2.5不仅影响大气能见度[2],而且严重威胁到人类的健康,长期暴露于细颗粒物污染会增加呼吸道、心血管和肾脏疾病的风险[1,5],尤其是PM2.5中具有病理学和毒性的重金属元素,如Cr、As、Cd和Ni等对人体具有一定的致癌作用[6],过度积累会导致人体出现一系列疾病[7 − 8]. 随着经济的快速发展,中国的空气污染,特别是城市区域的空气污染,已经成为严重的环境问题[7 − 9],而且城区人为污染源(如机动车排放和化石燃料的燃烧)排放的污染物可通过区域或长距离传输对背景或高山地区的PM2.5产生影响[10].
近年来,国内外对PM2.5中元素的污染特征、生态风险和健康风险进行了大量研究[6,9,11],大多集中在人口密集的城市. 雷文凯等[6]研究了保定市PM2.5中重金属元素的健康风险,其中As和Cr存在致癌风险,且成人明显高于儿童. 何瑞东等[9]评价了郑州市大气PM2.5中重金属元素的生态风险和健康风险,Cd元素不仅生态风险极强,而且还存在致癌风险. Zhang等[11]对日本北九州PM2.5中重金属进行了生态风险和健康风险评估,Se是生态风险贡献最高的重金属,As既存在非致癌风险又有致癌风险. 国内在高山和背景地区的研究大多集中在PM2.5的质量浓度、化学特征和来源分析[12 − 14]. Zhang等[15]在夏季对中国青藏高原东北部青海湖景区PM2.5的研究,确定了其化学成分和主要来源. 苏彬彬等[16]研究结果显示武夷山夏季PM2.5浓度最低(15 μg·m−3),春季最高(31 μg·m−3). Qie等[12]在泰山顶部对PM2.5中微量元素的来源解析表明,煤炭燃烧和机动车排放是微量元素的主要排放源. 目前,对高山地区PM2.5中重金属的研究较少,特别是针对重金属的生态风险和健康风险评估方面的研究相对较少.
武当山位于湖北省西北部的十堰市,地处鄂、豫、渝、陕交界地带,属华中地区城市群区域大气本底,武当山海拔高度为1612 m,受到本地污染源的影响较小,主要受长距离输送或区域传输的影响,可以代表华中地区的大气污染的区域背景状况[16 − 18]. 本研究于2018年夏季在武当山开展PM2.5滤膜样品的采集和分析,采用富集因子法探讨18种金属元素(Na、K、Ca、Mg、Al、Fe、V、Cr、Mo、Cu、Zn、Mn、Ni、As、Se、Cd、Ba和Pb)的富集程度和污染水平,利用生态风险评估方法(NIRI)和美国环保署(EPA)开发的健康风险评价模型对武当山大气PM2.5中元素的潜在生态风险和呼吸吸入途径的健康风险做出评价. 通过研究武当山细颗粒物中有毒有害重金属对生态环境和人体健康的影响,可为研究华中地区大气重金属污染特征和健康影响提供科学参考,为华中地区大气重金属风险防控提供理论依据.
-
本研究采样点位于武当山山顶国家空气质量监测站(32°23'N,111°02'E,海拔高度862 m). 武当山位于国家5A级景区武当山国家森林公园内. 采样点布设于屋顶2层,离地高度约6 m,站点周边视野开阔,多丘陵和山地,且森林覆盖率高,远离当地的重工业排放和其他人为污染源,能客观反映武当山高山背景区域的大气环境状况.
-
武当山高山采样点使用TH-16A型天虹四通道环境空气颗粒物智能采样器,采样滤膜为Teflon滤膜(直径为47 mm,Millipore,America),采样日期为2018年6月3日至2018年6月30日,采样时段为每日10:00至次日09:00,每日采样时长为23 h,共采集有效样品数28个.
采样前后将滤膜放置在温度为(20±2.5)℃、相对湿度为50%±5%的恒温恒湿箱中平衡48 h,使用十万分之一分析天平(Sartorius,Germany)称量滤膜质量. 剪取1/2滤膜样品置于30 mL洗净的聚四氟乙烯消解罐中,加入消解溶液(0.2 mL HF、2 mL H2O2 和6 mL HNO3),常温预消解45 min,按照程序升温进行微波消解(低温升到120 ℃保持3 min,持续升温到170 ℃保持10 min,最后升到190 ℃保持50 min). 将消解液移至PET瓶,超纯水定容到100 mL. 采用电感耦合等离子体质谱仪(ICP-MS,Agilent 7800,America)测定样品中18种元素(K、Ca、Na、Mg、Al、Fe、V、Cr、Mo、Cu、Zn、Mn、Ni、As、Se、Cd、Ba和Pb)的含量[19]. 每10个样品进行1个空白膜,平行样品和标准样品分析. 平行样品分析需保证相对误差小于20%,标准样品回收率控制在80%—120%之间,以减小误差对实验的影响.
-
富集因子法是一种广泛用于研究PM2.5中元素的富集程度以及确定其来源是自然源还是人为源的方法[9,11]. 富集因子(EFi)的计算公式[11]为:
式中,Ci为研究元素的实测浓度,Cref为参比元素的背景浓度,单位为μg·m−3;(Ci/Cref)PM2.5和(Ci/Cref)soil分别为PM2.5样品和土壤背景中研究元素与参比元素的比值;由于Al在PM2.5中普遍存在,性质比较稳定,且人为污染较小,故本研究以Al为参比元素. 土壤背景中各元素浓度采用中国环境土壤背景值中的湖北省A层土壤元素背景值[20].
若元素EF值大于1000,说明这些元素为超富集水平,主要来自人为源;若元素EF值在100—1000之间,表明这些元素为高度富集,且主要来自人为源;若EF值在10—100之间,为中度富集水平,表明这些元素主要来自包括地壳源和人为源在内的混合源,且人为源是主要的污染源;若EF值小于10,为无富集或轻度富集,可认为该元素的来源是土壤或地壳源.
-
利用SPSS 26.0统计软件对PM2.5中的元素组成和来源进行主成分-多元线性回归(PCA-MLR)分析. 主成分分析是利用“降维”的方法,压缩变量维数,将多个变量线性变换,分析多个变量之间的关系,将几个密切的变量归为同一类,同一类变量为一个因子,达到用较少的几个因子反映大量原始数据信息的目的[21]. 多元线性回归的目的是在源识别的基础上,通过最小二乘法多元线性回归,进一步确定不同污染源的贡献率[2,21].
-
综合风险指数(NIRI)是一种新的生态风险评价方法,该方法既考虑了重金属元素的毒性响应因子,又可灵活的应对重金属数量的变化[22]. 综合风险指数可以更准确地评价多种重金属的综合效应,并区分不同重金属的影响. NIRI的计算公式如下[22]:
式中,
Eir 是重金属i的潜在生态风险因子;Tir 是重金属i的毒性响应因子,元素Cd、Mo、Pb、As、Zn、Cu、V、Cr、Ni和Se的毒性响应因子[11],分别为30、18、5、10、1、5、2、2、5和1;Ci为元素i的浓度或含量,Si为元素i在土壤背景中的浓度或含量,单位为μg·m−3或mg·kg−1;Ei2rmax 和Ei2raverage 分别是Eir 的最大值和平均值. 潜在生态风险分类[8 − 9,22]如表1所示. -
根据美国EPA开发的健康风险评估模型对PM2.5中重金属进行健康风险评估. 考虑到行为和呼吸系统的差异,将人群分为儿童和成人两组[11,23]. 重金属主要通过呼吸吸入、手口摄入和皮肤接触影响人体健康[9],由于大气PM2.5颗粒物粒径较小,主要通过呼吸吸入进入人体,并对人体健康产生影响,故本文主要探究PM2.5中重金属以呼吸吸入途径对人体健康产生的非致癌风险(HQ)和致癌风险(CR). 非致癌风险评估主要针对As、Cu、Zn、Pb、Cd、V、Ni、Cr、Mo和Se元素,其中,对As、Pb、Cd、Cr和Ni元素进行致癌风险评估. 健康风险评估中,Cr为六价铬,其浓度计算为总铬的七分之一[11,23].
式中,EC为由呼吸吸入的接触浓度,μg·m−3;Cinh为重金属元素在颗粒物中的浓度,μg·m−3;公式中其他参数的含义和取值如表2所示[11].
非致癌风险(HQ)和致癌风险(CR)的计算公式如下[11]:
综合非致癌风险(HI)和综合致癌风险(CRT)的计算公式分别为:
式中,RfCi和IUR分别为吸入参考浓度和吸入单位风险,参数取值如表3所示[11]. 当HQ>1或HI>1时,存在非致癌风险;而当HQ≤1和HI≤1时,无非致癌风险. 当CR(CRT)>10−4时,认为存在致癌风险;当10−6≤CR(CRT)≤10−4时,认为具有潜在致癌风险;当CR(CRT)<10−6时,认为不存在致癌风险[25].
-
采样期间,武当山PM2.5的日均浓度范围为5.00—33.65 μg·m−3,平均浓度为(16.84±7.07)μg·m−3,均低于我国《环境空气质量标准》(GB 3095—2012)中的一级标准(日均值35 μg·m−3). 武当山浓度值远低于长江三角洲(南京122.50 μg·m−3,2003年)[26]和珠江三角洲区域主要城市(深圳47.10 μg·m−3,2002年;珠海31.00 μg·m−3,2002年)[27],略低于海西城市群[2](28.24 μg·m−3,2011年). 与国内其它山区对比,武当山PM2.5的日均浓度远低于泰山[28](123.10 μg·m−3,2006年)、庐山[13](55.20 μg·m−3,2011年)、长白山[29](38.80 μg·m−3,2007年)和鼎湖山(30.80 μg·m−3,2006),略高于九仙山[30](14.41 μg·m−3,2011年),说明武当山PM2.5污染较小.
表4列出了PM2.5中18种无机元素的浓度及其他高山地区研究结果. 武当山PM2.5中18种元素之和占PM2.5浓度的10.24%,说明无机元素是PM2.5的重要组成部分,其中,元素K、Na、Fe、Ca、Al、Mg和Zn的浓度较高,这7种元素占所分析元素的97.68%以上. PM2.5中地壳元素(K、Na、Fe、Ca、Al和Mg)的浓度范围为(1136.87—3196.06) ng·m−3,其浓度之和占无机元素质量分数的92.56%—98.15%,是PM2.5中微量元素的12.45—53.12倍,表明地壳元素才是主导元素. 微量元素(Zn、Pb、Mn、Cu、Ba、Cr、As、Se、V、Ni、Mo和Cd)的质量浓度较低,浓度范围为(24.95—134.13) ng·m−3,仅占无机元素质量分数的1.85%—7.44%,12种重金属在PM2.5中的浓度大小顺序为:Zn>Pb>Mn>Cu>Ba>Cr>As>Se>V>Ni>Mo>Cd,其中,Se、Cd、Pb、Zn和Mo分别为湖北省土壤背景值的316.84、167.25、33.81、19.58、19.81倍[20]. 结果与在海西城市群[2]和西安市[31]的研究结果基本一致,可以看出,山区和城区金属元素的浓度大小排序差别不大,但各元素的浓度和含量之间存在明显差异. 与国内其它山区(泰山[12]、庐山[13]、贡嘎山[14])研究结果对比,武当山地壳元素浓度之和高于泰山和庐山,低于贡嘎山,其中K元素在武当山是贡献程度最高的地壳元素,这与贡嘎山的研究结果一致,可能受生物质燃烧远距离传输的影响. 武当山微量元素浓度之和低于泰山、庐山和贡嘎山,其中 Zn元素均为贡献程度最高的微量元素,其次为Pb元素(庐山除外),Zn来源复杂,汽车橡胶磨损[21]和工业金属冶炼[32]都可释放一定的Zn,而Pb是机动车尾气的重要标识物[2],说明工业和机动车源的排放对PM2.5造成了一定的影响. 综上所述,武当山PM2.5中无机元素,如Se、Cd、Pb和Zn等元素不仅来自土壤扬尘和岩石风化等自然源,还可能受到周边人为排放等区域传输的影响.
-
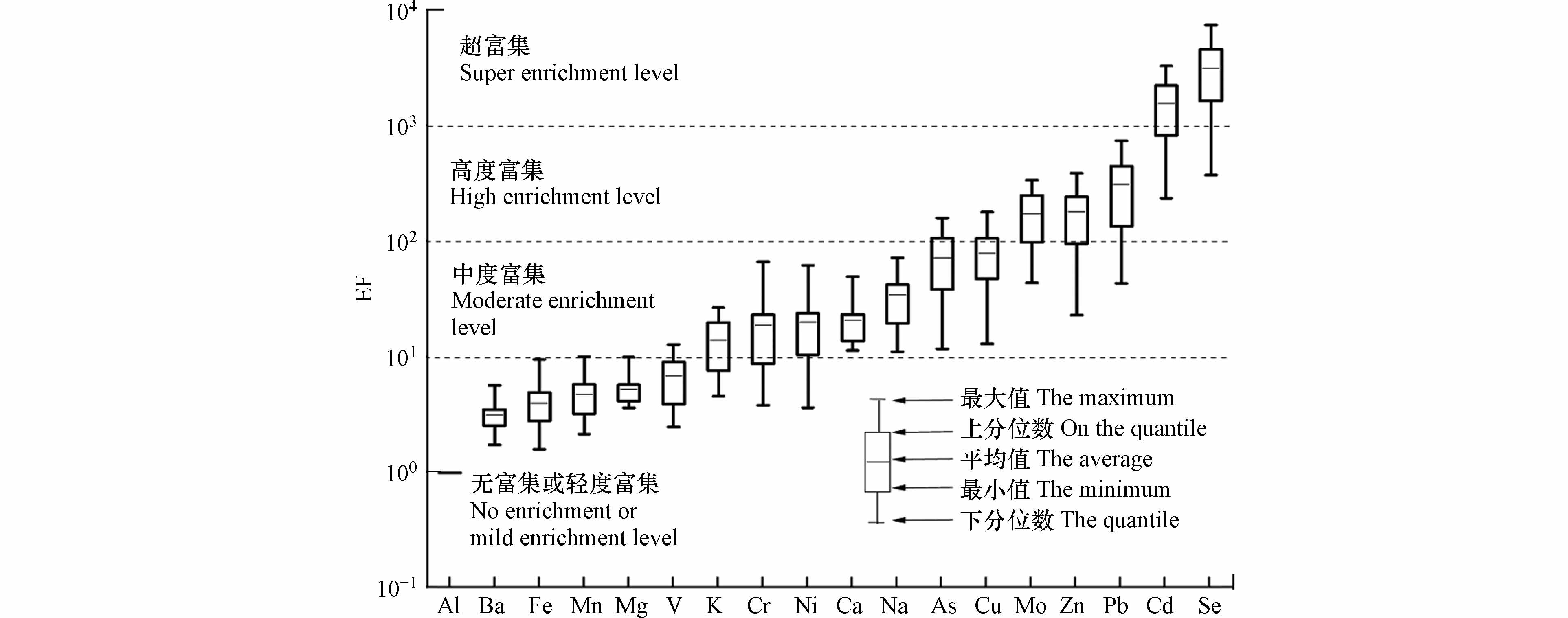
图1给出了武当山PM2.5中18种元素的EF值,各个元素的富集因子各不相同,说明这些元素均不同程度的受人为源和自然源的影响. 其中Al、Ba、Fe、Mn、Mg和V的EF值小于10,为无富集或轻度富集水平,认为这些元素主要来源于地壳,由土壤或岩石风化进入大气中导致的[8];K、Cr、Ni、Ca、Na、As和Cu的EF值在10—100之间,表现为中度富集,表明这些元素受一定的人为活动影响;Mo、Zn和Pb的EF值分别为172.52、179.68和312.02,均大于100为高度富集,受人为污染影响严重,其中Pb被认为是交通污染源的特征元素[33],Zn的来源广泛,包括垃圾焚烧、燃煤燃烧、机动车尾气和工业冶金等[32,34 − 35];Cd和Se的EF值分别为1551.09和3138.49,均大于1000为超富集水平,受强烈的人为污染影响,与胡月琪等[35] 的研究结果一致. As和Cd主要来源于燃煤活动[7],而Se在煤矿石中的富集系数很高[21],同时Se元素也是燃煤烟尘的特征元素[35,36].
-
表5为武当山PM2.5中元素PCA-MLR模型分析结果. 从表5中可知,通过PCA模型可以提取出3个因子与PM2.5中无机元素的污染源关系密切. 3个主要因子的因子载荷累积方差贡献率为80.07%,能反映数据表中的绝大部分信息.
主成分1中Na、Mg、Al、K、Ca、Mn、Fe、Ba和V载荷系数较高(>0.60),其中K、Na、Fe、Ca、Mn、Al和Mg为典型的地壳元素[37],且Al、Ba、Fe、Mn、Mg和V的富集因子显示为无富集或轻度富集水平,V元素含量均值低于湖北省A层土壤背景值,说明受人为活动影响较小,因此,推断主成分1为地壳,贡献率为19.91%. 主成分2中载荷系数高于0.60的元素为Cr、Ni、Cu和Zn,富集因子显示Cr、Ni和Cu为中度富集,Zn为高度富集,Cr和Ni同时是有色金属冶炼的标识物[38],Cu和Zn是工业排放的主要标识物[2,39],主要来自工业金属冶炼[32,40],虽然采样点区域不存在金属冶炼厂等工业排放源,但由于受远距离大气传输或区域传输的影响[9,41],可能导致Cr、Ni、Cu和Zn的累积,因此把主成分2归类为工业源,贡献率为22.52%. 主成分3中As、Cd和Pb的载荷系数分别为0.780、0.931和0.914,其中As和Pb既是机动车尾气的重要标识物[2,42],也是燃煤源的标识物[40,43],且汽车内部的磨损也会释放一定量的Pb[21],Cd 作为主要杂质存在于汽车轮胎和润滑油中[44],采样点周边无明显人为污染源,说明区域传输对武当山大气的影响较大,因此主成分3认定为燃煤和机动车的混合源,贡献率为57.57%. 综上所述,武当山大气PM2.5中的无机元素主要受燃煤和机动车源以及工业源的影响.
-
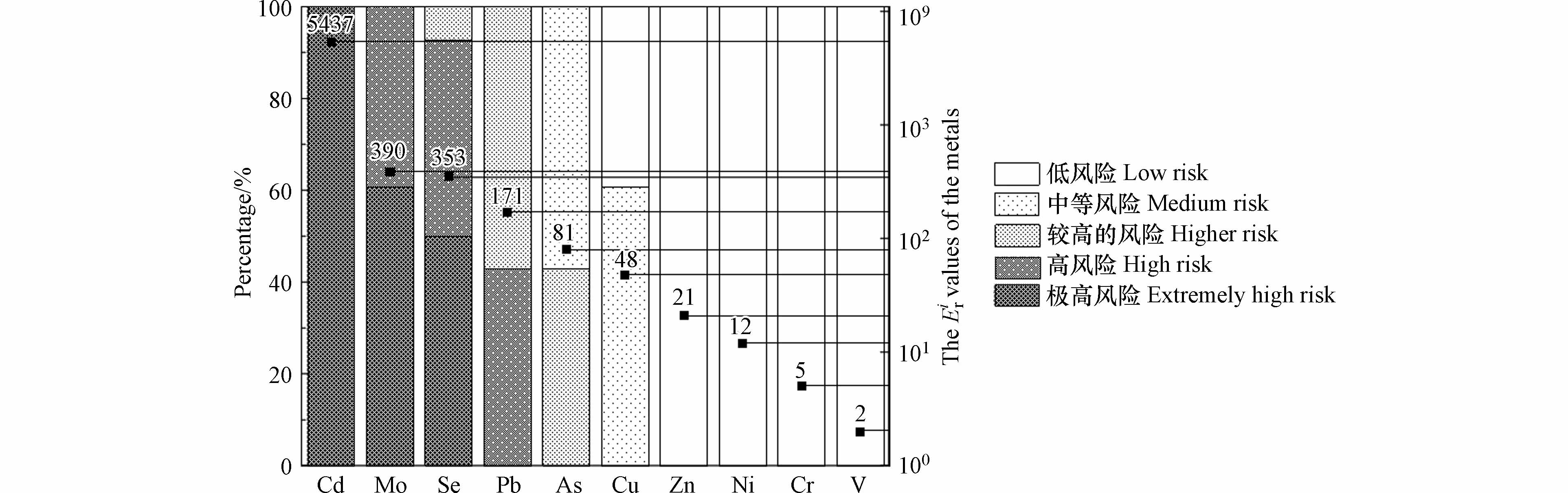
PM2.5中的重金属会对周边的生态环境存在一定的风险[9]. 图2为武当山PM2.5中10种重金属的潜在风险指数评价结果和每个风险水平的统计百分比. PM2.5中10种重金属的潜在生态风险强度顺序为Cd>Mo>Se>Pb>As>Cu>Zn>Ni>Cr>V,其中Zn、Ni、Cr和V的潜在生态风险指数(
Eir )均小于40,潜在生态危害程度比较轻,贡献程度忽略不计. Cu、As和Pb的Eir 值分别为48、81和171,生态潜在危害程度分别为中度、较高和高风险,其中Pb具有43%的高风险和57%低风险,As具有43%的较高风险和57%的中等风险. 对于Se和Mo来说,Eir 值分别为353和390,大于320,表明存在极高的潜在生态危害,该结果与日本北九州[11]的研究结果一致,其中Se和Mo分别具有50%和61%的极高风险,43%和39%的高风险. Cd的潜在生态风险指数(Eir )最高,为5437,远高于320,为100%的极高风险水平,说明Cd的潜在生态危害程度极强,这与北京(7977)[8]、黄石市(5962)[45]和郑州(70420)[9]的研究结果一致. 武当山潜在生态风险指数NIRI为3872,远远大于320,生态风险指数极强,应当引起重视. -
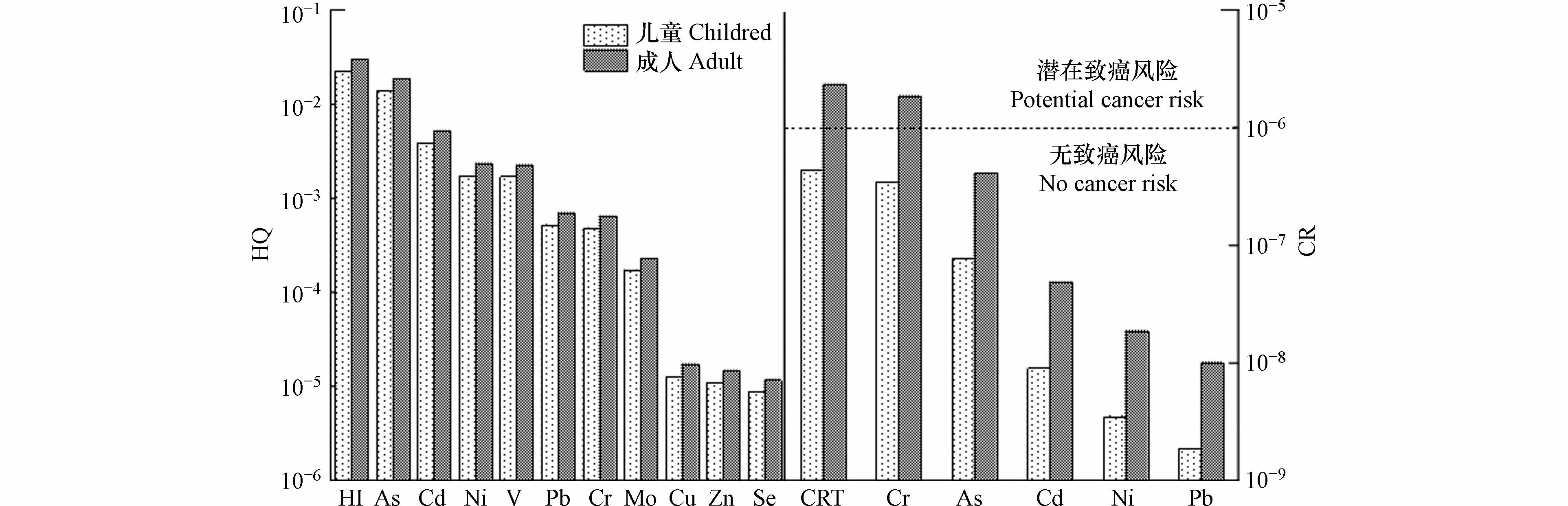
PM2.5中污染严重的重金属在对生态环境存在风险的同时,对人体也会造成一定的危害[32,41]. 图3为儿童和成人通过呼吸吸入暴露途径下的非致癌风险值(HQ). 10种单因子重金属非致癌风险(HQ)顺序依次为:As>Cd>Ni>V>Pb>Cr>Mo>Cu>Zn>Se,单因子重金属HQ值均低于可接受水平(HQ=1),说明10种重金属均无非致癌风险;As的非致癌风险最高,但也在可接受水平内,该结果与北京[46]和日本北九州[11]的研究结果一致. 同种金属单因子对人体的非致癌风险(HQ)均表现为:成人>儿童,且综合非致癌风险(HI)在儿童和成人中也表现为成人高于儿童,该结果与成人户外暴露时长普遍高于儿童[2],重金属在成人中的累积水平相对更高有关,且重金属在人体中与靶器官之间的敏感性也存在差异[11,47]. 综合非致癌风险(HI)在儿童和成人中分别为2.28×10−2和3.04×10−2,均在可接受水平内,说明武当山儿童和成人均无非致癌风险.
图3中儿童和成人在呼吸吸入暴露途径下的致癌风险结果显示,单因子重金属致癌风险(CR)顺序依次为:Cr>As>Cd>Ni>Pb,其中,Cr元素致癌风险最高,与在嘉峪关市[32]、兰州、西安、洛阳和乌鲁木齐[48]的研究结果一致,Cr在成人中的致癌风险为1.88×10−6,存在潜在的致癌风险,在儿童中为3.52×10−7,无致癌风险. 同种金属对人体的致癌风险(CR)表现为:成人>儿童. 综合致癌风险(CRT)在儿童和成人中分别为4.45×10−7和2.37×10−6,成人高于儿童,且成人CRT值在10−6—10−4之间,成人存在潜在的致癌风险,儿童CRT值低于10−6,不存在致癌风险.
-
(1)2018年夏季武当山PM2.5的日均浓度范围为5.00—33.65 μg·m−3,18种元素之和占PM2.5浓度的10.24%,说明无机元素是PM2.5的重要组成部分,其中地壳元素(K、Na、Fe、Ca、Al和Mg)的平均浓度为(1136.87—3196.06)ng·m−3,占无机元素质量分数的92.56%—98.15%. 微量元素的浓度大小顺序为:Zn>Pb>Mn>Cu>Ba>Cr>As>Se>V>Ni>Mo>Cd,浓度范围为(24.95—134.13) ng·m−3,仅占无机元素质量分数的1.85%—7.44%.
(2)富集因子表明,无机元素中Al、Ba、Fe、Mn、Mg和V为无富集或轻度富集水平,认为这些元素主要来源于地壳. K、Cr、Ni、Ca、Na、As和Cu表现为中度富集,表明这些元素受一定的人为活动影响. Mo、Zn和Pb的EF值分别为172.52、179.68和312.02,为高度富集,受人为污染影响严重. Cd和Se的EF值分别为1551.09和3138.49,为超富集水平,受强烈的人为污染影响.
(3)主成分-多元线性回归(PCA-MLR)解析出PM2.5中18种无机元素主要有3种主要来源,即燃煤和机动车混合源、工业源和地壳,贡献率分别为57.57%、22.52%和19.91%.
(4)武当山有毒金属元素的单因子生态风险排序为Cd>Mo>Se>Pb>As>Cu>Zn>Ni>Cr>V,Cd的潜在生态风险指数(
Eir )最高,为5437,远高于320,说明Cd的潜在生态危害程度极强. 多元素生态风险指数NIRI为3872,远远大于320,说明武当山生态风险极强.(5)武当山有毒金属对人体的非致癌风险中,单因子重金属非致癌风险(HQ)顺序依次为:As>Cd>Ni>V>Pb>Cr>Mo>Cu>Zn>Se,10种重金属均无非致癌风险,综合非致癌风险(HI)在儿童和成人中分别为2.28×10−2和3.04×10−2,均在可接受水平内,说明武当山儿童和成人均无非致癌风险. 单因子重金属致癌风险(CR)顺序依次为:Cr>As>Cd>Ni>Pb,Cr在成人中的致癌风险为1.88×10−6,存在潜在的致癌风险,综合致癌风险(CRT)在儿童和成人中分别为4.45×10−7和2.37×10−6,说明成人存在潜在的致癌风险. 同种金属对人体的非致癌风险和致癌风险均表现为:成人>儿童.
高山地区夏季大气PM2.5中元素的污染特征、生态风险及健康风险评估——以武当山为例
Pollution characteristics, ecological risk and health risk assessment of PM2.5 -bound elemental species at mountain site in summer: A case study of Mt.Wudang
-
摘要: 为了解华中高山地区夏季大气PM2.5中元素的污染特征,于2018年6月在湖北省十堰市武当山国家空气质量监测站采集PM2.5样品,利用电感耦合等离子体质谱仪(ICP-MS)测定样品中18种元素(Na、K、Ca、Mg、Al、Fe、V、Cr、Mo、Cu、Zn、Mn、Ni、As、Se、Cd、Ba和Pb)的浓度,并探讨了其来源、生态风险和健康风险. 结果表明,武当山PM2.5的日均浓度范围为5.00—33.65 μg·m-3,平均浓度为(16.84±7.07) μg·m-3;元素K、Na、Fe、Ca、Al、Mg和Zn的浓度较高,7种元素占所分析元素的97.68%以上;富集因子结果表明,Mo、Zn、Pb、Cd和Se的EF值高于100,可能受周边人为活动排放污染物的区域或长距离传输影响;主成分-多元线性回归(PCA-MLR)结果表明,PM2.5中元素主要来自于燃煤和机动车(57.57%)、工业源(22.52%)和地壳(19.91%);武当山PM2.5重金属的生态风险指数极高,其中Cd、Se和Mo的潜在生态危害程度极强;健康风险评估显示,综合非致癌风险(HI)在儿童和成人中分别为2.28×10-2和3.04×10-2,均在可接受水平内,综合致癌风险(CRT)在儿童和成人中分别为4.45×10-7和2.37×10-6,说明成人存在潜在的致癌风险;Cr在成人中的致癌风险为1.88×10-6,说明Cr在成人中存在潜在的致癌风险,同种金属对人体的非致癌风险和致癌风险均表现为成人>儿童.Abstract: To understand the pollution characteristics of PM2.5-bound elemental species at mountain site in summer, PM2.5 samples were collected at the Mt.Wudang National Air Quality Monitoring Station in Shiyan of Hubei Province in June 2018. The concentrations of 18 elements (Na, K, Ca, Mg, Al, Fe, V, Cr, Mo, Cu, Zn, Mn, Ni, As, Se, Cd, Ba and Pb) in PM2.5 were determined by inductively coupled plasma mass spectrometer (ICP-MS), and the sources, ecological and health risks were discussed. The results showed that the concentration of PM2.5 during observation period at Mt.Wudang were ranged from 5.00 μg·m-3 to 33.65 μg·m-3, with an average value of (16.84±7.07) μg·m-3. K, Na, Fe, Ca, Al, Mg and Zn) was the main elements accounting for 97.68% of all detected elements. The enrichment factor (EF) values showed that the EF values of Mo, Zn, Pb, Cd and Se were higher than 100, which may be affected by the regional or long-range transport of pollutants emitted from human activities. The principal component analysis-multiple linear regression (PCA-MLR) showed that the elements species of PM2.5 mainly come from coal burning and motor vehicles (57.57%), industrial production (22.52%) and crustal sources (19.91%). The ecological risk index of heavy metals in PM2.5 at Mt.Wudang is extremely high and Cd, Se and Mo have a very high degree of potential ecological damage. The health risk assessment showed that the comprehensive non-carcinogenic risks (HI) were 2.28×10-2 and 3.04×10-2 for children and adults, respectively, which are within the acceptable level. The comprehensive carcinogenic risks (CRT) were 4.45×10-7 and 2.37×10-6 for children and adults, respectively, indicating heavy metal had potential carcinogenic risk for adults. The carcinogenic risk of Cr for adults is 1.88×10-6, indicating that Cr has potential carcinogenic risk in adults. The non-carcinogenic risk and carcinogenic risk to human body followed the order of adults > children.
-
毒品属于精神活性物质,是一类使人体在吸收后产生生理和心理依赖的物质[1],主要包括阿片类的海洛因及吗啡(MOR)制品,可卡因、苯丙胺类的甲基苯丙胺(METH)、苯丙胺和摇头丸等[2-3],截至2020年底,联合国毒品和犯罪办公室及欧洲药物与成瘾监测中心(EMCDDA)共鉴定出1000余种精神活性物质[4-6]。根据《2021年世界毒品问题报告》的数据显示,去年全球约有2.75亿人接触过毒品,相比2010年增加了22%,在2019年,吸毒直接导致近50万人死亡,超过 5400 万人患精神障碍疾病或丧失生命[6],引发了极其严峻的全球公共卫生问题[7-9]。《2020年中国毒品形势报告》指出,由于疫情扩散蔓延,毒品泛滥态势仍然复杂但整体向好 ,截至2020年底,中国现有吸毒人员180.1万名,海洛因、冰毒等滥用品种仍维持较大规模[10],严重影响了社会治安并造成了极大的社会危害[11-15]。
毒品滥用是对公共卫生和社会安全的巨大威胁[16],并严重威胁着人体健康[17],毒品滥用趋势的实时预测和社会危害的准确评价是当前亟待解决的问题[18],基于污水流行病学发展而来的污水验毒技术恰好能够解决这一难题。冰毒和海洛因等传统毒品,经过人体吸食和代谢后,随着尿液排入各级污水处理系统并最终汇入环境。通过对环境样品的采集、处理和分析,可以直观获取环境中毒品母体及其代谢物的种类、浓度及变化趋势,结合数学模型计算,可反推目标区域的毒品滥用种类和滥用量[19]。该方法所得数据客观、时效性高,可用于不同区域横向比较,在估算传统毒品滥用量等方面发挥了巨大作用[20-24]。但在污水及河流等的传输过程中,由于本底因素复杂,目标物可能存在生物化学降解、吸附或其他转化过程[25]。不同水环境性质的差异对传统毒品及其代谢产物的稳定存在具有不同程度的影响[26]。Baker等[26]认为,中性水样中,METH具有较好的稳定性倾向[27]。但海洛因代谢产物6-单乙酰吗啡(6-MAM)非常不稳定,可进一步转化为MOR[28],在污水流行病学范畴内,海洛因的估算通常是以其代谢产物6-MAM作为标准进行的[29],但污水中,6-MAM的损失比例高达42%[26],从而该方法失效。张小寒[30]则认为pH值可通过影响水底质中悬浮物的表面电荷,使得水样中传统毒品含量测量值偏低。张春水等[31]认为,海洛因在碱性条件下会加速降解。此外,吕昱帆等[32]在其研究中发现盐析剂NaCl的使用对6-MAM及MOR的回收率具有不同程度的影响。
为明确水环境对METH、6-MAM和MOR的基质效应,本研究选取了山东省潍坊市11条不同河流的实际水样,测定相关水质参数,采用内标法和主成分分析法探讨基本水质参数对3种精神活性物质METH、6-MAM和MOR定量分析准确度的影响;设计不同梯度pH及氯离子浓度的模拟水样,加入定量METH、6-MAM和MOR并储存不同时间,测试分析其中目标物含量,验证pH、氯离子浓度及存储时间对3种精神活性物质检出浓度的影响。
1. 实验部分(Experimental section)
1.1 实验试剂与仪器
精神活性物质METH、6-MAM及MOR由山东省公安厅提供;氘代内标储备液MOR-D3、6-MAM-D3、METH-D8(100 μg·mL−1, 美国Cerilliant公司);实际水样来源于山东省潍坊市白浪河及利民河等处。主要化学试剂浓氨水、氢氧化钠、氯化钠、硝酸银、重铬酸钾、硫酸汞、高锰酸钾(分析纯,国药集团化学试剂有限公司),甲醇、二氯甲烷、甲酸(色谱纯,J&K百灵威公司)。
固相萃取仪(美国SUPELCO公司),Oasis MCX固相萃取小柱(美国Waters公司),0.45 μm微孔滤膜(天津津腾实验设备有限公司),氮吹仪(美国Organomation公司),XW-80A漩涡混合器(中国金昌实验仪器厂),三重四极杆液质联用仪(Thermo Scientific TSQ Quantiva LC-MS),水质多参仪(美国HACH公司),Milli-Q纯水机。
1.2 实验方法
1.2.1 毒品标准储备液的配制
用分析天平分别称取0.0500 g METH、6-MAM及MOR,逐级稀释溶解于色谱纯的甲醇中,得到浓度均为50 ng·mL−1的毒品标准储备液,超声45 min使其溶解完全。
1.2.2 不同pH、氯离子浓度模拟水样配制
取浓盐酸和NaOH,加入Milli-Q水中,配制pH值分别为2、4、7、10的溶液备用。称取NaCl固体,配制质量浓度为0、1、2、3、4、5 g·L−1的溶液。在50 mL模拟水样中分别加入毒品标准储备液100 μL,使METH、6-MAM及MOR的质量浓度均为100 ng·L−1,常温(25℃)下存储12 、24、36、48、72、120 h。
1.2.3 实际水样的采集
实验样品于2019年12月在山东省潍坊市内白浪河及利民河等11条河流中采集。每个采样点取水样1000 mL, 分为两份,均置于提前用甲醇和Milli-Q水洗净并烘干的棕色玻璃瓶中。采样结束后立即运回实验室,于 4 ℃冷藏。1份样品在48 h内处理完毕,另1份加入定量毒品标准储备液,使METH、6-MAM及MOR的质量浓度均为100 ng·L−1,常温保存72 h。同步参照国家标准测试温度、pH、氯离子浓度,化学需氧量等6项相关水质参数。
1.2.4 样品前处理
①过滤:将水样经过玻璃纤维滤膜(Whatman GF/F)过滤,去除悬浮颗粒物,收集滤液至少100 mL。②MCX小柱活化:依次将甲醇、Milli-Q水和 pH=2的水溶液通过MCX小柱,控制流速为1—2 mL·min−1,充分活化并平衡柱子。③配制MOR-D3、6-MAM-D3、METH-D8的内标溶液,浓度均为200 μg·L−1。④于pH=2的条件下加载已过滤并添加内标的样品,控制流速为1—2 mL·min−1。⑤对淋洗后的SPE小柱持续抽气20 min,直至MCX小柱完全干燥。依次用甲醇和氨水/甲醇溶液(5/100,质量比)洗脱干燥的Oasis MCX柱,并控制流速为1—2 mL·min−1。⑥收集洗脱液,33 ℃水浴下置于柔和的氮气流下吹至近干,用注射器取0.5 mL 20%的甲醇水溶液复溶氮吹残留物,涡旋振荡1 min,用注射器吸取溶液,用0.45 μm针头过滤器(Whatman)过滤并转移至HPLC-MS/MS专用样品瓶中,重复此操作一次。⑦样品测试前用0.2 μm滤膜过滤,滤液上机测试。
1.2.5 分析方法优化
流动相:0.12%甲酸和30 mmol·L−1甲酸铵超纯水溶液(A相);甲醇(B相),流速为0.3 mL·min−1,柱温为30 ℃,进样量为5 μL。以该液相色谱条件为初始方法[24],进一步手动优化,以获得对目标化合物的最高灵敏度(表1)。
表 1 HPLC-MS流动相洗脱梯度Table 1. HPLC-MS mobile phase elution gradient时间/min Time A/% B/% 0.0 95 5 3.0 70 30 6.0 20 80 6.5 10 90 8.0 10 90 8.5 95 5 11.0 95 5 质谱:离子源为电喷雾离子源(ESI),喷雾电压3500 V,离子传输管温度350 ℃,离子化模式为ESI(+);碰撞池气压(CAD)1.5 mTorr,鞘气压力(Sheath gas)为80 Arb,辅气压力(Aux gas)15 Arb。每种目标化合物及其相应内标的母离子和定量、定性离子的质荷比(m/z)见表2,其中,选取每种目标物丰度最大的离子对作为定量离子。
表 2 目标物测试质谱参数Table 2. Mass spectral parameters of the target compound化合物Compound 母离子Parent ion 定量离子Quantitative ion 定性离子Qualitative ion 保留时间/minRetention time m/z m/z DP/V CE/V m/z DP/V CE/V MOR 286 152.1 82 55 165 82 32 2.73 MOR-D3 289.2 152.1 80 55 165 80 41 2.72 METH 150.1 91.1 30 16 119.1 30 16 4.62 METH-D8 158.2 93.2 40 19 124.2 40 10.3 4.59 6-MAM 328.1 165.3 90 36 211.3 90 36 4.35 6-MAM-D3 331.1 165.1 90 38.3 211.2 90 25 4.36 2. 结果与讨论(Results and discussion)
2.1 分析方法的评价
2.1.1 回收率
取3种毒品储备液适量,配制成低、中、高浓度(100 ng·L−1、300 ng·L−1、400 ng·L−1)的质控样品,分别按相同的前处理方法平行操作;每一浓度进行双样本分析,根据当日标准曲线,计算样品测定浓度,得出METH、6-MAM和MOR的方法回收率,结果见表3。数据结果表明METH、6-MAM和MOR的回收率良好。
表 3 实验方法回收率、检出限及定量限Table 3. Experimental methods Recovery rate, detection limit and quantitation limit化合物Compound 加标浓度/(ng·L−1)Added 检出浓度/ (ng·L−1)Found 方法回收率/%Method recovery 检出限/(ng·mL−1) 定量限/(ng·mL−1) ILOD MLOD ILOQ MLOQ METH 400 377.0 94.25 0.2 0.0008 0.8 0.0032 300 304.9 101.63 100 102.6 102.60 6-MAM 400 384.2 96.05 0.2 0.0008 0.8 0.0032 300 283.7 94.57 100 101.4 101.4 MOR 400 418.0 104.50 0.2 0.0008 0.8 0.0032 300 294.8 98.27 100 102.3 102.3 2.1.2 线性范围、检出限及定量限
将低浓度目标物混合标准溶液上机测定,仪器检出限(ILOD)和仪器定量限(ILOQ)分别以3倍信噪比(S/N=3)和10倍信噪比(S/N=10)确定。方法检出限(MLOD)和方法定量限(MLOQ)分别通过以下公式计算得到:
MLOD(或MLOQ)=ILOD(或ILOQ)×200μL50mL 式中,200 μL为上机浓缩液的体积,50 mL为前处理所取水样的体积。
取混合毒品标准溶液适量,用流动相稀释,得质量浓度分别为1.5、3、6、12、25、50、100、150、200、250 ng·mL−1系列标准溶液。依次取上述各浓度标准溶液50 mL,按照相同的前处理方法操作,记录色谱图;以标准溶液中目标物的峰面积与同位素内标的峰面积之比为纵坐标(Y),进样浓度(X)为横坐标,进行线性回归运算,得METH、6-MAM和MOR回归方程:
Y=−0.040+0.033XR2=0.9996 Y=−0.044+0.023XR2=0.9998 Y=−0.042+0.023XR2=0.9992 结果表明METH、6-MAM及MOR质量浓度在1.5—250 ng·mL−1范围内线性关系良好,仪器的检出限和定量限见表3。
2.2 河流水质参数与毒品目标物检出浓度的相关性评价
水样温度、pH值、氯离子浓度、化学需氧量、氨氮、高锰酸盐指数和溶解氧等水质参数见表4。
表 4 样品水质参数Table 4. Water quality parameters of the samples样品名称Sample name 温度/℃Temperature pH 氯离子浓度/(mg·L−1)Chloride ion 化学需氧量/(mg·L−1)COD 氨氮/(mg·L−1)NH4+-N 高锰酸盐指数/(mg·L−1)Permanganate Index 溶解氧/(mg·L−1)DO YX 3.6 8.02 1.10×104 94.0 6.67 9.30 10.1 WS 7.0 8.27 9.09×102 9.50 3.81 11.6 9.50 BQ 2.6 8.34 2.25×102 24.0 1.22 6.70 13.1 GS 4.1 8.49 5.60×102 34.0 0.87 9.40 10.8 DH 2.6 8.50 1.30×103 41.0 0.89 10.0 11.6 BX 4.4 8.56 1.26×103 40.0 1.20 7.90 15.5 CZ 3.6 8.60 1.77×103 53.0 1.30 11.4 11.8 LZ -0.3 8.62 1.29×104 141 1.09 5.10 10.1 LX 0.6 8.64 1.24×104 126 0.88 10.5 14.0 XC 3.7 8.66 1.02×103 47.0 2.22 12.7 13.7 DX 4.3 8.68 1.13×103 39.0 1.08 10.5 14.2 检测水样中METH、MOR及6-MAM浓度(记为c1),在样品中均加入定量毒品标准储备液,使METH、6-MAM及MOR的质量浓度均为100 ng·L−1,常温保存72 h后按照2.3所述方法进行样品前处理,并检测3种毒品目标物加标后的浓度(记为c2),见表5。
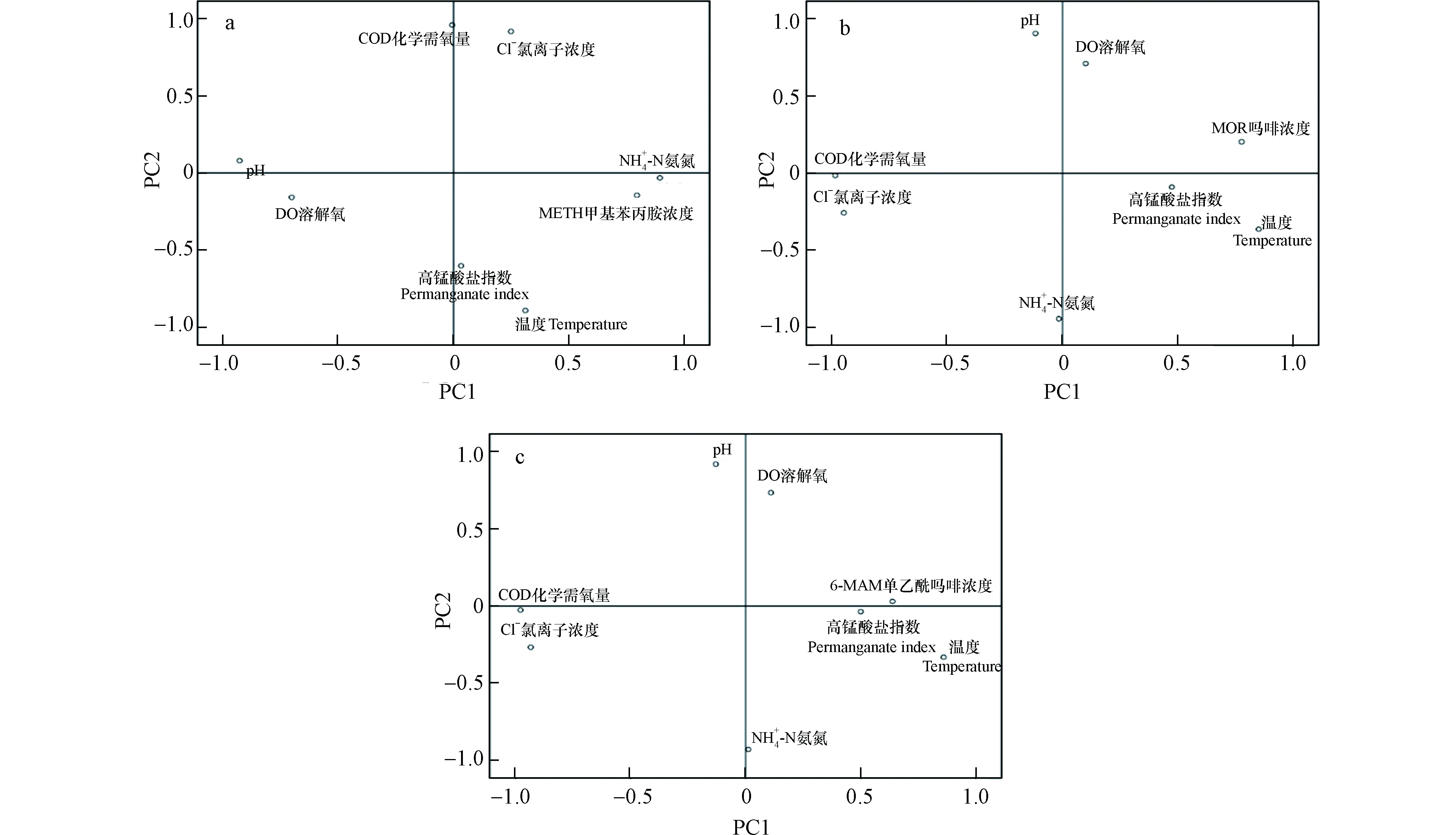
表 5 样品加标前后三种毒品目标物的检出浓度Table 5. Detected concentrations of three drug targets before and after labeling样品名称Sample name METH/(ng·L−1) MOR/(ng·L−1) 6-MAM/(ng·L−1) c1 c2 c1 c2 c1 c2 YX 3.19 90.61 n.d. 6.99 n.d. 1.67 WS 2.15 98.73 1.97 25.15 1.25 23.85 BQ 1.13 103.19 3.05 44.63 n.d. 47.25 GS 3.35 99.54 n.d. 42.98 3.29 42.25 DH n.d. 91.70 n.d. 21.36 n.d. 7.37 BX 2.73 94.57 n.d. 19.41 3.12 11.03 CZ n.d. 90.50 3.26 20.41 n.d. 3.34 LZ n.d. 90.27 2.91 7.13 n.d n.d LX 1.59 92.11 2.29 4.59 n.d. 1.91 XC 3.41 95.85 n.d. 24.33 n.d. 26.29 DX 1.28 94.95 3.01 23.97 n.d. 4.01 对河流水质参数及METH、6-MAM和MOR加标后的浓度分别进行主成分分析,探讨7个河流水质参数与污水样品中目标物检出浓度的相关性。主成分分析过程在 SPSS 20.0软件包中进行。对所有数据进行Bartlett球形度检验,相伴概率小于0.05,进行 PCA 以获得分数图和因子载荷,经变量最大旋转后,提取出特征值大于1的因子,主成分分析如图1所示。
METH与pH及溶解氧存在较强的负相关性,说明pH或溶解氧的升高可能会导致其检出浓度的下降。MOR与6-MAM均呈现出与化学需氧量及氯离子浓度的强负相关,说明较高浓度的氯离子浓度可能造成MOR及6-MAM检出浓度不准确。此外,METH与氨氮存在明显的正相关,而水体中氨氮的主要来源是生物体代谢所产生的尿素,与人口高度密切相关。METH是中国滥用人数最多且最为广泛的毒品,氨氮浓度较大的流域为人口聚集区域,METH浓度也呈现聚集趋势。MOR及6-MAM是海洛因的代谢产物,稳定性较低,在因子分析中表现为与温度及高锰酸盐指数相关。高锰酸盐指数是反映水体中有机和无机可氧化物质污染的常用指标,结果表明在较高温度及氧化性较强的水环境中,MOR及6-MAM易于分解。
2.3 验证水质参数对模拟样品中毒品目标物的检出影响
根据实验结果,pH、氯离子浓度等均会不同程度影响3种毒品目标物的准确检出,故选取pH、氯离子浓度作为变量,设计单因素模拟实验验证其对毒品目标物稳定性的影响,此外,在应用污水验毒技术评估地区毒情及进行环境风险评估时,需要对污水及地表水中各毒品目标物进行精确定量,毒品母体及其生物标志物在不同水环境中驻留时间各不相同,也应考虑常温下不同存储时间对毒品目标物的检出影响。
2.3.1 pH对模拟样品中毒品目标物的检出影响
取pH=2、pH=4、pH=7、pH=10的模拟水样各50 mL,分别向其加入METH、6-MAM及MOR标准溶液及内标,按照1.2.4进行前处理,3种目标物的检出浓度见表6。
表 6 不同条件下模拟样品中目标物的检出浓度(ng·L−1)Table 6. Detected concentration of target in simulated samples under different conditions (ng ·L−1)条件梯度Condition Gradient METH/(ng·L−1) 回收率/%Recovery MOR/(ng·L−1) 6-MAM/(ng·L−1) MOR与6-MAM回收率/%Recovery pH 2 84.05±10.21 81.92±9.95 42.44±2.52 150.35±3.86 94.88±3.13 4 85.45±16.65 83.28±16.23 50.71±16.99 136.71±6.03 92.19±11.27 7 85.88±3.03 83.7±2.95 63.87±1.22 117.78±5.75 89.3±3.44 10 68.32±9.19 66.59±8.96 54.42±3.62 150.78±11.71 100.95±7.54 氯化钠浓度/(g·L−1) 0 57.33±1.71 55.88±1.67 34.57±0.04 81.45±0.26 57.06±0.15 1 66.99±5.53 65.29±5.39 46.97±0.77 17.49±1.13 31.58±0.94 2 54.11±1.22 52.74±1.19 33.16±1.22 0 16.21±0.6 3 53.39±1.86 52.04±1.81 38.10±0.74 0 18.62±0.36 4 50.96±3.76 49.67±3.66 35.46±1.04 0 17.33±0.51 5 55.85±0.94 54.43±0.92 37.54±2.25 0 18.35±1.1 存储时间/h 12 102.60±4.29 100±4.18 73.26±6.35 202.54±2.87 135.68±4.52 24 79.59±6.29 77.57±6.13 61.15±4.24 137.83±5.43 97.85±4.75 36 67.29±4.10 65.58±4 47.47±3.05 128.44±9.03 86.53±5.94 48 62.64±2.80 61.05±2.73 49.65±2.60 115.97±7.38 81.45±4.91 72 61.85±2.92 60.28±2.85 27.12±1.24 97.78±6.17 61.47±3.65 120 57.89±3.23 56.42±3.15 29.93±3.72 92.24±4.47 60.11±4.02 当pH=2时,模拟样品中METH的回收率在71.97%—91.87%之间,pH值升高至4和7时,METH回收率为67.05%—99.51%,基本不变, pH升高至10时,METH的回收率明显降低,为57.63%—75.55%,即pH对METH的准确检出有影响,当水体呈现酸性及中性时,METH可以稳定存在并准确检出,在碱性水体中,METH稳定性发生改变,检出浓度下降,与实际水体因子分析的结论相符。原因可能为,在不同的pH体系中,METH的电离度及形态发生了变化。METH的结构中含有碱性的氨基官能团,溶液的pH会影响其质子化/去质子化的过程,此外,含胺类物质在水溶液中易发生光降解,且光解行为与氨基上N电子与三重激发物的转移有关,在低pH条件下,氢离子与N电子结合,阻碍了N电子向活性物的转化从而抑制其光降解,反之,N电子的可用性增强,加速了METH的降解[30]。模拟样品中,MOR在中性条件下检出浓度最高,酸性或碱性的条件下降低。6-MAM的变化趋势与其相反,中性条件下,其检出浓度最低,在酸性及碱性环境中,检出浓度较高,即pH也会干扰MOR和6-MAM在水体中的准确定量,张春水等[33]在研究中发现,海洛因的化学形式在不同pH环境下存在变化,当pH升高时,水解反应加剧,发生6-MAM向MOR的转化。实验结果对实际水体的主成分分析结果进行了补充,可知MOR在中性水体环境中较稳定,6-MAM在酸性条件下更稳定。
由图2可见,不同pH条件下, 6-MAM与MOR的浓度变化规律各不相同,两者呈现相反的趋势,在碱性水体环境中易发生6-MAM向MOR的转化,与张春水等[31]提出的海洛因在碱性条件下加速降解成MOR的结论一致。
在实际污水验毒工作中,6-MAM与MOR均被用来估算海洛因滥用量,在pH值为2、4、7、10时,6-MAM与MOR的回收率之和分别为95%、92%、89%和100%,可知pH对于二者的定量分析及海洛因滥用量的准确估算影响较小。
2.3.2 氯离子浓度对模拟样品中毒品目标物的检出影响
取不同氯离子浓度梯度的模拟水样各50 mL,分别加入METH、6-MAM及MOR标准溶液和内标,按照1.2.4节进行前处理,结果见表6。氯化钠浓度为0 g·L−1时,3种目标物都能在模拟水环境中稳定存在。METH的检出浓度随氯离子浓度升高基本不变;MOR的检出浓度在氯化钠浓度为1 g·L−1时最高,为47.74 ng·L−1,其它浓度时在31.94—39.79 ng·L−1范围内小幅波动,因此氯离子浓度的增大对MOR的稳定性存在负影响,与2.2主成分分析所得结论吻合;6-MAM的浓度随氯离子浓度的升高变化较大,在超过2 g·L−1的氯离子浓度的水环境中不能检出。吕昱帆等[32]在对腐败血中6-MAM和MOR的检出研究中发现,在2.5 mL样品中,加入盐析剂NaCl的质量大于30 mg时,6-MAM及MOR的回收率显著降低,与2.3.2节实验结果吻合,故氯离子浓度的影响在实际应用污水验毒技术的过程中不可忽略。
2.3.3 存储时间对模拟样品中毒品目标物的检出影响
对常温(20℃)下存储不同时间的模拟水样进行前处理和定量分析,结果见表6。常温存储会使METH、6-MAM及MOR的浓度均下降,METH在120 h内降解35%左右,6-MAM在120 h内降解50%左右,MOR在120 h内降解达到了60%,即常温存储会造成METH、6-MAM及MOR在水中降解。
3. 结论(Conclusion)
(1)本文研究了山东省潍坊市的11条河流中,不同水质参数与传统精神活性物质METH、MOR、6-MAM检出浓度的相关性,运用主成分分析法进行相关性评价。结果表明,METH与pH及溶解氧存在较强的负相关,与氨氮存在明显的正相关;MOR与6-MAM均与化学需氧量及氯离子浓度负相关,与其它水质参数相关性较小。
(2)根据实际水样主成分分析结果,选取相关性较大的水质参数进行单因素模拟实验,结果表明,METH在中性及酸性环境下较稳定,MOR在中性条件下较稳定,6-MAM在酸性和碱性条件下均能稳定存在和准确检出;METH的检出几乎不受氯离子浓度的影响,但6-MAM及MOR受氯离子浓度的影响较大;常温(20℃)保存120 h后,METH、6-MAM和MOR的含量均有不同程度的下降。
-
表 1 潜在生态风险分级
Table 1. Classification criteria of the potential ecological risk index
NIRI Eir 风险等级 Risk level NIRI≤40 Eir 低风险Low risk 40<NIRI≤80 40< Eir 中等风险Medium risk 80<NIRI≤160 80< Eir 较高的风险Higher risk 160<NIRI≤320 160< Eir 高风险High risk NIRI>320 Eir 极高风险Extremely high risk 表 2 重金属健康风险评价计算参数含义和取值
Table 2. Definitions and values of calculated parameters for health risk assessment of heavy metals
参数Parameter 符号Notation 单位Unit 儿童Children 成人Adults 暴露时间Exposure time ET h·d−1 24 24 暴露频率Exposure frequency Ef d·a−1 180 180 暴露年限Exposure duration ED a 6 24 平均寿命Average lifetime ATn h ED × 365 × 24(非致癌作用for non-carcinogens) ED × 365 × 24(非致癌作用for non-carcinogens) 70 × 365 × 24(致癌作用for carcinogens) 70 × 365 × 24(致癌作用for carcinogens) 种类Parameter RfCi/(mg·m−3) IUR/((μg·m−3)−1) Pb 3.52×10−3 0.000012 As 1.50×10−5 0.0043 Cr 1.00×10−4 0.084 Ni 9.00×10−5 0.00026 Cd 1.5×10−5 0.0018 Se 2.00×10−2 — Mo 4.00×10−4 — Zn 3.01×10−1 — Cu 4.02×10−2 — V 1.00×10−4 — “—”表示没有相关数据. “—” indicates no relevant data. 表 4 中国不同山地站点微量元素平均浓度(ng·m−3)
Table 4. Average trace elements concentrations at different mountain sites in China(ng·m−3)
项目Parameter 武当山Mt.Wudang 泰山[12]Mt.Tai 庐山[13]Mt.Lu 贡嘎山[14]Mt.Gongga 高度/mAltitude 862 1534 1165 1600 K 477.84±113.33 145.95 — 498.20 Na 398.47±81.17 340.25 — 211.50 Fe 305.53±104.41 152.07 330.40 224.00 Ca 215.52±82.32 355.48 — 372.80 Al 174.10±125.68 50.65 369.10 295.80 Mg 84.83±43.94 53.31 — 167.80 Zn 27.57±13.07 42.16 274.30 154.60 Pb 15.20±7.76 17.36 65.40 39.40 Mn 7.04±3.25 6.15 24.70 — Cu 4.27±1.31 3.22 13.20 2.20 Ba 3.71±1.85 6.26 66.00 6.00 Cr 2.78±1.13 1.62 18.20 — As 1.72±0.73 1.63 22.30 4.30 Se 1.47±0.69 1.20 7.60 — V 1.40±0.46 0.50 — 0.70 Ni 1.30±0.57 11.17 — 0.90 Mo 0.57±0.27 — — — Cd 0.48±0.19 0.34 2.80 — 注:“—”表示没有相关数据. “—” indicates no relevant data. 表 5 PM2.5中元素PCA-MLR结果
Table 5. Results of PCA-MLR of elements in PM2.5
元素Elements F1 F2 F3 Na 0.694 0.110 -0.402 Mg 0.977 0.039 -0.080 Al 0.981 -0.059 -0.030 K 0.73 -0.047 0.418 Ca 0.935 0.120 0.025 Mn 0.803 0.434 0.340 Fe 0.813 0.325 0.135 Ba 0.893 0.183 0.189 V 0.626 0.374 0.332 Mo 0.575 0.494 0.169 Cr 0.136 0.815 0.094 Ni 0.098 0.889 0.029 Cu 0.192 0.778 0.478 Zn 0.182 0.770 0.424 Se 0.035 0.596 0.525 As 0.067 0.425 0.780 Cd 0.107 0.167 0.931 Pb 0.074 0.202 0.914 方差贡献率/%Variance contribution rate 48.43 22.68 8.96 来源Sources 地壳Crustal sources 工业源Industrial production 燃煤和机动车Coal burning and motor vehicles 污染源贡献率/%Contribution rate of pollution sources 19.91 22.52 57.57 注:表中黑体字为影响较大的因子载荷(>0.60). Bold letters in the table for influential factor loading(>0.60). -
[1] WANG W J, CHEN C, LIU D, et al. Health risk assessment of PM2.5 heavy metals in County units of Northern China based on Monte Carlo simulation and APCS-MLR[J]. Science of the Total Environment, 2022, 843: 156777. doi: 10.1016/j.scitotenv.2022.156777 [2] 陈衍婷, 杜文娇, 陈进生, 等. 海西城市群PM2.5中重金属元素的污染特征及健康风险评价[J]. 环境科学, 2017, 38(2): 429-437. CHEN Y T, DU W J, CHEN J S, et al. Pollution characteristics of heavy metals in PM2.5 and their human health risks among the coastal city group along western Taiwan Straits region, China[J]. Environmental Science, 2017, 38(2): 429-437(in Chinese).
[3] KONG L W, TAN Q W, FENG M, et al. Investigating the characteristics and source analyses of PM2.5 seasonal variations in Chengdu, Southwest China[J]. Chemosphere, 2020, 243: 125267. doi: 10.1016/j.chemosphere.2019.125267 [4] FENG J L, YU H, MI K, et al. One year study of PM2.5 in Xinxiang City, North China: Seasonal characteristics, climate impact and source[J]. Ecotoxicology and Environmental Safety, 2018, 154: 75-83. doi: 10.1016/j.ecoenv.2018.01.048 [5] COPAT C, CRISTALDI A, FIORE M, et al. The role of air pollution (PM and NO2) in COVID-19 spread and lethality: A systematic review[J]. Environmental Research, 2020, 191: 110129. doi: 10.1016/j.envres.2020.110129 [6] 雷文凯, 李杏茹, 张兰, 等. 保定地区PM2.5中重金属元素的污染特征及健康风险评价[J]. 环境科学, 2021, 42(1): 38-44. LEI W K, LI X R, ZHANG L, et al. Pollution characteristics and health risk assessment of heavy metals in PM2.5 collected in Baoding[J]. Environmental Science, 2021, 42(1): 38-44(in Chinese).
[7] 庞晓晨, 韩新宇, 史建武, 等. 昭通市周边扬尘重金属污染特征及健康风险[J]. 环境科学, 2022, 43(1): 180-188. doi: 10.13227/j.hjkx.202106018 PANG X C, HAN X Y, SHI J W, et al. Pollution characteristics and health risk of heavy metals in fugitive dust around Zhaotong City[J]. Environmental Science, 2022, 43(1): 180-188(in Chinese). doi: 10.13227/j.hjkx.202106018
[8] 徐静, 李杏茹, 张兰, 等. 北京城郊PM2.5中金属元素的污染特征及潜在生态风险评价[J]. 环境科学, 2019, 40(6): 2501-2509. XU J, LI X R, ZHANG L, et al. Concentration and ecological risk assessment of heavy metals in PM2.5 collected in urban and suburban areas of Beijing[J]. Environmental Science, 2019, 40(6): 2501-2509(in Chinese).
[9] 何瑞东, 张轶舜, 陈永阳, 等. 郑州市某生活区大气PM2.5中重金属污染特征及生态、健康风险评估[J]. 环境科学, 2019, 40(11): 4774-4782. HE R D, ZHANG Y S, CHEN Y Y, et al. Heavy metal pollution characteristics and ecological and health risk assessment of atmospheric PM2.5 in a living area of Zhengzhou City[J]. Environmental Science, 2019, 40(11): 4774-4782(in Chinese).
[10] WU Z H, LIU F W, FAN W H. Characteristics of PM10 and PM2.5 at mount Wutai Buddhism scenic spot, Shanxi, China[J]. Atmosphere, 2015, 6(8): 1195-1210. doi: 10.3390/atmos6081195 [11] ZHANG X, ETO Y, AIKAWA M. Risk assessment and management of PM2.5-bound heavy metals in the urban area of Kitakyushu, Japan[J]. Science of the Total Environment, 2021, 795: 148748. doi: 10.1016/j.scitotenv.2021.148748 [12] QIE G H, WANG Y, WU C, et al. Distribution and sources of particulate mercury and other trace elements in PM2.5 and PM10 atop Mount Tai, China[J]. Journal of Environmental Management, 2018, 215: 195-205. [13] LI T, WANG Y, LI W J, et al. Concentrations and solubility of trace elements in fine particles at a mountain site, Southern China: Regional sources and cloud processing[J]. Atmospheric Chemistry and Physics, 2015, 15(15): 8987-9002. doi: 10.5194/acp-15-8987-2015 [14] YANG Y J, WANG Y S, WEN T X, et al. Elemental composition of PM2.5 and PM10 at mount Gongga in China during 2006[J]. Atmospheric Research, 2009, 93(4): 801-810. doi: 10.1016/j.atmosres.2009.03.014 [15] ZHANG N N, CAO J J, LIU S X, et al. Chemical composition and sources of PM2.5 and TSP collected at Qinghai Lake during summertime[J]. Atmospheric Research, 2014, 138: 213-222. doi: 10.1016/j.atmosres.2013.11.016 [16] 苏彬彬, 刘心东, 陶俊. 华东区域高山背景点PM10和PM2.5背景值及污染特征[J]. 环境科学, 2013, 34(2): 455-461. SU B B, LIU X D, TAO J. Characteristics of PM10 and PM2.5 concentrations in mountain background region of East China[J]. Environmental Science, 2013, 34(2): 455-461(in Chinese).
[17] 魏雅, 林长城, 胡清华, 等. 福建九仙山大气PM10及部分化学组成的季节变化[J]. 环境科学, 2017, 38(10): 4077-4083. WEI Y, LIN C C, HU Q H, et al. Seasonal variations in PM10 and associated chemical species in Jiuxian Mountain in Fujian Province[J]. Environmental Science, 2017, 38(10): 4077-4083(in Chinese).
[18] LI Y F, GAO R, XUE L K, et al. Ambient volatile organic compounds at Wudang Mountain in Central China: Characteristics, sources and implications to ozone formation[J]. Atmospheric Research, 2020, 250: 105359. [19] HJ657—2013空气和废气颗粒物中金属元素的测定电感耦合等离子体质谱法[S]. HJ657—2013 Ambient air and stationary source emission - Determination of metals in ambient particulate matter - Inductively coupled plasma/mass spectrometry (ICP-MS) (in Chinese).
[20] 魏复盛, 陈静生, 吴燕玉. 中国土壤元素背景值[M]. 北京: 中国环境科学出版社, 1990. WEI F S, CHEN J S, WU Y Y. China's soil element background value[M]. Beijing: China Environment Science Press, 1990(in Chinese).
[21] 刘威杰, 石明明, 程铖, 等. 夏季大气PM2.5中元素特征及源解析: 以华中地区平顶山-随州-武汉为例[J]. 环境科学, 2020, 41(1): 23-30. LIU W J, SHI M M, CHENG C, et al. Characteristics and sources of elements in PM2.5 during summer for three typical cities in Pingdingshan-Suizhou-Wuhan, central China[J]. Environmental Science, 2020, 41(1): 23-30(in Chinese).
[22] MEN C, LIU R M, XU L B, et al. Source-specific ecological risk analysis and critical source identification of heavy metals in road dust in Beijing, China[J]. Journal of Hazardous Materials, 2020, 388: 121763. doi: 10.1016/j.jhazmat.2019.121763 [23] DAHMARDEH BEHROOZ R, KASKAOUTIS D G, GRIVAS G, et al. Human health risk assessment for toxic elements in the extreme ambient dust conditions observed in Sistan, Iran[J]. Chemosphere, 2020, 262: 127835. [24] 国家卫生健康委员会. 大气污染人群健康风险评估技术规范: WS/T 666—2019[S]. 北京: 中国标准出版社, 2019. National Health Commission of the People’s Republic of China. Technical specifications for health risk assessment of ambient air pollution: WS/T 666—2019[S]. Beijing: Standards Press of China, 2019(in Chinese).
[25] 李星谕, 毛瑶, 陈展乐, 等. 华中地区冬季灰霾天气下PM2.5中重金属污染特征及健康风险评价: 以湖北黄冈为例[J]. 环境科学, 2021, 42(10): 4593-4601. LI X Y, MAO Y, CHEN Z L, et al. Characteristics and health risk assessment of heavy metals in PM2.5 under winter haze conditions in central China: A case study of Huanggang, Hubei Province[J]. Environmental Science, 2021, 42(10): 4593-4601(in Chinese).
[26] 樊曙先, 樊建凌, 郑有飞, 等. 南京市区与郊区大气PM2.5中元素含量的对比分析[J]. 中国环境科学, 2005, 25(2): 146-150. doi: 10.3321/j.issn:1000-6923.2005.02.005 FAN S X, FAN J L, ZHENG Y F, et al. Compared analysis of element content in atmospheric PM2.5 in Nanjing urban and suburban area[J]. China Environmental Science, 2005, 25(2): 146-150(in Chinese). doi: 10.3321/j.issn:1000-6923.2005.02.005
[27] LAI S C, ZOU S C, CAO J J, et al. Characterizing ionic species in PM2.5 and PM10 in four Pearl River Delta cities, South China[J]. Journal of Environmental Sciences (China), 2007, 19(8): 939-947. doi: 10.1016/S1001-0742(07)60155-7 [28] DENG C, ZHUANG G, HUANG K, et al. Chemical characterization of aerosols at the summit of mountain Tai in central East China[J]. Atmospheric Chemistry and Physics, 2011, 11(14): 7319-7332. doi: 10.5194/acp-11-7319-2011 [29] LI L, WANG W, FENG J L, et al. Composition, source, mass closure of PM2.5 aerosols for four forests in Eastern China[J]. Journal of Environmental Sciences, 2010, 22(3): 405-412. doi: 10.1016/S1001-0742(09)60122-4 [30] NIU Z C, WANG S, CHEN J S, et al. Source contributions to carbonaceous species in PM2.5 and their uncertainty analysis at typical urban, peri-urban and background sites in southeast China[J]. Environmental Pollution, 2013, 181: 107-114. doi: 10.1016/j.envpol.2013.06.006 [31] 樊馨瑶, 卢新卫, 刘慧敏, 等. 西安市高校校园地表灰尘重金属污染来源解析[J]. 环境科学, 2020, 41(8): 3556-3562. doi: 10.13227/j.hjkx.201912041 FAN X Y, LU X W, LIU H M, et al. Pollution and source analysis of heavy metal in surface dust from Xi'an university campuses[J]. Environmental Science, 2020, 41(8): 3556-3562(in Chinese). doi: 10.13227/j.hjkx.201912041
[32] 肖凯, 任学昌, 陈仁华, 等. 典型西北钢铁城市冬季大气颗粒物重金属来源解析及健康风险评价: 以嘉峪关为例[J]. 环境化学, 2022, 41(5): 1649-1660. doi: 10.7524/j.issn.0254-6108.2021010704 XIAO K, REN X C, CHEN R H, et al. Source analysis and health risk assessment of heavy metals in air particulates of typical northwest steel cities in winter: A case study in Jiayuguan[J]. Environmental Chemistry, 2022, 41(5): 1649-1660(in Chinese). doi: 10.7524/j.issn.0254-6108.2021010704
[33] WANG S, CAI L M, WEN H H, et al. Spatial distribution and source apportionment of heavy metals in soil from a typical County-level City of Guangdong Province, China[J]. Science of the Total Environment, 2019, 655: 92-101. doi: 10.1016/j.scitotenv.2018.11.244 [34] 陈江, 费勇, 马鑫雨, 等. 燃煤与垃圾焚烧飞灰中细颗粒物PM2.5的重金属元素风险评价[J]. 中国粉体技术, 2016, 22(2): 104-107. CHEN J, FEI Y, MA X Y, et al. Risk assessment on heavy metal elements of fine particulate matter PM2.5 in fly ash origin from coal and waste incineration[J]. China Powder Science and Technology, 2016, 22(2): 104-107(in Chinese).
[35] 胡月琪, 郭建辉, 张超, 等. 北京市道路扬尘重金属污染特征及潜在生态风险[J]. 环境科学, 2019, 40(9): 3924-3934. doi: 10.13227/j.hjkx.201903094 HU Y Q, GUO J H, ZHANG C, et al. Pollution characteristics and potential ecological risks of heavy metals in road dust in Beijing[J]. Environmental Science, 2019, 40(9): 3924-3934(in Chinese). doi: 10.13227/j.hjkx.201903094
[36] 王珍, 郭军, 陈卓. 贵阳市PM2.5主要污染源源成分谱分析[J]. 安全与环境学报, 2016, 16(2): 346-351. WANG Z, GUO J, CHEN Z. Analysis of the source componential spectrum of PM2.5 emission in Guiyang[J]. Journal of Safety and Environment, 2016, 16(2): 346-351(in Chinese).
[37] YANG Z P, LU W X, LONG Y Q, et al. Assessment of heavy metals contamination in urban topsoil from Changchun City, China[J]. Journal of Geochemical Exploration, 2011, 108(1): 27-38. doi: 10.1016/j.gexplo.2010.09.006 [38] XU L L, YU Y K, YU J S, et al. Spatial distribution and sources identification of elements in PM2.5 among the coastal city group in the Western Taiwan Strait region, China[J]. Science of the Total Environment, 2013, 442: 77-85. doi: 10.1016/j.scitotenv.2012.10.045 [39] CHEN P F, BI X H, ZHANG J Q, et al. Assessment of heavy metal pollution characteristics and human health risk of exposure to ambient PM2.5 in Tianjin, China[J]. Particuology, 2015, 20: 104-109. doi: 10.1016/j.partic.2014.04.020 [40] ZHANG N N, CAO J J, XU H M, et al. Elemental compositions of PM2.5 and TSP in Lijiang, southeastern edge of Tibetan Plateau during pre-monsoon period[J]. Particuology, 2013, 11(1): 63-69. doi: 10.1016/j.partic.2012.08.002 [41] 王申博, 余飞, 燕启社, 等. 典型背景区大气颗粒物中元素粒径分布特征[J]. 环境科学与技术, 2017, 40(6): 133-140. WANG S B, YU F, YAN Q S, et al. Size distributions of elements in atmospheric particulates of the typical background region[J]. Environmental Science and Technology, 2017, 40(6): 133-140(in Chinese).
[42] SONG Y, XIE S D, ZHANG Y H, et al. Source apportionment of PM2.5 in Beijing using principal component analysis/absolute principal component scores and UNMIX[J]. Science of the Total Environment, 2006, 372(1): 278-286. doi: 10.1016/j.scitotenv.2006.08.041 [43] ZHANG K, CHAI F H, ZHENG Z L, et al. Size distribution and source of heavy metals in particulate matter on the lead and zinc smelting affected area[J]. Journal of Environmental Sciences, 2018, 71: 188-196. doi: 10.1016/j.jes.2018.04.018 [44] 王士宝, 姬亚芹, 李树立, 等. 天津市春季道路降尘PM2.5和PM10中的元素特征[J]. 环境科学, 2018, 39(3): 990-996. WANG S B, JI Y Q, LI S L, et al. Characteristics of elements in PM2.5 and PM10 in road dust fall during spring in Tianjin[J]. Environmental Science, 2018, 39(3): 990-996(in Chinese).
[45] 虎彩娇, 成海容, 李锦伦, 等. 黄石市大气PM10和PM2.5中元素特征及重金属生态风险评价[J]. 环境化学, 2018, 37(1): 138-145. doi: 10.7524/j.issn.0254-6108.2017053106 HU C J, CHENG H R, LI J L, et al. Characteristics of elements and ecological risk assessment of heavy metals in PM10 and PM2.5 in Huangshi[J]. Environmental Chemistry, 2018, 37(1): 138-145(in Chinese). doi: 10.7524/j.issn.0254-6108.2017053106
[46] 周安琪, 刘建伟, 周旭, 等. 北京大气PM2.5载带金属浓度、来源及健康风险的城郊差异[J]. 环境科学, 2021, 42(6): 2595-2603. ZHOU A Q, LIU J W, ZHOU X, et al. Concentrations, sources, and health risks of PM2.5 carrier metals in the Beijing urban area and suburbs[J]. Environmental Science, 2021, 42(6): 2595-2603(in Chinese).
[47] SAH D, VERMA P K, KANDIKONDA M K, et al. Pollution characteristics, human health risk through multiple exposure pathways, and source apportionment of heavy metals in PM10 at Indo-Gangetic site[J]. Urban Climate, 2019, 27: 149-162. doi: 10.1016/j.uclim.2018.11.010 [48] 邢琼予, 戴启立, 毕晓辉, 等. 我国中西部典型城市PM2.5中痕量金属的时空分布特征和健康影响[J]. 中国环境科学, 2019, 39(2): 574-582. doi: 10.3969/j.issn.1000-6923.2019.02.016 XING Q Y, DAI Q L, BI X H, et al. Temporal-spatial variation and health effects of trace metals in PM2.5 in four central-western cities of China[J]. China Environmental Science, 2019, 39(2): 574-582(in Chinese). doi: 10.3969/j.issn.1000-6923.2019.02.016
-




 DownLoad:
DownLoad: