-
随着我国纺织印染行业的高速发展,纺织印染废水已经成为重要的工业废水排放来源. 据统计,我国染料年产量达到77万—79万t,约占全世界总产量的2/3[1]. 印染纺织废水具有成分复杂、色度高、可生化性差等特性,成为难处理工业废水之一. 活性红3BS是一种典型偶氮染料被广泛的应用于纺织印染行业中,对水体中的各类生物具有强烈的毒害作用,经过食物链富集进入人体后可以引起人类恶性肿瘤病变,引发各种恶性疾病[2].
染料的降解工艺主要包括生物法、物理法和化学法. 生物法具有成本低、环境友好等优点,但微生物容易被染料的毒性抑制,对高浓度染料废水去除效果并不理想;物理法主要是利用吸附剂的高比表面积将液相中的污染物吸附至固体表面或内部孔道,对多种类型的染料具备处理能力,但没有实现从根本上消除污染物,吸附剂的再生和处置可能会造成二次污染等问题[3]. 因此,基于硫酸根盐自由基(SO4·−)的高级氧化技术因其能高效、快速降解水体各类高浓度染料而受到广泛关注与研究[4]. 一般而言,激活过一硫酸盐(PMS)产生SO4·−的方法包括超声、光辐射、紫外光等,耗能较大且对设备要求较高[5];而在均相反应中引入过渡金属虽然能够提高催化效果,但又易造成金属离子溶出形成污染[6]. 因此,制备碳基载铁改性材料作为非均相催化剂既可有效激活PMS增强降解效率[7],又能避免金属离子的二次污染. 除此之外,磁性生物炭的磁响应特征可以提高催化材料的可回收率[8],具有较高的应用研究价值.
本文通过生物沥滤将离子态铁负载到生物炭上,通过对铁负载材料进行二次热解改性制备出具有磁性的铁基生物炭(Fe3O4@BC)用于高浓度染料废水脱色研究. 生物沥滤驱动制备的磁性生物炭相较于传统方法简洁高效,为磁性生物炭的制备提供了新的的方法与路径.
-
氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans,简称A.f 319)保存于武汉纺织大学微生物实验室. 使用改良后的9K培养基配方:KCL:0.1 g·L−1, (NH4)2SO4 :3 g·L−1 ,K2HPO4:0.5 g·L−1 ,MgSO4·7H2O :0.5 g·L−1,FeSO4·7H2O:40.0 g·L−1. 初始pH调至3.0. 实验所使用的活性红3BS、过一硫酸盐(PMS)、等试剂购于国药集团化学试剂有限公司. 生物炭材料来自湖北省通山县农业秸秆和木材气化副产物.
-
将活化后的A.f 319添加入生物炭材料的9 K培养基中富集培养,60 h后抽滤分离,60 ℃烘干备用. 该生物炭材料命名为BBC. 将烘干后的BBC放入管式炉中热解,升温至700 ℃,全程氮气气氛保护,升温速率5 ℃·min−1,保温1 h. 温度降至室温后取出,使用去离子水反复清洗烘干备用,该材料标注为PBC.
-
本实验使用扫描电子显微镜(Zeiss Gemini 300 ,德国Zeiss)分析材料的形貌特征;X射线衍射仪(Bruke D8 Advance ,德国Bruker )和傅立叶红外光谱仪(Thermo Scientific Nicolet 6700,美国)分析材料晶体结构和表面官能团;X射线光电子能谱技术(Thermo Scientific K-Alpha,美国 Thermo Scientific)分析材料表面元素及价态变化.
-
染料浓度设置为200 mg·L−1,考察BC、BBC、PBC不同材料(添加量固定为1 g·L−1)对活性红3BS吸附实验;染料浓度设置为200 mg·L−1,考察BC、BBC、PBC不同材料(添加量固定为1 g·L−1)PMS(添加量固定为0.5 g·L−1)对活性红3BS的催化降解实验.
活性氧化物种猝灭实验是先将猝灭剂加入200 mg·L−1的活性红3BS的溶液中再进行催化降解实验. 选取甲醇(MeOH)、叔丁醇、对苯醌、L-组氨酸对·OH和SO4·−、·OH、·O2、1O2进行淬灭.
催化剂重复使用性能实验是在反应后进行固液分离,对分离出的催化剂使用超纯水多次冲洗,放入真空干燥箱干燥,循环5次.
-
图1(a)、(b)所示为黄钾铁矾负载于生物炭上的扫描电镜图. 结晶状的黄钾铁矾负载于生物炭上,结晶颗粒呈现不规则的块状,粒径大小从0.5—1 μm不等,经ICP测试载铁含量达到197.6 mg·g−1 . 生物沥滤将离子态铁负载到了生物炭上,可能的反应见式(1—3)[9]:
图1(c)、(d)为热解过后的生物炭,SEM可观察到黄钾铁矾的晶体形态发生了变化,晶体粒径变小,金属颗粒均匀的分散在生物炭上,以更加规整的圆形或椭圆形附着,无明显的团聚.
-
用N2-BET对BC、BBC、PBC的比表面积和孔容孔径进行分析. 结果表明,PBC的比表面积(147.621 m2·g−1)相比BBC(52.743 m2·g−1)和BC(41.090 m2·g−1)显著提高(P<0.05),证明了Fe3O4负载于生物炭上可以提高材料的比表面积,增加有效的吸附点位,促进污染物在材料表面的吸附.
-
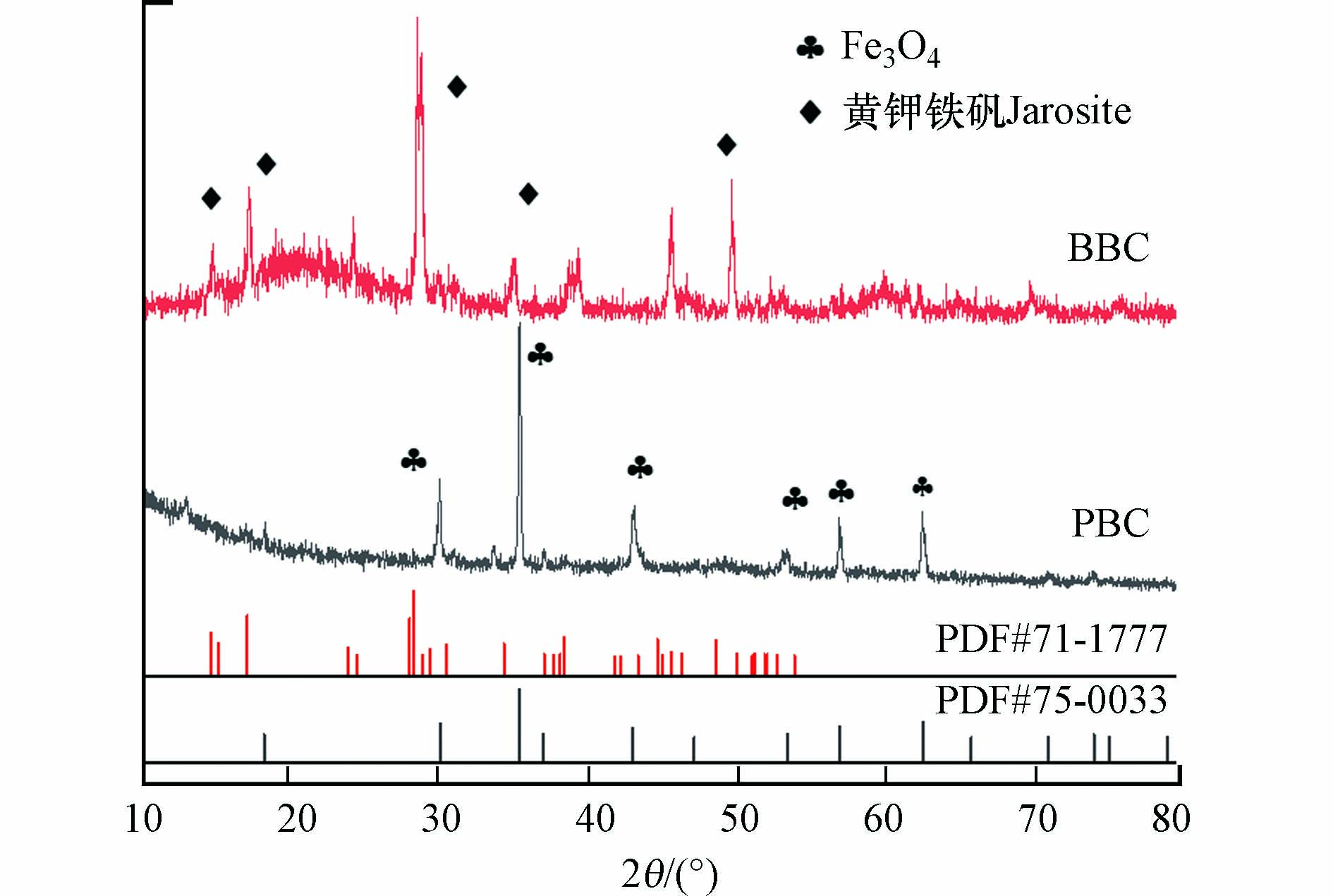
图2为负载黄钾铁矾的生物炭(BBC)与热解后的磁性生物炭(PBC)XRD图谱. BBC的主衍射峰与黄钾铁矾标准卡片PDF#71-1777中的17.4°、28.6°、28.9°、46.8°、49.9°高度吻合,表明黄钾铁矾被成功的负载于生物炭上. Fe3O4的衍射峰在29.9°、35.3°、43.1°、53.4°、57.2°和62.5°对应纯立方尖晶结构的(220)、(311)、(400)、(422)、(511)和(440)晶面,这些结果对应标准卡片PDF#75-0033,可以证明该材料为Fe3O4. 结合SEM图可以看出Fe3O4的比表面积明显大于热解前,暗示着在激活PMS产生自由基的催化反应中具有更好的活性位点[10].
-
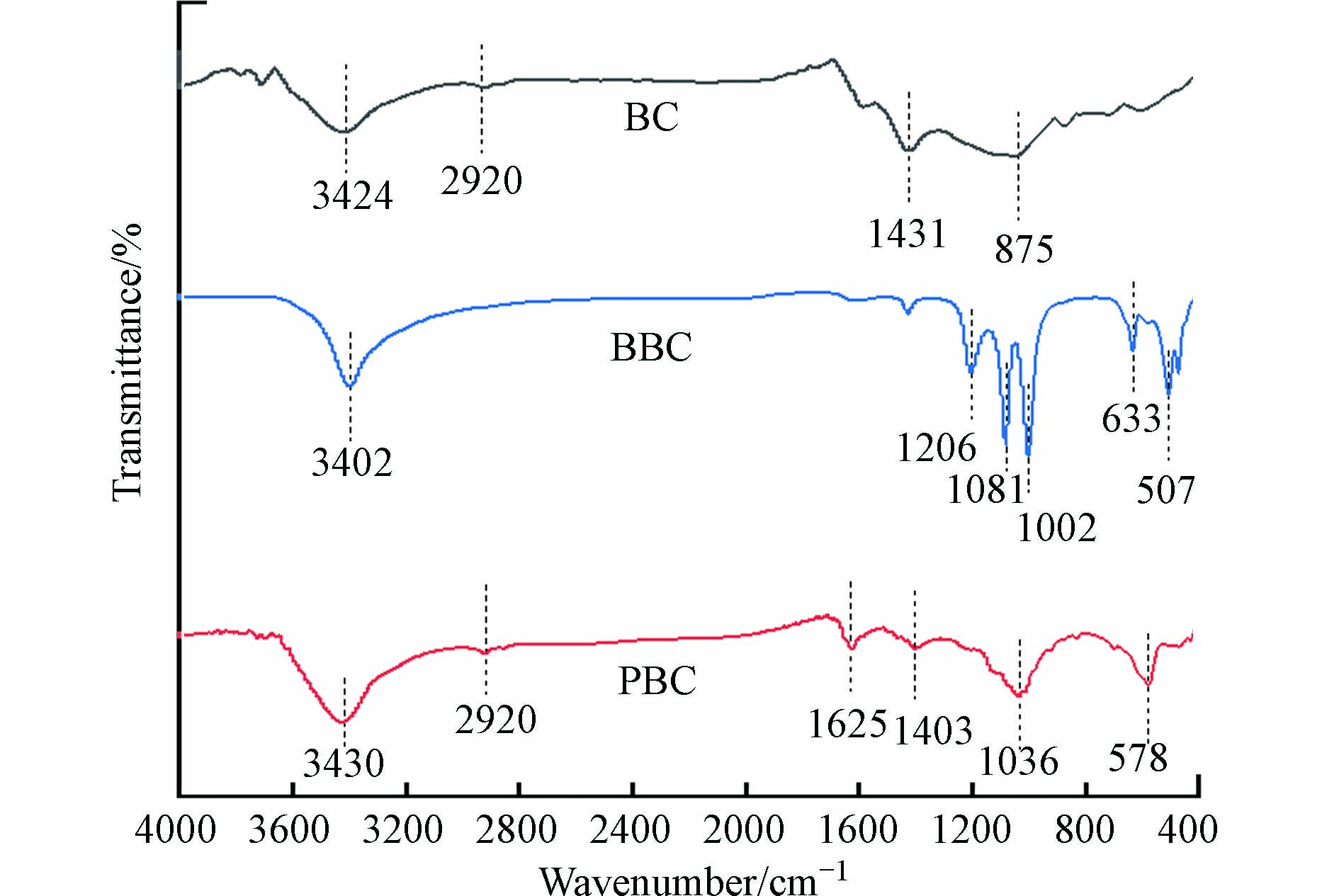
傅里叶红外光谱(FTIR)分析结果表明: BC、BBC和PBC的主要官能团有O—H、C—H、C=O和C—O组成(图3). 其中在3424 cm−1处的特征峰归证实存在O—H的伸缩振动,2920 cm−1处的特征峰归属于C—H的弯曲振动峰[11],1625 cm−1处的特征峰是C=O的伸缩振动,1036 cm−1处是C—O的伸缩振动特征峰[12]. BBC在1000 cm−1到1500 cm−1产生了大量的C—O组,507 cm−1处和633 cm−1处特征峰应归属于Fe—O特征峰. PBC的FTIR谱图显示在578 cm−1出现了属于Fe—O的典型特征峰[13].
-
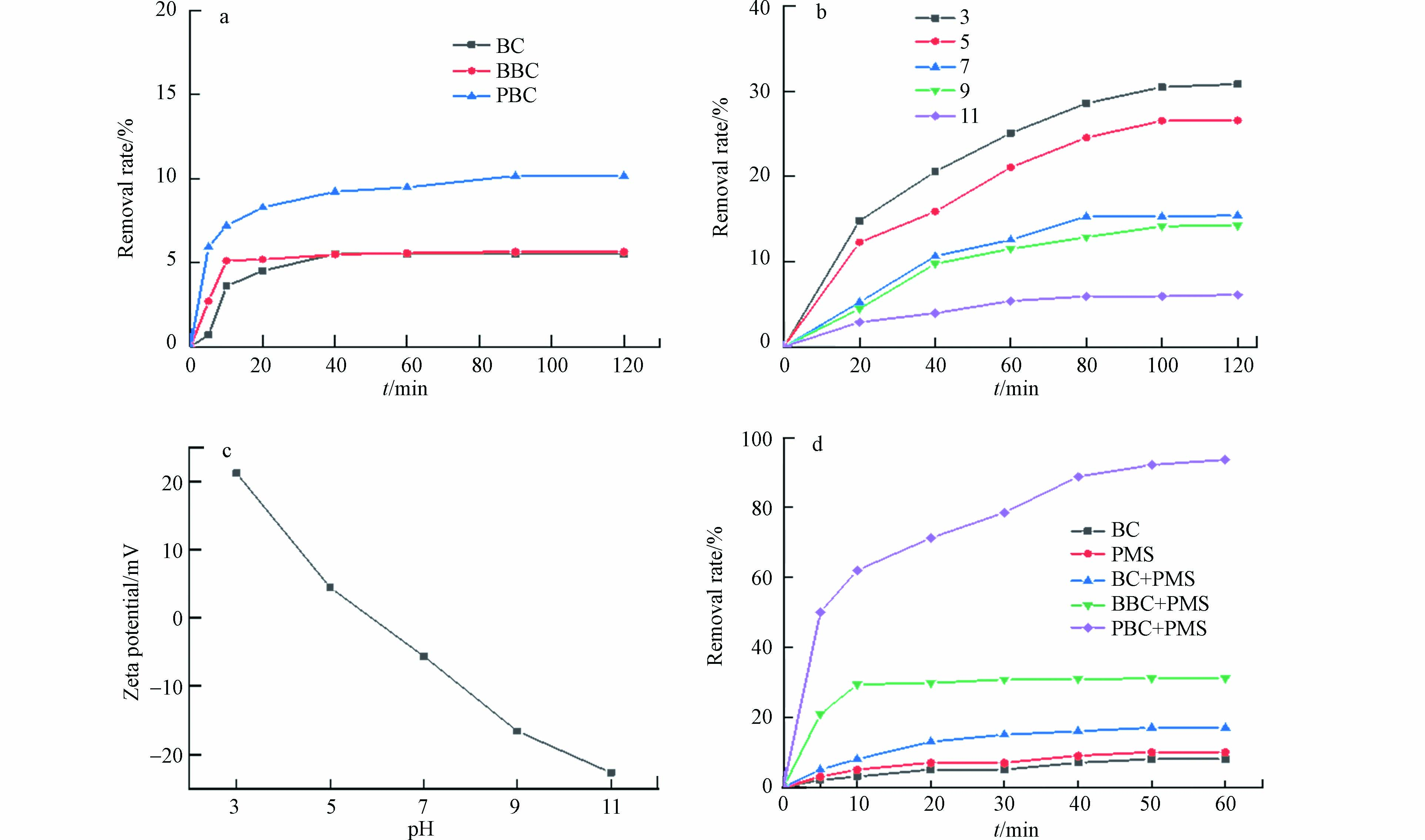
与BC和BBC相比,PBC显著提高了对活性红3BS(200 mg·L−1)的吸附效果,吸附能力分别提高了84.1%和79.5%(见图4a),Fe3O4的载入改善了生物炭的孔隙结构,提高材料的比表面积(表1),增强PBC对染料的吸附性能. 探讨了PBC在pH 3—11的范围内对染料的吸附作用,结果表明pH的增加会导致吸附效果逐渐下降(图4b). 结合Zeta电位结果(图4c),pH较低时碳材料表面带有强烈的正电荷,更容易吸附阴离子染料;随着pH的升高,碳材料表面去质子化带负电,与阴离子染料产生静电排斥从而降低了染料的去除效率[14].
PBC激活PMS对染料的催化降解能力明显优于BC、BBC以及单一的PMS,该反应体系在60 min内对200 mg·L−1染料去除率可达93.8 %(图4d),降解效率优于部分文献报道[15]. Fe3O4负载于生物炭表面不仅增强了对染料的吸附性能,而且能够通过Fe3O4中Fe2+和Fe3+电子穿梭进一步激活PMS产生更多活性物种,提高复合材料的协同降解能力. 在反应60 min后,活性红3BS的TOC去除率达到了67.1 %,这表明仍有部分物质没有被完全矿化[16].
-
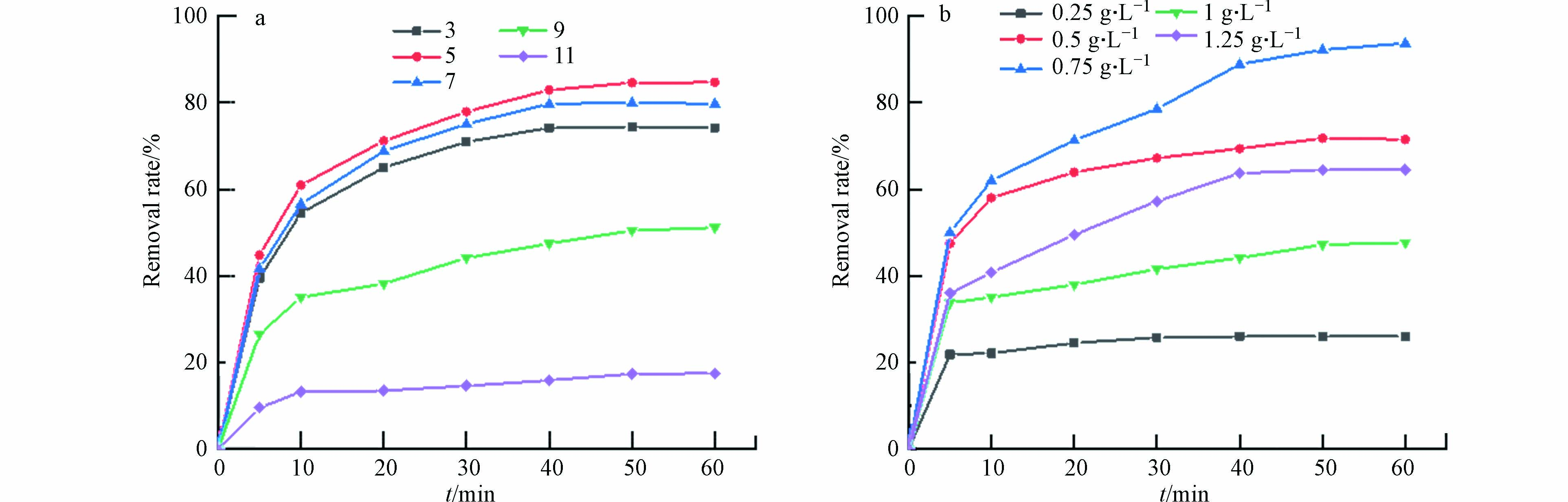
pH的变化会对Fe3O4@BC/PMS降解活性红3BS产生显著影响. 由图5(a)可知,在弱酸性条件下Fe3O4@BC对PMS的激活效果较好,pH为5时60 min内的降解率达到了84.69 %. 碱性条件下,随着pH的升高降解效率显著下降,推测是pH偏高时Fe3O4@BC表面的活性位点发生钝化,促进铁离子形成氢氧化铁沉淀,减弱了PBC对染料的吸附能力,同时降低了PMS产生自由基的能力.
PMS投加量的增加可以提高活性红3BS的去除效率. 当PMS的投加量增加到0.75 g·L−1时,对染料的去除率达到93.8 %. 然而,当PMS的投加量继续提高,污染物的降解效率却不增反降. 分析原因,可能是过量的PMS会在短时间内产生大量的·OH和SO4·−与PMS自身产生淬灭反应,生成了氧化能力较弱的SO5·−,导致了SO4·−的利用率降低[17].
-
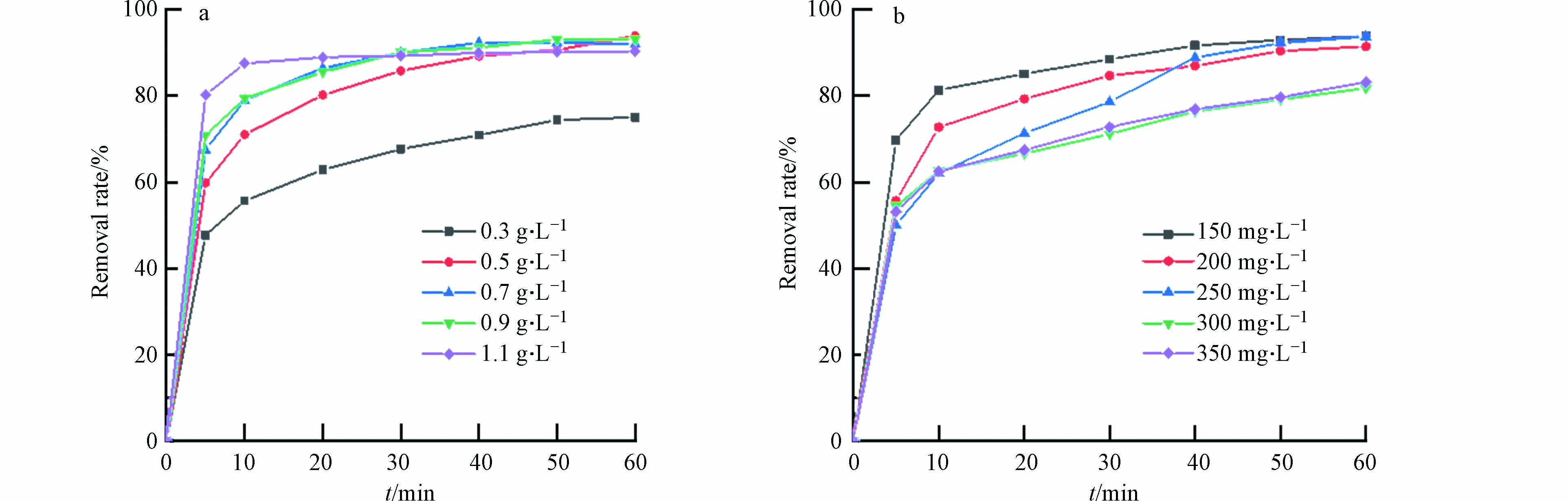
随着催化剂用量的增加,材料对活性红3BS的去除率也会逐步提升. 如图6(a)所示,当催化剂用量为0.5 g·L−1时,去除率达到了93.8 %. 继续增加催化剂的投加量,发现去除效果并不明显,这可能是该体系下PMS不足导致.
污染物的初始浓度升高对降解率影响并不显著. 如图6(b)所示,当污染物的初始浓度由150 mg·L−1增加到350 mg·L−1,60 min内污染物的降解率由95 %只下降到了81.8 %,可见Fe3O4@BC对高浓度染料废水也有较好的催化降解效果.
-
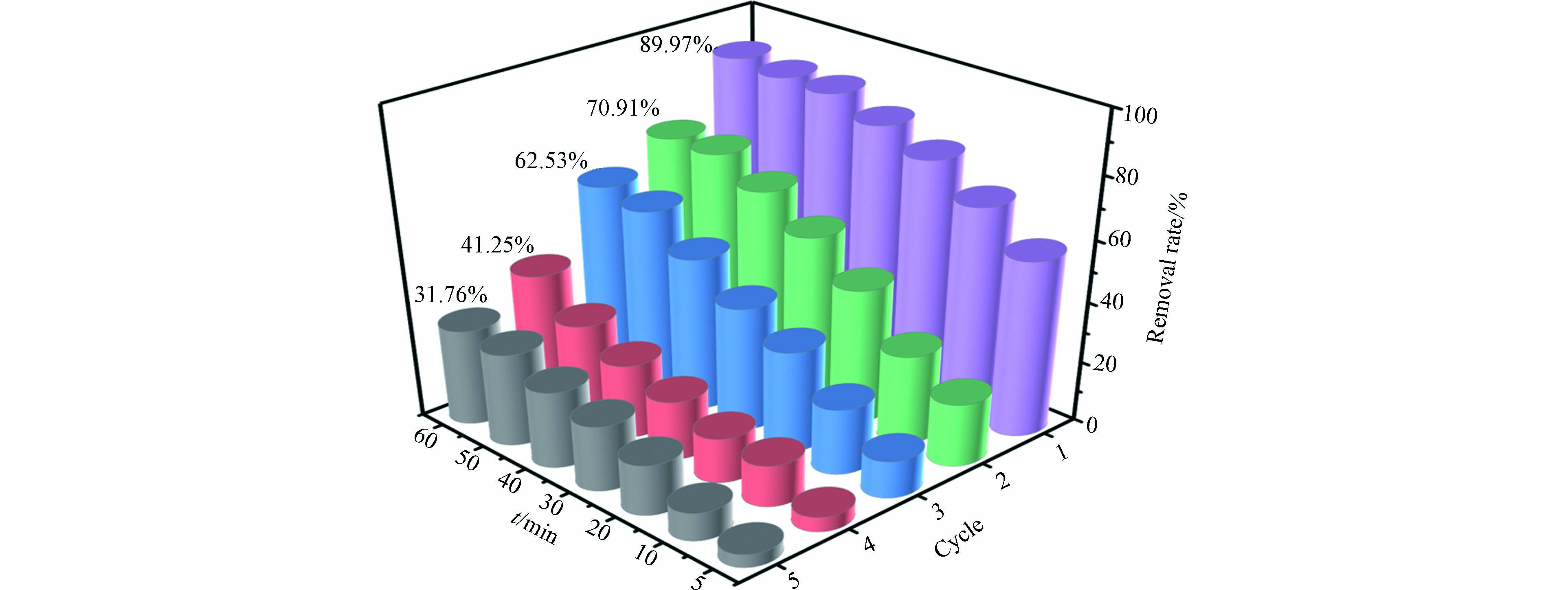
Fe3O4@BC在5次循环利用之后对活性红3BS仍然有一定的催化降解效果. 如图7所示,第一次实验活性红3BS降解率最高,污染物可以被大部分去除;第二次循环使用后,去除率达到70.91%;在随后的第3、4、5次循环中,去除率逐步下降,原因是反应过程中生物炭上的Fe3+和Fe2+循环参与对PMS的活化,造成铁离子溶出,导致了催化活性降低. 5次循环利用之后对污染物的降解率依然能够达到31.76 %,说明该材料是一种具有一定重复利用性的磁性催化剂.
-
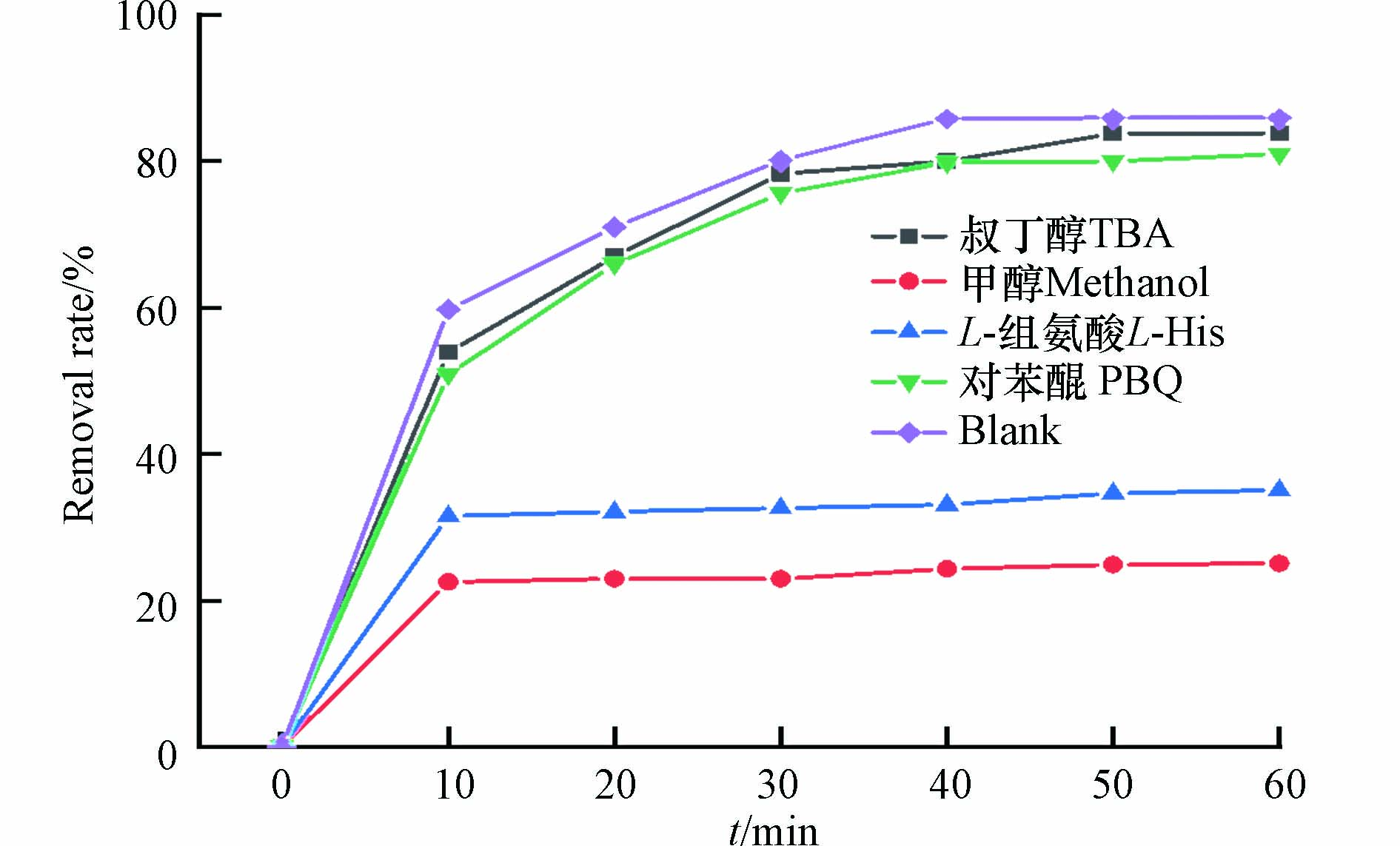
自由基淬灭实验确定磁性催化剂激活PMS起主要作用的自由基活性组分. 淬灭剂选用甲醇(MeOH)、叔丁醇(TBA)、对苯醌(PBQ)、L-组氨酸进行活性氧化物种猝灭实验. 甲醇是一种常见的·OH和SO4·−的自由基猝灭剂,二级反应速率常数k[MeOH,·OH]=9.7×108 mol·L−1·s−1,k[MeOH, SO4−·]=3.2×106 mol·L−1·s−1;叔丁醇是常用的·OH猝灭剂,反应常数k[·OH,TBA]=(3.8—7.6×108 mol·L−1·s−1);对苯醌可以抑制超氧自由基(·O2−), 反应速率常数为k[·O2−,PBA]=(1.0×109 mol·L−1·s−1);L-组氨酸捕获(1O2)的反应速率常数为1.6×106 mol·L−1·s−1[18].
图8展示了不同自由基淬灭剂对磁性生物炭活化PMS降解染料的影响. 投加叔丁醇和对苯醌对染料的去除并没有较大影响;投加甲醇会使染料的去除率下降60.79 %;L-组氨酸的加入会使染料的去除率下降50.82 %. 表明Fe3O4@BC/PMS体系中可能主要产生SO4−·和1O2而非·OH和·O2−[19]. 结合XPS分析反应前后 PBC 的化学价态变化(图9),PBC 拟合出的709.6 eV(Fe2+)和712.9 eV(Fe3+)两组峰,Fe2+和Fe3+的含量分别为66.1 %和33.9 %,反应后Fe2+的含量降低到了37.4 %,说明Fe3O4上颗粒的Fe3+和Fe2+存在电子转移机制,转化过程中的电子转移加速了污染物的降解[20]. 除此之外,生物炭表面的缺陷点位和部分官能团也可以作为活性点位活化PMS.
根据上述分析推测可能的降解机制. Fe3O4@BC活化PMS降解染料的机制主要包括自由基途径(SO4−·)和非自由基途径(1O2). 可能的反应过程见式(4—7):
-
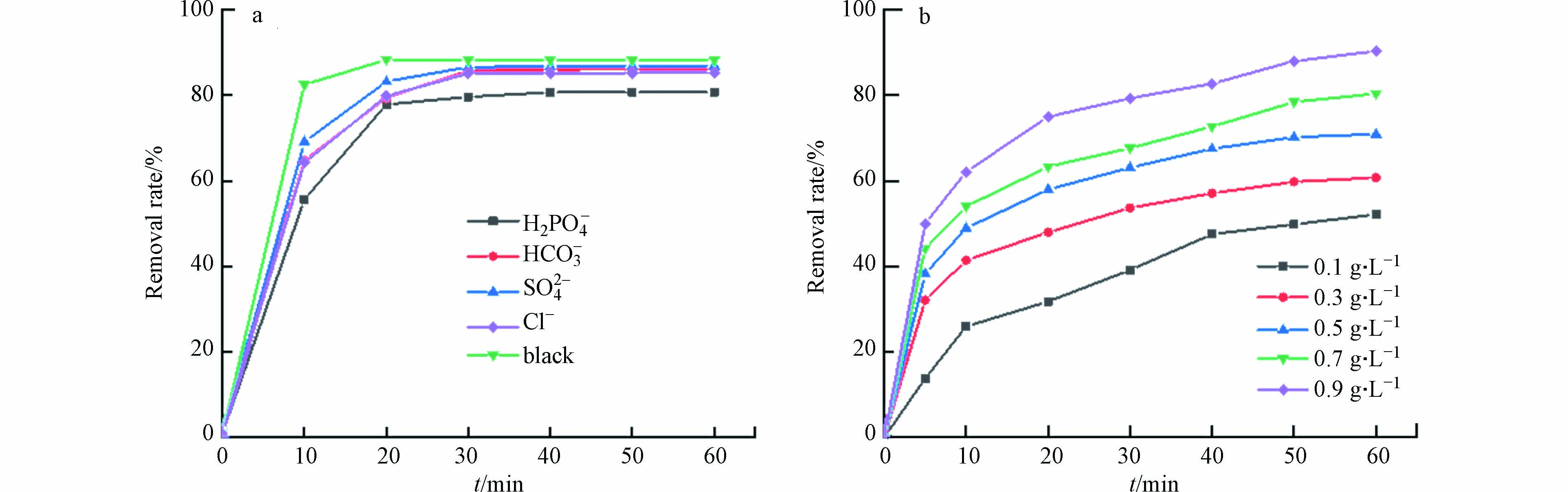
无机阴离子普遍存在于染料废水中,并且会对染料的降解效果产生影响[21]. 本实验选取了Cl−、HCO3−、SO42-和H2PO4−作为干扰离子,探究这些离子对活性红3BS催化降解的影响. 实验结果如图10(a)所示:干扰离子的添加对降解效率产生影响,尤其是H2PO4−的存在会使降解效率从88.2%下降到80.7%. 其原因可能是:(1)这些无机离子的引入会与染料竞争Fe3O4@BC上的活性位点;(2)无机离子可以清除体系中的自由基.
为考察Fe3O4@BC/PMS体系对其他类型染料降解能力,选取难降解蒽醌类染料亚甲基蓝作为目标污染物. 结果显示Fe3O4@BC/PMS体系对100 mg·L−1的亚甲基蓝具有良好的去除效果,催化剂投加量为0.9 g·L−1时,60 min内对亚甲基蓝的降解效率可以达到90.3%.
-
本文利用生物沥滤将离子态铁负载到生物炭上,对铁负载生物炭二次热解改性,成功制备出具备磁性效应的铁基生物炭. Fe3O4@BC/PMS体系相较于原始生物炭的催化降解能力显著提升,对几种类型染料具有催化降解能力,多次循环利用后仍然保持较高的降解效率. 自由基猝灭实验探讨了复合材料对染料的降解机制,Fe3O4@BC/PMS体系中SO4−·和1O2主导了对染料的降解过程. 结果表明Fe3O4@BC材料在处理难降解的染料废水方面具有较高的应用前景,本研究为磁性生物炭改性材料处理染料废水方面提供了新方法.
生物沥滤法制备Fe3O4@BC协同PMS对活性红3BS染料的降解
Study on the decolorization effect of bioleaching-driven Fe3O4@BC-activated PMS on reactive red 3BS
-
摘要: 磁性生物炭的制备方法包括物理法和化学法,制备要求较高. 本文通过生物沥滤将离子态铁负载到生物炭上,对铁负载生物炭二次热解改性,运用SEM、XRD、XPS、FTIR等手段对材料进行表征,制备出具有磁性的铁基生物炭(Fe3O4@BC). 研究材料改性前后及协同PMS对活性红3BS染料的降解过程及机理,探讨了环境因素对染料降解效果的影响,在最佳反应条件下,协同作用对200 mg·L−1的活性红3BS染料废水脱色效果达到93.8 %. 自由基猝灭实验证实反应机理是Fe3O4@BC/PMS体系中自由基和非自由基途径生成的SO4·−和1O2参与了对染料的协同降解. 五次循环利用后催化体系对染料的降解效率仍能达到31.2 %. 本研究为磁性生物炭在高浓度染料废水处理方向提供了新的方法和路径.Abstract: The preparation methods of magnetic biochar include physical and chemical methods with high preparation requirements. In this paper, iron-based biochar (Fe3O4@BC) with magnetic properties was prepared by loading ionic iron onto biochar through bioleaching, modifying iron-loaded biochar by secondary pyrolysis, and characterizing the material by using SEM, XRD, XPS, and FTIR. The degradation process and mechanism of reactive red 3BS dyestuff before and after material modification and synergistic PMS were investigated, and the influence of environmental factors on the degradation effect of dyestuff was discussed. Under the optimal reaction conditions, the synergistic effect on decolorization of 200 mg·L−1 reactive red 3BS dyestuff wastewater reached 93.8%. The free radical burst experiments confirmed the reaction mechanism that SO4·− and 1O2 generated by free radical and non-free radical pathways in the Fe3O4@BC/PMS system were involved in the synergistic degradation of the dye. The degradation efficiency of the catalytic system for the dye could still reach 31.2% after five cycles of recycling. This study provides a new method and pathway for magnetic biochar in the direction of high concentration dye wastewater treatment.
-
Key words:
- bioleaching /
- magnetic biochar /
- PMS /
- Azo dyes /
- decolorization
-
氯代多环芳烃(Cl-PAHs)是饮用水氯消毒[1]、电子垃圾的处理[2-3]、金属冶炼[4]、垃圾焚烧[5-6]以及烹饪[7]等人类活动过程中产生的副产物,它具有与多氯联苯和二噁英相似的平面结构和类似的环境行为[8],其毒性与多环芳烃母体相当甚至高于母体。目前已在大气[9-10]、沉积物[11]、汽车尾气[12]、冶炼厂废气[4]、垃圾焚烧厂的飞灰和烟道气[6]及烧烤食品[7]中检测到氯代多环芳烃。氯代多环芳烃作为一类新型的高风险有机污染物广泛存在于环境中,对人类健康具有一定的潜在威胁。
氯代多环芳烃(Cl-PAHs)和多环芳烃(PAHs)主要通过工业废水排放和大气沉降进入地表,造成土壤污染。低水溶性和相对较高的辛醇-水分配系数(lgKow)可导致其在土壤中的积累。目前土壤中多环芳烃的测定方法有索氏抽提-高效液相色谱法[13]、微波萃取-高效液相色谱法[14]、加速溶剂萃取气相色谱-质谱法[15-16] 、加速溶剂萃取高效液相色谱法[17] 等。土壤中氯代多环芳烃的测定方法主要有加速溶剂萃取气相色谱-质谱法[18-19]、超声萃取高效液相色谱法[3]、索氏抽提萃取气相色谱-质谱法[20] 等。加速溶剂萃取设备昂贵;索氏抽提虽然设备简单但要消耗大量的有机溶剂。此外这些方法均需要进一步的浓缩、净化,操作过程繁琐,费时费力。因此发展一种简便、快速、成本低廉、环境友好的样品前处理方法对于土壤中氯代多环芳烃(Cl-PAHs)和多环芳烃的测定很有意义。
超分子溶剂(supramolecular solvent, SUPRAS)是指含亲水基和疏水基的两亲性分子在水溶性有机溶剂作用下分散在水相中,通过疏水相互作用按照一定的顺序形成的一种具有纳米结构的胶束聚集体。超分子溶剂微萃取(supramolecular solvent-based microextraction, SSBME)是由西班牙学者Rubio 等[21]提出的一种以超分子溶剂为萃取剂的新型萃取技术。超分子溶剂的一个显著特点是其具有高浓度的亲和位点,使其在较小的溶剂体积下能取得高的萃取效率,因此特别适用于微萃取;此外超分子溶剂具有纳米孔腔结构,它可以使小分目标化合物进入其中,但对腐殖酸、蛋白质、糖类等大分子具有限制进入作用,从而在萃取的同时可以达到净化的目的;超分子溶剂还有一个优点,它具有非挥发性和不易燃性,使用安全。超分子溶剂微萃取具有简便、快速、环境友好、成本低廉等优点,已经在环境、食品等领域得到了广泛应用。目前已用于鱼和贝类中噁喹酸和氟甲喹[22]、水中磺胺类[23]、生小麦中的赭曲霉毒素A[24]、人尿液中羟基多环芳烃[25]等化合物的分析。
本文尝试采用SSBME结合高效液相色谱法建立一种同时测定土壤中氯代多环芳烃(Cl-PAHs)和多环芳烃(PAHs) 的简便快速方法。
1. 实验部分(Experimental section)
1.1 仪器与试剂
Agilent 1200 型高效液相色谱仪( 美国安捷伦公司),配二极管阵列紫外和荧光检测器;Vortex Genie 2涡旋振荡器 (美国 Scientific Industries);KMS-181E 磁力搅拌器(精凿科技上海有限公司);飞鸽牌TDL-4013离心机(上海安亭科学仪器厂);乙腈(LC- grade,美国 Honeywell 公司);实验用水为经Milli-Q净化系统制备的去离子水。1-己醇、1-庚醇、1-辛醇、四氢呋喃购于阿拉丁试剂(中国)有限公司,纯度 ≧98.0%;1-葵醇购于梯希爱(上海)化成工业发展有限公司,纯度 98.0%。
16种多环芳烃混标(200 µg·mL−1,其中苊烯无荧光,不在测定之列)及2-氯蒽、9-氯菲、9-氯蒽、9,10-二氯蒽、1-氯芘(纯度大于95%)均购于百灵威化学试剂有限公司。
1.2 色谱条件
色谱条件:色谱柱为多环芳烃专用分析柱(SUPELCOSILTMLC-PAH,150 mm×4.6 mm, 5 μm);流动相为乙腈-水,采用梯度洗脱,乙腈变化为:0—18 min,40%—64%;18—25 min,64%;25—35 min,64%—100%;35—44 min,100%。流速为2 mL·min−1; 进样量10 μL。
20种目标化合物的荧光激发和发射波长见表1,高效液相色谱图见图1。
表 1 荧光激发和发射波长Table 1. Fluorescent Excitation wavelength and Emission wavelength时间/min Time 激发波长/nm Ex 发射波长/nm Em 0.00 275 330 13.90 255 375 17.90 245 450 19.80 245 370 23.50 265 390 32.40 273 440 36.50 290 410 38.50 240 480 40.00 265 420 1.3 供试土壤样品的制备
40 g 风干的山参种植土用100 mL 丙酮-二氯甲烷(1:1)超声提取3次后,加入100 mL含2400 ng 氯代多环芳烃和多环芳烃的丙酮-二氯甲烷(1:1)溶液,搅拌混匀后于通风橱中氮气吹至近干,继续放置干透后储存于磨口玻璃瓶。此土壤样品含目标化合物60 ng·g−1,用于超分子溶剂的制备及萃取的优化。
1.4 超分子溶剂的制备
移取3 mL1-辛醇于50 mL聚四氟乙烯离心管中,加入8 mL四氢呋喃、29 mL去离子水,然后以900 r·min−1磁力搅拌5 min,静置2 min后3000 r·min−1 离心5 min,用玻璃滴管将上层形成的超分子溶剂转移到具塞玻璃瓶中,放于冰箱4 ℃储存备用。
1.5 超分子溶剂微萃取过程
于5 mL 聚丙烯离心管中加入200 mg 土壤,3粒玻璃珠(3 mm直径),加入400 μL 超分子溶剂,3200 r·min−1蜗旋振荡2 min,然后5000 r·min−1 离心5 min,用1 mL注射器移出上清液,过0.22 μm 滤膜后高效液相色谱测定。
1.6 标准工作曲线用标准样品制备
将16种多环芳烃混标和5种氯代多环芳烃用乙腈配制成10000 µg·L−1的混标储备溶液,并逐级稀释成1000、100、10 ng·mL−1使用液。将此混标使用溶液添加到用丙酮-二氯甲烷(1:1)超声提取过的空白山参种植土中,使添加浓度分别为2.5 、10 、50 、 250、500、1000 ng·g−1, 4 ℃冰箱放置过夜,然后按1.5节方法萃取,用于标准工作曲线的测定。
2. 结果与讨论(Results and discussion)
2.1 萃取条件的优化
以添加60 ng·g−1,目标化合物的200 mg供试土壤样品为萃取对象,以目标化合物的峰面积为指标,考察了超分子溶剂的组成(脂肪醇种类、脂肪醇的量、四氢呋喃量)、萃取溶剂体积、涡旋振荡时间等因素对萃取效率的影响。
2.1.1 不同链长脂肪醇制备的超分子溶剂对萃取效率的影响
超分子溶剂通常由两亲分子在分散剂存在下在水相体系中通过自组装生成。本研究采用烷基醇与四氢呋喃制备超分子溶剂。为此恒定总体积为40 mL,考察了1.5 mL1-己醇、1-庚醇、1-辛醇、1-葵醇在水中分别与8 mL四氢呋喃制备的超分子溶剂对萃取效率的影响。结果表明随着脂肪醇碳链的增加,制备的超分子溶剂萃取效率逐渐增大。超分子溶剂中有两类亲和位点,一种是极性端羟基产生的氢键作用力,另一种是醇碳链部分的疏水作用力(范德华力、色散力)。对于萃取多环芳烃及氯代多环芳烃这类非极性和弱极性化合物而言,醇碳链部分的疏水作用力起主要作用,而碳链越长,这种作用力越强,因而萃取效率越大。但实验发现1-葵醇制备的超分子溶剂导致部分目标化合物色谱峰展宽且重叠,无法准确定量。故以下实验选1-辛醇制备超分子溶剂。
2.1.2 1-辛醇用量对超分子溶剂体积和萃取效率的影响
四氢呋喃的量保持8 mL,制备体系总体积为40 mL,考察了1-辛醇用量为0.5、1、1.5、2、2.5、3 mL时对萃取效率的影响。结果表明,改变1-辛醇用量,对制备的超分子溶剂的萃取效率无明显影响;但是随着1-辛醇用量的增加,生成的超分子溶剂体积增大,见图2。有文献[26]报道SUPRAs的体积Y(mL) 与烷基醇的用量X(mg) 和四氢呋喃在溶液中的体积百分比Z之间呈如下关系:Y = X(0.17 + e0.0389Z),即超分子溶剂的体积与醇的用量呈线性关系,本实验结果与文献报道一致。为了一次能制备更多的超分子溶剂,选定1-辛醇用量为3 mL。
2.1.3 四氢呋喃用量对萃取效率的影响
作为超分子溶剂的组成部分,四氢呋喃的用量不仅与制备的超分子溶剂体积有关,而且对超分子溶剂的萃取效率亦有一定影响。为此固定1-辛醇用量为3 mL,制备体系总体积为40 mL,考察了不同四氢呋喃的量对萃取效率的影响,如图3所示。结果表明,四氢呋喃用量的增加对低分子量的目标化合物的萃取效率影响不大;但对于高分子量的目标化合物,随着四氢呋喃用量的增加,萃取效率增大;当四氢呋喃大于8 mL后趋于稳定。因此本实验制备超分子溶剂时选定四氢呋喃的量为8 mL。
2.1.4 超分子溶剂体积对萃取效率的影响
为取得理想的萃取结果,考查超分子溶剂体积分别为300、350、400、500、600、700、800 μL时对萃取效率的影响。结果表明,随着萃取溶剂体积的增大,目标化合物的峰面积明显下降,即检测灵敏度下降;但同时回收率逐渐增大,当超分子溶剂体积大于400 μL时回收率趋于平稳。虽然增加萃取溶剂的体积可以萃取出更多的目标化合物,提高萃取回收率,但同时也会使目标化合物在萃取相中浓度的下降,而二者相比后者影响更大,进而导致检测灵敏度下降。综合以上结果,选定萃取溶剂的体积为400 μL。
2.1.5 涡旋振荡时间的影响
涡旋振荡可以促进萃取溶剂与样品的充分接触,提高萃取效率。为此,考查了涡旋振荡时间分别为1、2、3、4、5、6、7、8 min时对萃取效率的影响,结果表明涡旋振荡时间大于2 min后,目标化合物的峰面积变化很小。
基于以上实验结果,优化后的实验条件为,以3 mL 1-辛醇、8 mL四氢呋喃和29 mL水混合制备超分子溶剂;萃取溶剂的体积为400 μL,涡旋振荡2 min。
2.2 方法的线性范围、检出限及定量限
在优化的萃取条件下,对添加 5 种氯代多环芳烃和15种多环芳烃系列浓度的空白土壤样品进行超分子溶剂微萃取,然后HPLC荧光测定,以质量浓度 C(ng·g−1)对峰面积 A 绘制校正曲线,得到20种目标化合物的线性回归方程、线性范围及相关系数;并以目标化合物的S/N=3时的浓度定义为方法的检出限,S/N=10时的浓度定义为方法的定量限,见表2。结果表明,范围内,目标化合物在2.5—1000 µg·kg−1(9-氯菲、1-氯芘在10—1000 µg·kg−1)范围内线性关系良好,线性相关系数均大于 0.999;方法的检出限为0.07—2.3 µg·kg−1,定量限为 0.2—7.0 µg·kg−1。
表 2 目标化合物的线性范围、线性方程、相关系数、检出限及定量限Table 2. Linear ranges ,regression equation, correlation coefficients(r), limits of detection (LOD, S/N=3) and limits of quantitation (LOQ, S/N=10) of target compoundsNo. 化合物Compound 线性范围/(µg·kg−1)Linear range 标准曲线方程Regression equation 相关系数R2 检出限/(µg·kg−1)LOD 定量限/(µg·kg−1)LOQ 1 萘(Na) 2.5—1000 A=0.3182C+6.4532* 0.999 0.3 0.9 2 苊(Ace) 2.5—1000 A=0.7244C+2.6573 0.999 0.6 1.8 3 芴(Fl) 2.5—1000 A=1.5523C+0.7832 0.999 0.3 1.0 4 菲(Phe) 2.5—1000 A= 1.1875C+14.6108 0.999 0.2 0.6 5 蒽(Ant) 2.5—1000 A=2.0918C+0.2058 0.999 0.2 0.8 6 荧蒽(Fu) 2.5—1000 A=0.4013C+3.0251 0.999 0.5 1.9 7 芘(Py) 2.5—1000 A=1.0748C+6.6492 0.999 0.2 0.7 8 9-氯菲(9-ClPhe) 10—1000 A=0.0600C+1.0583 0.999 2.3 7.0 9 9-氯蒽(9-ClAnt) 2.5—1000 A=0.4078C+0.8628 0.999 0.7 2.2 10 2-氯蒽(2-ClAnt) 2.5—1000 A=0.8810C+0.2803 0.999 0.5 1.5 11 苯并[a]蒽(BaA) 2.5—1000 A=1.3297C-0.4912 0.999 0.4 1.3 12 䓛(Chr) 2.5—1000 A=1.7998C+5.9356 0.999 0.2 0.6 13 1-氯芘(1-ClPy) 10—1000 A=0.2456C-0.7780 0.999 2.1 5.4 14 苯并[b]荧蒽(BbF) 2.5—1000 A=0.8110C+1.7058 0.999 0.1 0.4 15 9,10-二氯蒽(9,10-DClAnt) 2.5—1000 A=1.6689C+0.0170 0.999 0.1 0.3 16 苯并[k]荧蒽(BkF) 2.5—1000 A= 1.8488C+1.3040 0.999 0.07 0.2 17 苯并[a]芘(BaP) 2.5—1000 A=1.3673C-0.2231 0.999 0.09 0.3 18 二苯并[a,h]蒽(DahA) 2.5—1000 A=1.1604C+2.9443 0.999 0.1 0.4 19 苯并[ghi]苝(BghiP) 2.5—1000 A=0.6349C+0.3495 0.999 0.2 0.6 20 茚并[1,2,3-cd]芘(Ipy) 2.5—1000 A= 0.3413C-0.2224 0.999 0.3 1.0 * A: peak area ;C:concentration(µg·kg−1). 2.3 实际样品的测定及方法的加标回收率和精密度
用建立的超分子溶剂微萃取高效液相色谱分析方法对山参土(2018年5月采于吉林浑春某地)和大连某地环境污染土壤样品(采于2019年10月)进行了测定。并在山参土样品中添加低、中、高的3个浓度水平的混标溶液,每个浓度水平平行测定3次,结果如表3所示。结果显示,大连某环境污染样品所有目标化合物均检出,且污染严重;山参图样品中检出萘、菲、荧蒽和芘等化合物,其余目标化合物未检出;目标化合物的加标回收率为:76.5%—105.3%,相对标准偏差(RSD)0.2%—8.5%。
表 3 实际样品测定结果、方法的回收率及精密度(n=3)Table 3. Determination results in real soil samples and recoveries and precisions of methods (n=3)化合物Compound 污染土中含量/(µg·kg−1)Content of contamined soil 山参土中含量/(µg·kg−1)Content of mountain soil 加标水平/(µg·kg−1)Spiked level 加标回收率/%Recovery RSD/% 萘(Na) 63.2 8.0 10、100、1000 90.1、97.3、88.3 7.7、3.9、1.6 苊(Ace) 563.1 nd 10、100、1000 83.0、77.9、84.8 8.3、5.4、0.7 芴(Fl) 1442.5 nd 10、100、1000 102.1、86.2、85.1 5.7,3.0,0.5 菲(Phe) 11122.8 8.0 10、100、1000 80.2、91.8、87.0 3.3、1.6、0.6 蒽(Ant) 3756.6 nd 10、100、1000 88.9、77.6、78.2 5.2、0.3、0.6 荧蒽(Fu) 19443.7 3.3 10、100、1000 94.3、79.2、85.7 3.7、4.2、0.2 芘(Py) 21200 7.6 10、100、1000 78.5、100.8、95.6 7.6、2.3、0.5 9-氯菲(9-ClPhe) 2241.6 nd 10、100、1000 78.0、84.9、84.0 7.8、3.4、0.2 9-氯蒽(9-ClAnt) 4901.8 nd 10、100、1000 81.2、90.4、78.6 8.5、3.7、0.6 2-氯蒽(2-ClAnt) 7202 nd 10、100、1000 85.6、86.6、79.1 6.8、5.3、0.4 苯并[a]蒽(BaA) 8787.4 nd 10、100、1000 95.2、88.0、87.3 4.5、1.8、0.3 䓛(Chr) 7392.2 nd 10、100、1000 96.2、89.4、87.6 3.6、2.5、0.3 1-氯芘(1-ClPy) 3022.7 nd 10、100、1000 82.3、87.1、90.7 7.9、4.0、0.5 苯并[b]荧蒽(BbF) 9073.9 nd 10、100、1000 86.5、88.1、88.6 4.2、3.9、0.2 9,10-二氯蒽(9,10-DClAnt) 392.7 nd 10、100、1000 81.2、85.2、83.0 3.6、1.8、0.6 苯并[k]荧蒽(BkF) 4041.7 nd 10、100、1000 90.2、87.9、87.5 3.2、2.4、0.3 苯并[a]芘(BaP) 9703.7 nd 10、100、1000 85.0、89.3、87.6 4.2、3.1、0.4 二苯并[a,h]蒽(DahA) 2581.7 nd 10、100、1000 79.1、89.7、88.4 4.5、2.4、0.2 苯并[ghi]苝(BghiP) 8263 nd 10、100、1000 89.2、105.3、94.8 4.2、1.6、0.6 茚并[1,2,3-cd]芘(Ipy) 7178 nd 10、100、1000 78.3、79.5、76.5 6.8、7.6、2.5 * nd: not detected. 3. 结论(Conclusion)
本文建立了超分子溶剂微萃取结合高效液相色谱荧光检测技术快速测定土壤中5种氯代多环芳烃和15种多环芳烃的分析方法。方法的基质加标回收率为 76.5%—105.3%,相对标准偏差为 0.2%—8.5%。本方法简便、快速、成本低廉且环境友好,样品处理过程不超过15 min,而且一次可同时处理多个样品。本方法可用于土壤中5种氯代多环芳烃和15种多环芳烃的快速分析检测。
-
表 1 BC、BBC、PBC的比表面积和孔隙结构
Table 1. Specific surface area and pore structure of BC
样品 Sample 比表面积/(m2·g−1) Surface area 孔容/(cm3·g−1) Pore volume 平均孔径/ nm Average pore diameter BC 41.090 0.022 3.439 BBC 52.743 0.057 4.834 PBC 147.621 4.725 2.586 -
[1] 沈彧彧. 纺织行业节能减排现状与主要废水处理技术综述[J]. 中国资源综合利用, 2018, 36(1): 93-96. SHEN Y Y. Current status of energy saving and emission reduction in textile lndustry and summary of main wastewater treatment technologies[J]. China Resources Comprehensive Utilization, 2018, 36(1): 93-96(in Chinese).
[2] 王启明, 石旭, 朱茜茜, 等. 外加电场作用下希瓦氏菌对活性红3BS脱色效果研究[J]. 江西化工, 2019(1): 155-157. doi: 10.3969/j.issn.1008-3103.2019.01.038 WANG Q M, SHI X, ZHU X X, et al. Decolorization of reactive red 3BS by Shewanellaoneidensis applied electric field[J]. Jiangxi Chemical Industry, 2019(1): 155-157(in Chinese). doi: 10.3969/j.issn.1008-3103.2019.01.038
[3] OTHMAN N H, ALIAS N H, SHAHRUDDIN M Z, et al. Adsorption kinetics of methylene blue dyes onto magnetic graphene oxide[J]. Journal of Environmental Chemical Engineering, 2018, 6(2): 2803-2811. doi: 10.1016/j.jece.2018.04.024 [4] XIAO R Y, LUO Z H, WEI Z S, et al. Activation of peroxymonosulfate/persulfate by nanomaterials for sulfate radical-based advanced oxidation technologies[J]. Current Opinion in Chemical Engineering, 2018, 19: 51-58. doi: 10.1016/j.coche.2017.12.005 [5] SHAD A CHEN J, QU R J, et al. Degradation of sulfadimethoxine in phosphate buffer solution by UV alone, UV/PMS and UV/H2O2: Kinetics, degradation products, and reaction pathways[J]. Chemical Engineering Journal, 2020, 398: 125357. doi: 10.1016/j.cej.2020.125357 [6] 胡昊, 潘顺龙, 聂溪, 等. CoFe2O4的制备及其对有机膦酸的去除性能研究[J]. 环境科学学报, 2022, 42(8): 156-165. HU H, PAN S L, NIE X, et al. Preparation of CoFe2O4 as catalyst for the removal of phosphonates[J]. Acta Scientiae Circumstantiae, 2022, 42(8): 156-165(in Chinese).
[7] ZHU S S, HUANG X C, MA F, et al. Catalytic removal of aqueous contaminants on N-doped graphitic biochars: Inherent roles of adsorption and nonradical mechanisms[J]. Environmental Science & Technology, 2018, 52(15): 8649-8658. [8] HOSLETT J, GHAZAL H, KATSOU E, et al. The removal of tetracycline from water using biochar produced from agricultural discarded material[J]. The Science of the Total Environment, 2021, 751: 141755. doi: 10.1016/j.scitotenv.2020.141755 [9] 钟萍丽, 伍赠玲, 季常青, 等. 酸性矿山废水生物矿化源头控制技术研究进展[J]. 湿法冶金, 2022, 41(4): 289-294. ZHONG P L, WU Z L, JI C Q, et al. Research progress on source control technologies of biological mineralization for acid mine drainage[J]. Hydrometallurgy of China, 2022, 41(4): 289-294 (in Chinese).
[10] SUN J, ZHOU S B, HOU P, et al. Synthesis and characterization of biocompatible Fe3O4 nanoparticles[J]. Journal of Biomedical Materials Research Part A, 2007, 80A(2): 333-341. doi: 10.1002/jbm.a.30909 [11] WANG Y, YU L, WANG R T, et al. Microwave catalytic activities of supported perovskite catalysts MOx/LaCo0.5Cu0.5O3@CM (M = Mg, Al) for salicylic acid degradation[J]. Journal of Colloid and Interface Science, 2020, 564: 392-405. doi: 10.1016/j.jcis.2019.12.130 [12] HE X D, LI P Y. Surface water pollution in the middle Chinese Loess Plateau with special focus on hexavalent chromium (Cr6+): Occurrence, sources and health risks[J]. Exposure and Health, 2020, 12(3): 385-401. doi: 10.1007/s12403-020-00344-x [13] HUANG H X, GUO T, WANG K, et al. Efficient activation of persulfate by a magnetic recyclable rape straw biochar catalyst for the degradation of tetracycline hydrochloride in water[J]. Science of the Total Environment, 2021, 758: 143957. doi: 10.1016/j.scitotenv.2020.143957 [14] CELIK S, DUMAN N, SAYIN F, et al. Microbial cells immobilized on natural biomatrix as a new potential ecofriendly biosorbent for the biotreatment of reactive dye contamination[J]. Journal of Water Process Engineering, 2021, 39: 101731. doi: 10.1016/j.jwpe.2020.101731 [15] ARSLAN H, BOUCHAREB R, ARIKAN E B, et al. Iron-loaded leonardite powder for Fenton oxidation of Reactive Red 180 dye removal[J]. Environmental Science and Pollution Research International, 2022, 29(51): 77071-77080. doi: 10.1007/s11356-022-21306-7 [16] LIU J, CUI J N, ZHAO T Y, et al. Fe3O4-CeO2 loaded on modified activated carbon as efficient heterogeneous catalyst[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2019, 565: 59-69. [17] 方志勇, 郭枭杰, 周鑫, 等. Fe3O4/MoS2强化过氧化单硫酸盐活化去除2, 4-二氯苯氧乙酸[J]. 环境化学, 2022, 41(4): 1435-1443. doi: 10.7524/j.issn.0254-6108.2020122107 FANG Z Y, GUO X J, ZHOU X, et al. Removal of 2, 4-dichlorophenoxyacetic acid by Fe3O4/MoS2 enhanced PMS activation[J]. Environmental Chemistry, 2022, 41(4): 1435-1443(in Chinese). doi: 10.7524/j.issn.0254-6108.2020122107
[18] DU W Y, ZHANG Q Z, SHANG Y N, et al. Sulfate saturated biosorbent-derived nanoarchitecture as an efficient catalyst for peroxymonosulfate activation[J]. Applied Catalysis B:Environmental, 2020, 262: 118302. doi: 10.1016/j.apcatb.2019.118302 [19] YANG Y, BANERJEE G, BRUDVIG G W, et al. Oxidation of organic compounds in water by unactivated peroxymonosulfate[J]. Environmental Science & Technology, 2018, 52(10): 5911-5919. [20] WANG Q R, SHI Y X, LV S Y, et al. Peroxymonosulfate activation by tea residue biochar loaded with Fe3O4 for the degradation of tetracycline hydrochloride: Performance and reaction mechanism[J]. RSC Advances, 2021, 11(30): 18525-18538. doi: 10.1039/D1RA01640G [21] LI W Q, LI S Q, TANG Y, et al. Highly efficient activation of peroxymonosulfate by cobalt sulfide hollow nanospheres for fast ciprofloxacin degradation[J]. Journal of Hazardous Materials, 2020, 389: 121856. doi: 10.1016/j.jhazmat.2019.121856 -






 DownLoad:
DownLoad: