-
磺胺类抗生素(sulfonamides,SAs)是一类具有对氨基苯磺酰胺结构的抗菌药物,因其抗菌谱广、使用方便、价格低廉,在饲料添加剂或渔药中被经常使用. 水产养殖中,无论将药物混合在饲料中,还是直接池塘泼洒,药物都会溶于水体,而水体中残留的药物容易污染周围的河流、湖泊等自然水域[1-2]. 水环境中抗菌药物较高浓度的残留,可能会诱导细菌耐药性,对人体产生健康风险[3].
近年来,磺胺类抗生素的检测方法主要有高效液相色谱法(HPLC)[4-5]、液相色谱-串联质谱法(LC-MS/MS)[6-8]、酶联免疫分析法(ELISA)[9]等. 我国农村农业部发布了SC/T 9436-2020 《水产养殖环境(水体、底泥)中磺胺类药物的测定》,该标准提出对水产养殖环境中磺胺类药物使用液相色谱-串联质谱法进行测定[10]. 由于水体中抗生素的浓度较低,且存在大量的干扰物,因此在上机分析前需要对目标物进行分离和富集. 超高效液相色谱-串联质谱法因其检测灵敏度高、结果选择性好的特点, 已广泛应用于复杂基质中痕量物质的检测. 本文使用超高效液相色谱-三重四极杆质谱联用技术,建立了水产养殖水体中21种磺胺类药物残留量的测定方法,供相关检测人员参考使用.
-
LC-30A超高效液相色谱仪(日本岛津公司);LCMS-8045三重四极杆质谱仪,配置有加热型电喷雾离子源(HESI)及LabSolutions Ver.5.96色谱数据处理系统(日本岛津公司);超纯水仪,Milli Q型(美国Millipore公司);Oasis HLB固相萃取小柱,500 mg,6 mL(美国Waters公司).
甲醇:色谱纯,德国Merck公司产品;甲酸:色谱纯,上海安谱实验科技有限公司CNW产品;乙酸:色谱纯,美国Fisher Scientific公司产品;磺胺类药物标准物质(磺胺脒、磺胺醋酰、磺胺嘧啶、磺胺二甲嘧啶、磺胺噻唑、磺胺吡啶、磺胺甲嘧啶、磺胺对甲氧嘧啶、磺胺二甲唑、磺胺甲噻二唑、磺胺索嘧啶、甲氧苄啶、磺胺甲氧嗪、磺胺氯哒嗪、磺胺甲噁唑、磺胺间甲氧嘧啶、磺胺多辛、磺胺异噁唑、磺胺苯吡唑、磺胺地索辛、磺胺喹噁啉和磺胺邻二甲氧嘧啶-D3):德国Dr. Ehrenstorfer公司产品.
-
称取适量磺胺类抗生素的标准品,用甲醇稀释并定容,配制成100 μg·mL−1标准储备溶液,将该储备液于−20℃以下冷藏密封避光保存.
准确移取适量磺胺邻二甲氧嘧啶-D3储备溶液于容量瓶中,甲醇稀释并定容,配制成1 μg·mL−1磺胺邻二甲氧嘧啶-D3内标标准工作液. 准确移取适量各种磺胺类抗生素储备溶液于容量瓶中,用甲醇稀释并定容,配制成1 μg·mL−1混合标准中间溶液. 再移取混合标准中间溶液适量,使用初始流动相进行稀释,配制成浓度分别为5、10、20、30、40、50 ng·mL−1标准系列工作液,其中磺胺邻二甲氧嘧啶-D3内标浓度均为5 ng·mL−1.
-
准确量取200 mL(精确至0.1 mL)水样于250 mL广口玻璃瓶中,准确加入适量磺胺邻二甲氧嘧啶-D3内标标准工作液,混合均匀. 无需提取,待浓缩净化. 用5 mL甲醇和5 mL水依次活化和平衡Oasis HLB固相萃取柱,水体样品以2 mL·min−1流速过柱,1 mL实验用水淋洗,用0.1%甲酸-甲醇溶液分2次洗脱至10 mL离心管中,洗脱液最终定容至5 mL. 取200 µL洗脱液,加800 µL初始流动相稀释5倍,混匀后过 0.22 µm 微孔滤膜后进行LC-MS/MS上机分析.
-
色谱条件:Shim-pack Velox SP- C18(2.1 mm I.D.× 100 mm L, 1.8 μm)色谱柱;流动相:乙酸水溶液(V/V,1/81)(A)和0.1%甲酸-甲醇溶液(V/V)(B);梯度洗脱程序:0 min(5% B)— 1 min(5% B)—3.50 min(10% B)—13.00 min(45% B)—17.00 min(70% B)—18.00 min(70% B)—18.50 min(5% B);流速:0.45 mL·min−1;柱温30℃;进样量3 μL;总分析时间为22 min.
质谱条件: HESI正离子检测,多反应监测模(MRM)测定,主要质谱参数为:离子喷雾电压4.0 kV;雾化气:氮气3.0 L·min−1;干燥气:氮气 15 L·min−1;加热气:空气 10 L·min−1;脱溶剂管温度250℃;加热模块温度400℃;接口温度400℃;碰撞气:氩气. 磺胺类抗生素质谱参数见表1.
-
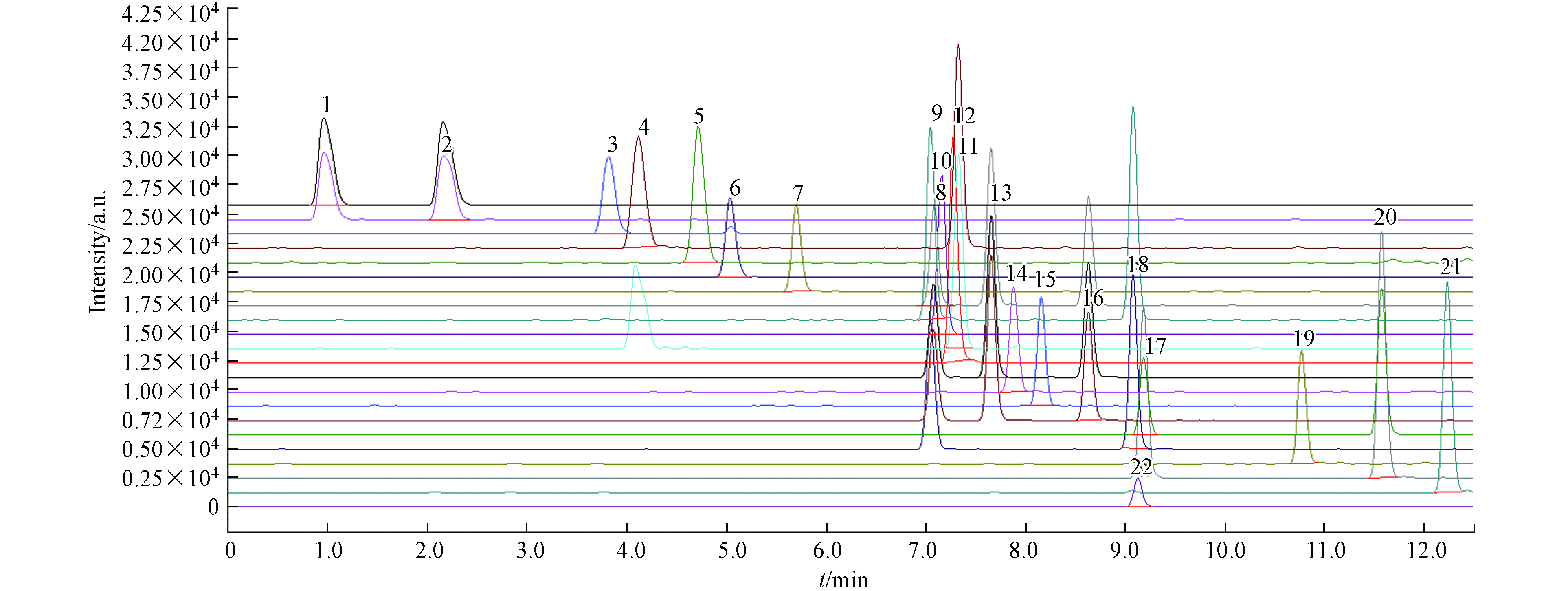
磺胺类抗生素都是以对位氨基苯磺酰胺为基本结构的衍生物,在质谱电喷雾电离(ESI)正离子模式下易形成 [M+H]+加合离子. 采用流动注射分析法,分别对21种磺胺类抗生素和磺胺邻二甲氧嘧啶-D3的单标标准溶液(1 μg·mL−1)进行一级质谱扫描(Q1 MS),得到磺胺类抗生素的前体离子. 使用LabSolutions软件自动方法优化功能,对碰撞能量和Q1、Q3预杆电压进行优化,优化后 MRM 参数参见 1.4节. 将10 ng·mL−1浓度的磺胺类抗生素混合标准工作液按1.4节进行测定,所得21种磺胺类抗生素的标准样品图谱如图1所示. 由图1可知,21种磺胺类抗生素在12.5 min之前全部出峰,各化合物峰形良好,且同分异构体均达到了基线分离.
-
将5、10、20、30、40 、50 ng·mL−1的磺胺类抗生素标准溶液,按1.4节的分析条件进行测定,使用内标法定量. 以浓度比为横坐标,峰面积比为纵坐标,绘制校准曲线. 所得校准曲线线性关系良好,相关系数r范围在0.995—0.999. 各磺胺类抗生素校准点准确度在87.7%—112.8%,其中, 校准点准确度由 A(%)=Ci/Cs×100%计算(Ci表示曲线回归方程计算得到的校准点浓度值, Cs表示真实校准点浓度值). 结果表明, 21种磺胺类抗生素在线性范围内线性关系良好, 校准点准确度较高. 以待测化合物的定量离子对色谱峰的信噪比大于或等于10(S/N≥10)的溶液浓度为该磺胺类抗生素的定量限(LOQ),本方法在水产养殖水体中21种磺胺类抗生素残留的定量限均为0.63 ng·mL−1.
-
取10、20、40 ng·mL−1的21种磺胺类药物标准工作液连续测定6次,保留时间和峰面积的重复性结果显示,磺胺脒等21种磺胺类药物保留时间和峰面积的相对标准偏差分别小于0.79%和6.61%,表明仪器精密度良好.
-
称取空白水体样品,加入少量磺胺脒等21种磺胺类抗生素混合标准品储备溶液,使水样中添加浓度为分别为1、2、5 ng·mL−1,平行做3份. 按照1.3样品前处理方法净化后,测定磺胺脒等21种磺胺类抗生素的添加回收率,各化合物的平均加标回收率结果在70.0%—110.0%之间.
-
本文建立了使用超高效液相色谱三重四极杆质谱联用系统测定水产养殖水体中21种磺胺类抗生素残留量的方法. 水体样品经过固相萃取柱净化后,采用超高效液相色谱-串联质谱法测定磺胺类抗生素. 结果表明,使用内标法定量,磺胺脒等21种磺胺类抗生素在5—50 ng·mL−1浓度范围内线性良好,各校准点准确度在87.7%—112.8%之间,且精密度和不同浓度水平的加标回收率实验结果良好. 该方法样品前处理过程简单,检测灵敏度高,分析速度快,可用于养殖水体中21种磺胺类抗生素残留量的测定和筛查. 本方法为准确评估磺胺类抗生素在环境水中残留状况提供了可靠手段.
超高效液相色谱-串联质谱法测定水产养殖水体中21种磺胺类抗生素残留量
Determination of sulfonamides in water from aquaculture environment by UHPLC-MS/MS
-
摘要: 本文建立了一种使用超高效液相色谱和三重四极杆质谱仪联用测定水产养殖水体中21种磺胺类抗生素残留量的方法. 水体样品经过Oasis HLB固相萃取柱净化后,使用C18色谱柱进行分离. 采用正离子模式进行电离,通过多反应监测模式对目标化合物进行测定. 使用内标法定量,磺胺脒等21种磺胺类抗生素在5—50 ng·mL−1范围内线性良好,所得校准曲线线性相关系数在0.995以上. 本方法在养殖水体中21种磺胺类抗生素残留的定量限均为0.63 ng·mL−1,且精密度和不同浓度水平的加标回收率实验结果良好.Abstract: To establish a quick and sensitive analytical method for the determination of 21 sulfonamides in water samples from aquaculture environment by ultra high performance liquid chromatography-electrospray tandem mass spectrometry (UHPLC-MS/MS). The water samples were extracted and cleaned by Solid Phase Extraction through Oasis HLB columns, and then Velox SP- C18 column was used for separation. The target compounds were determined by multiple reaction monitoring (MRM) mode and quantified by internal standard method. It was shown that the analysis of one sample needed only 12.5 minutes. The calibration curve of 21 sulfonamides residues were constructed with correlation coefficients (r) more than 0.995, respectively. Good reproducibility on both retention time and peak area were observed. The quantitation limit of 21 sulfonamides were all 0.63 ng·mL−1 in this method. The method could be used for fast and accurate quantitative determination of 21 sulfonamides residues in water.
-
Key words:
- tandem mass spectrometry /
- water /
- sulfonamides /
- solid phase extraction.
-
磺胺类抗生素(sulfonamides,SAs)是一类具有对氨基苯磺酰胺结构的抗菌药物,因其抗菌谱广、使用方便、价格低廉,在饲料添加剂或渔药中被经常使用. 水产养殖中,无论将药物混合在饲料中,还是直接池塘泼洒,药物都会溶于水体,而水体中残留的药物容易污染周围的河流、湖泊等自然水域[1-2]. 水环境中抗菌药物较高浓度的残留,可能会诱导细菌耐药性,对人体产生健康风险[3].
近年来,磺胺类抗生素的检测方法主要有高效液相色谱法(HPLC)[4-5]、液相色谱-串联质谱法(LC-MS/MS)[6-8]、酶联免疫分析法(ELISA)[9]等. 我国农村农业部发布了SC/T 9436-2020 《水产养殖环境(水体、底泥)中磺胺类药物的测定》,该标准提出对水产养殖环境中磺胺类药物使用液相色谱-串联质谱法进行测定[10]. 由于水体中抗生素的浓度较低,且存在大量的干扰物,因此在上机分析前需要对目标物进行分离和富集. 超高效液相色谱-串联质谱法因其检测灵敏度高、结果选择性好的特点, 已广泛应用于复杂基质中痕量物质的检测. 本文使用超高效液相色谱-三重四极杆质谱联用技术,建立了水产养殖水体中21种磺胺类药物残留量的测定方法,供相关检测人员参考使用.
1. 材料与方法(Materials and methods)
1.1 仪器与试剂
LC-30A超高效液相色谱仪(日本岛津公司);LCMS-8045三重四极杆质谱仪,配置有加热型电喷雾离子源(HESI)及LabSolutions Ver.5.96色谱数据处理系统(日本岛津公司);超纯水仪,Milli Q型(美国Millipore公司);Oasis HLB固相萃取小柱,500 mg,6 mL(美国Waters公司).
甲醇:色谱纯,德国Merck公司产品;甲酸:色谱纯,上海安谱实验科技有限公司CNW产品;乙酸:色谱纯,美国Fisher Scientific公司产品;磺胺类药物标准物质(磺胺脒、磺胺醋酰、磺胺嘧啶、磺胺二甲嘧啶、磺胺噻唑、磺胺吡啶、磺胺甲嘧啶、磺胺对甲氧嘧啶、磺胺二甲唑、磺胺甲噻二唑、磺胺索嘧啶、甲氧苄啶、磺胺甲氧嗪、磺胺氯哒嗪、磺胺甲噁唑、磺胺间甲氧嘧啶、磺胺多辛、磺胺异噁唑、磺胺苯吡唑、磺胺地索辛、磺胺喹噁啉和磺胺邻二甲氧嘧啶-D3):德国Dr. Ehrenstorfer公司产品.
1.2 标准品溶液的配制
称取适量磺胺类抗生素的标准品,用甲醇稀释并定容,配制成100 μg·mL−1标准储备溶液,将该储备液于−20℃以下冷藏密封避光保存.
准确移取适量磺胺邻二甲氧嘧啶-D3储备溶液于容量瓶中,甲醇稀释并定容,配制成1 μg·mL−1磺胺邻二甲氧嘧啶-D3内标标准工作液. 准确移取适量各种磺胺类抗生素储备溶液于容量瓶中,用甲醇稀释并定容,配制成1 μg·mL−1混合标准中间溶液. 再移取混合标准中间溶液适量,使用初始流动相进行稀释,配制成浓度分别为5、10、20、30、40、50 ng·mL−1标准系列工作液,其中磺胺邻二甲氧嘧啶-D3内标浓度均为5 ng·mL−1.
1.3 水样前处理方法
准确量取200 mL(精确至0.1 mL)水样于250 mL广口玻璃瓶中,准确加入适量磺胺邻二甲氧嘧啶-D3内标标准工作液,混合均匀. 无需提取,待浓缩净化. 用5 mL甲醇和5 mL水依次活化和平衡Oasis HLB固相萃取柱,水体样品以2 mL·min−1流速过柱,1 mL实验用水淋洗,用0.1%甲酸-甲醇溶液分2次洗脱至10 mL离心管中,洗脱液最终定容至5 mL. 取200 µL洗脱液,加800 µL初始流动相稀释5倍,混匀后过 0.22 µm 微孔滤膜后进行LC-MS/MS上机分析.
1.4 色谱-质谱条件
色谱条件:Shim-pack Velox SP- C18(2.1 mm I.D.× 100 mm L, 1.8 μm)色谱柱;流动相:乙酸水溶液(V/V,1/81)(A)和0.1%甲酸-甲醇溶液(V/V)(B);梯度洗脱程序:0 min(5% B)— 1 min(5% B)—3.50 min(10% B)—13.00 min(45% B)—17.00 min(70% B)—18.00 min(70% B)—18.50 min(5% B);流速:0.45 mL·min−1;柱温30℃;进样量3 μL;总分析时间为22 min.
质谱条件: HESI正离子检测,多反应监测模(MRM)测定,主要质谱参数为:离子喷雾电压4.0 kV;雾化气:氮气3.0 L·min−1;干燥气:氮气 15 L·min−1;加热气:空气 10 L·min−1;脱溶剂管温度250℃;加热模块温度400℃;接口温度400℃;碰撞气:氩气. 磺胺类抗生素质谱参数见表1.
表 1 磺胺类抗生素质谱采集参数Table 1. Parameters for MS/MS analysis of sulfonamides编号 化合物名称 英文名称 前体离子 产物离子 Q1 pre/V CE Q3 Pre/V 1 磺胺脒 Sulfaguanidine 215.05 92.05* −16 −25 −36 108.05 −16 −22 −22 2 磺胺醋酰 Sulfacetamide 215.05 92.05* −23 −23 −17 108.05 −16 −22 −22 3 磺胺嘧啶 Sulfadiazine 251.00 156.00* −30 −15 −29 92.05 −30 −25 −17 4 磺胺二甲嘧啶 Sulfamethazine 279.00 186.00* −30 −17 −20 92.05 −30 −31 −17 5 磺胺噻唑 Sulfathiazole 256.00 156.00* −30 −14 −30 92.05 −30 −28 −17 6 磺胺吡啶 Sulfapyridine 250.00 92.05* −30 −27 −17 156.00 −30 −16 −29 7 磺胺甲基嘧啶 Sulfamerazine 265.00 156.00* −30 −17 −28 92.10 −30 −28 −17 8 磺胺对甲氧嘧啶 Sulfameter 281.10 156.10* −30 −17 −29 108.10 −30 −26 −21 9 磺胺二甲唑 Sulfamoxole 268.10 156.10* −30 −15 −29 92.10 −30 −28 −17 10 磺胺甲噻二唑 Sulfamethizole 271.00 156.00* −23 −14 −16 108.00 −22 −23 −19 11 磺胺索嘧啶 Sulfisomidine 279.00 156.00* −27 −19 −16 186.00 −30 −17 −19 12 甲氧苄啶 Trimethoprim 291.10 230.15* −14 −23 −26 123.10 −14 −24 −24 13 磺胺甲氧哒嗪 Sulfamethoxypyridazine 281.00 156.00* −30 −17 −30 92.05 −30 −30 −17 14 磺胺氯哒嗪 Sulfaclorazina 285.00 156.00* −30 −14 −29 92.05 −30 −29 −17 15 磺胺甲噁唑 Sulfamethoxazole 254.00 156.00* −30 −16 −29 92.00 −30 −28 −17 16 磺胺间甲氧嘧啶 Sulfamonomethoxine 281.00 156.00* −12 −18 −16 108.00 −23 −18 −22 17 磺胺多辛 Sulfadoxine 311.00 156.00* −28 −26 −16 108.00 −30 −30 −19 18 磺胺异噁唑 Sulfisoxazole 268.10 156.00* −20 −13 −18 113.10 −20 −15 −24 19 磺胺苯吡唑 Sulfaphenazole 315.10 158.10* −30 −28 −30 92.05 −30 −21 −30 20 磺胺地索辛 Sulfadimethoxine 311.00 156.05* −23 −22 −29 92.05 −23 −35 −17 21 磺胺喹噁啉 Sulfaquinoxaline 301.00 155.95* −23 −17 −29 92.05 −23 −30 −17 22 氘代磺胺邻二甲氧嘧啶-D3 Sulfadoxine-D3 314.05 92.05* −23 −35 −17 156.00 −28 −26 −16 注:*表示定量离子 2. 结果与讨论(Results and discussion)
2.1 质谱条件优化
磺胺类抗生素都是以对位氨基苯磺酰胺为基本结构的衍生物,在质谱电喷雾电离(ESI)正离子模式下易形成 [M+H]+加合离子. 采用流动注射分析法,分别对21种磺胺类抗生素和磺胺邻二甲氧嘧啶-D3的单标标准溶液(1 μg·mL−1)进行一级质谱扫描(Q1 MS),得到磺胺类抗生素的前体离子. 使用LabSolutions软件自动方法优化功能,对碰撞能量和Q1、Q3预杆电压进行优化,优化后 MRM 参数参见 1.4节. 将10 ng·mL−1浓度的磺胺类抗生素混合标准工作液按1.4节进行测定,所得21种磺胺类抗生素的标准样品图谱如图1所示. 由图1可知,21种磺胺类抗生素在12.5 min之前全部出峰,各化合物峰形良好,且同分异构体均达到了基线分离.
2.2 线性范围与定量限
将5、10、20、30、40 、50 ng·mL−1的磺胺类抗生素标准溶液,按1.4节的分析条件进行测定,使用内标法定量. 以浓度比为横坐标,峰面积比为纵坐标,绘制校准曲线. 所得校准曲线线性关系良好,相关系数r范围在0.995—0.999. 各磺胺类抗生素校准点准确度在87.7%—112.8%,其中, 校准点准确度由 A(%)=Ci/Cs×100%计算(Ci表示曲线回归方程计算得到的校准点浓度值, Cs表示真实校准点浓度值). 结果表明, 21种磺胺类抗生素在线性范围内线性关系良好, 校准点准确度较高. 以待测化合物的定量离子对色谱峰的信噪比大于或等于10(S/N≥10)的溶液浓度为该磺胺类抗生素的定量限(LOQ),本方法在水产养殖水体中21种磺胺类抗生素残留的定量限均为0.63 ng·mL−1.
2.3 精密度实验
取10、20、40 ng·mL−1的21种磺胺类药物标准工作液连续测定6次,保留时间和峰面积的重复性结果显示,磺胺脒等21种磺胺类药物保留时间和峰面积的相对标准偏差分别小于0.79%和6.61%,表明仪器精密度良好.
2.4 加标回收率实验
称取空白水体样品,加入少量磺胺脒等21种磺胺类抗生素混合标准品储备溶液,使水样中添加浓度为分别为1、2、5 ng·mL−1,平行做3份. 按照1.3样品前处理方法净化后,测定磺胺脒等21种磺胺类抗生素的添加回收率,各化合物的平均加标回收率结果在70.0%—110.0%之间.
3. 结论(Conclusion)
本文建立了使用超高效液相色谱三重四极杆质谱联用系统测定水产养殖水体中21种磺胺类抗生素残留量的方法. 水体样品经过固相萃取柱净化后,采用超高效液相色谱-串联质谱法测定磺胺类抗生素. 结果表明,使用内标法定量,磺胺脒等21种磺胺类抗生素在5—50 ng·mL−1浓度范围内线性良好,各校准点准确度在87.7%—112.8%之间,且精密度和不同浓度水平的加标回收率实验结果良好. 该方法样品前处理过程简单,检测灵敏度高,分析速度快,可用于养殖水体中21种磺胺类抗生素残留量的测定和筛查. 本方法为准确评估磺胺类抗生素在环境水中残留状况提供了可靠手段.
-
表 1 磺胺类抗生素质谱采集参数
Table 1. Parameters for MS/MS analysis of sulfonamides
编号 化合物名称 英文名称 前体离子 产物离子 Q1 pre/V CE Q3 Pre/V 1 磺胺脒 Sulfaguanidine 215.05 92.05* −16 −25 −36 108.05 −16 −22 −22 2 磺胺醋酰 Sulfacetamide 215.05 92.05* −23 −23 −17 108.05 −16 −22 −22 3 磺胺嘧啶 Sulfadiazine 251.00 156.00* −30 −15 −29 92.05 −30 −25 −17 4 磺胺二甲嘧啶 Sulfamethazine 279.00 186.00* −30 −17 −20 92.05 −30 −31 −17 5 磺胺噻唑 Sulfathiazole 256.00 156.00* −30 −14 −30 92.05 −30 −28 −17 6 磺胺吡啶 Sulfapyridine 250.00 92.05* −30 −27 −17 156.00 −30 −16 −29 7 磺胺甲基嘧啶 Sulfamerazine 265.00 156.00* −30 −17 −28 92.10 −30 −28 −17 8 磺胺对甲氧嘧啶 Sulfameter 281.10 156.10* −30 −17 −29 108.10 −30 −26 −21 9 磺胺二甲唑 Sulfamoxole 268.10 156.10* −30 −15 −29 92.10 −30 −28 −17 10 磺胺甲噻二唑 Sulfamethizole 271.00 156.00* −23 −14 −16 108.00 −22 −23 −19 11 磺胺索嘧啶 Sulfisomidine 279.00 156.00* −27 −19 −16 186.00 −30 −17 −19 12 甲氧苄啶 Trimethoprim 291.10 230.15* −14 −23 −26 123.10 −14 −24 −24 13 磺胺甲氧哒嗪 Sulfamethoxypyridazine 281.00 156.00* −30 −17 −30 92.05 −30 −30 −17 14 磺胺氯哒嗪 Sulfaclorazina 285.00 156.00* −30 −14 −29 92.05 −30 −29 −17 15 磺胺甲噁唑 Sulfamethoxazole 254.00 156.00* −30 −16 −29 92.00 −30 −28 −17 16 磺胺间甲氧嘧啶 Sulfamonomethoxine 281.00 156.00* −12 −18 −16 108.00 −23 −18 −22 17 磺胺多辛 Sulfadoxine 311.00 156.00* −28 −26 −16 108.00 −30 −30 −19 18 磺胺异噁唑 Sulfisoxazole 268.10 156.00* −20 −13 −18 113.10 −20 −15 −24 19 磺胺苯吡唑 Sulfaphenazole 315.10 158.10* −30 −28 −30 92.05 −30 −21 −30 20 磺胺地索辛 Sulfadimethoxine 311.00 156.05* −23 −22 −29 92.05 −23 −35 −17 21 磺胺喹噁啉 Sulfaquinoxaline 301.00 155.95* −23 −17 −29 92.05 −23 −30 −17 22 氘代磺胺邻二甲氧嘧啶-D3 Sulfadoxine-D3 314.05 92.05* −23 −35 −17 156.00 −28 −26 −16 注:*表示定量离子 -
[1] LI L, LIU D, ZHANG Q, et al. Occurrence and ecological risk assessment of selected antibiotics in the freshwater lakes along the middle and lower reaches of Yangtze River Basin [J]. Journal of Environmental Management, 2019, 249: 1-8. [2] LI W H, GAO L H, SHI Y L, et al. Occurrence, distribution and risks of antibiotics in urban surface water in Beijing, China [J]. Environmental Science, 2015, 17(9): 1611-1619. [3] 唐娜, 张圣虎, 陈玫宏, 等. 长江南京段表层水体中12种磺胺类抗生素的污染水平及风险评价 [J]. 环境化学, 2018, 37(3): 505-512T. doi: 10.7524/j.issn.0254-6108.2017062705 [4] 李丹, 沈 昕, 张玉洁, 等. 高效液相色谱法测定鸡肉中5种磺胺类药物及乙氧酰胺苯甲酯增效剂残留量 [J]. 食品安全质量检测学报, 2020, 11(1): 202-208. doi: 10.19812/j.cnki.jfsq11-5956/ts.2020.01.038 [5] 李柳毅, 范辉, 范磊, 等. 固相萃取-高效液相色谱法测定地表水中4种磺胺类抗生素 [J]. 化学分析计量, 2017, 26(6): 38-40. doi: 10.3969/j.issn.1008-6145.2017.06.009 [6] XU Y, DING J, CHEN H Y, et al. Fast determination of sulfonamides from egg samples using magnetic multiwalled carbon nanotubes as adsorbents followed by liquid chromatography–tandem mass spectrometry [J]. Food Chemistry, 2013, 140: 83-90. doi: 10.1016/j.foodchem.2013.02.078 [7] CUI H Y, CHANG H, ZHENG H J, et al. Determination and occurrence of sulfonamide transformation products in surface waters [J]. Science of the Total Environment, 2021, 799: 146562. [8] CHEN Y P, XIA S D, HAN X Q, et al. Simultaneous determination of malachite green, chloramphenicols, sulfonamides, and fluoroquinolones residues in fish by liquid chromatography-mass spectrometry [J]. Journal of Analytical Methods in Chemistry, 2020: 3725618. [9] 陈曼娜. 磺胺类药物的多残留酶联免疫法检测 [J]. 质量安全与检验检测, 2020, 30(4): 46-47. [10] 中华人民共和国农业农村部. SC/T 9436-2020 水产养殖环境(水体、底泥)中磺胺类药物的测定[S]. 北京: 中国农业出版社, 2020. -






 DownLoad:
DownLoad: