-
土壤是人类农业生产的物质基础,一旦遭受污染,会对粮食安全和人体健康造成危害。2014年发布的《全国土壤污染状况调查公报》[1]显示,我国土壤重金属污染问题不容乐观,污染土壤中约82.4%的土壤受到重金属及准金属污染,且土壤重金属污染具有隐蔽性、滞后性、治理难、周期长的特点[2]。重金属极易在土壤-植株体系内迁移和累积,会造成环境污染和生态破坏。因此,对土壤重金属的治理迫在眉睫。
目前,土壤重金属的处理方法包括物理法(土壤淋洗、蒸汽浸提、电动力学修复)、化学法(化学修复剂)和生物法(微生物催化降解、植物修复、动物修复)[3]。化学原位钝化技术因其成本低、见效快、处理效果显著而得到广泛的应用[4]。常用的钝化剂主要有石灰[5]、磷酸盐[6]、有机质[7-8]、金属氧化物[9-11]和黏土矿物[12]。其中,凹凸棒石是一种典型的含水富镁铝硅酸盐黏土矿物,具有独特的化学成分和物理结构,内表面积大、孔隙较多、离子交换能力强,在化工、环保和印染等领域得到了广泛的应用。谭科艳等[13]研究了凹凸棒石对铜锌镉重金属污染土壤的修复效果,结果表明,适量添加凹凸棒石黏土矿物可对Cu的平均修复率达到31.50%,对Zn元素的平均修复率达到26.15%,对Cd元素的平均修复率达到34.92%,能够有效减少蔬菜对Cu、Zn、Cd元素的吸收。马博[14]研究表明,凹凸棒石综合钝化能力更强,且在酸性较高的极端条件下效果优于膨润土和沸石,低配比凹凸棒石对衡阳尾矿中Cr、Zn、Cd、Pb、Cu的钝化效果显著。ZHANG等[15]发现,凹凸棒石的施加可显著降低Cu的生物可利用态质量分数,缓解重金属Cu对油菜植株的生理胁迫效应。
常用的凹凸棒石改性方法有无机改性、有机改性、生物质改性和微波改性[16]。LIANG等[17]通过制备巯基改性凹凸棒石钝化Cd污染土壤,可显著增强土壤颗粒对Cd的吸附,抑制农作物对重金属Cd的吸收。XU等[18]将纳米零价铁负载凹凸棒石施用进土壤中,可有效促进重金属Cd、Cr和Pb发生形态转变,并将其固定下来。甘肃省具有丰富的凹凸棒石矿藏,但常常因为品位较低未能得到大规模开发利用。为解决此问题,制备5种不同体积分数H2SO4、不同改性时间的酸改性凹凸棒石,探讨不同钝化材料的添加量对土壤重金属Cu和Zn的钝化效果,并结合环境风险指数和重金属修复效率评估酸改性凹凸棒石的最佳投加量,以期为农田重金属污染土壤的治理和甘肃省凹凸棒石的应用提供参考。
-
重金属复合污染土壤采自甘肃省白银市东大沟(36° 59′ 96′′ N,104° 22′ 76′′ E)。土壤的基本理化性质为pH 7.28、土壤电导率(EC)1457 µS·cm−1、重金属Cu质量分数为1029.11 mg·kg−1、重金属Ni质量分数为87.18 mg·kg−1、重金属Zn质量分数为707.51 mg·kg−1。其中,Cu和Zn均远超国家标准限值,分别为《土壤环境质量农用地土壤污染风险管控标准》(GB 15618-2018)[19]的5.15倍和2.83倍。
凹凸棒石质黏土复合矿物(简称为“凹凸棒石”)购自甘肃当地,原矿采自甘肃省临泽县板桥镇红色凹凸棒石矿,土状结构,粒度为2 mm左右,主要的矿物成分为凹凸棒石29.7%、石英21.8%、长石14.6%、白云石 6.3%、其他组分27.6%,是一种由凹凸棒石为主,石英和长石以及碳酸盐矿物等伴生的黏土质复合非金属矿物。其主要化学成分为:SiO2 48.38%、Al2O3 11.24%、Fe2O3 4.78%、MgO 7%、CaO 7.41%[20]。
-
称取定量凹凸棒石,破碎、研磨,过200目筛(直径0.075 mm)。基于49种酸改性钝化材料的研究[21],制备5种优选酸改性凹凸棒石,具体配制条件见表1。将凹凸棒石粉末与不同体积分数的H2SO4溶液混合,固液比为1∶10(m∶v),500 r·min−1转速下搅拌一定时间后,烘干、研磨、过筛制得钝化材料。按2、4、8、16、24 g·kg−1的添加量,将酸改性凹凸棒石钝化材料加入到1.5 kg实际重金属复合污染土壤中,混合均匀,重量法添加去离子水,保持70%的田间持水量,钝化培育30 d后测定土壤的理化性质和重金属形态,每组处理设置不添加任何钝化材料的土壤样品作为对照,记为CK。
-
采用X射线衍射仪(MiniFlex600,日本Rigaku公司)分析改性前后的凹凸棒石晶体物相组成,扫描速度为10°·min−1,角度为5°~80°,扫描过程采用Cu-Kα 辐照。采用扫描电子显微镜(GeminiSEM500,德国ZEISS公司)观察改性前后凹凸棒石的表面形貌,将样品过200目筛网,在15 kV电压下以相同倍率下放大观察分析。
采用pH计(pHS-3C,上海仪电科学仪器股份有限公司)测定土壤pH,固液比为1∶2.5(m∶v)。采用电导率仪(DDS-307A,上海仪电科学仪器股份有限公司)测定土壤EC,固液比为1∶5(m∶v)。采用BaCl2-H2SO4强迫交换法测定土壤阳离子交换量(CEC)。采用BCR连续提取法测定土壤重金属化学形态。土壤重金属总量经HCl-HNO3-HF-HClO4消解后,火焰原子吸收分光光度计(TAS-990,北京普析通用仪器有限责任公司)测定浓度。
本实验选用H2O和DTPA作为提取剂来评价土壤重金属的生物有效性。土壤重金属水溶态测定时,称取5 g土壤样品与50 mL蒸馏水均匀混合,25 ℃下充分振荡24 h,火焰原子吸收分光光度法测定上清液中重金属浓度。土壤重金属DTPA提取态测定时,称取2 g土壤样品与40 mL DTPA提取液均匀混合,25 ℃下振荡12 h,火焰原子分光光度法测定上清液中重金属浓度。
-
污染土壤的生态风险指数(Ecological risk index,ERI)指土壤中活性较高的生物有效态质量分数与重金属总量之比,用于表示土壤中重金属的生态环境风险,常用于底泥沉积物、土壤和污泥中重金属的风险评价,通常分为5个等级,即无风险(<1%)、低风险(1%~10%)、中风险(10%~30%)、高风险(30%~50%)、极高风险(>50%)。按式(1)计算[22-23]。
式中:Cbs为土壤中有效态重金属的质量分数,mg·kg−1,Cs为土壤中重金属的质量分数,mg·kg−1。
此外,潜在风险指数(potential ecological risk index)可用于评价多种重金属复合污染的生态风险,可按式(2)、式(3)计算。
式中:
Eir 为单种重金属元素的潜在风险指数;Cid 为土壤中重金属质量分数,mg·kg−1;Cib 为国家土壤中重金属标准质量分数限值(CCub =100 mg·kg−1,CZnb =250 mg·kg−1);Tir 为单种重金属元素的生物毒性因子,其中TCur =5,TZnr =1;RI为重金属总的生态风险指数。风险等级划分依据如表2和表3所示。污染土壤中重金属的修复效率(Remediation ratio,RR)指BCR多级提取法中较稳定的重金属残渣态(S4)与土壤重金属4种形态总和的比值,可用于评估重金属的潜在活化风险,按式(4)计算[24]。
式中: S1为重金属元素酸溶态质量分数,mg·kg−1;S2为重金属元素还原态质量分数,mg·kg−1;S3为重金属元素氧化态质量分数,mg·kg−1;S4为重金属元素残渣态质量分数,mg·kg−1。
-
土壤pH、电导率和阳离子交换量影响着重金属的化学形态,是评价重金属迁移转化和作物生长发育情况的重要指标[25]。施用不同酸改性凹凸棒石后的土壤pH见图1(a),与对照组相比,向土壤中施加5种酸改性凹凸棒石后,土壤pH均呈现显著降低的趋势。在同一投加量水平下,A3处理组pH显著低于其他处理组。这是因为,天然的凹凸棒石本身呈弱碱性,含有大量的羟基等官能团[26],而改性添加的H2SO4具有强酸性,能够和土壤及凹凸棒石中的碱性物质发生反应,从而降低土壤pH,调节土壤的酸碱度。本研究采用的实际污染土壤为北方地区常见的碱性土壤,酸改性凹凸石的施用有效改善了土壤的酸碱环境。不同酸改性凹凸棒石处理后的土壤EC见图1(b),在同一酸改性凹凸棒石处理组中,土壤EC随着添加量的增加而显著增加,且A5处理组EC值显著高于其他处理组。土壤CEC随着凹凸棒石添加量的增加而增加,但不同添加量间差异性不显著(图1(c))。除A4材料投加量为8 mg·kg−1时土壤CEC较高外,其他投加量水平下,A5处理组CEC也显著高于其他处理组。一方面,凹凸棒石的表面带有Na+、K+和Ca2+等阳离子,本身具有较高的阳离子交换容量,随着投加量的增加,土壤中带电的离子浓度升高,从而提高土壤电导率[27];另一方面,当改性时添加的H2SO4体积分数较大时,凹凸棒石表面会带有大量的H+,这些活泼的阳离子可能会和土壤中的Cu2+、Zn2+发生阳离子交换反应,提高土壤的EC和CEC [28]。
-
土壤中重金属的水溶态可直观地反映重金属的生物可利用度,这部分形态的重金属质量分数很低,但是却可以直接被植物吸收利用,具有极强的迁移性和毒性,因此常常作为土壤重金属污染评价的重要指标[29]。不同改性凹凸棒石处理后的土壤生物有效态重金属质量分数见图2。从图2可以看出,添加酸改性凹凸棒石后,水溶态Cu和Zn的质量分数均较对照组显著降低。尽管随着投加量的增加,水溶态重金属质量分数出现了先降低后轻微升高的趋势,但差异并未达显著水平。实验结果表明,当投加量为16 g·kg−1时,酸改性凹凸棒石对Cu、Zn的钝化效果最好。其中,A5处理组中水溶态Cu的质量分数最低,较对照组降低了47.38%;A3处理组中水溶态Zn的质量分数最低,较对照组降低了64.44%。土壤中DTPA提取态重金属质量分数常常用来评估植物对重金属的吸收情况,DTPA络合剂能够与重金属离子结合,形成稳定的水溶性络合物,可直观地评价重金属的生物有效性[30]。添加酸改性凹凸棒石后,Cu和Zn的DTPA提取态质量分数均较对照组显著降低。当投加量为16 g·kg−1时,A5处理组中DTPA提取态Cu的质量分数最低,较对照组下降了24.25%,A3处理组中DTPA提取态Zn的质量分数最低,较CK下降了46.77%。DTPA提取态重金属的降低趋势与水溶态重金属基本保持一致。这与罗宁临等[31]的研究结果基本一致。造成以上结果的原因可能是:1)酸改性使得凹凸棒石表面和孔隙内的碳酸盐杂质得以去除,晶束团聚结构变得更加紧密,内表面积和缝隙增大,增强了其对重金属Cu、Zn的吸附能力[32];2)酸改性凹凸棒石的施用提高了土壤的阳离子交换容量,土壤中游离的Cu2+、Zn2+通过阳离子交换作用,与带有负电荷的凹凸棒石和土壤颗粒结合,显著降低了重金属的生物有效性[27,33];3)凹凸棒石表面带有大量的硅羟基等官能团,能与重金属发生络合反应,从而将其固定[14,34]。本研究结果说明,采用优质的钝化材料是降低土壤重金属毒性的关键,而控制合适的投加量对农田土壤的修复也至关重要。
-
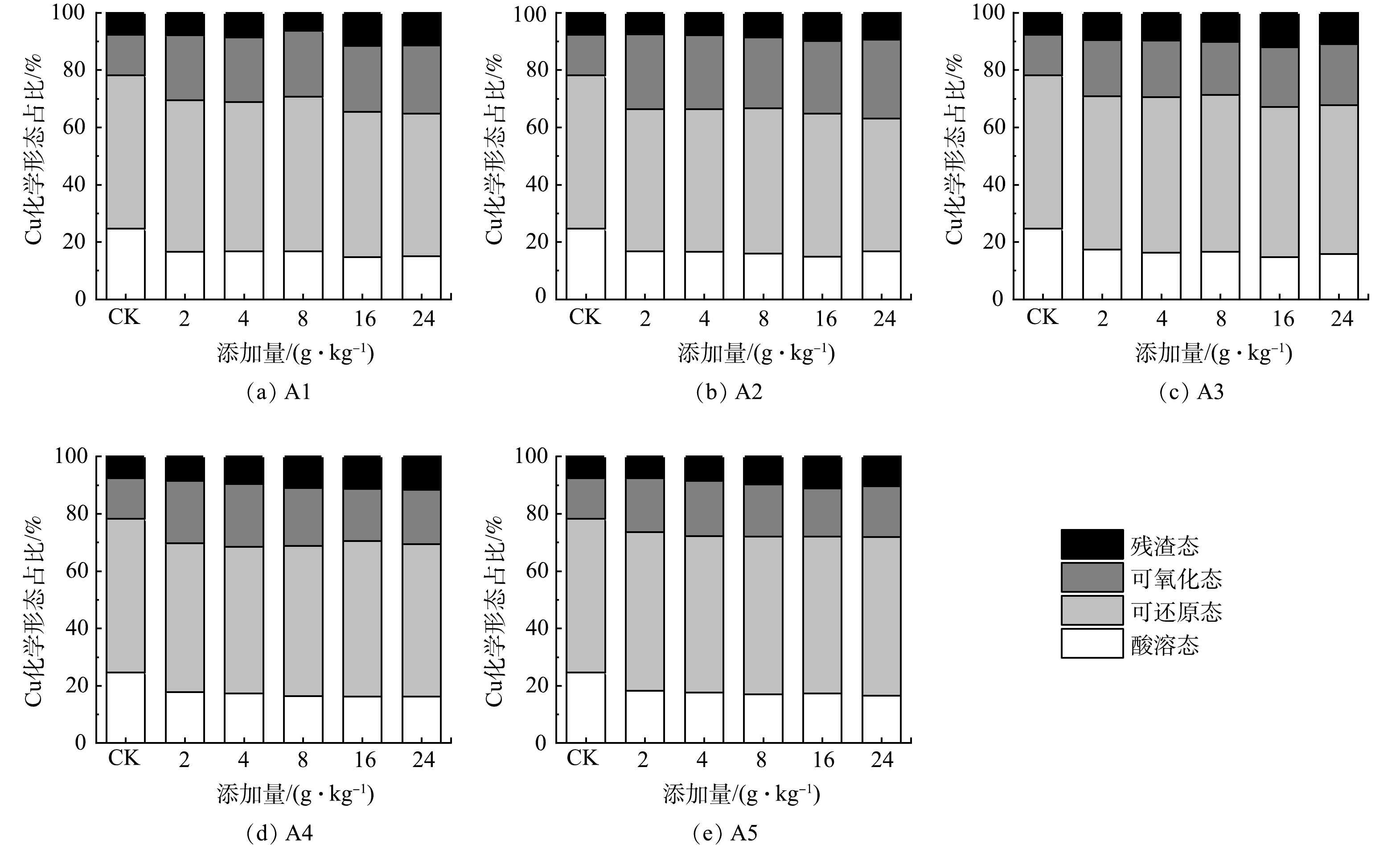
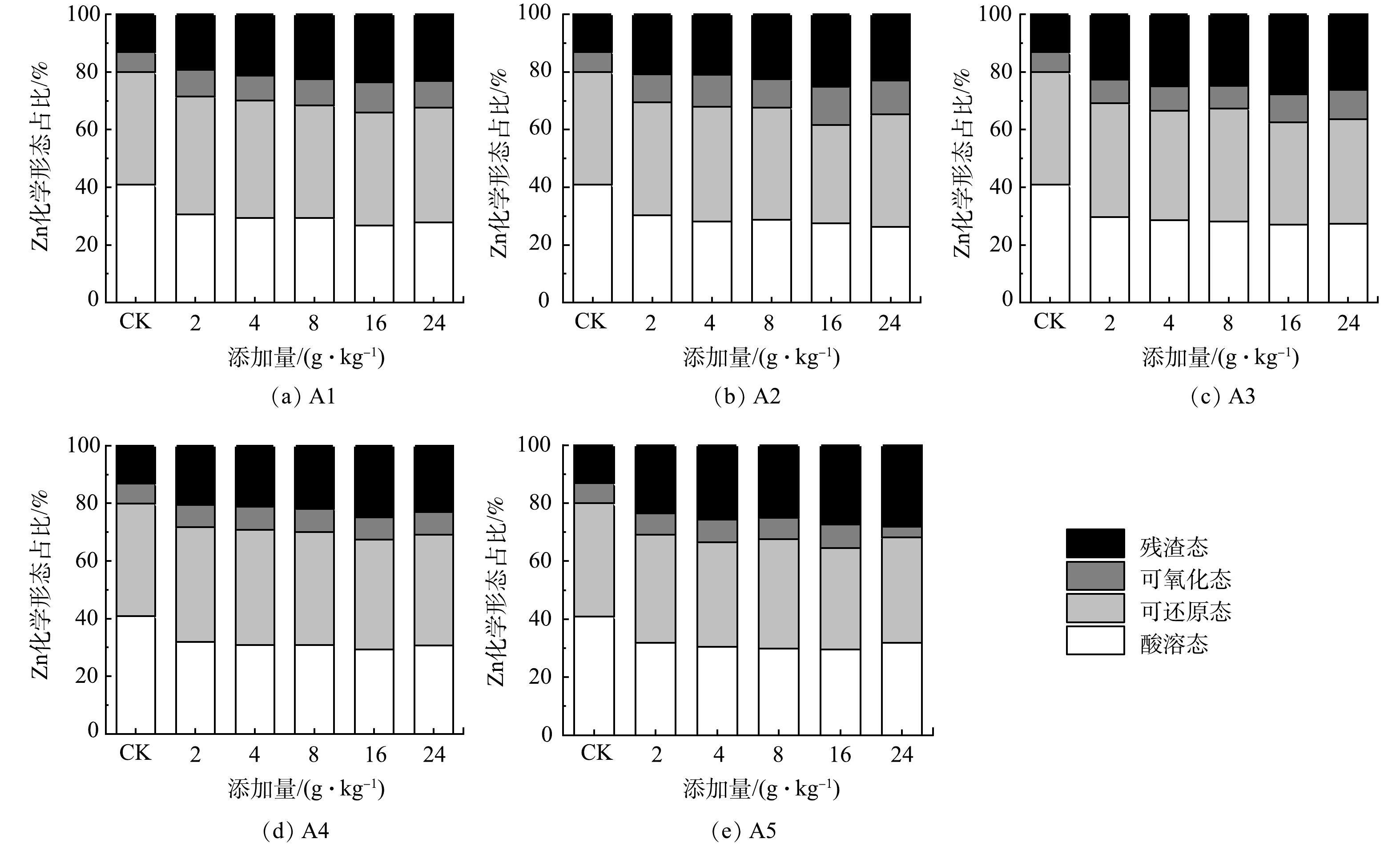
BCR多级提取法中,重金属各种形态的活性大小依次为酸溶态>可还原态>可氧化态>残渣态[35]。其中,酸溶态重金属的生物可利用度最高,可还原态和可氧化态重金属容易随着pH和氧化还原电位等环境条件的变化而变化,重新释放到环境介质中,残渣态重金属最稳定,不易在土壤中迁移转化,生态毒性最低[35-37]。酸改性凹凸棒石钝化后土壤中重金属形态分布见图3和图4。添加不同酸改性凹凸棒石后,酸溶态Cu和Zn的质量分数较对照组显著降低,而残渣态Cu和Zn的质量分数上升(图3,图4)。当投加量为16 g·kg−1时,A3处理组中酸溶态Cu和Zn的占比最低,残渣态Cu的比例较对照组上升了3.96%;残渣态Zn的比例较对照组上升了15.26%,这与武成辉等[38]和陶玲等[39]的研究结果一致。添加不同酸改性凹凸棒石可影响重金属在土壤中的形态,促进重金属从活性较高的酸溶态、可还原态向活性较低的可氧化态、残渣态转变,降低了Cu、Zn的生态毒性,实现了土壤的钝化修复。其原因可能是:1)凹凸棒石及其改性材料的添加可通过一系列吸附、离子交换、沉淀和络合作用降低酸溶态Cu、Zn质量分数[40];2)凹凸棒石经过酸处理后,起支撑作用的八面体和四面体溶解,导致凹凸棒石的孔道增大,比表面积增加,凹凸棒石的吸附性能提高[41];3)残渣态重金属 Cu、Zn一般存在于硅酸盐、原生和次生矿物等土壤的晶格中,当向污染土壤中施用酸改性凹凸棒石后,随着钝化时间的延长,低价的Cu2+、Zn2+可能会在凹凸棒石八面体或四面体结构中与Si4+发生晶格置换,能长期稳定在土壤中[42]。
-
为验证上述作用机理,本实验对凹凸棒石改性前后的微观形貌和晶体结构进行表征,扫描电子显微镜图像如图5所示。供试凹凸棒石原矿(ATP)主要呈棒状晶束堆积结构,晶束较长,棒晶密实,孔道结构较少。经不同浓度H2SO4和不同活化时间处理后,凹凸棒石的棒晶发生解束,晶束变短,排列相对松散,可直接接触的点位增多,增强了凹凸棒石对重金属的吸附能力。这与陈雪芳[43]等的研究结果一致:酸改性能够溶解凹凸棒石中的八面体阳离子和四面体硅,使得八面体结构起主要的支撑作用,凹凸棒石孔道开放,孔径增大,比表面积增大,吸附性能提高。但是,当酸浓度较高时,会对层间的阳离子起较强的溶出作用,破坏晶体结构,进而降低凹凸棒石的吸附性能[44]。
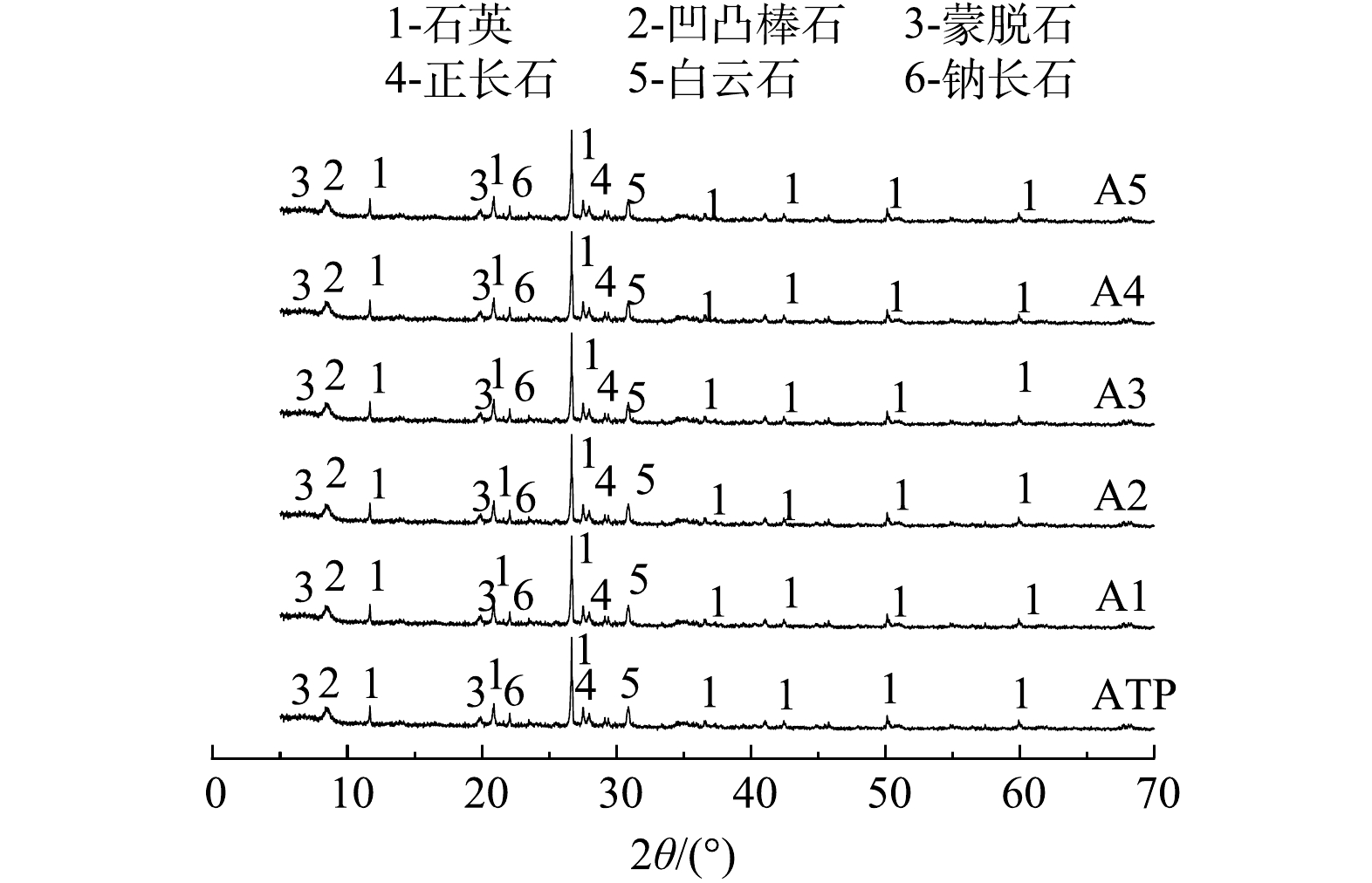
酸改性凹凸棒石的X射线衍射图谱结果见图6。凹凸棒石的特征峰位于8.40°处,与标准衍射图谱(JCPDFNo.020018)一致。石英特征衍射峰的存在证实了凹凸棒石中伴生有其他物相的杂质。从图中可以看出,经过酸改性后,凹凸棒石质黏土复合矿物物相组成及凹凸棒石、白云石物相的衍射峰峰强度没有明显改变,石英杂质的峰强度有轻微减弱。这表明,酸改性过程溶解了碳酸盐等杂质,但是并未破坏凹凸棒石的骨架结构。该结果与雷春生等[45]和张萍等[46]的研究结果一致。本研究结果表明,适宜的酸浓度和改性时间能够有效改善天然凹凸棒石原矿的表面形貌和孔隙结构,使得钝化材料孔隙结构增多,孔径变大,比表面积增大,促进了其对重金属的钝化修复。
-
与土壤中重金属的总量相比,水溶态Cu和Zn的质量分数占比不到0.01%。因此,本研究根据DTPA提取态重金属的质量分数来评价酸改性凹凸棒石钝化剂对土壤重金属的修复效率和生态风险。对照组污染土壤中Cu和Zn的环境风险指数分别对应为24.4%和11.51%。经不同的钝化材料处理后,土壤重金属的环境风险均较对照组显著降低(表4)。当施用A5钝化材料且投加量为16 g·kg−1时,酸改性凹凸棒石处理后Cu的环境风险指数降至最低。土壤Zn的环境风险由中风险降为低风险(表5),当施用A3材料且投加量为16 g·kg−1时,Zn的环境风险指数最低。
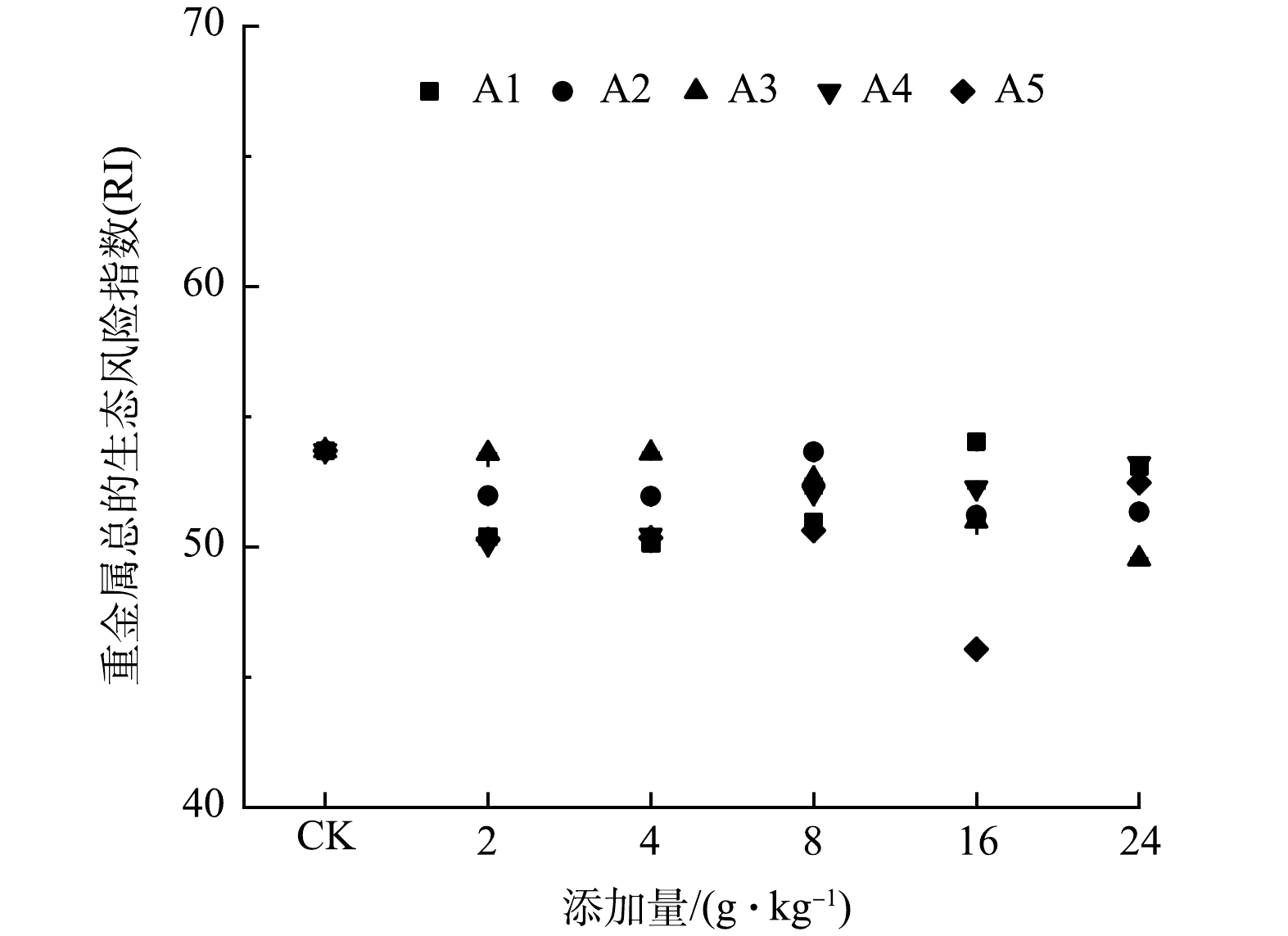
在复合重金属污染土壤中,除了考虑单一重金属的环境风险外,受元素共存的联合作用影响,本研究评价了多种重金属的总环境风险指数RI。除添加量为16 g·kg−1的A1处理外,其他处理均显著降低了土壤RI。由图7可知,A3材料在较高添加量(≥8 g·kg−1)时,土壤RI指数随着添加量的增加显著降低。施用A5材料且添加量为16 g·kg−1时土壤中Cu、Zn的总生态风险指数达到最低。
钝化完成后,通常根据土壤中重金属的修复效率来评价钝化材料的实际应用价值。添加酸改性凹凸棒石后,Cu的修复效率随着投加量的增加呈先升高后轻微降低的趋势(表6),当钝化材料的投加量为16 g·kg−1时,重金属Cu的修复效率明显高于其他处理组。其中,A3处理组的钝化修复效率最高,达11.96%。重金属Zn修复效率的变化趋势与Cu基本一致(表7),当向土壤中施加16 g·kg−1的酸改性凹凸棒石后,Zn的修复效率明显高于其他处理组。其中,A3处理组Zn的钝化修复效率最高,为27.70%。
-
1)当H2SO4的体积分数为12.5%和15%,改性时间为72 h时,制得的酸改性凹凸棒石对Cu、Zn的钝化效果最佳,其最优投加量为16 g·kg−1。
2)向土壤中施加酸改性凹凸棒石,可显著降低重金属Cu、Zn的生物有效态质量分数,当钝化材料的投加量为16 g·kg−1时,H2O提取态Cu、Zn分别降低了25.91%~47.87%和49.69%~65%,DTPA提取态Cu、Zn分别降低了8.63%~24.30%和28.26%~46.84%。这说明,16 g·kg−1凹凸棒石可以有效降低Cu、Zn的生物有效性。
3)酸改性凹凸棒石的添加促使重金属Cu、Zn由活性较高的酸溶态向活性较低的残渣态转变,提高土壤重金属修复效率,当H2SO4的体积分数为12.5%,改性时间为72 h时,向土壤中投加16 g·kg−1酸改性凹凸棒石,Cu、Zn的修复效率最高,可达11.96%和27.70%,此时Zn的环境风险最低,降至6.13%,处于低风险。
酸改性凹凸棒石对土壤Cu-Zn的钝化修复
Stabilization of Cu-Zn in soil by acid-modified attapulgite
-
摘要: 过量的重金属积累在农田土壤中会对粮食安全和人体健康造成危害。通过调整酸体积分数和改性时间,制备5种酸改性凹凸棒石,分别按2、4、8、16和24 g·kg−1的投加量施用于土壤中,通过钝化实验,结合单级提取态和BCR多级提取态,对酸改性凹凸棒石的钝化效果进行评价,并分析了重金属污染土壤钝化前后的环境风险因子和修复效率。结果表明,添加16 g·kg−1的酸改性凹凸棒石,可有效改善土壤理化性质,H2O提取态Cu、Zn质量分数分别较对照组降低了25.91%~47.87% 和49.69%~65%,二乙烯三胺五乙酸提取态(DTPA提取态)Cu、Zn质量分数分别较对照组降低了8.63%~24.30% 和28.26%~46.84%。酸改性凹凸棒石的施用也促进了重金属Cu和Zn由酸溶态、可还原态向较稳定的可氧化态、残渣态转变。当投加量为16 g·kg−1时,12.5%体积分数H2SO4改性72 h制得的酸改性凹凸棒石处理组对Cu、Zn的修复效率最高,分别为11.96%和27.70%,本研究结果可为北方碱性农田重金属污染的钝化修复提供参考。Abstract: Excessive accumulation of heavy metals in farmland soil will do harm to food security and human health. In this study, five kinds of acid modified attapulgite were prepared by adjusting acid concentration and modification time and then applied to the soil at the dosage of 2, 4, 8, 16 and 24 g·kg−1, respectively. The stabilization effect of acid modified attapulgite was evaluated by stabilization experiment, combined with bioavailable extraction and BCR extraction. The environmental risk factor and remediation ratio of contaminated soil by heavy metals before and after stabilization were analyzed. The results showed that the addition of 16 g·kg−1 acid modified attapulgite could effectively improve the physical and chemical properties of soil. Compared with the control group, the H2O- extracted Cu and Zn were reduced by 25.91%~47.87% and 49.69%~65%, respectively. The diethylenetriamine pentaacetic acid extracted-Cu and Zn (DTPA-extracted Cu and Zn) were decreased by 18.63%~24.30% and 28.26%~46.84% respectively. The application of acid modified attapulgite also promoted the transformation of heavy metals Cu and Zn from acid soluble and reducible speciation to more stable oxidizable and residual speciation. When the dosage was 16 g·kg−1, the acid modified attapulgite treatment group prepared by 12.5% volume fraction H2SO4 modification for 72 hours had the highest remediation ratio for Cu and Zn, which was 11.96% and 27.70%, respectively. The results of this study can provide a reference for the stabilization and remediation of heavy metal pollution in alkaline farmland in north China.
-
Key words:
- attapulgite /
- acid modification /
- heavy metal /
- stabilization and remediation /
- environmental risk
-
土壤是人类农业生产的物质基础,一旦遭受污染,会对粮食安全和人体健康造成危害。2014年发布的《全国土壤污染状况调查公报》[1]显示,我国土壤重金属污染问题不容乐观,污染土壤中约82.4%的土壤受到重金属及准金属污染,且土壤重金属污染具有隐蔽性、滞后性、治理难、周期长的特点[2]。重金属极易在土壤-植株体系内迁移和累积,会造成环境污染和生态破坏。因此,对土壤重金属的治理迫在眉睫。
目前,土壤重金属的处理方法包括物理法(土壤淋洗、蒸汽浸提、电动力学修复)、化学法(化学修复剂)和生物法(微生物催化降解、植物修复、动物修复)[3]。化学原位钝化技术因其成本低、见效快、处理效果显著而得到广泛的应用[4]。常用的钝化剂主要有石灰[5]、磷酸盐[6]、有机质[7-8]、金属氧化物[9-11]和黏土矿物[12]。其中,凹凸棒石是一种典型的含水富镁铝硅酸盐黏土矿物,具有独特的化学成分和物理结构,内表面积大、孔隙较多、离子交换能力强,在化工、环保和印染等领域得到了广泛的应用。谭科艳等[13]研究了凹凸棒石对铜锌镉重金属污染土壤的修复效果,结果表明,适量添加凹凸棒石黏土矿物可对Cu的平均修复率达到31.50%,对Zn元素的平均修复率达到26.15%,对Cd元素的平均修复率达到34.92%,能够有效减少蔬菜对Cu、Zn、Cd元素的吸收。马博[14]研究表明,凹凸棒石综合钝化能力更强,且在酸性较高的极端条件下效果优于膨润土和沸石,低配比凹凸棒石对衡阳尾矿中Cr、Zn、Cd、Pb、Cu的钝化效果显著。ZHANG等[15]发现,凹凸棒石的施加可显著降低Cu的生物可利用态质量分数,缓解重金属Cu对油菜植株的生理胁迫效应。
常用的凹凸棒石改性方法有无机改性、有机改性、生物质改性和微波改性[16]。LIANG等[17]通过制备巯基改性凹凸棒石钝化Cd污染土壤,可显著增强土壤颗粒对Cd的吸附,抑制农作物对重金属Cd的吸收。XU等[18]将纳米零价铁负载凹凸棒石施用进土壤中,可有效促进重金属Cd、Cr和Pb发生形态转变,并将其固定下来。甘肃省具有丰富的凹凸棒石矿藏,但常常因为品位较低未能得到大规模开发利用。为解决此问题,制备5种不同体积分数H2SO4、不同改性时间的酸改性凹凸棒石,探讨不同钝化材料的添加量对土壤重金属Cu和Zn的钝化效果,并结合环境风险指数和重金属修复效率评估酸改性凹凸棒石的最佳投加量,以期为农田重金属污染土壤的治理和甘肃省凹凸棒石的应用提供参考。
1. 材料与方法
1.1 实验原料
重金属复合污染土壤采自甘肃省白银市东大沟(36° 59′ 96′′ N,104° 22′ 76′′ E)。土壤的基本理化性质为pH 7.28、土壤电导率(EC)1457 µS·cm−1、重金属Cu质量分数为1029.11 mg·kg−1、重金属Ni质量分数为87.18 mg·kg−1、重金属Zn质量分数为707.51 mg·kg−1。其中,Cu和Zn均远超国家标准限值,分别为《土壤环境质量农用地土壤污染风险管控标准》(GB 15618-2018)[19]的5.15倍和2.83倍。
凹凸棒石质黏土复合矿物(简称为“凹凸棒石”)购自甘肃当地,原矿采自甘肃省临泽县板桥镇红色凹凸棒石矿,土状结构,粒度为2 mm左右,主要的矿物成分为凹凸棒石29.7%、石英21.8%、长石14.6%、白云石 6.3%、其他组分27.6%,是一种由凹凸棒石为主,石英和长石以及碳酸盐矿物等伴生的黏土质复合非金属矿物。其主要化学成分为:SiO2 48.38%、Al2O3 11.24%、Fe2O3 4.78%、MgO 7%、CaO 7.41%[20]。
1.2 实验方法
称取定量凹凸棒石,破碎、研磨,过200目筛(直径0.075 mm)。基于49种酸改性钝化材料的研究[21],制备5种优选酸改性凹凸棒石,具体配制条件见表1。将凹凸棒石粉末与不同体积分数的H2SO4溶液混合,固液比为1∶10(m∶v),500 r·min−1转速下搅拌一定时间后,烘干、研磨、过筛制得钝化材料。按2、4、8、16、24 g·kg−1的添加量,将酸改性凹凸棒石钝化材料加入到1.5 kg实际重金属复合污染土壤中,混合均匀,重量法添加去离子水,保持70%的田间持水量,钝化培育30 d后测定土壤的理化性质和重金属形态,每组处理设置不添加任何钝化材料的土壤样品作为对照,记为CK。
表 1 酸改性凹凸棒石的制备方法Table 1. The preparation method of acid modified attapulgite实验编号 H2SO4体积分数/% 反应时间/h A1 10.0 72 A2 12.5 48 A3 12.5 72 A4 12.5 96 A5 15.0 72 1.3 分析方法
采用X射线衍射仪(MiniFlex600,日本Rigaku公司)分析改性前后的凹凸棒石晶体物相组成,扫描速度为10°·min−1,角度为5°~80°,扫描过程采用Cu-Kα 辐照。采用扫描电子显微镜(GeminiSEM500,德国ZEISS公司)观察改性前后凹凸棒石的表面形貌,将样品过200目筛网,在15 kV电压下以相同倍率下放大观察分析。
采用pH计(pHS-3C,上海仪电科学仪器股份有限公司)测定土壤pH,固液比为1∶2.5(m∶v)。采用电导率仪(DDS-307A,上海仪电科学仪器股份有限公司)测定土壤EC,固液比为1∶5(m∶v)。采用BaCl2-H2SO4强迫交换法测定土壤阳离子交换量(CEC)。采用BCR连续提取法测定土壤重金属化学形态。土壤重金属总量经HCl-HNO3-HF-HClO4消解后,火焰原子吸收分光光度计(TAS-990,北京普析通用仪器有限责任公司)测定浓度。
本实验选用H2O和DTPA作为提取剂来评价土壤重金属的生物有效性。土壤重金属水溶态测定时,称取5 g土壤样品与50 mL蒸馏水均匀混合,25 ℃下充分振荡24 h,火焰原子吸收分光光度法测定上清液中重金属浓度。土壤重金属DTPA提取态测定时,称取2 g土壤样品与40 mL DTPA提取液均匀混合,25 ℃下振荡12 h,火焰原子分光光度法测定上清液中重金属浓度。
1.4 指数计算与数据处理方法
污染土壤的生态风险指数(Ecological risk index,ERI)指土壤中活性较高的生物有效态质量分数与重金属总量之比,用于表示土壤中重金属的生态环境风险,常用于底泥沉积物、土壤和污泥中重金属的风险评价,通常分为5个等级,即无风险(<1%)、低风险(1%~10%)、中风险(10%~30%)、高风险(30%~50%)、极高风险(>50%)。按式(1)计算[22-23]。
ERIm=CbsCs×100% (1) 式中:Cbs为土壤中有效态重金属的质量分数,mg·kg−1,Cs为土壤中重金属的质量分数,mg·kg−1。
此外,潜在风险指数(potential ecological risk index)可用于评价多种重金属复合污染的生态风险,可按式(2)、式(3)计算。
Eir=TirCidCib (2) RI=∑ni=1Eir (3) 式中:
Eir Cid Cib CCub CZnb Tir TCur TZnr 表 2 土壤中单一重金属(Er)的潜在生态风险指数Table 2. The potential ecological risk index of single heavy metal (Er) in SoilEr 风险程度 Er ≤ 40 低风险 40 ≤Er <80 中风险 80 ≤ Er < 160 较高风险 160 ≤ Er < 320 高风险 Er > 320 极高风险 表 3 土壤中复合重金属(RI)的潜在生态风险指数Table 3. The potential ecological risk index of total heavy metals (RI) in SoilRI 风险程度 RI ≤ 150 低风险 150 ≤ RI <300 中风险 300 ≤ RI <600 高风险 RI ≥ 600 极高风险 污染土壤中重金属的修复效率(Remediation ratio,RR)指BCR多级提取法中较稳定的重金属残渣态(S4)与土壤重金属4种形态总和的比值,可用于评估重金属的潜在活化风险,按式(4)计算[24]。
RR=S4S1+S2+S3+S4×100% (4) 式中: S1为重金属元素酸溶态质量分数,mg·kg−1;S2为重金属元素还原态质量分数,mg·kg−1;S3为重金属元素氧化态质量分数,mg·kg−1;S4为重金属元素残渣态质量分数,mg·kg−1。
2. 结果与讨论
2.1 土壤理化性质
土壤pH、电导率和阳离子交换量影响着重金属的化学形态,是评价重金属迁移转化和作物生长发育情况的重要指标[25]。施用不同酸改性凹凸棒石后的土壤pH见图1(a),与对照组相比,向土壤中施加5种酸改性凹凸棒石后,土壤pH均呈现显著降低的趋势。在同一投加量水平下,A3处理组pH显著低于其他处理组。这是因为,天然的凹凸棒石本身呈弱碱性,含有大量的羟基等官能团[26],而改性添加的H2SO4具有强酸性,能够和土壤及凹凸棒石中的碱性物质发生反应,从而降低土壤pH,调节土壤的酸碱度。本研究采用的实际污染土壤为北方地区常见的碱性土壤,酸改性凹凸石的施用有效改善了土壤的酸碱环境。不同酸改性凹凸棒石处理后的土壤EC见图1(b),在同一酸改性凹凸棒石处理组中,土壤EC随着添加量的增加而显著增加,且A5处理组EC值显著高于其他处理组。土壤CEC随着凹凸棒石添加量的增加而增加,但不同添加量间差异性不显著(图1(c))。除A4材料投加量为8 mg·kg−1时土壤CEC较高外,其他投加量水平下,A5处理组CEC也显著高于其他处理组。一方面,凹凸棒石的表面带有Na+、K+和Ca2+等阳离子,本身具有较高的阳离子交换容量,随着投加量的增加,土壤中带电的离子浓度升高,从而提高土壤电导率[27];另一方面,当改性时添加的H2SO4体积分数较大时,凹凸棒石表面会带有大量的H+,这些活泼的阳离子可能会和土壤中的Cu2+、Zn2+发生阳离子交换反应,提高土壤的EC和CEC [28]。
2.2 土壤重金属的生物有效态
土壤中重金属的水溶态可直观地反映重金属的生物可利用度,这部分形态的重金属质量分数很低,但是却可以直接被植物吸收利用,具有极强的迁移性和毒性,因此常常作为土壤重金属污染评价的重要指标[29]。不同改性凹凸棒石处理后的土壤生物有效态重金属质量分数见图2。从图2可以看出,添加酸改性凹凸棒石后,水溶态Cu和Zn的质量分数均较对照组显著降低。尽管随着投加量的增加,水溶态重金属质量分数出现了先降低后轻微升高的趋势,但差异并未达显著水平。实验结果表明,当投加量为16 g·kg−1时,酸改性凹凸棒石对Cu、Zn的钝化效果最好。其中,A5处理组中水溶态Cu的质量分数最低,较对照组降低了47.38%;A3处理组中水溶态Zn的质量分数最低,较对照组降低了64.44%。土壤中DTPA提取态重金属质量分数常常用来评估植物对重金属的吸收情况,DTPA络合剂能够与重金属离子结合,形成稳定的水溶性络合物,可直观地评价重金属的生物有效性[30]。添加酸改性凹凸棒石后,Cu和Zn的DTPA提取态质量分数均较对照组显著降低。当投加量为16 g·kg−1时,A5处理组中DTPA提取态Cu的质量分数最低,较对照组下降了24.25%,A3处理组中DTPA提取态Zn的质量分数最低,较CK下降了46.77%。DTPA提取态重金属的降低趋势与水溶态重金属基本保持一致。这与罗宁临等[31]的研究结果基本一致。造成以上结果的原因可能是:1)酸改性使得凹凸棒石表面和孔隙内的碳酸盐杂质得以去除,晶束团聚结构变得更加紧密,内表面积和缝隙增大,增强了其对重金属Cu、Zn的吸附能力[32];2)酸改性凹凸棒石的施用提高了土壤的阳离子交换容量,土壤中游离的Cu2+、Zn2+通过阳离子交换作用,与带有负电荷的凹凸棒石和土壤颗粒结合,显著降低了重金属的生物有效性[27,33];3)凹凸棒石表面带有大量的硅羟基等官能团,能与重金属发生络合反应,从而将其固定[14,34]。本研究结果说明,采用优质的钝化材料是降低土壤重金属毒性的关键,而控制合适的投加量对农田土壤的修复也至关重要。
2.3 土壤重金属形态分布
BCR多级提取法中,重金属各种形态的活性大小依次为酸溶态>可还原态>可氧化态>残渣态[35]。其中,酸溶态重金属的生物可利用度最高,可还原态和可氧化态重金属容易随着pH和氧化还原电位等环境条件的变化而变化,重新释放到环境介质中,残渣态重金属最稳定,不易在土壤中迁移转化,生态毒性最低[35-37]。酸改性凹凸棒石钝化后土壤中重金属形态分布见图3和图4。添加不同酸改性凹凸棒石后,酸溶态Cu和Zn的质量分数较对照组显著降低,而残渣态Cu和Zn的质量分数上升(图3,图4)。当投加量为16 g·kg−1时,A3处理组中酸溶态Cu和Zn的占比最低,残渣态Cu的比例较对照组上升了3.96%;残渣态Zn的比例较对照组上升了15.26%,这与武成辉等[38]和陶玲等[39]的研究结果一致。添加不同酸改性凹凸棒石可影响重金属在土壤中的形态,促进重金属从活性较高的酸溶态、可还原态向活性较低的可氧化态、残渣态转变,降低了Cu、Zn的生态毒性,实现了土壤的钝化修复。其原因可能是:1)凹凸棒石及其改性材料的添加可通过一系列吸附、离子交换、沉淀和络合作用降低酸溶态Cu、Zn质量分数[40];2)凹凸棒石经过酸处理后,起支撑作用的八面体和四面体溶解,导致凹凸棒石的孔道增大,比表面积增加,凹凸棒石的吸附性能提高[41];3)残渣态重金属 Cu、Zn一般存在于硅酸盐、原生和次生矿物等土壤的晶格中,当向污染土壤中施用酸改性凹凸棒石后,随着钝化时间的延长,低价的Cu2+、Zn2+可能会在凹凸棒石八面体或四面体结构中与Si4+发生晶格置换,能长期稳定在土壤中[42]。
2.4 酸改性凹凸棒石的表征分析
为验证上述作用机理,本实验对凹凸棒石改性前后的微观形貌和晶体结构进行表征,扫描电子显微镜图像如图5所示。供试凹凸棒石原矿(ATP)主要呈棒状晶束堆积结构,晶束较长,棒晶密实,孔道结构较少。经不同浓度H2SO4和不同活化时间处理后,凹凸棒石的棒晶发生解束,晶束变短,排列相对松散,可直接接触的点位增多,增强了凹凸棒石对重金属的吸附能力。这与陈雪芳[43]等的研究结果一致:酸改性能够溶解凹凸棒石中的八面体阳离子和四面体硅,使得八面体结构起主要的支撑作用,凹凸棒石孔道开放,孔径增大,比表面积增大,吸附性能提高。但是,当酸浓度较高时,会对层间的阳离子起较强的溶出作用,破坏晶体结构,进而降低凹凸棒石的吸附性能[44]。
酸改性凹凸棒石的X射线衍射图谱结果见图6。凹凸棒石的特征峰位于8.40°处,与标准衍射图谱(JCPDFNo.020018)一致。石英特征衍射峰的存在证实了凹凸棒石中伴生有其他物相的杂质。从图中可以看出,经过酸改性后,凹凸棒石质黏土复合矿物物相组成及凹凸棒石、白云石物相的衍射峰峰强度没有明显改变,石英杂质的峰强度有轻微减弱。这表明,酸改性过程溶解了碳酸盐等杂质,但是并未破坏凹凸棒石的骨架结构。该结果与雷春生等[45]和张萍等[46]的研究结果一致。本研究结果表明,适宜的酸浓度和改性时间能够有效改善天然凹凸棒石原矿的表面形貌和孔隙结构,使得钝化材料孔隙结构增多,孔径变大,比表面积增大,促进了其对重金属的钝化修复。
2.5 土壤重金属的环境风险评价和钝化修复效率
与土壤中重金属的总量相比,水溶态Cu和Zn的质量分数占比不到0.01%。因此,本研究根据DTPA提取态重金属的质量分数来评价酸改性凹凸棒石钝化剂对土壤重金属的修复效率和生态风险。对照组污染土壤中Cu和Zn的环境风险指数分别对应为24.4%和11.51%。经不同的钝化材料处理后,土壤重金属的环境风险均较对照组显著降低(表4)。当施用A5钝化材料且投加量为16 g·kg−1时,酸改性凹凸棒石处理后Cu的环境风险指数降至最低。土壤Zn的环境风险由中风险降为低风险(表5),当施用A3材料且投加量为16 g·kg−1时,Zn的环境风险指数最低。
表 4 不同添加量酸改性凹凸棒石钝化土壤中Cu的环境风险指数Table 4. The environmental risk index of Cu in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) ERI/% A1 A2 A3 A4 A5 2 21.81±0.13Aa 20.80±0.02Ab 20.40±0.11Ac 20.35±0.07Ac 20.49±0.23Ac 4 21.72±0.06Aa 20.32±0.14Bb 19.88±0.26BCc 19.77±0.15BCc 20.28±0.13Ab 8 20.26±0.07Ba 19.97±0.14Cb 20.10±0.13ABab 19.42±0.18Dab 19.36±0.06Bc 16 19.80±0.15Ca 19.35±0.21Db 19.67±0.11Ca 19.87±0.07Ba 18.48±0.17Dc 24 19.43±0.18Dab 19.24±0.15Db 19.35±0.17Dab 19.56±0.10CDab 18.78±0.09Cc 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 5 不同添加量酸改性凹凸棒石钝化土壤中Zn的环境风险指数Table 5. The environmental risk index of Zn in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) ERI/% A1 A2 A3 A4 A5 2 9.47±0.03Aa 8.85±0.09Ab 8.55±0.11Ac 8.24±0.11Ad 8.31±0.04Ad 4 8.52±0.11BCab 8.59±0.11Ba 8.36±0.06Abc 8.00±0.08Bd 8.31±0.15Ac 8 8.83±0.10BCa 8.39±0.10Cb 8.48±0.19Ab 7.29±0.15Cc 8.21±0.20Ab 16 8.27±0.06Ca 8.13±0.09Da 6.13±0.10Bc 7.09±0.10Db 8.11±0.16Aa 24 8.88±0.66Ba 8.14±0.15Db 6.23±0.22Bd 7.00±0.09Dc 8.26±0.14Ab 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 在复合重金属污染土壤中,除了考虑单一重金属的环境风险外,受元素共存的联合作用影响,本研究评价了多种重金属的总环境风险指数RI。除添加量为16 g·kg−1的A1处理外,其他处理均显著降低了土壤RI。由图7可知,A3材料在较高添加量(≥8 g·kg−1)时,土壤RI指数随着添加量的增加显著降低。施用A5材料且添加量为16 g·kg−1时土壤中Cu、Zn的总生态风险指数达到最低。
钝化完成后,通常根据土壤中重金属的修复效率来评价钝化材料的实际应用价值。添加酸改性凹凸棒石后,Cu的修复效率随着投加量的增加呈先升高后轻微降低的趋势(表6),当钝化材料的投加量为16 g·kg−1时,重金属Cu的修复效率明显高于其他处理组。其中,A3处理组的钝化修复效率最高,达11.96%。重金属Zn修复效率的变化趋势与Cu基本一致(表7),当向土壤中施加16 g·kg−1的酸改性凹凸棒石后,Zn的修复效率明显高于其他处理组。其中,A3处理组Zn的钝化修复效率最高,为27.70%。
表 6 不同添加量酸改性凹凸棒石钝化土壤中Cu的修复效率Table 6. The remediation ratio of Cu in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) RR/% A1 A2 A3 A4 A5 2 7.90±0.22Dc 7.48±0.26Cc 9.52±0.12Ca 8.55±0.58Cb 7.64±0.17Dc 4 8.56±0.12Cb 7.82±0.31BCc 9.74±0.25Ca 9.62±0.23BCa 8.55±0.26Cb 8 9.11±0.12Bcd 8.53±0.24Bd 10.20±0.45BCb 11.01±0.62ABa 9.76±0.20Bbc 16 11.51±0.30Aa 9.87±0.28Ab 11.96±0.93Aa 11.24±0.15Aab 11.15±0.32Aab 24 11.30±0.31Aab 9.47±0.88Ac 11.00±0.38Bab 11.58±0.60Aa 10.35±0.74Bbc 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 7 不同添加量酸改性凹凸棒石钝化土壤中Zn的修复效率Table 7. The remediation ratio of Zn in soil stabilized with different amount of acid-modified attapulgite酸改性凹凸棒石添加量/(g·kg−1) RR/% A1 A2 A3 A4 A5 2 19.21±0.40Cc 20.83±0.38Cb 22.62±0.47Da 20.51±0.98Db 23.52±0.99Ca 4 21.20±0.48Bb 20.86±0.46Cb 24.86±1.00Ca 21.18±0.30CDb 25.63±0.30ABa 8 22.39±0.72ABb 22.50±0.60BCb 24.74±0.34Ca 21.97±0.52BCb 25.14±0.72BCa 16 23.55±0.12Ac 25.16±0.15Abc 27.70±0.11Aa 24.82±0.11Ac 27.40±0.14Aab 24 23.06±0.70Ab 22.91±0.15Bb 26.23±0.36Ba 23.06±0.39Bb 26.77±0.12ABa 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 3. 结论
1)当H2SO4的体积分数为12.5%和15%,改性时间为72 h时,制得的酸改性凹凸棒石对Cu、Zn的钝化效果最佳,其最优投加量为16 g·kg−1。
2)向土壤中施加酸改性凹凸棒石,可显著降低重金属Cu、Zn的生物有效态质量分数,当钝化材料的投加量为16 g·kg−1时,H2O提取态Cu、Zn分别降低了25.91%~47.87%和49.69%~65%,DTPA提取态Cu、Zn分别降低了8.63%~24.30%和28.26%~46.84%。这说明,16 g·kg−1凹凸棒石可以有效降低Cu、Zn的生物有效性。
3)酸改性凹凸棒石的添加促使重金属Cu、Zn由活性较高的酸溶态向活性较低的残渣态转变,提高土壤重金属修复效率,当H2SO4的体积分数为12.5%,改性时间为72 h时,向土壤中投加16 g·kg−1酸改性凹凸棒石,Cu、Zn的修复效率最高,可达11.96%和27.70%,此时Zn的环境风险最低,降至6.13%,处于低风险。
-
表 1 酸改性凹凸棒石的制备方法
Table 1. The preparation method of acid modified attapulgite
实验编号 H2SO4体积分数/% 反应时间/h A1 10.0 72 A2 12.5 48 A3 12.5 72 A4 12.5 96 A5 15.0 72 表 2 土壤中单一重金属(Er)的潜在生态风险指数
Table 2. The potential ecological risk index of single heavy metal (Er) in Soil
Er 风险程度 Er ≤ 40 低风险 40 ≤Er <80 中风险 80 ≤ Er < 160 较高风险 160 ≤ Er < 320 高风险 Er > 320 极高风险 表 3 土壤中复合重金属(RI)的潜在生态风险指数
Table 3. The potential ecological risk index of total heavy metals (RI) in Soil
RI 风险程度 RI ≤ 150 低风险 150 ≤ RI <300 中风险 300 ≤ RI <600 高风险 RI ≥ 600 极高风险 表 4 不同添加量酸改性凹凸棒石钝化土壤中Cu的环境风险指数
Table 4. The environmental risk index of Cu in soil stabilized with different amount of acid-modified attapulgite
酸改性凹凸棒石添加量/(g·kg−1) ERI/% A1 A2 A3 A4 A5 2 21.81±0.13Aa 20.80±0.02Ab 20.40±0.11Ac 20.35±0.07Ac 20.49±0.23Ac 4 21.72±0.06Aa 20.32±0.14Bb 19.88±0.26BCc 19.77±0.15BCc 20.28±0.13Ab 8 20.26±0.07Ba 19.97±0.14Cb 20.10±0.13ABab 19.42±0.18Dab 19.36±0.06Bc 16 19.80±0.15Ca 19.35±0.21Db 19.67±0.11Ca 19.87±0.07Ba 18.48±0.17Dc 24 19.43±0.18Dab 19.24±0.15Db 19.35±0.17Dab 19.56±0.10CDab 18.78±0.09Cc 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 5 不同添加量酸改性凹凸棒石钝化土壤中Zn的环境风险指数
Table 5. The environmental risk index of Zn in soil stabilized with different amount of acid-modified attapulgite
酸改性凹凸棒石添加量/(g·kg−1) ERI/% A1 A2 A3 A4 A5 2 9.47±0.03Aa 8.85±0.09Ab 8.55±0.11Ac 8.24±0.11Ad 8.31±0.04Ad 4 8.52±0.11BCab 8.59±0.11Ba 8.36±0.06Abc 8.00±0.08Bd 8.31±0.15Ac 8 8.83±0.10BCa 8.39±0.10Cb 8.48±0.19Ab 7.29±0.15Cc 8.21±0.20Ab 16 8.27±0.06Ca 8.13±0.09Da 6.13±0.10Bc 7.09±0.10Db 8.11±0.16Aa 24 8.88±0.66Ba 8.14±0.15Db 6.23±0.22Bd 7.00±0.09Dc 8.26±0.14Ab 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 6 不同添加量酸改性凹凸棒石钝化土壤中Cu的修复效率
Table 6. The remediation ratio of Cu in soil stabilized with different amount of acid-modified attapulgite
酸改性凹凸棒石添加量/(g·kg−1) RR/% A1 A2 A3 A4 A5 2 7.90±0.22Dc 7.48±0.26Cc 9.52±0.12Ca 8.55±0.58Cb 7.64±0.17Dc 4 8.56±0.12Cb 7.82±0.31BCc 9.74±0.25Ca 9.62±0.23BCa 8.55±0.26Cb 8 9.11±0.12Bcd 8.53±0.24Bd 10.20±0.45BCb 11.01±0.62ABa 9.76±0.20Bbc 16 11.51±0.30Aa 9.87±0.28Ab 11.96±0.93Aa 11.24±0.15Aab 11.15±0.32Aab 24 11.30±0.31Aab 9.47±0.88Ac 11.00±0.38Bab 11.58±0.60Aa 10.35±0.74Bbc 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 表 7 不同添加量酸改性凹凸棒石钝化土壤中Zn的修复效率
Table 7. The remediation ratio of Zn in soil stabilized with different amount of acid-modified attapulgite
酸改性凹凸棒石添加量/(g·kg−1) RR/% A1 A2 A3 A4 A5 2 19.21±0.40Cc 20.83±0.38Cb 22.62±0.47Da 20.51±0.98Db 23.52±0.99Ca 4 21.20±0.48Bb 20.86±0.46Cb 24.86±1.00Ca 21.18±0.30CDb 25.63±0.30ABa 8 22.39±0.72ABb 22.50±0.60BCb 24.74±0.34Ca 21.97±0.52BCb 25.14±0.72BCa 16 23.55±0.12Ac 25.16±0.15Abc 27.70±0.11Aa 24.82±0.11Ac 27.40±0.14Aab 24 23.06±0.70Ab 22.91±0.15Bb 26.23±0.36Ba 23.06±0.39Bb 26.77±0.12ABa 注:大写字母表示不同投加量之间的差异性,小写字母表示不同钝化材料之间的差异性。 -
[1] 环境保护部, 国土资源部. 全国土壤污染状况调查公报(2014)[EB/OL]. [2014-04-17]. http://www.zhb.gov.cn/gkml/hbb/qt/201404/t20140417_270670.htm. [2] 焦丽香, 郭加朋. 土壤重金属的污染与治理进展研究[J]. 科技情报开发与经济, 2009, 19(1): 155-156. [3] 黄益宗, 郝晓伟, 雷鸣, 等. 重金属污染土壤修复技术及其修复实践[J]. 农业环境科学学报, 2013, 32(3): 409-417. [4] 李剑睿, 徐应明, 林大松, 等. 农田重金属污染原位钝化修复研究进展[J]. 生态环境学报, 2014, 23(4): 721-728. doi: 10.3969/j.issn.1674-5906.2014.04.029 [5] GUO F Y, DING C F, ZHOU Z G, et al. Stability of immobilization remediation of several amendments on cadmium contaminated soils as affected by simulated soil acidification[J]. Ecotoxicology And Environmental Safety, 2018, 161: 164-172. doi: 10.1016/j.ecoenv.2018.05.088 [6] HUANG G Y, GAO R L, YOU J W, et al. Oxalic acid activated phosphate rock and bone meal to immobilize Cu and Pb in mine soils[J]. Ecotoxicology And Environmental Safety, 2019, 174.: 401-407. doi: 10.1016/j.ecoenv.2019.02.076 [7] LIU Y Y, XU Y M, QIN X, et al. Effects of water and organic manure coupling on the immobilization of cadmium by sepiolite[J]. Journal of Soils and Sediments, 2019, 19(2): 798-808. doi: 10.1007/s11368-018-2081-5 [8] MU J, HU Z Y, HUANG L J, et al. Influence of alkaline silicon-based amendment and incorporated with biochar on the growth and heavy metal translocation and accumulation of vetiver grass (Vetiveria zizanioides) grown in multi-metal-contaminated soils[J]. Journal of Soils and Sediments, 2019, 19(5): 2277-2289. doi: 10.1007/s11368-018-2219-5 [9] YU Y Q, ZHANG K W, YANG J Y. Stabilization of Cd and Zn in soil using pairwise mixed amendments of three raw materials: nanohydroxyapatite, nanoiron and nanoalumina[J]. Research on Chemical Intermediates, 2018, 44(5): 2965-2981. doi: 10.1007/s11164-018-3288-1 [10] FAJARDO C, COSTA G, MANDE M, et al. Heavy metals immobilization capability of two iron-based nanoparticles (nZVI and Fe3O4): Soil and freshwater bioassays to assess ecotoxicological impact[J]. Science of the Total Environment, 2019, 656: 421-432. doi: 10.1016/j.scitotenv.2018.11.323 [11] 袁峰, 唐先进, 吴骥子, 等. 两种铁基材料对污染农田土壤砷、铅、镉的钝化修复[J]. 环境科学, 2021, 42(7): 3535-3548. [12] 丁园, 敖师营, 陈怡红, 等. 4种钝化剂对污染水稻土中Cu和Cd的固持机制[J]. 环境科学, 2021, 42(8): 4037-4044. [13] 谭科艳, 刘晓端, 刘久臣, 等. 凹凸棒石用于修复铜锌镉重金属污染土壤的研究[J]. 岩矿测试, 2011, 30(4): 451-456. doi: 10.3969/j.issn.0254-5357.2011.04.012 [14] 马博. 凹凸棒石对重金属的钝化及在尾矿和农田中的应用研究[D]. 北京: 中国地质大学, 2018. [15] ZHANG M D, RAN R L, NAO SAI W Q, et al. Physiological effects of short-term copper stress on rape (Brassica napus L. ) seedlings and the alleviation of copper stress by attapulgite clay in growth medium[J]. Ecotoxicology and Environmental Safety, 2019, 171: 876-886. [16] 田振华, 薛胜平. 凹凸棒石改性及其修复重金属污染土壤的研究[J]. 应用化工, 2019, 48(4): 883-887. doi: 10.3969/j.issn.1671-3206.2019.04.036 [17] LIANG X F, LI N, HE L Z, et al. Inhibition of Cd accumulation in winter wheat (Triticum aestivum L. ) grown in alkaline soil using mercapto-modified attapulgite[J]. Science of the Total Environment, 2019, 688: 818-826. doi: 10.1016/j.scitotenv.2019.06.335 [18] XU C B, QI J, YANG W J, et al. Immobilization of heavy metals in vegetable-growing soils using nano zero-valent iron modified attapulgite clay[J]. Science of the Total Environment, 2019, 686: 476-483. doi: 10.1016/j.scitotenv.2019.05.330 [19] 生态环境部. 土壤环境质量农用地土壤污染风险管控标准(试行): GB 15618-2018[S]. 北京: 中国标准出版社, 2018. [20] 任珺, 刘丽莉, 陶玲, 等. 甘肃地区凹凸棒石的矿物组成分析[J]. 硅酸盐通报, 2013, 32(11): 2362-2365. [21] 陶玲, 杨欣, 颜子皓, 等. 酸活化坡缕石制备重金属钝化材料的研究[J]. 非金属矿, 2018, 41(1): 11-14. doi: 10.3969/j.issn.1000-8098.2018.01.004 [22] XUE W J, HUANG D L, ZENG G M, et al. Nanoscale zero-valent iron coated with rhamnolipid as an effective stabilizer for immobilization of Cd and Pb in river sediments[J]. Journal of Hazardous Materials, 2018, 341: 381-389. doi: 10.1016/j.jhazmat.2017.06.028 [23] KE X, GUI S F, HUANG H, et al. Ecological risk assessment and source identification for heavy metals in surface sediment from the Liaohe River protected area, China[J]. Chemosphere, 2017, 175: 473-481. doi: 10.1016/j.chemosphere.2017.02.029 [24] NEMATI K, ABU B N K, ABAS M R, et al. Speciation of heavy metals by modified BCR sequential extraction procedure in different depths of sediments from Sungai Buloh, Selangor, Malaysia[J]. Journal of Hazardous Materials, 2011, 192(1): 402-410. [25] 王英杰, 邹佳玲, 杨文弢, 等. 组配改良剂对稻田系统Pb、Cd和As生物有效性的协同调控[J]. 环境科学, 2016, 37(10): 4004-4010. [26] WANG W, CHEN H, WANG A. Adsorption characteristics of Cd (II)from aqueous solution onto activated palygorskite[J]. Separation and Purification Technology, 2007, 55(2): 157-164. doi: 10.1016/j.seppur.2006.11.015 [27] 廖启林, 刘聪, 朱伯万, 等. 凹凸棒石调控Cd污染土壤的作用及其效果[J]. 中国地质, 2014, 41(5): 1693-1704. doi: 10.3969/j.issn.1000-3657.2014.05.023 [28] 赵廷伟, 李洪达, 周薇, 等. 施用凹凸棒石对Cd污染农田土壤养分的影响[J]. 农业环境科学学报, 2019, 38(10): 2313-2318. doi: 10.11654/jaes.2019-0783 [29] 雷鸣, 廖柏寒, 秦普丰. 土壤重金属化学形态的生物可利用性评价[J]. 生态环境, 2007(5): 1551-1556. [30] 关天霞, 何红波, 张旭东, 等. 土壤中重金属元素形态分析方法及形态分布的影响因素[J]. 土壤通报, 2011, 42(2): 503-512. doi: 10.19336/j.cnki.trtb.2011.02.049 [31] 罗宁临, 李忠武, 黄梅, 等. 壳聚糖(改性)-沸石对农田土壤重金属镉钝化技术研究[J]. 湖南大学学报(自然科学版), 2020, 47(4): 132-140. [32] 章绍康, 弓晓峰, 申钊颖, 等. 改性凹凸棒土对土壤中Cd2+吸附解吸及钝化效果影响[J]. 环境工程, 2019, 37(3): 192-197. [33] 陈炳睿, 徐超, 吕高明, 等. 6种固化剂对土壤Pb Cd Cu Zn的固化效果[J]. 农业环境科学学报, 2012, 31(7): 1330-1336. [34] 韩君, 梁学峰, 徐应明, 等. 黏土矿物原位修复镉污染稻田及其对土壤氮磷和酶活性的影响[J]. 环境科学学报, 2014, 34(11): 2853-2860. [35] 赵庆圆, 李小明, 杨麒, 等. 磷酸盐、腐殖酸与粉煤灰联合钝化处理模拟铅镉污染土壤[J]. 环境科学, 2018, 39(1): 389-398. [36] ZHU Y G, CHEN S B, YANG J C. Effects of soil amendments on lead uptake by two vegetable crops from a lead-contaminated soil from Anhui, China[J]. Environ International, 2004, 30(3): 351-356. doi: 10.1016/j.envint.2003.07.001 [37] WEN J, ZENG G M. Chemical and biological assessment of Cd-polluted sediment for land use: The effect of stabilization using chitosan-coated zeolite[J]. Journal of Environmental Management, 2018, 212: 46-53. [38] 武成辉, 李亮, 雷畅, 等. 硅酸盐钝化剂在土壤重金属污染修复中的研究与应用[J]. 土壤, 2017, 49(3): 446-452. [39] 陶玲, 张晓郡, 刘瑞珍, 等. 热改性坡缕石对土壤镉污染的钝化效果及对土壤镉生态毒性的影响[J]. 环境工程学报, 2021, 15(6): 2008-2017. doi: 10.12030/j.cjee.202101103 [40] WANG H, WANG X J, Li J, et al. Comparison of palygorskite and struvite supported palygorskite derived from phosphate recovery in wastewater for in-situ immobilization of Cu, Pb and Cd in contaminated soil[J]. Journal of Hazardous Materials, 2018, 346: 273-284. doi: 10.1016/j.jhazmat.2017.12.042 [41] 于方群, 周健民, 王火焰, 等. 凹凸棒石环境矿物材料的制备及应用[J]. 土壤, 2009, 41(4): 525-533. doi: 10.3321/j.issn:0253-9829.2009.04.004 [42] 黄昌勇. 土壤学[J]. 中国农业出版社, 2010: 158-168. [43] 陈雪芳, 熊莲, 王璨, 等. 酸改性对低品位凹凸棒石的白度和组成结构的影响[J]. 硅酸盐通报, 2017, 36(12): 4198-4204. [44] 于方群, 周健民, 王火焰, 等. 不同浓度酸改性对凹凸棒石黏土磷吸附性能的影响[J]. 土壤学报, 2010, 47(2): 319-324. doi: 10.11766/trxb2010470216 [45] 雷春生, 朱晓峰, 高雯, 等. 酸活化凹凸棒黏土对印染废水中亚甲基蓝的吸附性能[J]. 环境工程学报, 2017, 11(2): 885-891. doi: 10.12030/j.cjee.201509236 [46] 张萍, 文科, 王钺博, 等. 酸处理对坡缕石结构及其苯吸附性能的影响[J]. 矿物学报, 2018, 38(1): 93-99. doi: 10.16461/j.cnki.1000-4734.2018.011 -




 DownLoad:
DownLoad: