-
高炉煤气是炼铁行业的主要副产物,是钢铁企业重要的二次能源,已成为钢铁企业节能降耗及达标排放的关键[1-3]。高炉煤气气量大,每炼1 t铁可生产1 700~2 500 m3高炉煤气。目前,我国高炉煤气的产量高达2.33×109~2.67 ×109 m3·d−1,为将其净化并后续应用,主要采用重力除尘器联用袋式除尘器以去除颗粒物。在其经余压发电后送往高炉热风炉、轧钢加热炉、煤气发电等用户单元作为燃料使用,但未经脱硫净化处理的高炉煤气在燃烧后会产生SO2。这使得烟气的SO2质量浓度无法满足国家超低排放限值50 mg·m−3,故亟待治理[4]。
高炉煤气成分与高炉所用燃料、所炼生铁的品种和冶炼工艺有关[5-6],主要成分包括CO、CO2、N2、O2、H2,以及少量硫化物。其中,硫化物包括羰基硫(carbonyl sulfide,COS)、H2S、二硫化碳(CS2)、硫醇、硫醚和噻吩等,以COS、H2S为主。COS约占总硫的80%。H2S易与碱性物质发生中和反应而去除,而有机硫COS相对比较稳定,用常规方法难以直接脱除。这亦成为高炉煤气精脱硫技术的主要对象和技术突破点[7-8]。
高炉煤气精脱硫是一项正研发试用中的新兴技术。目前,高炉煤气脱硫主要工艺路线为:高炉煤气
→ 重力除尘→ 袋式除尘→ 有机硫水解转化→ 余压透平发电系统(blast furnace top gas recovery turbine unit,TRT)→ 干法或湿法脱除硫化氢→ 管网。此工艺包含水解和H2S脱除两段工序。工艺尚存在投资高、水解催化剂技术不成熟、使用寿命短等问题;在有机硫水解转化后高炉煤气中H2S增多,H2S处于高温高压环境中并溶于煤气冷凝水,会形成氢硫酸并对TRT设施和附属管道带来腐蚀作用[4]。脱硫设备阻力会提高TRT背压,从而影响TRT的发电量[9-10]。为简化脱硫工艺、解决脱硫系统对除尘系统和TRT的发电量影响、反应器和附属管道的腐蚀等问题,本研究提出一种电化学协同增效湿法吸收精脱硫工艺:高炉煤气
→ 重力除尘→ 袋式除尘→ 余压透平发电系统(TRT)→ 电化学协同湿法吸收脱硫→ 管网。基于电化学协同湿法吸收精脱硫工艺方法,得到复合吸收剂(Na2CO3+EDTA+EDTA-2Na)的最佳组分配比、脱硫性能规律及机理,以期为高炉煤气精脱硫技术发展及关键工艺参数的确定提供参考。 -
实验所用原料气为模拟高炉煤气的标气配气,其中各组分的参数见表1。
-
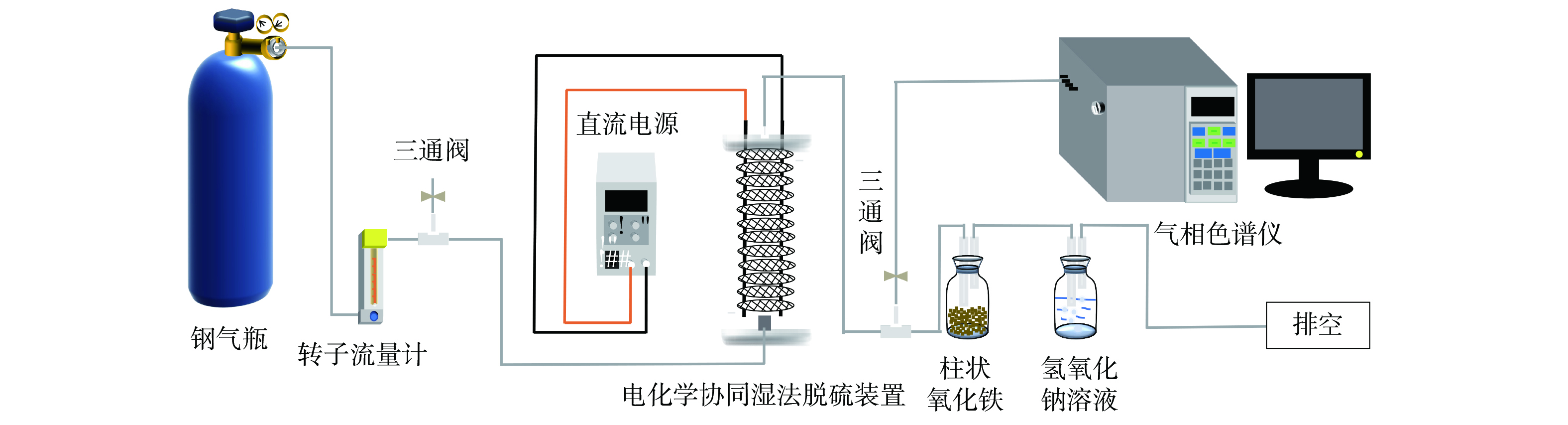
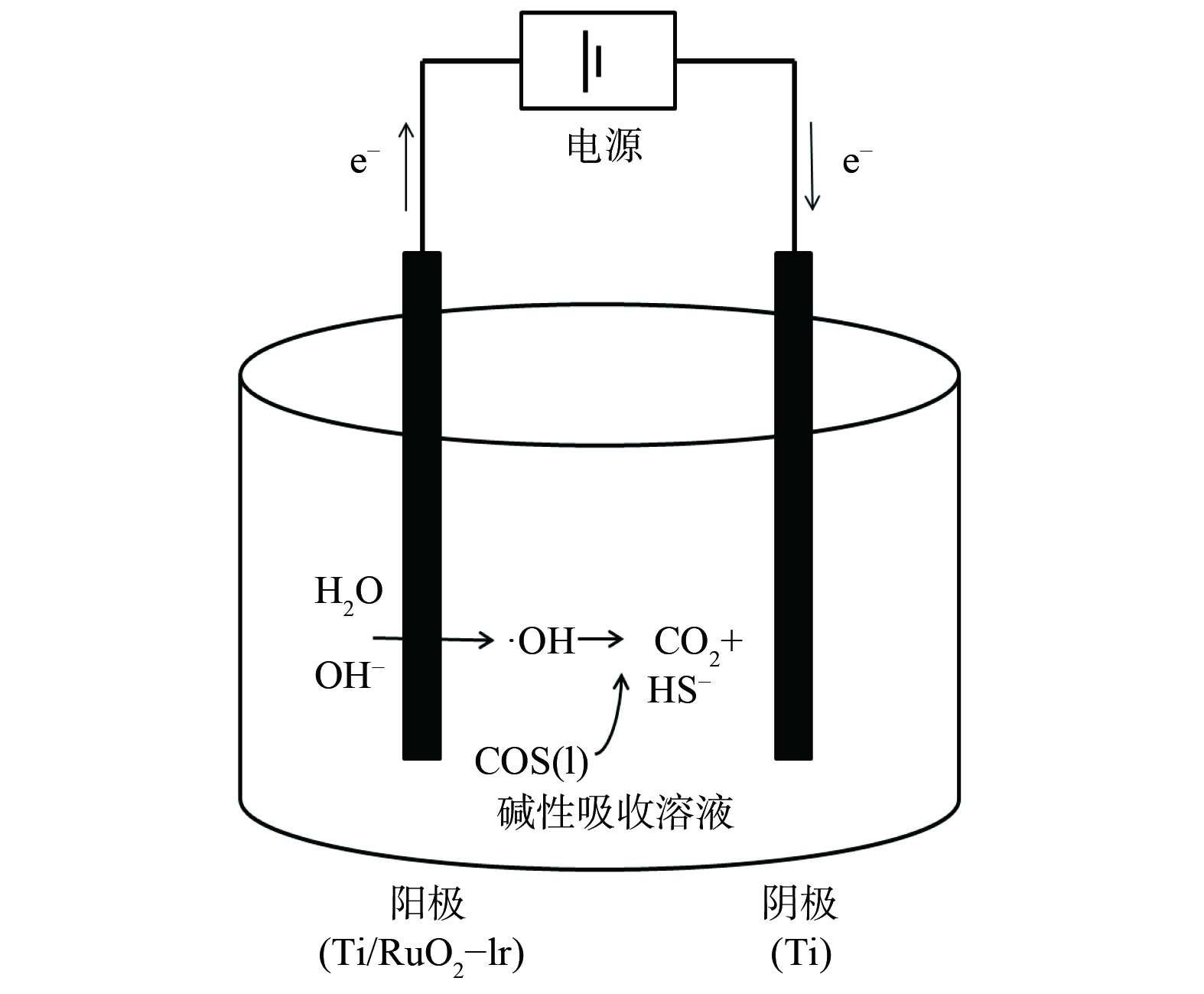
实验系统主要由配气系统、电化学协同湿法吸收装置、尾气吸收瓶和气体分析检测系统组成(图1)。电化学协同湿法吸收装置的主体为Φ65 mm圆柱形石英玻璃管。石英玻璃壳体外部下端设有进气口(配气进入反应装置的压力为0.04 MPa)、出液口,上端设有出气口、进液口。系统中内置有长度60 cm、直径2 mm的惰性阴极柱、阳极柱浸泡于吸收液中,吸收液液位高度为45.20 cm,且外加电源的负极和正极分别与其相连接。阳极柱和阴极柱分别与涂有贵金属钌铱的金属钛网和金属钛网镶嵌链接。两种钛网相互交错,构成层式塔状结构以增加COS与电极接触面积和接触时间。吸收装置压降为3.5~4.0 kPa。气体分析检测采用GC9790Ⅱ气相色谱仪(浙江福立,FPD检测器)。
-
电化学较常规碱性介质脱除COS方法提高了反应速率和脱除率。电化学催化氧化脱硫机理如图2所示,该方法借助电化学电极催化活性,在阳极电极界面附近直接或间接产生具有更高氧化能力的
⋅OH 等活性物质,并利用这些活性物质打开C==S、分解COS,将COS催化氧化为CO2和HS−,从而提高了有机硫的去除效率[11]。 -
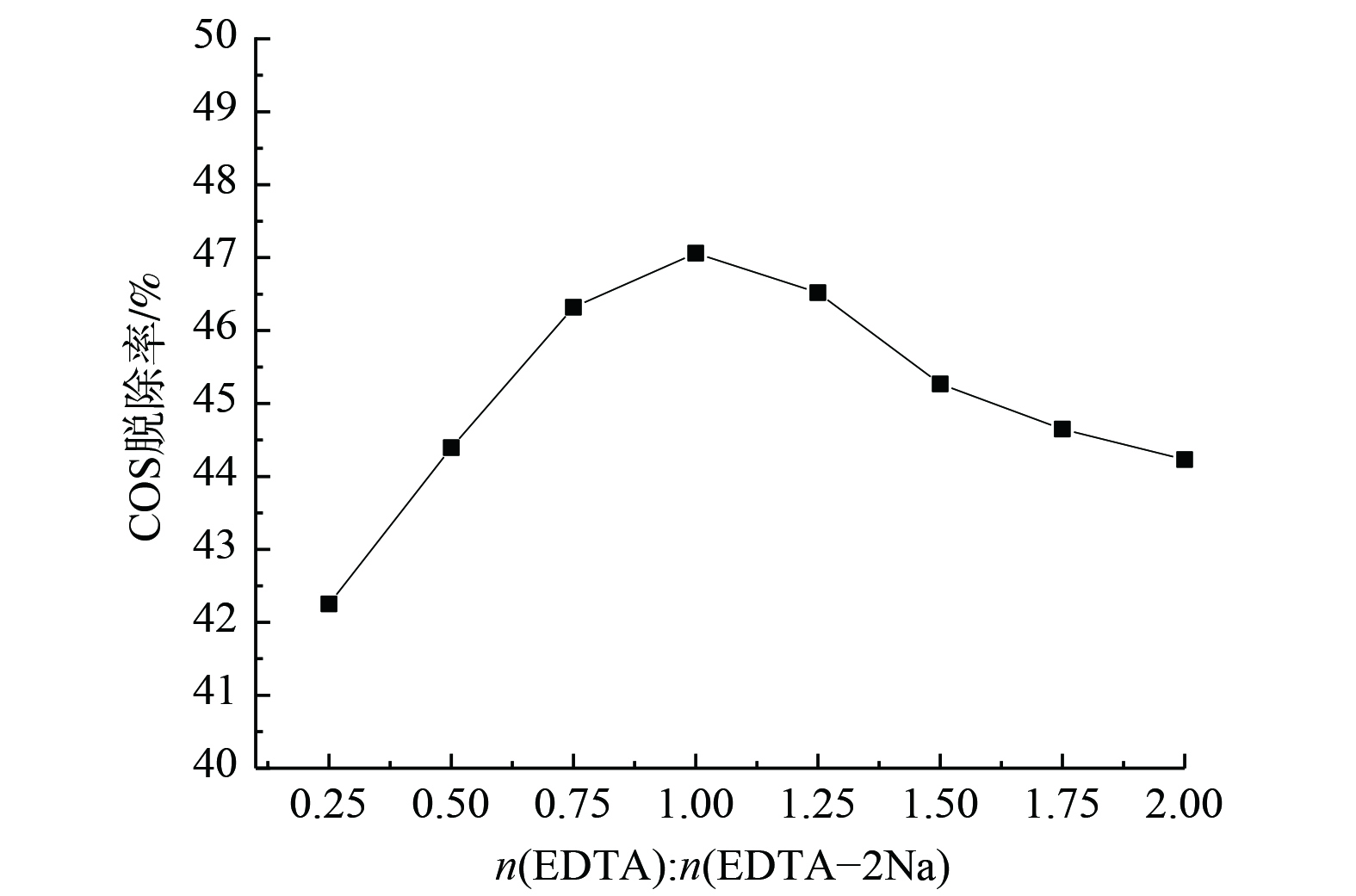
当吸收剂中Na2CO3与(EDTA+EDTA-2Na)质量分数均为5%时,EDTA与EDTA-2Na的不同配比对COS脱除效率的影响如图3所示。随着两者比值的增加,COS脱除效率呈先增大后减小的趋势。只有当比值接近等物质的量时,脱硫效率方可达到最佳。这是由于EDTA、EDTA-2Na在溶解后会形成酸碱共轭体系,其反应机理为:在溶液中EDTA与Na2CO3反应生成EDTA-2Na,碱性介质促进了COS更大程度地水解生成H2S。而加入EDTA溶液还可提高通气时硫化氢溶液的稳定性,之后由于EDTA酸性介于碳酸和氢硫酸之间,EDTA-2Na与已吸收的H2S(以氢硫酸形式存在)反应,同时EDTA得以再生[12-13]。因此,只有当EDTA与EDTA-2Na物质的量之比为1时,二者才能起到协同作用以增强液相中碳酸钠对COS的去除效果。
-
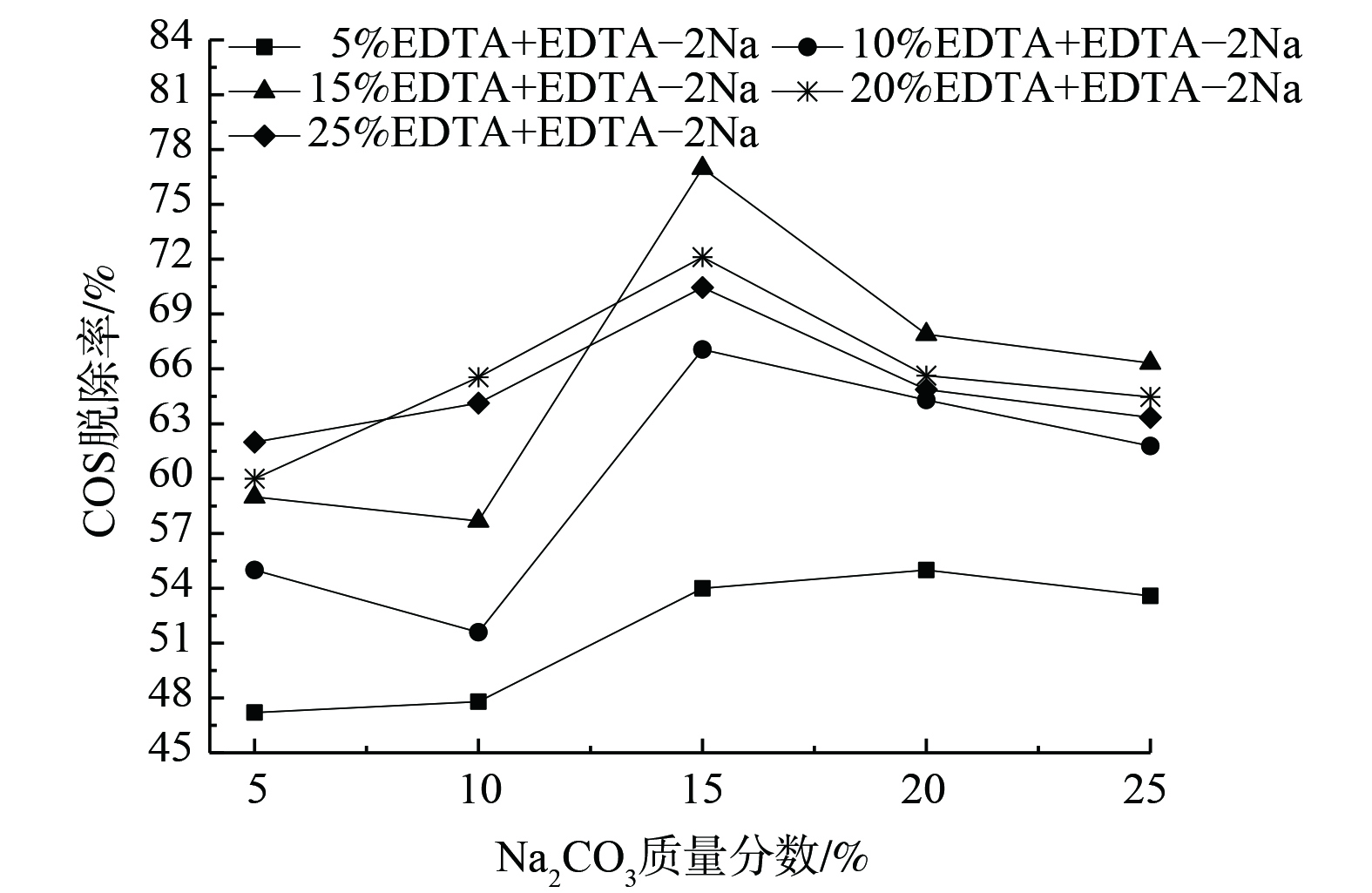
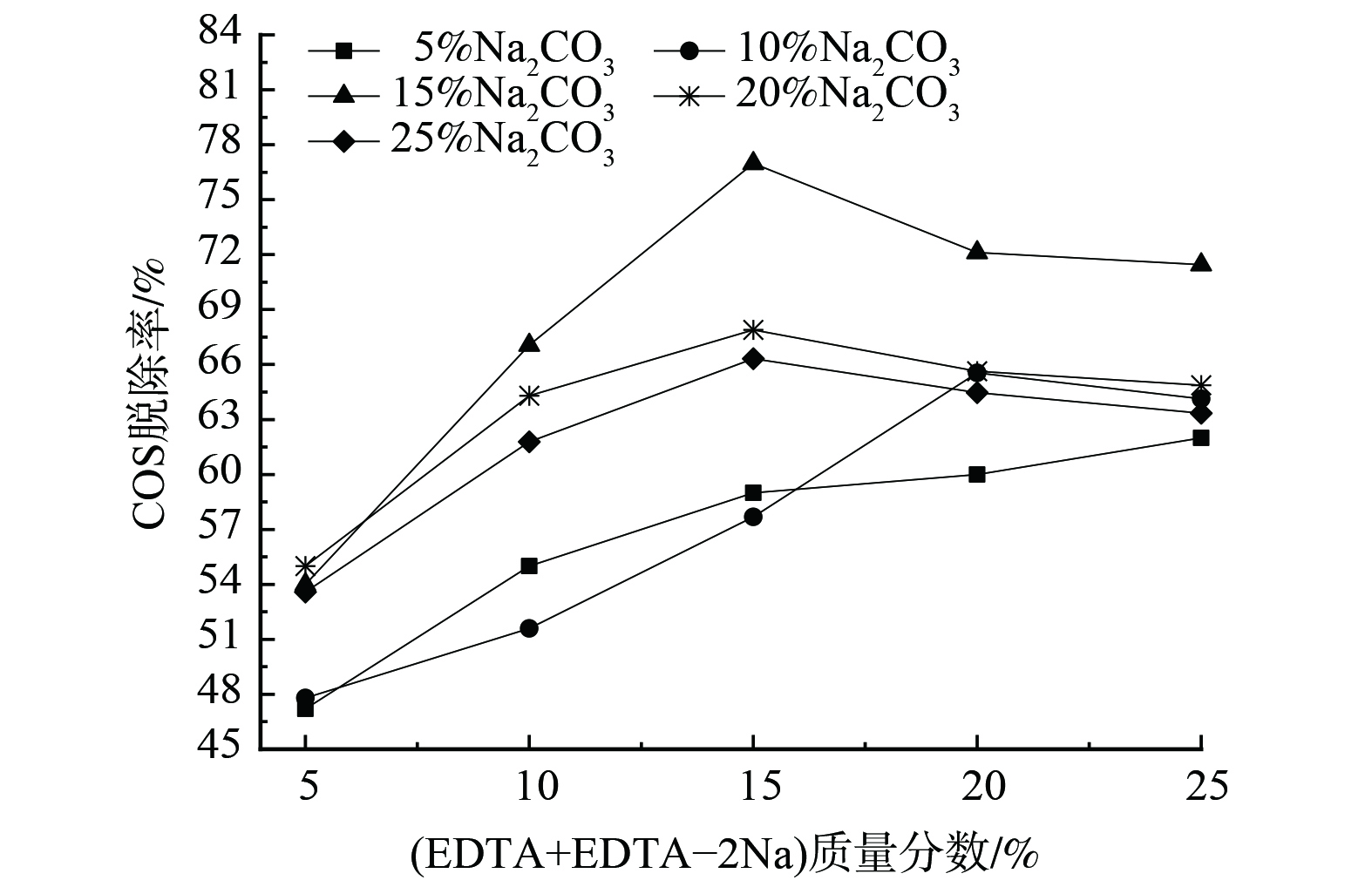
当n(EDTA):n(EDTA-2Na)=1:1时,调整吸收剂中Na2CO3或(EDTA+EDTA-2Na)的质量分数,其脱硫性能如图4和图5所示。
图4表明,随着Na2CO3质量分数的增加,COS脱除效率呈先增加后减少趋势。在15% Na2CO3处达到最佳,为76.98%,且EDTA+EDTA-2Na质量分数越大越有利于复配吸收剂对COS的脱除。Na2CO3质量分数的增加可有效增加COS在吸收剂中的溶解度,使得催化作用增强,COS的水解速率升高。但加入过多Na2CO3时,水解生成的H2S会同时与Na2CO3反应生成NaHS。在长时间运行后,NaHS在碱液中积累会导致脱硫黏度增大。并且,煤气中的CO2会与Na2CO3反应,生成NaHCO3等副产物,从而造成脱硫液物理性质的改变并增加碱耗[14]。
图5表明,复配吸收剂中EDTA+EDTA-2Na质量分数为5%~15%。COS脱除率逐渐增加,并在15%(EDTA+EDTA-2Na)处达到最佳。当其增至20%、25%时,其脱硫效率反而降低,但降幅变缓;且Na2CO3浓度越高,COS脱除效率越好。EDTA和EDTA-2Na的加入增强了液相碳酸钠吸收COS的活性,提高了对煤气中COS的吸收率。然而,EDTA+EDTA-2Na含量的增加使复配溶液的黏度增大,不利于气液传质过程,从而导致脱硫效率降低[15]。综上所述,复合吸收液的最佳配比为15% Na2CO3+15%(EDTA+EDTA-2Na)。
-
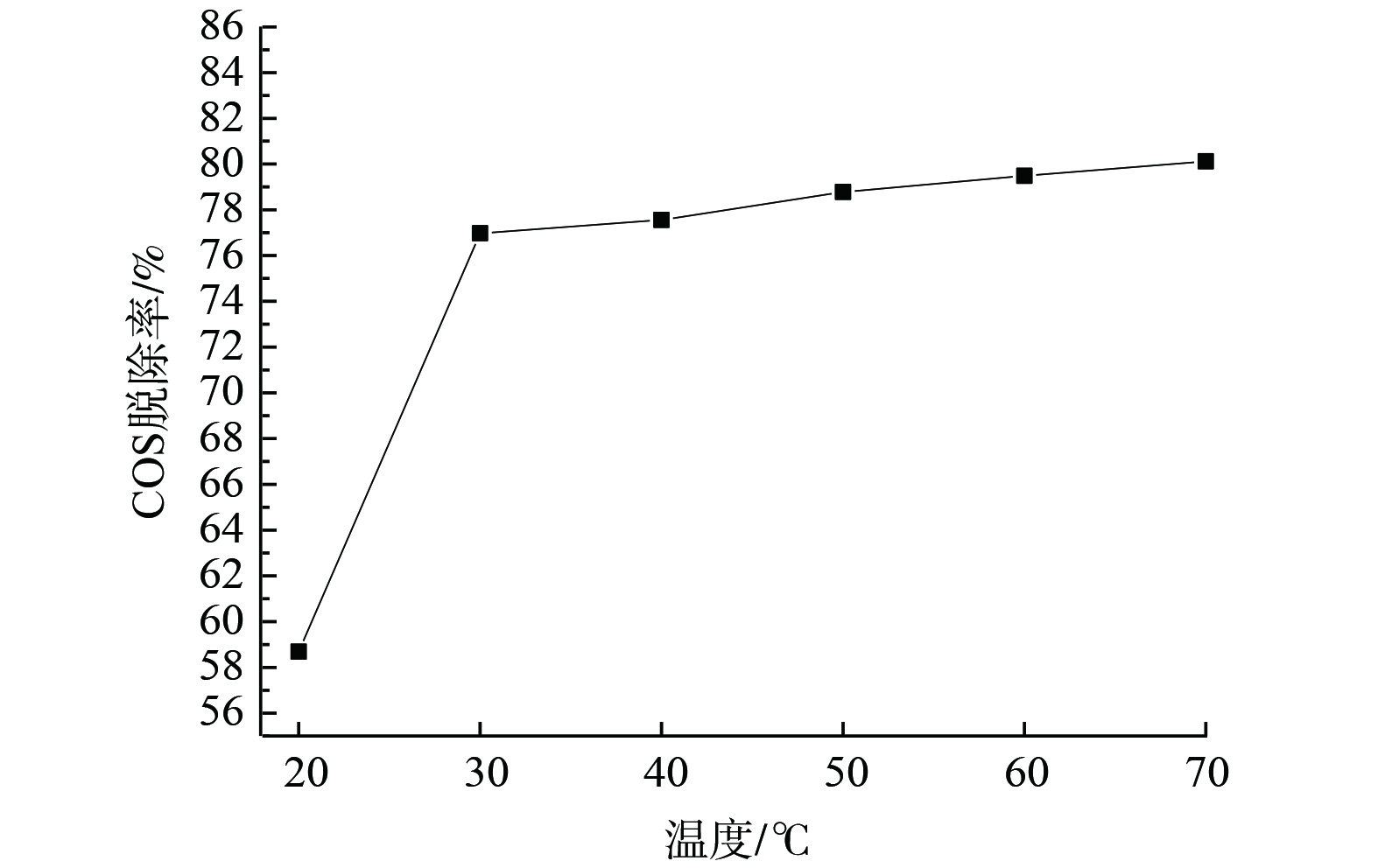
在反应时间30 min、空塔气速0.25 cm·s−1工作电压3 V及电流密度2.5 A·mm−2的实验条件下,复合吸收剂配比为15%Na2CO3+15%(EDTA+EDTA-2Na)(n(EDTA)∶n(EDTA-2Na)=1∶1)时,改变温度,系统脱硫性能变化如图6所示。当吸收液温度由20 ℃升至30 ℃,其COS脱除效率从58.69%升至76.98%,提升了18.29%。当吸收液温度增至30 ℃后,其脱除效率基本保持平稳。温度升高、吸收液黏度降低有利于气体在吸收液中的传质扩散,从而促使C==S键发生水解氢化反应[15-16];另外,升高吸收液温度,阳极电极电势的数值会降低,使得溶液中通过电量增大、电解溶液中的液相电阻值减小,这不仅增大了液相传质的作用,还补偿了因反应物浓度降低而引起的浓度极化,且有利于电化学氧化过程中活性离子的生成,故更易发生氧化反应,最终提高了COS的脱除性能。然而,高炉煤气中的硫化物与配方吸收剂中的活性组分反应为放热反应,因此,当温度升至一定程度后,反应开始朝着不利于吸收的方向进行并导致了脱硫效率增幅变缓。
-
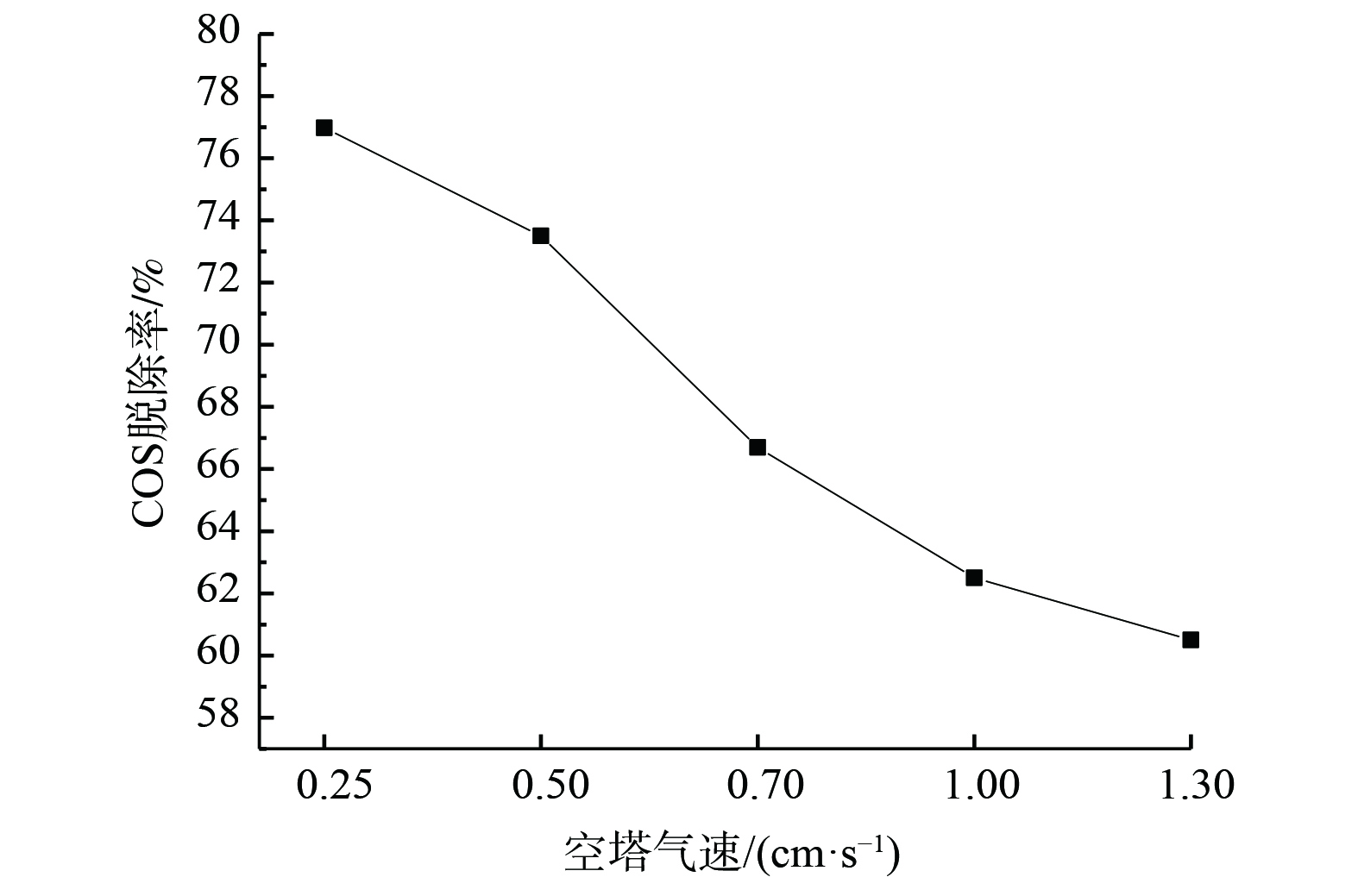
在反应时间30 min、温度30 ℃、工作电压3 V及电流密度2.5 A·mm−2的实验条件下,复合吸收剂配比为15%Na2CO3+15%(EDTA+EDTA-2Na)(n(EDTA)∶n(EDTA-2Na)=1∶1)时,改变空塔气速,其脱硫性能变化如图7所示。空塔气速与脱除效率呈反比关系。当空塔气速0.25 cm·s−1时,效率达到76.98%。然而,随着空塔气速的增大,系统脱硫效率不断降低。在原料气组分不变的前提下,增大气速意味着增大了溶剂酸气负荷,从而导致溶剂中有效活性组分浓度降低、气液接触时间缩短[17-18],并使吸收推动力减弱、较多COS未反应排出,最终脱硫效果变差。
-
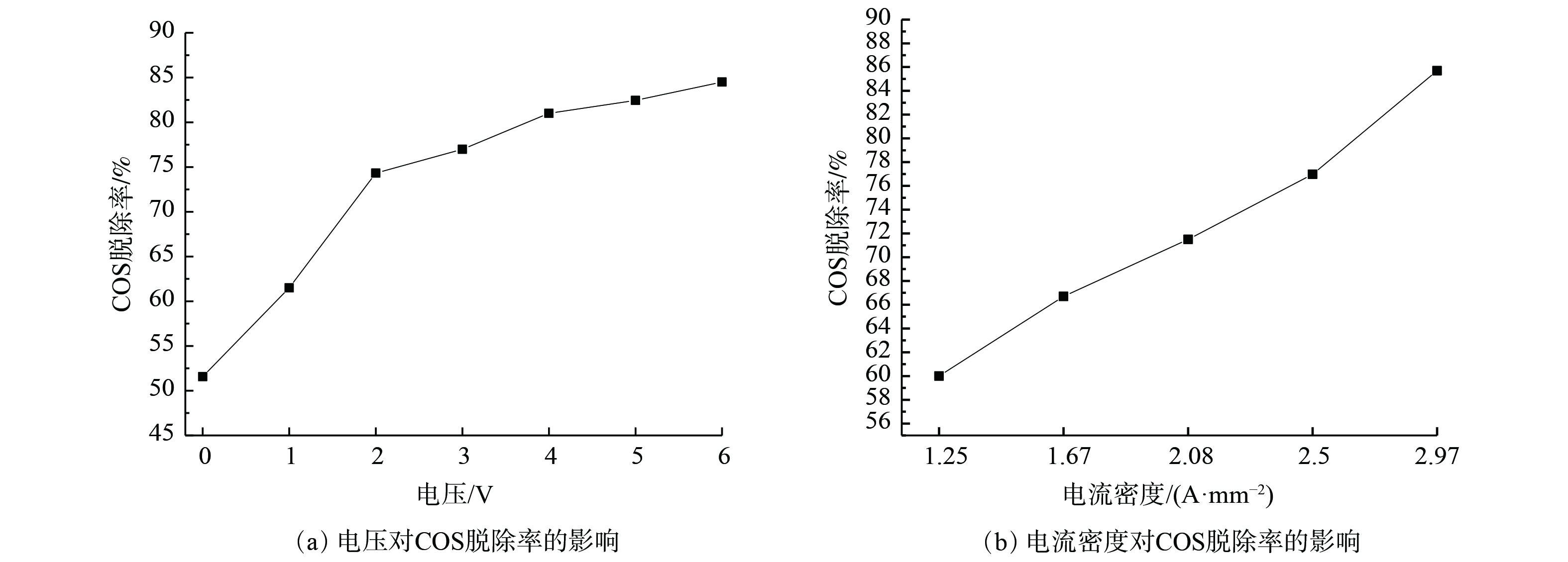
在反应时间30 min、温度30 ℃、空塔气速0.25 cm·s−1实验条件下,复合吸收剂配比为15%Na2CO3+15%(EDTA+EDTA-2Na)(n(EDTA)∶n(EDTA-2Na)=1∶1)时,调整工作电压及电流密度,其脱硫性能变化如图8所示。
图8(a)表明,当电压为0时,脱除效率为51.18%。随着电压增大至6 V,脱硫效率增至84.20%。这表明与零电压情况相比,施加工作电压使脱硫率提高了约1.6倍;工作电压升高,则在单位时间内注入反应器的能量增加,促进了活性氧的生成,并增强了电极的反应能力,故有利于提高硫化物的氧化程度,使得脱硫效率逐步提高[19-20]。当电压增至6 V时,反应过程消耗电功率0.35 W。考虑资源、能量消耗因素,故选工作电压3 V为宜。图8(b)表明,COS的脱除效率随电流密度增加呈上升趋势。在电流密度增大过程中,电解溶液中的电化学反应加剧,在电极表面发生的电化学反应速度增大,使得在一定时间内脱硫率逐步增大[21-23]。电催化反应电位随所设电流的提高而逐渐增大。当电流密度大于2.5 A·mm−2时,电解电压大于3 V,使得反应所需电功率增加。因此,仅通过增加电流密度的方式提高对COS脱除效率并无实际意义,工作电流密度以2.5 A·mm−2为宜。
-
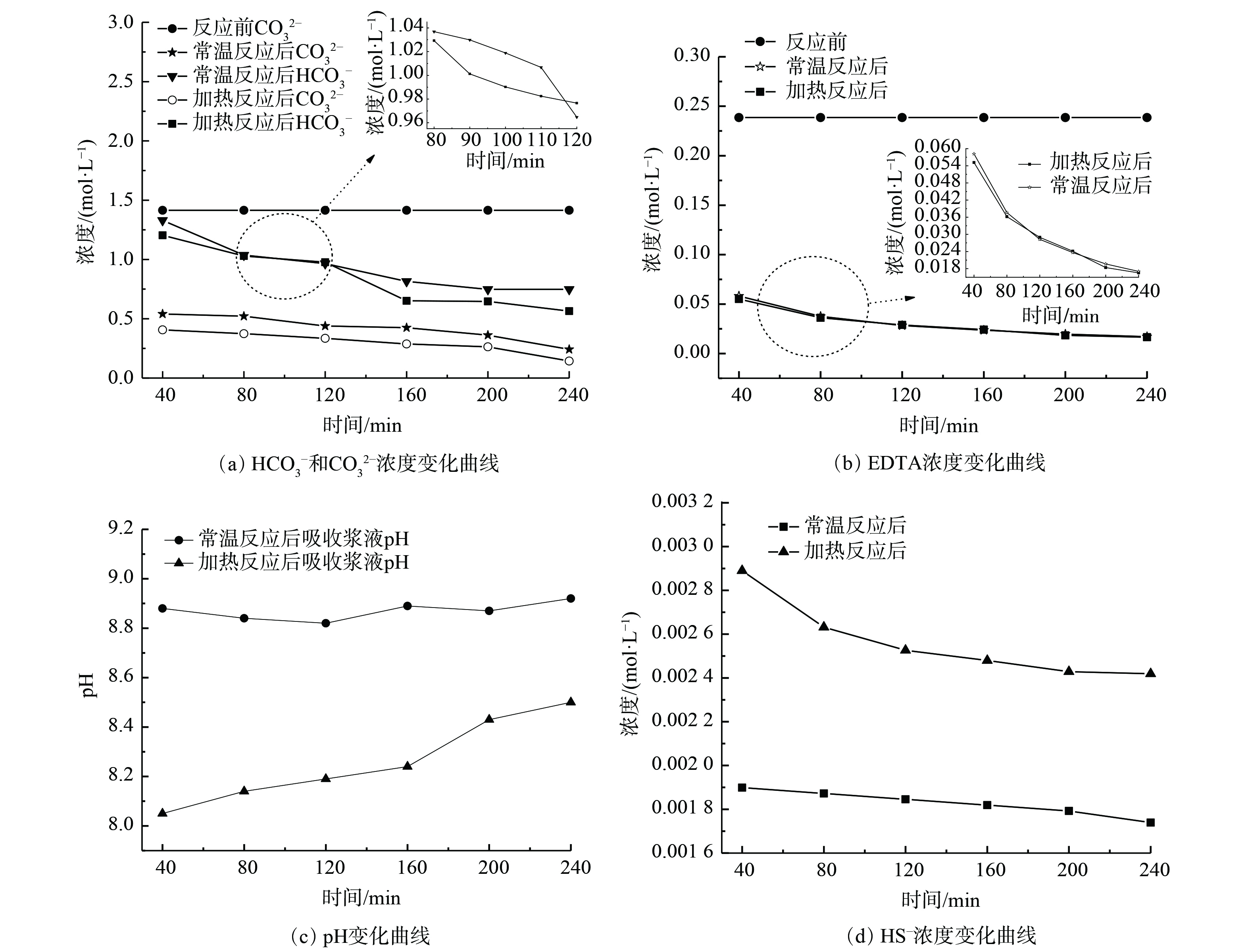
为进一步研究电化学脱硫反应的作用机理,在进口COS质量浓度为280 mg·m−3、空塔气速0.25 cm·s−1、工作电压3 V的工况下,复合吸收剂配比为15% Na2CO3+15%(EDTA+EDTA-2Na)(n(EDTA)∶n(EDTA-2Na)=1∶1)时,分析反应温度为常温20 ℃与加热至30 ℃时脱硫液反应前后产物的离子成分及浓度变化规律,结果如图9所示。
图9(a)表明,
CO2−3、HCO−3 浓度随时间递增逐渐减少,且在加热情况下吸收剂中HCO−3、CO2−3 浓度较常温更低。这说明Na2CO3与EDTA的反应导致了CO2−3、HCO−3 浓度降低。图9(b)表明,吸收剂脱除COS会消耗EDTA。随着反应进行,EDTA减少,且浓度降幅平缓。这说明EDTA与EDTA-2Na按照物质的量1∶1添加可形成酸碱共轭体系,并发生Na2CO3与EDTA间的反应生成了EDTA-2Na;之后EDTA-2Na与H2S反应生成Na2S和NaHS,同时EDTA得以再生,故在反应时间段内其浓度减幅平缓。图9(c)表明,反应消耗Na2CO3,且加热条件下比常温消耗碱多,故加热反应后pH较平常低。然而,随着反应的推进,在加热情况下CO2−3 水解程度深、碱性增强,且pH增加较快。这说明脱硫反应可保持在碱性介质中进行。图9(d)表明,随着反应时间延长,由于吸收剂中碱性物质消耗较多,COS的水解和氧化程度减弱,HS− 浓度逐渐降低。然而,加热条件下的电化学协同作用较常温情况下更强,生成的高活性自由基会促进COS的水解和氧化,更利于脱硫液对COS的吸收,且生成的H2S以HS− 形式存在于吸收剂中,故在加热情况下吸收剂中HS− 浓度更高。 -
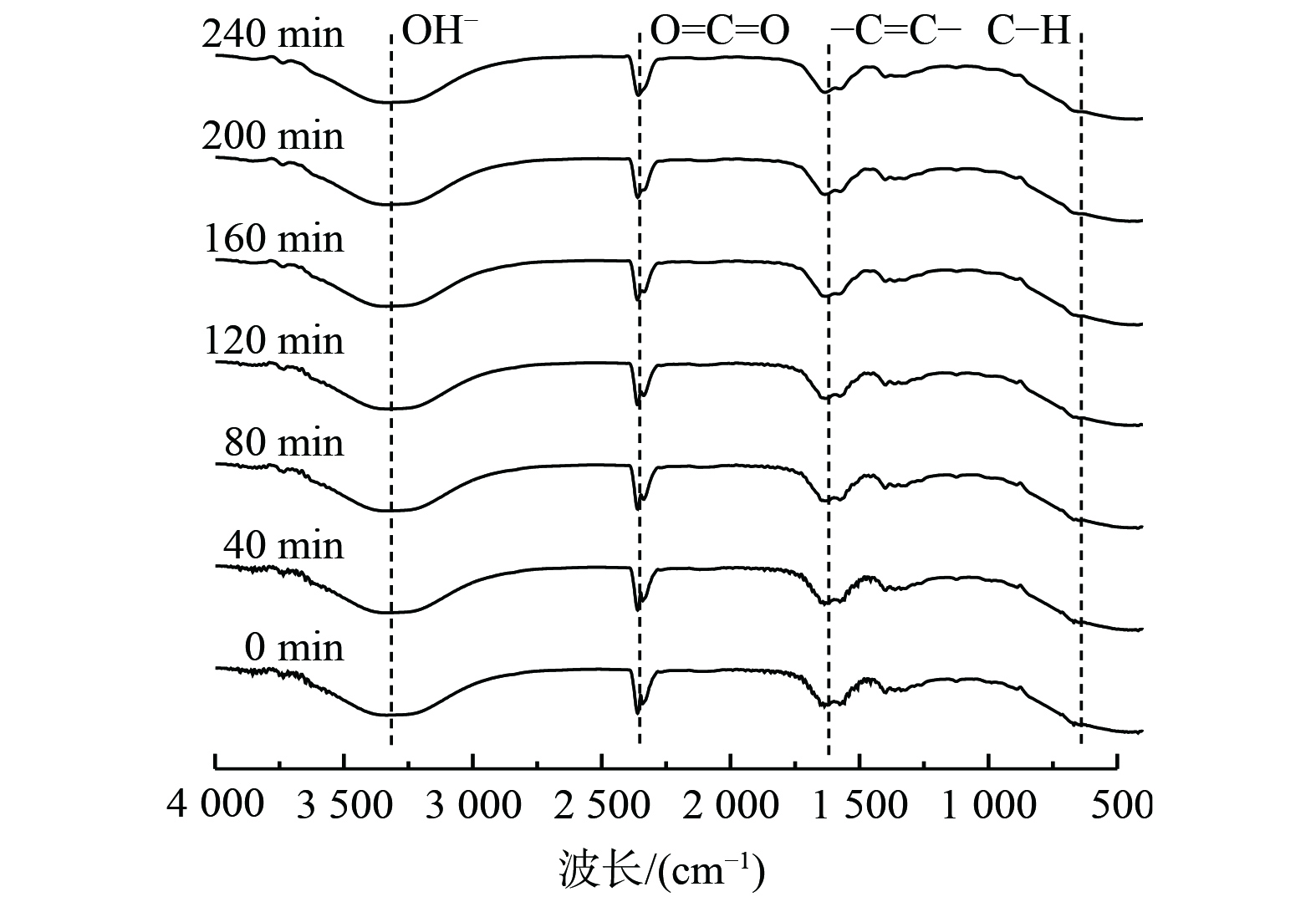
采用红外光谱检测方法,对0~240 min反应过程前后的脱硫液进行分析,结果如图10所示。反应前后脱硫液的红外特征峰的吸光度大小、位置、面积一致,无新峰。这表明脱硫溶液在脱硫前后有较好的稳定性。在3 750~3 000 cm−1附近出现O—H伸缩振动区。这表明阴阳极柱附近反应生成大量
OH− 。在碱性介质中,阳极OH− 表面首先失去大量电荷,短暂形成高活性的自由基⋅OH ,与COS发生断键反应[24]。 -
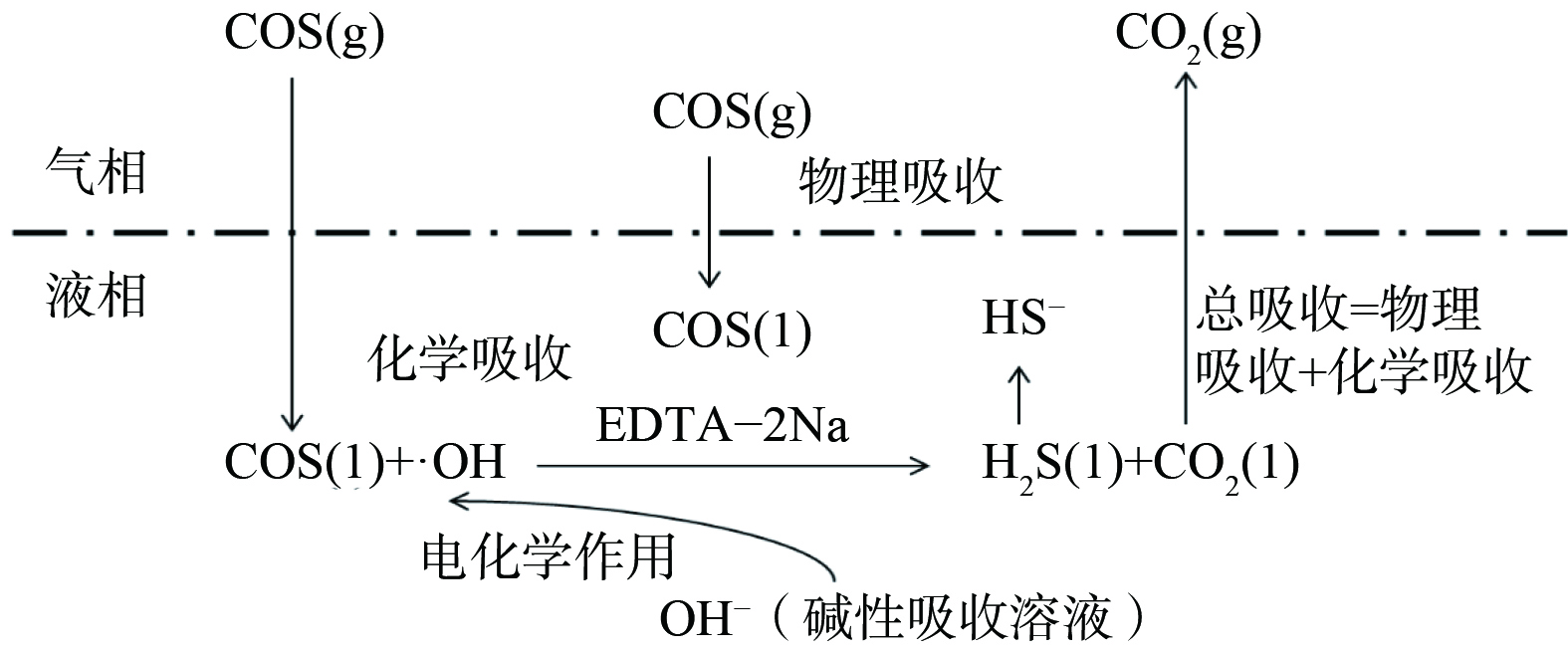
图11表明,整个脱硫过程包括混合溶液对COS的吸收和转化。气相中的COS通过脱硫液物理吸收作用进入液相后,在电催化作用的碱性介质中下,与水发生水解反应生成CO2和H2S。当CO2进入气相后,H2S以
HS− 离子和少量分子的形式存在与液相中。通过2.6和2.7分析可得脱硫过程的反应式为式(1)~式(4)。
-
1)在反应温度30 ℃、空塔气速0.25 cm·s−1、工作电压3 V及电流密度2.5 A·mm−2条件下,配比为15%Na2CO3+15% (EDTA+EDTA-2Na)(n (EDTA): n (EDTA-2Na)=1:1)的复合脱硫剂具有较好的电化学协同脱硫性能。在该实验条件下,其COS脱除效率可达76.98%。同时,等物质量的EDTA和EDTA-2Na在溶解后形成酸碱共轭体系,能增强液相碳酸钠吸收COS的活性,进而提高COS的脱除率。
2)在Na2CO3、EDTA和EDTA-2Na三者共同作用下,COS在复合吸收剂中被催化水解为
HS−和HCO−3 ,有效避免了副产物的产生,且溶剂具有良好稳定性,有一定应用前景。3)复合吸收剂借助电催化电极材料的催化活性,利用吸收液碱性环境,在电极柱附近产生具有更高氧化能力的活性氧(如
⋅OH、O⋅ 等),可促进COS催化转化,并提高了COS的脱除效率。
高炉煤气电化学协同湿法精脱硫复合吸收剂Na2CO3+EDTA+EDTA-2Na的脱除效果及工艺条件
Removal effect and process conditions of composite absorbent Na2CO3+EDTA+EDTA-2Na for wet desulfurization of blast furnace gas by electrochemical synergistic method
-
摘要: 针对钢铁行业全流程超低排放改造要求,结合当前高炉煤气精脱硫技术不成熟、需求迫切的现状,提出了电化学催化氧化协同增效湿法吸收精脱硫方法,考察了Na2CO3+EDTA+EDTA-2Na复合吸收剂脱除羰基硫(COS)的性能,对其工艺条件进行了优化。通过对脱硫产物及反应前后脱硫液进行表征检测,分析了电化学协同湿法吸收脱硫机制。结果表明:在反应温度30 ℃、空塔气速0.25 cm·s−1、工作电压3 V及电流密度2.5 A·mm−2的条件下,配比为15%Na2CO3+15%(EDTA+ EDTA-2Na)、(n (EDTA)∶ n (EDTA-2Na)=1∶1)的复合吸收剂的COS脱除效率可达76.98%;复合吸收剂通过电化学催化协同吸收COS,不仅可有效避免副产物产生,且溶剂具有良好的稳定性和可行性。本研究提出的高炉煤气电化学协同湿法精脱硫技术可为钢铁行业开展全流程超低排放改造提供参考。Abstract: In response to the ultra-low emission transformation requirements of the entire process of the steel industry, combined with the current immature and urgent needs of blast furnace gas fine desulfurization technology, this paper proposed an electrochemical catalytic oxidation assisted synergistic wet absorption fine desulfurization method, and investigated the performance of the composite absorbent (Na2CO3+EDTA+EDTA-2Na) to remove carbonyl sulfide (COS), and optimized its process conditions. And the electrochemical cooperative wet absorption desulfurization mechanism was analyzed by characterizing the desulfurization product and the desulfurization solution before and after the reaction. The results showed that the removal rate of COS in desulfurization liquid with a ratio of 15%Na2CO3+15% EDTA and EDTA-2Na (n(EDTA): n(EDTA-2Na)=1:1) could reach 76.98%, when the reaction temperature was 30 ℃, the empty tower flow rate of 0.25 cm·s−1, the working voltage was 3 V and the current density was 2.5 A·mm−2. The composite absorbent synergistically absorbed COS through electrochemical catalysis, in which the production of by-products could be effectively avoided, and the solvent also possessed good stability and feasibility. It can provide a reference for the optimization of the electrochemical synergistic wet fine desulfurization technology of blast furnace gas.
-
Key words:
- blast furnace gas /
- carbon oxide sulfide(COS) /
- EDTA /
- wet desulfurization /
- electrochemistry
-
我国是印染大国,纺织印染行业是我国的支柱产业之一。2016年,我国规模以上印染企业印染布产量9.7×1010 m[1],在环保压力提升的背景下,中小企业因环保压力被动停产或寻求兼并,印染行业的区域集中度逐渐提高。我国印染行业主要集中在东部沿海地区,截至2015年,浙江地区已经汇集了全国接近63%的印染行业产能[2]。印染行业在带来巨大经济利益的同时,也带来了非常严重的环境污染问题[3],尤其是VOCs的污染问题。印染行业作为纺织行业的关键行业,生产过程中需要使用大量挥发性助剂,目前我国印染助剂年使用量为1.2×105 t[4],助剂的大量使用导致了严重的VOCs污染,2012年,长江三角洲区域纺织印染行业VOCs总排放量达到7.5×104 t[5]。VOCs与PM2.5的形成有密切关系,也是光化学烟雾的源头,如果未经治理的印染废气大量排放,会直接影响大气环境,部分有毒VOCs长期累积排放会直接影响企业职工的身体健康,容易造成职工的呼吸道疾病,甚至发生癌变,还会影响周边居民的生活质量[6],印染行业的VOCs排放问题也因此获得重点关注。我国于2015年推出了《纺织染整工业大气污染物排放标准》[7],其中关于VOCs的各项标准相比于之前沿用的《大气污染物综合排放标准》[8]和《恶臭污染物排放标准》[9]更加严格。目前,我国缺乏印染废气尤其是VOCs的产生特征及去除特性研究,这增加了印染废气的处理难度,因此,研究印染行业VOCs产生特征是十分必要的。本研究以浙江省内一家典型的印染企业为研究对象,着重对该企业内3个分厂进行废气监测,以了解其VOCs的产生特征,为进一步了解印染VOCs产生特征以及提高印染废气治理效果提供参考,为解决印染VOCs污染提供技术支持。
1. 采样与分析方法
1.1 调研企业概况
本研究选取了浙江省印染企业高度集聚区的一家典型印染企业。该企业每年印染布产量达7.8×107 m,每年印染布产量为2.5×104 t。本研究对该企业3个印染分厂(产品分别为针织布、梭织布以及化纤涤纶布,编号为A分厂、B分厂、C分厂)及印染污水站进行VOCs产生特征的探究。有组织废气源主要包括定型机、配料间及污水站。该企业对A分厂和B分厂定型机废气采用“间接冷却+静电除尘”装置进行治理,对C分厂定型机废气采用“水喷淋+静电除尘”装置进行废气治理,对各分厂配料间废气及污水站废气采用“次氯酸钠洗涤+碱洗”二级喷淋装置进行治理。
1.2 采样及测定点位
印染行业的工艺流程主要包括胚布准备、前处理、后整理和成品4个阶段,各个印染企业使用的工序及原料会有所不同,但是整体工艺流程[10]相似。
该企业各废气源如图1所示。该企业共有45台定型机,定型机废气主要来自胚布表面溶剂的受热挥发[11];配料间包括配料车间和染料仓库,配料间产生的废气主要是来自于配料过程中助剂染料的挥发,也包括染料仓库中存放的助剂及染料的自然挥发;该企业污水站恶臭气体的主要产生单元包括调节池、水解酸化池及污泥浓缩池,所产生的废气经负压管道收集后经过处理直接排放。故选择以上3个有组织废气源作为废气监测点。经过现场调研了解到,印染企业中无组织废气主要来自设备运行以及配料间的配料过程,所以选取染色定型车间以及定型车间进行无组织废气特征测定。同时,污水站内未封闭的处理单元也会产生一定的无组织废气,故污水站无组织废气测定点选择好氧池、厌氧池、初沉池。在无组织废气测定过程中,车间内依据印染设备不同距离各取3个点位进行测定,对污水站各处理单元附近上下风向各取3个点位进行测定。针对该企业各分厂的废气处理装置,测定点位选取在各废气装置的进出气口,监测指标为VOCs浓度及H2S浓度。
1.3 分析方法
废气测定指标包括温度、湿度、流量、VOCs浓度、VOCs组分。其中温度采用Testo 905-T1-温度计测量。湿度采用Testo 605-H1-温湿度仪测量。废气流量通过废气气速与废气排风管横截面积计算,流速使用Testo 416 -精密型叶轮风速仪进行测量。VOCs浓度采用PhoCheck Tiger VOC检测仪进行现场测定。VOCs采样方法采用固相微萃取采样(SPME),采样点设在各测定点尾气收集管道内,将SPME萃取头伸入废气管道内部,吸附采样时间为10 min。VOCs组分测定采用国家标准方法(HJ 73-4-2014),即“SPME+气相色谱质谱联用仪(GC-MS)”检测方法[12]。采用安捷伦气相色谱/质谱联用仪,将SPME萃取头插入进样口,吸附在萃取头上的VOCs物质随着高纯氦气(纯度99.999%)进入HP-5ms色谱柱(30 m×0.25 mm×1 μm,Agilent Technologies,美国)中进行分离。气体经分离后进入ECD检测器、FID检测器、质谱监测仪,依据各物质停留时间以及峰面积,对VOCs组分进行定性半定量分析。针对废气处理装置增加了进出气H2S浓度指标的测定,采用HND88式便携式H2S检测仪进行检测分析。
2. 结果与讨论
2.1 废气温度、湿度、产生量及VOCs浓度
由于染色和漂洗过的纺织品需要在定型机内进行烘干拉幅和热处理[13],同时纺织品上携带的水分受热大量蒸发,所以定型机所产生的废气平均温度和湿度较高,平均温度为135 ℃,相对湿度已饱和;配料间内无加热装置,产生废气的温度为24 ℃,与室温相近,废气湿度随配料间配料时间的改变而变化;污水站废气温度约为26 ℃,湿度为60%~70%。
该企业各有组织废气的废气特征如表1所示,定型机、配料间及污水站产生的有组织废气流量分别为8.6×105、7.4×104、2.8×104 m3·h−1,产生的VOCs平均浓度分别为14.7、9.0和14.9 mg·m−3。《纺织染整工业大气污染物排放标准》对VOCs限值为40 mg·m−3,《大气污染物综合排放标准》对非甲烷总烃的限值为120 mg·m−3,排放速率限值为15 kg·h−1,各废气源的VOCs浓度均满足排放标准的要求。
表 1 各有组织废气源废气特征Table 1. Characteristics of organized exhaust gas from different sources废气源 分厂 废气产生量/(104 m3·h−1) VOCs浓度/(mg·m−3) 总气源数量/个 总废气产生量/(×104 m3·h−1) 总VOCs产生速率/(kg·h−1) 定型机 A 1.9±0.3 14.5±0.6 45 86.9±9.9 12.8±1.6 定型机 B 1.7±0.2 15.7±0.5 定型机 C 2.0±0.2 14.1±0.9 配料间 B 1.8±0.4 8.8±0.1 5 7.4±2.9 6.57±0.31 配料间 C 1.3±0.4 9±0.2 污水站 — 2.8±0.2 14.9±0.7 1 2.8±1.5 4.13±0.6 由于该印染企业配料间及污水站废气产生量较低,且配料间为非连续运行模式,每天工作时间不定,平均为3 h,所以印染企业生产过程中,定型机是最大的VOCs产生源。通过调研了解到,企业每年运行约300 d,定型机和污水站每天运行约20 h,配料间每天工作约3 h,由此计算得该企业每年定型机总VOCs产生量约为76.8 t,配料间VOCs年产生量约为0.6 t,污水站VOCs年产生量为2.5 t,企业每年VOCs产生总量约为79.9 t,印染过程中VOCs产生量约为31.9 kg·t−1 (产品)。
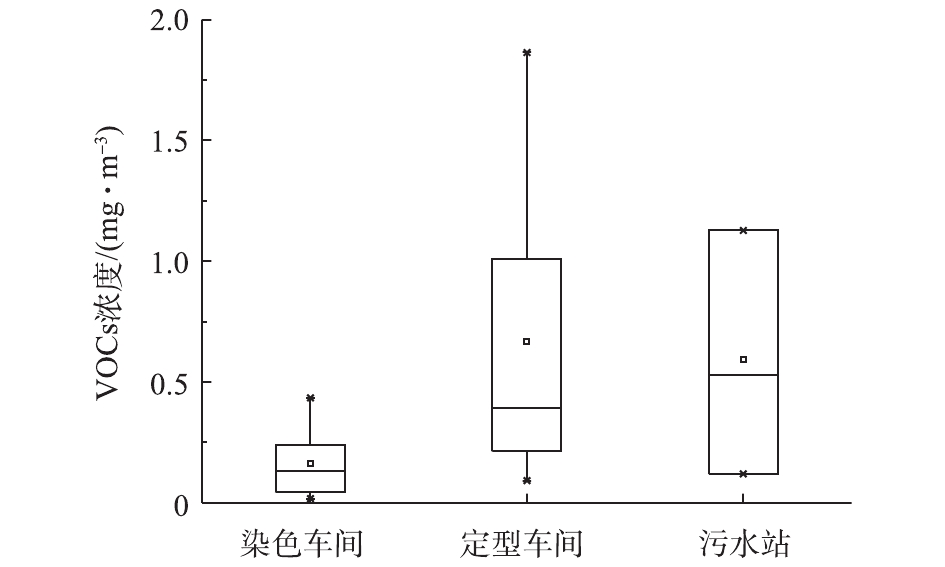
各无组织废气源的VOCs浓度如图2所示。染色车间VOCs平均浓度在0.16 mg·m−3左右。相比染色车间,定型车间内的VOCs浓度要高得多,浓度为0.1~1.9 mg·m−3,平均浓度约为0.66 mg·m−3,污水站的VOCs浓度为0.1~1.1 mg·m−3,平均浓度约为0.59 mg·m−3。定型车间和污水站产生无组织VOCs浓度具有区域性,不同测定点VOCs浓度差异较大。
2.2 各有组织废气源的VOCs组分特征
2.2.1 定型机产生的VOCs组分特征
在热定型过程中,纤维布料上残留的有机物受热挥发,产生大量VOCs气体,VOCs气体组分易受到定型过程中助剂成分的影响。各分厂定型机VOCs组分如图3所示。A分厂定型机所产生的VOCs中氟代烃为主要物质,包括占比为22.7%的五氟丙酸三十八烷酯以及占比为23.3%的五氟丙酸三十烷酯。这是由于印染行业中经常会使用含氟的有机润滑剂(如氯化三氟乙烯、氟硅类、二酯、矿物油等物质),染色过程也会使用含氟的活性染料[14],其他VOCs还包括烷烃、异喹啉等。B分厂定型机的VOCs与A分厂定型机VOCs组分类似,同样是以卤代有机物为主,卤代有机物中的卤素为氯与氟,典型组分包括占比为12.2%的五氟丙酸三十八烷酯,以及占比为3.7%的三氯甲烷,其他VOCs组分包括乙二醇丁醚、二十一烷等物质,乙二醇醚类是印染过程常用的有机溶剂[15]。相关毒理学研究[16]表明,乙二醇醚类对人具有血液毒性、肝肾毒性等的不良影响。C分厂定型机废气VOCs检测出的成分以苯系物为主,VOCs中典型污染物为苯甲酸苄酯,约占为72%,苯甲酸苄酯主要用作乙酸纤维和硝酸纤维的溶剂,塑料增塑剂[17]。C分厂定型机VOCs的成分与A、B分厂有很大差异,主要原因为C分厂的加工产品为化纤布,在化纤布印染过程中会大量使用苯类助剂[18]。
2.2.2 配料间产生VOCs的组分特征
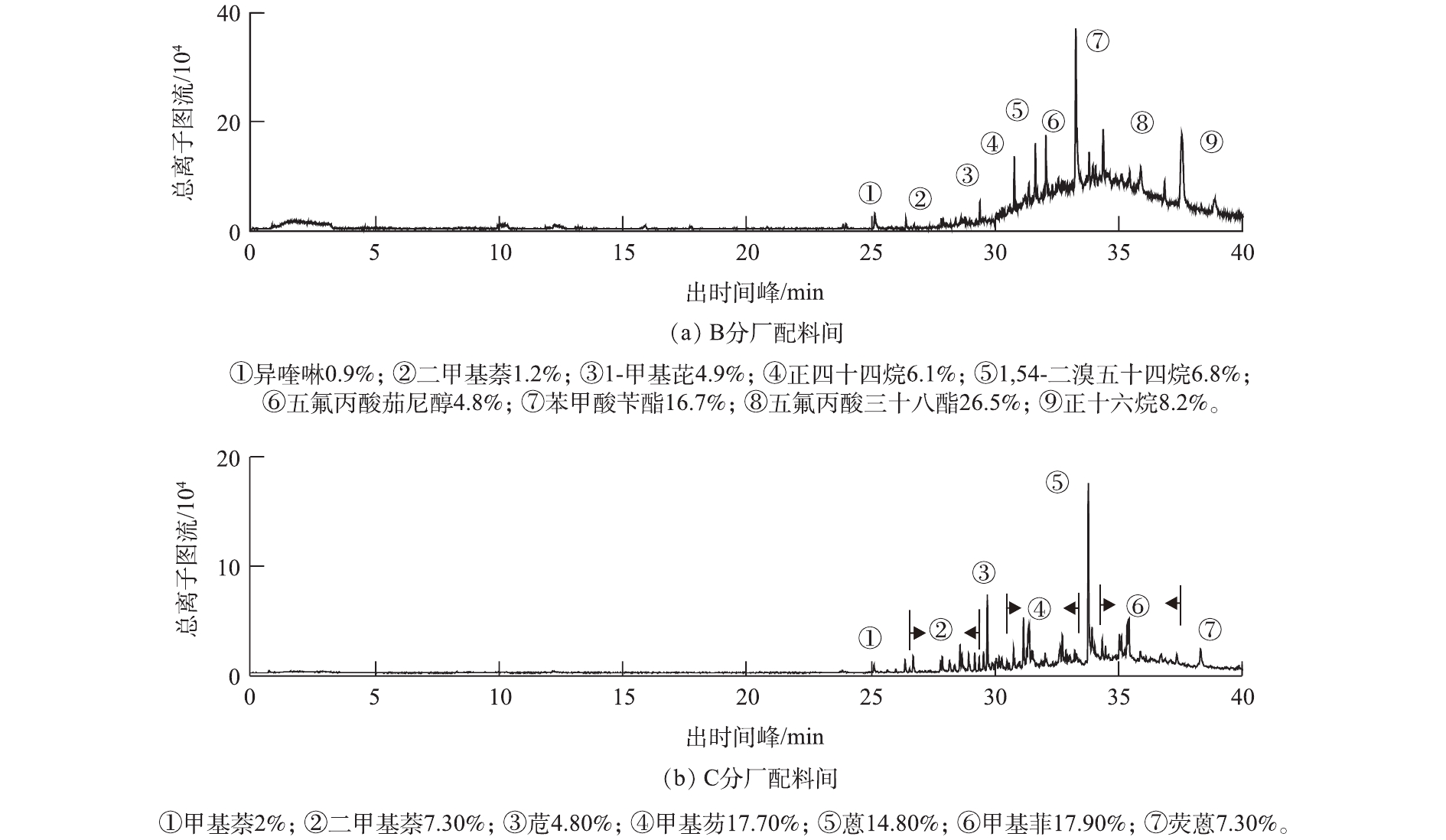
配料间所挥发出的VOCs组分取决于使用助剂的成分及挥发性,配料间非连续的工作时间及不同的配料方式也易对VOCs的组分产生影响,所以B分厂及C分厂的VOCs组分测定目的仅为确定印染配料间的典型VOCs组分,各分厂配料间组分如图4所示。B分厂配料间检测出的VOCs组分主要包括苯系物、卤代烃,VOCs组分与B分厂定型机测出的组分十分类似,如图4所示,VOCs主要包括含氟有机物、苯甲酸苄酯等物质。C分厂配料间所产生VOCs的组分十分复杂,VOCs主要为苯系物,主要成分包括蒽、甲基萘、甲基菲、甲基芴等。
印染企业配料间VOCs与定型机所产生VOCs组分类似,表明定型机所挥发出的VOCs组分受使用助剂种类影响较大,所以降低定型机产生的VOCs应该重点关注印染配料所使用的原料助剂的种类。
2.2.3 污水站产生VOCs的组分特征
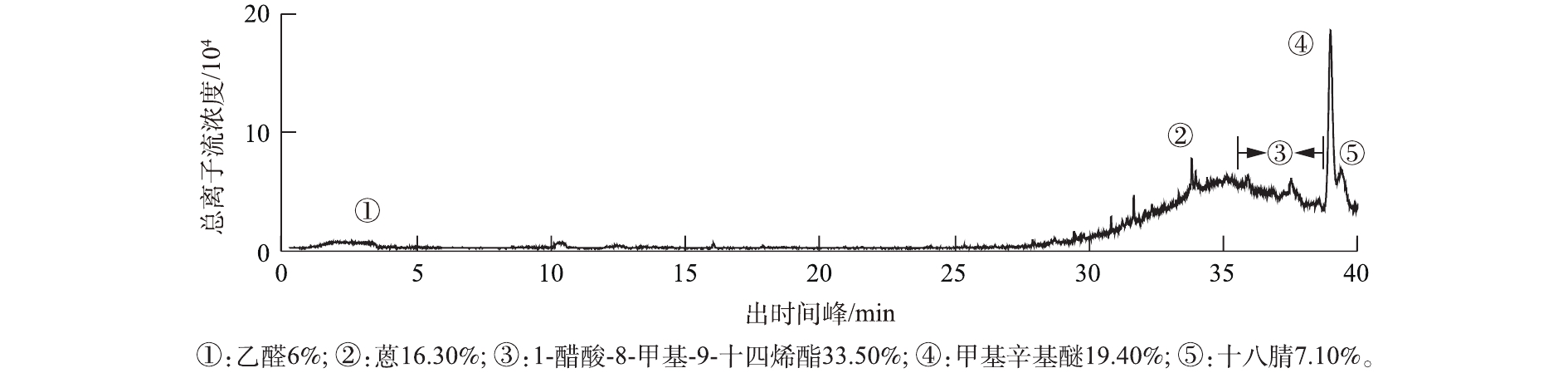
印染企业耗水量大,且其中含有高浓度的染料、印染助剂等有机物,污水处理过程中挥发出的VOCs组分也因为污水中的多种溶剂变得十分复杂[19],VOCs的成分特征如图5所示。印染污水处理过程所产生的VOCs包括蒽、乙醛、甲基辛基醚、十八腈等物质,甲基辛基醚占总VOCs比例为12%;其余VOCs包括1-醋酸-8-甲基-9-十四烯酯,占比为33.50%,蒽占比为16.30%。蒽类芳香族有机化合物同样也是印染污水中的主要污染物[20],十八腈常用作印染布料的表面活性剂[21]。
2.3 印染VOCs去除特性及处理技术分析
2.3.1 印染VOCs去除特性
该企业针对印染废气安装了“间接冷却+静电除尘”、“喷淋+静电除尘”和“次氯酸钠洗涤+碱洗”3类处理系统。根据卢滨等[22]对杭州市工业源VOCs治理设施的调研结果,在杭州市的纺织印染企业的废气治理设施中,“静电除尘”和“水/酸/碱吸收”占比分别为46.47%和20%。说明静电除尘及“水/酸/碱吸收”是印染企业常用的废气治理设施,对该企业各废气处理装置的测定结果具有一定的代表意义。各处理装置对VOCs的处理效果如图6所示。“间接冷却+静电除尘”装置对定型机的VOCs去除率仅为2%~6%,“水喷淋+静电除尘”装置对VOCs去除率为15%~40%,其中“水喷淋”阶段对VOCs去除率较高,去除率为13%~32%,水喷淋之后的静电除尘装置对VOCs去除率依然很低,表明印染企业增设的静电除尘装置对VOCs几乎没有去除能力。“次氯酸钠洗涤+碱洗二级喷淋”装置对VOCs具有一定的去除效果,但是各分厂配料间所挥发出的VOCs组分不同,喷淋装置对VOCs处理率差异较大,去除率为8%~58%。二级喷淋装置对污水站的H2S仅有57%的去除率。
2.3.2 印染废气治理技术分析
定型机产生废气气量较大,不仅含有油滴等颗粒物,也含有浓度较低的VOCs污染物,虽然静电除尘装置对定型废气中颗粒物的去除具有一定效果,但是该技术对VOCs去除效果较差。企业单台静电除尘装置投资费用为250万元,企业总静电除尘装置每日所耗电费约为1.5万元,且每套装置每天需停止运行0.5 h进行人工清洁,存在着能耗较大,维护成本较高等问题,定型机废气处理技术的提升方向应该重点关注这几方面的问题。
配料间为非连续废气源,废气产生量较小,VOCs浓度较低,“次氯酸钠+碱洗”二级喷淋塔投资较低,配料间所配置的喷淋塔投资为20万元,且二级喷淋塔运行灵活,适合配料间的废气治理。
污水站所产生的废气量较大,目前使用的二级喷淋塔对于大风量的废气处理,存在药剂量消耗大、产生大量废液的问题,该企业污水站的二级喷淋装置每天需要消耗20 kg次氯酸钠溶液,10 kg碱液。生物法已经在各行业污水厂废气治理领域得到广泛应用,对于印染企业污水站所产生的大风量、低浓度VOCs的废气,可以选择生物法作为印染污水厂的废气治理技术,生物法对印染污水站所产生的苯系物、酯、醚、H2S等物质去除效果较好[23],污水站的VOCs的产生特征符合生物法的应用条件。
3. 结论
1)定型机废气具有高温、高湿的物理特征,且定型机废气是印染废气的主要来源,该企业各废气定型机、配料间及污水站产生的有组织废气流量分别为8.6×105、7.4×104、2.8×104 m3·h−1,产生的VOCs平均浓度分别为14.7、9.0和14.9 mg·m−3。该企业每年总VOCs产生量可达79.8 t,经估算得,印染过程中VOCs产生量约为31.9 kg·t−1 (产品)。印染企业各车间无组织VOCs平均浓度较低,但是VOCs浓度分布具有区域性,需要对定型车间中VOCs浓度较高的区域增加相应的处理措施。因此,建议增大通风量,或者完善定型机废气收集系统。
2)印染行业VOCs成分复杂,且多为大分子物质,虽然不同分厂VOCs组分相差较大,但是各有组织废气源VOCs组分种类类似,VOCs中的苯系物主要包括苯甲酸苄酯、蒽类、喹啉类等,氟代有机物包括五氟丙酸酯及氯代有机物,印染VOCs主要来源于印染助剂的挥发。
3)印染企业各类废气处理装置对印染VOCs的去除效果差异较大,对于VOCs产生量最大的定型机,所采用的废气治理技术主体为静电除尘装置,静电除尘对印染VOCs去除率仅为2%~6%,说明印染企业针对定型机VOCs并未采取有效的控制措施,同时静电除尘装置存在着能耗大、维护成本高等问题。二级喷淋对配料间及污水站的VOCs去除率为8%~58%,对于印染污水站的VOCs治理,生物法是应用前景较好的技术。
-
表 1 实验气体中各组分的含量
Table 1. The content of each component in the experimental gas
H2 CO CO2 N2 O2 COS 1.99% 26.62% 11.77% 余 0.32% 280.0 mg·m−3 注:H2、CO、CO2、O2的百分数均为体积分数;体系载气为N2,故体系内除其他气体组分外,其余均为N2。 -
[1] 上官方钦, 干磊, 周继程, 等. 钢铁工业副产煤气资源化利用分析及案例[J]. 钢铁, 2019, 54(7): 114-120. doi: 10.13228/j.boyuan.issn0449-749x.20190034 [2] 郭玉华. 高炉煤气净化提质利用技术现状及未来发展趋势[J]. 钢铁研究学报, 2020, 32(7): 525-531. doi: 10.13228/j.boyuan.issn1001-0963.20190274 [3] 孙加亮, 杨伟明, 杜雄伟. 高炉煤气脱硫现状及技术路线分析[J]. 冶金动力, 2020(10): 13-18. doi: 10.13589/j.cnki.yjdl.2020.10.006 [4] 魏振浩. CODS溶剂脱除高炉煤气中有机硫性能考察[J]. 中国冶金, 2020, 30(10): 87-91. doi: 10.13228/j.boyuan.issn1006-9356.20200111 [5] 李均, 陈志炜. 高炉煤气精脱硫技术的研究与应用[N]. 世界金属导报, 2019-07-30(B06). [6] 张波, 薛庆斌, 牛得草, 等. 高炉煤气利用现状及节能减排新技术[J]. 炼铁, 2018, 37(2): 51-55. [7] 李翔, 王学谦, 李鹏飞, 等. 高炉煤气特征组分分析及其对脱硫过程的影响[J]. 化工进展, 2021, 40(12): 6629-6639. doi: 10.16085/j.issn.1000-6613.2021-0081 [8] 周守毅. 钢铁企业副产煤气中硫化物的测定[J]. 环境科学与技术, 2017, 40(S1): 252-254. [9] 贾彩清, 谢建. 高炉煤气干法脱硫系统及方法: 中国, CN110387270A[P]. 2019-10-29. [10] 魏振浩, 章昌兵, 龙志峰, 等. 用于高有机硫浓度的高炉煤气湿法脱硫系统及工艺: 中国, CN110776961A[P]. 2020-02-10. [11] IGNASI S, ENNRIC B, A MEHMET O, et al. Electrochemical advanced oxidation processes: today and tomorrow. A review[J]. Environmental Science and Pollution Research, 2014, 21(14): 8336-8367. doi: 10.1007/s11356-014-2783-1 [12] 王玉芝, 于天霞, 邢宇. 加入EDTA改进硫化氢吸收液的方法探讨[J]. 化学与黏合, 2011, 33(3): 77-79. [13] 张少杰, 李斌, 赵光明. Na2CO3+EDTA+EDTA-2Na吸收剂对湿法烟气深度脱硫性能的实验研究[J]. 山东化工, 2017, 46(7): 193-194. doi: 10.3969/j.issn.1008-021X.2017.07.075 [14] 张爽. 直接催化氧化法脱除酸性气体中硫化氢工艺研究[D]. 长春: 东北师范大学, 2016. [15] 刘雪珂. 有机介质脱硫体系的构建及其氧化羰基硫工艺[D]. 北京: 北京化工大学, 2020. [16] PRAKASH D V, EUGENY Y K. Kinetics of carbonyl sulfide reaction with alkanolamines: A review[J]. Chemical Engineering Journal, 2009, 148(2/3): 207-211. [17] 马少宁, 王智. 精馏过程中气-液比条件的工程意义[J]. 化工时刊, 2014, 28(8): 36-39. doi: 10.3969/j.issn.1002-154X.2014.08.013 [18] 周向, 陈燕, 陈瑜, 等. 吸收烟气中低浓度CO2的操作条件分析[J]. 中国冶金, 2019, 29(7): 61-65. [19] 李胜利, 胡胜, 冯求宝, 等. 脉冲放电条件下用高炉煤气洗涤水脱硫的研究[J]. 环境科学学报, 2011, 31(1): 186-192. doi: 10.13671/j.hjkxxb.2011.01.006 [20] YADOLLAH T, MOHAMMAD S, FATOLA F. Electrochemical oxidative desulfurization for high sulfur content crude gas oil[J]. Separation and Purification Technology, 2020, 248: 117117. doi: 10.1016/j.seppur.2020.117117 [21] 田建勋, 祁贵生, 刘有智, 等. 碳酸钠溶液吸收硫化氢富液的直接电解工艺[J]. 化工进展, 2015, 34(2): 325-329. doi: 10.16085/j.issn.1000-6613.2015.02.005 [22] 罗万江, 兰新哲, 宋永辉. 煤的电化学脱硫技术研究及进展[J]. 选煤技术, 2009(3): 64-67. doi: 10.3969/j.issn.1001-3571.2009.03.026 [23] TANG X D, HU T, LI J J, et al. Desulfurization of kerosene by the electrochemical oxidation and extraction process[J]. Energy Fuels, 2015, 29(4): 2097-2103. doi: 10.1021/ef502437m [24] 苗沛然, 杨晓东, 王永敏. 直接碱催化水解法脱除羰基硫的技术经济分析[J]. 中国冶金, 2019, 29(1): 77-82. doi: 10.13228/j.boyuan.issn1006-9356.20180142 -





 下载:
下载: