-
磷是自然界中重要的化学元素,广泛应用于人类的生产生活中。然而,过量的磷排放会引起水体富营养化,导致全球30%~50%水资源水质恶化[1]。另一方面,磷作为不可再生资源,其全球储量估计在未来50~100 a内耗尽[2],全球粮食供应将面临巨大挑战[3]。目前,用于去除或回收污水中磷的方法包括生物法、化学沉淀法、离子交换法、吸附法等[3],其中吸附法因其去除率高、操作简单、可回收利用、无二次污染等优点成为研究热点[5],尤其是天然矿物、农业废物、工业废物等廉价材料的吸附研究[6-8]。
给水厂污泥(DWTR)是饮用水处理过程中不可避免的副产品。根据《城市建设统计年鉴》中的估算值,2019年我国给水厂污泥产量可达到320×104 t,预计到2030年将突破400×104 t,这不仅会增加环境负担,而且会增加处理成本[9]。由于DWTR中含有无定形态的铁铝等元素,有较大的比表面积和丰富的孔隙结构,对水中阴离子尤其是
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 具有选择性吸附,其吸附机理是DWTR表面羟基与${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 发生配体交换形成内球络合物[10]。但大多数研究中DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量为3.5~23.0 mg·g−1,吸附性能有限[11]。因此,研究人员通过酸活化[12]、热活化[12]、降低到纳米级粒径[13]或者金属负载等方法对DWTR进行改性。其中金属改性可丰富吸附材料表面的官能团,提高吸附剂对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附能力[14]。有研究[15-16]表明,镧对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 具有很强的亲和力,但较高的价格限制了镧的广泛应用。而铁元素资源丰富,廉价易得,但对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附容量较低[16]。若以给水厂污泥为原材料,将镧和铁负载到DWTR上,发挥镧铁的协同作用,则有望实现吸附剂的高效吸附和经济实用的双重目标。基于上述背景,本研究采用沉淀法制备了镧铁负载给水厂污泥复合材料(LaFe-DWTR),研究了LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的静态吸附过程,探讨了吸附剂投加量、吸附等温线、吸附动力学、pH以及共存离子的影响特征,考察了LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附性能,并结合FTIR和XPS对LaFe-DWTR表征结果揭示了可能的吸附机理,以期为LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 吸附的应用提供参考。 -
实验试剂:七水合氯化镧(LaCl3·7H2O)、氯化铁(FeCl3)、磷酸二氢钾(KH2PO4)、硫酸(H2SO4)、抗坏血酸(C6H8O6)、钼酸铵((NH4)2MoO4)、酒石酸锑钾(CHKOSb)、盐酸(HCl)、氢氧化钠(NaOH)等,均为分析纯。
实验仪器:UV2600型紫外分光光度计(日本岛津)、AL204型电子分析天平(瑞士梅特勒-托利多)、HZQ-F160型恒温振荡箱(哈尔滨东联电子)、Zeiss Merlin型场发射扫描电子显微镜-能谱仪(德国蔡司)、Nano ZS90型zeta电位仪(英国马尔文)、TriStar II 3020型比表面积测定仪(美国麦克)、Master sizer2000型粒径分析仪(英国马尔文)、ICP-MS7900型电感耦合等离子体质谱仪(美国安捷伦)、Frontier FTIR型傅里叶变换红外光谱仪(美国珀金埃尔默)、PHI Quantera型X射线光电子能谱仪(日本理学)。
-
LaFe-DWTR的制备。将自然风干后的给水厂污泥(DWTR)于105 ℃烘箱干燥24 h,研磨过120目筛保存(粒径≤0.125 mm)。将一定质量的LaCl3·7H2O和FeCl3溶解于250 mL去离子水中,加入5 g DWTR搅拌均匀,缓慢滴加3.0 mol·L−1 NaOH至混合液pH为11后,在500 r·min−1的条件下连续搅拌5 h,再陈化24 h;然后倾去上清液,用去离子水洗涤沉淀物至中性,于105 ℃烘箱干燥12 h,研磨后过120目筛保存备用。
静态吸附实验。配制50.00 mg·L−1的
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 溶液,加入2.0 g·L−1的LaFe-DWTR,使用0.1 mol·L−1的NaOH和HCl调节pH为6.0,在25 ℃、160 r·min−1的条件下振荡,反应24 h后取上清液,过0.45 μm滤膜测定${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 质量浓度。按照静态吸附实验操作程序,在0.5~6.0 g·L−1内优化LaFe-DWTR的投加量,定期采样,分析吸附动力学过程;吸附等温实验的初始${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 质量浓度为0~300.00 mg·L−1,分别研究pH为2.0~11.0和Cl−、${\rm{NO}}_3^ - $ 、${\rm{SO}}_4^{2 - }$ 、${\rm{HCO}}_3^ - $ 、${\rm{SiO}}_3^{2 - }$ 和HA质量浓度为50.00~250.00 mg·L−1时对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 吸附效果的影响。采用经典的吸附等温线和动力学模型对吸附数据进行拟合[17]。采用1.1中的实验仪器对LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 前后的表面形貌、元素分布、表面电位、表面官能团和元素价态分布进行表征与分析。 -
DWTR和LaFe-DWTR的SEM和EDS如图1所示。DWTR呈无规则的片层絮状结构,负载镧和铁元素后,LaFe-DWTR表面更为松散粗糙,有较多小颗粒聚集,应该为镧铁复合氢氧化物颗粒[18]。一般而言,纯氢氧化镧形态为棒状。而上述现象说明铁的掺入形成了球状聚集体颗粒,此现象与镧铁氢氧化物的SEM形貌特征相似[16]。图1(d)中LaFe-DWTR的DES面扫描结果证实:Fe、La、Al和O元素分布在LaFe-DWTR表面。这说明La和Fe成功负载到DWTR上。
DWTR和LaFe-DWTR的表面元素含量变化见表1。DWTR主要由C、O、Al、Mg、Si、Fe等元素组成,这与以往研究[19]报道的DWTR成分相似。负载镧和铁之后,LaFe-DWTR中C、O、Al、Mg、Si等元素含量降低,Fe元素含量明显升高,同时出现了La元素,其质量百分数为27.79%。
DWTR和LaFe-DWTR的理化性质见表2。负载镧和铁导致DWTR的比表面积由36.17 m2·g−1增加到98.57 m2·g−1,孔体积由0.09 m3·g−1增加到0.17 m3·g−1。这可能是由于镧铁氢氧化物在DWTR表面沉淀增大了其比表面积和孔体积。有研究[16]表明,铁的掺入可使晶体结构规则的氢氧化镧转化为微晶结构,可增加材料的比表面积和活性位点,从而促进对
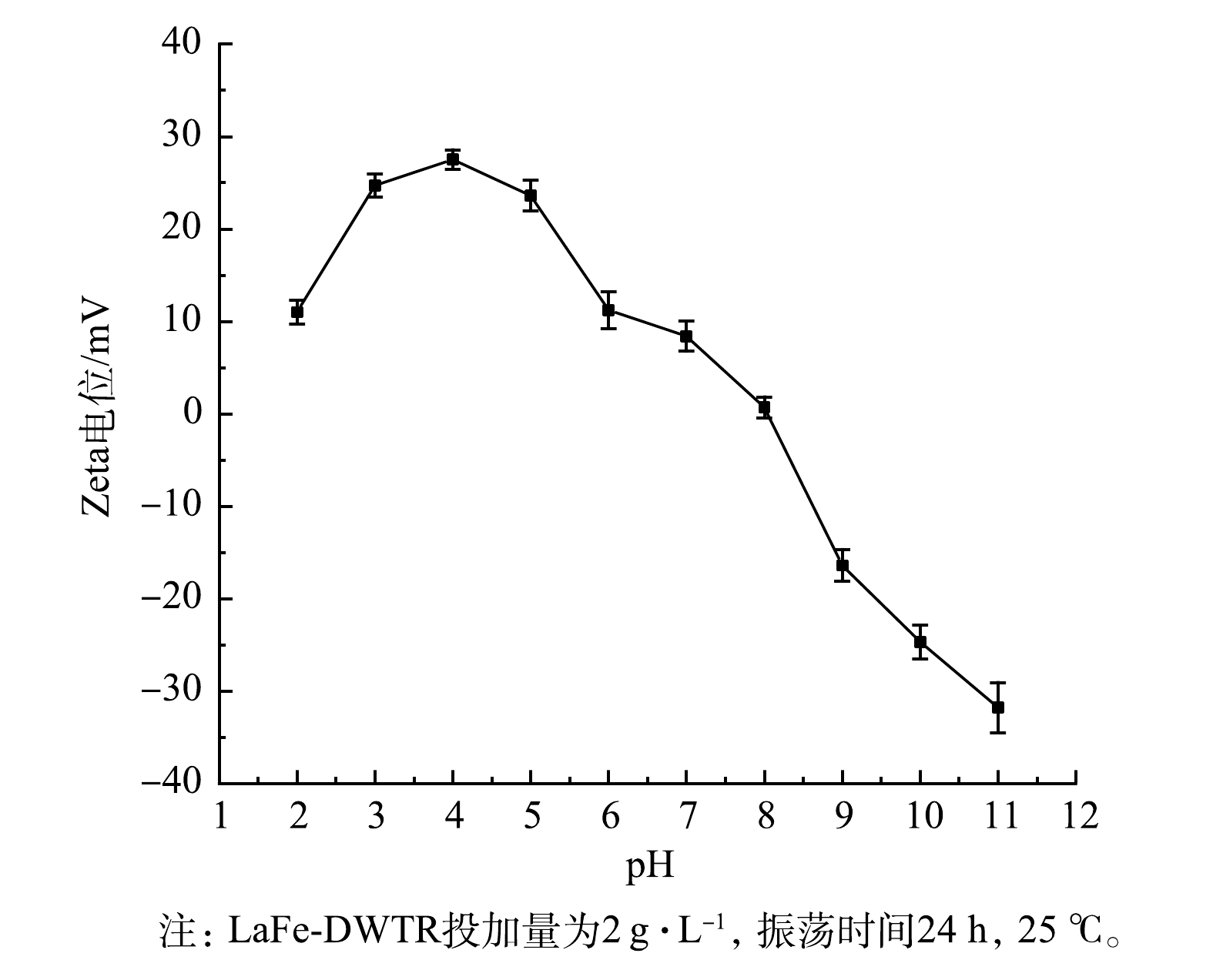
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附。采用ICP测得DWTR中铁的质量浓度为34.7 mg·g−1,LaFe-DWTR中镧和铁的质量浓度分别为175.1 mg·g−1和107.6 mg·g−1。这说明较高含量的镧、铁是提高${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 吸附量的关键。LaFe-DWTR在不同pH下的Zeta电位如图2所示。显然,LaFe-DWTR的表面电荷随着pH的增加逐渐降低,等电点为8.04。这与镧铁氢氧化物在不同pH下的Zeta电位变化趋势接近[20]。当溶液pH低于8.04时,LaFe-DWTR表面羟基质子化带正电,LaFe-DWTR与
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 之间的静电吸引有利于去除${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 。另一方面,当pH大于8.04时,LaFe-DWTR表面羟基脱质子化产生氧负离子而带负电,因而不利于${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 吸附。 -
1) LaFe-DWTR投加量对吸附的影响。如图3所示,随着投加量的增加,LaFe-DWTR对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量持续下降,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 去除率先迅速增加后趋于平缓。当LaFe-DWTR投加量由0.5 g·L−1增加到2.0 g·L−1时,吸附量由44.77 mg·g−1下降到23.91 mg·g−1,去除率由44.76%增加到95.62%。该结果说明:随着LaFe-DWTR投加量增加,吸附位点增多,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 去除率保持相对稳定的增长速率。当投加量由2.0 g·L−1增加到6.0 g·L−1时,吸附量从23.91 mg·g−1持续下降到8.33 mg·g−1,但材料对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的去除率增长幅度很小。这说明:LaFe-DWTR投加量较高时,虽然去除率逐渐趋于100%,但LaFe-DWTR的吸附量很低,吸附位点未能充分利用。考虑到处理效率和经济成本,选择2.0 g·L−1为LaFe-DWTR的最佳投加量。2)吸附等温线。LaFe-DWTR吸附
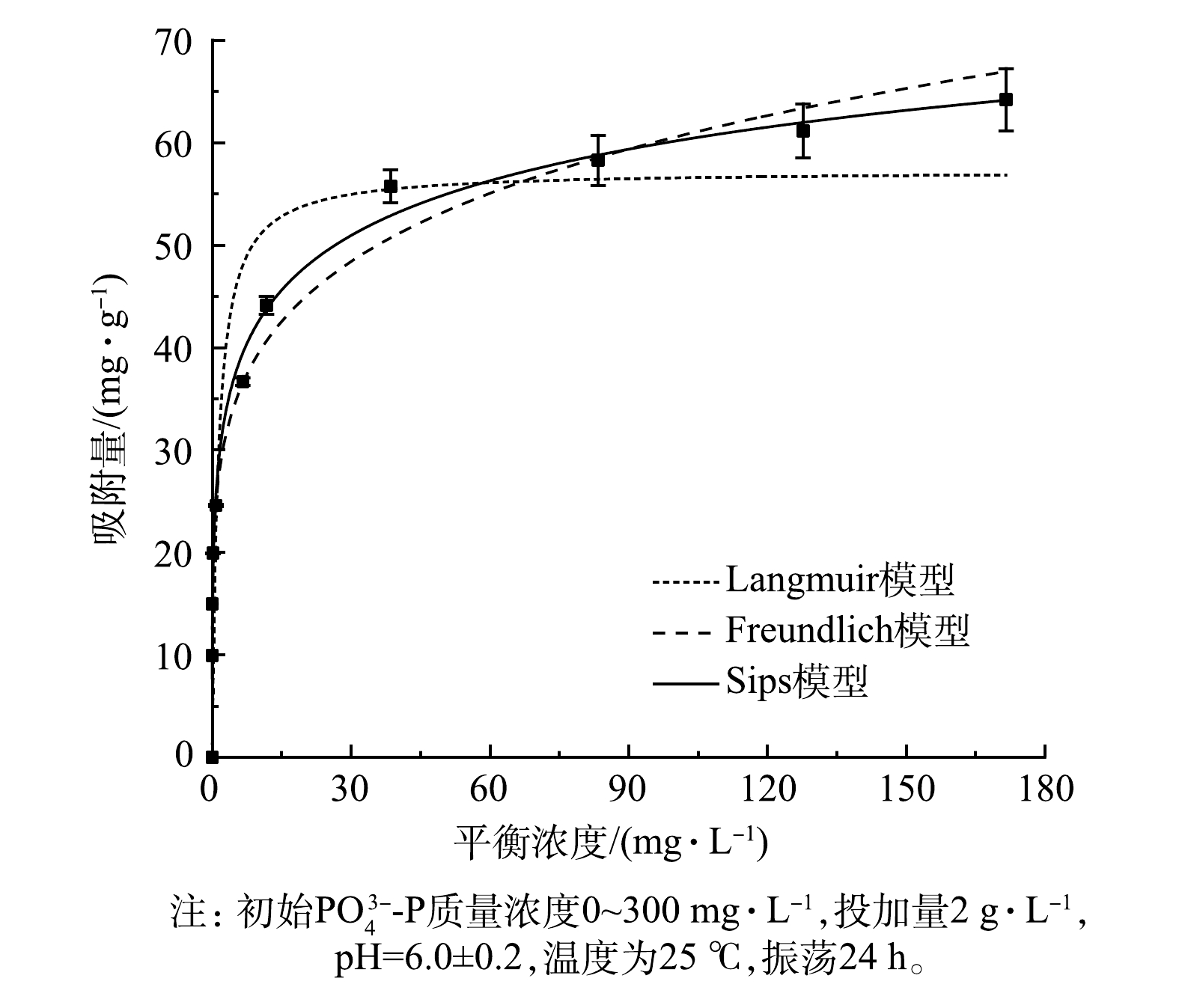
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的等温线曲线如图4所示。LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量随着${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 平衡浓度的增加而增加,并逐渐趋于平缓。采用Langmuir,Freundlich和Sips模型对LaFe-DWTR的吸附等温线进行拟合,具体参数如表3所示。可见,LaFe-DWTR的Sips模型对等温线拟合程度较好(R2=0.98)。这说明:在初始${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 质量浓度为0~300 mg·L−1时,LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附过程可用非均匀的多分子层吸附模型模拟[21]。由图4可见,在平衡质量浓度为30~180 mg·L−1时,LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量接近57.27 mg·g−1。比较不同吸附材料对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的理论吸附量 (表4),发现LaFe-DWTR具有明显的优势。3)吸附动力学。LaFe-DWTR对
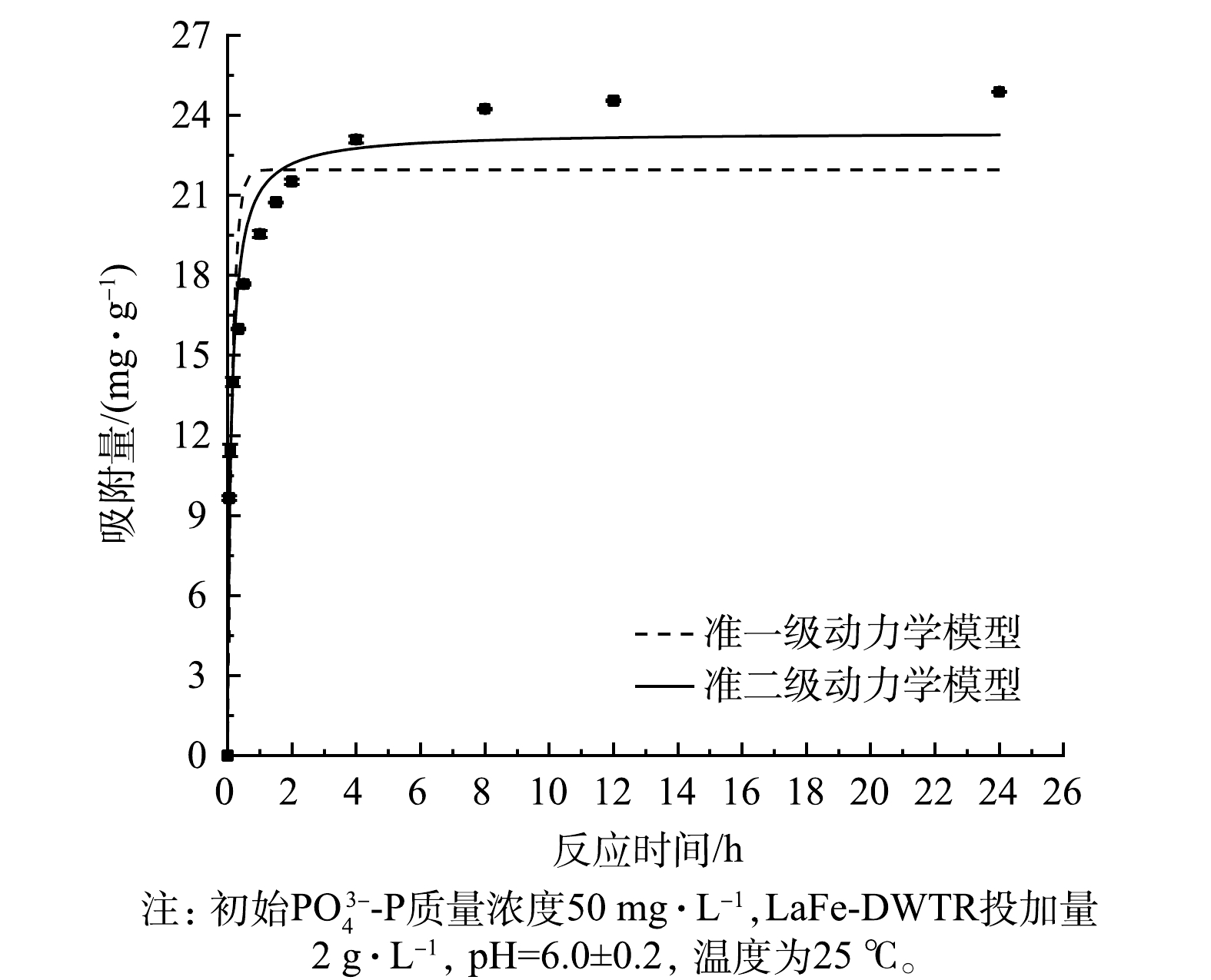
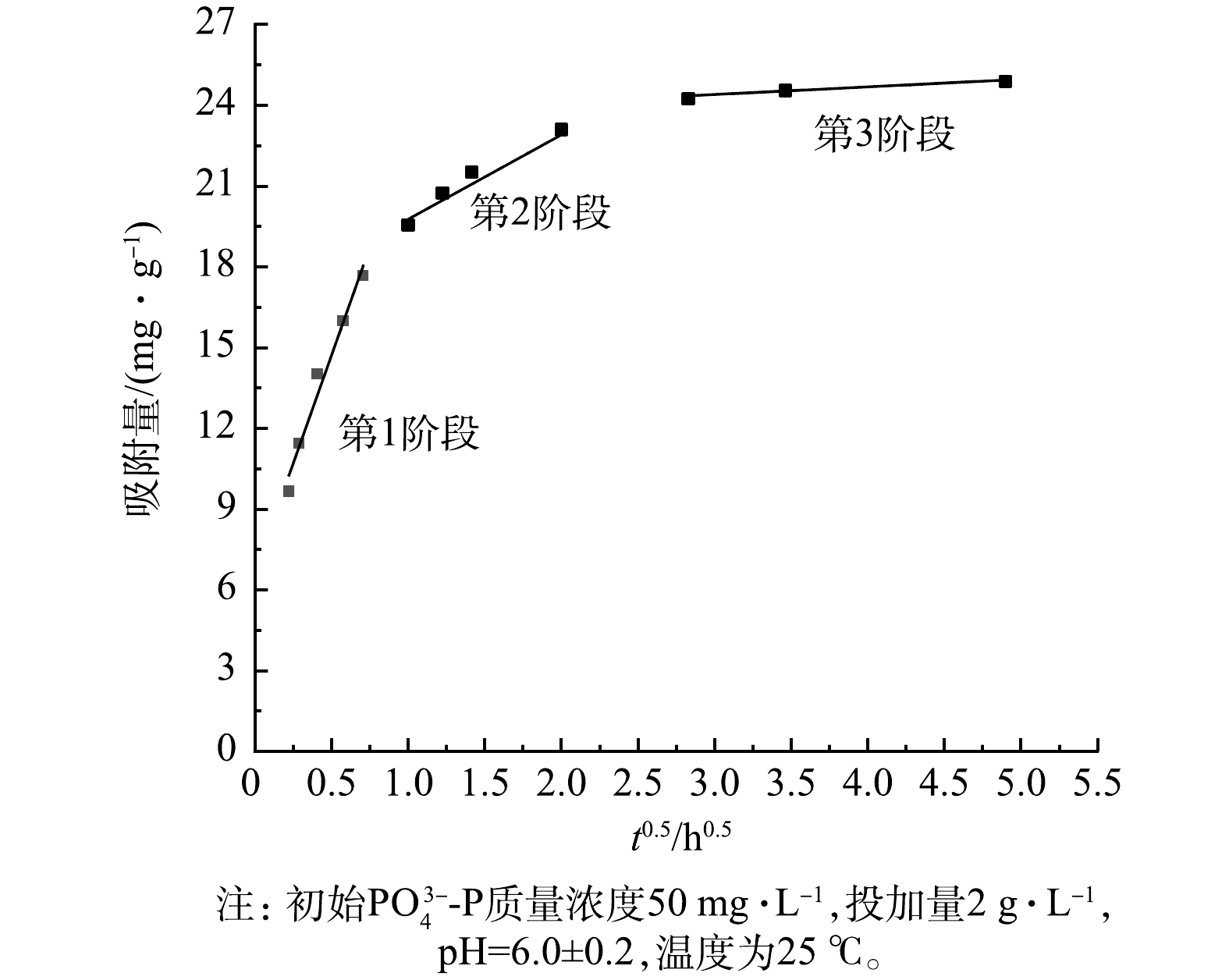
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的动力学曲线如图5所示。LaFe-DWTR吸附量在最开始的2 h内迅速增加,吸附量可达到最大吸附量的86.45%,并在8 h后趋于稳定,24 h时达到最大。而文献报道La/Fe为1∶1的镧铁氢氧化物对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量在6 h才达到最大吸附量的87.9%[20]。这可能是由于:LaFe-DWTR的平均孔径(6.00 nm)大于镧铁氢氧化物的平均孔径(2.00 nm)[16],有利于${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的表面扩散与吸附。采用准一级和准二级动力学模型进行动力学曲线拟合,相应的参数如表5所示。可见,LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附过程更符合准二级动力学模型。计算得出的${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的平衡吸附量(23.36 mg·g−1)接近平衡吸附量的实验结果(24.88 mg·g−1),表明LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的决定性步骤是化学吸附[28]。进一步通过Weber-Morris模型进行动力学曲线拟合,结果分别见图6和表6。吸附过程分为3个阶段,说明颗粒内扩散参与了吸附过程;拟合直线均未经过原点,说明颗粒内扩散不是吸附过程的限制步骤[28]。第1阶段的拟合直线斜率较大,表明吸附开始阶段以表面扩散为主。吸附初期,LaFe-DWTR表面提供大量的吸附位点,且LaFe-DWTR固液界面的
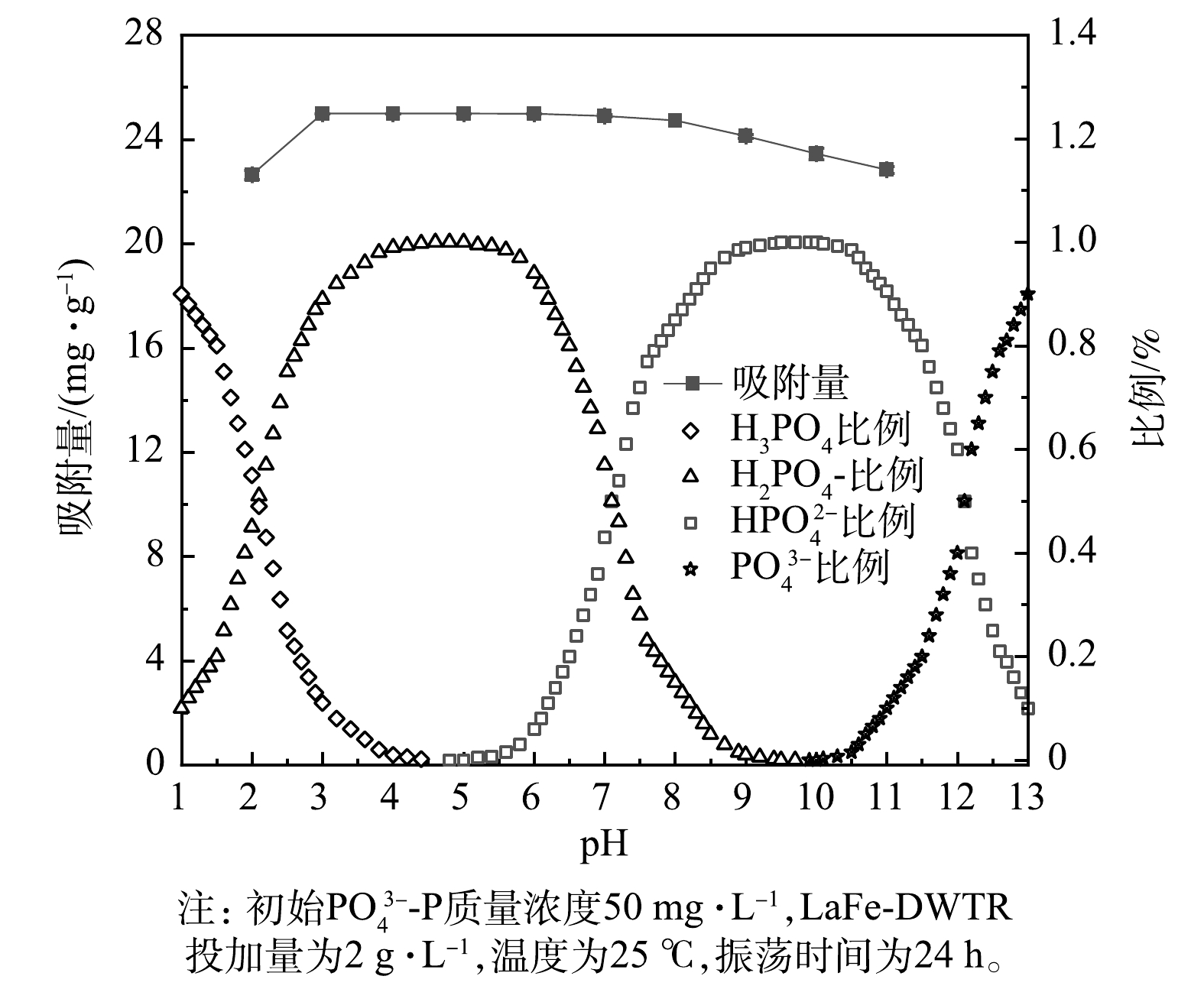
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 浓度梯度大,有利于${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 从固液界面向LaFe-DWTR表面迁移,并与LaFe-DWTR表面羟基发生配体交换作用。第2阶段拟合直线的斜率较低,LaFe-DWTR表面的活性位点被占据,此时内膜扩散起主要作用,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 经颗粒内扩散吸附在LaFe-DWTR的中孔、微孔结构中。第3阶段拟合直线斜率进一步降低,此时溶液中${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 浓度降低,传质速率下降,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 在颗粒内部扩散逐渐减弱直到吸附平衡。4)pH的影响。由图7可以看出,随着pH由2.0增加到3.0,LaFe-DWTR对
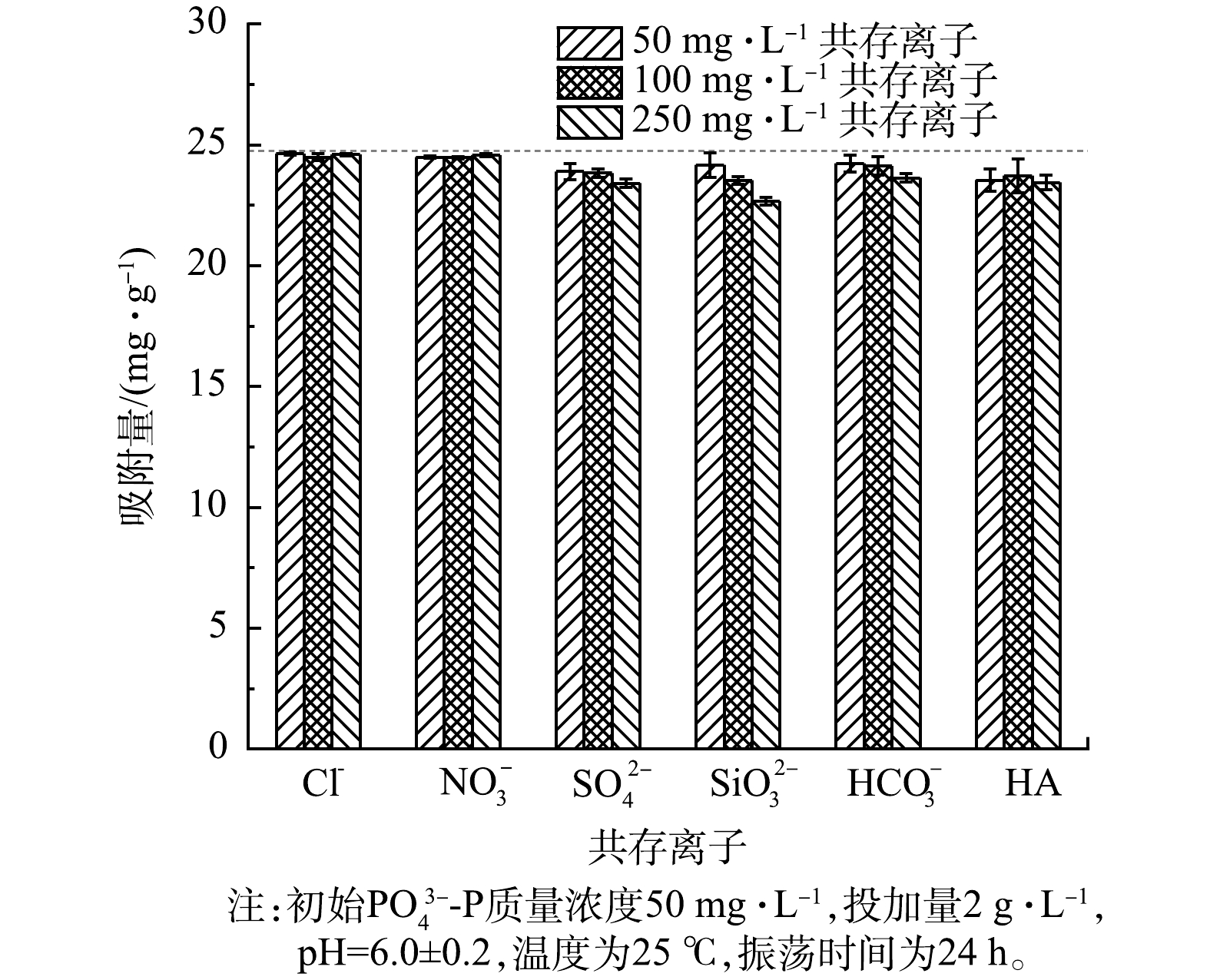
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量由22.64 mg·g−1增加到最大值24.99 mg·g−1。当pH为3.0~8.0时,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量基本保持稳定;随着pH升高到11.0,吸附量逐渐下降到22.83 mg·g−1。可见,酸性条件下LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 吸附效果更好,在实验的pH 范围内,LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的去除率依然保持在90%以上。而有研究[20]中镧铁氢氧化物对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附随着pH增加逐渐降低。这说明DWTR作为镧铁的载体可以降低LaFe-DWTR对pH的依赖。${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量受pH变化的影响主要归因于不同pH下P的形态、LaFe-DWTR的表面电荷和表面羟基质子化。当pH为2.0时,磷的形态以${{\rm{H}}_2}{\rm{PO}}_4^ - $ 和H3PO4为主,由于H3PO4不显电性且难与镧铁氢氧化物结合,且镧和铁在酸性条件下易溶出[18],从而抑制LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附。随着pH由2.0升至4.0,H3PO4不断减少,${{\rm{H}}_2}{\rm{PO}}_4^ - $ 逐渐增加,LaFe-DWTR表面金属质子化以M—${\rm{OH}}_2^ + $ 形式存在,此时静电引力作用可以强化LaFe-DWTR对${{\rm{H}}_2}{\rm{PO}}_4^ - $ 的吸附[29]。当pH由4.0升至8.0时,磷的形态以${{\rm{H}}_2}{\rm{PO}}_4^ - $ 和${\rm{HPO}}_4^{2 - }$ 为主,此时静电引力逐渐减弱,但LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量依然保持稳定。这说明LaFe-DWTR的表面羟基与${{\rm{H}}_2}{\rm{PO}}_4^ - $ 和${\rm{HPO}}_4^{2 - }$ 主要通过配体交换形成内球络合物[17]。随着pH由8.0升至11.0,磷的形态以${\rm{HPO}}_4^{2 - }$ 和${\rm{PO}}_4^{3 - }$ 为主。理论上${\rm{HPO}}_4^{2 - }$ 比单电荷的${{\rm{H}}_2}{\rm{PO}}_4^ - $ 更容易与LaFe-DWTR结合[1],但LaFe-DWTR表面羟基的脱质子化程度增加导致静电斥力增强,不利于LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附,而且配体交换也因OH-的竞争作用而受到抑制[20],路易斯酸碱作用成为LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的主要机制[17]。5)共存离子的影响。共存离子对LaFe-DWTR吸附
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的影响如图8所示。总体来说,LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量维持在10%以内,说明LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 具有很强的选择性。进一步分析表明,Cl-、${\rm{NO}}_3^ - $ 对LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的影响可以忽略。这是由于Cl-和${\rm{NO}}_3^ - $ 主要通过非特异性的静电作用在LaFe-DWTR表面形成外球络合物,而LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附主要通过配体交换或路易斯酸碱作用形成内球络合物[30]。但${\rm{HCO}}_3^ - $ 、${\rm{SiO}}_3^{2 - }$ 、${\rm{SO}}_4^{2 - }$ 和HA对LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 有轻微抑制作用,并且${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附量随着共存离子浓度的增加逐渐降低。一般情况下,${\rm{HCO}}_3^ - $ 可通过静电作用在LaFe-DWTR表面形成外球络合物[30],但${\rm{HCO}}_3^ - $ 水解导致溶液pH上升,进而抑制LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附[18]。另外,Si和P具有相似的结构和化学性质,La4(SiO4)3与LaPO4的Ksp值相近,因此,${\rm{SiO}}_3^{2 - }$ 可抑制LaFe-DWTR对${\rm{PO}}_4^{3 - }$ 的吸附[17]。而${\rm{SO}}_4^2$ 的离子半径(0.230 nm)与${{\rm{H}}_2}{\rm{PO}}_4^ - $ 的离子半径(0.238 nm)接近,能够竞争LaFe-DWTR表面的金属活性位点形成内球络合物[31]。HA是带有羟基、羧基等多种官能团的高分子聚芳族化合物,可与LaFe-DWTR发生络合反应[32]。 -
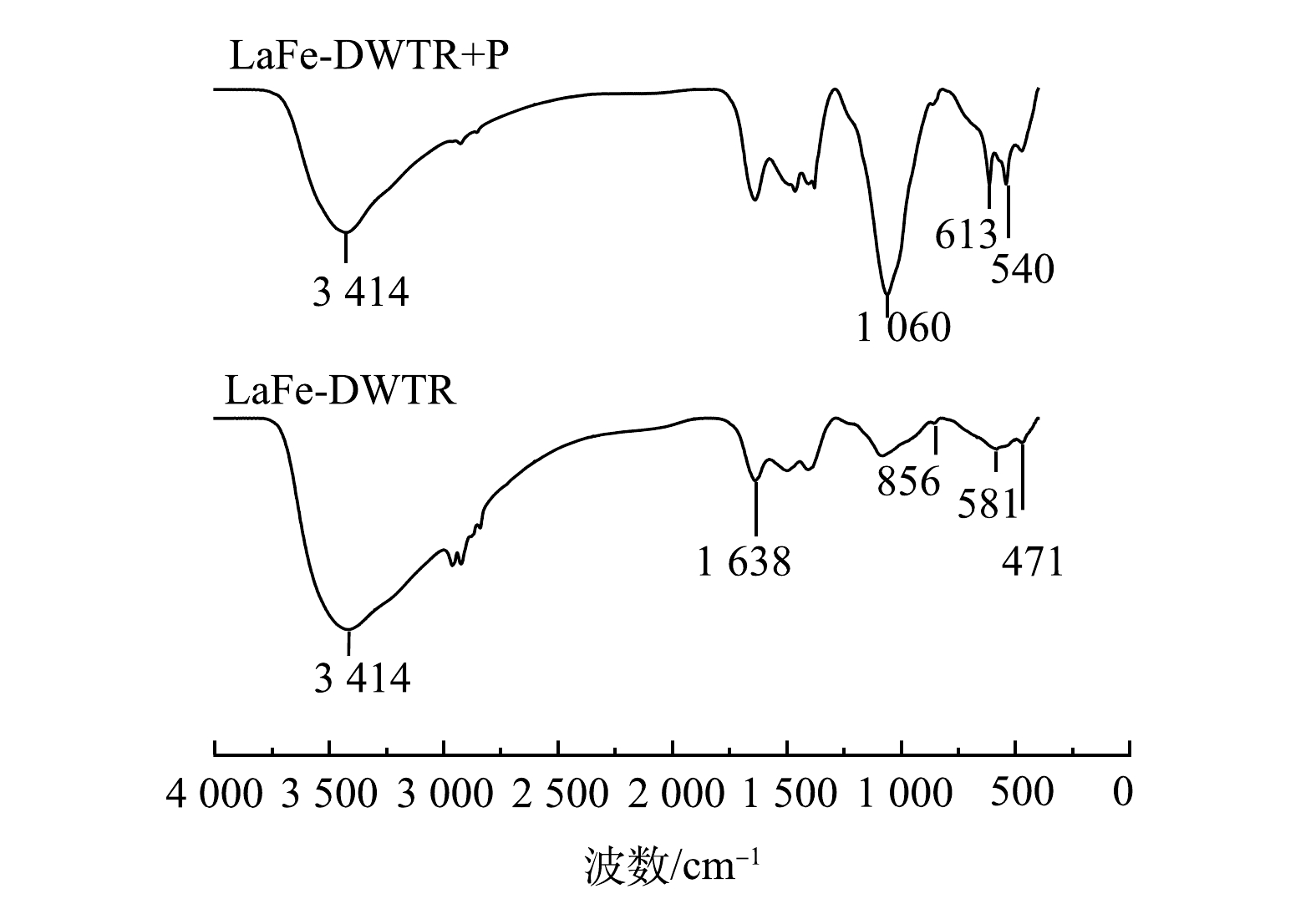
1)FTIR分析。LaFe-DWTR吸附
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 前后的FTIR如图9所示。吸附前的LaFe-DWTR在3 200~3 500 cm−1内出现了分子间氢键O—H的伸缩振动吸收峰,吸收峰面积比较大。这是由于镧铁负载DWTR产生大量羟基,在1 638 cm−1处的强峰是M—OH与吸收水分子之间的伸缩振动吸收峰[16]。856 cm−1处的弱峰是La—O键振动峰[17],581 cm−1和471 cm−1处的吸收峰分别与Fe—O和Al—O振动吸收峰很好地对应[6, 16],说明镧和铁元素成功负载到DWTR上。LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 后,3 200~3 500 cm−1处的峰面积明显减小,表明表面—OH被取代。同时,在1 060、613、540 cm−1处出现了新的吸收峰,其中613 cm−1和540 cm−1处的弱峰可能是${\rm{PO}}_4^{3 - }$ 中O—P—O的υ4振动峰,1 060 cm−1处的强峰来源于${\rm{HPO}}_4^{2 - }$ 或${{\rm{H}}_2}{\rm{PO}}_4^ - $ 中P—O的υ3振动峰[20]。由此可知,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 成功吸附到LaFe-DWTR上。2)吸附前后XPS分析。LaFe-DWTR吸附
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 前后的XPS全谱图、O1s、P2p、La3d、Fe2p、Al2p的XPS扫描光谱如图10所示。所有结果均用C1s(284.6 eV)校准。由图10(a)可以看出,LaFe-DWTR中存在La、Fe、Al、O等元素,吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 后出现了P2p峰,证明${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 已被LaFe-DWTR成功吸附。由图10(b)可以看出:O1s光谱可以分为3个重叠峰,532.8 cm−1处的吸收峰对应与金属结合氧化物的氧(M—O);531.42 cm−1和531.53 cm−1处的吸收峰对应与金属结合的羟基氧(M—OH);530.38 cm−1和530.55 cm−1处的吸收峰对应吸附水中的氧(H2O)[4]。LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 前后O1s的XPS分峰拟合数据如表7所示。可见,LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 后,M—OH键对应的峰面积由57.69%下降到45.56%,而M—O键对应的峰面积从36.77%增加到41.85%。这表明吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的过程中形成了La—O或Fe/Al—O键,因而进一步证实了${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 主要通过与LaFe-DWTR表面的-OH进行配体交换而被吸附[4]。此外,为探究LaFe-DWTR与
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 之间的相互作用,进一步分析了P2p、La3d、Al2p和Fe2p的XPS图谱。由图10(c)可以看出,LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 后出现了P2p的特征光谱(132.95 eV),与KH2PO4的标准P2p光谱(134.0 eV)相比,降低了1.05 eV。这表明${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 与LaFe-DWTR形成了内球络合物[4]。由图10(d)可以看出,LaFe-DWTR中La3d5/2的吸收峰位于834.85 eV和838.65 eV,La3d3/2的吸收峰位于851.75 eV和855.25 eV[1]。吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 后,La3d5/2的新峰位于835.5 eV和838.75 eV,La3d3/2的新峰位于852.15 eV和855.6 eV,结合能升高了0.1~0.65 eV。这证明${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 与La—OH发生配体交换作用[33]。结合图10(e)、图10(f)可以看出,吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 后,铁结合能由710.7 eV增加到711.1 eV,铝结合能由73.65 eV增加到73.95 eV。这说明Fe—OH和Al—OH基团在吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的过程中也发挥了作用[23]。 -
1)采用沉淀法成功制备出镧铁负载给水厂污泥复合材料(LaFe-DWTR),其对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的饱和吸附量为57.27 mg·g−1,等温吸附过程可用非均匀的多分子层吸附描述;吸附动力学符合准二级动力学,在前2 h的吸附量可以达到最大吸附量的86.45%。2) LaFe-DWTR在较宽的pH范围内能够保持对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的稳定吸附,在共存离子存在下对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 具有较好的吸附选择性。3) LaFe-DWTR对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附以化学吸附为主,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 与LaFe-DWTR表面羟基的配体交换为主要吸附机理。
镧铁负载给水厂污泥复合材料对水中磷酸盐的吸附性能及机理
Performance and mechanism of phosphorus adsorption by lanthanum/iron-loaded drinking water treatment residues
-
摘要: 采用沉淀法制备了镧铁负载给水厂污泥(DWTR)复合材料(LaFe-DWTR),对其微观形貌和理化性质进行了表征,考察了LaFe-DWTR对水中
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附等温线和吸附动力学,探讨了吸附剂投加量、pH和共存离子对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 吸附效果的影响,并揭示了可能的吸附机理。结果表明:相比DWTR,镧和铁负载的DWTR比表面积和孔体积明显增加;当LaFe-DWTR投加量为2.0 g·L−1,${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 初始质量浓度为50 mg·L−1时,LaFe-DWTR对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的吸附等温线符合Sips模型,吸附动力学符合准二级动力学模型,说明吸附过程主要受化学吸附和颗粒内扩散控制;LaFe-DWTR在pH 2.0~11.0内对${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的去除率均在90%以上,共存离子对LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的影响较小;LaFe-DWTR吸附${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 的主要机理是配体交换。Abstract: In this study, a precipitation method was used to prepare lanthanum/iron-loaded drinking water treatment residues (LaFe-DWTR) composite material. Its micro-morphology and physicochemical properties were characterized, and the adsorption isotherms and kinetics of LaFe-DWTR towards${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ in water, as well as the effects of dosage, pH and coexisting ions on${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ adsorption effect, were investigated. Furthermore, the corresponding adsorption mechanism between LaFe-DWTR and${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ was identified. The results showed that lanthanum/iron loading led to a significant increase of the specific surface area and pore volume of DWTR. At LaFe-DWTR dosage of 2.0 g·L−1 and initial${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ concentration of 50 mg·L−1, the adsorption isotherm and kinetics could be well fitted by sips model and pseudo-second-order kinetic model, respectively. The adsorption process was mainly dominated by chemical adsorption and intra-particle diffusion. At pH 2.0~11.0, over 90%${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ in water could be removed by LaFe-DWTR. The coexisting ions had slight effect on${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ adsorption. Ligand exchange was the main adsorption mechanism between LaFe-DWTR and${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ .-
Key words:
- lanthanum/iron loading /
- drinking water treatment residues /
- adsorption /
- phosphorus /
- ligand exchange
-

-
表 1 DWTR和LaFe-DWTR的表面元素分布比例
Table 1. Proportion of elements in DWTR and LaFe-DWTR
% 材料 C O Al Si Mg Fe La 总量 DWTR 24.34 30.42 9.04 12.12 4.17 9.47 — 89.56 LaFe-DWTR 16.12 19.28 4.24 3.95 3.55 15.03 27.79 89.96 表 2 DWTR和LaFe-DWTR的理化性质对比
Table 2. Comparison of physical properties between DWTR and LaFe-DWTR
材料 形貌 外观 比表面积/(m2·g−1) 孔径/nm 孔体积/(cm3·g−1) 粒径/μm 铁含量/(mg·g−1) 镧含量/(mg·g−1) DWTR 粉末 黄褐色 36.17 7.02 0.09 21.16 34.70 - LaFe-DWTR 粉末 黄褐色 98.57 6.00 0.17 22.70 107.60 175.10 表 3 LaFe-DWTR对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ Table 3. Fitting results of adsorption isotherms of LaFe-DWTR towards
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ Langmuir Freundlich Sips qm kL RL2 kF 1/n RF2 Ks βS αS RS2 57.27 0.78 0.86 25.69 0.19 0.97 360.54 0.23 0.06 0.98 表 4 不同材料的
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ Table 4. Comparison of adsorption capacity of different materials
原材料 改性方法 初始 ${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 理论吸附量/(mg·g−1) 参考文献 DWTR - 5.00~100.00 4.17~8.20 [22] DWTR 球形颗粒(D=6 mm) 0.31~310.00 19.70 [23] DWTR 热活化 52.00~930.00 29.66 [12] DWTR 酸活化 52.00~930.00 22.86 [12] DWTR 热酸活化 155.00~3 100.00 53.23 [24] DWTR 铁改性 10.00~150.00 24.69 [25] DWTR 镧改性 0.50~8.00 12.30 [26] 活性炭纤维 镧铁改性 10.00~60.00 29.44 [18] 膨润土 镧铁改性 2.00~40.00 14.30 [27] 蒙脱石 镧铁改性 0.49~4 032.24 17.86 [6] 膨胀石墨 镧铁改性 20.00~60.00 34.72 [28] DWTR 镧铁改性 0~300.00 57.27 本研究 表 5 LaFe-DWTR对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ Table 5. Fitting results of adsorption kinetics of LaFe-DWTR towards
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 准一级动力学模型 准二级动力学模型 qe/(mg·g−1) k1 R2 qe/(mg·g−1) k2 R2 21.96 0.30 0.88 23.36 0.40 0.92 表 6 LaFe-DWTR对
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ Table 6. Fitting results of Weber-Morris intraparticle models of LaFe-DWTR towards
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 第1阶段 第2阶段 第3阶段 kp1/(mg·(g·h0.5)−1) R12 kp2/(mg·(g·h0.5)−1) R22 kp3/(mg·(g·h0.5)−1) R32 16.06 0.97 3.14 0.96 0.28 0.61 表 7 LaFe-DWTR吸附
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ Table 7. Deconvolution of XPS O1s spectra for LaFe-DWTR before and after
${\rm{PO}}_4^{3 - } {\text{-}} {\rm{P}}$ 材料 分峰 结合能/eV 半峰全宽/eV GL/% 峰面积 百分比/% 吸附前 H2O 532.80 1.07 80 6 912.87 5.54 M—OH 531.42 1.55 80 71 963.55 57.69 M—O 530.38 1.52 80 45 864.25 36.77 吸附后 H2O 532.80 1.30 80 21 552.21 12.59 M—OH 531.53 1.30 80 77 969.30 45.56 M—O 530.55 1.22 80 71 612.05 41.85 -
[1] LI X L, WANG Y L, LI J Y, et al. Rapid and selective harvest of low-concentration phosphate by La(OH)3 loaded magnetic cationic hydrogel from aqueous solution: Surface migration of phosphate from -N+(CH3)3 to La(OH)3[J]. Science of the Total Environment, 2021, 800(15): 149481. [2] LUO F, FENG X N, JIANG X Q, et al. Lanthanum molybdate/magnetite for selective phosphate removal from wastewater: Characterization, performance, and sorption mechanisms[J]. Environmental Science and Pollution Research, 2020, 28(4): 1-10. [3] SHAN S J, WANG W, LIU D M, et al. Remarkable phosphate removal and recovery from wastewater by magnetically recyclable La2O2CO3/γ-Fe2O3 nanocomposites[J]. Journal of Hazardous Materials, 2020, 397(5): 122597. [4] SHI W M, FU Y W, WEI J, et al. Enhanced phosphate removal by zeolite loaded with Mg-Al-La ternary (hydr)oxides from aqueous solutions: Performance and mechanism[J]. Chemical Engineering Journal, 2019, 357: 33-44. doi: 10.1016/j.cej.2018.08.003 [5] XIE J, WANG Z, LU S Y, et al. Removal and recovery of phosphate from water by lanthanum hydroxide materials[J]. Chemical Engineering Journal, 2014, 254: 163-170. doi: 10.1016/j.cej.2014.05.113 [6] CASTRO L F, BRANDAO V, BERTOLINO L C, et al. Phosphate adsorption by montmorillonites modified with lanthanum/iron and a laboratory test using water from the Jacarepaguá Lagoon (RJ, Brazil)[J]. Journal of the Brazilian Chemical Society, 2019, 30(3): 641-657. [7] QIU H, NI W X, ZHANG H H, et al. Fabrication and evaluation of a regenerable HFO-doped agricultural waste for enhanced adsorption affinity towards phosphate[J]. Science of the Total Environment, 2020, 703(PT.2): 135493.1-135493.11. [8] RAZALI M, ZHAO Y Q, BRUEN M. Effectiveness of a drinking-water treatment sludge in removing different phosphorus species from aqueous solution[J]. Separation and Purification Technology, 2007, 55(3): 300-306. doi: 10.1016/j.seppur.2006.12.004 [9] 崔競文, 郑晓英, 邱丽佳, 等. 城市给水厂污泥对污水中磷的动态吸附[J]. 环境工程学报, 2020, 14(4): 917-924. doi: 10.12030/j.cjee.201906110 [10] TAHMAZI T A, BABATUNDEA A O. Mechanistic study of P retention by dewatered waterworks sludges[J]. Environmental Technology & Innovation, 2016, 6: 38-48. [11] EVERAERT M, BERGMANS J, BROOS K, et al. Granulation and calcination of alum sludge for the development of a phosphorus adsorbent: From lab scale to pilot scale[J]. Journal of Environmental Management, 2020, 279: 111525. [12] 高思佳, 王昌辉, 裴元生. 热活化和酸活化给水处理厂废弃铁铝泥的吸磷效果[J]. 环境科学学报, 2012, 32(3): 606-611. [13] ELKHATIB E A, MAHDY A M, SALAMA K A. Green synthesis of nanoparticles by milling residues of water treatment[J]. Environmental Chemistry Letters, 2015, 13(3): 333-339. doi: 10.1007/s10311-015-0506-6 [14] 蒋亚辉, 张增强, 李荣华, 等. 铁锰氧化物改性铝污泥对Pb2+和Cu2+的吸附性能[J]. 西北农林科技大学学报(自然科学版), 2019, 47(4): 97-106. [15] SONG Q X, HUANG S Z, LI X, et al. Synthesis of magnetite/lanthanum hydroxide composite and magnetite/aluminum hydroxide composite for removal of phosphate[J]. Science of the Total Environment, 2020, 723: 137838. doi: 10.1016/j.scitotenv.2020.137838 [16] YU J, XIANG C, ZHANG G, et al. Activation of lattice oxygen in LaFe(Oxy)hydroxides for efficient phosphorus removal[J]. Environmental Science & Technology, 2019, 53(15): 9073-9080. [17] DONG S X, WANG Y L, ZHAO Y W, et al. La3+/La(OH)3 loaded magnetic cationic hydrogel composites for phosphate removal: Effect of lanthanum species and mechanistic study[J]. Water Research, 2017, 126(1): 433-441. [18] LIU J Y, ZHOU Q, CHEN J H, et al. Phosphate adsorption on hydroxyl-iron-lanthanum doped activated carbon fiber[J]. Chemical Engineering Journal, 2013, 215-216(2): 859-867. [19] ZHAO Y Q, NZIHOU A, REN B, et al. Waterworks sludge: An underrated material for beneficialreuse in water and environmental engineering[J]. Waste and Biomass Valorization, 2021, 12(8): 4239-4251. doi: 10.1007/s12649-020-01232-w [20] DUAN H J, ZHANG L, WANG Y L, et al. Phosphate removal from aqueous solution by Fe-La binary (hydr)oxides: Characterizations and mechanisms[J]. Environmental Science and Pollution Research, 2021. [21] CHEN Y N, XU R, LIU Y H, et al. La(OH)3-modified magnetic CoFe2O4 nanocomposites: A novel adsorbent with highly efficient activity and reusability for phosphate removal[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2020, 599(12): 124870. [22] BAI L L, WANG C H, HE L S, et al. Influence of the inherent properties of drinking water treatment residuals on their phosphorus adsorption capacities[J]. Journal of Environmental Sciences, 2014, 26: 2397-2405. doi: 10.1016/j.jes.2014.04.002 [23] LI X Q, CUI J, PEI Y S. Granulation of drinking water treatment residuals as applicable media for phosphorus removal[J]. Journal of Environmental Management, 2018, 213: 36-46. [24] WANG C H, GAO S J, WANG T X, et al. Effectiveness of sequential thermal and acid activation on phosphorus removal by ferric and alum water treatment residuals[J]. Chemical Engineering Journal, 2011, 172(2-3): 885-891. doi: 10.1016/j.cej.2011.06.078 [25] 马啸宙. 铁优化给水污泥降解水中磷行为特性及机理探讨[D]. 兰州: 兰州交通大学, 2016. [26] WANG C H, HAO Z, WEI Z, et al. A simple method to improve the adsorption properties of drinking water treatment residue by lanthanum modification[J]. Chemosphere, 2019, 221: 750-757. doi: 10.1016/j.chemosphere.2019.01.099 [27] LIN J W, ZHAO Y Y, ZHAN Y H, et al. Control of internal phosphorus release from sediments using magnetic lanthanum/iron-modified bentonite as active capping material[J]. Environmental Pollution, 2020, 264: 114809. doi: 10.1016/j.envpol.2020.114809 [28] ZHANG L, JIN S W, WANG Y, et al. Phosphate adsorption from aqueous solution by lanthanum-iron hydroxide loaded with expanded graphite[J]. Environmental Technology, 2018, 39(8): 997-1006. doi: 10.1080/09593330.2017.1317843 [29] ZHOU Y Q, WANG Y L, DONG S X, et al. Phosphate removal by a La(OH)3 loaded magnetic MAPTAC-based cationic hydrogel: Enhanced surface charge density and Donnan membrane effect[J]. Journal of Environmental Sciences, 2022, 113: 26-39. doi: 10.1016/j.jes.2021.05.041 [30] WU B, WAN J, ZHANG Y Y, et al. Selective phosphate removal from water and wastewater using sorption: Process fundamentals and removal mechanisms[J]. Environmental Science & Technology, 2020, 54(1). [31] LI R H, WANG J J, ZHOU B Y, et al. Enhancing phosphate adsorption by Mg/Al layered double hydroxide functionalized biochar with different Mg/Al ratios[J]. Science of the Total Environment, 2016, 559: 121-129. doi: 10.1016/j.scitotenv.2016.03.151 [32] BROWN P A, GILL S A, ALLEN S J. Metal removal from wastewater using peat[J]. Water Research, 2000, 34(16): 3907-3916. doi: 10.1016/S0043-1354(00)00152-4 [33] WU B, FANG L P, FORYNER J D, et al. Highly efficient and selective phosphate removal from wastewater by magnetically recoverable La(OH)3/Fe3O4 nanocomposites[J]. Water Research, 2017, 126(1): 179-188. -


















 下载:
下载: