-
截至2020年底,我国污泥产量已超过6 000×104 t(含水率80%),给污水处理厂带来了沉重的负担。然而,剩余污泥中含有大量的有机质,如蛋白质、多糖等。利用厌氧发酵产挥发性脂肪酸(volatile fatty acids,VFAs)技术可实现污泥的减量化和资源化。但是,有机物转化率低是制约此技术推广应用的关键问题[1]。污泥高温热水解技术已被广泛用于污泥预处理,以提高发酵产酸性能。有研究报道指出,利用污泥热水解上清液进行液态发酵产酸,可明显提高产酸效率[2]。但是,在热水解过程中,会有一些具有抑制特性的有机物被大量释放至上清液,其中就包括腐殖酸(humic acids,HAs)。腐殖酸作为城市污泥的主要有机组分,一般占挥发性悬浮固体的6%~20%[3],其主要以惰性状态存在于污泥固相中。在传统发酵过程中,腐殖酸对污泥厌氧发酵产酸的影响常常被忽略。然而,在热水解上清液中,溶解性腐殖酸含量可高达1.0 g·L−1[4]。腐殖酸含有许多活性官能团,化学结构非常复杂[5]。这导致腐殖酸不仅会抑制污泥水解酶的活性[6],还会与底物结合,使微生物无法接触并利用底物[7]。因此,热水解释放的大量溶解性腐殖酸不可被忽略;如何避免腐殖酸对厌氧发酵产酸的抑制已成为研究热点。
现阶段,膜过滤法、混凝-超滤等常被用于处理饮用水中的溶解性腐殖酸。但这类方法易形成膜污染,影响膜的使用寿命且去除效率低下[8]。目前,国内外对于污泥中腐殖酸类物质的去除,主要是采用添加金属离子,通过静电力和阳离子交换作用来缓解腐殖酸对污泥厌氧发酵产酸的抑制作用[9]。然而,有研究者报道,热水解可促进大量腐殖酸由固相进入液相[10],其浓度约为天然水中的100倍[11]。如采用金属离子屏蔽腐殖酸,则需要投加过量金属离子,这就可能对环境造成二次污染。
腐殖酸是一种光敏化材料,利用光催化技术可高效去除天然水体中的腐殖酸[12]。但是,污泥水解液中溶解性腐殖酸含量较高,故较难去除。为此,本研究利用紫外光催化、钙盐化学絮凝以及这2种方法的耦合技术,对污泥中的腐殖酸进行结构特性以及可絮凝性的改变,以最终实现腐殖酸改性和去除的目的。该方法可为缓解厌氧发酵过程中腐殖酸对产酸的抑制作用,从而提高污泥有机物转化率提供参考。
全文HTML
-
城市污泥来自无锡市某污水处理厂的二沉池,其中钙离子质量浓度为10.0~12.0 mg·L−1。厌氧发酵产酸种泥来自江苏某能源有限公司的UASB 厌氧颗粒污泥,使用前进行了驯化。驯化过程为:将厌氧颗粒通过在105 ℃下处理2 h以杀死产甲烷菌;为了重新活化产乙酸细菌,将热处理过的污泥添加到装有营养液的1 000 mL摇瓶中,当出水pH降至4.0以下时,则认为产酸种泥驯化完成[13]。产酸种泥使用前,需要用生理盐水冲洗3遍,以洗去其中残留的溶解性有机物[14]。
1)污泥水解液制备。污泥热水解反应釜的有效容积为0.6 L,由控制器、电加热、冷却系统、温度计、压力表和减压阀组成。先将污泥含固率调节至100 g·L−1,设置3组平行试验,所需温度为160 ℃,恒温30 min后停止加热,打开冷却系统;当温度降至40 ℃时,开启减压阀[15];最后,将热水解污泥以10 000 r·min−1的转速离心10 min,固液分离,收集上清液,置于4 ℃避光保存,作为本实验液态发酵产酸的底物。上清液SCOD为15 000~18 000 mg·L−1。
2)污泥腐殖酸的提取依据国际腐殖酸协会规定的方法[16]。使用真空冷冻干燥技术将腐殖酸样品冷冻干燥成固体粉末;常温、避光、干燥保存以备用。
-
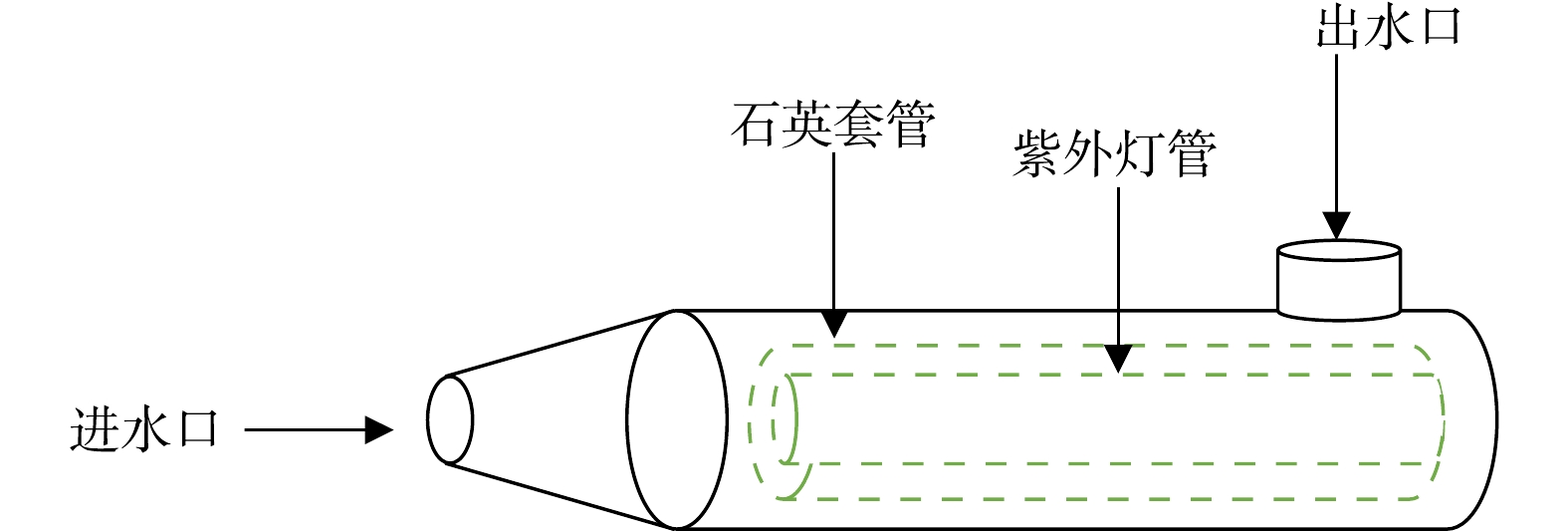
紫外光催化处理系统为双层柱状不锈钢结构,内层为具有石英玻璃保护套管的紫外灯,紫外灯输出功率为21 W,灯管型号为GPH450T5L。外层为反应腔,长1.0 m,有效容积约1.0 L,反应腔上侧设有进水口和出水口。本实验紫外光催化时长均为2 h,样品从进水口加入反应腔,紫外光催化后打开出水口取样。图1为实验装置示意图。
-
1)腐殖酸抑制污泥液态发酵产酸实验。供试污泥首先通过高温热水解,将有机物充分至到液相;固液分离后,利用上清液进行发酵产酸。投加0.6 g·L−1腐殖酸,产酸底物为污泥热水解上清液,底物和接种污泥的体积比为9∶1;将底物和接种污泥装入血清瓶(工作体积为250 mL,顶空体积为250 mL)中,用稀释的盐酸和氢氧化钠溶液调节pH至10.0±0.2;通入氮气,曝气15 min以去除底物和顶空中的氧气,期间保持严格的厌氧条件。整个过程中,血清瓶置于转速为130~170 r·min−1、温度为(35±2) ℃的恒温培养箱中。每隔24 h从瓶子里取10 mL样品进行分析,为期10 d。监测每天的pH,并且将pH调回至10.0±0.2,继续曝气15 min以保持严格的厌氧条件。实验中,同步进行了3组平行实验。
2)紫外光催化和化学絮凝对腐殖酸的影响实验。为了探究光催化耦合化学絮凝缓解腐殖酸对厌氧发酵产酸的抑制机理,提取、纯化热水解释放的溶解性腐殖酸。分别经过紫外光催化、化学絮凝以及2种技术的耦合处理方式后,观察腐殖酸含量以及结构特征的变化。
紫外光催化实验:首先在碱性条件下将提取的腐殖酸溶解,质量浓度调节至1.0 g·L−1;然后向腐殖酸溶液中投加300 mg·L−1 TiO2作为光催化剂,在200 r·min−1的强度下搅拌15 min,混合均匀后将溶液加入至紫外光催化处理系统中进行光催化反应,光照时间为2 h。同步进行了3组平行实验。
CaCl2化学絮凝实验:首先在碱性条件下将提取的腐殖酸溶解,质量浓度调节至1.0 g·L−1;然后加入300 mg·L−1 CaCl2,在100 r·min−1的强度下搅拌2 h,待体系静止沉淀30 min。同步进行了3组平行实验。
紫外光催化耦合化学絮凝实验:结合紫外光催化和CaCl2化学絮凝实验2种方法,即首先将腐殖酸溶液进行紫外光催化,然后加入CaCl2进行化学絮凝。同步进行了3组平行实验。
3)紫外光催化和化学絮凝对腐殖酸抑制厌氧发酵产酸的缓解效果。在碱性条件下(pH为10.0±0.2),向血清瓶中加入0.6 g·L−1腐殖酸。经过紫外光催化、CaCl2化学絮凝以及耦合2种方式处理后,在5 000 r·min−1条件下离心10 min,取上清液进行发酵产酸,探究这3种方法对缓解腐殖酸抑制发酵产酸的效果。同步进行了3组平行实验。
-
采用紫外-可见全波长分光光度计(Shimadzu UV-1800,日本HITACHI公司)测定腐殖酸的全波长光谱,用于表征其光催化前后的电子跃迁能力;用激光粒度分析仪(Anton Paar Litesizer™,奥地利Anton Paar公司)测定腐殖酸胶体的Zeta电位,以表征腐殖酸胶体的稳定性;用原子光谱仪(Thermo Scientific™ iCE™ 3000,美国赛默飞世尔科技公司)测定污泥中Ca2+浓度;三维荧光扫描仪(F-7000 FL Spectrophotometer,日本HITACHI公司)设定激发波长(λex)为200~550 nm、发射波长(λem)为200~550 nm、间隔为5 nm,以测定腐殖酸光催化前后的三维荧光光谱图,用于表征其分子量和芳香缩合度的变化[17];高效气相色谱仪(2010型,岛津公司)用于测定VFAs[13];紫外-可见光分光光度计(1800 PC,上海美谱达公司)测定腐殖酸样品在465和665 nm处的吸光度,用于表征光催化前后腐殖酸的E4/E6比值,该比值与腐殖酸的芳香缩合度呈反比,与其腐殖化程度呈正比[18]。用总有机碳分析仪(TOC-VCPH,日本HITACHI公司)测定碱性条件下溶解的腐殖酸。腐殖酸作为一种大分子有机物,可用TOC值来表征腐殖酸的去除率以及矿化情况。在碱性条件下溶解1.0 g·L−1腐殖酸,过0.45 μm滤膜后其滤出液TOC含量为294.73 mg·L−1[19]。每次测定设置3个平行;每次测样的取样体积均为10 mL。
1.1. 实验原料
1.2. 实验装置
1.3. 实验方法
1.4. 分析方法
-
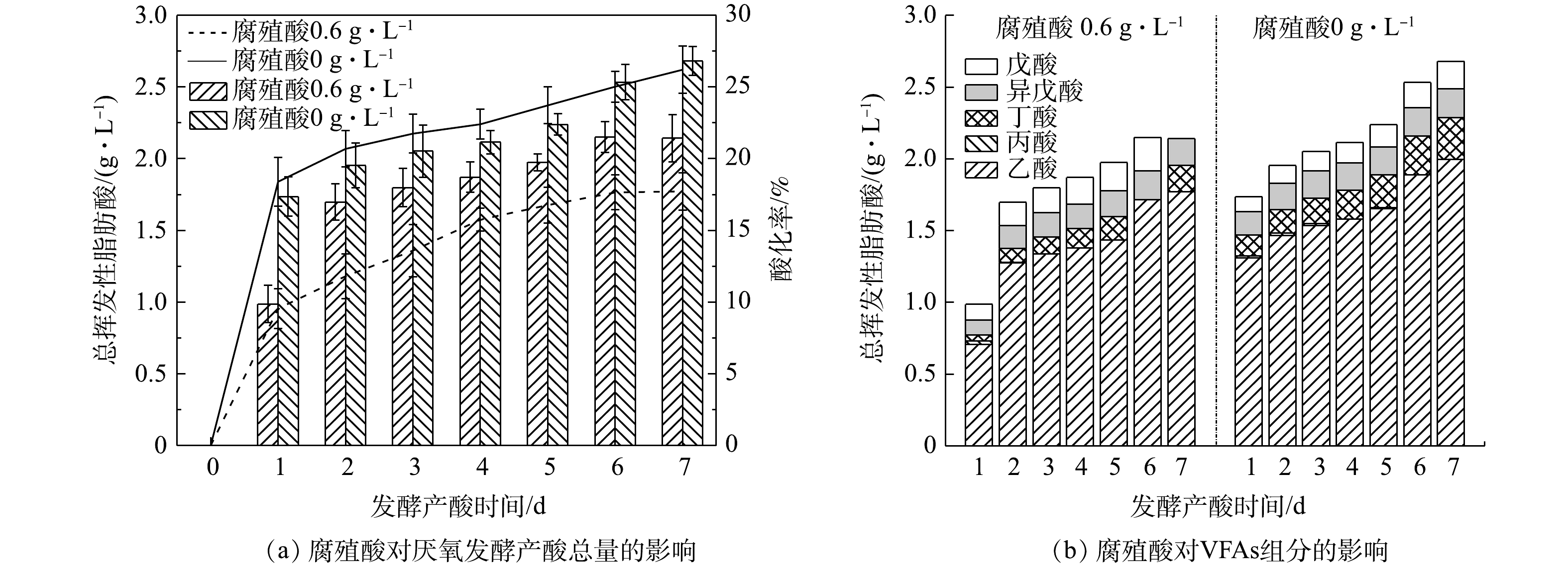
如图2(a)所示,热水解释放的腐殖酸可抑制污泥厌氧发酵产酸;不投加腐殖酸时,产酸酸化率为26.21%;而当腐殖酸质量浓度为0.6 g·L−1时,污泥发酵产酸的酸化率下降至17.72%。但是,如图2(b)所示,腐殖酸对污泥厌氧发酵产VFAs的组成没有明显影响,乙酸仍是VFAs的主要成分。腐殖酸对污泥厌氧消化的影响机理主要包括捆绑作用、电子穿梭作用、微生物调控作用和金属络合作用[7]。由于腐殖酸对总挥发性脂肪酸的组分影响不显著,所以,腐殖酸对微生物群落的组成、代谢途径的影响可能不是主要抑制途径。其次,由于本实验所用污泥中的重金属含量水平较低,因此,腐殖酸对厌氧发酵过程中水解酶的影响可能是主要原因,腐殖酸可与水解酶捆绑,使得酶的结合位点减少、活性下降[20]。
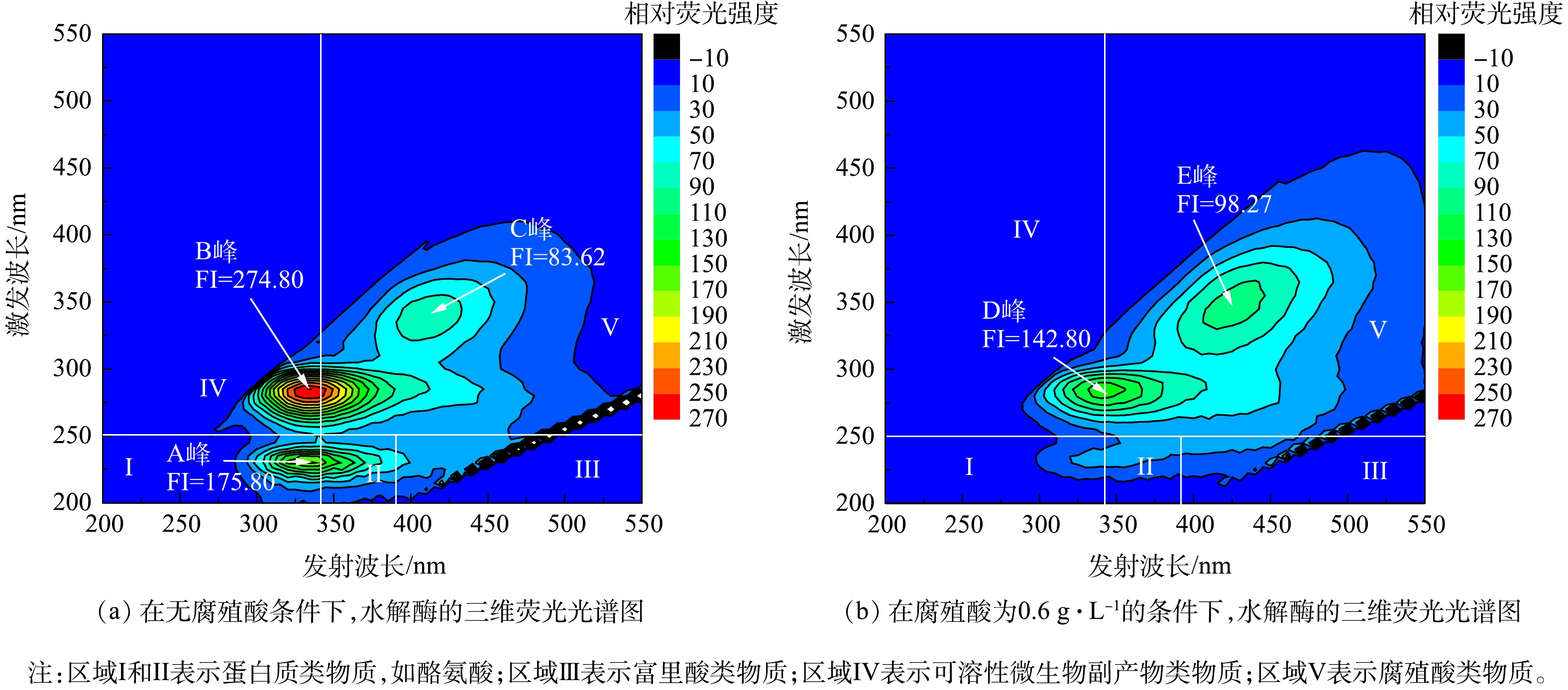
腐殖酸对水解产酸阶段的关键酶具有荧光淬灭作用。荧光淬灭是指由于荧光物质分子与溶剂分子或者其他溶质分子的相互作用,如激发态反应、能量转移、配合物形成和碰撞淬灭而引起荧光强度下降的现象[21]。由图3可知,未添加腐殖酸的实验组中,出现了3个明显的峰,而添加0.6 g·L−1腐殖酸的实验组仅出现了2个峰,原先水解酶所在区域的峰消失。这说明,水解酶所在酪氨酸区域的峰被荧光淬灭。图3(a)中,A峰代表了酪氨酸类物质,水解酶在该区域I存在特定峰;该峰的消失表明腐殖酸分子与水解酶之间存在相互作用,而腐殖酸与水解酶的结合也使酪氨酸基团附近的微环境发生变化[21]。这是因为,腐殖酸会将水解酶包裹在其疏水区域,从而增强了水解酶的极性,这种包裹也有效地减少了细胞外酶活性位点。因此,腐殖酸会导致水解产酸阶段的关键酶发生荧光淬灭反应,减少酶活性位点,从而对厌氧发酵产酸产生抑制作用。
-
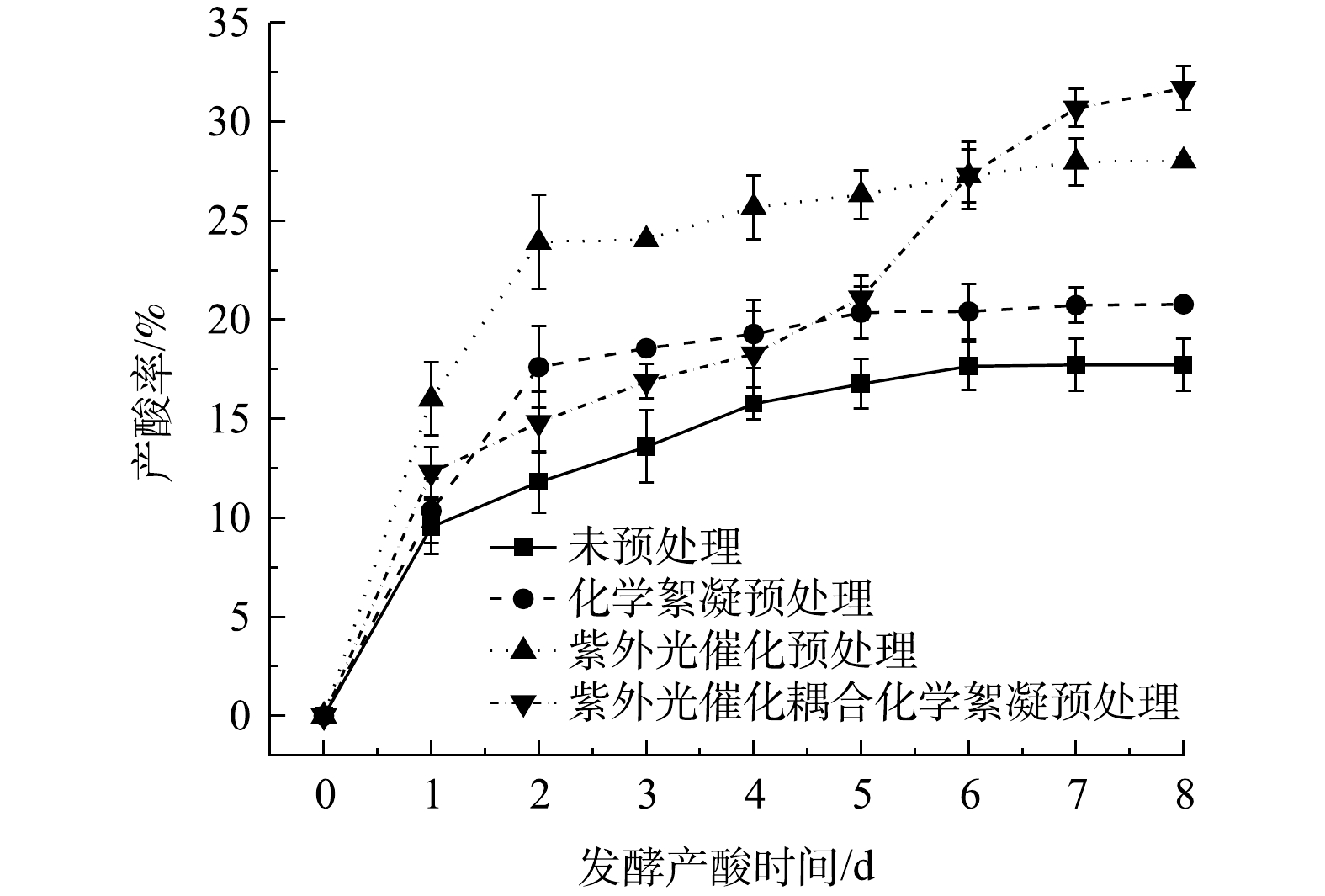
不同预处理方法对缓解腐殖酸抑制污泥厌氧发酵产酸的效果见图4。如图4所示,当腐殖酸质量浓度为0.6 g·L−1时,单独采用紫外光催化技术时,其最终的产酸率为26.96%;单独采用CaCl2絮凝技术时,其最终的产酸率为20.74%;将2种技术耦合,其最终产酸率上升至31.63%。可见,经过2种技术的耦合处理后,前5天的产酸速率并没有明显提升。这是因为,光催化后部分腐殖酸以及有机物被分解为分子量更小的有机物,Ca2+不仅絮凝了腐殖酸,还絮凝水解液中的部分有机小分子,从而导致底物有机物不充足。但是,在振荡过程中,腐殖酸和小分子有机物会出现解絮现象,释放出的腐殖酸已被光催化改性而无毒性作用;而释放出的小分子有机底物被微生物利用,则出现了第5天后产酸速率明显上升的现象[22]。因此,光催化耦合化学絮凝的方法可显著提高污泥液态发酵产酸的效率。
-
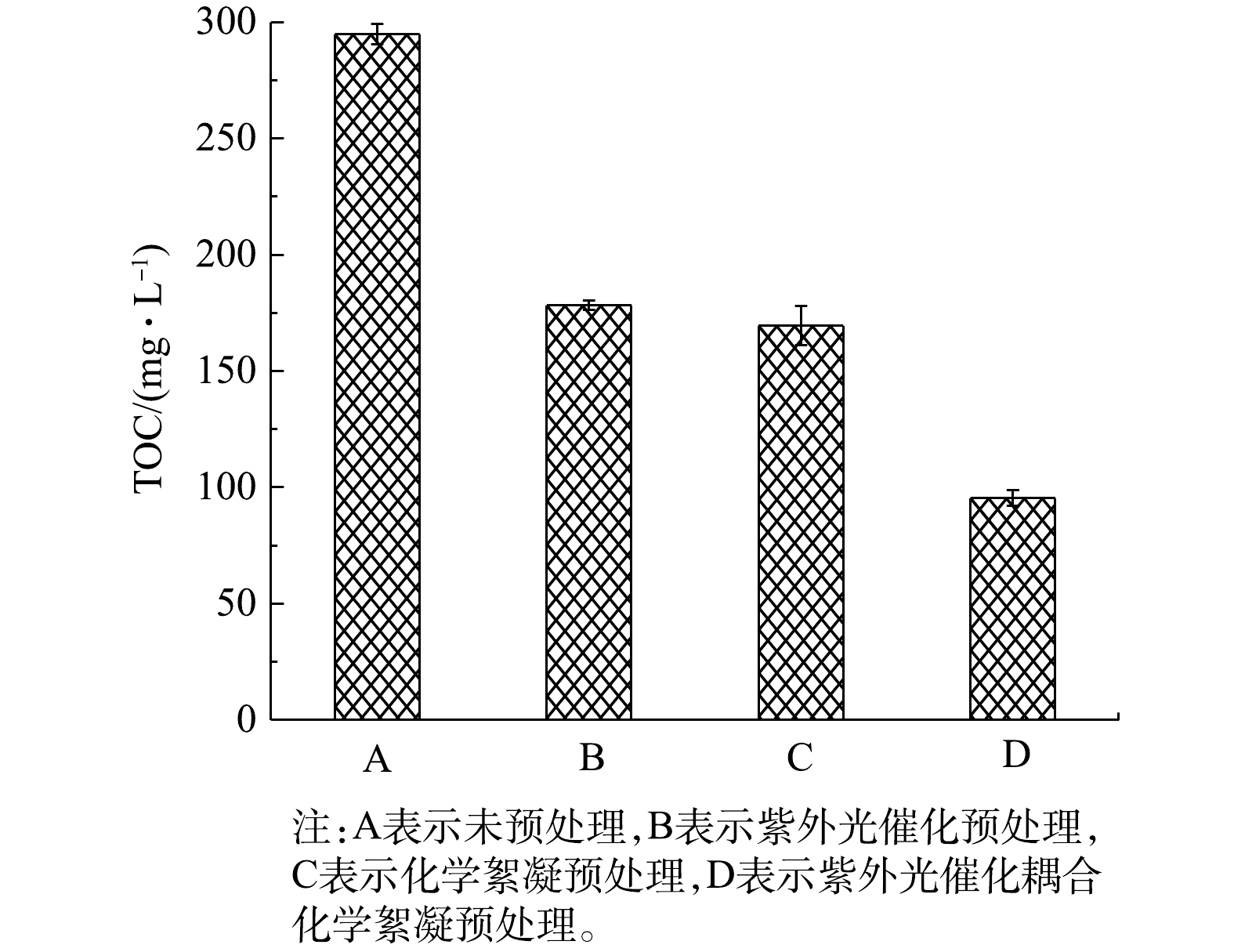
不同预处理方式降低腐殖酸含量的幅度见图5。通过比较腐殖酸对应的TOC值在预处理前后的变化程度,可说明腐殖酸的去除效果和矿化情况[19]。与未预处理相比,3种预处理均降低了腐殖酸的含量。如图5所示,当单独采用紫外光催化处理2 h后,TOC含量可由294.73 mg·L−1降至178.23 mg·L−1,腐殖酸去除率为39.53%。这是因为,腐殖酸经紫外光催化后,激活了其表面的一些活性官能团;部分腐殖酸分子在获得光能后发生矿化反应,有机碳分解为CO2,使得溶液中的有机组分含量降低。而当单独利用CaCl2化学絮凝时,TOC含量降至169.51 mg·L−1,腐殖酸去除率为42.49%。这是因为,Ca2+和腐殖酸之间的内部边界复合物通过静电力和阳离子交换形成Ca(OH)2,Ca2+还可以通过卷扫絮凝和共沉淀与腐殖酸相互作用形成絮凝沉淀物,从而降低了腐殖酸含量[23]。光催化耦合CaCl2化学絮凝处理后,TOC含量降至95.43 mg·L−1,腐殖酸去除率提高至67.62%。这主要是因为,光催化使得一部分腐殖酸发生矿化作用;还有一部分腐殖酸的经过光催化后由大分子分解为小分子结构,暴露出更过羟基结合位点[24],从而与Ca2+形成紧密的絮体颗粒。因此,紫外光催化耦合化学絮凝技术明显促进了溶解性腐殖酸的去除,且有利于缓解其对厌氧发酵产酸的抑制作用。
-
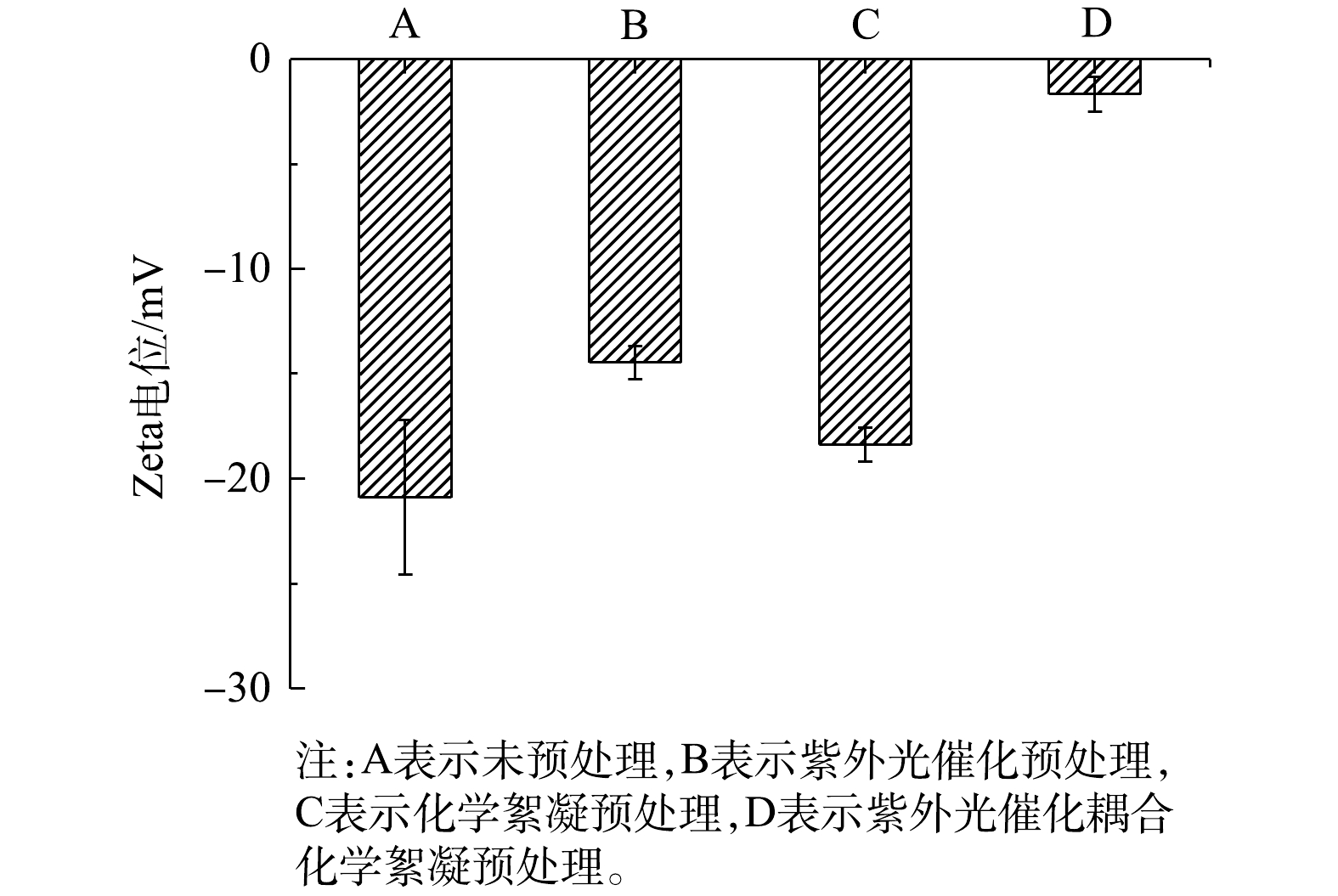
不同预处理方式对腐殖酸胶体Zeta电位的影响见图6。如图6所示,不同方式处理后的腐殖酸Zeta电位发生了不同的变化。与单独采用CaCl2化学絮凝处理相比,单独采用紫外光催化处理腐殖酸的Zeta电位没有显著的差别。这可能因为,光催化导致腐殖酸的大分子结构分解,分解出较多的羧基和羰基等官能团,这些官能团不利于腐殖酸胶体稳定性下降[11]。此外,未经光催化的腐殖酸,其暴露的负电荷游离官能团较少,故Ca2+只能结合部分腐殖酸。但是,经紫外光催化耦合化学絮凝后,腐殖酸胶体的Zeta电位由原本的−20.9 mV上升至−1.76 mV。故可知,紫外光催化耦合化学絮凝可以明显提高腐殖酸胶体的絮凝性能。这说明光催化分解出较多的羧基和羰基等官能团,在Ca2+投入后,发挥了重要的吸附架桥作用[11],从而促进了腐殖酸胶体的絮凝。
-
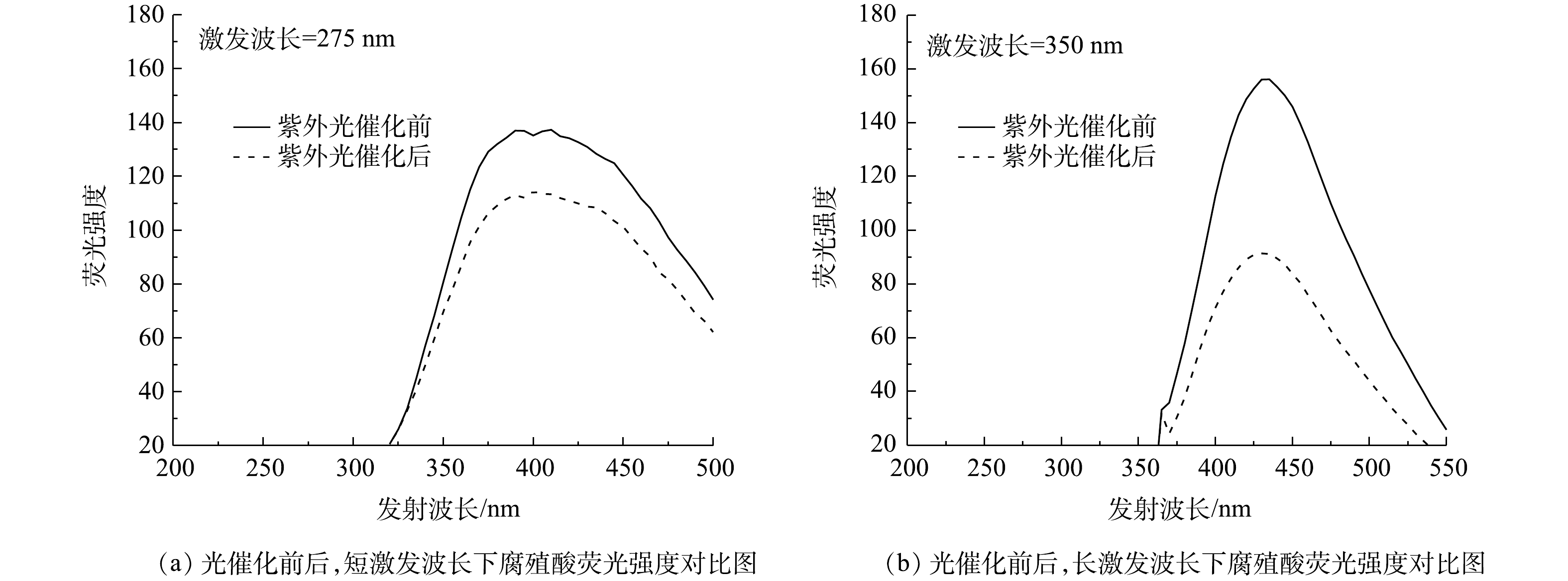
紫外光催化后腐殖酸的芳香缩合度以及分子量大小见图7。由图7可见,紫外光催化可降低腐殖酸的芳香缩合度和分子量。腐殖酸在光催化前后均存在2个特征峰,其激发波长分别为275和350 nm,但光催化后这2个峰的强度均降低。三维荧光的荧光强度与大分子中芳香族化合物的分子量和缩聚程度有关[25]。上述结果表明,紫外光催化降低了腐殖酸的分子量以及芳香缩合度。腐殖酸含有大量的功能官能团,例如醛基、醌基和酮基等,这些不饱和基团在光催化后会发生脱落或者重排,使得醌基含量减少,从而导致芳香缩合度降低[26]。芳香环的数量以及共轭键减少,有利于其由大分子分解为小分子[27]。因此,紫外光催化改变了腐殖酸的结构特征,活性基团的消失和重构降低了其对厌氧发酵产酸的抑制性。
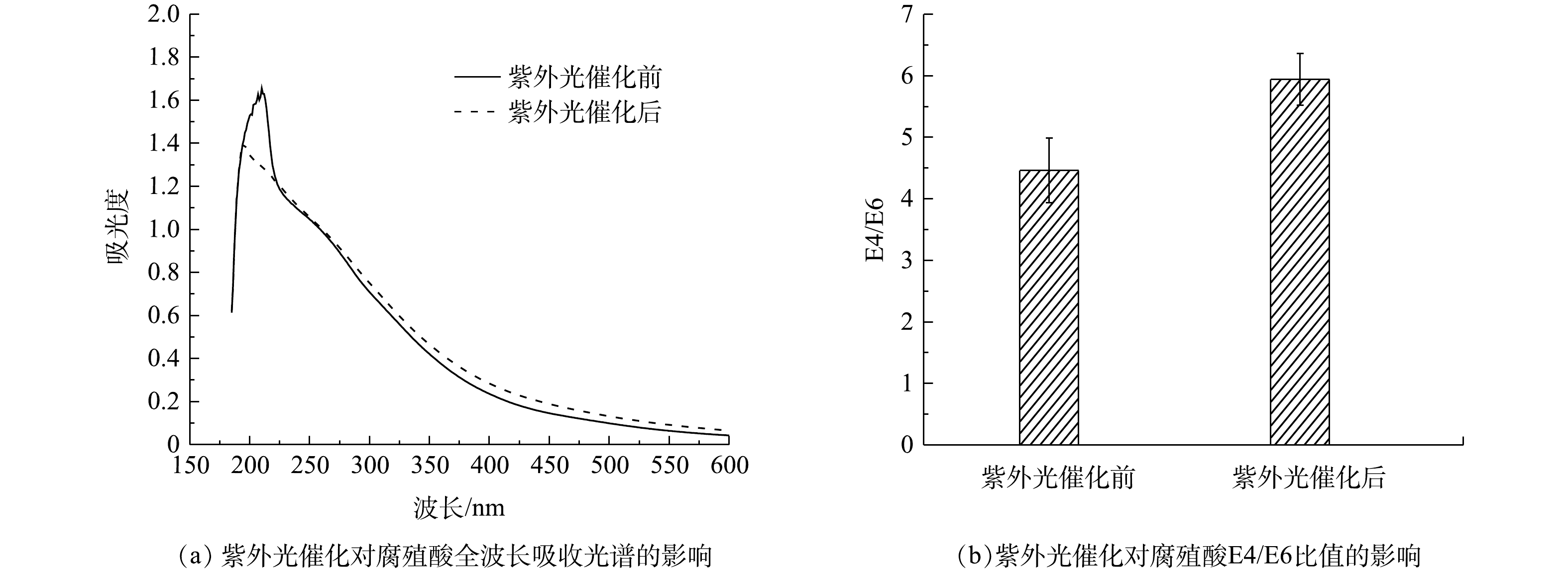
紫外光催化后腐殖酸的电子跃迁能力见图8(a)。由全波长光谱扫描(图8(a))可看出,腐殖酸对能量的吸收主要集中在紫外区。经过紫外光催化的腐殖酸在180~250 nm波长下的光吸收强度明显下降,这代表了其电子跃迁能力的降低[11, 19]。此外,腐殖酸在短波长处吸光度的降低也说明了其电子跃迁能力的减弱,这是芳香碳和共轭基团上的电子转移能力降低造成的[28]。紫外光催化后的腐殖酸在250~600 nm的波长下,各波长下的吸光度都略微上升。这是因为,长波区段中多个大分子的共轭苯环结构发生分解[28],可生成更多小分子助色团,从而降低了腐殖酸的分子量。
紫外光催化后腐殖酸的腐殖化程度、芳香族化合物组分的变化见图8(b)。光催化前腐殖酸的E4/E6值为4.98,光催化后上升为6.01。E4/E6值升高表明了芳香族化合物组分相对减少,而脂肪族化合物组分相对增加,可生物降解的能力提高[29]。这是因为,光催化使腐殖酸的芳香族结构发生裂解,暴露出更多的简单结构组分,例如脂肪族类基团的增加[26]。因此,腐殖酸被光催化后,其芳香缩合度和腐殖化程度降低,其可生物利用性增加,因而削弱了其对厌氧发酵产酸的毒性抑制作用。
2.1. 腐殖酸抑制厌氧发酵产酸
2.2. 不同预处理方式对腐殖酸抑制污泥发酵产酸的缓解效果
2.3. 不同预处理方式下腐殖酸含量的降低幅度
2.4. 不同预处理方式对腐殖酸胶体稳定性的影响
2.5. 紫外光催化对腐殖酸分子结构的影响
-
1)污泥热水解释放的腐殖酸对厌氧发酵产酸有明显抑制作用。当腐殖酸的质量浓度为0.6 g·L−1时,产酸酸化率由对照组的26.21%下降至17.72%。
2)紫外光催化、化学絮凝以及这2者的耦合技术均缓解了腐殖酸对污泥厌氧发酵产酸的抑制作用,且耦合技术的缓解效果最佳,产酸效率可由原来的17.72%上升至31.63%。
3)紫外光催化不仅可以降低腐殖酸的含量,还可改变腐殖酸的结构特性,使得其官能团发生重排或脱落,从而降低了腐殖化程度、芳香缩合度、分子量以及电子跃迁能力,最终提高了腐殖酸的可絮凝性。添加Ca2+有助于降低腐殖酸胶体稳定性,Zeta电位由原本的−20.9 mV上升至−1.67 mV,以达到凝聚状态。



 下载:
下载: