-
废水生物脱氮、防治水体富营养化一直都是水处理方向面临的主要问题之一[1]。传统的生物脱氮方法主要为全程硝化反硝化脱氮。短程硝化作为一种新型生物脱氮工艺,是将硝化反应控制在氨氧化阶段,将亚硝酸盐氧化菌(nitrite oxidizing bacteria,NOB)分离出反应器并将氨氧化菌(ammania oxidizing bacteria,AOB)保留在反应器中,实现氨氮氧化产物为亚硝酸盐的过程[2]。相比传统的全程硝化,短程硝化可以节省25%曝气量和30%的反应时间[3],节约碳源40%[4],具有较低的污泥产量[5]。目前提出的控制短程硝化的影响因素包括游离氨(free ammonia,FA)、游离亚硝酸(free nitrite acid,FNA)、溶解氧(dissolved oxygen,DO)、温度、pH等[6-9]。此外,曝气时间也是实现和维持稳定短程硝化的主要控制因素,曝气时间短导致反应不完全,出水不达标[10];曝气时间过长,短程硝化会转化为全程硝化[11]。因此,维持稳定长久的短程硝化需要综合考虑各种控制因素,以实现对反应过程的综合控制。
除上述影响因素外,盐度也会对生物脱氮处理过程产生影响。有研究表明,低浓度的盐可以促进微生物的生长,盐度过高则会影响细胞的渗透压,导致微生物的活性受到抑制[12]。盐度对微生物虽有毒害作用,但可通过逐步提高盐度或投加耐盐污泥,使微生物适应盐环境,减轻盐度对微生物的抑制作用[13]。HAMODA等[14]研究发现,采用活性污泥法处理高盐废水时,系统生物活性和有机物去除率均有提高;ASIAN等[15]研究表明,一定的盐度对微生物活性有促进作用;徐洁等[16]采用序批式曝气生物滤池工艺处理含海水的污水,发现AOB的耐盐能力高于NOB。因此,可通过添加盐度驯化的方式,抑制NOB的活性,实现短程硝化。短程硝化技术应用前景广泛,但通过活性污泥法进行短程硝化,稳定性较难控制,且硝化细菌本身作为自养菌生长缓慢,非常容易从反应器中流失[17],这都增加了短程硝化工艺运行的困难。
包埋固定化技术通过包埋材料(人工或天然高分子材料)将游离细胞或者酶定位于限定区域,使其保持活性并可反复利用,是一种有效的防止菌体流失、提高反应器内生物量的生物截留手段[18-20]。与活性污泥法相比,包埋固定化技术具有处理效率高、反应易于控制、菌种高纯高效、生物浓度高、固液分离效果好等优点[21]。因此,本研究采用水性聚氨酯(waterborne polyurethane,WPU)为包埋材料制作硝化包埋颗粒,研究盐度及曝气时间对包埋颗粒短程硝化效果的影响,并以盐度为控制因素探究其对连续流短程硝化反应器启动及运行的影响,以期为包埋固定化技术与短程硝化工艺的耦合脱氮提供参考,并为含盐废水的处理提供参考。
-
实验所用硝化污泥取自青岛市某污水处理厂消化池,具有良好的硝化性能。选取一定量的污泥,采用0.1 mol·L−1盐酸进行酸化处理,之后采用去离子水和PBS缓冲溶液各洗3次,以去除污泥中残留的
NH+4 -N,得到水泥复合物。以质量分数计,将10%的WPU与90%的水泥复合物混匀,依次加入10%的四甲基乙二胺,4%的过硫酸钾溶液(KPS)和3%的粉末活性炭,迅速搅拌均匀,约30 min后,混合液凝胶成固态,将固态胶体切割成3 mm×3 mm×3 mm的立方体,得到包埋固定化颗粒。制得的包埋颗粒为黑色,在水中呈均相,具有良好的物理强度和化学稳定性。包埋剂(WPU)和交联剂/引发剂(四甲基乙二胺、KPS)均为分析纯。图1为包埋颗粒的数码照片。 -
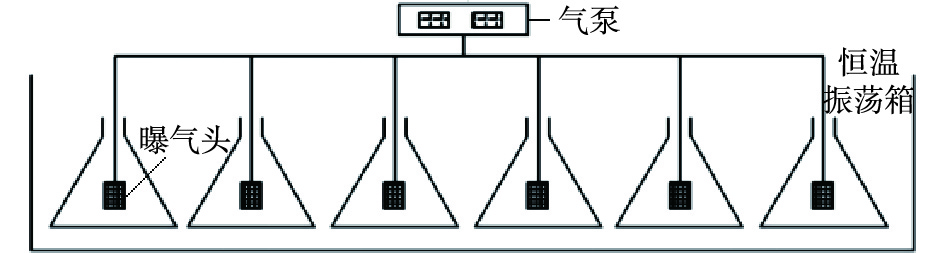
为研究不同盐度对包埋颗粒短程硝化反应过程的影响,采用6个250 mL的锥形瓶作为SBR进行批次实验,图2为实验反应装置。包埋颗粒投加率为10%,初始
NH+4 -N浓度为100 mg·L−1。反应器进水NaCl浓度分别为0、5、10、20、30、50 g·L−1,运行周期为12 h,包括进水5 min,出水5 min。以曝气砂头曝气,曝气量维持为0.1 L·min−1;通过NaHCO3调节pH至7.5~8.0;通过恒温振荡箱,将反应器温度控制在30 ℃。实验采用人工配水。周期结束后,检测出水ρ(NH+4 -N)、ρ(NO−2 -N)和ρ(NO−3 -N),分析氨氮去除率(ηA)、NO−2 -N积累率(RNAR)和硝酸盐积累率(R硝酸盐积累率)的变化情况,以判断不同盐度对短程硝化反应的影响。在SBR反应系统中,继续进行不同曝气时间下的批次实验,运行条件与不同盐度下的批次实验条件相同。每隔2 h取水样,测定一个SBR周期(12 h)内各形态氮(
NH+4 -N、NO−2 -N、NO−3 -N)含量的变化情况,并计算ηA、RNAR和R硝酸盐积累率。ηA、RNAR和R硝酸盐积累率分别按式(1)~式(3)计算。式中:ηA为氨氮去除率;ρ进水(
NH+4 -N)、ρ出水(NH+4 -N)分别为进、出水NH+4 -N浓度,mg·L−1;RNAR为亚硝态氮积累率;ρ出水(NO−2 -N)为出水NO2−-N浓度,mg·L−1;R硝酸盐积累率为硝酸盐积累率;ρ进水(NO−3 -N)、ρ出水(NO−3 -N)分别为进、出水NO3−-N浓度,mg·L−1。 -
实验采用连续流的升流式厌氧污泥床(up-flow anaerobic sludge bed,UASB)反应器,实验装置见图3。反应器由有机玻璃制成,有效容积为5 L,采用下部进水,上部出水的方式。包埋颗粒投加率为10%。反应器上部设有溢流堰,防止包埋颗粒随出水流出。以曝气砂头曝气,维持曝气量为0.1 L·min−1;通过加热棒维持反应器内温度为30 ℃,通过NaHCO3维持pH至7.5~8.0,HRT为8 h。周期结束后,检测出水ρ(
NH+4 -N)、ρ(NO−2 -N)和ρ(NO−3 -N)。 -
实验采用人工模拟废水,
NH+4 -N由NH4Cl提供。主要成分如下:NH4Cl 305 mg·L−1,NaCl 20.5 mg·L−1,KCl 9.6 mg·L−1,NaHCO3 468 mg·L−1,CaCl2·2H2O 9.6 mg·L−1,MgSO4·7H2O 33.6 mg·L−1,NaH2PO4·12H2O 46.4 mg·L−1。微量元素[22]添加量为1 mL·L−1,主要成分下:FeSO4·7H2O 1 g·L−1,MnCl2·4H2O 0.2 g·L−1,CuSO4·5H2O 0.1 g·L−1,CoCl2·6H2O 0.3 g·L−1,H3BO3 0.2 g·L−1,ZnSO4·7H2O 0.2 g·L−1,NiCl2·6H2O 0.2 g·L−1。 -
NH+4 -N:纳氏试剂分光光度法;NO−2 -N:N-(1-萘基)-乙二胺分光光度法;NO−3 -N:麝香草酚分光光度法[23];DO:JPBJ-608便携式溶解氧测定仪;pH:PHS-3C pH计。 -
取25 mL成功启动短程硝化反应器的包埋颗粒于250 mL锥形瓶中,加入模拟废水。以NH4Cl配制不同浓度的
NH+4 -N溶液,其余组分同表1模拟废水成分。将锥形瓶放入30 ℃恒温振荡培养箱中,120 r·min−1振荡培养。pH为7.5~8.0,维持曝气量为0.1 L·min−1,间隔8 h,取样测定水中NH+4 -N浓度,对包埋颗粒的基质动力学进行分析。 -
不同盐度对包埋颗粒短程硝化的影响。以硝化污泥制作包埋颗粒,按填充率10%投入反应器中。通过批次实验研究不同盐度对包埋颗粒短程硝化反应的影响,反应器进水
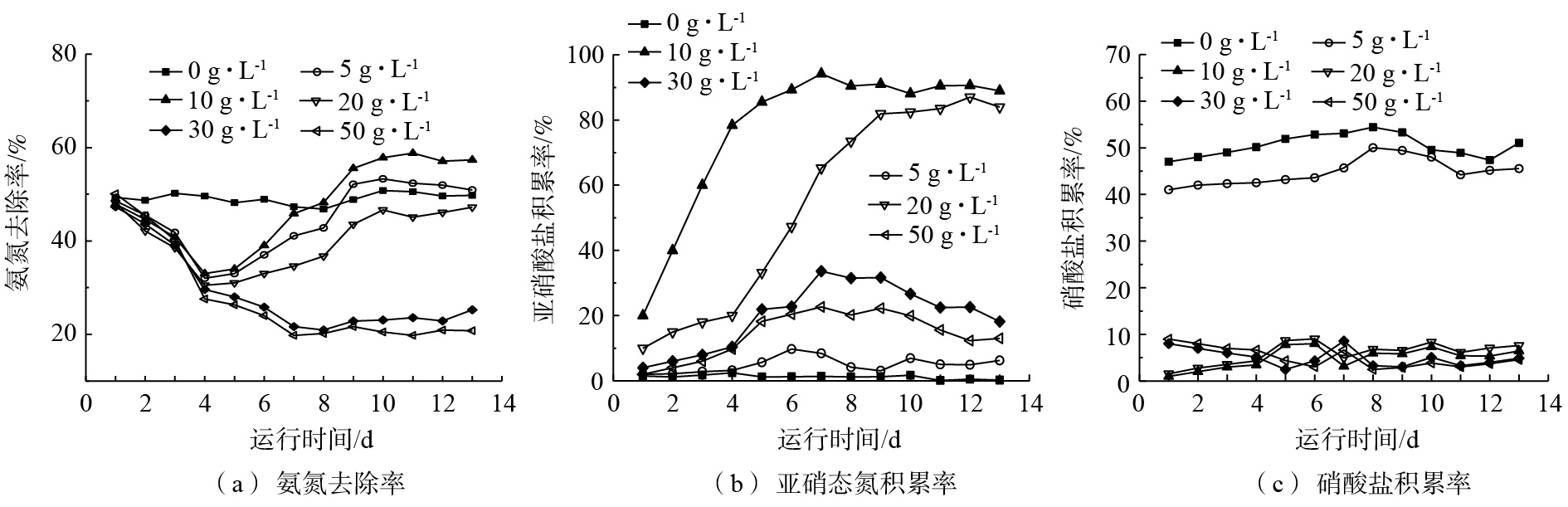
NH+4 -N浓度为100 mg·L−1,NO−2 -N和NO−3 -N浓度均为0 mg·L−1。图4为不同盐度系统中ηA、RNAR和R硝酸盐积累率的变化。向锥形瓶中投加NaCl后,ηA及RNAR均受到不同程度的影响。由图4(a)可知,由于NaCl的突然加入,系统内的微生物活性出现了短暂的下降,分析认为,可能是微生物不能马上适应在盐环境下生长,活性受到抑制。此时ρ(NaCl)为0 g·L−1的系统中ηA最高。运行一段时间后,包埋颗粒系统中的微生物开始适应盐环境。这可能是由于在长时间的选择与淘汰中,包埋颗粒系统中不能适应有盐环境的微生物受到抑制,能适应环境的菌群通过不断调节已经从被迫改变到积极适应[24],成为优势菌群[25],使处理效果有了进一步提高。从第4天开始,ρ(NaCl)为5 g·L−1和10 g·L−1的系统中,ηA开始呈现上升趋势,并分别在第9天和第8天超过ρ(NaCl)为0 g·L−1的系统;随着反应器的持续运行,ηA逐渐趋于稳定。其中ρ(NaCl)为0 g·L−1时,ηA始终维持在45%以上;ρ(NaCl)为5 g·L−1系统中,ηA在第9天后稳定在50%左右,ρ(NaCl)为10 g·L−1系统中,ηA在稳定运行后维持在55%以上;ρ(NaCl)为20 g·L−1的系统中,ηA也存在上升趋势,但低于0 g·L−1的系统;而ρ(NaCl)为30 g·L−1和50 g·L−1系统中,高盐环境使AOB和NOB的活性被抑制,氨氮去除受到影响,稳定运行后ηA仅为20%左右。
由图4(b)和图4(c)可知,ρ(NaCl)为0 g·L−1和5 g·L−1系统的RNAR基本为0%,而R硝酸盐积累率可达到40%以上,系统中的
NH+4 -N基本都经过硝化反应由NO−2 -N转化为NO−3 -N,为全程硝化反应。ρ(NaCl)为10 g·L−1系统中,RNAR呈现逐步上升的趋势,经过6 d的运行之后,RNAR达到90%,而R硝酸盐积累率趋于0%。ρ(NaCl)为20 g·L−1的系统中,RNAR稳定后可达到80%以上。ρ(NaCl)为30 g·L−1和50 g·L−1系统中,RNAR较低,且出水NO−3 -N浓度基本为0 g·L−1,表明系统内NOB的活性受到了抑制,不能完成将NO−2 -N氧化为NO−3 -N的过程。由此可见,盐度可作为脱氮系统中脱氮种群的抑制剂,在长期运行条件下,NOB菌群的活性被抑制,实现AOB菌群的优化,使短程硝化过程得以实现;但是盐度过高也会抑制AOB的活性。在不同的盐度条件下,AOB和NOB受到的抑制程度不同;在相同的盐度条件下,AOB比NOB有更强的耐盐性。叶柳[26]通过微生物计数实验(MPN法)发现,虽然盐度对AOB和NOB都有抑制作用,但2种菌群对盐度的适应能力不同,AOB的耐盐能力要强于NOB;雷中方[27]通过实验证明,废水中含盐量的增加,可能导致微生物的正常代谢功能遭到破坏;CUI等[28]的研究表明,无机盐对NOB有较强的抑制能力,可以通过向普通废水中投加无机盐实现短程硝化。通过分析可知,当盐度超过10 g·L−1时,NOB的活性受到抑制;超过20 g·L−1时,盐度的升高使细胞渗透压增大[29],不利于细胞内底物和氧的传递,导致AOB的活性也受到抑制。因此,10 g·L−1 NaCl浓度下短程硝化效果较好,可作为包埋系统短程硝化反应器的启动盐度。
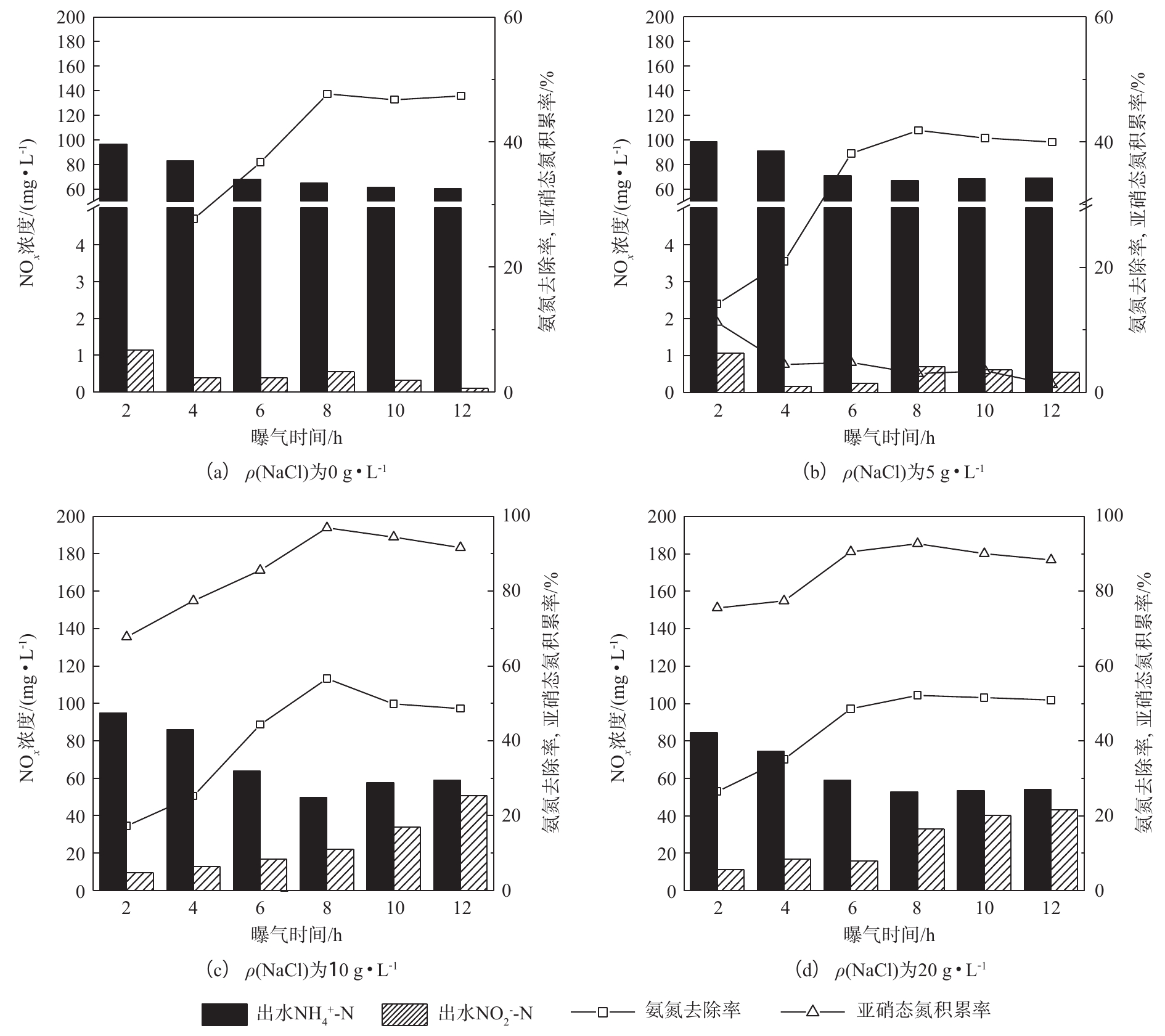
曝气时间对包埋颗粒短程硝化稳定性的影响。通过控制盐度运行短程硝化反应器后,继续进行批次实验,研究曝气时间对包埋颗粒短程硝化稳定性的影响。测得系统中不同曝气时间下各系统出水三氮浓度、ηA和RNAR的变化,如图5所示。实验进水 NH+4 -N浓度为100 mg·L−1,曝气量为0.1 L·min−1,系统内DO浓度小于1 mg·L−1。由分析可知,ρ(NaCl)超过20 g·L−1时AOB和NOB活性均受到抑制,系统短程硝化效果受到影响,因此,ρ(NaCl)为30 g·L−1和50 g·L−1系统不再进行稳定性实验。由图5可见,ρ(NaCl)为0 g·L−1的系统中,ηA呈现先上升后下降的趋势,曝气时间为8 h时达到最大值47%,随后开始下降;RNAR随曝气时间的增加而下降,基本趋于0%。ρ(NaCl)为5 g·L−1时,ηA在8 h时达到最大值41%,而RNAR仅为3.04%。ρ(NaCl)为10 g·L−1,曝气时间为8 h时系统的短程硝化效果最好,此时系统出水ρ(
NH+4 -N)为42 mg·L−1,ηA可达到56%;出水ρ(NO−2 -N)为50 mg·L−1,RNAR达到96%。ρ(NaCl)为20 g·L−1时,ηA和RNAR分别在曝气时间为8 h时达到50%和90%,短程硝化效果低于ρ(NaCl)为10 g·L−1的系统。由图5可知,各系统在不同曝气时间下包埋颗粒短程硝化的效果是不同的。进水ρ(NaCl)为10 g·L−1,曝气时间为8 h时RNAR最高,短程硝化稳定性最好。虽然在低DO环境下,AOB对氧的亲和力大于NOB,但当曝气时间超过8 h时,NOB会逐渐适应低氧环境,且大量
NO−2 -N的存在为NOB提供了基质[30]。如不控制曝气时间,NO−2 -N会在NOB的作用下向NO−3 -N转化,导致RNAR下降,短程硝化转化为全程硝化。因此,维持短程硝化反应需要保持一定的曝气时间,以实现NO−2 -N的积累。 -
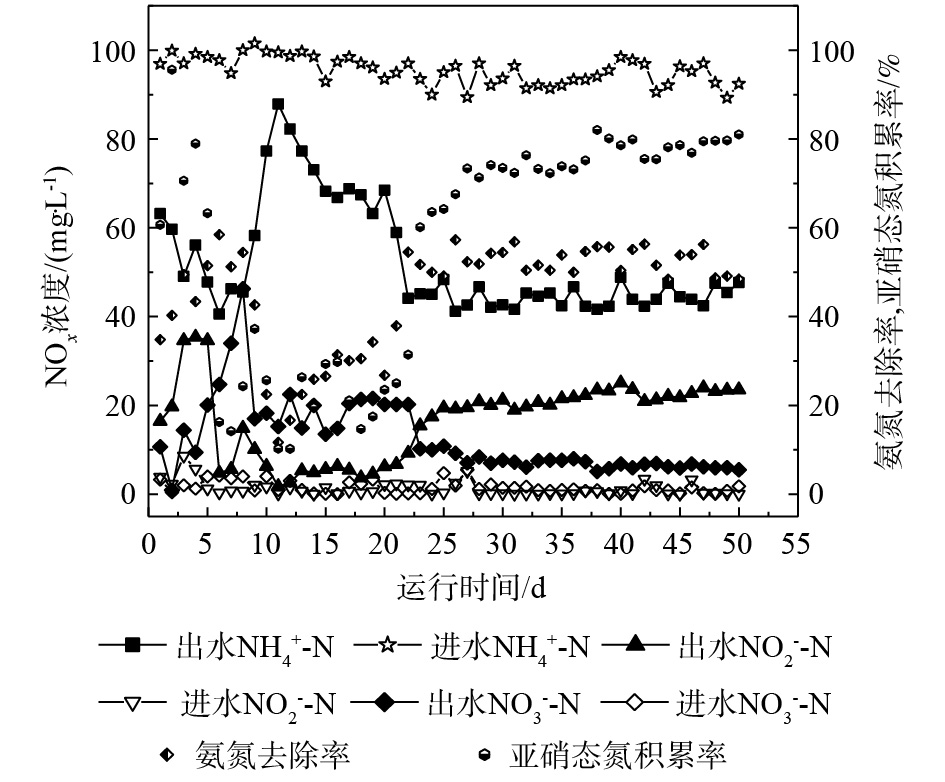
由批次实验可知,10 g·L−1 NaCl浓度可用于启动包埋颗粒短程硝化反应器。图6为连续流UASB反应器运行期间进、出水中
NH+4 -N、NO−2 -N、NO−3 -N的浓度变化。进水NH+4 -N浓度为100 mg·L−1,NO−2 -N和NO−3 -N浓度均为0 mg·L−1。可以看出,包埋颗粒从第1天开始就出现NH+4 -N的去除,ηA为34.82%,表现出良好的性能。但系统的短程硝化效果不稳定,第11天时,ηA仅达到11.70%,原因可能是,包埋颗粒在反应器内分布不均匀,导致出水水质受到影响。第15天向系统内投加10 g·L−1 NaCl,经过一段时间的盐度驯化后,包埋颗粒开始适应盐环境。第20天开始,出水中ρ(NH+4 -N)明显降低,并逐渐趋于稳定,ηA可稳定在50%以上。出水中ρ(NO−2 -N)从第20天开始逐渐升高,RNAR由第11天的10.25%增加到第50天的81.03%。由此可见,NaCl的加入抑制了NOB的活性,使NO−2 -N转化为NO−3 -N的过程受到影响,出水中ρ(NO−2 -N)升高而ρ(NO−3 -N)逐渐降低,RNAR增大。由分析可知,10 g·L−1 NaCl的加入初步实现了连续流UASB包埋颗粒短程硝化反应器的启动。盐度对短程硝化反应的影响在目前研究中的结果并不一致,就现有的研究[31]看,不同的工艺类型以及接种的生物来源(盐度驯化种群、非盐度驯化种群、或者耐盐种群)和处理废水类型(在大多数研究中采用人工配水)可能是造成目前研究很不一致的重要因素。王淑莹等[25]采用全程硝化反硝化研究SBR工艺的脱氮效果发现,7.5 g·L−1的NaCl浓度可以作为活性污泥系统短程硝化反硝化的启动盐度;一定浓度的NaCl盐度可以作为一种化学抑制剂实现对硝化菌的选择性抑制。崔有为等[32]的实验结果表明,采用MUCT工艺处理低含盐量的生活污水,在不超过8 g·L−1的盐度环境内,生物可以实现良好的处理效率,亚硝酸盐积累明显;叶柳等[24]在使用MUCT工艺处理含盐生活污水时,稳定盐度在10 g·L−1后,在好氧段实现了高的亚硝酸盐积累,从而通过回流至缺氧段实现了短程脱氮。由此可见,在不同的运行工艺条件下,盐度对短程硝化反应会造成不同的影响。此外,有研究[32]表明,不同功能菌群对盐度耐受能力与盐度实施的选择作用有关,不同种属的微生物或不同功能的微生物耐盐能力有差异,这种差异表现在应对盐度抑制时不同的调节能力上。
-
选用成功启动短程硝化反应器的包埋颗粒,在10 g·L−1盐度、8 h的曝气时间下进行动力学实验,以测定包埋颗粒的基质动力学特性。包埋颗粒的短程硝化动力学过程受
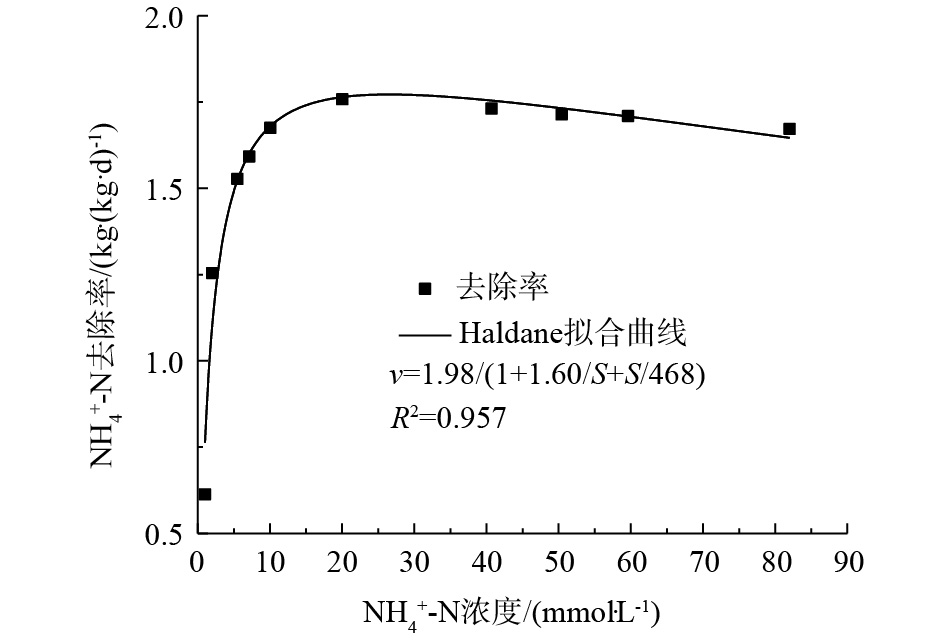
NH+4 -N浓度的限制,在处理过程中,高氨氮环境会形成较高浓度的游离氨(FA)[33]。FA是AOB的生长基质,高浓度FA会对AOB的氨氧化过程产生抑制;且NOB对FA有潜在的适应性,在反应器运行后期,FA对NOB的抑制会大幅降低[34]。因此,研究NH+4 -N对包埋颗粒短程硝化的基质抑制特性有利于进一步强化短程硝化效果。假设在实验过程中氨氧化菌细胞数量不发生变化,且反应器内始终处于完全混合状态,那么可用Haldane模型[35]对包埋颗粒短程硝化的动力学特性进行描述,其计算公式见式(4)。式中:v为反应速率,kg·(kg·d)−1;vmax为最大反应速率,kg·(kg·d)−1;S为基质浓度,mmol·L−1;Km为半速率常数,mmol·L−1;Ki为半抑制常数,mmol·L−1。实验测得,包埋颗粒短程硝化速率与基质浓度的对应关系见表1。
通过origin软件,以Haldane模型对表1中实验数据进行非线性拟合,得到包埋颗粒对NH4+-N的动力学方程。由基质浓度降解曲线,计算出包埋颗粒的最大氨反应速率(SAA-
NH+4 -N)[36]。由图7可知,包埋颗粒最大氨反应速率(SAA-NH+4 -N)为1.98 kg·(kg·d)−1,对氨的半速率常数为1.60 mmol·L−1,氨的半抑制常数为468 mmol·L−1,R2为0.957,表现出良好的相关性。较高的反应速率可以促进基质的转化,而包埋颗粒对氨的半速率常数较小,表明其对基质的亲和力较大,利于短程硝化反应的进行[18]。因此,10 g·L−1盐度系统中的包埋颗粒具有优良的动力学特性,有助于短程硝化反应器的高效运行。 -
1)研究表明,盐度对包埋颗粒短程硝化反应器的启动存在一定的影响。在NaCl浓度为10 g·L−1的盐度系统中,硝化污泥包埋颗粒的ηA和RNAR最高,分别可达到55%和90%,成功实现了包埋颗粒的短程硝化反应;控制曝气时间可以保证包埋颗粒短程硝化过程的稳定运行,进水ρ(NaCl)为10 g·L−1,曝气时间为8 h时系统的短程硝化效果最好,ηA可达到56%,RNAR达到96%。
2)在NaCl浓度为10 g·L−1,曝气时间为8 h的条件下可实现包埋颗粒UASB反应器的初步启动,ηA和RNAR分别可达到50%和80%以上;基质动力学研究表明,包埋颗粒对氨氮的动力学特性符合Haldane基质抑制动力学模型,包埋颗粒具有优良的动力学特性。此项研究可为含盐废水的氨氮处理提供参考。
盐度和曝气时间对包埋颗粒短程硝化启动的影响及其动力学分析
Effect of salinity and aeration time on the start-up of partial nitrification of immobilized particles and its kinetics analysis
-
摘要: 针对短程硝化反应器启动时间长、效果不稳定等问题,使用水性聚氨酯(WPU)制作硝化污泥包埋颗粒,利用SBR设置盐度梯度以及不同曝气时间进行批次实验,启动短程硝化;通过控制最佳反应条件启动UASB短程硝化反应器,同时进行动力学分析。结果表明:在批次实验过程中,随着盐度的增加,氨氮去除率(ηA)及
NO−2 -N积累率(RNAR)先上升后下降。当NaCl浓度为10 g·L−1时,短程硝化效果最佳,ηA为55%,RNAR为90%;不同曝气时间对短程硝化的稳定性有较大的影响,曝气时间为8 h时短程硝化效果最稳定,ηA和RNAR分别达到56%和96%。控制NaCl浓度为10 g·L−1,HRT为8 h,成功实现了UASB短程硝化反应器的启动;包埋颗粒对氨氮的动力学特性符合Haldane基质抑制动力学模型,具有优良的动力学特性。研究可为包埋颗粒与短程硝化工艺的耦合脱氮提供参考,并为含盐废水的处理提供技术支持。Abstract: In view of the long start-up time and unstable effect of partial nitrification reactor, waterborne polyurethane (WPU) was used to prepare the immobilized particles of nitrification sludge. The partial nitrification was started up through batch tests in the SBR reactor at different salinity gradients and different aeration times. The UASB partial nitrification reactor was started up by controlling the optimum conditions, and the kinetic analysis was performed simultaneously. The results showed that the ammonia nitrogen removal rate (ηA) andNO−2 -N accumulation rate (RNAR) increased firstly and then gradually decreased as the salinity increased in batch tests. The partial nitrification effect reached the best when the NaCl concentration was 10 g·L−1, and ηA and RNAR were 55% and 90%, respectively. Different aeration time had a great influence on the stability of partial nitrification. The partial nitrification effect was the most stable when the aeration time was 8 h, and ηA and RNAR reached 56% and 96%, respectively. The UASB reactor was successfully started up by controlling the NaCl concentration at 10 g·L−1 and HRT at 8 h. The kinetics of the immobilized granules on ammonia nitrogen was in accordance with the Haldane matrix inhibition kinetics model, which indicated that the immobilized granules had excellent kinetic characteristics. The study can provide a reference for the coupling denitrification of immobilized granules and partial nitrification processes, and provide technical support for saline wastewater treatment.-
Key words:
- immobilized granules /
- partial nitrification /
- salinity /
- start-up /
- aeration time /
- kinetic analysis
-
表 1 基质浓度对短程硝化反应的影响
Table 1. Effect of substrate concentrationon partial nitrification
水样序号 NH+4 -N浓度 /(mmol·L−1)NH+4 -N去除/(kg·(kg·d)−1)1 1 0.613 2 2 1.254 3 5.5 1.527 4 7.14 1.592 5 10.07 1.675 6 20.04 1.758 7 40.71 1.731 8 50.42 1.714 9 59.64 1.709 10 82 1.672 -
[1] 李凌云, 彭永臻, 吴蕾, 等. 短程硝化颗粒污泥的培养与特性分析[J]. 土木建筑与环境工程, 2010, 32(3): 119-123. doi: 10.11835/j.issn.1674-4764.2010.03.021 [2] 赵梦月, 彭永臻, 王博, 等. SBR工艺实现长期稳定的部分短程硝化[J]. 化工学报, 2016, 67(6): 2525-2532. [3] ISANTA E, REINO C, CARRERA J, et al. Stable partial nitritation for low-strength wastewater at low temperature in an aerobic granular reactor[J]. Water Research, 2015, 80: 149-158. doi: 10.1016/j.watres.2015.04.028 [4] GE S J, WANG S Y, YANG X, et al. Detection of nitrifiers and evaluation of partial nitrification for wastewater treatment: A review[J]. Chemosphere, 2015, 140: 85-98. doi: 10.1016/j.chemosphere.2015.02.004 [5] 侯爱月, 李军, 卞伟, 等. 不同短程硝化系统中微生物群落结构的对比分析[J]. 中国环境科学, 2016, 36(2): 428-436. doi: 10.3969/j.issn.1000-6923.2016.02.019 [6] GARRIDO J M, VANBENTHUM W A, VANLOOSDRECHT M C, et al. Influence of dissolved oxygen concentration on nitrite accumulation in a biofilm airlift suspension reactor[J]. Biotechnology and Bioengineering, 1997, 53(2): 168-178. doi: 10.1002/(ISSN)1097-0290 [7] CIUDAD G, GONZALEZ R, BORNHARDT C, et al. Modes of operation and pH control as enhancement factors for partial nitrification with oxygen transport limitation[J]. Water Research, 2007, 41(20): 4621-4629. doi: 10.1016/j.watres.2007.06.036 [8] 张小玲, 彭党聪, 王志盈. 传统与短程反硝化的影响因素及特性研究[J]. 中国给水排水, 2002, 18(9): 1-3. doi: 10.3321/j.issn:1000-4602.2002.09.001 [9] GUO J H, PENG Y Z, HUANG H J, et al. Short- and long-term effects of temperature on partial nitrification in a sequencing batch reactor treating domestic wastewater[J]. Journal of Hazardous Materials, 2010, 179(1/2/3): 471-479. [10] 彭永臻, 杨岸明, 李凌云, 等. 短程硝化最优曝气时间控制与硝化种群调控[J]. 哈尔滨工业大学学报, 2013, 45(2): 101-105. doi: 10.11918/j.issn.0367-6234.2013.02.018 [11] 吴煌州, 邱凌峰, 陈益明, 等. 不同曝气量对短程硝化特性的影响[J]. 福州大学学报(自然科学版), 2014, 42(1): 161-166. doi: 10.7631/issn.1000-2243.2014.01.0161 [12] LI X, YUAN Y, YUAN Y, et al. Effects of salinity on the denitrification efficiency and community structure of a combined partial nitritation- anaerobic ammonium oxidation process[J]. Bioresource Technology, 2018, 249: 550-556. doi: 10.1016/j.biortech.2017.10.037 [13] 张晓玲. 盐度对SBR和SBBR工艺短程硝化反硝化的影响[D]. 青岛: 中国海洋大学, 2015. [14] HAMODA M F, AL-ATTAR M S. Effects of high sodium chloride concentrations on activated sludge treatment[J]. Water Science and Technology, 1995, 31(9): 61-72. doi: 10.2166/wst.1995.0345 [15] ASLAN S, SIMSEK E. Influence of salinity on partial nitrification in a submerged biofilter[J]. Bioresource Technology, 2012, 80: 24-29. [16] 徐洁, 熊小京, 郑天凌, 等. 序批式曝气生物滤池处理含海水污水中的硝化性能[J]. 环境工程学报, 2015, 9(3): 1062-1066. doi: 10.12030/j.cjee.20150312 [17] 陈光辉, 李军, 邓海亮, 等. 热冲击法实现包埋活性污泥稳定亚硝化[J]. 四川大学学报(工程科学版), 2015, 47(5): 196-202. [18] 陈光辉, 李军, 邓海亮, 等. 包埋菌启动厌氧氨氧化反应器及其动力学性能[J]. 化工学报, 2015, 66(4): 1459-1466. [19] CHEN Y, LIU Q G, ZHOU T, et al. Ethanol production by repeated batch and continuous fermentations by saccharomyces cerevisiae immobilized in a fibrous bed bioreactor[J]. Journal of Microbiology and Biotechnology, 2013, 23(4): 511-517. doi: 10.4014/jmb [20] DONG Y M, ZHANG Z J, JIN Y W, et al. Nitrification characteristics of nitrobacteria immobilized in waterborne polyurethane in wastewater of corn-based ethanol fuel production[J]. Journal of Environmental Sciences, 2012, 24(6): 999-1005. doi: 10.1016/S1001-0742(11)60893-0 [21] 李尧, 张振家, 方海军. 包埋固定化微生物工艺技术处理高氨氮化工废水[J]. 净水技术, 2012, 31(3): 32-35. doi: 10.3969/j.issn.1009-0177.2012.03.008 [22] STROUS M, GERVEN E V, ZHENG P, et al. Ammonium removal from concentrated waste streams with the anaerobic ammonium oxidation (anammox) process in different reactor configurations[J]. Water Research, 1997, 31(8): 1955-1962. doi: 10.1016/S0043-1354(97)00055-9 [23] 张倩, 王淑莹, 苗圆圆, 等. 间歇低氧曝气下CANON工艺处理生活污水的启动[J]. 化工学报, 2017, 68(1): 289-296. [24] 叶柳, 彭永臻, 崔有为, 等. 革新MUCT工艺处理含盐污水[J]. 北京工业大学学报, 2006, 32(12): 1087-1092. doi: 10.11936/bjutxb2006121087 [25] 王淑莹, 唐冰, 叶柳, 等. NaCl盐度对活性污泥系统脱氮性能的影响[J]. 北京工业大学学报, 2008, 34(6): 631-635. doi: 10.11936/bjutxb2008060631 [26] 叶柳. 含盐生活污水脱氮除磷的特性及优化控制[D]. 北京: 北京工业大学, 2010. [27] 雷中方. 高浓度钠盐对废水生物处理系统的失稳影响综述[J]. 工业水处理, 2000, 20(4): 6-9. doi: 10.3969/j.issn.1005-829X.2000.04.002 [28] CUI Y W, PENG Y Z, GAN X Q, et al. Achieving and maintaining biological nitrogen removal via nitrite under normal conditions[J]. Journal of Environmental Sciences, 2005, 17(5): 794-797. [29] SANCHEZ O, MARTI M C, ASPE E, et al. Nitrification rates in a saline medium at different dissolved oxygen concentrations[J]. Biotechnology Letters, 2001, 23(19): 1597-1602. doi: 10.1023/A:1011977629398 [30] 张昭, 李冬, 仲航, 等. 常温下低氨氮污水的短程硝化启动研究[J]. 中国给水排水, 2012, 28(9): 35-39. doi: 10.3969/j.issn.1000-4602.2012.09.009 [31] YE L, PENG C Y, TANG B, et al. Determination effect of influent salinity and inhibition time on partial nitrification in a sequencing batch reactor treating saline sewage[J]. Desalination, 2009, 246(1/2/3): 556-566. [32] 崔有为, 彭永臻, 李晶. 盐度抑制下的MUCT处理效能及其微生物种群变化[J]. 环境科学, 2009, 30(2): 488-492. doi: 10.3321/j.issn:0250-3301.2009.02.030 [33] 李芸, 熊向阳, 李军, 等. 膜生物反应器处理晚期垃圾渗滤液亚硝化性能及其抑制动力学分析[J]. 中国环境科学, 2016, 36(2): 419-427. doi: 10.3969/j.issn.1000-6923.2016.02.018 [34] 胡晓娜, 戴晓虎, 曹达文, 等. 限氧条件下亚硝化的稳定运行及动力学[J]. 化工进展, 2015, 34(12): 4198-4202. [35] 许晓毅, 尤晓露, 吕晨培, 等. 包埋固定化活性污泥脱氮特性与微生物群落分析[J]. 环境科学, 2017, 38(5): 2052-2058. [36] 唐崇俭, 熊蕾, 王云燕, 等. 高效厌氧氨氧化颗粒污泥的动力学特性[J]. 环境科学, 2013, 34(9): 3544-3551. 期刊类型引用(2)
1. 黄旭敏. 膜生物反应技术在环境工程污水处理中的应用. 造纸装备及材料. 2024(01): 125-127 .  百度学术
百度学术
2. 单明娥,李辉. 膜生物反应污水处理技术对水质优化的影响研究. 能源与环保. 2024(10): 159-164+170 .  百度学术
百度学术
其他类型引用(0)
-









 下载:
下载: