-
近年来,在西方部分国家大麻合法化的冲击下,大麻逐渐成为全球范围内使用最广的成瘾性物质. 《2021年中国毒情形势报告》[1]指出,北美地区大麻向我国输入大幅增加,涉及我国23个省份. 因此,对我国大麻滥用情况进行准确评估愈加重要. 由于毒品犯罪的特殊性和隐蔽性,传统意义上的精神活性物质调查方法较难获得准确的吸毒人员情况,污水流行病学凭借便捷、客观和实时监测等优势在毒情研判领域起到了愈加重要的作用[2 − 3]. 利用污水验毒技术评估大麻滥用情况时,常以大麻植物中的主要精神活性成分四氢大麻酚(tetrahydrocannabinol, THC)的生物代谢物四氢大麻酸(tetrahydrocannabinoic acid, THC-COOH)作为目标检测物[4 − 6]. 但由于THC-COOH是THC人体代谢后的产物,检测结果仅反映了被人体吸收代谢后的部分,忽略了通过非生物代谢等其他方式进入水环境中的部分[7],因此采用THC-COOH作为生物标志物评估大麻使用人群、追溯大麻来源时存在一定的偏差. THC、大麻酚(cannabinol, CBN)和大麻二酚(cannabidiol, CBD)是大麻植物中的三种主要活性成分[8 − 10],经人体吸食、代谢后随尿液进入污水处理系统或自然环境中,以THC、CBN和CBD作为目标物质进行大麻使用评估可能更具有代表性.
生活污水是从居民住户、公共设施和工厂的厨房、浴室、卫生间和洗衣房等生活设施中排放的废水. 人们日常生活中消费的烟草[11]、药物[12]、个人护理用品[13],以及瘾君子吸食精神活性物质后[14 − 15],其中的有效成分和代谢产物也通过生活污水排放到环境中. 因此,未处理的生活污水中也记载着这些物质的消费量等重要信息,成为污水流行病学的主要信息载体. 但精神活性物质及其代谢产物的输入一定程度上会改变水质的稳定状态,另一方面,水质参数又一定程度上影响着精神活性物质及其代谢产物的稳定性[16 − 18]. 也就是说,污水中精神活性物质及其代谢产物的稳定性与污水水质参数存在着密切联系,因此,测定生活污水中的COD、NH3-N、TP、TN、pH等基本水质参数,并研究它们与THC、CBN、CBD和THC-COOH稳定性的关系,有助于对生活污水中上述目标物进行更准确的定量分析.
本研究选取青岛市某污水处理厂的生活污水样品为研究基质,为提高污水验毒工作的准确性,采用标准加入法,研究避光和光照条件下,18 h内生活污水加标样中THC、CBN和CBD的稳定性;探究加标后样品24 h内THC、CBN、CBD和THC-COOH的浓度变化,并同步监测前述基本污水水质参数的变化情况,通过多元线性回归及相关性分析研究目标物在生活污水中的稳定性与水质参数的关系,为准确定量目标物提供依据.
-
本研究所用主要仪器设备包括:Qtrap
5500 plus型液相色谱-质谱联用仪(美国 AB SCIEX公司);SPE固相萃取仪(SUPELCO公司);12通道氮吹仪(杭州奥盛仪器有限公司);XW-80A涡旋混合器(上海精科实业有限公司);DR2800型分光光度计、DR200型消解仪(美国 HACH 公司);SHZ-D(Ш)循环水式多用真空泵(巩义市予华仪器有限责任公司);0.22 μm有机相针式滤器(上海安谱实验科技股份有限公司).主要耗材和试剂包括:Oasis MCX固相萃取小柱(美国Waters公司);氨氮试剂盒(0—50 mg·L−1)、COD试剂盒(20—
1500 mg·L−1)和TN试剂盒(0—150 mg·L−1)(美国HACH 公司);总磷试剂盒(江苏盛奥华环保科技有限公司);标准品储备液THC-COOH(1 mg·mL−1)、THC (100 μg·mL−1)、CBN (1 mg·mL−1)和CBD (1 mg·mL−1)以及氘代内标储备液THC-D3、CBN-D3、CBD-D3(均为1 mg·mL−1)(美国Cerilliant公司);甲酸铵(分析纯,国药集团化学试剂有限公司);甲醇、二氯甲烷、甲酸(液相色谱级,J&K百灵威公司). 所有大麻素类物质标准品及氘代内标均经山东省禁毒委员会备案,严格按照公安部门的要求管理使用. -
不同滥用药物在不同污水环境中稳定性存在较大差异,通常可以通过添加杀菌剂抑制生物活性以降低被生物降解的可能性,如加入浓盐酸调节水样至pH = 2等,经滤膜过滤后根据目标物的理化性质选择合适的存储条件. 但对于大麻素类物质及其主要生物代谢产物而言,酸性条件下更容易吸附到悬浮颗粒物上[3, 19],在冷冻条件下可以稳定存储大约1个月[3]. 因此,生活污水自山东省青岛市某污水处理厂采集后,不酸化样品,直接冷冻避光保存. 水样中THC、CBN、CBD和THC-COOH的初始浓度均为未检出(低于检出限).
-
THC、CBN、CBD前处理方法:冷冻的样品取出经室温化冻后使用. 向50 mL水样中添加50 μL浓度为200.00 μg·L−1 THC-D3、CBN-D3、CBD-D3内标混合溶液,以1—2 mL·min−1的流速过Oasis MCX萃取柱(经6 mL甲醇和4 mL纯水活化平衡)富集,富集后真空抽干多余水分,萃取柱用6 mL甲醇进行洗脱,洗脱流速小于1 mL·min−1,收集洗脱液,在低于40 ℃的氮气流下吹至近干,用200 μL甲醇复溶样品,涡旋40 s,经0.22 μm有机相尼龙膜过滤后低温避光保存,待测. 对THC-COOH前处理时,除了不使用0.22 μm有机相尼龙膜过滤外,其他流程与上述一致.
-
本研究采用QTRAP Enabled Triple Quad
5500 plus + 型液相色谱-质谱联用仪检测目标物,色谱柱为Kinetex 2.6u BiphenyLC(100 mm × 2.1 mm). -
流动相分别为2 mmol·L−1甲酸铵 + 1‰甲酸超纯水溶液(A相),甲醇(B相),流速为0.3 mL·min−1, 进样2 μL. 流动相洗脱梯度见表1.
质谱扫描模式为MRM扫描,离子源为电喷雾离子源(ESI),气帘气(CUR)为30 psi,碰撞气(CAD)为9 psi,离子化电压(IS)为
5500 V,温度(TEM)为550 ℃,离子化模式为ESI(+),喷雾气1为(GS1)55 psi,喷雾气2为(GS2)60 psi,THC、CBN和CBD及其相应内标的母离子和定性、定量离子的质荷比(m/z)及相应质谱参数见表2. -
流动相分别为5 mmol·L−1甲酸铵 + 0.75‰甲酸超纯水溶液(A相),1‰甲酸乙腈(B相),流速为0.3 mL·min−1,进样2 μL,流动相洗脱梯度见表3. 质谱扫描模式为MRM扫描,离子源为电喷雾离子源(ESI),气帘气(CUR)为35 psi,碰撞气(CAD)为9 psi,离子化电压(IS)为-
4500 V,温度(TEM)为500 ℃,喷雾气1为(GS1)50 psi,喷雾气2为(GS2)50 psi,THC-COOH的母离子和定性、定量离子的质荷比(m/z)及相应质谱参数见表2. -
THC、CBN和CBD采用内标法定量. 移取适量THC、CBN和CBD及其氘代内标的标准溶液,甲醇稀释为300.00、250.00、200.00、150.00、100.00、50.00、25.00、12.50、6.25、3.13、1.56 ng·mL−1混合标准工作液. 将配制好的标准工作液按浓度从低到高的顺序,按照“1.4.1”中的仪器分析条件依次上机测试.
THC-COOH采用外标法定量. 移取适量THC-COOH标准工作溶液,甲醇稀释为浓度分别为250.00、200.00、100.00、50.00、25.00、10.00、5.00、2.50、1.00、0.50、0.10 ng·mL−1的标准工作液,按浓度从低到高的顺序,按照“1.4.2”的仪器分析条件上机测试. 线性回归方程见表4. 结果表明,THC、CBN和CBD在1.56 — 300.00 ng·mL−1范围内、THC-COOH在0.10 — 250.00 ng·mL−1范围内,R2均大于0.99,线性关系良好.
为保证数据质量,本研究采取了严格的质量控制与保障(QA/QC)手段,主要包括:现场空白(以超纯水为空白)、全过程程序空白、空白加标和基质(污水样品)加标实验. 加标实验设置低(40.00 ng·L−1)、中(200.00 ng·L−1)、高(800.00 ng·L−1)的3个浓度梯度. 每10组样品各添加一组空白质控(仅加入氘代内标)和阳性质控(加入定量的混合标准溶液(200.00 ng·L−1)和对应内标).
所有现场空白、全过程程序空白、空白质控样均未检测到目标物(低于检出限),阳性质控样的目标物回收率在80.8% — 102.2%之间;4种目标物THC、CBN、CBD和THC-COOH的空白加标回收率分别为101.2% — 116.4%、93.7% — 116.5%、97.6% — 111.1%和102.3% — 109.9%,基质加标回收率依次分别为79.9% — 118.7%、98.8% — 118.7%、82.1% — 117.6%和112.5% — 118.6%. 这些结果表明,采样、样品前处理和分析检测过程以及所用试剂均不存在目标物污染,加标回收率满足痕量有机物质的分析要求(70% — 120%之间),且仪器在整个分析过程中处于持续良好的工作状态.
-
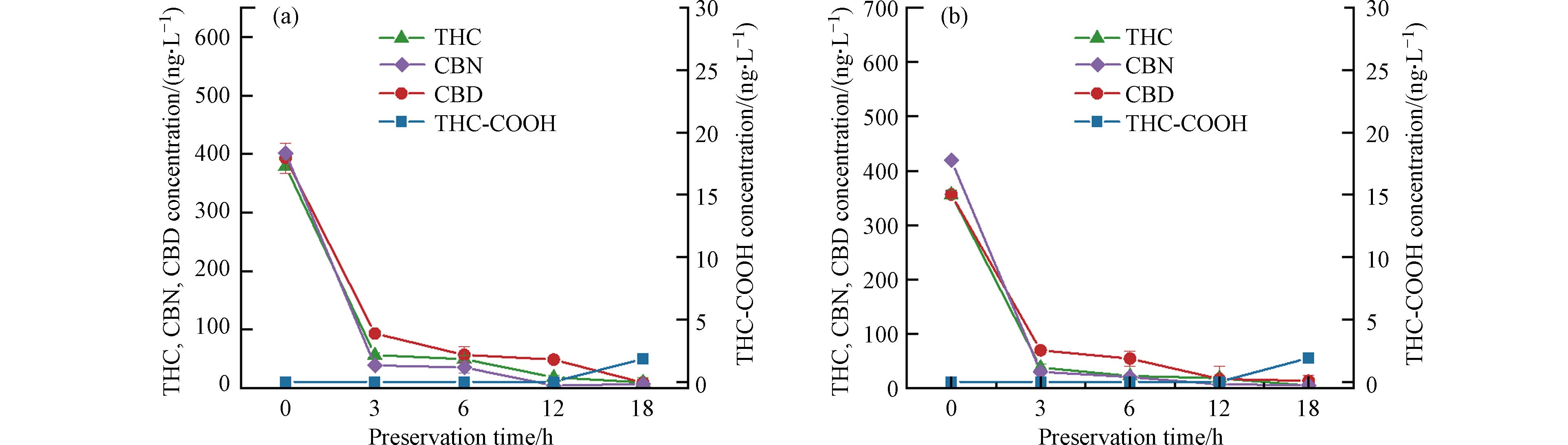
取50 mL生活污水样品,经检测水样中THC、CBN、CBD和THC-COOH的浓度均为未检出(低于检出限,记为0.00 ng·L−1). 向水样中添加THC、CBN和CBD混合标准物,目标物初始质量浓度为400.00 ng·L−1,常温避光和光照下保存18 h后进行分析,结果如图1所示. 可以看到,污水中添加THC、CBN和CBD后,随着存储时间的延长,无论避光或光照条件,均会生成一定量的THC-COOH(18 h时样品中的检测浓度分别为1.86 ng·L−1和1.92 ng·L−1),且随存储时间的增加,THC-COOH的浓度均呈增加趋势. Heuett等[20]认为,毒品在暴露于人体或自然环境中时,可通过水解、还原和氧化等Ⅰ期反应,引入—OH、—NH2、—SH、—COOH等官能团;How等[21]认为,THC在污水中可能会降解产生THC-COOH. 本实验水样中含量较低的THC-COOH有可能为THC在生活污水中通过引入羧基官能团生成.
为更直观地描述THC、CBN和CBD在生活污水中的降解,本研究利用去除率(按式1计算)来表征目标物的浓度变化. 去除率随保存时间的变化如表5所示.
式中,
Ri 表示目标物的去除率,%;Cini 为目标物的初始浓度,ng·L−1;Cfin 表示在存储不同时间后的目标物浓度的平均值,ng·L−1.结果表明,光照条件下THC、CBN和CBD的去除率均高于避光条件下,说明光照一定程度上会加快THC、CBN和CBD在生活污水环境中的降解,这与孙维来[22]、杨雨[23]等的结果一致. 他们认为光照是影响大麻素类降解的重要因素. 因此样品测试前避光保存有助于更准确地定量THC、CBN和CBD.
Boix等的研究结果[24]表明,在自然环境中光照条件下,大麻素类物质除了生成THC-COOH外,还能通过羟基化反应和环己酸环上的去甲基化等反应生成C20H26O6、C21H28O6、C20H28O6、C9H13O4、C9H15O4等物质.
-
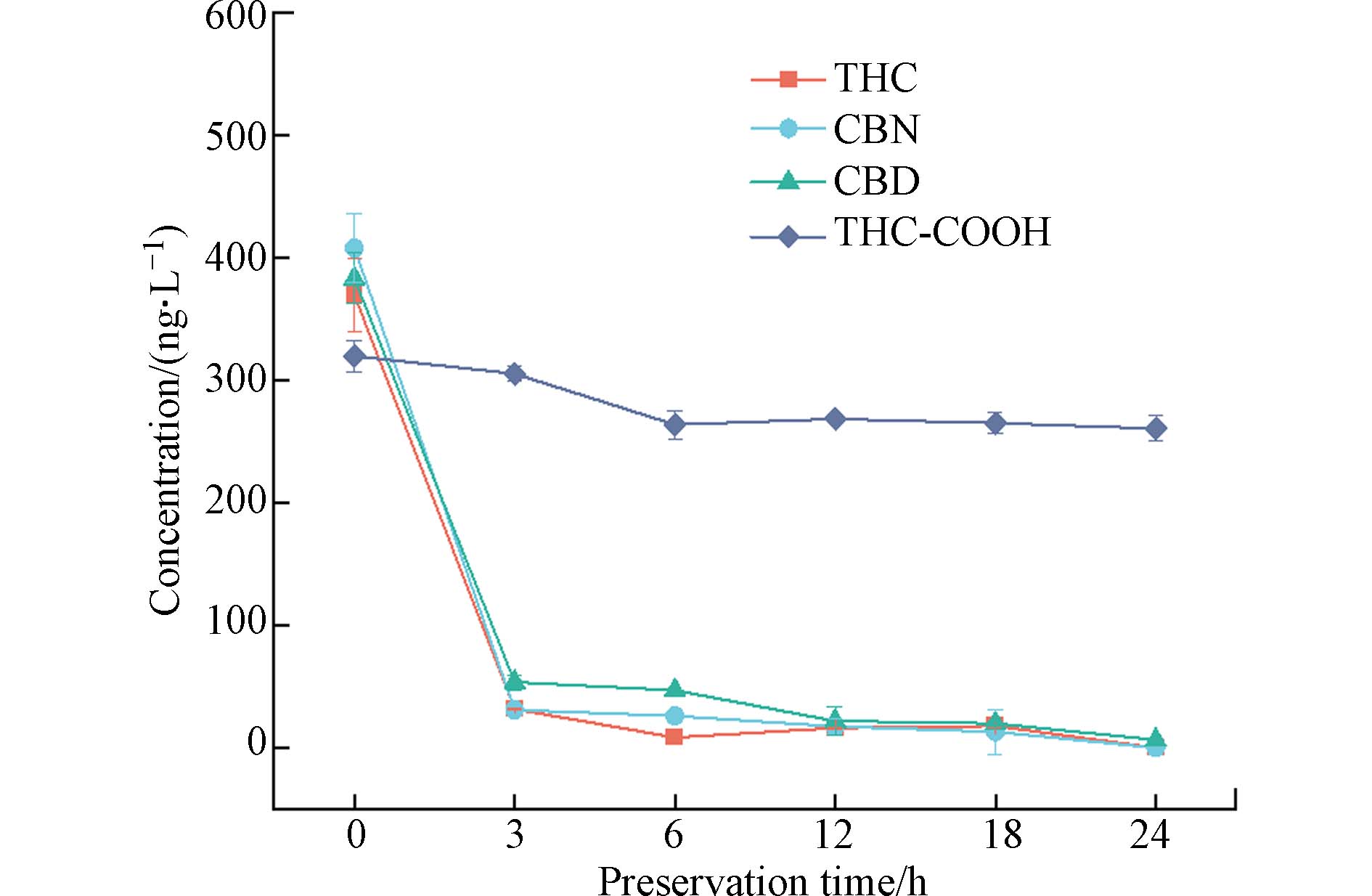
随着样品保存时间延长,无论避光或光照条件下生活污水加标样(加THC、CBN或CBD)中均有THC-COOH生成;为避免在稳定性研究中产生相互影响,将THC、CBN和CBD与THC-COOH作为两个独立体系进行研究. 分别向水样中加入THC、CBN和CBD混合标准工作溶液以及THC-COOH标准溶液,目标物初始质量浓度均为400.00 ng·L−1,常温避光保存0、3、6、12、18、24 h后进行分析. 24 h内目标物浓度变化如图2,去除率(按式1计算)结果见表6.
由图2和表6可知,避光条件下生活污水中THC、CBN、CBD和THC-COOH的检出浓度均随存储时间的延长而降低. THC、CBN和CBD的去除速度快,存储3 h后去除率分别达到了92.09%、92.27%和86.61%,24 h时THC和CBN已被完全去除,CBD去除率为98.39%. 即THC、CBN和CBD在生活污水中稳定性较差,一方面可能与污水中的微生物丰富,促进了目标物降解有关,另一方面由于大麻素具有低水溶性,易被吸附在颗粒物上而沉积到沉积物(污泥)中[21],这与Carmona等[25]在沉积物中检测到THC浓度为42.00 ng·g−1,而在同一地点的水样中未检测到THC的研究结果一致. THC-COOH在生活污水中的降解较慢,24 h内去除率维持在20.13% — 34.86%之间,稳定性高于THC、CBN和CBD. 因此,对生活污水进行大麻滥用评估时,以THC-COOH作为目标分析物,并在24 h内完成测试为佳.
-
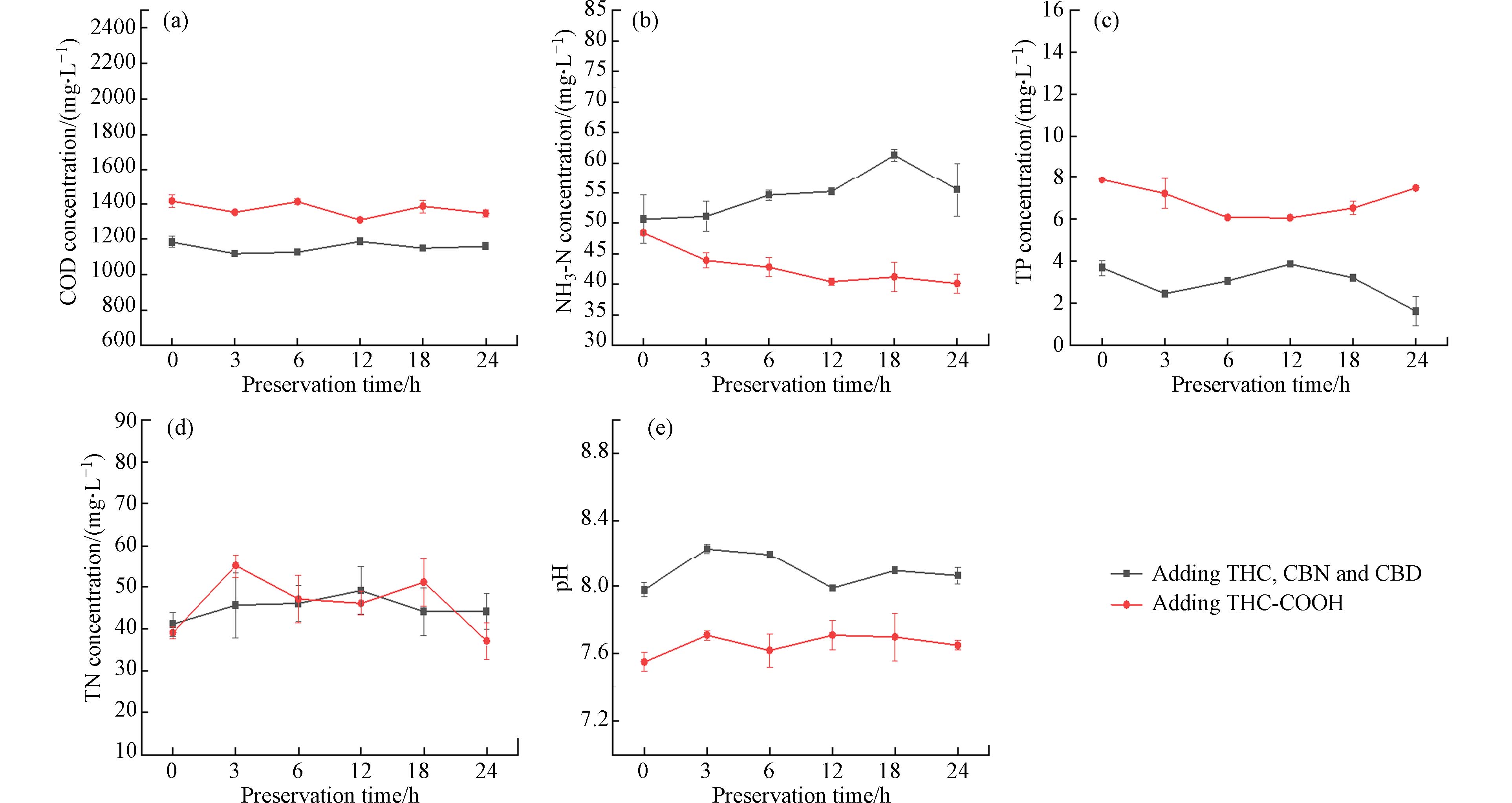
向生活污水中加入目标物质后,水样中COD、NH3-N、TP、TN浓度和pH值变化趋势如图3所示. 由图3可知,生活污水中加入THC、CBN和CBD后,24 h内COD、TP浓度随存储时间增加先降低后升高再降低,NH3-N浓度逐渐升高,TN浓度和pH值先升高后降低. 加入THC-COOH后,COD浓度随存储时间增加先降低后升高再降低,NH3-N浓度逐渐降低,TP浓度先降低后升高,TN浓度在37 — 55 mg·L−1范围内波动,pH值先升高后降低.
为确定生活污水中THC、CBN和CBD以及THC-COOH稳定性与存储时间(t)、水质参数之间的关系,本研究采用逐步分析法,对生活污水样品保存过程中自变量(t、COD、NH3-N、TP、TN浓度和pH)与因变量(THC、CBN、CBD和THC-COOH去除率)进行多元线性回归. 共线性诊断结果表明,自变量的VIF值均小于10,不存在多重共线性,可进行多元线性分析. 通过SPSS statistics软件计算确定回归方程(如式 (2) — 式 (5)),方差分析结果如表7所示. 所有回归模型的R2大于0.89,P值低于0.05,说明拟合的方程具有统计意义,且存储时间、COD浓度、NH3-N浓度等自变量可以较好地解释生活污水中THC、CBN、CBD和THC-COOH去除率的变化规律.
生活污水加标样品中目标物去除率的多元线性回归方程分别为:
其中,自变量X1、X2、X3、X4、X5和X6分别为存储时间/h、COD浓度/(mg·L−1)、NH3-N浓度/(mg·L−1)、TP浓度/(mg·L−1)、TN浓度/(mg·L−1)和pH值(无计量单位),μ为随机误差.
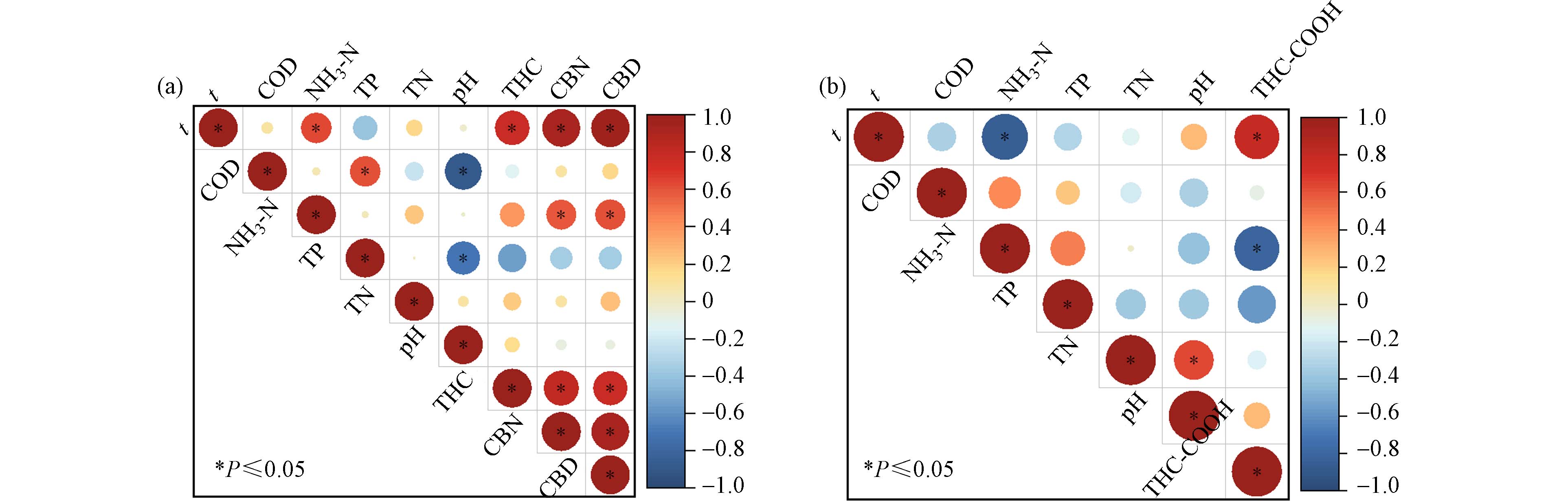
运用Origin使用Spearman相关绘制相关性热图,如图4所示. 在P ≤ 0.05的置信水平上,THC去除率与t(r = 0.78)具有正相关性,CBN、CBD去除率均与t(r分别为0.93、0.96)和NH3-N(r分别为0.59、0.61)存在正相关性,相关性强弱为t > NH3-N,THC-COOH去除率与t(r = 0.79)具有正相关性,与NH3-N(r = −0.80)存在负相关性,相关性强弱为NH3-N > t. 这表明t对上述四种目标物去除率均有较大的影响,NH3-N对CBN、CBD和THC-COOH去除率影响较大,说明硝化作用对生活污水中目标物稳定性具有重要作用[26].
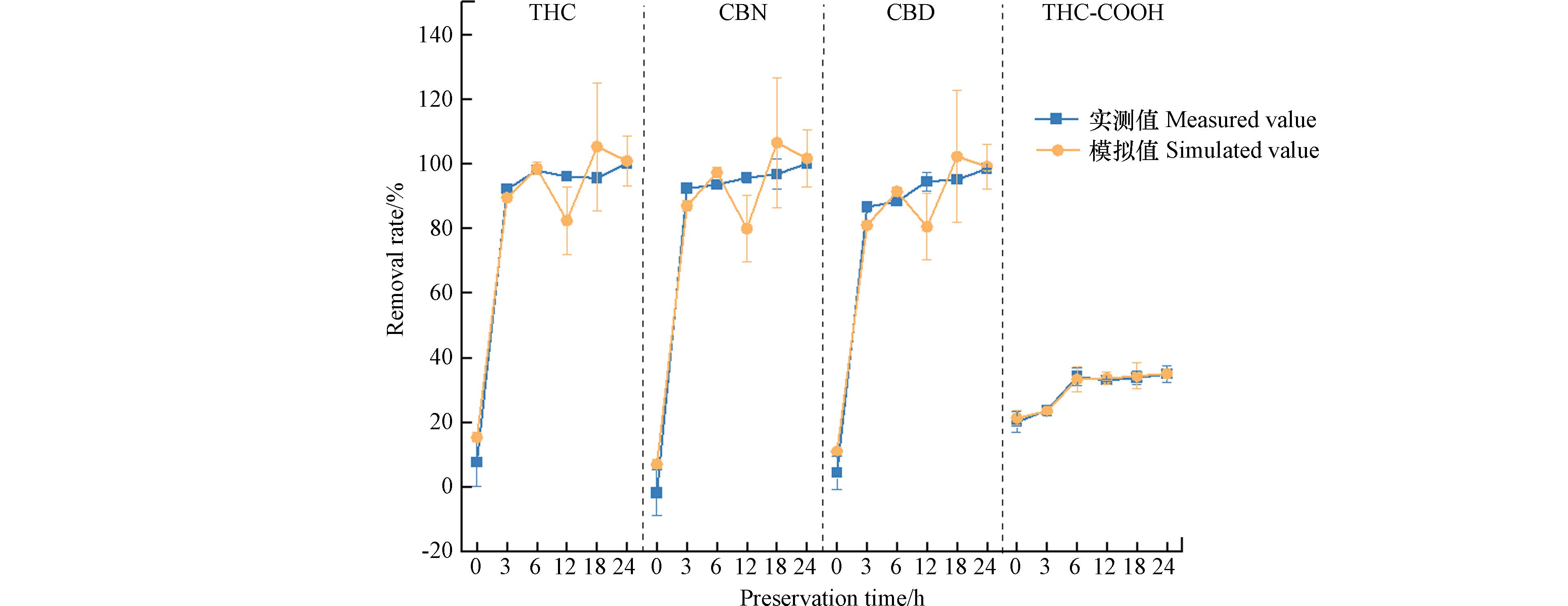
实测值与模型值的比较如图5所示. 运用自变量由模型得出的四种目标物去除率的模拟值与实测值接近,说明模型具有较好的预测准确性和可靠性.
-
1)避光和光照条件下,THC、CBN和CBD在生活污水中均能降解产生较低浓度的THC-COOH,光照会加快THC、CBN和CBD的降解,样品测试前避光保存对于大麻素类物质的准确定量非常重要.
2)生活污水中THC-COOH稳定性高于THC、CBN和CBD. 因此,利用生活污水进行大麻滥用评估时,以THC-COOH作为目标分析物,且在24 h内完成分析测试为佳.
3)生活污水加标样中大麻素类物质去除率与样品保存时间和常规水质参数(COD、NH3-N、TP、TN浓度和pH值)有较好的相关性. 其中THC去除率与保存时间具有正相关性,CBN、CBD去除率均与保存时间和NH3-N存在正相关性,THC-COOH去除率与保存时间具有正相关性,与NH3-N存在负相关性. 表明存储时间对所有目标物的稳定性均有较大影响,取样后尽快完成测试对于准确定量目标物至关重要.
生活污水中大麻素类物质及其主要生物代谢产物的稳定性研究
Stability of cannabinoids and the major bio-metabolite in domestic wastewater
-
摘要: 近年来,以污水流行病学为基础的污水验毒技术在大麻滥用评估中应用愈加广泛,大麻中主要活性物质及其生物代谢产物的稳定性是准确评估滥用量的关键. 本研究通过标准加入法,研究了避光和光照条件下生活污水中四氢大麻酚(THC)、大麻酚(CBN)、大麻二酚(CBD)的稳定性,并与其主要生物代谢产物四氢大麻酸(THC-COOH)进行了比较;采用多元线性回归以及相关性分析,探讨了样品存储时间(t)、污水水质参数(化学需氧量 (COD)、氨氮 (NH3-N)、总磷 (TP)、总氮 (TN) 浓度和pH)对THC、CBN、CBD和THC-COOH稳定性的影响. 结果表明:避光和光照条件下,18 h内THC、CBN和CBD均降解产生较低浓度的THC-COOH,光照会加快THC、CBN和CBD的降解;24 h内THC-COOH稳定性高于THC、CBN和CBD;4种目标物去除率与t、水质参数的多元线性回归方程中,R2值均大于0.89,在 P ≤ 0.05 的置信水平上,THC去除率与t具有正相关性,CBN、CBD去除率均与t和NH3-N存在正相关性,THC-COOH去除率与t具有正相关性,与NH3-N存在负相关性. 因此,利用生活污水样品进行大麻滥用评估时,以THC-COOH作为目标分析物为佳,取样后避光保存且尽快完成测试(24 h内)对于准确评估大麻滥用量至关重要.Abstract: In recent years, sewage epidemiology-based drug testing techniques are increasingly used in cannabis abuse assessment. The stability of the main active substances in cannabis and the bio-metabolite is critical to accurate determination of the concentration and the assessment of cannabis abuse. In this study, the stability of tetrahydrocannabinol (THC), cannabinol (CBN), and cannabidiol (CBD) in domestic wastewater under dark and light irradiation was investigated by the standard addition method. Their stability was compared with that of tetrahydrocannabinoic acid (THC-COOH), which is a major bio-metabolite of cannabinoids in human body. A multiple linear regression and correlation analysis was adopted to evaluate the effects of sample storage time (t), water quality parameters (including chemical oxygen demand (COD), ammonia nitrogen (NH3-N), total phosphorus (TP), total nitrogen (TN) concentration and pH) in domestic wastewater on the stability of THC, CBN, CBD and THC-COOH. The results showed that the degradation of THC, CBN and CBD in domestic wastewater, both in dark and under light irradiation, produced very low concentrations of THC-COOH within 18 h, and the degradation was accelerated by light irradiation. THC, CBN and CBD in domestic wastewater were less stable than THC-COOH within 24 h. The R2 values of multiple linear regression model, for correlating the removal rates of the four target compounds with sample storage time (t) and water quality parameters in domestic wastewater, were greater than 0.89 in any case. At a confidence level of P ≤ 0.05, the removal rate of THC had a positive correlation with t, and those of CBN and CBD both had a positive correlation with t and NH3-N, and that of THC-COOH had a positive correlation with t and a negative correlation with NH3-N. Therefore, when using domestic wastewater for cannabis abuse assessment, THC-COOH was better as a target analyte. It is also essential to store samples away from light and complete the test as soon as possible after sampling (preferably within 24 h) for accurate assessment of cannabis abuse.
-
Key words:
- tetrahydrocannabinol /
- cannabinol /
- cannabidiol /
- tetrahydrocannabinic acid /
- stability.
-
偶氮染料是纺织业中使用最多的一类染料 [1],具有难降解的特性。常见的处理方法包括物化法、化学法和生物法。物化法不能彻底降解污染物,化学法成本过高,生物法降解缓慢[2],因此限制了这些方法的应用。
次氯酸钠氧化法广泛用于降解废水中的污染物,并以污染物去除效率高、设备简单、经济性等优点而受到人们的重视。NaClO溶液的稳定性较差,大大降低了其氧化性的利用率。此外,采用NaClO直接氧化废水,会产生具有强致癌性的氯代有机物。增强NaClO的氧化性和消除氯代有机物对拓宽其在水处理中的应用极为重要。镍基催化剂能促进NaClO溶液的分解增强其氧化性,且以催化效果好、便宜等优点而备受关注[3]。NaClO在氧化镍的作用下生成具有极强活性的原子氧,迅速氧化废水中的污染物,从而达到去除COD和脱色的目的[4-5]。本课题组研发的NaClO催化氧化法能有效降解活性艳红K-2BP、酸性大红3R等偶氮染料,活性艳红K-2BP的脱色率在120 min达到94%以上[6],而酸性大红3R的脱色率在35 min达到90%以上。原子氧在脱色降解过程起了主导作用,因此未在染料降解产物中发现氯代有机物。
研究染料的分子结构与脱色性能之间的关系对废水的处理至关重要。染料种类繁多,结构各异,可以采用QSPR (quantitative molecular structure-properties relationships)法研究分子结构和脱色性能的关系。该方法简单易行,了解了分子结构信息,就可以分析和预测染料的理化性质或环境行为[7]。
本研究分别采用NaClO催化氧化法和NaClO氧化法脱色降解活性黄X-R废水,考察比较两种方法的脱色效果;比较催化氧化法对活性黄X-R和另外两种偶氮染料的脱色效果,在此基础上采用QSPR分析该方法处理不同染料效果存在差异的原因,进而指出其适用范围。本研究选择适当的染料分子结构描述符,通过线性回归法研究上述目标染料分子结构与NaClO催化氧化法对其脱色效果之间的关系。研究结果将为推广应用NaClO催化氧化法提供理论依据。
1. 材料与方法 (Materials and methods)
1.1 实验材料
催化剂载体选用水处理用耐酸碱的γ-Al2O3小球,参数如下:直径为 2−3 mm,Al2O3 > 92%,孔容为0.35 mL·g−1,比表面积大于300 m2·g−1。Na2S2O8 (99%)、NAOH (99%)、Ni(NO3)2·6H2O (99%)、H2SO4 (98%)、呋喃甲醇(99.2%)和叔丁醇(99.9%)均为分析纯,NaClO溶液有效氯含量大于10%。
仪器包括:ZYL便携式余氯分析仪、MIT-3F型COD检测仪、723N扫模型可见光分光光度计、Rigaku Smartlab9 x射线衍射仪(日本理学)、EscaLab 250Xi型X射线光电子能谱仪,Al-Kα射线单色源(美国赛默飞)、扫描电镜SEM(美国FEI Inspect F50)。
1.2 催化剂制备
催化剂制备步骤如下:先将γ-Al2O3小球浸泡在摩尔浓度为0.6 mol·L−1 Na2S2O8和0.5 mol·L−1 NaOH的混合液里,在振荡器上以100 r·min−1的频率振荡2 h,将得到的Na2S2O8-NaOH/Al2O3小球滤出后烘干。然后将Na2S2O8-NaOH/Al2O3小球浸泡在含有0.6 mol·L−1 Ni2+的溶液里发生反应,在γ-Al2O3表面形成一层镍氧化物/镍氢氧化物沉淀,将制得的小球滤出后烘干,得到镍基Al2O3小球。将得到的镍基Al2O3小球再次浸泡在Na2S2O8-NaOH混合液里,在振荡器上以100 r·min−1的频率振荡2 h后将催化剂小球滤出,用蒸馏水清洗。最后将洗净的催化剂置于马弗炉中低温焙烧2 h,制得催化氧化实验所需的催化剂样品。
Ni(OH)2为还原性氢氧化物,能和强氧化剂反应生成羟基氧化镍NiOOH。通过Ni2+在碱性溶液中被Na2S2O8氧化的反应来合成NiOOH(见式(1)和式(2)),从中可以看出,碱性条件促进Ni(OH)2和NiOOH的生成。
Ni2++2OH−⟶Ni(OH)2 (1) 2Ni(OH)2+S2O2−8+2OH−⟶2NiOOH+2SO2−4+2H2O (2) 在NiOOH存在的情况下,NaClO的分解反应2NaClO→2NaCl+O2↑可以看作是反应(3)和反应(4)的总和:
2NiOOH+NaClO⟶NaCl+2NiO2+H2O (3) 2NiO2+NaClO+H2O⟶2NiOOH+NaCl+O2 (4) 产生的氧分子能被物理吸附在镍基催化层上(式5),捕获电子后转化为化学吸附氧
O−2 O2(g)+S↔O2 (5) O2+e−↔O−2+∗ (6) O−2\xLeftrightarrowΔG1O−+O (7) O2\xLeftrightarrowΔG22O (8) 其中,O2(g)为气态氧,S为表面吸附位置,O2为表面物理吸附的氧,*和e−代表导带底部空位和导带电子,ΔG为反应能。反应产生的原子氧O非常活跃,可以快速氧化和分解有机物。羟基氧化镍可以长时间用作催化剂,因为它可以通过反应(3)和(4)进行再生利用。
1.3 活性黄X-R浓度的检测
染料废水在波长为390 nm处有最大特征吸收峰,在390 nm检测不同浓度废水的吸光度,建立质量浓度和吸光度的标准曲线方程y =96.877 x –1.1831,R2 = 0.9987。
1.4 染料脱色率分析
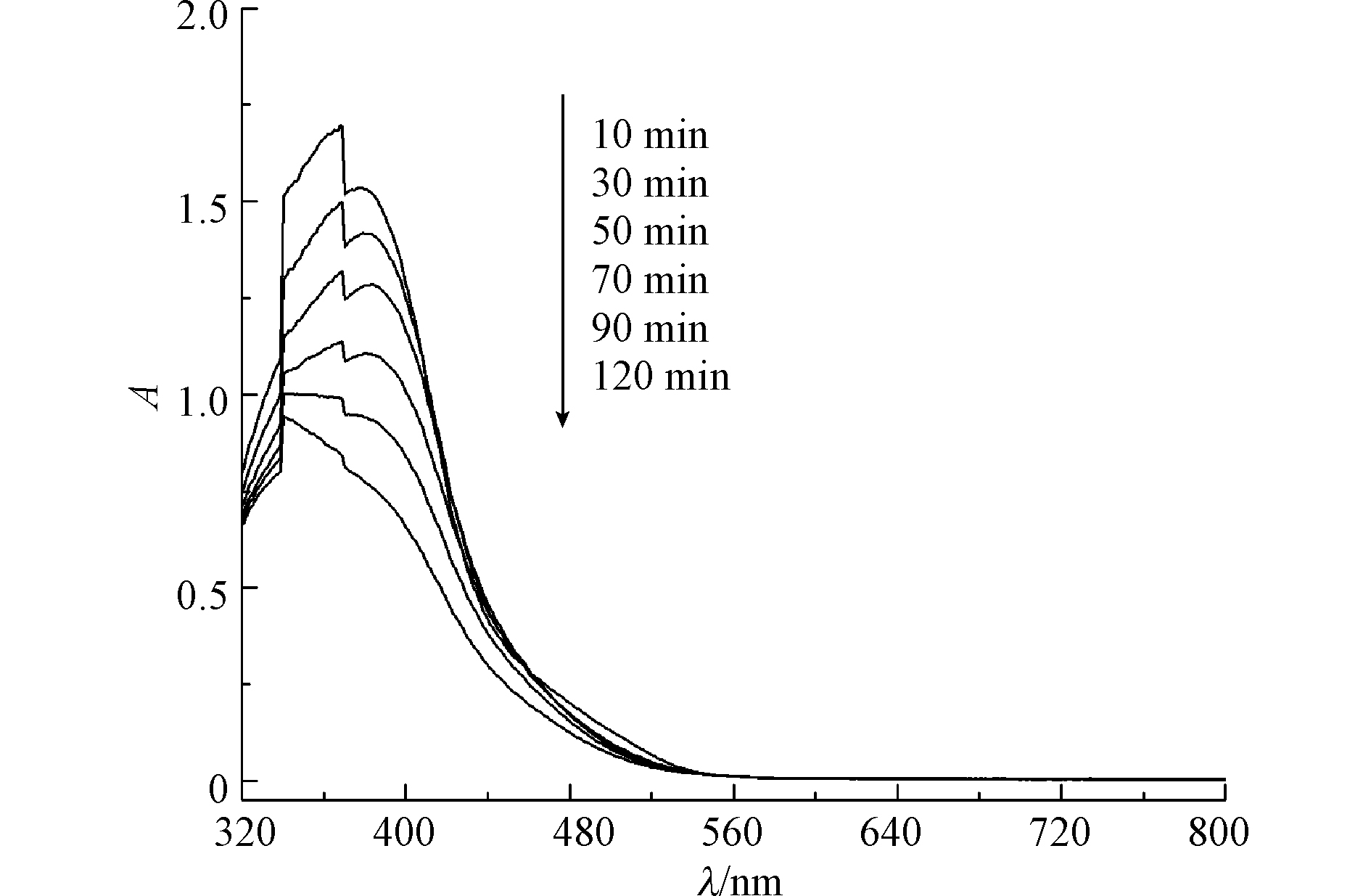
配制一定浓度的活性黄X-R溶液,加入一定量的NaClO溶液,充分搅拌,调节pH至所需值,得到废水/NaClO混合液。取50 mL混合液放入100 mL锥形瓶内,把一定量催化剂样品快速放入溶液中。在振荡器上以100 r·min−1的速度振荡120 min。分别在第10、30、50、70、90、120 min时取3 mL左右上清液,直接测其吸光度,利用标准曲线方程求得染料的浓度,按公式(9)计算其脱色率。测好吸光度后将染料溶液倒回锥形瓶中继续反应。
脱色率=C0−CtC0×100(%) (9) 式中,C0 和Ct 分别为初始染料浓度和t时刻染料浓度,mg·L−1。
1.5 自由基清除剂实验
配制质量浓度为200 mg·L−1的活性黄X-R溶液,加入120 mg·L−1的NaClO溶液,充分搅拌,调节到pH 9,得到废水/NaClO混合液。在两个相同组分的混合液中分别加入20 mmol·L−1的叔丁醇和呋喃甲醇,与催化剂一起放入100 mL锥形瓶内,在振荡器上以100 r·min−1的速度振荡反应,检测染料的脱色率变化,并以此来判断在反应中起主导作用的自由基。叔丁醇是一种良好的OH·和
SO−4⋅ 2. 结果与讨论 (Results and discussion)
2.1 反应条件对活性黄X-R溶液脱色率的影响
2.1.1 染料浓度对脱色率的影响
检测了当pH 为9、有效氯浓度为120 mg·L、催化剂投加量为240 g·L−1、初始染料浓度为100、200、300、400 mg·L−1时的脱色率,结果如图1所示。前期的研究结果表明[11],有催化剂时,弱碱性环境pH 9有利于反应(1)和反应(2)的发生,促进活性氧的产生,增大NaClO的转化率。当催化剂存在时,脱色率随着初始染料浓度的增加而增加:当染料浓度为100、200、300、400 mg·L−1时,脱色率在120 min时分别为41.1%、41.21%、42.47%和50.03%。没有催化剂时,当初始染料浓度为100、200、300、400 mg·L−1时,脱色率在反应120 min时分别为43.7%、42.67%、41.78%和40.17%。加入催化剂后,初始染料浓度为100、200、300 mg·L−1溶液在120 min时的脱色率基本没有发生变化,可能是因为NaClO的直接氧化起了主导作用。当初始染料浓度为400 mg·L−1时,催化剂的加入使脱色率增加到50.03%,催化剂的吸附和活性氧的氧化作用对脱色率的增量做了一定的贡献,吸附量随着染料浓度的增加而增大,进而促进了活性氧与之发生反应。
催化氧化法对活性黄X-R的脱色效果远差于其对活性艳红K-2BP和酸性大红3R的脱色效果,脱色率随浓度变化的趋势也和后面两种染料的相反,活性艳红K-2BP和酸性大红3R的脱色率随着染料初始浓度的增加而减小(图2),因为反应的速率受到活性氧产量的限制,高浓度溶液需要更多的活性氧才能保持同样的降解速率。
 图 2 初始染料浓度对脱色率的影响Figure 2. Effect of initial dye concentration on color removal ratepH为9,催化剂投加量为240 g·L−1和 (a) 活性艳红K-2BP,有效氯为120 mg·L−1 (b) 酸性大红3R,有效氯为60 mg·L−1pH 9, catalyst dosage 240 g·L−1 and (a) reactive brilliant red K-2BP, available chlorine 120 mg·L−1 (b) acid red 3R, available chlorine 60 mg·L−1
图 2 初始染料浓度对脱色率的影响Figure 2. Effect of initial dye concentration on color removal ratepH为9,催化剂投加量为240 g·L−1和 (a) 活性艳红K-2BP,有效氯为120 mg·L−1 (b) 酸性大红3R,有效氯为60 mg·L−1pH 9, catalyst dosage 240 g·L−1 and (a) reactive brilliant red K-2BP, available chlorine 120 mg·L−1 (b) acid red 3R, available chlorine 60 mg·L−1以上实验结果表明,催化氧化体系降解活性黄X-R的机理可能有别于活性艳红K-2BP和酸性大红3R的降解机理,NaClO更倾向于直接氧化活性黄X-R,因此抑制了其本身的催化分解反应,减少了活性氧的产量;活性黄X-R分子也可能不易被具有亲电子性的活性氧攻击,使NaClO的直接氧化作用在脱色反应中占据了主导地位。因此,当NaClO有效氯浓度足够高的时候,染料的分解速率随着染料浓度的增加而增大,从表观上看,脱色率增大。
2.1.2 有效氯浓度对脱色率的影响
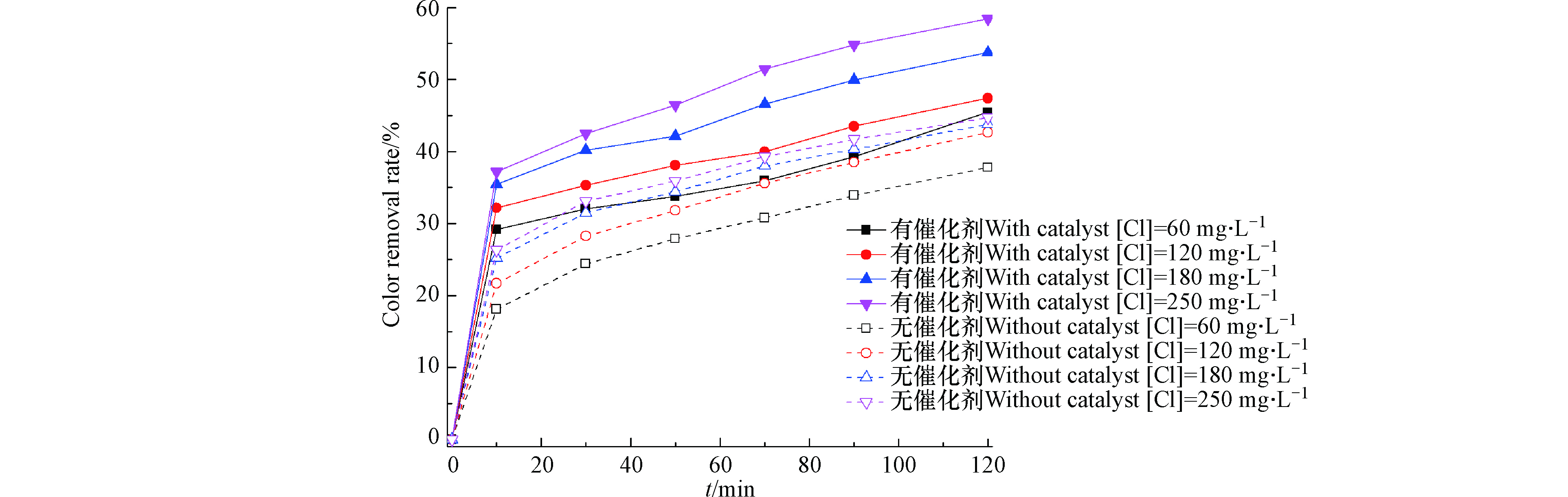
检测了当pH 9、染料浓度为200 mg·L−1、催化剂投加量为240 g·L−1、 有效氯为60、120、180 、250 mg·L−1时的脱色率,结果如图3所示。脱色率随着有效氯浓度的增加而增大。有催化剂存在时,当有效氯浓度从60 mg·L−1增加到250 mg·L−1,120 min时染料的脱色率从45%提升到了58%,增幅有限,主要是因为NaClO的直接氧化起了主导作用。NaClO在pH 9时的氧化性较弱,脱色效果差,单独氧化时NaClO的利用率较低[12]。有效氯浓度的增大也促进了NaClO直接氧化染料反应的进行,改善了活性黄X-R的脱色效果:当初始有效氯浓度从60 mg·L−1增加到250 mg·L−1,染料的脱色率从37.8%提升到了44.7%,比催化剂存在时的脱色率低6.3%–13.3%,增值是由催化剂的吸附和产生的活性氧作用所导致的。
2.1.3 pH对脱色率的影响
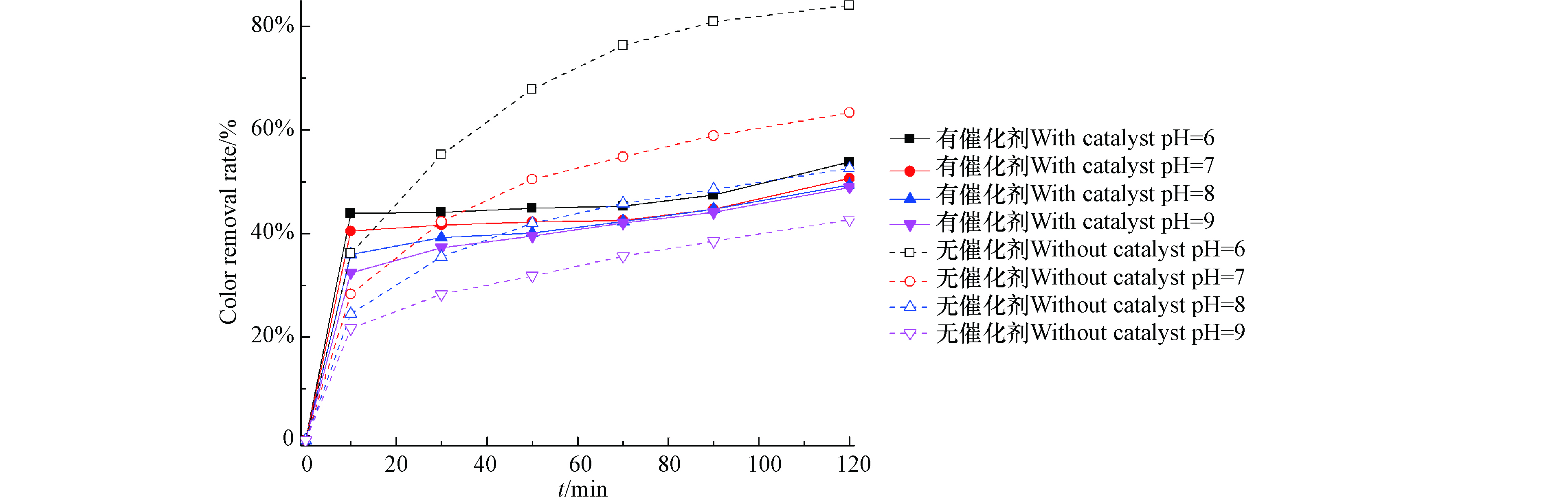
检测了当有效氯为120 mg·L−1、染料浓度为200 mg·L−1、催化剂投加量为240 g·L−1、初始pH值为6、7、8、9时的脱色率,结果如图4所示。NaClO催化氧化法的脱色率随着pH的提升而减小,pH 6、7时的脱色效果略胜于pH 8、9时的脱色效果,初始pH为6时的脱色效果最好,当反应时间为120 min,脱色率达到53.8%,远低于弱碱性条件下NaClO催化氧化降解活性艳红K-2BP和酸性大红3R溶液的脱色率(图5),催化作用明显受到了抑制,这是因为反应机理不同而导致的。原子氧在活性艳红K-2BP和酸性大红3R的脱色中起了主导作用,NaClO的直接氧化在活性黄X-R的脱色中起了主导作用。当初始pH为9,加催化剂反应120 min,活性黄X-R的脱色率达到49%,无催化剂时脱色率为42.7%(图4)。NaClO法降解活性黄X-R的脱色率随着pH的增加明显降低,当pH值从6增加到9,脱色率从84.1%降到42.7%,这是因为NaClO在酸性条件下会以游离氯存在,氧化性能大大提升。
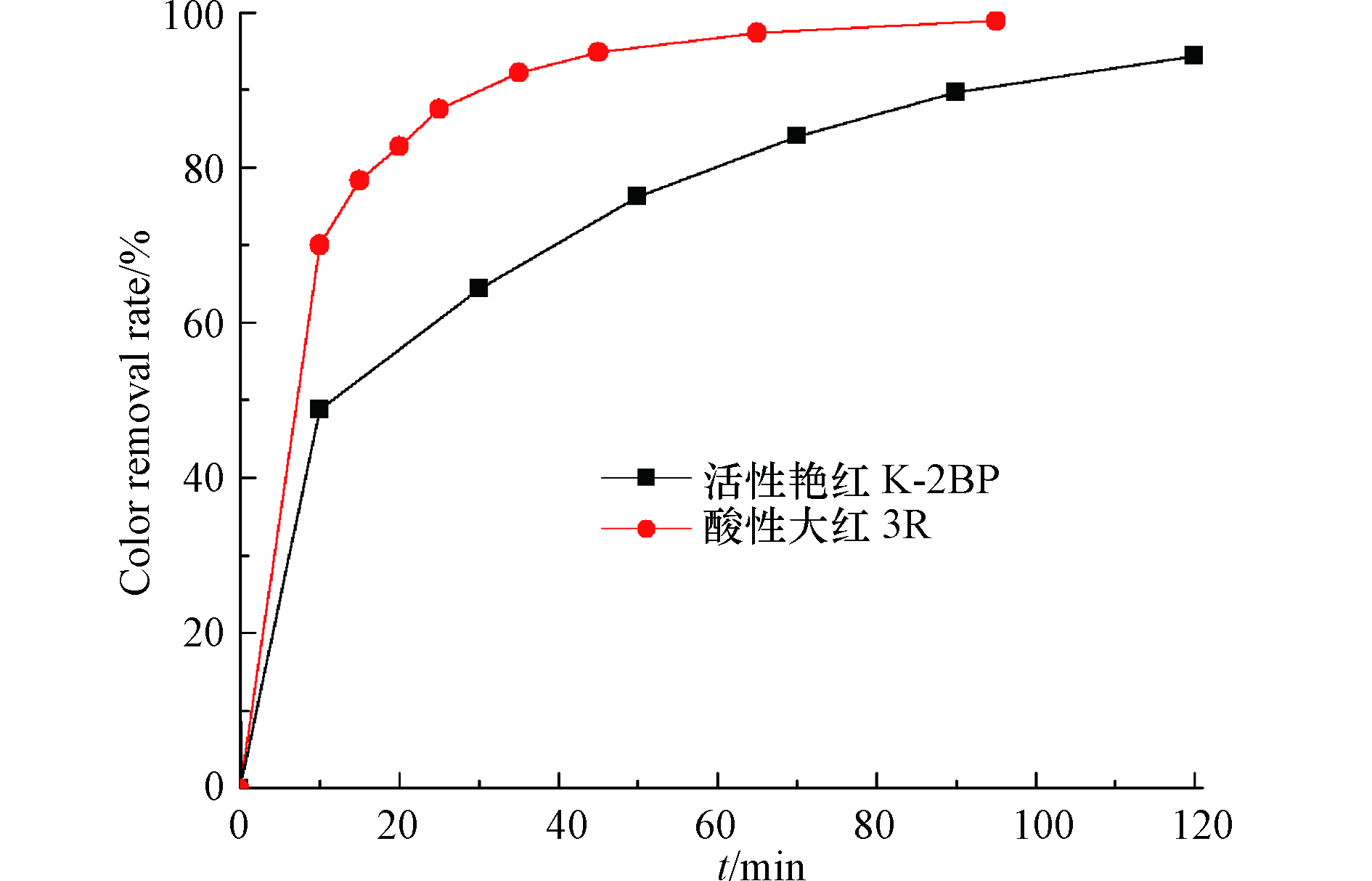 图 5 不同偶氮染料对脱色率的影响Figure 5. Effect of different azo-dyes on color removal rate初始pH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1initial pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant red K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red and available chlorine are 200 mg·L−1 and 60 mg·L−1
图 5 不同偶氮染料对脱色率的影响Figure 5. Effect of different azo-dyes on color removal rate初始pH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1initial pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant red K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red and available chlorine are 200 mg·L−1 and 60 mg·L−1当pH值为6、7、8时,加入催化剂反而导致活性黄X-R的脱色效果变差(图4)。当pH 6时,NaClO主要以HClO的形式存在。随着pH值的提升,ClO−的量增多,pH 9时NaClO主要以ClO−的形式存在。催化剂表面含有大量Ni(OH)2,带有正电荷[13]。当pH 6时,催化剂与次氯酸电荷相斥,不利于其在催化剂表面的有效吸附;当pH值为8、9,催化剂与ClO−存在电荷相吸作用,有利于NaClO在催化剂表面的有效吸附。催化剂表面和含有磺酸根离子的染料分子之间的静电吸引可能有利于染料在其表面的有效吸附。因此,当pH 6时,催化剂的存在降低了HClO与染料分子之间的反应几率,从而降低了脱色率,虽然此时的溶液具有较强的氧化性。当pH值为8、9,NaClO和染料分子在催化剂表面的有效吸附使两者之间的反应几率增大,从而使脱色率和酸性条件下的相差不大。催化剂存在时,弱碱性条件促进了活性氧的产生,但对染料的脱色率基本没有产生影响,可能是活性氧与染料分子之间的反应受到了阻碍。
采用NaClO催化氧化法降解活性艳红K-2BP和酸性大红3R,初始pH 9时的脱色效果最好(图6),弱碱性条件有利于NiOOH的生成和催化层的固定(式(1)和式(2)),进而促进原子氧的产生(式(3)—(8));同时,弱碱性条件还能抵消由于降解过程产生有机酸而导致的pH值的下降,起到平衡pH值的作用。
 图 6 pH对不同偶氮染料脱色率的影响Figure 6. Effect of different azo-dyes on color removal ratepH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red 3R and available chlorine are 200 mg·L−1 and 60 mg·L−1
图 6 pH对不同偶氮染料脱色率的影响Figure 6. Effect of different azo-dyes on color removal ratepH 9,催化剂投加量240 g·L−1,活性艳红K-2BP和有效氯浓度为200 mg·L−1和120 mg·L−1,酸性大红3R和有效氯浓度为200 mg·L−1和60 mg·L−1pH 9, catalyst dosage 240 g·L−1, the concentrations of reactive brilliant K-2BP and available chlorine are 200 mg·L−1 and 120 mg·L−1, while the concentrations of acid red 3R and available chlorine are 200 mg·L−1 and 60 mg·L−12.1.4 催化剂对脱色率的影响
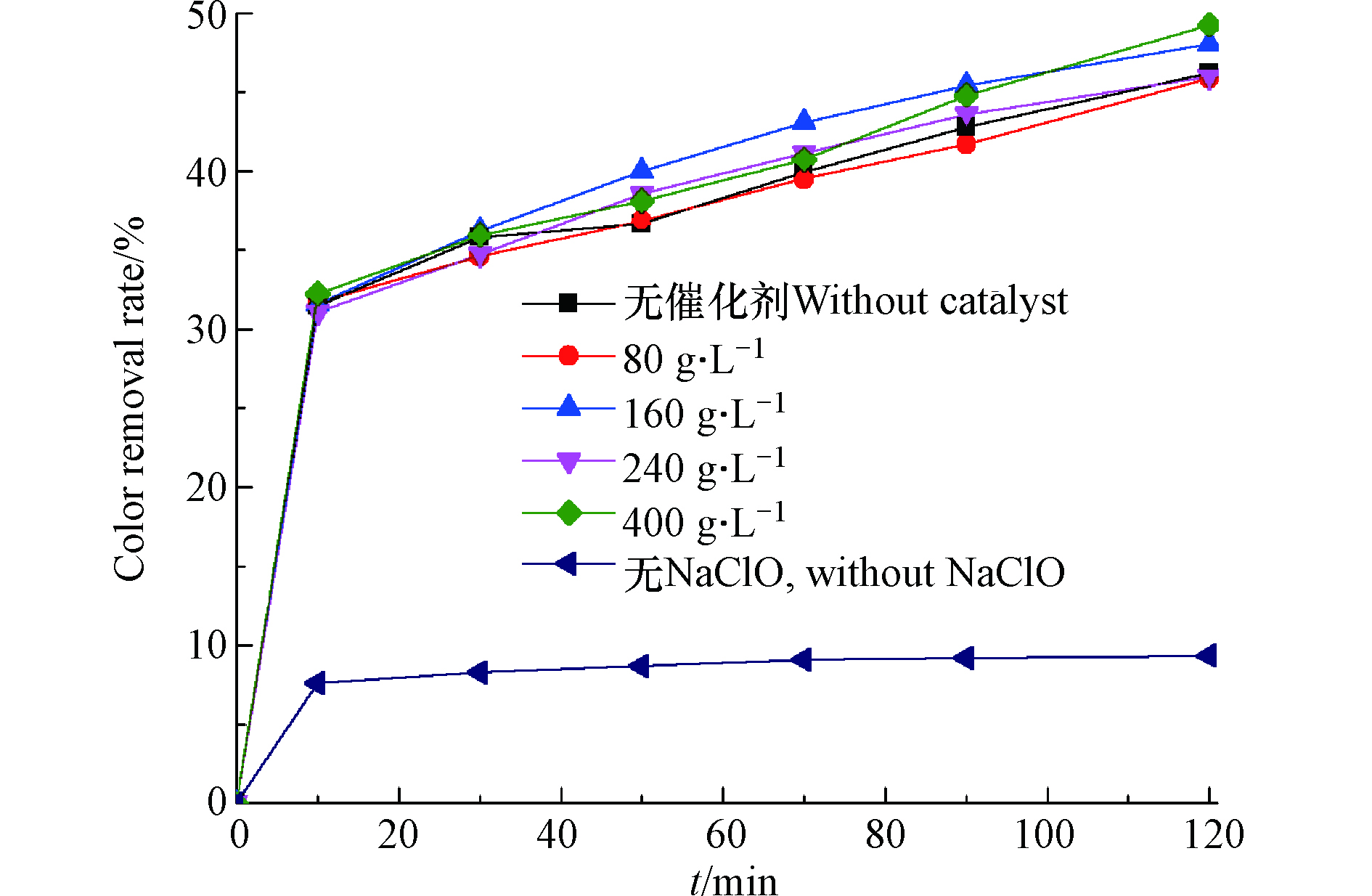
检测了当有效氯浓度为120 mg·L−1、染料浓度为200 mg·L−1、初始pH为9、催化剂投加量为80、160、240、400 g·L−1时的脱色率,结果如图7所示。催化剂投加量的增加对染料脱色率的影响很小,当催化剂投加量从80 g增加到400 g·L−1,脱色率在反应120 min时只提升了3.4%。单独使用NaClO时的脱色率与催化剂存在时的基本相同。单独使用400 g·L−1新制备的催化剂处理废水120 min,仅有7.6%–9.4%的脱色率,随着反应时间的延长,脱色率变化幅度很小,说明这部分脱色率主要是由吸附导致的,其贡献较小。实验结果再次验证了NaClO的氧化在脱色反应中的主导作用,当初始pH为9时,催化剂对脱色反应的影响甚微,催化作用受到了抑制。因此,催化氧化法不太适用于脱色降解活性黄X-R废水。
2.1.3节的研究结果表明,当pH为6,200 mg·L−1活性黄X-R废水中有效氯浓度达到120 mg·L−1,反应 120 min后脱色率达到84.1%。继续调低pH能进一步提升脱色率,但是NaClO氧化法会导致出水中产生毒性较强的氯代有机物。王元刚等[14]采用Mg(OH)2混凝脱色降解浓度为100 mg·L−1的活性黄X-R废水,当pH 值为12、Mg2+投加量为216 mg·L−1时,脱色率达到90%以上。王昶等[15]采用蛭石类芬顿降解活性黄X-R染料,结果表明,把蛭石粉碎到7.5 μm的颗粒,其投加量为1.0 g·L−1、pH 3、H2O2用量 2.94 mmol·L−1时,反应180 min 后,50—300 mg·L−1活性黄X-R 脱色率均能达到95%以上。后面两种方法的运行成本偏高。
2.2 机理研究
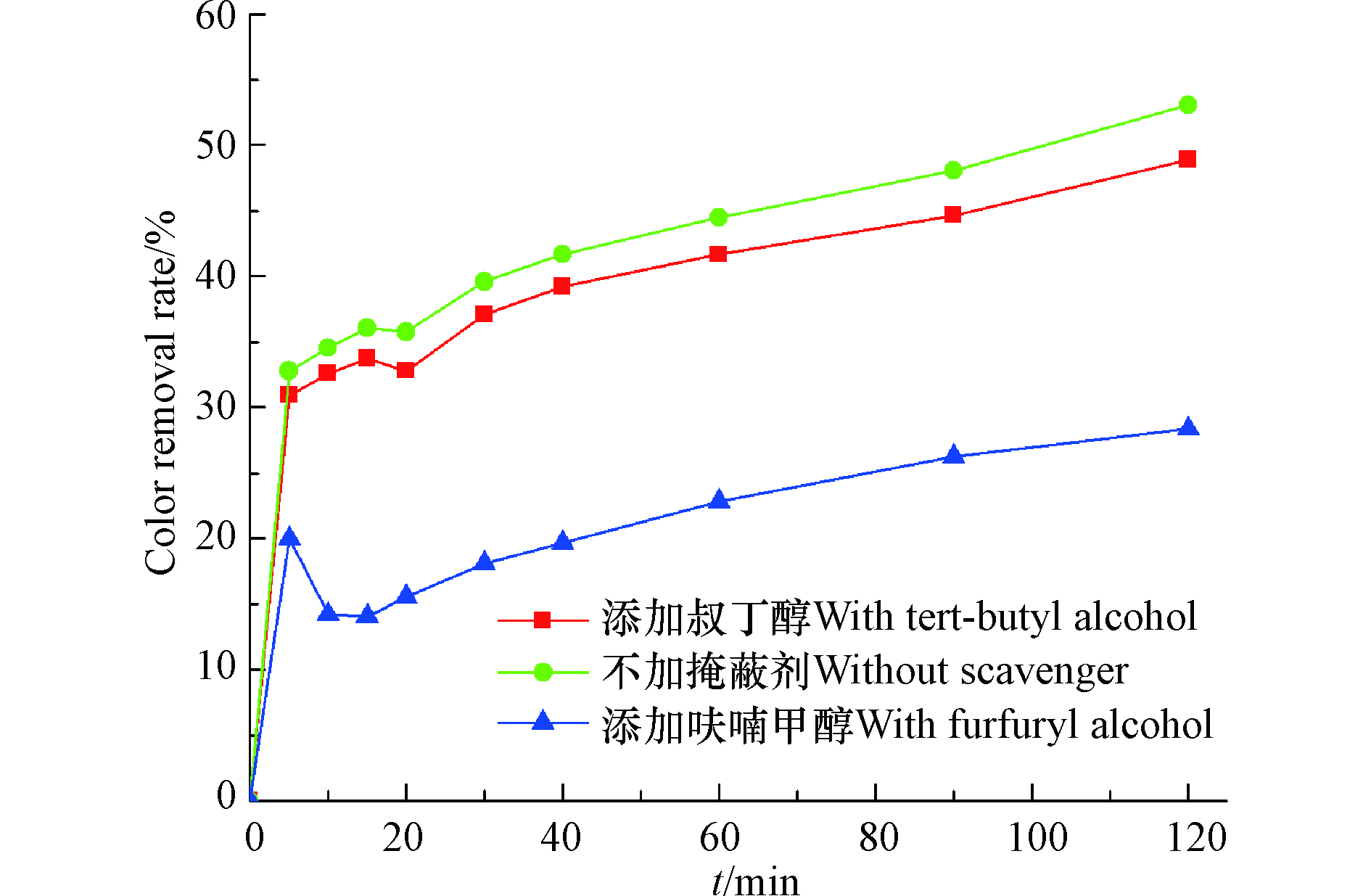
叔丁醇的加入对活性黄X-R的降解过程几乎没有影响,而呋喃甲醇对脱色具有一定的抑制作用,两者之间的脱色率差值在12%―24%之间(图8),因此可以断定原子氧在染料脱色过程中起了一定的作用,OH·和
SO−4⋅ 活性黄X-R在390 nm的最大吸收峰对应偶氮键(图9),该峰随着反应的进行逐渐减小,但没有消失,可见偶氮键并未被完全破坏。367―370 nm之间为萘环的吸收峰,峰面积随着反应的进行减小,但反应120 min后该特征吸收峰还在,萘环没有完全打开。
2.3 染料分子结构与脱色率的关系
根据染料的分子结构特征及脱色率,选择磺酸基(
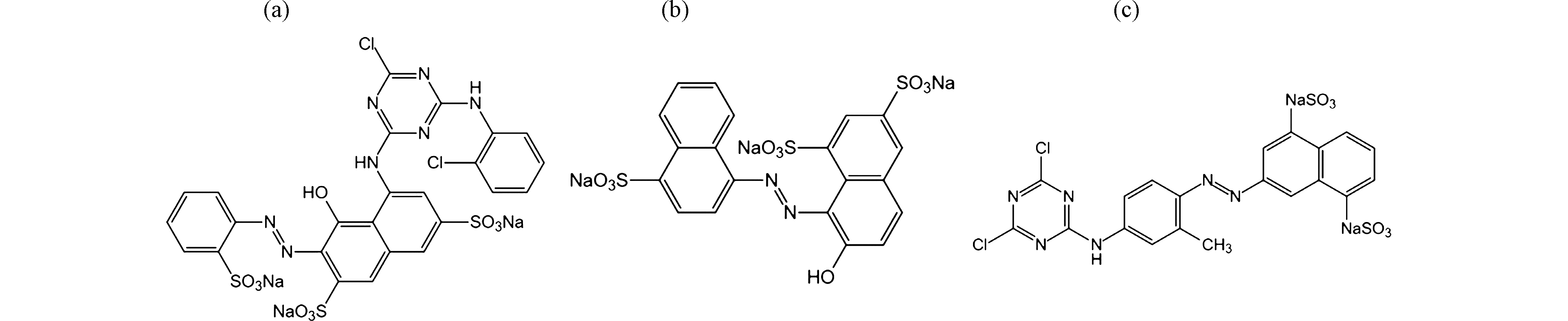
SO−3 分别配制浓度为200 mg·L−1的活性艳红K-2BP、酸性大红3R和活性黄X-R溶液,往里投加NaClO,使混合液中有效氯浓度达到120 mg·L−1,调节废水/NaClO混合液的pH值到9,投加催化剂240 g·L−1,在振荡器上反应90 min后取样,于染料的最大吸收波长下测定溶液的吸光度,换算成浓度,计算其脱色率。3种染料都属于偶氮染料,它们的分子结构见图10,它们的去除率和分子结构描述符见表1.
表 1 偶氮染料的去除率和分子结构描述符Table 1. Removal rate and molecular structure descriptor of the azo dyes染料名称Dye name 分子结构描述符Molecular structure descriptor 脱色率/%Color removal rate A B C 活性艳红K-2BP 3 3.95 5 91.3 酸性大红3R 3 6.25 4 99.69 活性黄 X-R 2 3.14 4 39.3 对表1中的分子结构描述符与脱色率进行线性回归分析,其线性回归方程和参数如表2所示。A、B与脱色率的线性回归数值比较高,说明目标染料的去除率与染料分子结构中磺酸基数目和I/O值之间具有较强的线性相关性,其中磺酸基数目A对去除率的影响尤为突出。染料分子的A值升高,其脱色率增加,这是因为磺酸基数目的增加使染料分子的电子云密度增加,原子氧具有较强的亲电子性,易与偶氮键发生加成反应。染料分子的B值升高,其无机性增强,电离度也随之增大,溶液中磺酸根离子的量增加,原子氧与染料分子之间的反应几率也因此增大,染料的脱色效率提高。C值增大,脱色率也随之增加,但去除率和C值的相关性较差,R2=0.1481,染料分子中C值一般小于10。因此,C值对脱色率的影响很小。
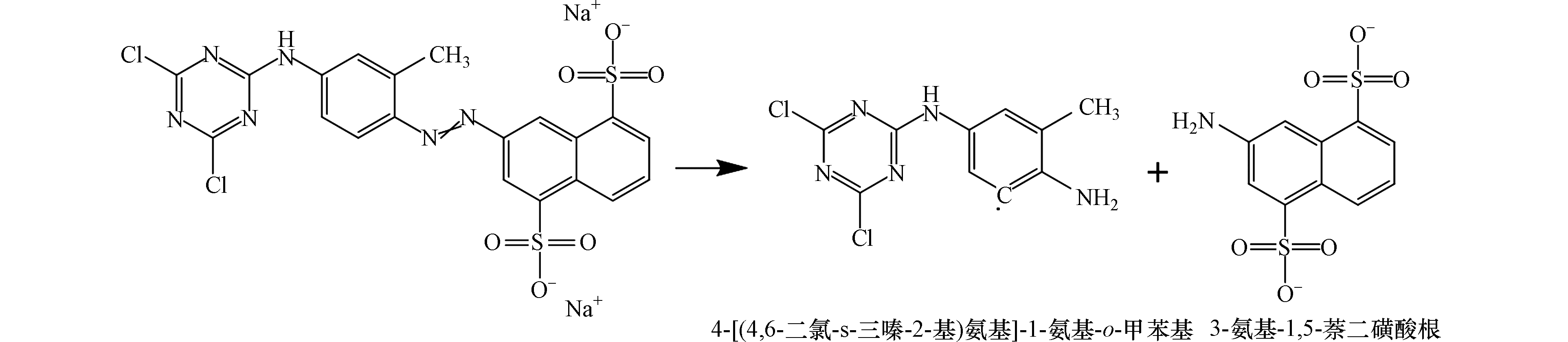
表 2 分子结构描述符与去除率的线性回归方程Table 2. Linear regression equation between molecular structure descriptor and removal rate分子结构描述符Molecular structure descriptor 回归方程Regression equation R2 F A ω 0.9836 59.815 B ω 0.6194 2.627 C ω 0.1481 0.174 偶氮键断开后,活性黄X-R分子被分解成2个芳胺:3-氨基-1,5-萘二磺酸根和4-[(4,6-二氯-s-三嗪-2-基)氨基]-1-氨基-o-甲苯基 (图11)。3-氨基-1,5-萘二磺酸根包含一个萘环,萘环上引入了两个磺酸基,其耐氯牢度大大提高,也就是说OCl−的进攻能力减弱;引入磺酸基的数目越多,耐氯牢度提升也越大[18]。活性黄X-R分子含有二氯均三嗪活性基,由于两个氯原子的吸电子诱导效应,环上的电子云密度较低,故其活性较高,水解率高,固色效果差,容易被浓度高氧化能力弱一些的OCl−进攻。活性艳红K-2BP的分子包含1个偶氮基、一氯均三嗪基、2个苯环和1个萘环(图10)。一氯均三嗪环上的电子云密度高,稳定性强,固色效果好,不易被OCl−进攻[19],却能被氧化性极强的原子氧脱色降解。董亚荣等[20]曾对10种染料的生物降解脱色性能进行了研究,结果表明,X型染料最易降解,K型染料次之。实验结果与该结论吻合。酸性大红3R分子包含1个偶氮基、1个羟基和2个萘环;萘环上有3个磺酸基,其中1个磺酸基位于偶氮基的邻位(图10),其耐氯稳定性好[19],降解过程不易产生有机氯产物。
综上,活性黄X-R分子的耐氯牢度较低,NaClO倾向将其直接氧化,从而抑制了NaClO的催化分解和原子氧的产生,降低了原子氧对脱色降解过程的贡献度。活性艳红K-2BP和酸性大红3R的耐氯稳定性好。NaClO催化氧化法更适合降解耐氯性强的K型活性偶氮染料和含有磺酸钠盐的酸性偶氮染料,不太适合于降解X型活性偶氮染料。苯环染料比萘环染料耐氯性好,这也是吴正雷等[5]用NaClO/镍基催化剂处理甲基橙(对二甲氮基偶苯磺酸钠)废水,没有发现有机氯产物的原因。
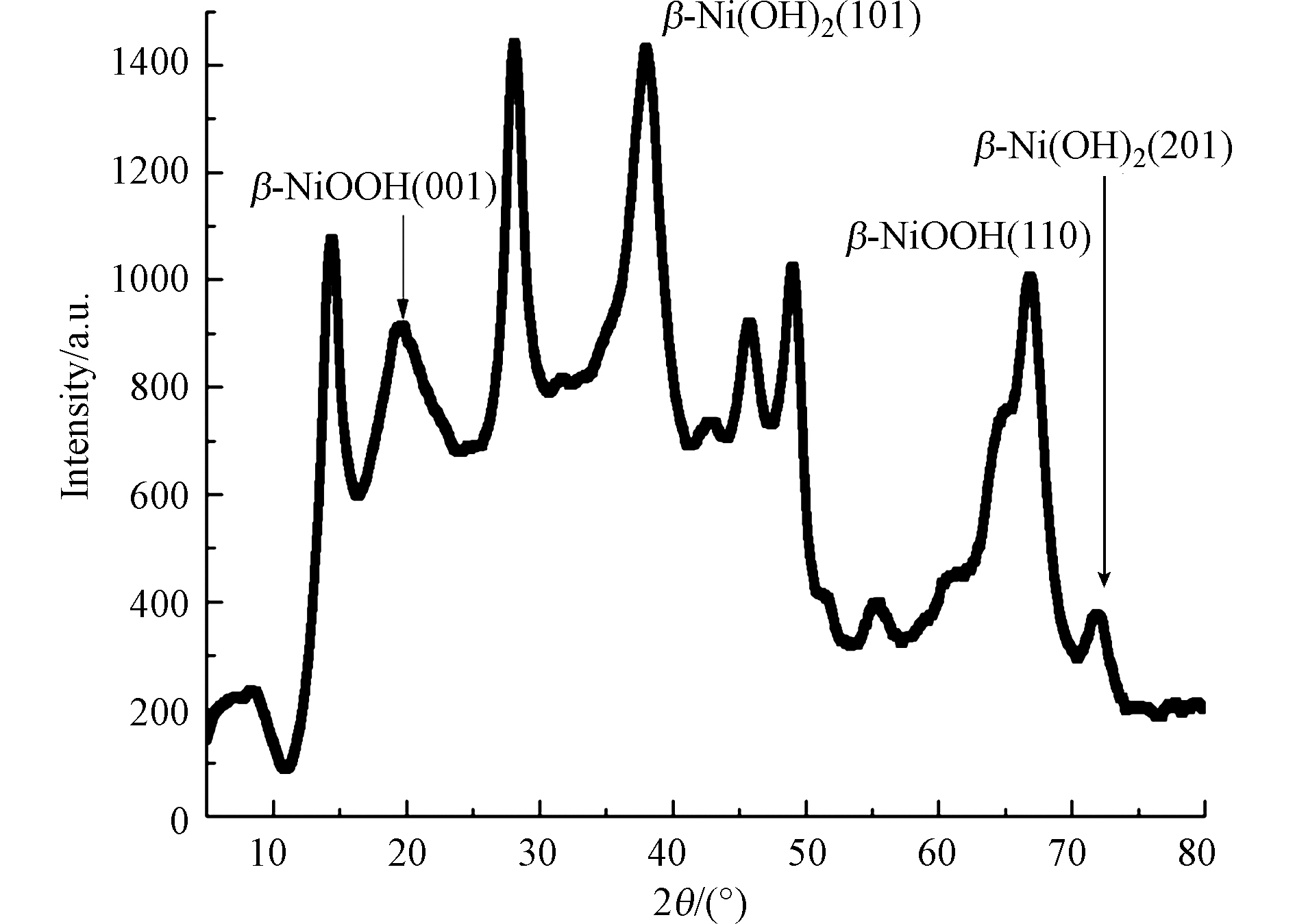
采用XRD对催化剂表层进行物相分析。样品在19.2°和66.7°附近有强的衍射峰(图12),与标准卡(卡号60141)对比可知,样品里含有β-NiOOH,两个衍射峰分别为001和110晶面。样品在38.5°和72.2°处出现两个衍射峰,与标准卡(卡号14117)对比可知,样品里含有β-Ni(OH)2,两个衍射峰分别为101和201晶面。
采用XPS分析法检测催化剂表面的元素及其相对含量。选取新制备的催化剂和分别处理过3000 min不同偶氮染料的三个催化剂小球作为检测样品。样品中氧元素的含量在78%以上(表3)。531.46 eV左右的峰为化学吸附氧引起的[21]。处理过3000 min染料的催化剂样品中氧元素的含量有不同程度的减小,主要是因为产生的原子氧参与降解染料。855.79―856.14 eV的峰是由Ni(Ⅱ)引起的,861.59―861.95 eV的峰是由Ni(Ⅲ)引起的[22]。新制的催化剂样品的Ni(Ⅲ)/Ni(Ⅱ)比值为0.62,处理过3000 min三种不同染料的催化剂样品中Ni(Ⅲ)/Ni(Ⅱ)比值分别为0.46、0.44和0.42,Ni(Ⅲ)的相对含量减少,催化性能略微降低。
表 3 催化剂表面元素的相对占比Table 3. Relative proportion of catalyst surface elements元素Elements 峰位置Position 结合能/eVBinding energy 相对含量/% Relative content 新制备的催化剂New catalyst 处理过3000 min活性艳红K-2BP的催化剂Catalyst of K-2BP treated for 3000 min 处理过3000 min酸性大红3R的催化剂Catalyst of 3R treated for 3000 min 处理过3000 min活性黄X-R的催化剂Catalyst of X-R treated for 3000 min Ni Ni(OH)2,2p3/2 855.98 6.34 10.61 13.46 10.50 Ni Ni(OH)2,2p1/2 873.61 Ni NiOOH,2p3/2 861.86 3.92 4.84 5.95 4.43 Ni NiOOH,2p1/2 879.81 O O1s 531.40 87.67 83.08 78.46 83.83 S S2p 168.67 2.07 1.47 2.13 1.24 图13为新制备的催化剂的SEM照片。由图13可见,催化剂的表面比较平整,镍的沉淀物较为均匀且致密地包裹在氧化铝小球表面,因此,Ni2+不容易渗透到Al2O3小球里。β-NiOOH为球形粒子,β-Ni(OH)2具有六方晶系结构[23],两者紧密缠绕。
3. 结论 (Conclusion)
(1) NaClO催化氧化法对活性黄X-R废水的脱色效果欠佳,催化剂对脱色率的影响甚微。NaClO的直接氧化在脱色过程起了主导作用,原子氧的作用次之。
(2) NaClO催化氧化法更加适合于降解具有较多磺酸基和较高I/O值的偶氮染料。该工艺更加适合于降解稳定性强、耐氯性好的K型活性染料、含有磺酸钠盐的酸性染料和苯环染料。可以采用Mg(OH)2混凝法和Fenton法降解活性黄X-R染料。
(3) XPS分析表明,与用过3000 min的催化剂比较,新制备催化剂表面化学吸附氧占比略高;用过催化剂表面的Ni(Ⅲ)的相对含量减少,催化剂的性能略有降低。化学吸附氧消耗在染料的脱色降解。
-
表 1 THC、CBN、CBD检测的LC-MS/MS流动相洗脱梯度
Table 1. LC-MS/MS mobile phase elution gradient for the detection of THC, CBN and CBD
时间/minTime A/% B/% 0.0 95.0 5.0 0.5 95.0 5.0 6.0 5.0 95.0 8.0 5.0 95.0 8.1 95.0 5.0 10.0 95.0 5.0 表 2 目标物离子对及相应质谱检测参数
Table 2. Targeted ion pair and corresponding mass spectrum parameters for targets detection
目标物质Target substances 母离子Parent ionm/z 定量离子Quantitative ion 定性离子Qualitative ion 保留时间/minRetention time m/z DP/V CE/eV m/z DP/V CE/eV THC 315.1 193.1 80.0 32.30 259.4 80.0 27.30 7.33 CBN 311.0 223.1 80.0 30.24 241.3 80.0 29.60 7.21 CBD 315.1 193.1 80.0 32.30 259.4 80.0 27.30 6.91 THC-D3 318.3 196.3 80.0 29.88 262.1 80.0 28.87 7.30 CBN-D3 314.1 223.3 100.0 31.00 296.3 100.0 25.79 7.20 CBD-D3 318.3 196.3 80.0 29.88 262.1 80.0 28.87 6.91 THC-COOH 357.2 313.2 100.0 −35.00 245.3 100.0 −45.00 注:DP——去簇电压,CE——碰撞能量. 表 3 THC-COOH检测的LC-MS/MS流动相洗脱梯度
Table 3. LC-MS/MS mobile phase elution gradient for the detection of THC-COOH
时间/minTime A/% B/% 1.5 95.0 5.0 3.4 5.0 95.0 5.0 5.0 95.0 5.1 95.0 5.0 8.0 95.0 5.0 表 4 THC、CBN、CBD和THC-COOH标准品的线性回归方程(n = 11)
Table 4. Linear regression equations of THC, CBN, CBD and THC-COOH standards (n = 11)
目标物质Target substances 线性回归方程Linear regression equations 相关系数(R2)Related coefficient 检出限/(ng·mL−1) LOD THC Y = 1.26160 X +0.00413 0.9979 0.14 CBN Y = 0.79960 X +0.08911 0.9975 0.28 CBD Y = 0.96553 X −0.00675 0.9985 0.21 THC-COOH Y = 21815 X −43168 0.9967 1.62 表 5 避光、光照条件下18 h内生活污水中THC、CBN和CBD的去除率
Table 5. Removal rates of THC, CBN and CBD in domestic sewage within 18 h in dark and under light irradiation
保存条件Preservation conditions 保存时间/hPreservation time Ri/% THC CBN CBD 避光In dark 0 5.16 ± 6.03 −0.36 ± 1.29 1.69 ± 12.85 3 85.93 ± 1.99 90.32 ± 0.38 76.68 ± 0.67 6 87.63 ± 2.67 91.12 ± 4.81 85.75 ± 6.72 12 95.40 ± 1.90 98.94 ± 2.99 87.81 ± 1.59 18 97.50 ± 4.40 98.23 ± 1.16 97.77 ± 3.43 光照Under light irradiation 0 10.93 ± 4.10 −4.92 ± 1.06 10.90 ± 3.24 3 90.57 ± 3.58 92.53 ± 0.41 82.59 ± 2.15 6 94.43 ± 8.90 94.93 ± 1.58 86.45 ± 6.75 12 95.40 ± 0.73 98.30 ± 1.45 95.79 ± 11.87 18 98.96 ± 2.45 98.64 ± 0.43 96.63 ± 5.19 表 6 生活污水加标后样品避光保存24 h内THC、CBN、CBD和THC-COOH的去除率
Table 6. Removal rates of THC, CBN, CBD and THC-COOH in spiked domestic wastewaters within 24 hours in dark
保存时间/hPreservation time Ri/% THC CBN CBD THC-COOH 0 7.69 ± 7.60 −1.90 ± 7.07 4.31 ± 5.15 20.13 ± 3.22 3 92.09 ± 0.10 92.27 ± 0.78 86.61 ± 1.52 23.72 ± 1.56 6 97.88 ± 0.09 93.49 ± 0.94 88.27 ± 0.28 34.09 ± 2.86 12 95.95 ± 0.21 95.62 ± 1.45 94.50 ± 2.88 32.95 ± 0.47 18 95.55 ± 0.40 96.72 ± 4.64 95.04 ± 0.32 33.79 ± 2.20 24 100.00 ± 0.00 100.00 ± 0.00 98.39 ± 0.26 34.86 ± 2.54 表 7 污水加标样中目标物去除率与样品保存时间t和典型水质参数间的回归方差分析
Table 7. Variance analysis for the correlation between removal rates of THC, CBN, CBD, THC-COOH in spiked domestic wastewaters and sample preservation time t as well as common water quality parameters
目标物质Target substances F P R2 THC 7.602 0.021 0.901 CBN 6.878 0.026 0.892 CBD 8.253 0.018 0.908 THC-COOH 14.550 0.005 0.946 -
[1] 国家禁毒委员会办公室. 2021年中国毒情形势报[EB/OL]. [2023-10-31]. [2] 侯臣之, 花镇东, 徐鹏, 等. 基于污水分析法的毒情评估研究及应用进展[J]. 中国药科大学学报, 2018, 49(4): 502-508. HOU C Z, HUA Z D, XU P, et al. Research and application progress on evaluation of the abuse of illicit drugs based on wastewater analysis[J]. Journal of China Pharmaceutical University, 2018, 49(4): 502-508 (in Chinese).
[3] 郑晓雨, 袁明俊, 王德高, 等. 基于污水流行病学的毒情研判技术研究进展[J]. 生态毒理学报, 2020, 15(4): 79-87. doi: 10.7524/AJE.1673-5897.20190805001 ZHENG X Y, YUAN M J, WANG D G, et al. Sewage epidemiology for drug situation assessment[J]. Asian Journal of Ecotoxicology, 2020, 15(4): 79-87 (in Chinese). doi: 10.7524/AJE.1673-5897.20190805001
[4] 王德高. 污水流行病学[M]. 北京: 科学出版社, 2018. WANG D G. Sewage epidemiology[M]. Beijing: Science Press, 2018 (in Chinese).
[5] KHAN U, van NUIJS A L N, LI J, et al. Application of a sewage-based approach to assess the use of ten illicit drugs in four Chinese megacities[J]. Science of the Total Environment, 2014, 487: 710-721. doi: 10.1016/j.scitotenv.2014.01.043 [6] BIJLSMA L, EMKE E, HERNÁNDEZ F, et al. Investigation of drugs of abuse and relevant metabolites in Dutch sewage water by liquid chromatography coupled to high resolution mass spectrometry[J]. Chemosphere, 2012, 89(11): 1399-1406. doi: 10.1016/j.chemosphere.2012.05.110 [7] 胡鹏, 张艳, 郭昌胜, 等. 水环境中滥用药物的环境学研究进展[J]. 环境化学, 2017, 36(8): 1711-1723. doi: 10.7524/j.issn.0254-6108.2017010301 HU P, ZHANG Y, GUO C S, et al. Environmental studies on drugs of abuse in the aquatic environment[J]. Environmental Chemistry, 2017, 36(8): 1711-1723 (in Chinese). doi: 10.7524/j.issn.0254-6108.2017010301
[8] 董晓茹, 姜宴, 叶永红, 等. 大麻类物质体内代谢毒理及检测研究进展[J]. 药物分析杂志, 2016, 36(6): 939-949. DONG X R, JIANG Y, YE Y H, et al. Research progress on metabolism and determination of cannabinoids[J]. Chinese Journal of Pharmaceutical Analysis, 2016, 36(6): 939-949 (in Chinese).
[9] 孙维来, 郑晓雨, 赵彦彪, 等. 大麻组分检测及化学分型研究进展[J]. 中成药, 2019, 41(2): 402-411. doi: 10.3969/j.issn.1001-1528.2019.02.031 SUN W L, ZHENG X Y, ZHAO Y B, et al. Research progress on detection and chemical typing of hemp components[J]. Chinese Traditional Patent Medicine, 2019, 41(2): 402-411 (in Chinese). doi: 10.3969/j.issn.1001-1528.2019.02.031
[10] IZZO A A, BORRELLI F, CAPASSO R, et al. Non-psychotropic plant cannabinoids: New therapeutic opportunities from an ancient herb[J]. Trends in Pharmacological Sciences, 2009, 30(10): 515-527. doi: 10.1016/j.tips.2009.07.006 [11] 李成, 郑秋达, 杜娟, 等. 污水流行病学方法评价大连市人群烟草流行率[J]. 环境卫生学杂志, 2017, 7(1): 15-18,23. LI C, ZHENG Q D, DU J, et al. Exploitation of sewage epidemiological survey to investigate tobacco consumption in Dalian[J]. Journal of Environmental Hygiene, 2017, 7(1): 15-18,23 (in Chinese).
[12] 叶璞, 游文丹, 杨滨, 等. 典型药物在医院废水和城市污水处理厂中的污染特征及去除情况[J]. 环境科学, 2021, 42(6): 2928-2936. YE P, YOU W D, YANG B, et al. Pollution characteristics and removal of typical pharmaceuticals in hospital wastewater and municipal wastewater treatment plants[J]. Environmental Science, 2021, 42(6): 2928-2936 (in Chinese).
[13] 王龙, 朱丹, 曹云霄, 等. 北京市污水处理厂出水中药物和个人护理品的季节变化及其生态风险评价[J]. 环境科学学报, 2021, 41(7): 2922-2932. WANG L, ZHU D, CAO Y X, et al. Seasonal changes and ecological risk assessment of pharmaceutical and personal care products in the effluents of wastewater treatment plants in Beijing[J]. Acta Scientiae Circumstantiae, 2021, 41(7): 2922-2932 (in Chinese).
[14] POSTIGO C, de ALDA M L, BARCELÓ D. Evaluation of drugs of abuse use and trends in a prison through wastewater analysis[J]. Environment International, 2011, 37(1): 49-55. doi: 10.1016/j.envint.2010.06.012 [15] 金航标, 杨丹, 赵美蓉, 等. 以污水流行病学监测广西某市12个污水处理厂服务区域精神活性物质的消耗量[J]. 环境化学, 2022, 41(1): 251-259. doi: 10.7524/j.issn.0254-6108.2020082802 JIN H B, YANG D, ZHAO M R, et al. Estimation of the consumption of psychoactive substances in the service areas of 12 wastewater treatment plants in a city of Guangxi, China using wastewater-based epidemiology[J]. Environmental Chemistry, 2022, 41(1): 251-259 (in Chinese). doi: 10.7524/j.issn.0254-6108.2020082802
[16] BAKER D R, KASPRZYK-HORDERN B. Multi-residue analysis of drugs of abuse in wastewater and surface water by solid-phase extraction and liquid chromatography-positive electrospray ionisation tandem mass spectrometry[J]. Journal of Chromatography A, 2011, 1218(12): 1620-1631. doi: 10.1016/j.chroma.2011.01.060 [17] JAIDEE W, SIRIDECHAKORN I, NESSOPA S, et al. Kinetics of CBD, Δ9-THC degradation and cannabinol formation in Cannabis resin at various temperature and pH conditions[J]. Cannabis and Cannabinoid Research, 2022, 7(4): 537-547. doi: 10.1089/can.2021.0004 [18] 房梦月, 刘和平, 陈志香, 等. 污水水质参数与精神活性物质检测准确度的相关性初探[J]. 中国司法鉴定, 2022(5): 57-66. doi: 10.3969/j.issn.1671-2072.2022.05.007 FANG M Y, LIU H P, CHEN Z X, et al. The correlation study between the sewage parameters and the accuracy of psychoactive substances detection[J]. Chinese Journal of Forensic Sciences, 2022(5): 57-66 (in Chinese). doi: 10.3969/j.issn.1671-2072.2022.05.007
[19] CAUSANILLES A, BAZ-LOMBA J A, BURGARD D A, et al. Improving wastewater-based epidemiology to estimate cannabis use: focus on the initial aspects of the analytical procedure[J]. Analytica Chimica Acta, 2017, 988: 27-33. doi: 10.1016/j.aca.2017.08.011 [20] HEUETT N V, BATCHU S R, GARDINALI P R. Understanding the magnitude of emergent contaminant releases through target screening and metabolite identification using high resolution mass spectrometry: Illicit drugs in raw sewage influents[J]. Journal of Hazardous Materials, 2015, 282: 41-50. doi: 10.1016/j.jhazmat.2014.08.009 [21] HOW Z T, GAMAL EL-DIN M. A critical review on the detection, occurrence, fate, toxicity, and removal of cannabinoids in the water system and the environment[J]. Environmental Pollution, 2021, 268: 115642. doi: 10.1016/j.envpol.2020.115642 [22] 孙维来, 赵彦彪, 郑晓雨, 等. 不同储存条件对大麻化学稳定性的影响[J]. 广西植物, 2017, 37(9): 1204-1212. doi: 10.11931/guihaia.gxzw201706018 SUN W L, ZHAO Y B, ZHENG X Y, et al. Effects of storage conditions on the chemical potency of Cannabis[J]. Guihaia, 2017, 37(9): 1204-1212 (in Chinese). doi: 10.11931/guihaia.gxzw201706018
[23] 杨雨, 刘超, 孙武兴, 等. 大麻二酚的强制降解研究[J]. 绿色科技, 2020(8): 143-146,149. doi: 10.3969/j.issn.1674-9944.2020.08.058 YANG Y, LIU C, SUN W X, et al. Study on forced degradation of cannabidiol[J]. Journal of Green Science and Technology, 2020(8): 143-146,149 (in Chinese). doi: 10.3969/j.issn.1674-9944.2020.08.058
[24] BOIX C, IBÁÑEZ M, BIJLSMA L, et al. Investigation of cannabis biomarkers and transformation products in waters by liquid chromatography coupled to time of flight and triple quadrupole mass spectrometry[J]. Chemosphere, 2014, 99: 64-71. doi: 10.1016/j.chemosphere.2013.10.007 [25] CARMONA E, ANDREU V, PICÓ Y. Occurrence of acidic pharmaceuticals and personal care products in Turia River Basin: From waste to drinking water[J]. Science of the Total Environment, 2014, 484: 53-63. doi: 10.1016/j.scitotenv.2014.02.085 [26] Di MARCANTONIO C, CHIAVOLA A, GIOIA V, et al. A step forward on site-specific environmental risk assessment and insight into the main influencing factors of CECs removal from wastewater[J]. Journal of Environmental Management, 2023, 325(Pt A): 116541. -









 下载:
下载: