-
西藏一江两河(雅鲁藏布江山南段、拉萨河、年楚河)流域地处青藏高原腹地. 该流域面积仅占西藏的5.48%,但人口约占总人口的1/3,经济总量也远超西藏其他区域[1]. 一江两河流域的农业活动和特殊的水文地质,使得水体中重金属含量引起广泛关注. 人工神经网络(ANNs)是以数学模型模拟神经元活动的一种信息处理系统,表现出优于传统模型的特点,是近年来的研究热点[2-3]. 其中,反向传播神经网络(BPNN)是典型的人工神经网络,在水体透明度遥感估算[4]、土壤重金属含量[5]、空气质量指数[6]、降雨量[7]、水中化学需氧量(COD)[8] 和溶解氧 (DO)[9]等预测研究方面具有广泛应用,也可以用于预测水体中重金属浓度.
国外已有较多的研究将BPNN运用到水体重金属预测,Rooki等[10]采用BPNN对酸性矿水中重金属铜(Cu)、铁(Fe)、锰(Mn)、锌(Zn)进行预测,得到预测值与实测值的相关系数R分别为0.92、0.22、0.92和0.92,表明BPNN可以作为一种可行的方法来快速和经济有效地预测酸性矿水中的重金属含量. 国内大多数研究将BPNN运用于水质中其他指标的监测. 符东等[11]为准确掌握沱江水质状况,探明沱江主要污染物,对沱江水质进行了模糊综合评价和BPNN预测. 研究表明,沱江受总氮的污染较为严重,构建沱江的BPNN模型可实现沱江总氮浓度的准确预测. 李峻等[12]以水质因子CODCr为例,构建并训练BPNN预测模型,对青弋江水质进行时空预测,并用实际监测值检验预测精度,结果表明BPNN在青弋江水质的预测方面是一种简单有效的方法. 目前针对青藏高原一江两河流域的研究,很少有直观的针对该流域中水体重金属浓度进行预测,大多数局限于生态风险评价和水质时空特征分析方面. 周晨霓等[13]对西藏拉萨河流域进行水质监测,并利用单污染指数法评价单因子对环境产生的等效影响程度,采用综合指数法评价该流域水质综合质量现状. 李红敬等[14]对雅鲁藏布江的水质研究结果表明,雅鲁藏布江干流中上游江段Cu含量超出渔业水质标准.
青藏高原一江两河流域水环境复杂,地球化学水文地质各因素之间的影响关系不明确,许多仪器和方法在高原上并不适用,传统水质预测方式普遍存在着操作繁琐、预测精度不高等问题,所以亟需寻找一种新的简单可行的途径去预测高原水体中重金属浓度,从而为防治水体重金属污染提供参考依据. BPNN具有强大的非线性映射能力和自动学习、适应能力,在分析处理复杂的水质关系方面,可以提高预测精度,降低预测方式操作难度,得到拟合程度较高的实测值和预测值的曲线. 因此将BPNN用于青藏高原一江两河重金属浓度预测研究是一种新的思路和途径.
年楚河流域农田土壤重金属研究表明砷(As)、Mn在该流域的平均浓度超过其背景值[15]. 西藏中部河流和湖泊表层沉积物重金属研究结果显示锑(Sb)与As显著相关,表明Sb和As来源相似,不仅受到农业活动影响,亦受地热等因素影响[16]. 本文对一江两河流域水体中金属检出水平和Pearson相关性分析,发现钼(Mo)和As、Sb显著相关,表明水体中Mo和As、Sb具有相同来源. 基于以上研究,本文选择以As、Sb、Mn、Mo元素为研究对象,通过建立BPNN模型,预测该流域水环境中4种重金属浓度,旨在了解河流中4种元素的环境行为,进而揭示一江两河流域的水体环境洁净度,为预防青藏高原水环境污染提供数据参考和理论支持.
-
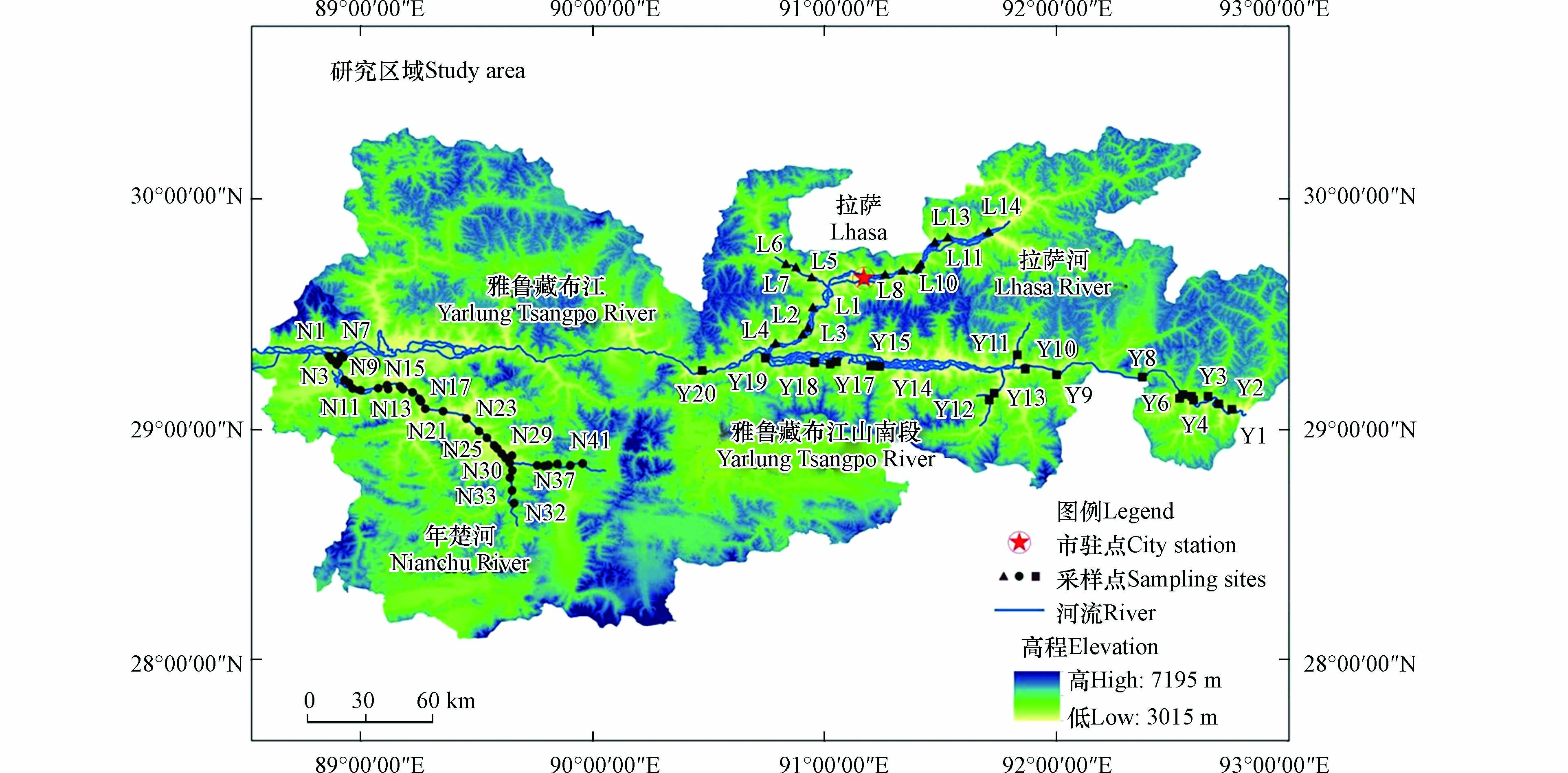
雅鲁藏布江是青藏高原的最长的河流,具有年楚河、拉萨河等主要支流[17]. 研究区域的范围为28°40′44′′N—29°51′38′′N,88°51′50′′E—92°45′34′′E,如图1所示,采样点主要集中在雅鲁藏布江的山南段、年楚河和拉萨河流域,一江两河流域受人类活动影响较大.
水样的采集严格按照《水质采样技术指导》(HJ494-2009). 2021年9—10月,从雅鲁藏布江山南段、拉萨河和年楚河流域采集了75个样品,其中在年楚河流域共41个采样点,编号为N1-41,布设间隔约2.5—10 km;在拉萨河流域共14个采样点,编号为L1-14,布设间隔约5—10 km;在雅鲁藏布江山南段共20个采样点,编号为Y1-20,布设间隔约5—10 km. 采样点平均海拔高度达到3762.68 m,平均大气压约为58.28 kPa.
水质分析检测严格按照《饮用天然矿泉检验方法》(GB 8538-2016)、《生活饮用水标准检验方法》(GB/T 5750-2006)进行. 采用便携式溶氧仪(JPB-607A)和便携式多功能参数测量仪(PCS Testr 35)现场测定:溶解氧(DO)(量程 0.00—20.00 mg·L−1,分辨率 0.01 mg·L−1)、水温(T)(量程 0.0—50.0 ℃,分辨率 0.1 ℃)、电导率(EC)(量程 0.0—199.9 μS·cm−1、200—1999 μS·cm−1、2.00—20.00 mS·cm−1,分辨率 0.1 μS·cm−1、1 μS·cm−1、0.01 mS·cm−1)、pH(量程 0.00—14.00)、总溶解固体(TDS)(量程 0.0—99.9 mg·L−1、100—999 mg·L−1、1.00—10.00 ng·L−1,分辨率0.1 mg·L−1、1 mg·L−1、0.01 ng·L−1)、盐度(SAL)(量程0.0—99.9 mg·L−1、100—999 mg·L−1、1.0—10.00 ng·L−1;分辨率0.1 mg·L−1、1 mg·L−1、0.01 ng·L−1). 通过电感耦合等离子体发射光谱仪(Optima 5300DV)检测Fe(方法检出限MDL:0.0045 mg·L−1)、Sb(MDL:0.000078 mg·L−1)、Mo(MDL:0.00006 mg·L−1)、Mn(MDL:0.00006 mg·L−1);原子荧光光谱仪(AFS-830)检测As(MDL:0.0004 mg·L−1);紫外可见分光光度计(Lamda35)检测氨氮含量(NH3-N)(MDL:0.02 mg·L−1)和总磷(TP)(MDL:0.01 mg·L−1).
-
运用ArcGIS 10.7作研究区域图,通过Origin 2021对输入层变量进行Pearson相关性分析,再用MATLAB R2020b处理水样数据. 本研究将水样的DO、pH、EC、TP和Fe为神经网络的输入层,以As、Sb、Mo、Mn含量作为网络的输出层. 最佳隐藏层的确定是基于MATLAB R2020b神经网络的Levenberg-Marquardt (LM)的算法训练,计算部分分为训练集、验证集和测试集的3组,以数据70%为训练集,验证集和测试集各15%,训练次数1000次,选出最佳的R值和MSE值.
-
由于水体中重金属行为的复杂性,输入数据大小和输入参数多少不能确保测试阶段模型的运行一定不会出现错误[18]. 因此,识别最佳输入组合是模型建立的第一步. Fe在西藏河流含量丰富,而且Fe的产生与其他金属关系密切[19-20]. 因此,为了更好的建模效果,本研究选择Fe为输入参数,此外,DO、pH、EC、TDS、SAL、T、NH3-N、TP的值被认为是输入参数的候选者.
-
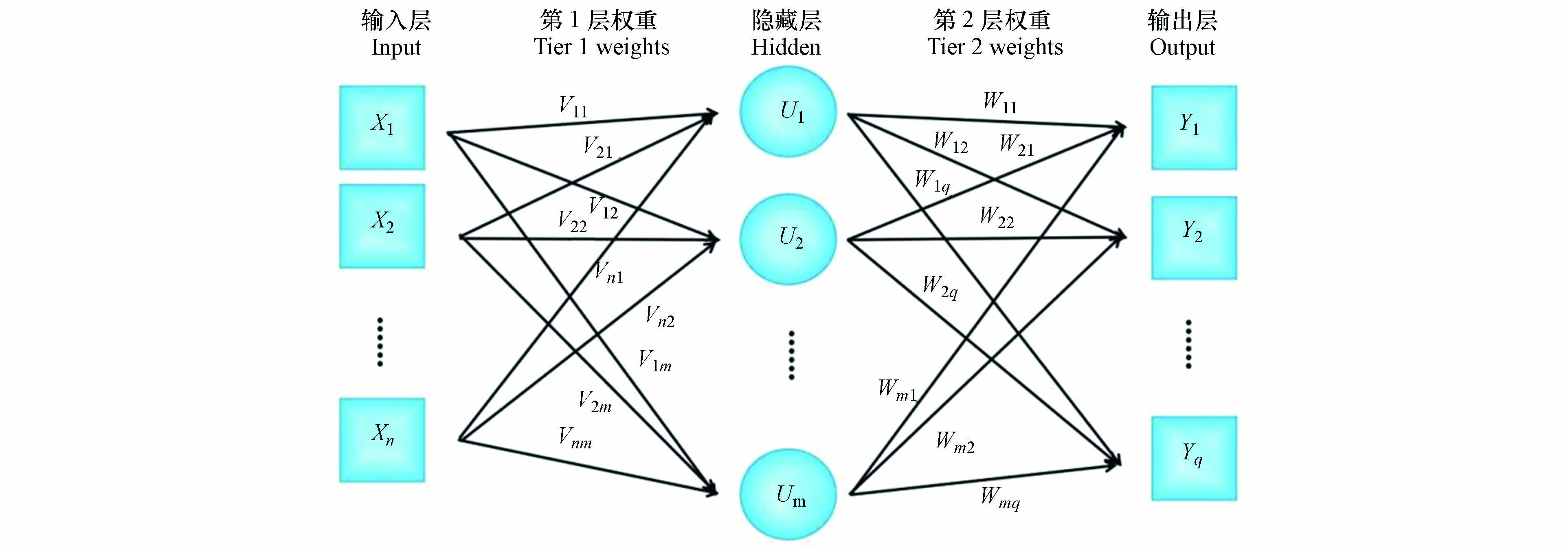
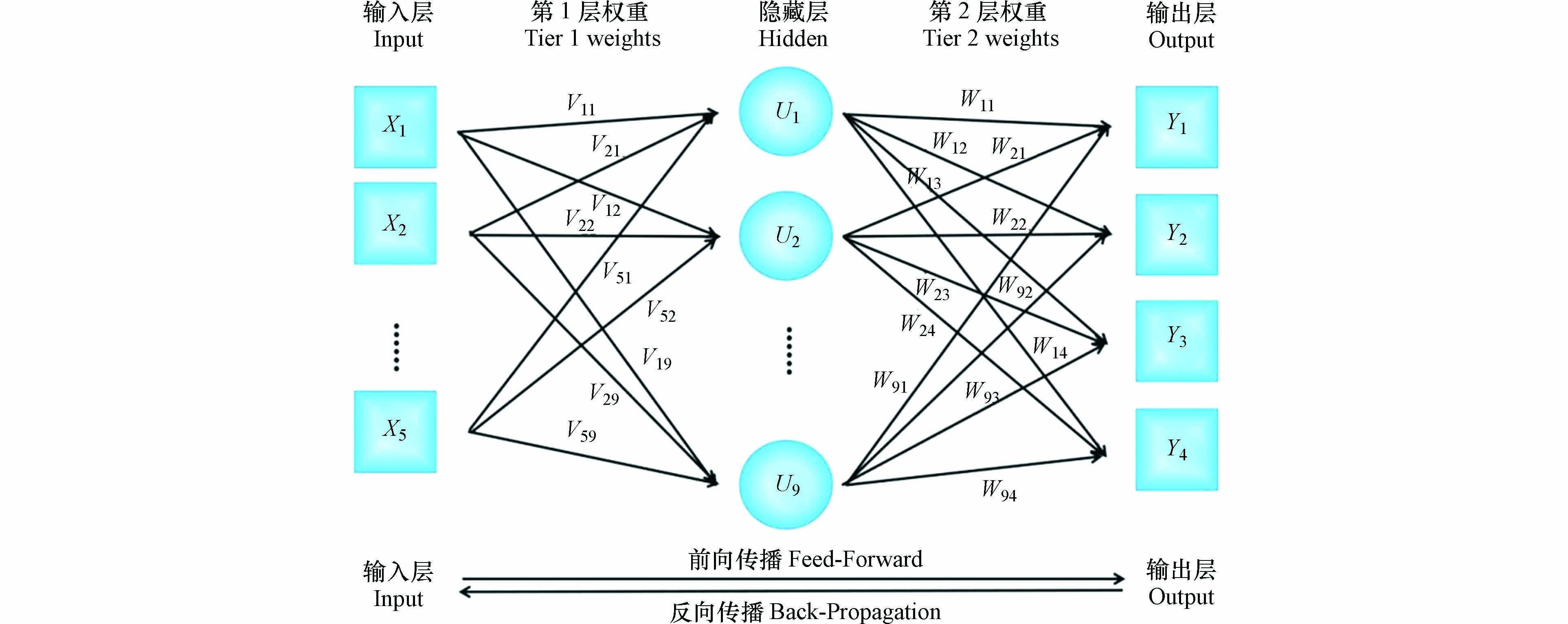
BPNN采用三层网络结构,由输入层、隐藏层和输出层组成,通过LM算法训练,如图2所示,LM是一种经典的反向传播算法和启发式算法,依靠数值优化技术来加速计算过程,从而实现更快的训练[21]. BPNN的最佳隐藏神经元数量由试错程序确定.
在前向传播公式中隐藏层神经元
uj 的输出,如公式(1)所示:式中,
vij 为第i个输入变量与第j个隐藏层神经元的权重;buj 为隐藏层u第j个神经元的阀值,或者称为偏置项.在前向传播公式中输出层神经元
yk 的输出,如公式(2)所示:式中, w jk 为第 j 个隐藏层神经元与第 k 个输出层神经元的权重; byk 为输出层 y 第 k 个神经元的阀值,激活函数由MATLAB R2020b中的tansig、logsig和purelin选择.
在反向传播过程中,使用平方误差函数,得到第p个样本的误差
Ep . 目标旨在让真实值与预测值之间的误差尽可能小[22],目标函数(3)设定为:式中,
ˆypk 是神经网络预测的输出值,ypk 是真实的输出值.LM算法类似于牛顿式中Hessian矩阵[22] ,如公式(4):
式中,J是雅可比矩阵,包含权重和偏差的网络误差的一阶导数;E是网络误差的向量;μ是一个标量,其初始值为 0.001;I是单位矩阵;Δw表示当前权重值的调整.
采用的三层网络. 隐藏层中的数量由方程式中给出的经验公式(5)进行估算[23]:
其中,m是隐藏层中的神经元数量;n是输入变量的数量;q是输出变量的数量;a是 0—10之间的常数,通过反复试验确定其最佳值并逐渐改变隐藏层中的节点数来确定隐藏层的最佳神经元数. 由此可得隐藏层神经元m在3—13范围内,选择RMSE相对较小,R相对较大的最佳隐藏层神经元数.
-
通过决定系数R2和均方根误差RMSE的误差来评估模型的性能. R2用于评估模型的预测能力和准确性,如方程式(6)所示[24]:
RMSE是实测值( yj)和预测值(
ˆyj )之间差异的量度,用方程式(7)表示[25]:R2值越高,RMSE值越低,表明适应度越好,实测与预测之间的差异越小. 通常,R2大于0.6且RMSE小于实测值范围的10%被认为是两个系列之间的可接受适应度.
-
(1) 输入选择
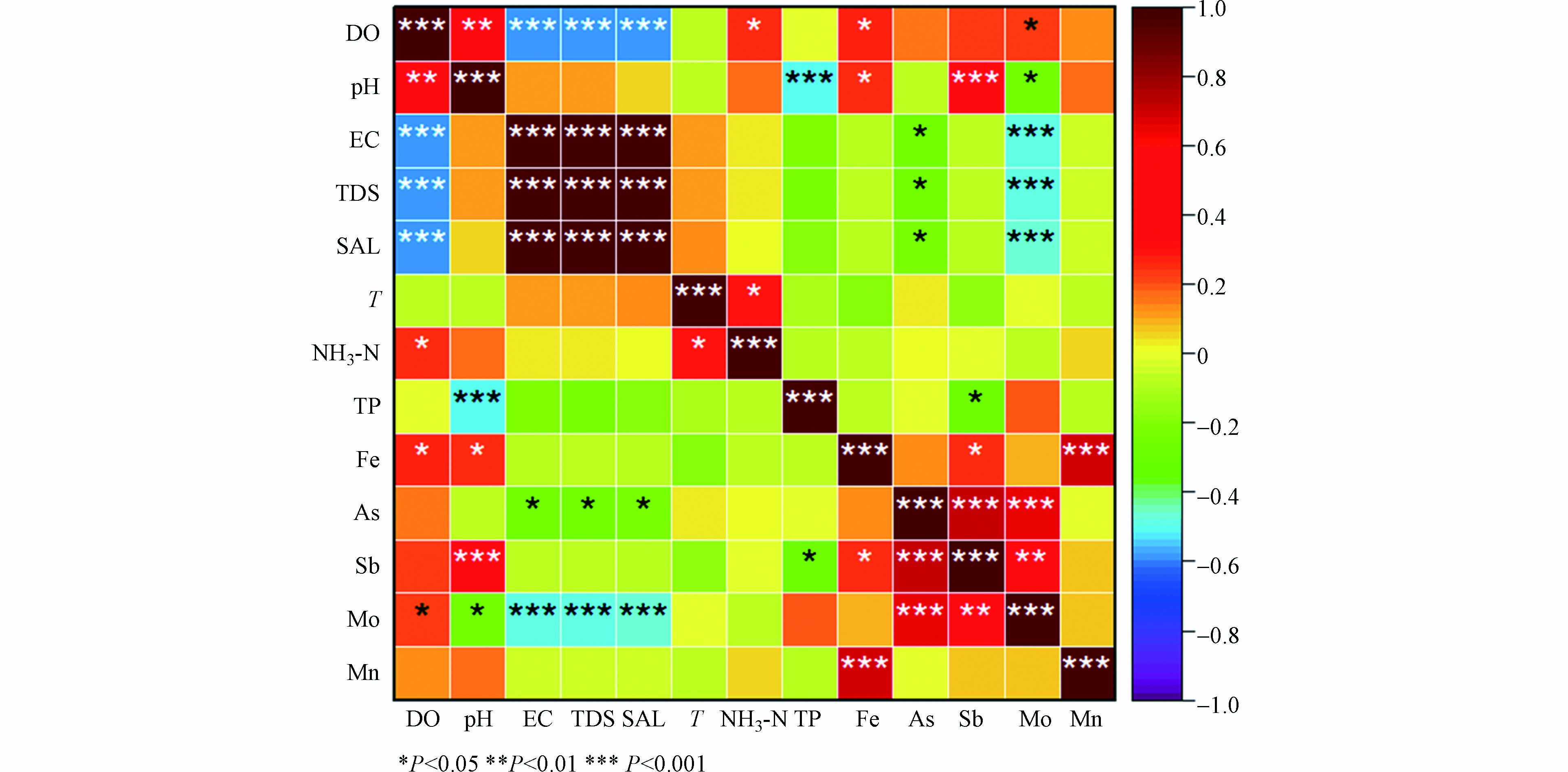
已有研究表明,Fe、As、Sb、Mo和Mn的出现通常与工业活动有关[26]. 但是青藏高原受工业污染较轻,因此河流中这些元素主要受到农业活动和高原地质影响[27-32]. pH值会影响水中TP、Fe、Sb和Mo的浓度. 此外,pH值和DO会影响水中Mo、Fe的形态. As和Mo可以传导电流,呈现固有的EC值[33-34]. 考虑到Pearson相关系数的统计分析和显著性分析,选择最优输入变量组合来估计重金属浓度,从图3可以看出,除了T和NH3-N,其他输入变量与预测因子之间的都呈现显著性相关水平(P<0.05),此外,要选择差异大的自变量作为输入变量,由于EC和TDS、SAL具有强相关性,剔除TDS和SAL,因此将DO、pH、EC、TP、Fe作为输入变量.
(2) 输入层贡献值分析
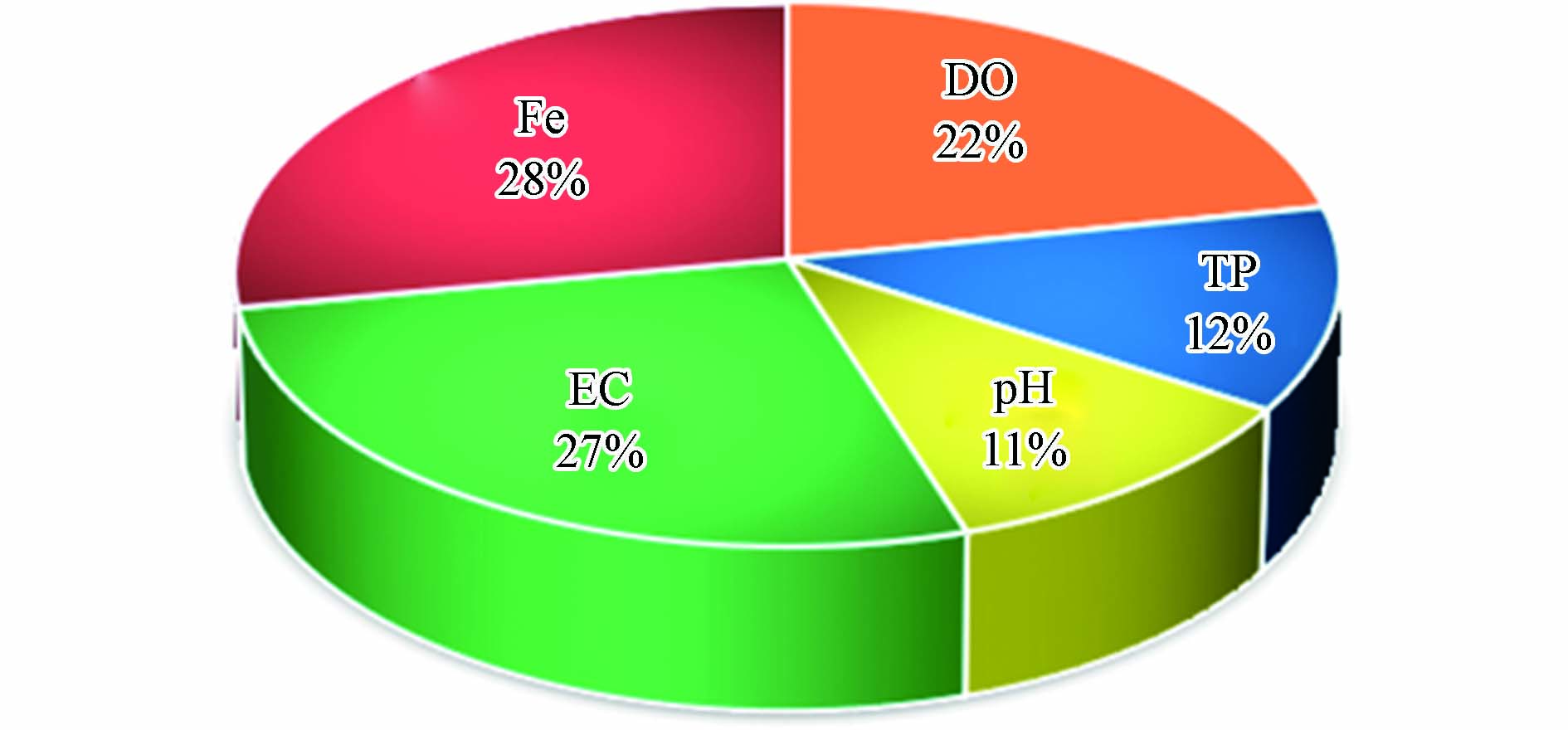
输入层因子DO、pH、EC、TP、Fe单独对As、Sb、Mo、Mn浓度的响应贡献值,如图4所示,DO贡献22%,pH贡献11%,EC贡献27%,TP贡献12%,Fe贡献28%.
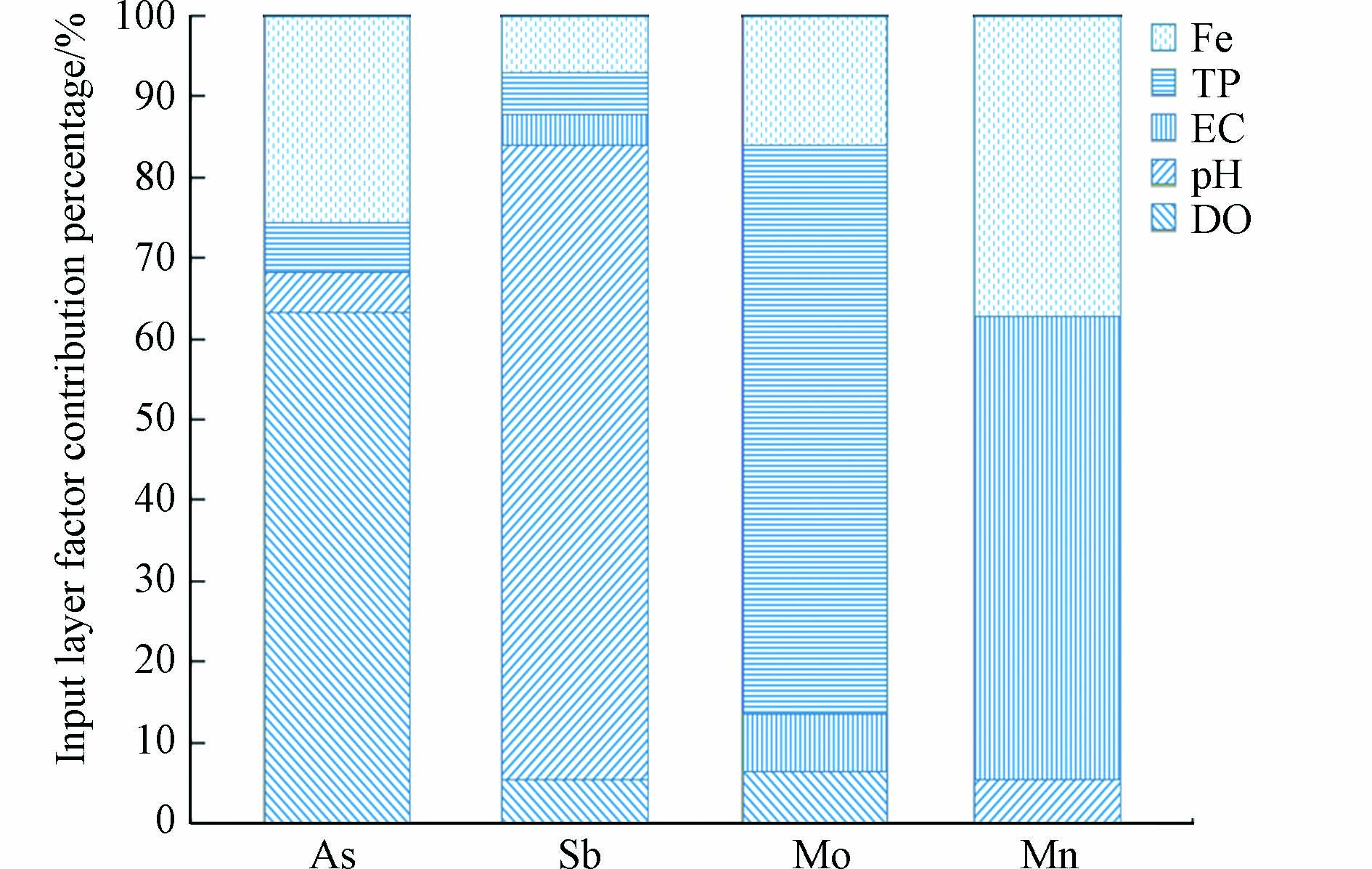
运用PMF软件计算出5个输入层因子对单独输出层元素As、Sb、Mo、Mn相对贡献指纹图,如图5所示. (1)如果输出层是As,DO贡献63.5%,pH贡献4.6%,EC贡献0.3%,TP贡献5.9%,Fe贡献25.7%;(2)如果输出层是Sb,DO贡献5.3%,pH贡献78.9%,EC贡献3.6%,TP贡献5.3%,Fe贡献6.9%;(3)如果输出层是Mo,DO贡献6.5%,EC贡献7.1%,TP贡献70.6%,Fe贡献15.8%;(4)如果输出层是Mn,pH贡献5.6%,EC贡献57.2%,Fe贡献37.2%.
(3) 输出选择
BPNN模型构建需要确定输入层数据和输出层数据,输入层数据为不同输入因子的实测值,由Pearson分析确定为DO、pH、EC、TP、Fe,输出层数据为水体中重金属(As、Sb、Mo、Mn)浓度的预测值. 运用Matlab神经网络可以得到4个预测因子 (隐藏层神经元数在m=3—13范围内) 的相关系数 (R) 和均方误差 (MSE) 值. 从表1 重金属浓度预测值和实测值的R和MSE可以看出,无论输出层为单元素(As、Sb、Mo、Mn),还是4个元素共同作为输出层,最佳隐藏层神经元数都为9.
(4) 模型结构
BPNN隐含层神经元的传递函数采用双曲正切S形函数tansig,输出层神经元传递函数采用线性激励函数purelin,训练函数为trainlm,训练算法为LM. 具体的BPNN结构:(1)单元素作为输出层: BPNN结构是5-9-1 ;(2)4个元素共同作为输出层:如图6所示,BPNN结构是5-9-4.
-
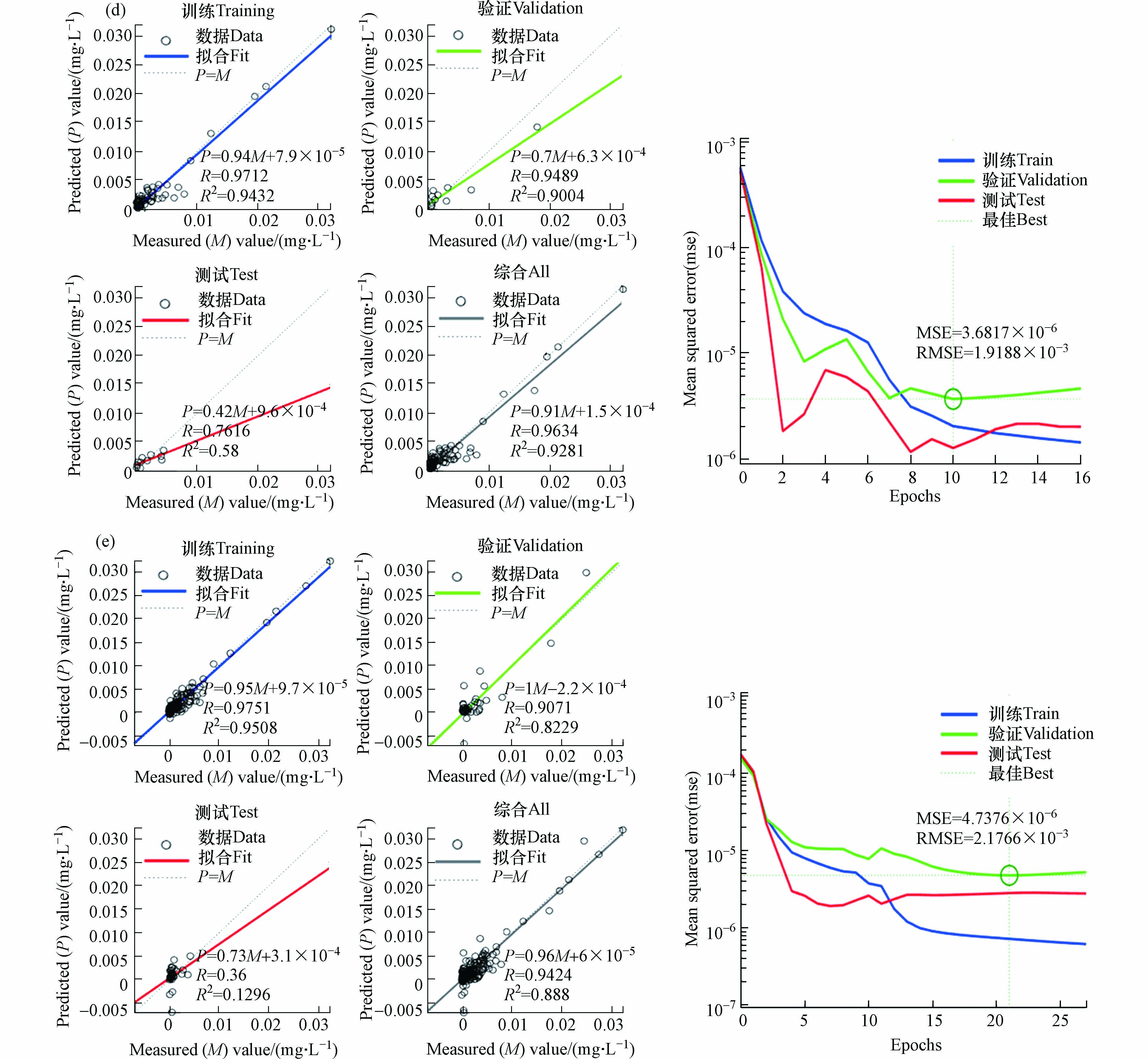
根据构建的BPNN预测模型,MATLAB进行编程,利用样本数据进行预测,重金属预测值与实测值的相关系数(R)、决定系数(R2)、均方误差(MSE)、均方根误差(RMSE)如图7 所示. 通过训练集、验证集、测试集曲线拟合得到综合曲线. 综合曲线反应了各元素预测值(P)和实测值(M)的相关性,如As预测值和实测值的关系曲线(图7a):P=0.98×M-3.1×10−5,相关系数R=0.99,决定系数R2=0.98,最优迭代26次时,均方误差MSE=9.4417×10−7,均方根误差RMSE=9.7168×10−4. 同理Sb预测值和实测值的关系曲线(图7b):P=0.96×M+1.4×10−5,相关系数R=0.966,决定系数R2=0.933,最优迭代16次时,均方误差MSE=1.5644×10−8,均方根误差RMSE=1.2508×10−4;Mo的预测值和实测值的关系曲线(图7c):P=0.96×M+8.3×10−5,相关系数R=0.946,决定系数R2=0.894,最优迭代13次时,均方误差MSE=1.0995×10−7,均方根误差RMSE=3.3159×10−4;Mn的预测值和实测值的关系曲线(图7d):P=0.91×M+1.5×10−4,相关系数R=0.963,决定系数R2=0.928,最优迭代10次时,均方误差MSE=3.6817×10−6,均方根误差RMSE=1.9188×10−3;4个元素的预测值和实测值的关系曲线(图7e):P=0.96×M+6×10−5,相关系数R=0.942,决定系数R2=0.888,最优迭代21次时,均方误差MSE=4.7376×10−6,均方根误差RMSE=2.1766×10−3.
R 越接近1,相关性越高,预测值和实测值越接近,表明拟合程度越好,预测精度越高. 从图7 中R值对比看出,(1)BPNN模型对4个元素预测效果排序:As(0.99)
> Sb(0.966)> Mn(0.963)> Mo(0.946);(2) BPNN模型单独对4个元素预测效果比同时对4个元素预测效果好. 该模型预测重金属As、Sb、Mo、Mn浓度拟合直线明显靠近期望值1∶1直线,MSE数值越低,说明预测效果较好,用该预测模型进行河流重金属浓度的预测是可行的.R2值都达到0.6以上,且RMSE值小于实测值范围的10%,说明该预测模型能较好应用于西藏一江两河流域水体中重金属浓度的预测.
-
青藏高原地理位置特殊,水体环境复杂,本研究通过建立BPNN模型对一江两河流域水体中重金属浓度进行预测,提高了预测精度,降低了操作难度,得到的各重金属浓度实测值和预测值的曲线且拟合程度较高,能够较好地监测一江两河流域水体中重金属的浓度,揭示水环境的清洁程度,进而为研究青藏高原其他水体中重金属浓度预测提供参考.
(1) BPNN模型以DO、pH、EC、TP、Fe作为网络的输入层,以As、Sb、Mo、Mn的含量单独或共同作为网络的输出层进行对比分析,使用LM算法进行训练. 研究发现每个元素单独作为输出层时BPNN的拟合效果会比共同作为输出层更好.
(2) BPNN对As、Sb、Mo、Mn预测效果排序:As
> Sb> Mn> Mo,整体来说,模型对As拟合程度最好,预测精度也相对最高.
基于BPNN的一江两河流域水体中重金属浓度预测
Prediction of heavy metal concentration in water of one river and two tributaries based on BPNN
-
摘要: 本文将反向传播神经网络(BPNN)应用于青藏高原一江两河流域(雅鲁藏布江山南段、拉萨河、年楚河)水体中重金属浓度预测,探讨了输入变量、预测因子、隐藏层节点数和模型结构的影响. 模型以溶解氧(DO)、pH、电导率(EC)、总磷(TP)、铁(Fe)作为网络的输入层,重金属砷(As)、锑(Sb)、钼(Mo)、锰(Mn)的含量作为网络的输出层,使用Levenberg-Marquardt (LM)算法进行训练. 其中,BPNN隐藏层的传递函数为tansig,隐藏层节点数为9,输出层的传递函数为purelin,输出层节点数为4. 结果表明:(1)以单个元素作为预测因子时,As、Sb、Mo、Mn预测值和实测值的决定系数(R2)分别为0.98、0.933、0.894、0.928;均方根误差(RMSE)分别为:9.7168×10−4、1.2508×10−4、3.3159×10−4、1.9188×10−3. (2)以4个元素作为预测因子时,预测值和实测值的决定系数(R2)为0.888;均方根误差(RMSE)为2.1766×10−3. R2值越高,RMSE值越低,表明实测值和预测值拟合程度和适应性良好,证明BPNN能较好地应用于青藏高原一江两河流域水体中重金属浓度预测.
-
关键词:
- 反向传播神经网络(BPNN) /
- 一江两河流域 /
- 重金属 /
- 青藏高原
Abstract: In this paper, backpropagation neural network (BPNN) is applied to the prediction of heavy metal concentration in water bodies of one river and two tributaries basins (the Shannan section of Yarlung Tsangpo River, Lhasa River and Nianchu River) of the Qinghai-Tibet Plateau, and the influence of input variables, predictors, number of hidden layer nodes and model structure are discussed. The model uses dissolved oxygen (DO), pH, electrical conductivity (EC), total phosphorus (TP) and iron (Fe) as the input layer of the network, and the content of heavy metals arsenic (As), antimony (Sb), molybdenum (Mo) and manganese (Mn) as the output layer of the network. Levenberg-Marquardt (LM) algorithm is used for training. The transfer function of the BPNN hidden layer is tansig and the number of nodes in the hidden layer is 9, and the transfer function of the output layer is purelin and the number of nodes in the output layer is 4. The results showed that : (1) When a single element was used as a predictor, the determination coefficients (R2) of the predicted and measured values of As, Sb, Mo and Mn were 0.98, 0.933, 0.894 and 0.928, respectively. The root mean square error (RMSE) was 9.7168×10−4, 1.2508×10−4, 3.3159×10−4 and 1.9188×10−3, respectively. (2) When the four elements were used as predictors, the determination coefficients (R2) between the predicted and measured values was 0.888. The root mean square error (RMSE) was 2.1766×10−3. The higher the R2 value, the lower the RMSE value, indicating that the measured and predicted values are well fitted and adaptable, which proves that BPNN can be better applied to the prediction of heavy metal concentrations in water bodies in one river and two tributaries basins on the Qinghai-Tibet Plateau. -
餐饮源污染物成分复杂[1-2],它们是食物烹饪和加工过程中产生的挥发性油脂等有机物,以及加热分解或开裂的产物等. 根据它们的形态,一般可分为颗粒物和气态物质[3-4]. 餐饮源污染物的排放多数属于低空排放,排放后可冷凝形成颗粒物,因此餐饮源是二次有机气溶胶(SOA)的重要前体物[5]. 餐饮源排放的PM2.5可占到PM10的80%及以上,PM1.0可占到PM2.5的50%—85%[6]. 针对颗粒物的组分分析通常包括分析有机碳(OC)分析、元素碳(EC)分析、有无机离子组分分析、元素组分分析、多环芳烃(PAHs)分析等. 气体物质主要为VOCs,成分复杂多达上百种,餐饮源VOCs主要分为烷烃、烯烃、芳香烃、卤代烃、醇类、醛酮类和其它等[7-9]. VOCs种类繁多,可分为烷烃、烯烃、芳香烃、卤代烃、OVOCs和其他类等,污染源的VOCs成分谱是对污染源排放的污染物进行采样、分析并计算各物种污染物质量浓度百分比的过程,对于后续的模型模拟研究、机理研究等存在重要的意义,是不可或缺的基础数据[10].
1980年左右,美国最早开展VOCs成分谱研究. EPA开发了 SPECIATE 数据库,是一个较为全面记录VOCs成分谱的数据库,并且不断更新,目前被广泛应用于大气污染研究[11]. Wei[12]估算了2005—2020年中国人为源VOCs详细的化学特征,计算了7个活性扇区的VOCs的化学分布情况,计算了我国VOCs按照烷烃、烯烃/炔烃、芳香烃、醇、酮、醛、酯、醚和卤代烃的占比情况,并预测了其15年内的占比变化情况. 此外还分析了东西部省份之间VOCs组分的差异和排放量,是一份较为完善详细的成分谱. Lee等[13]研究了烤肉类VOCs的排放特征,通过实测法获取率烤肉店VOCs的排放特征及其排放因子,苯、醋酸乙烯酯、己烯和丁烷是主要的VOCs. 我国在VOCs源成分谱的上取得了一定的研究成果,但在本地化源成分谱的研究、源谱物质统一性和基础数据的获取上均存在一定的不足[10,14-16].
为获得成都市餐饮源114种VOCs排放特征,建立餐饮源VOCs成分谱;并探索餐饮源VOCs全组分特征,故进行本研究.
1. 材料与方法(Materials and methods)
1.1 监测对象选择依据
餐饮源具有一定的复杂性,餐饮类型、餐饮规模、采样时间段等都会影响最终的采样结果. 为尽量全面、准确地评估成都市餐饮源的VOCs污染情况,在采样前,通过高德地图POI结合现场问卷调查的方式对于成都市餐饮源情况进行调查分析.
首先,通过高德地图POI数据获取成都市餐饮源位置、数量及餐饮类型等情况,得到成都市餐饮源中烧烤、中餐、快餐、火锅和其他类型的占比情况,分别为7.3%、44.5%、34.1%、10.0%和4.1%. 烧烤、中餐、快餐、火锅累计占比达95%以上.
其次,通过问卷调查获得成都市不同餐饮类型的用油量、餐饮规模、燃料类型、用餐时间段及油烟净化设施情况等. 问卷调查范围包括5个主城区(锦江区、青羊区、成华区、高新区和天府新区)、2个二圈层区县(郫都区和青白江区)、2个三圈层县级市(彭州市和邛崃市),共计收回有效问卷716份. 问卷调查结果表明,中餐类中川菜占比最高;在规模方面,特大型及大型占比31.0%,中型占比32.4%,小型占比36.6%;家庭餐饮和食堂餐饮的人均用油量、燃料类型等差异不大.
综上所述,餐饮源监测对象的选择上,涵盖烧烤、川菜、商业综合体、快餐、火锅、家庭餐饮和食堂餐饮,以及小型、中型、大型和特大型4种规模. 在监测前还需要通过实地走访和现场调查,综合考虑餐饮企业油烟排放口位置是否便于采样、采样时能否有电力保障等采样基础条件,并在烹饪高峰期进行采样. 本研究涵盖的餐饮类型与规模较为全面且具有本地特色,具有一定的代表性.
1.2 监测对象信息
综合考虑餐饮企业餐饮类型、餐饮规模以及污染物的产生与排放情况等,选择了7家典型餐饮企业作为社会餐饮监测对象,涵盖烧烤、川菜、商业综合体、快餐和火锅5种类型和小型、中型、大型和特大型4种规模,涵盖的餐饮类型与规模较为全面且具有成都市本地特色;3家家庭餐饮监测对象包含25年以上老旧低层住宅(家庭1)、15年以上高层住宅(家庭2)和5年左右较新的高层住宅(家庭3);选择1家市级事业单位的中型规模食堂作为食堂餐饮监测对象;11个餐饮源监测对象基本信息见表1. 监测对象能一定程度地反映成都市餐饮源污染情况,具有一定的代表性.
表 1 监测对象基本信息Table 1. Monitoring objects’ basic information监测对象Monitoring objects 采样时间/hSampling time 排风量/(m3·h−1)Exhaust air volume 用油量/kgAmount of oil used 就餐人数/人Number of diners 灶头数量/个Number of stoves 油烟净化设施Fume purification facilities 中型烧烤 1 25788 2.5 70 4 静电式 小型烧烤 1 10443 1 35 4 静电式 中型川菜 1 16908 14.6 133 8 静电式 特大型川菜 1 44214 25 273 21 静电式 商业综合体 1 20457 18.65 158 26 静电式 大型快餐 1 3599 15.8 100 12 静电式 中型火锅 0.5 600 2.5 5 23 静电式 家庭1 0.5 600 0.25 8 2 家用油烟机 家庭2 0.5 600 0.15 5 2 家用油烟机 家庭3 0.5 960 0.2 7 2 家用油烟机 中型食堂 0.5 6800 7 100 3 静电式 根据问卷调查结果,社会餐饮就餐高峰期集中在11:30—12:30和18:00—19:00,故选择在中午或晚上就餐高峰期采样,采样时间设置为1.0 h. 家庭餐饮和食堂餐饮通常烹饪一餐的时间只有0.5 h,故采样时间设置为0.5 h. 火锅的监测时间覆盖包间内客人就餐全过程,也为0.5 h.
1.3 采样方法
根据《固定污染源排气中颗粒物测定与气态污染物采样方法》(GB/T 16157—1996)对社会餐饮和食堂餐饮进行采样. 家庭餐饮采样点设置遵守《室内环境空气质量监测技术规范》(HJ/T 167—2004),在关闭门窗及抽油烟机的情况下进行采样[17-19];所有污染物均需采集现场空白样品.
1.4 监测方法及质控
监测方法根据《固定污染源废气挥发性有机物的采样气袋法》(HJ 732—2014),采用ZR3520真空箱气袋采样器和聚氟乙烯(PVF)气袋进行采样. 调节采样器的抽气速率,每次采集时间为5—10 min,烹饪全过程采样,并采集现场空白样,样品采集后避光保存并在8 h内进行分析. 根据《固定污染源废气总烃、甲烷和非甲烷总烃的测定气相色谱法》(HJ 38—2017)测定NMHCs浓度.
质控 样品采集后避光保存并在8 h内进行分析;样品校准曲线相关系数均大于0.995,满足HJ38—2017的规定要求;实验室空白样品的测定值小于检出限,满足规定要求;选取10%的样品,作为实验室平行样进行分析,相对偏差均小于15%,满足规定要求.
1.5 114种VOCs组分分析
1.5.1 组分分析方法
采样方法同1.2节,烹饪全过程采样,并采集现场空白样. 在NMHCs浓度分析完成后,将NMHCs浓度最高的1个气袋中的气体进行VOCs组分分析,得到监测对象样品浓度. 将现场空白样按照同样的方法进行VOCs组分分析,得到背景浓度.
按照《环境空气挥发性有机物的测定罐采样/气相色谱-质谱法》(HJ 759—2015),VOCs气体样品在冷阱中浓缩,进行热解,进入气相色谱法分离,用质谱检测器检测,通过与标准物质质谱图以及保留时间进行比较,用内标法进行定量. 气体样品首先通入自动预浓缩仪进行前处理. 一级冷阱为空阱,去除水汽;二级冷阱装有Tenax吸附剂,去除CO2;三级冷阱(空管)冷冻聚焦,富集VOCs组分. 经过三级冷阱中进行预浓缩后系统迅速升温,使冷阱中富集的VOCs组分进入GC/MS-FID系统,进行分离和定量. 气相分析过程利用了冷柱箱装置,使柱温能达到-50 ℃. VOCs组分通过HP-1色谱柱(60 m×0.32 mm×1.0 μm)进行分离,进入MSD进行检测.
1.5.2 仪器配置与标气
Entech7200三级冷阱浓缩仪;安捷伦7890B-5977B 气相色谱质谱联用仪. 采用PAMS、TO-15、13种醛酮类3种标准气体(Linde , USA)和含有4 种化合物(一溴一氯甲烷、1,4-二氟苯、氯苯-d5和4-溴氟苯)的内标标准气对仪器进行标定.
1.5.3 质量保证和质量控制
仪器分析前用4-溴氟苯检查GC/MS的性能,符合标准要求;实验室空白和运输空白中目标物的浓度必须低于方法测定下限;每24 h对校准曲线的中间浓度点进行分析,测量值与初始浓度值的相对偏差在30%以下.
1.6 VOCs全组分分析
1.6.1 全组分样品采集
采用吸附管(不锈钢材质,内径5 mm)采集VOCs样品,采样流量为50 mL·min−1,采样持续时间为1—3 h. 采样前,吸附管需经过老化处理24 h. 吸附管采用Tenax为吸附剂.
采样点:油烟排气口,具体的点位设置应遵守《固定污染源排气中颗粒物测定与气态污染物采样方法》(GB/T 16157—1996),采样点位于餐馆排烟筒的采样孔内(净化设施后).
采样时间:中午或晚上营业高峰期,持续1—3 h.
1.6.2 全组分分析方法
VOCs样品分析遵循《固定污染源废气挥发性有机物的测定固相吸附-热脱附/气相色谱-质谱法》(HJ 734—2014)的具体分析步骤,分析得到样品中VOCs的成分. 将吸附管置于热脱附仪中进行二级热脱附,脱附气体经气相色谱分离后用质谱检测. 根据污染物质谱图、保留时间(min)、匹配因子(%)和峰面积等信息,基于内标法计算,确定餐饮源VOCs污染物物种.
1.6.3 仪器与设备
TW-2100型微小流量空气采样器:青岛拓威智能仪器有限公司;Agilent 6890气相色谱仪:美国Agilent公司;Agilent 5973质谱检测器:美国Agilent公司.
1.6.4 质量保证和质量控制
实验室空白和运输空白中目标物的浓度必须低于方法测定下限;每批样品应校核点的相对误差应在30%以内.
2. 结果与讨论(Results and discussion)
2.1 餐饮源VOCs成分谱建立
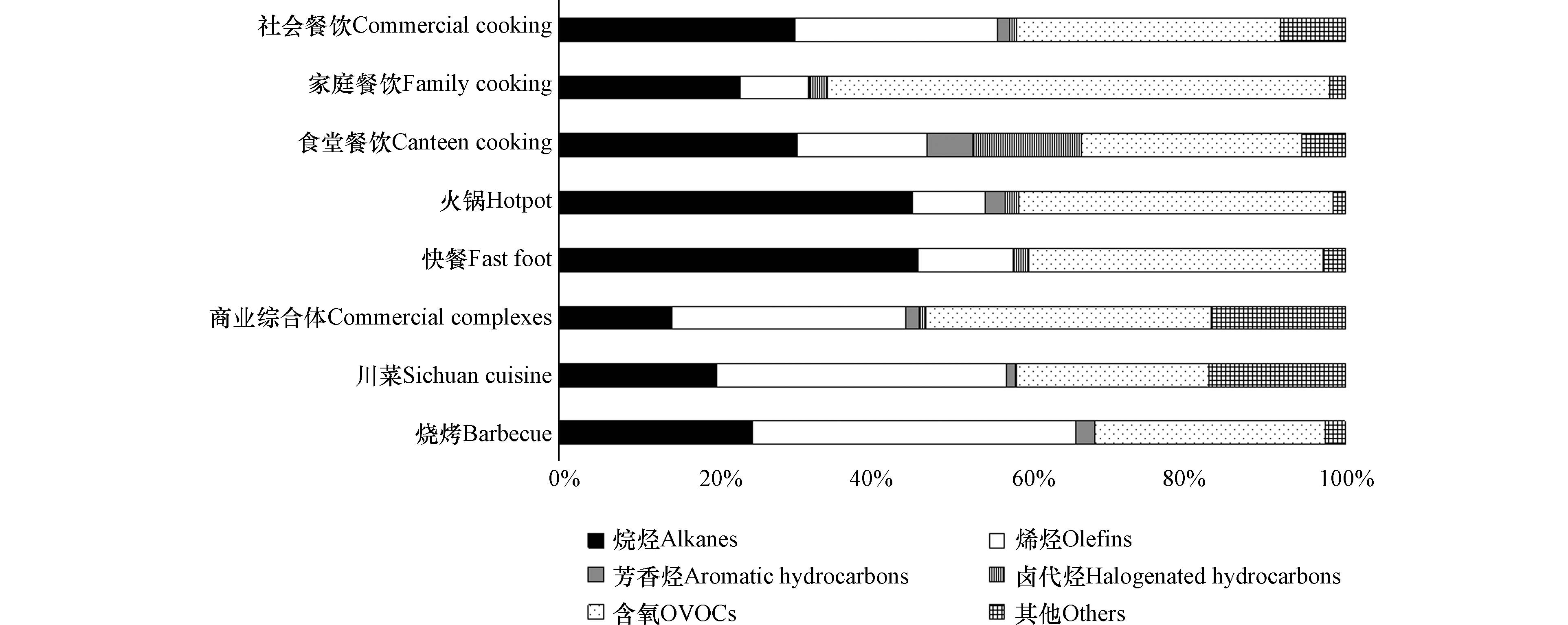
成都市餐饮源VOCs各组分浓度质量百分比详见表2,建立成都市餐饮源成分谱. 将VOCs组分分为烷烃、烯烃、芳香烃、卤代烃、OVOCs和其他六类. 由表2可知,餐饮源中烷烃占比为23.12%—30.29%,烯烃占比为8.61%—25.78%,芳香烃占比为0.16%—5.86%,卤代烃占比为0.86%—13.82%,OVOCs占比为28.02%—63.77%,其他占比为2.02%—8.26%. OVOCs、烷烃和烯烃3类占比最高,3类污染物累计质量浓度百分比在75%以上,是餐饮源重要的污染物类型.
表 2 成都市餐饮源VOCs成分谱组分质量分数表(%)Table 2. Mass fraction of VOCs composition source profile for catering sources in Chengdu(%)序号Serial number 组分类别Grouping categories 化合物名称Name of compound 社会餐饮Commercial cooking 家庭餐饮Family cooking 食堂餐饮Canteen cooking 占比Percentage 标准差Standard deviation 占比Percentage 标准差Standard deviation 占比Percentage 标准差Standard deviation 1 烷烃 乙烷 10.44 11.11 4.50 1.51 14.68 1.21 2 烷烃 丙烷 2.70 2.23 2.49 2.87 0.72 0.05 3 烷烃 异丁烷 1.25 1.49 2.86 3.47 0.30 0.19 4 烷烃 正丁烷 2.70 1.37 2.65 2.99 1.14 0.22 5 烷烃 异戊烷 1.14 1.08 0.65 0.46 0.50 0.15 6 烷烃 正戊烷 9.42 11.59 6.42 4.61 1.39 0.30 7 烷烃 环戊烷 0.03 0.04 0.00 0.00 0.13 0.06 8 烷烃 2,2-二甲基丁烷 0.26 0.43 0.00 0.00 8.81 4.15 9 烷烃 2,3-二甲基丁烷 0.03 0.03 0.03 0.04 0.04 0.02 10 烷烃 2-甲基戊烷 0.04 0.07 0.00 0.00 0.17 0.08 11 烷烃 3-甲基戊烷 0.00 0.01 0.00 0.00 0.13 0.06 12 烷烃 正己烷 0.21 0.28 0.08 0.12 0.13 0.06 13 烷烃 甲基环戊烷 0.01 0.02 0.00 0.00 0.06 0.03 14 烷烃 环己烷 0.00 0.01 0.00 0.00 0.08 0.04 15 烷烃 2,4-二甲基戊烷 0.04 0.08 0.00 0.00 0.10 0.05 16 烷烃 2-甲基己烷 0.00 0.00 0.00 0.00 0.30 0.14 17 烷烃 2,3-二甲基戊烷 0.00 0.00 0.00 0.00 0.11 0.05 18 烷烃 3-甲基己烷 0.00 0.00 0.00 0.00 0.33 0.16 19 烷烃 正庚烷 0.98 1.58 1.19 1.69 0.15 0.06 20 烷烃 甲基环己烷 0.01 0.01 0.00 0.00 0.06 0.03 21 烷烃 2,2,4-三甲基戊烷 0.00 0.00 0.00 0.00 0.00 0.00 22 烷烃 2,3,4-三甲基戊烷 0.00 0.00 0.00 0.00 0.14 0.07 23 烷烃 2-甲基庚烷 0.00 0.01 0.00 0.00 0.20 0.09 24 烷烃 3-甲基庚烷 0.00 0.01 0.00 0.00 0.13 0.06 25 烷烃 正辛烷 0.61 1.07 1.18 1.67 0.09 0.04 26 烷烃 正壬烷 0.03 0.05 0.00 0.00 0.04 0.02 27 烷烃 癸烷 0.00 0.01 0.00 0.00 0.00 0.00 28 烷烃 十一烷 0.03 0.02 0.02 0.02 0.36 0.16 29 烷烃 十二烷 0.02 0.02 1.05 1.37 0.00 0.02 烷烃小计 29.97 — 23.12 — 30.29 — 30 烯烃 乙烯 8.63 6.36 2.44 1.74 12.52 3.06 31 烯烃 丙烯 1.83 1.24 0.93 0.81 0.50 0.55 32 烯烃 正丁烯 1.20 0.51 0.26 0.18 0.28 0.28 33 烯烃 丁二烯 10.78 9.07 3.00 2.12 0.15 8.52 34 烯烃 反式-2-丁烯 0.33 0.34 0.01 0.02 1.68 0.79 35 烯烃 顺式-2-丁烯 0.25 0.25 0.00 0.00 0.55 0.26 36 烯烃 1-戊烯 1.77 2.74 0.14 0.20 0.04 0.17 37 烯烃 异戊二烯 0.26 0.44 1.72 1.13 0.05 0.04 38 烯烃 反式-2-戊烯 0.31 0.48 0.07 0.10 0.40 0.19 39 烯烃 顺式-2-戊烯 0.06 0.08 0.00 0.00 0.13 0.06 40 烯烃 1-己烯 0.34 0.39 0.04 0.06 0.21 0.09 烯烃小计 25.78 — 8.61 — 16.51 — 41 芳香烃 苯 0.76 0.46 0.08 0.06 0.32 0.18 42 芳香烃 甲苯 0.62 0.73 0.08 0.12 0.99 0.41 43 芳香烃 乙苯 0.02 0.04 0.00 0.00 0.73 0.35 44 芳香烃 间、对二甲苯 0.19 0.22 0.00 0.00 1.21 0.51 45 芳香烃 苯乙烯 0.01 0.02 0.00 0.00 1.02 0.48 46 芳香烃 邻二甲苯 0.01 0.01 0.00 0.00 0.58 0.27 47 芳香烃 异丙苯 0.01 0.01 0.00 0.00 0.04 0.02 48 芳香烃 正丙苯 0.00 0.00 0.00 0.00 0.00 0.00 49 芳香烃 间乙基甲苯 0.00 0.00 0.00 0.00 0.11 0.05 50 芳香烃 对乙基甲苯 0.01 0.02 0.00 0.00 0.28 0.13 51 芳香烃 1,3,5-三甲基苯 0.00 0.00 0.00 0.00 0.06 0.03 52 芳香烃 邻乙基甲苯 0.01 0.01 0.00 0.00 0.21 0.10 53 芳香烃 1,2,4-三甲苯 0.00 0.00 0.00 0.00 0.11 0.05 54 芳香烃 1,2,3-三甲苯 0.00 0.00 0.00 0.00 0.10 0.05 55 芳香烃 间二乙基苯 0.00 0.00 0.00 0.00 0.03 0.01 56 芳香烃 对二乙基苯 0.00 0.00 0.00 0.00 0.03 0.01 57 芳香烃 萘 0.00 0.01 0.00 0.00 0.04 0.02 芳香烃小计 1.63 — 0.16 — 5.86 — 58 卤代烃 二氟二氯甲烷 0.00 0.00 0.00 0.00 0.00 0.00 59 卤代烃 一氯甲烷 0.26 0.38 0.40 0.36 0.25 0.10 60 卤代烃 一溴甲烷 0.00 0.00 0.00 0.00 0.00 0.00 61 卤代烃 一氟三氯甲烷 0.00 0.00 0.00 0.00 0.08 0.04 62 卤代烃 二氯甲烷 0.05 0.06 0.15 0.13 0.67 0.30 63 卤代烃 三氯甲烷 0.08 0.11 0.23 0.30 0.13 0.06 64 卤代烃 四氯化碳 0.00 0.00 0.00 0.00 0.04 0.02 65 卤代烃 一溴二氯甲烷 0.00 0.01 0.00 0.00 0.00 0.00 66 卤代烃 二溴一氯甲烷 0.00 0.00 0.00 0.00 0.00 0.00 67 卤代烃 三溴甲烷 0.00 0.00 0.00 0.00 0.00 0.00 68 卤代烃 四氟二氯乙烷 0.00 0.00 0.00 0.00 0.00 0.00 69 卤代烃 氯乙烯 0.00 0.01 0.00 0.00 0.09 0.04 70 卤代烃 氯乙烷 0.00 0.01 0.00 0.00 0.00 0.00 71 卤代烃 1,1-二氯乙烯 0.00 0.00 0.00 0.00 0.00 0.00 72 卤代烃 三氟三氯乙烷 0.00 0.00 0.00 0.00 0.00 0.00 73 卤代烃 反式-1,2-二氯乙烯 0.00 0.00 0.00 0.00 0.04 0.02 74 卤代烃 1,1-二氯乙烷 0.00 0.00 0.00 0.00 0.22 0.11 75 卤代烃 顺式-1,2-二氯乙烯 0.00 0.00 0.00 0.00 0.00 0.00 76 卤代烃 1,2-二氯乙烷 0.13 0.17 1.54 1.36 0.38 0.18 77 卤代烃 1,1,1-三氯乙烷 0.00 0.00 0.00 0.00 0.00 0.00 78 卤代烃 三氯乙烯 0.00 0.00 0.00 0.00 0.00 0.00 79 卤代烃 1,1,2-三氯乙烷 0.00 0.00 0.00 0.00 0.00 0.00 80 卤代烃 1,2-二溴乙烷 0.00 0.00 0.00 0.00 0.00 0.00 81 卤代烃 四氯乙烯 0.00 0.00 0.00 0.00 0.00 0.00 82 卤代烃 四氯乙烷 0.00 0.00 0.00 0.00 0.00 0.00 83 卤代烃 1,2-二氯丙烷 0.00 0.01 0.00 0.00 0.06 0.03 84 卤代烃 反式-1,3-二氯-1-丙烯 0.05 0.10 0.00 0.00 0.67 0.32 85 卤代烃 顺式-1,3-二氯-1-丙烯 0.14 0.28 0.00 0.00 10.06 4.74 86 卤代烃 六氯丁二烯 0.00 0.01 0.00 0.00 0.04 0.02 87 卤代烃 氯苯 0.03 0.06 0.00 0.00 0.36 0.17 88 卤代烃 对二氯苯 0.00 0.01 0.00 0.00 0.03 0.01 89 卤代烃 间二氯苯 0.02 0.03 0.00 0.00 0.63 0.30 90 卤代烃 邻二氯苯 0.00 0.00 0.00 0.00 0.00 0.00 91 卤代烃 1,2,4-三氯苯 0.00 0.01 0.00 0.00 0.03 0.01 92 卤代烃 氯代甲苯 0.07 0.15 0.00 0.00 0.04 0.02 卤代烃小计 0.86 — 2.32 — 13.82 — 93 含氧 乙醛 10.95 4.56 9.01 8.89 8.57 1.44 94 含氧 丙烯醛 8.88 3.40 24.32 14.56 0.15 4.99 95 含氧 丙酮 4.31 4.33 20.19 13.78 3.51 0.99 96 含氧 丙醛 1.12 1.41 0.08 0.12 0.76 0.31 97 含氧 甲基丙烯醛 0.48 0.73 0.17 0.14 3.19 1.48 98 含氧 乙酸乙烯酯 0.15 0.28 0.00 0.00 0.00 0.00 99 含氧 正丁醛 0.65 0.38 0.36 0.52 1.08 0.24 100 含氧 2-丁酮 0.18 0.20 0.02 0.03 1.55 0.72 101 含氧 乙酸乙酯 0.59 0.60 5.33 6.71 3.21 1.27 102 含氧 四氢呋喃 0.00 0.01 0.00 0.00 0.13 0.06 103 含氧 丁烯醛 0.02 0.03 0.40 0.56 0.21 0.10 104 含氧 1,4-二氧六环 0.00 0.01 0.00 0.00 0.03 0.01 105 含氧 甲基叔丁基醚 0.07 0.13 0.03 0.04 2.81 1.32 106 含氧 戊醛 2.33 1.35 1.17 1.66 0.74 0.58 107 含氧 甲基丙烯酸甲酯 0.11 0.21 0.03 0.04 0.21 0.10 108 含氧 4-甲基-2-戊酮 0.00 0.01 0.00 0.00 0.34 0.16 109 含氧 2-己酮 0.08 0.11 0.00 0.00 0.13 0.06 110 含氧 己醛 3.47 1.02 2.50 3.11 0.54 1.81 111 含氧 苯甲醛 0.01 0.01 0.16 0.22 0.15 0.06 112 含氧 间甲基苯甲醛 0.09 0.17 0.00 0.00 0.71 0.33 OVOCs小计 33.51 — 63.77 — 28.02 — 113 其他 二硫化碳 0.01 0.02 0.39 0.28 0.38 0.18 114 其他 乙炔 8.25 7.29 1.63 0.21 5.14 7.72 其他小计 8.26 — 2.02 — 5.52 — 注:食堂餐饮标准差与川菜1、川菜2计算得到. Note: The standard deviation of canteen catering was calculated with Sichuan Cuisine 1 and Sichuan Cuisine 2. 由表2可知,社会餐饮共检测出87种VOCs,其中烷烃24种、烯烃11种、芳香烃13种、卤代烃17种、OVOCs 20种、其他2种;家庭餐饮共检测出43种VOCs,其中烷烃12种、烯烃9种、芳香烃2种,卤代烃4种、OVOCs 14种、其他2种;食堂餐饮共检测出92种VOCs,其中烷烃26种、烯烃11种、芳香烃16种、卤代烃18种、OVOCs 19种、其他2种. 社会餐饮和食堂餐饮VOCs组分较家庭餐饮更为复杂,家庭餐饮烷烃、芳香烃和卤代烃污染物的种类较少.
如图1所示,社会餐饮中OVOCs(33.51%)、烷烃(29.97%)和烯烃(25.78%)的3类占比最高,是社会餐饮重要的污染物类型. OVOCs污染物物种方面,醛酮类较为重要,其中乙醛(6.19%—17.69%)、丙烯醛(4.89%—15.05%)、丙酮(2.34%—10.77%)、己醛(2.23%—4.8%)和戊醛(1.02%—4.91%)占比较高,是社会餐饮OVOCs中的代表性物质. 川菜、烧烤的烯烃占比高,可能与有大火烹饪过程的、烹饪温度较高有关,而对于火锅和快餐这类烹饪温度较低的餐饮类型烷烃占比相对较高.
家庭餐饮中OVOCs(63.76%)和烷烃(23.12%)两类占比最高,是家庭餐饮重要的污染物类型. 家庭餐饮中芳香烃的含量最低,扣除VOCs背景浓度的影响,仅检测到苯和甲苯两种苯系物,有文献指出[15]烹饪燃料、食用油量及油温影响餐饮源VOCs苯系物的排放. 家庭餐饮相较于社会餐饮和食堂餐饮其用油量较小、油温较低,使得其苯系物产生较少.
食堂餐饮中烷烃(30.29%)和OVOCs(28.02%)两类占比最高,是食堂餐饮重要的污染物类型. 其中芳香烃浓度占比为5.86%,高于社会餐饮和家庭餐饮,且芳香烃检出种类最多,这可能与食用油油温有关. 何万清[20]的研究表明,当食用油在130℃低温及260℃高温时,其产生的芳香烃种类最多.
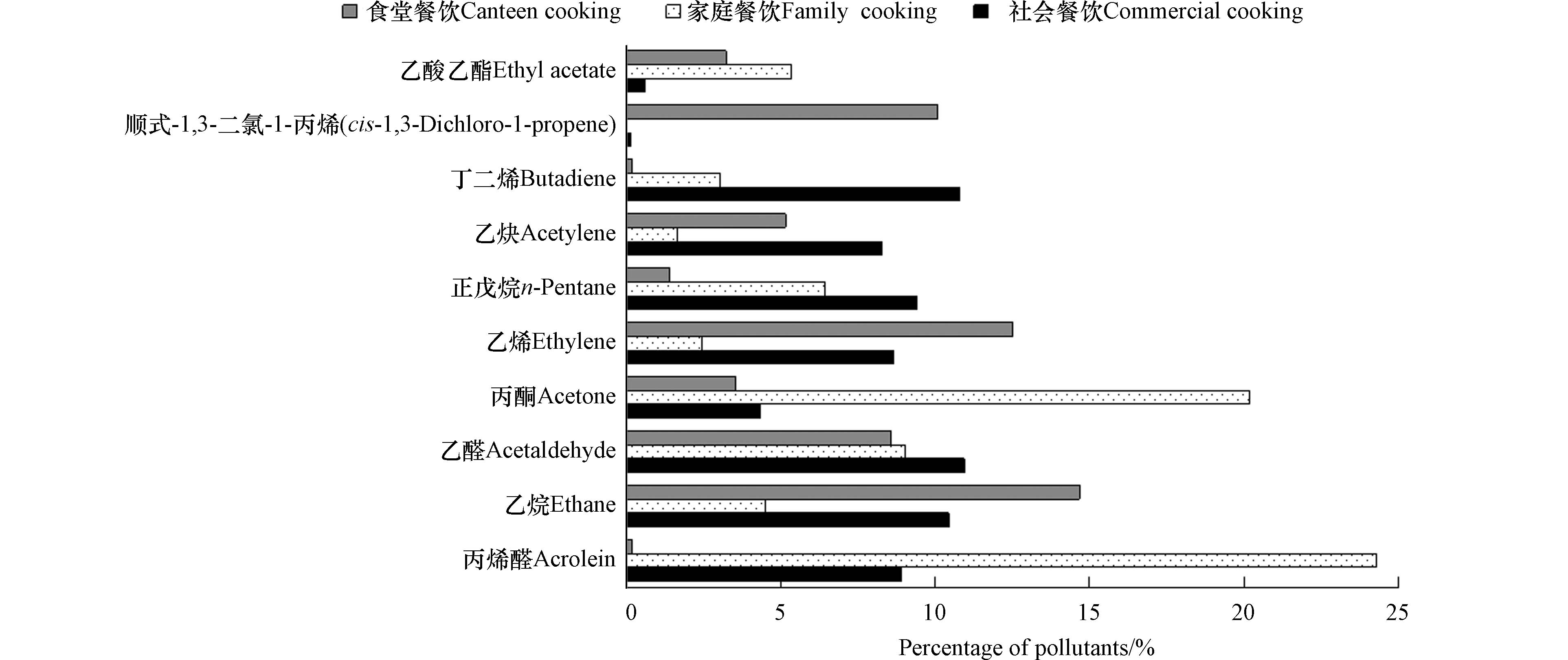
本研究涵盖多种餐饮类型,不同类型的特征污染物略有不同,详见表3. 根据不同餐饮类型污染物占比均值大小,计算餐饮源排名前10的VOCs分别是丙烯醛(11.12%)、乙烷(9.87%)、乙醛(9.51%)、丙酮(9.34%)、乙烯(7.86%)、正戊烷(5.74%)、乙炔(5.01%)、丁二烯(4.64%)、顺式-1,3-二氯-1-丙烯(3.4%)和乙酸乙酯(3.04%),如图2所示. 它们在污染物浓度中占有较高权重,是餐饮源的特征污染物.
表 3 不同餐饮类型VOCs特征污染物Table 3. VOCs characteristic pollutants of different catering types类型Types 特征VOCsCharacteristics of VOCs 社会餐饮 乙醛(11.13%)、乙烷(10.38%)、丁二烯(9.75%)、正戊烷(9.37%)、丙烯醛(8.28%)、乙烯(8.22%)、乙炔(7.44%)、丙酮(4.42%)、己醛(3.21%) 家庭餐饮 丙烯醛(24.32%)、丙酮(20.19%)、乙醛(9.01%)、正戊烷(6.42%)、乙酸乙酯(5.33%)、乙烷(4.5%)、丁二烯(3%) 食堂餐饮 乙烯(16.62%)、乙烷(15.33%)、乙炔(13.25%)、丁二烯(10.44%)、乙醛(6.76%)、丙烯醛(6.18%)、顺式-1,3-二氯-1-丙烯(3.35%)、己醛(3.1%) 烧烤 丁二烯(22.75%)、丙烯醛(15.05%)、乙烯(8.35%)、乙醛(6.19%)、丙烷(5.65%)、正戊烷(4.98%)、正丁烷(4.92%)、丙烯(4%)、异丁烷(3.99%)和己醛(3.47%) 川菜 乙烯(16.62%)、乙烷(15.33%)、乙炔(13.25%)、丁二烯(10.44%)、乙醛(6.76%)、丙烯醛(6.18%)、顺式-1,3-二氯-1-丙烯(3.35%)、己醛(3.1%) 商业综合体 乙炔(17.03%)、丁二烯(15.22%)、乙醛(14.14%)、乙烯(11.86%)、丙酮(8.18%)、丙烯醛(7.13%)、正戊烷(4.08%)、乙烷(3.47%)、异戊烷(3.2%) 快餐 正戊烷(32.51%)、乙醛(10.89%)、丙烯醛(8.15%)、1-戊烯(7.19%)、戊醛(4.91%)、己醛(4.8%)、正庚烷(4.1%)、丙醛(3.89%)、 火锅 乙烷(29.94%)、乙醛(17.69%)、丙酮(10.77%)、丙烷(5.18%)、丙烯醛(4.89%)、乙烯(3.91%)、正戊烷(3.48%) 2.2 餐饮源VOCs成分谱对比
将餐饮源VOCs按照烷烃、烯烃、芳香烃、卤代烃、OVOCs和其他6类进行汇总,结果详见表4. 针对餐饮源VOCs成分谱的研究主要集中在社会餐饮和食堂餐饮,社会餐饮中通常包括川菜和烧烤两类. 本研究不仅包括常见的川菜、烧烤和食堂,还增加了商业综合体、快餐和火锅3类,使得社会餐饮具有成都市本地化特色. 此外,鲜有研究针对家庭餐饮VOCs建立成分谱,家庭餐饮作为餐饮源中重要的组成部分,本研究也对其进行了研究.
表 4 餐饮源VOCs组分构成(%)Table 4. Catering sources VOCs component composition(%)餐饮类型Catering Types 烷烃Alkanes 烯烃Olefins 芳香烃Aromatic hydrocarbons 卤代烃Halogenated hydrocarbons 含氧OVOCs 其他Others 数据来源Reference 社会餐饮 29.97 25.78 1.63 0.86 33.51 8.26 本研究 家庭餐饮 23.12 8.61 0.16 2.32 63.77 2.02 本研究 食堂餐饮 30.29 16.51 5.86 13.82 28.02 5.52 本研究 烧烤 24.67 41.05 2.46 0.04 29.23 2.55 本研究 川菜 20.03 36.92 1.12 0.08 24.56 17.3 本研究 商业综合体 14.41 29.72 1.71 0.8 36.32 17.03 本研究 快餐 45.72 12.02 0.24 1.78 37.39 2.86 本研究 火锅 45.02 9.18 2.61 1.61 40.04 1.55 本研究 烧烤 53.2 42.8 2.2 0.1 — — [21] 烧烤 28.4 58.3 13.3 0 — — [22] 川菜 14.79 12.44 1.39 0.44 66.76 4.19 [23] 川菜 47.9 41.1 10.8 0.2 — — [22] 食堂 64 21 3 1 11 — [21] 根据文献[21-22]可知,烧烤占比最高的污染物是烯烃,占比为42.8%—58.3%,占比第二的是烷烃,占比为28.4%—53.2%;本研究中烧烤的烷烃类相对较低,由于文献[21-22]未监测OVOCs,可能导致结果与本研究有些不同,但总体而言,本研究烧烤VOCs组分构成与文献相近. 文献[23]中关于川菜的OVOCs占比最高为66.76%,烷烃与烯烃占比相近,芳香烃和卤代烃占比都较低. 本研究中川菜的烯烃含量相对较高,OVOCs含量相对较低,可能是由于本研究的川菜存在大火烹饪或烹饪温度等因素导致存在一些差异. 文献[21]中食堂的烷烃含量相对较高,本研究中的OVOCs和卤代烃相对较高,可能是监测组分不同导致结果与本研究存在差异. 总体而言,本研究的餐饮源VOCs与参考文献结果相近,并增加了家庭餐饮以及社会餐饮中的商业综合体、快餐和火锅3类,具有成都市本地化特色.
2.3 餐饮源VOCs全组分探索
2.3.1 VOCs全组分分析结果
本研究2.1节中建立了成都市餐饮源VOCs成分谱,其中OVOCs、烯烃和烷烃是餐饮源VOCs的最主要组分,3类污染物累计质量分数百分比在75%以上,为明确OVOCs、烯烃和烷烃在全组分分析中的物种组成及占比情况,全组分分析的占比情况根据某类污染物峰面积比上总峰面积计算得到. 将全组分分析与114种污染物分析的污染物种类、物种数量及占比情况进行对比分析,详见表5.
表 5 VOCs全组分分析污染物种类及占比情况Table 5. VOCs full-component analysis of pollutant types and the proportion类型Types 污染物种类Pollutant type 物种数量Number of Species 占比情况/%Percentage 烧烤-全组分分析 OVOCs 161 41.1 烯烃 87 36.4 烷烃 27 8.1 烧烤-114种污染物分析 OVOCs 20 29.2 烯烃 11 41.1 烷烃 15 24.7 川菜-全组分分析 OVOCs 127 65.0 烯烃 27 15.8 烷烃 12 4.3 川菜-114种污染物分析 OVOCs 20 25.7 烯烃 11 30.1 烷烃 27 23.5 食堂-全组分分析 OVOCs 149 54.8 烯烃 46 18.7 烷烃 24 6.9 食堂-114种污染物分析 OVOCs 19 28.0 烯烃 11 16.5 烷烃 27 30.3 注:全组分分析的占比根据污染物峰面积比上总峰面积计算得到. Note: The percentage of full-component analysis was calculated based on the contaminant peak area divided by the total peak area. VOCs全组分分析共检测到207—343种VOCs,其中烧烤全组分分析检测到343种VOCs,川菜检测到207种VOCs,食堂检测到267种VOCs. 全组分分析相较于114种污染物成分谱,得到的污染物种类更加复杂、多样. OVOCs仍然是最主要的污染物种类,占比高达41.1%—65.0%,全组分分析得到的OVOCs种类、结构更加复杂. 烯烃也是餐饮源中重要的污染物,占比为15.8%—36.4%. 在全组分分析中得到的烷烃占比相对较小,为4.3%—8.1%.
2.3.2 VOCs全组分分析代表物质
全组分分析中OVOCs、烯烃和烷烃的代表性物质及占比情况见表6,OVOCs的代表性物质为芳樟醇、己醛、反式茴香脑,烯烃代表性物质为长叶烯和柠檬烯,烷烃代表性物质为正十五烷、正庚烷. 探索了餐饮源VOCs在114种组分之外的成分情况,寻找完善餐饮源成分谱物种的代表性物质.
表 6 VOCs全组分分析代表物质Table 6. Representative substances for full-component analysis of VOCs类型Types 污染物种类Pollutant type 代表物质Representative substances 占比/%Percentage 烧烤-全组分 OVOCs 反式茴香脑、芳樟醇、己醛、桉油精 2.6、2.1、1.7、1.3 烯烃 柠檬烯、长叶烯、(E)-Β-罗勒烯 4.1、3.7、2.3 烷烃 正十五烷、正庚烷、正辛烷 1.1、1.0、0.9 烧烤-114 OVOCs 丙烯醛、乙醛、己醛 15.1、6.2、3.5 烯烃 丁二烯、乙烯、丙烯 22.8、8.4、4.0 烷烃 丙烷、正戊烷、正丁烷 5.7、5.0、4.9 川菜-全组分 OVOCs 乙酸、己醛、十二醇、芳樟醇 2.0、1.5、1.2、1.2 烯烃 长叶烯、柠檬烯、L-β-蒎烯 10.0、1.4、0.5 烷烃 正十六烷、正十三烷、正十五烷 1.1、0.9、0.8 川菜-114 OVOCs 乙醛、丙烯醛、己醛 6.7、6.2、3.1 烯烃 乙烯、丁二烯、丙烯 16.6、10.4、1.1 烷烃 乙烷、2,2-二甲基丁烷、正戊烷 15.3、2.9、1.8 食堂-全组分 OVOCs 芳樟醇、己醛、2-苯基-2-丙醇、乙酸 2.8、1.6、1.3、0.8 烯烃 长叶烯、α-愈创木烯、柠檬烯 5.2、2.1、1.4 烷烃 正十四烷、正十五烷、正庚烷 1.1、0.9、0.9 食堂-114 OVOCs 乙醛、丙酮、乙酸乙酯 8.6、3.5、3.2 烯烃 乙烯、反式-2-丁烯、顺式-2-丁烯 12.5、1.7、0.6 烷烃 乙烷、2,2-二甲基丁烷、正戊烷 14.7、8.8、1.4 餐饮源114种污染物分析得到的OVOCs代表性物质为丙烯醛、乙醛、己醛、丙酮、乙酸乙酯;烯烃代表物质为丁二烯、乙烯、丙烯、反式-2-丁烯、顺式-2-丁烯;烷烃为丙烷、正戊烷、正丁烷、乙烷、2,2-二甲基丁烷. 在全组分分析中,丙烯醛、顺式-2-丁烯和正庚烷占比较低,主要是因为餐饮源全组分VOCs成分复杂、物种多样,单一物种的占比则更低.
为完善餐饮源VOCs在114种组分之外的成分谱物种,可根据实际情况综合考虑,选择表5中关于烧烤、川菜和食堂增加OVOCs、烯烃和烷烃类的代表物质增加监测,旨在更全面地反映餐饮源VOCs的特征.
2.4 SOA生成潜势
二次有机气溶胶(SOA)是由天然源和人为源排放的VOCs或半挥发性有机物(SVOCs)与大气中的氧化剂(O3等)发生光化学反应,并通过气体粒子转化或凝结在现有粒子上而形成的有机气溶胶[24-25]. SOA是大气气溶胶的重要组成部分,也是PM2.5的重要组成部分,可占PM2.5有机组分的20%—50%[26].
计算SOA生成潜势计算的方法主要有生成有水溶性有机物(WSOC)测算法、机碳(OC)/无机碳(EC)比率法和气溶胶生成系数(FAC)法[27]. 本研究采用FAC法计算成都市餐饮源二次有机气溶胶生成潜势,计算公式如下:
SOAi=VOCsi0×FACi 式中,SOAi 为第i种 VOCs 生成 SOA 的浓度,μg·m−3;VOCsi0 为第 i 种 VOCs 的初始浓度,μg·m−3;FACi 为第i种VOCs生成 SOA的气溶胶生成系数. 监测过程中得到的VOCs 浓度是氧化后的VOCs浓度,第i种VOCs的初始浓度 VOCsi0计算公式如下:
VOCsi=VOCsi0×(1−FVOCsi) 式中,VOCsi为监测到的i组分浓度,μg·m−3.
FVOCsi FVOCsi 由表7可知,芳香烃的排放浓度和二次有机气溶胶排放贡献占比均为最大. 餐饮源SOA生成潜势为1220.7 μg·m−3,社会餐饮SOA生成潜势为914.2 μg·m−3,家庭餐饮SOA生成潜势为 11.5 μg·m−3,食堂餐饮SOA生成潜势为295.0 μg·m−3. 社会餐饮是餐饮源SOA生成潜势占比为74.9%,食堂餐饮占比为24.2%,家庭餐饮占比为0.9%. 社会餐饮是餐饮源SOA生成潜势最大的组成部分.
表 7 餐饮源SOA生成潜势计算结果Table 7. Catering source SOA formation potential calculation results类别Types 化合物名称Compounds name 社会餐饮Commercial cooking 家庭餐饮Family cooking 食堂餐饮Canteen cooking 餐饮源Catering sources SOAi 贡献率/%Contribution SOAi 贡献率/%Contribution SOAi 贡献率/%Contribution SOAi 贡献率/%Contribution 烷烃 2-甲基戊烷 0.1 0.0 0.0 0.0 1.1 0.4 1.2 0.1 3-甲基戊烷 0.0 0.0 0.0 0.0 0.8 0.3 0.8 0.1 正己烷 4.7 0.5 0.1 0.6 0.1 0.0 4.9 0.4 甲基环戊烷 0.0 0.0 0.0 0.0 0.1 0.0 0.1 0.0 环己烷 0.0 0.0 0.0 0.0 0.2 0.1 0.2 0.0 正庚烷 5.5 0.6 1.0 8.9 0.1 0.0 6.6 0.5 甲基环己烷 3.3 0.4 0.0 0.0 2.4 0.8 5.7 0.5 2,2,4-三甲基戊烷 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 2-甲基庚烷 0.8 0.1 0.0 0.0 1.2 0.4 2.0 0.2 3-甲基庚烷 0.0 0.0 0.0 0.0 0.8 0.3 0.8 0.1 正辛烷 0.9 0.1 1.0 9.1 0.1 0.0 2.0 0.2 正壬烷 23.5 2.6 0.0 0.0 0.9 0.3 24.4 2.0 癸烷 0.1 0.0 0.0 0.0 0.0 0.0 0.1 0.0 十一烷 12.9 1.4 0.6 5.5 13.3 4.5 26.8 2.2 十二烷 8.0 0.9 1.1 9.2 0.0 0.0 9.1 0.7 小计 59.9 6.6 3.8 33.3 21.1 7.2 84.8 6.9 芳香烃 苯 237.2 25.9 1.4 12.4 8.0 2.7 246.6 20.2 甲苯 512.6 56.1 6.2 54.2 68.1 23.1 586.9 48.1 乙苯 66.3 7.3 0.0 0.0 52.1 17.7 118.4 9.7 间、对二甲苯 16.4 1.8 0.0 0.0 30.0 10.2 46.4 3.8 邻二甲苯 18.5 2.0 0.0 0.0 43.9 14.9 62.4 5.1 异丙苯 0.4 0.0 0.0 0.0 1.8 0.6 2.2 0.2 正丙苯 0.0 0.0 0.0 0.0 0.0 0.0 0.0 0.0 间乙基甲苯 0.0 0.0 0.0 0.0 11.0 3.7 11.0 0.9 对乙基甲苯 0.4 0.0 0.0 0.0 9.8 3.3 10.2 0.8 1,3,5-三甲基苯 0.0 0.0 0.0 0.0 7.8 2.6 7.8 0.6 邻乙基甲苯 0.7 0.1 0.0 0.0 17.5 5.9 18.2 1.5 1,2,4-三甲苯 0.1 0.0 0.0 0.0 5.7 1.9 5.8 0.5 1,2,3-三甲苯 0.1 0.0 0.0 0.0 8.1 2.7 8.2 0.7 间二乙基苯 0.0 0.0 0.0 0.0 3.6 1.2 3.6 0.3 对二乙基苯 0.5 0.1 0.0 0.0 3.6 1.2 4.1 0.3 萘 1.2 0.1 0.0 0.0 2.9 1.0 4.1 0.3 小计 854.3 93.4 7.6 66.7 273.9 92.8 1135.8 93.1 合计 914.2 100.0 11.5 100.0 295.0 100.0 1220.7 100.0 在污染物类别方面,餐饮源中芳香烃SOA生成潜势贡献率为93.1%,烷烃SOA生成潜势贡献率为6.9%,芳香烃为餐饮源重要的SOA生成潜势污染物. 社会餐饮中,芳香烃SOA生成潜势贡献率为93.4%,烷烃SOA生成潜势贡献率为6.6%. 家庭餐饮中,烷烃SOA生成潜势贡献率为33.3%,芳香烃SOA生成潜势贡献率为66.7%. 食堂餐饮中,烷烃SOA生成潜势贡献率为7.2%,芳香烃SOA生成潜势贡献率为92.8%. 社会餐饮和食堂餐饮的烷烃类SOA生成潜势贡献率较低,在家庭餐饮中相对较高;芳香烃类SOA生成潜势贡献率在3类餐饮中都较高.
3. 结论(Conclusion)
(1)建立成都市餐饮源本地化成分谱,共检测出95种VOCs,包含烷烃27种、烯烃11种、芳香烃16种、卤代烃19种、OVOCs 20种、其他2种. OVOCs、烷烃和烯烃3类占比最高,是餐饮源重要的污染物类型. 餐饮源VOCs的特征污染物是丙烯醛(11.12%)、乙烷(9.87%)、乙醛(9.51%)、丙酮(9.34%)、乙烯(7.86%)、正戊烷(5.74%)、乙炔(5.01%)、丁二烯(4.64%)、顺式-1,3-二氯-1-丙烯(3.4%)和乙酸乙酯(3.04%).
(2)OVOCs仍然是最主要的污染物种类,全组分分析得到的OVOCs种类、结构更加复杂. 全组分特征得到OVOCs的代表性物质为反式茴香脑和芳樟醇等,烯烃代表性物质为长叶烯和柠檬烯等,烷烃代表性物质为正十五烷和正庚烷等.
(3)采用FAC法计算餐饮源VOCs二次有机气溶胶生成潜势. 餐饮源SOA生成潜势为1220.7 μg·m−3,芳香烃贡献率最大,贡献率为93.1%.
-
表 1 重金属浓度预测值和实测值的R和MSE值
Table 1. The R and MSE values with predicted and measured heavy metal concentrations
m 砷 As 锑 Sb 钼 Mo 锰 Mn 砷、锑、钼、锰共同输出Common output R MSE R MSE R MSE R MSE R MSE 3 0.93123 1.4421×10−6 0.94879 4.1252×10−8 0.89247 4.982×10−7 0.90532 6.1007×10−6 0.90946 3.553×10−6 4 0.96537 2.3252×10−6 0.93571 4.7251×10−8 0.89988 4.2321×10−7 0.92603 1.9196×10−6 0.91861 1.7203×10−6 5 0.96925 7.5378×10−6 0.9193 2.6065×10−8 0.89576 2.1519×10−7 0.94441 2.3075×10−6 0.91739 1.567×10−6 6 0.96464 8.0868×10−7 0.94248 2.809×10−8 0.91896 1.3364×10−7 0.93395 2.7313×10−6 0.91548 3.9952×10−6 7 0.97951 1.8694×10−6 0.95308 6.7504×10−8 0.92315 3.1197×10−7 0.95523 4.1893×10−6 0.91648 5.2032×10−6 8 0.97774 2.8463×10−6 0.94575 4.5302×10−8 0.92513 2.7051×10−7 0.95293 5.9712×10−6 0.93654 4.5672×10−6 9 0.98978 9.4417×10−7 0.96594 1.5644×10−8 0.94555 1.0995×10−7 0.96337 3.6817×10−6 0.94235 4.7376×10−6 10 0.94838 1.7545×10−6 0.93021 3.8875×10−8 0.90364 1.2402×10−7 0.9602 3.5023×10−6 0.91799 5.3717×10−6 11 0.95096 8.1691×10−6 0.95992 3.0469×10−8 0.92018 1.7863×10−7 0.925 1.9336×10−6 0.91465 3.115×10−6 12 0.96107 5.8699×10−6 0.92848 2.0744×10−7 0.93814 4.9283×10−8 0.95628 5.6111×10−6 0.92473 2.1818×10−6 13 0.94508 6.7089×10−6 0.92151 1.1668×10−7 0.92059 3.4499×10−7 0.94545 1.9454×10−6 0.92939 1.3172×10−6 注:m:隐藏层数;R:相关系数;MSE:均方误差. -
[1] 陈安, 李景吉, 王茂生, 等. 西藏“一江两河”流域生态系统服务变化及权衡与协同关系研究 [J]. 水土保持研究, 2022, 29(2): 313-319. CHEN A, LI J J, WANG M S, et al. Research for change of ecosystem service and the tradeoff-synergy relation of the YLN Basin in the Tibet Autonomous Region [J]. Research of Soil and Water Conservation, 2022, 29(2): 313-319(in Chinese).
[2] ARDABILI S, MOSAVI A, DEHGHANI M, et al. Deep learning and machine learning in hydrological processes climate change and earth systems a systematic review[C]//Várkonyi-Kóczy A. International Conference on Global Research and Education. Cham: Springer, 2020: 52-62. [3] BEJOU D, WRAY B, INGRAM T N. Determinants of relationship quality: An artificial neural network analysis [J]. Journal of Business Research, 1996, 36(2): 137-143. doi: 10.1016/0148-2963(95)00100-X [4] 刁瑞翔, 青松, 越亚嫘, 等. 基于BP神经网络算法的内蒙古岱海水体透明度遥感估算 [J]. 灌溉排水学报, 2022, 41(8): 114-121. DIAO R X, QING S, YUE Y L, et al. Using back propagation neural network algorithm and remote sensing to estimate lake water transparency [J]. Journal of Irrigation and Drainage, 2022, 41(8): 114-121(in Chinese).
[5] 黄煜韬, 施维林, 纪娟, 等. 基于BP神经网络对某电镀厂土壤重金属预测及人体健康风险评价 [J]. 生态毒理学报, 2022, 17(2): 278-289. HUANG Y T, SHI W L, JI J, et al. Prediction of soil heavy metals based on BP neural network and assessment of human health risk of an electroplating plant [J]. Asian Journal of Ecotoxicology, 2022, 17(2): 278-289(in Chinese).
[6] 尤游, 张林静. 贝叶斯正则化BP神经网络在空气质量指数预测中的应用 [J]. 重庆科技学院学报(自然科学版), 2022, 24(1): 78-82. YOU Y, ZHANG L J. Application of Bayesian regularized BP neural network in air quality index prediction [J]. Journal of Chongqing University of Science and Technology (Natural Sciences Edition), 2022, 24(1): 78-82(in Chinese).
[7] 朱琳, 李明河, 陈园. 基于EHO优化的BP神经网络污水处理出水COD预测模型 [J]. 重庆工商大学学报(自然科学版), 2022, 39(3): 26-32. ZHU L, LI M H, CHEN Y. Prediction model for effluent COD in sewage treatment based on BP neural network optimized by EHO [J]. Journal of Chongqing Technology and Business University (Natural Science Edition), 2022, 39(3): 26-32(in Chinese).
[8] ANOCHI J A, de CAMPOS VELHO H F. Climate precipitation prediction by neural network [J]. Journal of Mathematics and System Science, 2015, 5(5): 207-213. [9] MOGHADAM S V, SHARAFATI A, FEIZI H, et al. An efficient strategy for predicting river dissolved oxygen concentration: Application of deep recurrent neural network model [J]. Environmental Monitoring and Assessment, 2021, 193(12): 798. doi: 10.1007/s10661-021-09586-x [10] ROOKI R, ARDEJANI F D, ARYAFAR A, et al. Prediction of heavy metals in acid mine drainage using artificial neural network from the Shur River of the Sarcheshmeh porphyry copper mine, Southeast Iran [J]. Environmental Earth Sciences, 2011, 64(5): 1303-1316. doi: 10.1007/s12665-011-0948-5 [11] 符东, 吴雪菲, 易珍言, 等. 沱江水质模糊综合评价及主要污染物的预测研究 [J]. 农业环境科学学报, 2020, 39(12): 2844-2852. FU D, WU X F, YI Z Y, et al. Fuzzy comprehensive assessment of water quality and prediction of main pollutants in the Tuo River [J]. Journal of Agro-Environment Science, 2020, 39(12): 2844-2852(in Chinese).
[12] 李峻, 孙世群. 基于BP网络模型的青弋江水质预测研究 [J]. 安徽工程科技学院学报(自然科学版), 2008, 23(2): 23-26. LI J, SUN S Q. Water quality prediction in qinyijiang River Wuhu area based on BP artificial neural network [J]. Journal of Anhui University of Technology and Science (Natural Science), 2008, 23(2): 23-26(in Chinese).
[13] 周晨霓, 潘刚. 西藏拉萨河流域湿地水质分析与评价 [J]. 贵州农业科学, 2014, 42(9): 249-252. ZHOU C N, PAN G. Analysis and evaluation of water quality of plateau wetlands in Lhasa River basin [J]. Guizhou Agricultural Sciences, 2014, 42(9): 249-252(in Chinese).
[14] 李红敬, 张娜, 林小涛. 西藏雅鲁藏布江水质时空特征分析 [J]. 河南师范大学学报(自然科学版), 2010, 38(2): 126-130. LI H J, ZHANG N, LIN X T. Spatio-temporal characteristics of Yarlung Zangbo River in Tibet [J]. Journal of Henan Normal University (Natural Science), 2010, 38(2): 126-130(in Chinese).
[15] 杜梅, 张强英, 任培, 等. 西藏年楚河流域农用地土壤重金属分布与生态风险评价 [J]. 环境工程技术学报, 2022, 12(5): 1618-1625. DU M, ZHANG Q Y, REN P, et al. Distribution of soil heavy metals and ecological risk assessment of agricultural land in Nianchu River basin, Tibet [J]. Journal of Environmental Engineering Technology, 2022, 12(5): 1618-1625(in Chinese).
[16] 杨安, 邢文聪, 王小霞, 等. 西藏中部河流、湖泊表层沉积物及其周边土壤重金属来源解析及风险评价 [J]. 中国环境科学, 2020, 40(10): 4557-4567. YANG A, XING W C, WANG X X, et al. Source and risk assessment of heavy metals in surface sediments of rivers, lakes and their surrounding soils in central Tibet [J]. China Environmental Science, 2020, 40(10): 4557-4567(in Chinese).
[17] 马腾霄, 杨文光, 朱利东, 等. 雅鲁藏布江中游地貌参数特征及其构造地貌意义 [J]. 成都理工大学学报(自然科学版), 2022, 49(4): 502-512. MA T X, YANG W G, ZHU L D, et al. Geomorphic parameters and their tectonic geomorphic significance in the middle reaches of Yarlung Zangbo River, China [J]. Journal of Chengdu University of Technology (Science & Technology Edition), 2022, 49(4): 502-512(in Chinese).
[18] BRAY M, HAN D W. Identification of support vector machines for runoff modelling [J]. Journal of Hydroinformatics, 2004, 6(4): 265-280. doi: 10.2166/hydro.2004.0020 [19] HONG N, GUAN Y J, YANG B, et al. Quantitative source tracking of heavy metals contained in urban road deposited sediments [J]. Journal of Hazardous Materials, 2020, 393: 122362. doi: 10.1016/j.jhazmat.2020.122362 [20] 万子益. 西藏主要铁矿类型地质特征简介 [J]. 矿床地质, 1986, 5(4): 24-33. WAN Z Y. A brief introduction to the major types of iron deposits in Tibet and their geological setting [J]. Mineral Deposits, 1986, 5(4): 24-33(in Chinese).
[21] 徐宗宝. 基于混合优化BP神经网络的水质预测系统的研究与实现[D]. 北京: 北京工业大学, 2020. XU Z B. Research and realization of water quality prediction system based on hybrid optimized BP neural network[D]. Beijing: Beijing University of Technology, 2020 (in Chinese).
[22] LI P F, HUA P, GUI D W, et al. A comparative analysis of artificial neural networks and wavelet hybrid approaches to long-term toxic heavy metal prediction [J]. Scientific Reports, 2020, 10(1): 1-15. doi: 10.1038/s41598-019-56847-4 [23] 范佳妮, 王振雷, 钱锋. BP人工神经网络隐层结构设计的研究进展[J]. 控制工程, 2005, 12(增刊1): 109-113. FAN J N, WANG Z L, QIAN F. Research progress structural design of hidden layer in BP artificial neural networks[J]. Control Engineering of China, 2005, 12(Sup 1): 109-113. (in Chinese)
[24] 段宁, 杨思言, 魏婉婷. 基于BP神经网络的铅酸蓄电池厂地下水重金属浓度预测 [J]. 环境科学与技术, 2016, 39(1): 194-198. DUAN N, YANG S Y, WEI W T. Prediction of heavy metal concentrations of the groundwater from a lead-acid battery factory based on BP neural network [J]. Environmental Science & Technology, 2016, 39(1): 194-198(in Chinese).
[25] ALEXANDER D L J, TROPSHA A, WINKLER D A. Beware of R2: Simple, unambiguous assessment of the prediction accuracy of QSAR and QSPR models [J]. Journal of Chemical Information and Modeling, 2015, 55(7): 1316-1322. doi: 10.1021/acs.jcim.5b00206 [26] ABDULLAHI N, IGWE E C, DANDAGO M A. Heavy metals contamination sources in Kano, Nigeria and their concentrations along Jakara River and its agricultural produce: A review[J]. Moroccan Journal of Agricultural Sciences 2021, 2(2): 106-113. [27] 胡志华, 高洪雷, 万汉平, 等. 西藏羊八井地热田水热蚀变的时空演化特征 [J]. 地质论评, 2022, 68(1): 359-374. HU Z H, GAO H L, WAN H P, et al. Temporal and spatial evolution of hydrothermal alteration in the Yangbajing Geothermal Field, Xizang(Tibet) [J]. Geological Review, 2022, 68(1): 359-374(in Chinese).
[28] LIU R, XU Y, ZHANG J, et al. A comparative study of the content of heavy metals in typical metallic mine rivers of the Tibetan Plateau [J]. Geological Bulletin of China, 2018, 37(12): 2154-2168. [29] HUANG X, SILLANPÄÄ M, DUO B, et al. Water quality in the Tibetan Plateau: Metal contents of four selected rivers [J]. Environmental Pollution, 2008, 156(2): 270-277. doi: 10.1016/j.envpol.2008.02.014 [30] HUANG X, SILLANPÄÄ M, GJESSING E T, et al. Water quality in the Tibetan Plateau: Major ions and trace elements in the headwaters of four major Asian rivers [J]. Science of the Total Environment, 2009, 407(24): 6242-6254. doi: 10.1016/j.scitotenv.2009.09.001 [31] ZHANG Y L, SILLANPÄÄ M, LI C L, et al. River water quality across the Himalayan regions: Elemental concentrations in headwaters of Yarlung Tsangbo, Indus and Ganges River [J]. Environmental Earth Sciences, 2015, 73(8): 4151-4163. doi: 10.1007/s12665-014-3702-y [32] LIU C W. Reactive transport of arsenic-enriched geothermal spring water into a sedimentary aquifer [J]. Environmental Geochemistry and Health, 2019, 41(2): 633-648. doi: 10.1007/s10653-018-0156-2 [33] H V P T, BONNET T, GARAMBOIS S, et al. Arsenic in shallow aquifers linked to the electrical ground conductivity: The Mekong delta source example [J]. Geosciences Research, 2017, 2(3): 180-195. [34] SHARMA S, KHANDELWAL A, AMALADASS E P, et al. Studies on DC transport and terahertz conductivity of granular molybdenum thin films for microwave radiation detector applications [J]. Journal of Applied Physics, 2020, 128(18): 183901. doi: 10.1063/5.0013939 期刊类型引用(1)
1. 高燕. 胶黏剂产品中VOCs含量与类别的检测方法. 塑料助剂. 2024(03): 38-42 .  百度学术
百度学术
其他类型引用(0)
-






 DownLoad:
DownLoad: