-
海岸带是陆地和海洋生态系统之间水文循环和物质交换的重要场所,该区域内发生着诸多化学元素的生物地球化学过程,这些生物地球化学过程维系着海岸带水资源和生态环境的可持续[1]. 在海岸带区域,海洋潮汐周期性波动和气象季节性动态使得海岸带浅部地下水中的物理化学参数(如温度、盐度、溶解氧、营养盐等)发生着不同时间尺度(如小时尺度、月尺度、年尺度等)上的变化,进而影响着海岸带地下水中的生物地球化学演化过程[2]. 海岸带生物地球化学过程演化一直是水文地质学和环境科学的重要研究内容之一,研究海岸带地下水中生物地球化学过程的演化机制,厘清控制生物地球化学演化的关键因素,对于深入理解自然和社会环境变化条件下的海岸带生态环境变化具有重要意义.
时空变异特征是海岸带生物地球化学过程演化的直观表现. 在海岸带,高频次的海水潮汐过程使得海岸带地下水与海水水力联系和物质交互剧烈,且具有周期性特征;此外,海水—地下水之间密度梯度作用及潮汐作用使得地下水与海水之间的水循环形成了地下水淡水排泄和海水再循环并存的特征,并形成了上部咸水区—淡水排泄区—海水楔形区共存的咸淡水分带特征,咸淡水分带及其内部的水循环和物质迁移速率差异使得海岸带地下水循环过程表现出时间变异特征[3-4]. 已有研究表明,在水循环和物质迁移的时间变异特征的影响下,海岸带地下水中化学组分的循环及生物地球化学过程也具有时间变异特征[5-7]. 开展时空变异特征研究能够为揭示海岸带生物地球化学过程动态演化机制提供重要支撑.
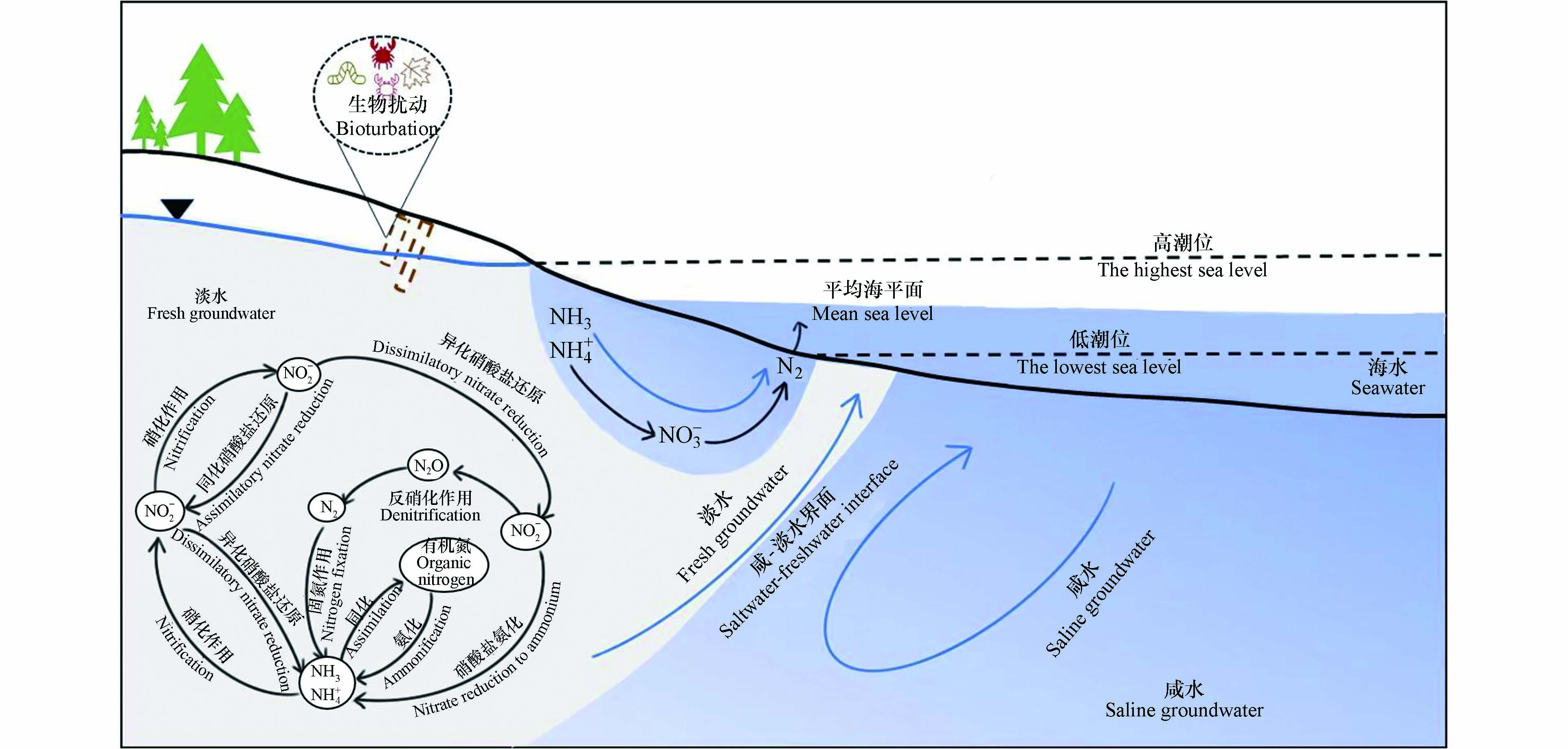
氮是所有生物细胞合成所必需的重要元素之一,其循环对于调节海岸带生态环境质量起着关键作用. 有大量文献指出由于受到人类活动的影响,部分海岸带氮循环已经遭到严重破坏,海岸带含水层内过量的氮排放至海洋会导致沿海地区发生严重的环境问题如水体富营养化、生物多样性减退甚至会对人体身体健康产生影响等[1, 8-11]. 氮元素在海岸带发生较多复杂的生物地球化学作用,主要有固氮、硝化、反硝化、有机氮的氨化、厌氧氨氧化等作用(图1). 这些作用受到生物活动、气候变化、陆地海洋水文动态等多重因素的影响[8, 12],上述影响因素的动态变化控制着海岸带内地下水水动力条件、氧化还原条件、化学组分等的变化[13],进而会影响水中氮元素组分的径流途径以及滞留时间,进而使得氮组分及其生物地球化学过程随时间发生变化[14-15].
本文围绕海岸带地下水中氮生物地球化学过程演化机制这一科学问题,开展文献调研分析,以归纳分析海岸带氮元素地球化学过程演化的主要影响因素,并总结氮生物地球化学过程演化的主要研究方法,为深入认识海岸带氮生物地球化学演化及其研究方法提供支撑.
-
氮元素作为海洋生物生长的必须营养元素之一 ,在环境中以多种形式存在,可以将其分为惰性氮和活性氮[16]. 上述氮循环过程中所涉及的反应可以分为两类,一类是主要是将外界含氮化合物转化为活性氮而富集于海岸带含水层的固氮作用、硝化作用以及有机氮的氨化作用. 另一类则是将活性氮转化为惰性氮而释放到大气的反硝化作用以及厌氧氨氧化作用,这一类作用均可称为脱氮作用,海岸带中含水层内脱氮作用主要以反硝化作用为主[8, 17].
在气候波动和潮汐水文动态的影响下,海岸带地下水与海洋的水动力条件和化学环境会发生季节性和潮汐周期性的变化,进而导致海岸带地下水氮元素生物地球化学过程的时间差异性. 如Liu等[18]的研究指出中国香港Tolo港口海岸带含水层内氮元素组分赋存量具有时间变化性,夏季硝酸根、亚硝酸根的赋存量以及流向海洋的速率均比其余季节大,而铵根则表现为夏冬季储存量较多,春秋季较少. 王军等[19]通过修正GIDS(Gradient plus Inverse Distance Squared)梯度平方反比插值法,指出长江口滨海湿地在春季主要向海水排放无机氮,排放量为
1.33×104t ,而在夏、秋和冬季主要是吸收水体中的无机氮,吸收量高达12.1×104t . Couturier等[20]揭示了加拿大Magdalen群岛4个不同年限春季的海岸带氮元素各个形态含量分布情况,地下水在高达166 d的滞留时间以及缺氧条件使得大量氮被消耗,并发现是由于有机质的溶解增加了Fe2+离子浓度,进而消耗沿岸的氮元素. 上述研究均表明海岸带含水层内氮元素形态并不是固定不变,而是随着时间推移发生不同情况的富集与迁移. 本文主要从温度、潮汐与波浪、海水入侵、盐度、生物扰动以及地下水动力条件等物理化学条件方面归纳海岸带氮的生物地球化学过程动态演化机制及其主控因素(表1). -
气候季节性变化作用下,海岸带海水和地下水的温度会出现周期性变化. 温度在多个方面直接与间接影响着固氮以及脱氮过程. 王东启等[31]在对长江口崇明岛潮滩反硝化速率测量时,发现夏冬季较强,初春晚秋的速率较弱,并指出温度与溶解氧的差异是引起反硝化速率季节性变化的主要因素. 其中温度能够直接影响参与氮循环过程的微生物活性,各类微生物的适宜生长温度不一致会导致在不同季节下微生物具有不同的组成及活性特征,进而导致海岸带内地下水中的氮元素形态及其演变存在时间变异性特征. 另一方面温度能够间接地影响咸淡水界面的位置,改变海水再循环与淡水排泄等水循环过程,进而影响海岸带生物地球化学过程的时变特征.
-
在海岸带内沉积物中发生的固氮、硝化、反硝化、有机氮的氨化以及厌氧氨氧化反应均受到微生物的驱动[32-34]. 温度的改变能够影响相关微生物的活性,通常在一定范围内温度的升高与硝化与反硝化反应均表现出一定的正相关关系. 但是已有相关研究指出这两类反应适宜的温度范围不一致,其中硝化作用的适宜温度为15—35 ℃之间,而反硝化作用的适宜温度则在5—75 ℃之间[35]. 如Herbert[36]在丹麦海岸带沉积物研究时,发现该研究区内硝化速率从春季(平均温度2 ℃)到秋季(平均温度22 ℃)增加了5倍. 需要指出的是,温度对硝化过程的促进作用会受到沉积物中溶解氧含量的影响. 例如,在有机质丰富的沉积物中,微生物呼吸作用加强进而消耗大量的氧气,会导致溶解氧含量成为硝化作用限制因素[37].
-
由于含水层条件复杂,外界对其影响存在延迟性,故在季节温度发生改变时海岸带内地下水与海水之间存在的温度差将导致平衡界面的移动. 这一过程会改变海岸带内地下水与海水之间的盐量发生交换和加快海岸带沉积物矿物组分的溶解,从而在一定程度上影响氮循环过程中物质组分的含量. Cogswell等[21]模拟分析了海岸带含水层中咸淡水界面随温度的变化规律,指出在海水温度降低时界面向陆地方向迁移,反之,界面向海水方向迁移. Pu等[22]通过实验模拟了无潮汐影响下的咸淡水界面随温度的变化过程,得到了与Cogswell相同的结论,此外还发现,在高温度海水情况下,除原有咸淡水循环外,还会产生一个新逆时针的反向循环,并使得含水层盐度分布更加混乱. 温度变化下的海水再循环通量及咸淡水界面的变化将能够进一步影响到氮及其生物地球化学过程在含水层中的分布及时间变异特征.
-
高频次的海水潮汐过程使得海岸带内地下水与海水水力联系和物质交互剧烈,且具有周期性特征. 在部分海岸带地区,除了深部地下水与海水楔形区外,在涨潮时大量海水涌入海岸带,通过松散孔隙下渗至海岸带含水层中,并在深部海水楔形区上形成范围相对较小的上部咸水区,这部分海水与地下水混合后于潮汐退潮期大多数又排泄至海水. 诸多研究已表明,上部咸水区的海水再循环流速快、周期短、频次高[23, 38-40],这在一定程度上影响着海岸带内地下水中氮元素生物地球化学过程的物质循环速率和时间变异特征. 例如,潮汐与海浪的作用使得海岸带内含水层沉积物周期性与海水、空气交替接触,进而导致上覆含水层溶解氧以及有机质的含量发生周期性的变化[3, 41];Heiss等[42]指出潮汐驱动的海水和地下水之间的混合促进了沿海含水层的反硝化,导致海岸带含水层内大量硝酸根被去除;陈杰[43]对海岸带氮元素输出量进行模拟,发现海岸带沉积物中铵根与硝酸根向海洋排泄量以及通过反硝化产生的
N2O 量均随着潮汐频率的增加而逐渐降低. -
含水层内溶解氧的含量在海岸带内氮循环过程中扮演着十分重要的角色,一是直接影响氮循环中硝化与反硝化速率,二是影响氮循环过程中相关好氧微生物的活性来间接影响氮循环过程. 潮汐的动态特征使得海岸带含水层中的溶解氧含量也在发生着周期性改变,在涨潮时,大量的含氧海水渗入到含水层中[44-45],在退潮时,沉积物中溶解氧逐渐被消耗,海岸带内溶解氧的含量与孔隙水的滞留时间有关. Kim等[39]对Cape Shores海岸带的多层位孔隙水测试和数值模拟结果表明,在上部咸水区靠近排泄点的地方,氮气的产生率升高与氧气的消耗升高保持一致. 赵世彬等[46]在对金沙滩海岸带进行研究时,发现该研究区内地下水的氮元素存在形态与当日海水的潮位存在响应即在开始涨潮后2 h内亚硝酸根及铵根浓度均增加至最大值,后到开始落潮时降低至最小值,随着落潮浓度又开始增加. 而硝酸盐浓度在退潮前后两小时内出现极小值,且发现硝酸根占无机氮的99%,还原氮含量十分低,这是因为取样点受潮汐影响显著,使得富含氧气的海水频繁渗入,造成一个相对氧化的环境.
-
在缺氧以及厌氧环境下,海岸带含水层内有机质取代氧气作为异养微生物合成能量的电子供体,将溶解的硝酸根还原为氮气以及一氧化二氮排放至大气,这样的过程即为反硝化作用. 虽然反硝化作用被认为海岸带减少氮元素向海水中排放的主要过程,但是部分海岸带内有机质的含量处于较低水平,因此反硝化过程难以发生[47]. 但随着潮汐以及波浪的影响,海水携带大量有机质涌入海岸带,使得有机质含量增加,进而为反硝化细菌提供充足的能源,并且在这过程有机物会发生矿化作用,消耗大量的氧气的同时产生大量无机氮[27, 48]. 这一过程不仅为反硝化作用提供了良好的氧化还原环境,还为反应提供了反应基质,极大的增加了反硝化作用速率. 如Charbonnier等[45]对Gironde和Adour河口之间的法国西南海岸内孔隙水化学进行了季节性监测,发现涨潮期间,海水携带的溶解氧以及有机质在海岸带中有足够的时间被矿化,并发现氧气消耗以及硝酸盐的富集在夏季比冬季强得多. 同样Liu等[49]在对中国香港Tolo海岸带不同潮汐下海岸带内营养盐的不同情况研究时,发现潮汐通过控制有机物的输入量进而影响海岸带内有机质的矿化反应,其中海水涌入带入大量有机质,反应生成的铵根数量超过该区域含水层内铵根总量的65%,硝化作用对铵根的去除率高达84%.
-
海水入侵是指在自然和人为影响下,海岸带含水层中的水动力条件发生变化,使得海岸带地下淡水与海水之间的平衡受到破坏,导致的含水层中咸淡水过渡带向陆地方向入侵的现象[50]. 海水入侵过程在一定程度上也影响了海岸带的氮循环. 例如,吴自军等[25]在对广西北海市近海岸地下水盐分的分层监测结果表明,潜水硝酸根浓度呈现出从陆地至海岸带逐渐减少的趋势,并猜测是由于海水入侵导致该区域内发生反硝化作用. Ardón等[26]发现在夏末干旱时期,North Carolina平原由于受到长年反复的海水入侵影响,含水层盐度得到增加导致离子交换增加以及硫化物的增加削弱了硝化作用,导致各类型湿地的铵根浓度均有增加. 由于海水入侵常受到季节气候或人类活动的影响,使得海水入侵具有周期性变化规律,如在枯水期与丰水期或者农业灌溉期与非农灌溉期海水入侵有着较大的差异,从而影响海岸带内含水层中氮元素的年内变化.
-
海岸带海水和地下水盐度对氮循环过程影响作用主要体现在以下四个方面:一是盐度的增加直接会影响海岸带内氮循环过程所需微生物群落的组成[51],高盐度条件下,硝化、反硝化作用受到抑制,而有机氮的矿化以及异化硝酸盐还原到氨作用增强[52]. 赵林丽等[53]通过改变进水盐度大小来模拟盐度变化对人工湿地除氮的影响,研究发现随着盐度的增加,总无机氮、硝酸根、铵根的去除率虽均表现逐渐降低的趋势,但是其抑制程度并不一样;Zhou等[27]和张林海等[54]发现在不同海岸带区域,盐度对氮循环过程的影响是不一样的,在部分海岸带硝化与反硝化作用受盐度的影响有限,但盐度能够促进有机氮的矿化以及异化硝酸盐还原到氨等过程. 二是盐度通过影响含水层的电导率来间接影响氮循环过程,杨长明等[55]的咸水入侵模拟过程表明,土壤中反硝化速率与电导率之间的关系为明显的负相关. 三是盐度能够增强离子交换作用,进而导致氮反应组分含量的改变及氮循环过程[56]. 四是盐度的增加会促进硫酸盐还原为硫化氢,从而影响海岸带沉积物内氮循环过程[57]. 在部分海岸带地区盐度还受着农业用地的影响,施肥的季节性施用会导致海岸带含水层内盐度会发生改变,进而影响海岸带的氮循环过程[58].
-
海岸带是多种生物栖息、活动的场所,这些生物会影响海岸带氮循环过程,主要体现在以下几方面[28, 59-60]:一是通过挖掘洞穴以及相关活动导致海岸带内渗透结构发生改变,改变原含水层内地下水的动力条件,进而影响海岸带内营养盐的富集与迁移;二是会导致介质之间物质流动与接触更加频繁,加快相应的反应过程;三是会改变海岸带内含水层中化学物质组分,比如螃蟹通过摄食落叶加速叶片中氮元素的矿化进程,且其排泄物能够增加元素含量或者影响酶与菌落的分布. 如刘敏等[61]通过室内模拟实验对比发现,螃蟹挖洞过程引起氧气进入含水层,加剧了含水层中的氨化以及硝化作用.
目前关于生物扰动对于海岸带地下水氮元素生物地球化学过程的时间变异性的相关研究还较少,但已有部分研究论证到海滩生物的摄食活动与大气温度之间存在较为显著的相关性[62],故可以推断,生物扰动对于海岸带内氮循环过程的影响也具有一定的周期季节性.
-
海岸带内沉积物多表现为疏松多孔的孔隙结构,造成其间地下水水流通道十分复杂. 而海岸带内地下水动力条件又受到地形地貌、季节性降雨、潮汐以及波浪的影响,水动力特征更加的复杂[63-66]. 水流的多种运动形式以及受到多种因素的影响,会使得海岸带内沉积物中地下水具有各向异性、溶解物质出现浓度差以及氧化还原环境出现周期性改变,这也会使得氮元素的迁移与富集表现出一定的时间变异性[67-68]. Santos等[29]在研究过程中发现反硝化速率的峰值出现在实验平流速率的中值(30—80 L·m−2·h−1),并猜测中等平流速率增加了地下水对沉积物的冲洗速率,让沉积物中存在氧气梯度、更高的细菌丰度以及更大的pH缓冲能力. Loveless等[30]发现在低地下水流速(0.14—0.18 m·d−1)、TOC(Total Organic Carbon)为0.35—4.9 mmol·L−1、DOC(Dissolved Organic Carbon)为0.28—4.6 mmol·L−1以及DO(Dissolved Oxygen)为0.4%—24%时氮硝化作用最易发生,并计算了在这样的理想环境下Cockburn Sound海岸带内地下水中
NO-x 的含量分别为:0.4—13 kg·d−1,NH+4 为0.2—24 kg·d−1,氮元素总量为2.5—43 kg·d−1,较以前估计量的少1—2个数量级. -
目前关于海岸带地下水中氮生物地球化学过程的时间变异特征的研究方法主要包括:野外水化学监测、室内氮循环实验和数值模拟方法,各个研究方法介绍如表2所示.
-
野外水化学监测作为调查海岸带氮生物地球化学的时间变异性的第一步需要做到:识别海岸带水的来源特征以清楚理解海岸带沉积物内氮元素的迁移与富集过程;厘清沉积物中海水与地下水的交互与转化过程[73]. 常见的野外水化学监测主要可以分为以下两种类型:一是直接在海岸带布设监测点,定期测定各点以及各点下不同深度处氮化合物的种类及含量[14]. 该方法能够较为直观的了解海岸带内各氮元素的分布情况,但是不同的测量方法具有一定的误差,如胡娜娜等[74]发现在对海岸带内沉积物中铵根测量时,在水体盐度小于4.0时,国际标准法中测量地表水与海水中氮的方法均适用,而当盐度大于4.0时,需对水样的pH进行校正以达到海水法所需的碱性环境,之后采用对海水测定氮元素的方法进行测定;对于亚硝酸盐而言,不论盐度如何变化,两种测量方法均适用;而对总氮测量时,水体盐度小于5采用对淡水测量氮元素方法,反之则使用对海水中氮元素的测量方法. 二是利用自然界中15N、14N、16O、17O以及18O稳定同位素,通过分析水体中同位素的丰度进而推断各种氮化物的来源与迁移情况[24, 75]. Heaton等[58]对Malta和Gozo海岸带内平均海平面以下的沉积物、高地(远离海岸带处)沉积物进行同位素测量研究时,发现Malta高地地下水中含量非常高,而Malta和Gozo海岸带内硝酸根浓度为14
mg∙L-1 和10mg∙L-1 ,通过对比15N/ 14N以及18O/ 16O发现该变化范围较大并不是反硝化作用造成,而是与地表水中微生物作用生成氮化合物相关,并推测造成该地硝酸盐分布情况是由于该地具有长期种植历史有关,微生物矿化作用生成大量硝酸盐,进而渗滤至海岸带中. 虽然上述野外水化学测量方法能够揭示海岸带含水层内氮元素分布及其变化的一定规律,但这些测量均难以做到连续长期的监测,且难以刻画海岸带内氮循环的动态特征. -
室内模拟实验是在监测数据基础下,通过刻画自然环境条件,模拟野外氮生物地球化学过程. 探究氮元素生物地球化学时间变异性的室内模拟实验主要可以分为两类:一是通过概化或改变实验条件,定性或定量分析氮生物地球化学过程及其对实验条件的响应规律. 如覃超梅等[9]对珠江口淇澳岛海岸带沉积物样品培养后,采用
N2 通气法直接测定反硝化速率,发现该区域反硝化速率主要受到大型红树植物的影响,其次是硝酸盐的利用率大小,最小为有机质的含量. 陈力琦[76]与张锋等[69]物理模拟了海水与地下水相混合的水动力条件及其时空变化规律,并观察水量、水温以及pH的改变对营养盐的迁移与转化过程,结果表明地下水与海水的混合比例会影响铵根与硝酸根含量(即铵根与硝酸根含量随地下水占比的增加而增加)、温度能够影响含水层中三氮含量的变化、海水pH值增加会使得含水层中内三氮含量降低. 二是在培养样品中直接添加一定量的稳定同位素示踪剂,后直接测定不同无机氮中稳定同位素的含量,进而可以得到氮循环过程中硝化、反硝化以及氨化等过程的速率[77]. 如Marchant等[70]通过同位素示踪剂法计算得到反硝化生成的硝酸根占总的50%—70%,异化硝酸盐还原为铵占硝酸浓度的10%—20%. 又如林来昌等[78]通过向培养样品中添加15N,在不同的时间测定样本中硝酸根与铵根离子中15N的含量,发现硝化速率与碳氮元素比值、含水率、铵根浓度呈显著正相关,与硝酸根浓度呈负相关,而与pH与电导率则无相关关系;在判定反硝化速率的影响因素时发现仅与硝酸浓度呈负相关,与其余因素均无关. 室内模拟方法能够阐明氮循环过程对物理化学条件的响应规律,但该方法对实验环境要求较高,也较难以刻画真实的海岸带地下水与海洋的水动力和化学条件. -
数值模拟是基于水文地质—气象水文—水化学等数据,在进行水文地质条件分析并概化的基础上,利用适用于海岸带变密度变饱和特征的模拟软件(如SEAWAT[79]、SUTRA[80-82]、MARUN[83-84])进行数值模型构建,进而模拟量化评估海岸带氮元素的运移及化学反应过程,并厘定其主控因素. 如Meile等[85]在研究美国McIntosh沿海含水层受到化粪池渗滤液的影响时,建立了二维变密度水流和反应运移数值模型,结果发现增加化粪池离地表水体的距离生物去除氮的比例增加,并且计算得到通过反硝化作用去除的硝酸根占输入总量的3%—60%. 并且发现硫酸盐还原产生的硫化物可以限制
N2 的产生. Spiteri等[71]通过二维变密度水流和反应运移数值模拟研究了不同氧化还原环境下氮元素的迁移与转移特征,结果表明在地下水与海水均处于氧化环境下,硝酸根的去除率非常低;在地下水处于氧化环境海水处于还原环境下,硝化作用会降低地下水中的铵根,但是由于地下水处于氧化环境,有机质的矿化作用又会增加铵根的浓度,由海水输入的铵根会被地下水中的氧气硝化为硝酸根,并且硝酸根的净去除量很小,主要是因为地下水中的氧气阻碍了反硝化作用;在地下水处于还原环境海水处于氧化环境时,在地下水中能够看到硝酸根的明显减小,同时在地下水与海水接触处能够观察到同时发生了硝化与反硝化作用;在海水与地下水均处于还原状态时,大部分人为硝酸根被去除. 数值模拟方法的优势在于能够较为直观地量化含氮元素组分的时空分布特征及其影响因素.SEAWAT软件是耦合MODFLOW和MT3D的变密度三维有限差分地下水模拟软件,该软件主要基于地下水流服从达西定律、流体间能够完全混溶且不可被压缩、含水层处于饱和状态等假设基础上. 该软件界面简单易操作以及其准确性较高,得到国内外学者广泛运用. 如Anwar等[79]通过SEAWAT-2005软件模拟研究了潮汐波动所引起的地下水中有机物含量变化,发现海水所引起海岸带内有机质含量的增加会促进反硝化作用的发生,并指出在仅考虑氧气的增加但未考虑有机质含量增加时硝酸根含量增长了32%,同时考虑氧气与有机质含量增加的情况发现硝酸根的去除率为90%.
MARUN(MARine UNsaturated)二维变饱和有限元模拟程序最早是由Boufadel教授研发[86],该软件具有开源功能,能够根据研究需求对原程序进行修改或添加,现如今该软件已能够刻画海浪、蒸散发、海岸带入渗边界等复杂条件,能够应用于潮汐作用下海岸带多孔介质内地下水的流动以及溶质迁移的模拟研究,在量化模拟海岸带地下水中营养盐、污染物、示踪剂以及溶解氧等方面具有良好的应用效果[83- 84]. 如Xiao等[87]通过MARUN模拟对比分析了海水盐度变化对硝化与反硝化作用的影响,并指出海水盐度恒定与否将改变硝化与反硝化发生区域和反应速率,在海水盐度恒定的情形下硝酸根与铵根去除率为78.6%和53%,而在海水盐度变化的情形下去除率则高达85.7%和72.2%,这表明潮汐变化的盐度条件通过改变反硝化和硝化的位置以及反应速率来影响海岸带内氮元素的生物地球化学反应.
SUTRA(Saturated-Unsaturated Transport)饱和/非饱和带运移模型是由美国地质调查局开发的,能够用以模拟饱和/非饱和带中水头、污染物浓度以及水温的时空分布. Nguyen等[72]通过实验和SUTRA-MS模拟得到,与等温条件相比,当海水温度高于地下水温度时,海岸带含水层中潮汐诱导的海水循环增加40%. Schutte等[88]通过SUTRA软件建立了Cabretta岛地下水流动模型,计算了在潮汐影响作用下海岸带内含水层内地下水的流速,为后续判定
N2O 的来源做理论支撑. -
本文论述了海岸带地下水中氮循环动态演化机制的主要影响因素,前述影响因素并不是独立存在的,往往是几个因素相互协同或者拮抗从而对海岸带内氮循环产生影响. 此外,同一个影响因素造成的影响结果也不尽相同,如温度能够通过增强微生物活性而加快氮化学反应速率,也会导致微生物呼吸速率加快,使得含水层中溶解氧含量降低进而抑制氮循环需氧反应的发生. 因此,需要进一步探究单一影响因素对氮循环过程的影响贡献占比. 此外,文献调研表明,对于海岸带内地下水氮元素地球化学过程的时间变异特征的某些控制因素的研究还较少,如降雨蒸发动态、渗透结构及其非均性、长时间尺度下的海洋和地下水动力条件演化.
现有关于海岸带含水层内氮元素的分布以及循环过程的研究多以非连续的化学监测为主,受限于监测效率,尚未揭示长时间尺度下水动力循环过程中的氮地球化学过程的时间变异规律. 现有室内实验研究主要集中在对化学条件的改变上,尚未充分考虑微生物、水动力等复杂因素的影响,并且受限于实验条件,未能实现不同空间尺度的氮生物地球化学过程的研究. 氮生物地球化学过程时间变异的模拟应结合室内外监测方法,综合考虑气象水文、潮汐水动力、温度—盐度环境、生物扰动及含水层非均质性等因素,以实现复杂条件下的高精度氮地球化学过程及其变化的定量识别.
海岸带地下水中氮生物地球化学过程研究进展
Research progress on nitrogen biogeochemical processes in coastal groundwater
-
摘要: 海岸带氮地球化学过程及其演化是海岸带水资源管理与生态环境保护的关键内容. 在气候波动以及海洋潮汐动态的影响下,海岸带地下水中氮的地球化学过程会表现出时间变异性. 基于国内外研究成果调研,本文针对海岸带含水层中的氮元素地球化学过程演化机制这一科学问题,归纳了影响海岸带氮元素地球化学过程的6个因素,包括温度、潮汐与波浪、海水入侵、盐度、生物扰动以及地下水动力条件;总结了氮生物地球化学过程动态演化机制的主要研究方法,包括野外水化学监测、室内氮循环实验和数值模拟方法;指出数值模拟应与室内外方法相结合,并综合考虑气象水文、潮汐水动力、温度、盐度、生物扰动及含水层非均质性等因素,以实现复杂条件下的高精度氮地球化学过程及其变化的定量识别.Abstract: Nitrogen biogeochemical processes and evolution in the coastal zone are key issues of water resources management and ecological environment protection of the coastal area. Under the influences of climate fluctuation and ocean tide dynamic, the nitrogen biogeochemical processes in coastal groundwater generally exhibit temporal variability. Aiming at the scientific problem of evolution mechanism of coastal nitrogen biogeochemical processes, based on literature research, this paper summarized six factors affecting the nitrogen biogeochemical processes in coastal zones, including temperature, tide and wave, seawater intrusion, salinity, biological disturbance and groundwater dynamic conditions. In addition, this paper summarized the main research methods for researching coastal nitrogen biogeochemical processes, including field monitoring, laboratory experiment and numerical simulation. Furthermore, to achieve high precision quantitative identification of nitrogen biogeochemical processes under complex conditions, we suggest that the numerical simulation should be combined applied with indoor and outdoor methods based on a comprehensive consideration of multi-factors such as meteorology and hydrology, tide dynamic, temperature, salinity, biological disturbance and aquifer heterogeneity.
-
表 1 海岸带地下水中氮生物地球化学过程演化机制主控因素
Table 1. The main controlling factors of the evolution mechanism of nitrogen biogeochemical processes in coastal groundwater
影响因素Influence factors 影响机制Mechanism of influence 参考文献Reference 温度 影响微生物活性影响咸淡水过渡带位置及海水再循环程度 [21-22] 潮汐与波浪 改变含水层咸淡水分布和水循环速率引起海岸带化学组分(如溶解氧和有机质)在沉积物和海水之间输运过程和含量 [23-24] 海水入侵 破坏原有咸淡水平衡状态增强离子交换 [25-26] 盐度 改变海岸带内氮循环过程所需微生物群落的组分改变地下水的电导率并间接影响氮循环过程增强离子交换促进硫酸盐还原为硫化氢,影响氮循环过程 [27] 生物扰动 挖掘洞穴导致海岸带含水介质渗透结构和水动力条件的改变增强含水介质中物质迁移,加快地球化学反应过程 [28] 地下水动力条件 引起地下水渗流速率时空差异控制溶解物质迁移速率和氧化还原环境变化 [29-30] 表 2 海岸带地下水中氮生物地球化学过程演化的主要研究方法
Table 2. Main methods for researching the evolution of nitrogen biogeochemical processes in coastal groundwater
研究方法Research method 方法描述Method description 优点Advantage 缺点Disadvantage 运用实例Examples 野外水化学监测 基于野外分层取样测定海岸带地下水中氮元素组分浓度动态分析氮循环过程和反应速率 能够较为直观地查明海岸带地下水中氮组分分布规律 难以进行高精度的连续监测,较难阐明氮循环动态规律 [58] 室内氮循环实验 基于室内刻画海岸带物理化学环境,模拟分析氮生物地球化学过程 能够阐明理想环境下氮循环过程对物理化学条件的响应规律 对实验环境要求较高,难以准确刻画海岸带实际的水动力与水化学条件 [69-70] 数值模拟 基于海岸带水动力水化学条件的概化,通过数值计算高性能多情景地模拟量化海岸带氮生物地球化学过程演化规律 能够多情景的三维展示氮组分的时空分布,并有助于揭示主控因素 模型概化过程中会简化实际物理化学条件 [71-72] -
[1] 王焰新, 甘义群, 邓娅敏, 等. 海岸带海陆交互作用过程及其生态环境效应研究进展 [J]. 地质科技通报, 2020, 39(1): 1-10. WANG Y X, GAN Y Q, DENG Y M, et al. Land-ocean interactions and their eco-environmental effects in the coastal zone: Current progress and future perspectives [J]. Bulletin of Geological Science and Technology, 2020, 39(1): 1-10(in Chinese).
[2] RIGAUD S, DEFLANDRE B, MAIRE O, et al. Transient biogeochemistry in intertidal sediments: New insights from tidal pools in Zostera noltei meadows of Arcachon Bay (France) [J]. Marine Chemistry, 2018, 200: 1-13. doi: 10.1016/j.marchem.2018.02.002 [3] HEISS J W, ULLMAN W J, MICHAEL H A. Swash zone moisture dynamics and unsaturated infiltration in two sandy beach aquifers [J]. Estuarine, Coastal and Shelf Science, 2014, 143: 20-31. doi: 10.1016/j.ecss.2014.03.015 [4] 季仲强, 翁焕新, 张锋, 等. 海底地下水排泄及其对沿海海域生态环境的潜在影响 [J]. 浙江大学学报(理学版), 2010, 37(5): 588-599. JI Z Q, WENG H X, ZHANG F, et al. Submarine groundwater discharge and its potential effect on coastal ocean's ecological environment [J]. Journal of Zhejiang University(Science Edition), 2010, 37(5): 588-599(in Chinese).
[5] JANSEN S, WALPERSDORF E, WERNER U, et al. Functioning of intertidal Flats inferred from temporal and spatial dynamics of O2, H2S and pH in their surface sediment [J]. Ocean Dynamics, 2009, 59(2): 317-332. doi: 10.1007/s10236-009-0179-4 [6] DENIS L, GEVAERT F, SPILMONT N. Microphytobenthic production estimated by in situ oxygen microprofiling: Short-term dynamics and carbon budget implications [J]. Journal of Soils and Sediments, 2012, 12(10): 1517-1529. doi: 10.1007/s11368-012-0588-8 [7] DELGARD M L, DEFLANDRE B, METZGER E, et al. In situ study of short-term variations of redox species chemistry in intertidal permeable sediments of the Arcachon lagoon [J]. Hydrobiologia, 2012, 699(1): 69-84. doi: 10.1007/s10750-012-1154-5 [8] 屠霄霞. 海岸带的脱氮过程研究进展 [J]. 浙江万里学院学报, 2013, 26(4): 1-5. doi: 10.3969/j.issn.1671-2250.2013.04.001 TU X X. The research progress of denitrification in the coastal zone [J]. Journal of Zhejiang Wanli University, 2013, 26(4): 1-5(in Chinese). doi: 10.3969/j.issn.1671-2250.2013.04.001
[9] 覃超梅, 周怀阳, 吴自军, 等. 珠江口淇澳岛海岸带反硝化作用研究 [J]. 海洋科学, 2009, 33(2): 74-79. QIN C M, ZHOU H Y, WU Z J, et al. The study of denitrification rate in Qi'ao Island coastal zone, Pearl River Estuary [J]. Marine Sciences, 2009, 33(2): 74-79(in Chinese).
[10] 晏维金, 章申, 王嘉慧. 长江流域氮的生物地球化学循环及其对输送无机氮的影响: 1968—1997年的时间变化分析 [J]. 地理学报, 2001, 56(5): 504-513. YAN W J, ZHANG S, WANG J H. Nitrogen biogeochemical cycling in the Changjiang drainage basin and its effect on Changjiang River dissolved inorganic nitrogen: Temporal trend for the period 1968-1997 [J]. Acta Geographica Sinica, 2001, 56(5): 504-513(in Chinese).
[11] LEE Y W, KIM G. Linking groundwater-borne nutrients and dinoflagellate red-tide outbreaks in the southern sea of Korea using a Ra tracer [J]. Estuarine, Coastal and Shelf Science, 2007, 71(1/2): 309-317. [12] 彭晓彤, 周怀阳. 海岸带营养盐生物地球化学研究评述 [J]. 海洋通报, 2002, 21(3): 69-77. doi: 10.3969/j.issn.1001-6392.2002.03.011 PENG X T, ZHOU H Y. A review of nutrient biogeochemistry research of the coastal zone [J]. Marine Science Bulleten, 2002, 21(3): 69-77(in Chinese). doi: 10.3969/j.issn.1001-6392.2002.03.011
[13] GONNEEA M E, CHARETTE M A. Hydrologic controls on nutrient cycling in an unconfined coastal aquifer [J]. Environmental Science & Technology, 2014, 48(24): 14178-14185. [14] 姜德娟, 毕晓丽. 流域-河口-近海系统氮、磷营养盐输移研究综述 [J]. 水科学进展, 2010, 21(3): 421-429. JIANG D J, BI X L. Review of studies on nitrogen and phosphorus transport in the continuum of watersheds, estuaries and offshore areas [J]. Advances in Water Science, 2010, 21(3): 421-429(in Chinese).
[15] MARCHANT H K, HOLTAPPELS M, LAVIK G, et al. Coupled nitrification-denitrification leads to extensive N loss in subtidal permeable sediments [J]. Limnology and Oceanography, 2016, 61(3): 1033-1048. doi: 10.1002/lno.10271 [16] 郭靖. 广西北部湾近岸海域氮生物地球化学过程及营养盐沉积记录[D]. 南宁: 广西大学, 2020. GUO J. Nitrogen biogeochemical processes and geochemical record of anthropogenic nutrient loading in coastal regions of beibu gulf, Guangxi Province[D]. Nanning: Guangxi University, 2020(in Chinese).
[17] 徐继荣, 王友绍, 孙松. 海岸带地区的固氮、氨化、硝化与反硝化特征 [J]. 生态学报, 2004, 24(12): 2907-2914. doi: 10.3321/j.issn:1000-0933.2004.12.036 XU J R, WANG Y S, SUN S. The characteristics of nitrogen fixation, ammonification, nitrification and denitrification in coastal zones [J]. Acta Ecologica Sinica, 2004, 24(12): 2907-2914(in Chinese). doi: 10.3321/j.issn:1000-0933.2004.12.036
[18] LIU Y, LIANG W Z, JIAO J J. Seasonality of nutrient flux and biogeochemistry in an intertidal aquifer [J]. Journal of Geophysical Research:Oceans, 2018, 123(9): 6116-6135. doi: 10.1029/2018JC014197 [19] 王军, 陈振楼, 王东启, 等. 长江口滨岸湿地无机氮界面交换通量量算 [J]. 地理学报, 2006, 61(7): 729-740. doi: 10.3321/j.issn:0375-5444.2006.07.007 WANG J, CHEN Z L, WANG D Q, et al. Calculation of inorganic nitrogen fluxes in the Yangtze Estuary tidal wetland [J]. Acta Geographica Sinica, 2006, 61(7): 729-740(in Chinese). doi: 10.3321/j.issn:0375-5444.2006.07.007
[20] COUTURIER M, TOMMI-MORIN G, SIROIS M, et al. Nitrogen transformations along a shallow subterranean estuary [J]. Biogeosciences, 2017, 14(13): 3321-3336. doi: 10.5194/bg-14-3321-2017 [21] COGSWELL C, HEISS J W. Climate and seasonal temperature controls on biogeochemical transformations in unconfined coastal aquifers [J]. Journal of Geophysical Research:Biogeosciences, 2021, 126(12): e2021JG006605. [22] PU L, XIN P, NGUYEN T T M, et al. Thermal effects on flow and salinity distributions in coastal confined aquifers [J]. Water Resources Research, 2020, 56(10): e2020WR027582. [23] HEISS J W, MICHAEL H A. Saltwater-freshwater mixing dynamics in a sandy beach aquifer over tidal, spring-neap, and seasonal cycles [J]. Water Resources Research, 2014, 50(8): 6747-6766. doi: 10.1002/2014WR015574 [24] KROEGER K D, CHARETTE M A. Nitrogen biogeochemistry of submarine groundwater discharge [J]. Limnology and Oceanography, 2008, 53(3): 1025-1039. doi: 10.4319/lo.2008.53.3.1025 [25] 吴自军, 王富康, 崔振昂, 等. 基于近岸系列分层竖井的海底地下水排泄及其营养盐输入研究 [J]. 同济大学学报(自然科学版), 2021, 49(3): 449-457. doi: 10.11908/j.issn.0253-374x.20313 WU Z J, WANG F K, CUI Z A, et al. Submarine groundwater discharge and dependent nutrient input based on a series of layered monitoring wells [J]. Journal of Tongji University(Natural Science), 2021, 49(3): 449-457(in Chinese). doi: 10.11908/j.issn.0253-374x.20313
[26] ARDÓN M, MORSE J L, COLMAN B P, et al. Drought-induced saltwater incursion leads to increased wetland nitrogen export [J]. Global Change Biology, 2013, 19(10): 2976-2985. doi: 10.1111/gcb.12287 [27] ZHOU M H, BUTTERBACH-BAHL K, VEREECKEN H, et al. A meta-analysis of soil salinization effects on nitrogen pools, cycles and fluxes in coastal ecosystems [J]. Global Change Biology, 2017, 23(3): 1338-1352. doi: 10.1111/gcb.13430 [28] 肖凯. 滨海湿地潮间带氮循环及大孔隙优先流机制研究[D]. 北京: 中国地质大学(北京), 2018. XIAO K. Nitrogen cycle and hydrodynamics of macropores as preferential flow conduits in the intertidal zone of coastal wetlands[D]. Beijing: China University of Geosciences, 2018(in Chinese).
[29] SANTOS I R, EYRE B D, GLUD R N. Influence of porewater advection on denitrification in carbonate sands: Evidence from repacked sediment column experiments [J]. Geochimica et Cosmochimica Acta, 2012, 96: 247-258. doi: 10.1016/j.gca.2012.08.018 [30] LOVELESS A M, OLDHAM C E. Natural attenuation of nitrogen in groundwater discharging through a sandy beach [J]. Biogeochemistry, 2010, 98(1/2/3): 75-87. [31] 王东启, 陈振楼, 许世远, 等. 长江口崇明东滩沉积物反硝化作用研究 [J]. 中国科学. D辑:地球科学, 2006, 36(6): 544-551. WANG D Q, CHEN Z L, XU S Y, et al. Study on the denitrification of sediments in Chongming Dongtan at the mouth of the Yangtze River [J]. Science in China (Series D:Earth Sciences), 2006, 36(6): 544-551(in Chinese).
[32] 蔡有军. 中国典型潮间带沉积物厌氧脱氮通量及其微生物驱动机制研究[D]. 扬州: 扬州大学, 2019. CAI Y J. Anaerobic nitrogen removal flux of typical intertidal sediments in China and its microbial driving mechanism[D]. Yangzhou: Yangzhou University, 2019(in Chinese).
[33] KUYPERS M M M, MARCHANT H K, KARTAL B. The microbial nitrogen-cycling network [J]. Nature Reviews Microbiology, 2018, 16(5): 263-276. doi: 10.1038/nrmicro.2018.9 [34] 周煜琦, 张照婧, 位光山, 等. 全球变化下海岸带微生物生态研究进展 [J]. 微生物学报, 2021, 61(6): 1743-1760. ZHOU Y Q, ZHANG Z J, WEI G S, et al. The impact of global change on microbes in coastal ecosystem [J]. Acta Microbiologica Sinica, 2021, 61(6): 1743-1760(in Chinese).
[35] 孙志强, 郝庆菊, 江长胜, 等. 农田土壤N2O的产生机制及其影响因素研究进展 [J]. 土壤通报, 2010, 41(6): 1524-1530. SUN Z Q, HAO Q J, JIANG C S, et al. Advances in the study of nitrous oxide production mechanism and its influencing factors in agricultural soils [J]. Chinese Journal of Soil Science, 2010, 41(6): 1524-1530(in Chinese).
[36] HERBERT R A. Nitrogen cycling in coastal marine ecosystems [J]. FEMS Microbiology Reviews, 1999, 23(5): 563-590. doi: 10.1111/j.1574-6976.1999.tb00414.x [37] 龚骏, 张晓黎. 微生物在近海氮循环过程的贡献与驱动机制 [J]. 微生物学通报, 2013, 40(1): 44-58. GONG J, ZHANG X L. Contribution and mechanism of microbe-driving nitrogen cycling processes in coastal ecosystems [J]. Microbiology China, 2013, 40(1): 44-58(in Chinese).
[38] BECK M, RECKHARDT A, AMELSBERG J, et al. The drivers of biogeochemistry in beach ecosystems: A cross-shore transect from the dunes to the low-water line [J]. Marine Chemistry, 2017, 190: 35-50. doi: 10.1016/j.marchem.2017.01.001 [39] KIM K H, HEISS J W, MICHAEL H A, et al. Spatial patterns of groundwater biogeochemical reactivity in an intertidal beach aquifer [J]. Journal of Geophysical Research:Biogeosciences, 2017, 122(10): 2548-2562. [40] ROBINSON C, LI L, BARRY D A. Effect of tidal forcing on a subterranean estuary [J]. Advances in Water Resources, 2007, 30(4): 851-865. [41] 屈璠, 刘敏, 侯立军, 等. 潮汐循环影响下上覆水环境因子和氮营养盐的变化及其相关关系 [J]. 长江流域资源与环境, 2007, 16(3): 345-350. QU F, LIU M, HOU L J, et al. Change of environmental parameters and inorganic nitrogen in overlying water in relation with tidal cycles [J]. Resources and Environment in the Yangtze Basin, 2007, 16(3): 345-350(in Chinese).
[42] HEISS J W, POST V E A, LAATTOE T, et al. Physical controls on biogeochemical processes in intertidal zones of beach aquifers [J]. Water Resources Research, 2017, 53(11): 9225-9244. [43] 陈杰. 中国潮间带滩涂沉积物碳氮磷的埋藏特征[D]. 上海: 华东师范大学, 2021. CHEN J. The characteristics of carbon, nitrogen and phosphorus burial in Chinese intertidal wetlands[D]. Shanghai: East China Normal University, 2021(in Chinese).
[44] ABARCA E, KARAM H, HEMOND H F, et al. Transient groundwater dynamics in a coastal aquifer: The effects of tides, the lunar cycle, and the beach profile [J]. Water Resources Research, 2013, 49(5): 2473-2488. [45] CHARBONNIER C, ANSCHUTZ P, DEFLANDRE B, et al. Measuring pore water oxygen of a high-energy beach using buried probes [J]. Estuarine, Coastal and Shelf Science, 2016, 179: 66-78. [46] 赵世彬, 陈广泉, 张晓影, 等. 潮汐影响下的海岸带地下河口水交换及其生物地球化学效应 [J]. 海洋地质前沿, 2018, 34(9): 73-78. ZHAO S B, CHEN G Q, ZHANG X Y, et al. Water exchange and biogeochemical effects of subterranean estuary with tide [J]. Marine Geology Frontiers, 2018, 34(9): 73-78(in Chinese).
[47] RECKHARDT A, BECK M, SEIDEL M, et al. Carbon, nutrient and trace metal cycling in sandy sediments: A comparison of high-energy beaches and backbarrier tidal flats [J]. Estuarine, Coastal and Shelf Science, 2015, 159: 1-14. [48] ANSCHUTZ P, CHARBONNIER C, DEBORDE J, et al. Terrestrial groundwater and nutrient discharge along the 240-km-long Aquitanian coast [J]. Marine Chemistry, 2016, 185: 38-47. [49] LIU Y, JIAO J J, LIANG W Z, et al. Tidal pumping-induced nutrients dynamics and biogeochemical implications in an intertidal aquifer [J]. Journal of Geophysical Research:Biogeosciences, 2017, 122(12): 3322-3342. [50] 熊贵耀, 付腾飞, 徐兴永, 等. 滨海含水层海水入侵影响因素研究综述 [J]. 海洋科学, 2019, 43(6): 102-112. XIONG G Y, FU T F, XU X Y, et al. Review of factors affecting seawater intrusion in coastal aquifers [J]. Marine Sciences, 2019, 43(6): 102-112(in Chinese).
[51] 蔡舰, 白承荣, 巴图那生, 等. 盐度对芦苇(Phragmites australis)表流湿地除氮效果的影响 [J]. 湖泊科学, 2017, 29(6): 1350-1358. CAI J, BAI C R, BA T, et al. Effect of salinity on nitrogen removal performance in a Phragmites australis constructed surface flow wetland [J]. Journal of Lake Sciences, 2017, 29(6): 1350-1358(in Chinese).
[52] SANTORO A E. Microbial nitrogen cycling at the saltwater–freshwater interface [J]. Hydrogeology Journal, 2010, 18(1): 187-202. [53] 赵林丽, 姜小三, 邵学新, 等. 模拟盐度变化对人工湿地脱氮除磷效果的影响 [J]. 土壤, 2019, 51(6): 1122-1128. ZHAO L L, JIANG X S, SHAO X X, et al. Effects of simulated salinity change on nitrogen and phosphorus removal in constructed wetland [J]. Soils, 2019, 51(6): 1122-1128(in Chinese).
[54] 张林海, 刘荣芳, 仝川, 等. 盐度对闽江河口淡水洲滩土壤潜在反硝化速率及脱氮效率的影响 [J]. 湿地科学, 2015, 13(5): 528-534. ZHANG L H, LIU R F, TONG C, et al. Effect of salinity on the potential denitrification rate and nitrogen removal of the Min River estury freshwater river beach soil [J]. Wetland Science, 2015, 13(5): 528-534(in Chinese).
[55] 杨长明, 蔡雯娟, 李建华. 模拟咸水入侵对崇明岛河岸带根际土壤微生物及反硝化作用的影响 [J]. 应用生态学报, 2012, 23(4): 1083-1089. YANG C M, CAI W J, LI J H. Effects of saltwater incursion on the microbiological characteristics and denitrification in a riparian rhizosphere soil in Chongming Island of Shanghai, East China [J]. Chinese Journal of Applied Ecology, 2012, 23(4): 1083-1089(in Chinese).
[56] 覃超梅. 珠江口淇澳岛海岸带氮生物地球化学研究[D]. 北京: 中国科学院研究生院(广州地球化学研究所), 2005. QIN C M. The study of nitrogen biogeochemistry in the coastal zone of the qi’ao island, pearl piver estuary[D]. Beijing: Institute of Chemistry, Chinese Academy of Sciences, 2005(in Chinese).
[57] LARSEN L, MOSEMAN S, SANTORO A, et al. A complex-systems approach to predicting effects of sea level rise and nitrogen loading on nitrogen cycling in coastal wetland ecosystems[J]. Ecological Dissertations in the Aquatic Sciences Symposium Proceedings, 2010: 67-92. [58] HEATON T H E, STUART M E, SAPIANO M, et al. An isotope study of the sources of nitrate in Malta's groundwater [J]. Journal of Hydrology, 2012, 414/415: 244-254. [59] KRISTENSEN E. Mangrove crabs as ecosystem engineers; with emphasis on sediment processes [J]. Journal of Sea Research, 2008, 59: 30-43. [60] 陈淑云. 螃蟹对闽江河口互花米草湿地土壤理化性质、温室气体排放与枯落物分解影响[D]. 福州: 福建师范大学, 2016. CHEN S Y. Effect of crabs on soil properties, greenhouse gases emission and litter decomposition in Minjiang River estuarine Spartina alternifora wetland[D]. Fuzhou: Fujian Normal University, 2016(in Chinese).
[61] 刘敏, 侯立军, 许世远, 等. 长江口潮滩生态系统氮微循环过程中大型底栖动物效应实验模拟 [J]. 生态学报, 2005, 25(5): 1132-1137. LIU M, HOU L J, XU S Y, et al. Experimental simulation of the effects of macrobenthos on the microcycling of nitrogen in the Yangtze estuarine and tidal flat ecosystem [J]. Acta Ecologica Sinica, 2005, 25(5): 1132-1137(in Chinese).
[62] 陈光程. 九龙江口秋茄红树植被与主要大型底栖动物某些生态关系的研究[D]. 厦门: 厦门大学, 2009. CHEN G C. Study of certain ecological relationships between Kandelia candel vegetation and common macro-benthic fauna in Jiulongjiang Estuary[D]. Xiamen: Xiamen University, 2009(in Chinese).
[63] SANTOS I R, EYRE B D, HUETTEL M. The driving forces of porewater and groundwater flow in permeable coastal sediments: A review [J]. Estuarine, Coastal and Shelf Science, 2012, 98: 1-15. [64] BAKHTYAR R, BROVELLI A, BARRY D A, et al. Wave-induced water table fluctuations, sediment transport and beach profile change: Modeling and comparison with large-scale laboratory experiments [J]. Coastal Engineering, 2011, 58(1): 103-118. [65] RIEDEL T, LETTMANN K, BECK M, et al. Tidal variations in groundwater storage and associated discharge from an intertidal coastal aquifer [J]. Journal of Geophysical Research Atmospheres, 2010, 115(C4): C04013. [66] CARDENAS M B, COOK P L M, JIANG H S, et al. Constraining denitrification in permeable wave-influenced marine sediment using linked hydrodynamic and biogeochemical modeling [J]. Earth and Planetary Science Letters, 2008, 275(1/2): 127-137. [67] GAO H, SCHREIBER F, COLLINS G, et al. Aerobic denitrification in permeable wadden sea sediments [J]. The ISME Journal, 2010, 4(3): 417-426. [68] SCHUTTE C A, HUANCA-VALENZUELA P, LAVIK G, et al. Advection drives nitrate past the microphytobenthos in intertidal sands, fueling deeper denitrification [J]. Frontiers in Microbiology, 2021, 12: 556268. [69] 张锋, 翁焕新, 陈力琦, 等. 海底地下水和海水混合营养盐变化的模拟实验研究 [J]. 海洋学报(中文版), 2010, 32(3): 167-175. ZHANG F, WENG H X, CHEN L Q, et al. The simulation study on changes of nutrients in mixing of groundwater with seawater [J]. Acta Oceanologica Sinica, 2010, 32(3): 167-175(in Chinese).
[70] MARCHANT H K, LAVIK G, HOLTAPPELS M, et al. The fate of nitrate in intertidal permeable sediments [J]. PLoS One, 2014, 9(8): e104517. [71] SPITERI C, SLOMP C P, TUNCAY K, et al. Modeling biogeochemical processes in subterranean estuaries: Effect of flow dynamics and redox conditions on submarine groundwater discharge of nutrients [J]. Water Resources Research, 2008, 44(2): W02430. [72] NGUYEN T T M, YU X Y, PU L, et al. Effects of temperature on tidally influenced coastal unconfined aquifers [J]. Water Resources Research, 2020, 56(4): e2019WR026660. [73] 康萍萍. 滨海地下水氮的同位素溯源及其源贡献率研究[D]. 大连: 大连理工大学, 2016. KANG P P. Identifying nitrogen sources and quantitfying the contributions of nitrate sources in coastal zone[D]. Dalian: Dalian University of Technology, 2016(in Chinese).
[74] 胡娜娜, 盛彦清, 唐琪, 等. 海岸带水体氮、磷的测定方法与准确测定 [J]. 海洋科学进展, 2022, 40(2): 274-286. HU N N, SHENG Y Q, TANG Q, et al. Determination method and accurate determination of nitrogen and phosphorus in coastal water [J]. Advances in Marine Science, 2022, 40(2): 274-286(in Chinese).
[75] 曹慧丽, 樊丹丹, 姚敏杰, 等. 土壤反硝化过程速率测定方法 [J]. 应用与环境生物学报, 2021, 27(4): 1102-1109. CAO H L, FAN D D, YAO M J, et al. Methods for measuring soil denitrification rate [J]. Chinese Journal of Applied and Environmental Biology, 2021, 27(4): 1102-1109(in Chinese).
[76] 陈力琦. 地下水与海水混合过程中营养盐变化的模拟研究[D]. 杭州: 浙江大学, 2008. CHEN L Q. Indoor modeling investigation of nutritious salt in commixxing of groundwater and seawater by different conditions[D]. Hangzhou: Zhejiang University, 2008(in Chinese).
[77] 郎漫, 李平, 蔡祖聪. 反硝化测定方法的评述 [J]. 土壤通报, 2012, 43(4): 1019-1024. LANG M, LI P, CAI Z C. The Comments on Methods for Measuring Denitrification [J]. Chinese Journal of Soil Science, 2012, 43(4): 1019-1024(in Chinese).
[78] 林来昌, 林燕臻, 李家兵. 闽江口互花米草入侵年限对沉积物的硝化-反硝化影响 [J]. 泉州师范学院学报, 2022, 40(2): 24-30. LIN L C, LIN Y Z, LI J B. Effects of invasion years of Spartina alterniflora on the nitrification and denitrification of sediments in the Min River Estuary [J]. Journal of Quanzhou Normal University, 2022, 40(2): 24-30(in Chinese).
[79] ANWAR N, ROBINSON C, BARRY D A. Influence of tides and waves on the fate of nutrients in a nearshore aquifer: Numerical simulations [J]. Advances in Water Resources, 2014, 73: 203-213. [80] 辛沛, 金光球, 李凌. 潮汐作用下盐沼孔隙水流动及溶质运移模拟 [J]. 水科学进展, 2009, 20(3): 379-384. XIN P, JIN G Q, LI L. Modelling of tide induced pore water flow and solute transport in a salt marsh [J]. Advances in Water Science, 2009, 20(3): 379-384(in Chinese).
[81] 李采, 何庆成. 饱和带/非饱和带运移模型(SUTRA)软件介绍 [J]. 水文地质工程地质, 2005, 32(1): 119-120. LI C, HE Q C. The introduction to saturated/unsaturated band migration model (SUTRA) software [J]. Hydrogeology and Engineering Geology, 2005, 32(1): 119-120(in Chinese).
[82] 薛显武. 基于GIS的威海市海水入侵可视化数值模拟系统研究[D]. 南京: 河海大学, 2007. XUE X W. GIS-based visualized numerical modeling system for seawater intrusion in Weihai City[D]. Nanjing: Hohai University, 2007(in Chinese).
[83] 王梦婷. 海岸带潜水含水层传统盐楔中营养盐运移反应的数值模拟[D]. 北京: 中国地质大学(北京), 2020. WANG M T. Numerical simulation of nutrient transport and transformations in traditional saltwater wedge of coastal aquifer[D]. Beijing: China University of Geosciences, 2020(in Chinese).
[84] 孙锐. 利用运移—反应数值模型模拟海岸带营养盐输入过程[D]. 北京: 中国地质大学(北京), 2018. SUN R. Numerical simulation of coastal nutrient input processes using transport-reaction numerical model[D]. Beijing: China University of Geosciences, 2018(in Chinese).
[85] MEILE C, PORUBSKY W P, WALKER R L, et al. Natural attenuation of nitrogen loading from septic effluents: Spatial and environmental controls [J]. Water Research, 2010, 44(5): 1399-1408. [86] BOUFADEL M C, SUIDAN M T, VENOSA A D. A numerical model for density-and-viscosity-dependent flows in two-dimensional variably saturated porous media [J]. Journal of Contaminant Hydrology, 1999, 37(1/2): 1-20. [87] XIAO K, LI H, XIA Y, et al. Effects of Tidally Varying Salinity on Groundwater Flow and Solute Transport: Insights From Modelling an Idealized Creek Marsh Aquifer [J]. Water Resources Research, 2019, 55(11): 9656-9672. [88] SCHUTTE C A, JOYE S B, WILSON A M, et al. Intense nitrogen cycling in permeable intertidal sediment revealed by a nitrous oxide hot spot [J]. Global Biogeochemical Cycles, 2015, 29(10): 1584-1598. -




 下载:
下载:













