-
新型有机污染物(emerging organic contaminants, EOCs)指环境中新出现或最近引起关注,可能对生态系统和人体健康产生风险,管理措施不足或尚未纳入管理的有机污染物[1-4]. 主要包括药品和个人护理品(pharmaceuticals and personal care products, PPCP)、阻燃剂(flame retardant)、塑化剂(plasticizers)、杀虫剂,激素、表面活性剂等[3,5]. 这些EOCs在日常生活和工业生产中被频繁使用并广泛存在,如多溴联苯醚(polybrominated diphenyl ethers, PBDEs)是一种典型的溴代阻燃剂,具有阻燃效果好、生产成本低等特点,曾是应用最广泛的阻燃剂[6]. 近些年研究发现其具有环境持久性、生物累积性和生物毒性,目前已在全球范围内被禁用,并逐渐被有机磷酸酯阻燃剂(organophosphate flame retardants, OPFRs)取代[6—7]. 邻苯二甲酸酯(phthalic acid esters, PAEs)具有可塑性、耐久性,能够提高材料强度和透明度等优点[7—8],是一种常用的塑料添加剂,进入人体后经代谢转化可形成单酯或单酯的氧化产物即邻苯二甲酸酯代谢物(phthalate metabolites,mPAEs). 全氟及多氟烷基化合物(per-fluorinatedand polyfluoroalkyl compounds,PFASs)具有化学及热稳定性[9]、高表面活性及疏水疏油性[10]等特点,结构中含有极其稳定的C—F键,不易发生热解、光解、水解和生物降解,具有较强的生物蓄积性[11]. 上述化合物常以非化学键或直接添加的形式在塑料、建材、食品包装材料、电子设备、玩具、化妆品、农药、纸张、地毯、纺织品、家具等产品中被广泛使用[9,12—15],因而容易在产品生产、使用及回收处理过程经磨损、挥发等途径释放到环境中[16]. 目前已在土壤[17]、水体[18]、室内灰尘[19]等环境介质以及鱼[20]、蛋[21]等日常食品中被广泛检出,并可通过食物摄入、呼吸吸入和皮肤接触等途径进入人体,如血液、尿液、母乳、指甲等人体样品中已有关于PBDEs、PFASs、OPFRs、PAEs以及mPAEs检出的报道[22—26]. 同时研究发现这些EOCs能够导致人体内分泌紊乱,具有神经毒性、生殖毒性、内分泌毒性和致癌性等[27—28].
相较于血液、尿液、母乳等传统生物基质,头发具有采集方便、易储存、非侵入性采样、易被采集对象接纳等优点,常做为生物监测材料用于法医、毒品、重金属及有机污染物等研究,反映人体长期暴露情况. 尽管目前已有多篇文献报道了关于头发中EOCs检测方法[11, 29—31],但能够同时分析头发中多种EOCs的研究较为缺乏. 现有文献多采用硝酸消解的方法检测头发中的PBDEs、OPFRs和PAEs等污染物[6, 32—34],PFASs则多使用碱消解[35]. 两种消解方式存在费时、耗费溶剂、缺乏安全性等缺点. 此外有研究显示,酸/碱消解破坏头发结构的同时释放的一些内源性物质可能会影响头发中目标污染物如PFASs[11]的检测,具有一定局限性;相比之下,头发研磨后经有机溶剂萃取,能够更准确的反映头发中PFASs的污染水平[11, 36-37],然而该方法是否同样适用于其他种类的EOCs目前还缺少相关的文献报道.
因此,本研究在以往研究的基础上,通过优化有机萃取溶剂和分散固相萃取剂种类,建立了仅用少量头发样品(0.1 g)和有机溶剂即可同时检测头发中15种PAEs、12种PFASs、11种OPFRs、8种mPAEs及8种PBDEs共5大类54种EOCs的前处理方法,该方法节约溶剂且更为安全快速,同时采用本研究建立的前处理方法,分析了广州市10例普通男性头发中5类有机污染物的浓度水平.
-
材料与试剂:离心管(目盛付,日本),色谱级乙酸铵(CH3COONH4)、甲酸(HCOOH)、乙腈(ACN)、乙酸乙酯(EtAC)、甲基叔丁基醚(MTBE)、异辛烷(ISO)、正己烷(HEX)、二氯甲烷(DCM)和丙酮(ACE),无水硫酸镁(MgSO4)、无水硫酸钠(Na2SO4)、N-丙基乙二胺(PSA)、十八烷基硅烷键合硅胶(C18)和石墨化炭黑(GCB)(上海安谱实验科技股份有限公司,中国),甲醇(MEOH)(默克,德国).
仪器:AB SCIEX API 4000三重四极杆质谱仪(AB SCIEX, 美国);Agilent 7890B气相色谱仪、Agilent 1260液相色谱仪、Agilent 5977A质谱仪、Agilent 5975C质谱仪、DB-5HT毛细管柱(15 m×0.25 mm i.d., 0.10 μm)、DB-5MS毛细管柱(30 m×0.25 mm i.d., 0.25 μm)、Poroshell 120EC-C18(2.1 mm×100 mm, 2.7 μm)(安捷伦,美国);Kinetex EVO-C18100 A色谱柱(2.1 mm×100 mm, 5 μm),Kinetex×2.6 μm Bipheny l00 A(2.1 mm×100 mm)(Phenomenex,美国). 分析天平(上海安亭电子仪器厂,中国),氮吹仪(柏林河西路,美国),Milli-Q超纯水系统(默克,德国),涡旋振荡器(特朗纳,美国),冷冻干燥机(SP Scientific,美国),Eppendorf 5810低速冷冻离心机(Eppendorf,比利时). KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司,中国),行星式球磨仪(弗卡斯实验仪器有限公司,中国).
-
PBDEs、PAEs、mPAEs化合物标准品(AccuStandard,美国),PFASs化合物标准品(wellington,加拿大),OPFRs化合物标准品(CIL(Cambridge Isotope Laboratorie),美国)及对应内标标准品信息见表1.
-
以广州市年龄在18—40岁,且近期无烫染发行为的男性作为研究对象,志愿者在了解本次研究目的并签署知情同意书后,贴近头皮采集全部头发样品,铝箔纸包裹编号后放入密实袋,干燥阴凉处保存,每份样品大于5 g. 采集后的头发置于锥形瓶, Milli-Q水振荡清洗两遍,去除头发表面附着的灰尘等外部污染物,进行冷冻干燥. 实验前用HEX洗过的不锈钢剪刀将其剪短至0.5—1 cm. 采用行星式球磨仪将头发样品充分研磨成粉/絮状. 取0.1 g研磨头发于离心管加入1mL EtAC及20 μL各类目标物的同位素内标(OPFRs、PFASs、mPAEs的内标及13C12-BDE 209的质量浓度为100 ng·mL−1,BDE 118、BDE 128的质量浓度为200 ng·mL−1,PAEs 内标的质量浓度为500 ng·mL−1),通风橱静置过夜使溶剂挥发. 然后加入HEX、ACE、ACN及EtAC(1:1:1:1, V/V/V/V)的混合溶液4 mL,2000 r·min−1涡旋4 min, 20 ℃ 超声20 min,4000 r·min−1离心15 min取上清,重复3次. 上清液氮吹浓缩至1 mL后加入 20 mg 无水Na2SO4和100 mg C18进行净化. 1200 r·min−1涡旋7 min、3500 r·min−1离心15 min,转移上清液至干净的玻璃管中,氮吹近干后200 μL MEOH复溶,-20 ℃下静置4—6 h冷冻沉淀除杂,上清液待GC-MS、GC-MS/MS和LC-MS/MS检测分析.
-
PBDEs和PAEs分别采用气相色谱-质谱联用仪(GC-MS)和三重四极杆气相色谱质谱联用仪(GC-MS/MS)进行分析. PBDEs:负化学离子源(NCI),DB-5HT色谱柱(15 m×0.25 mm i.d., 0.10 μm)分离. 起始温度110 °C,保留5 min,20 °C·min−1升至200 °C,保持4.5 min,10 °C·min−1升至310 °C,保持15 min. PAEs:DB-5MS毛细管柱(30 m × 0.25 mm i.d., 0.25 μm),进样口温度290℃,传输线温度150 ℃;载气为氦气,流速1 mL·min−1;起始温度90 ℃,15 °C·min−1的速率升至310 ℃,保持5 min. 溶剂延迟5 min,EI源,电子轰击能量70 eV,多重反应监测模式(MRM);离子源温度230 ℃,四极杆温度150 ℃. 不分流进样且进样量均为1 μL.
OPFRs、PFASs、mPAEs使用Agilent 1260液相色谱仪、AB SCIEX API 4000+ MS/MS三重四极杆串联质谱仪分析(LC-MS/MS),色谱柱分别为:Kinetex 2.6 μm Biphenyl 100 A(2.1 mm×100 mm)、Poroshell 120 EC-C18(4.6 mm× 100 mm, 2.7 μm)、Kinetex EVO-C18 100 A(2.1 mm × 100 mm,5 μm),均采用电喷雾电离源(ESI)及多反应监测模式(MRM),进样量5 μL,其余仪器分析条件见表2.
-
所有玻璃器材使用前均采用碱液(pH>11)浸泡4 h以上,经自来水及超纯水冲洗并用烘箱烘干,再在400 ℃的马弗炉中焙烧4 h,使用前经DCM和HEX淋洗吹干. 方法定量限(limit of quantification,LOQ)和方法检出限(limit of detection,LOD)为空白样品中目标化合物浓度的均值加10倍或者3倍标准差,空白未检出时定义为10倍或者3倍信噪比. 实验采用内标法定量,设置空白、基质、空白加标和基质加标等4组实验且每组3个重复,用空白加标和基质加标浓度减去空白和基质的平均浓度计算回收率和相对标准差.
-
现有研究中,EtAC、HEX、ACE、MTBE常用作OPFRs、PAEs、PAFSs和PBDEs的提取剂或洗脱剂[38—42] ,本研究在以往研究基础上首先采用ACE、HEX和MTBE对头发中污染物进行提取[16]. 分散固相萃取剂参考Zafeiraki [21]和熊仕茂[43]对OPFRs和PFASs的净化条件,具体如表3中方案1所示. 另有文献指出,研磨处理可提高头发样品中污染物的提取效率[11,37,44],故本研究在进行EOCs提取前将所有头发充分研磨成粉/絮状.
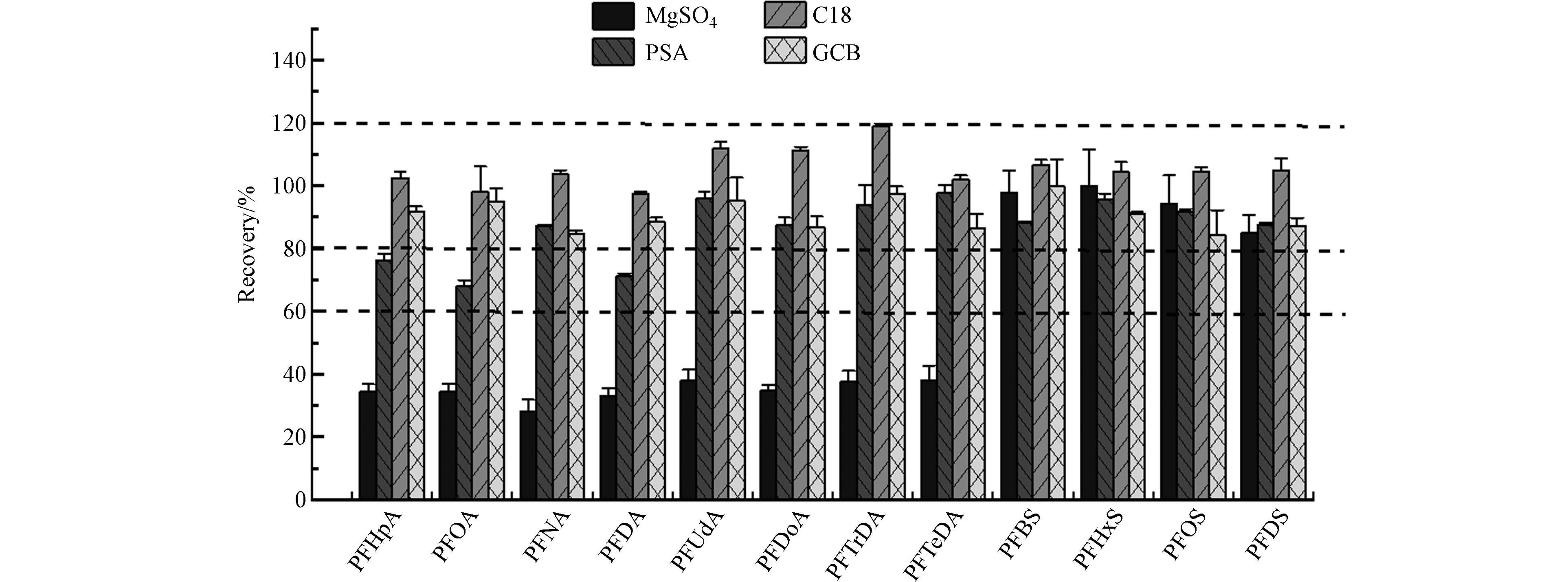
头发样品经方案1处理后,PBDEs、OPFRs和PAEs三类污染物均有较好效果,回收率和相对标准偏差分别介于40%—129%和0.1%—21.4%之间. 而PFASs中仅PFHxS、PFOS和PFDS的回收率在60%以上,其余几种化合物空白和基质加标的回收率小于7%,损失较为严重. 为进一步探究分散固相萃取填料对PFASs的影响,溶剂加标后分别采用MgSO4、PSA、C18和GCB净化,结果如图1所示. PFASs的回收率整体呈现C18>GCB>PSA>MgSO4的趋势. 其中经MgSO4处理后,8种全氟烷酸的回收率均低于50%,推测MgSO4可能对PFASs类污染物具有较强的吸附效应,因此回收率相对差. MgSO4作为干燥剂可吸收溶液中的微量水分[38, 45],考虑到可能存在的吸附作用,后续实验改用无水Na2SO4. C18一般用于去除脂肪等非极性杂质[38],研究结果显示其对大多数化合物的影响最小[46],因此实验选用无水Na2SO4和C18作为净化填料.
-
确定净化填料后,进一步对有机萃取溶剂展开优化. Alves等[22]分别比较了乙酸乙酯、异丙醇、四氢呋喃/异丙醇的(50:50, V/V)对PFASs的提取效果,发现乙酸乙酯效果最好(回收率69.0%—141%之间). 此外乙酸乙酯常作为OPFRs优良的提取剂或洗脱剂,能够获得较好的回收效果[41],故本研究分别对比了ACE+HEX+MTBE(方案2)和EtAC+HEX+MTBE(方案3)对5类污染物的提取效率. 结果显示,经方案2处理后,EHDPP、PFHpA和PFOA的回收率较差,回收率在29.6%—42.8%之间;而方案3处理后EHDPP、PFBS的回收率在21.4%—48.2%之间,两种方案均存在一定的缺陷.
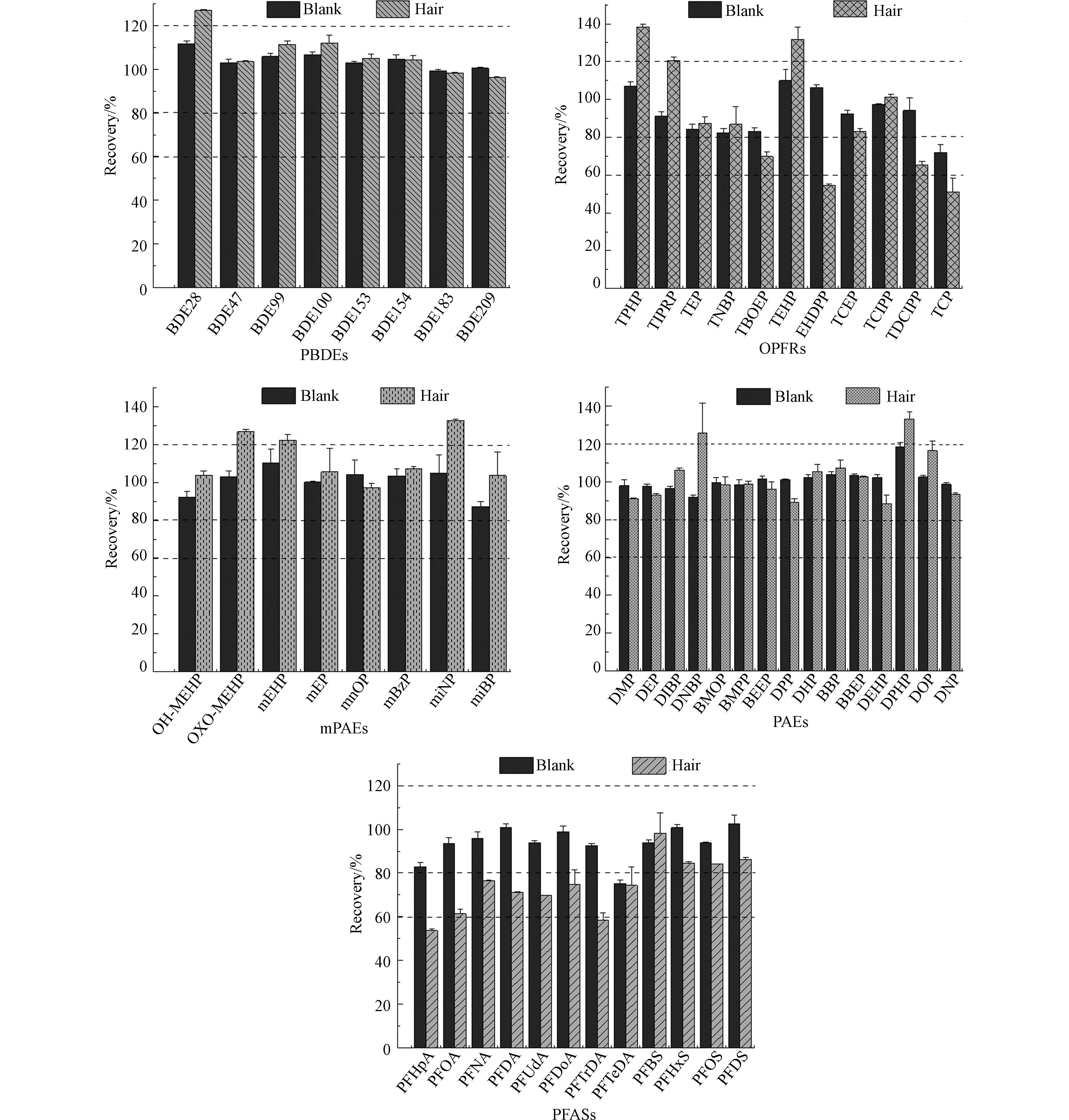
综合以上实验结果,考虑到mPAEs属于亲水性化合物,因此进一步采用EtAC+HEX+ACE+ ACN(方案4)作为提取剂,无水Na2SO4和C18作为净化剂对头发进行前处理,结果如图2所示. PBDEs、PFASs、OPFRs、PAEs和mPAEs基质加标回收率在53.6%—138%之间,RSD:0.01%—18.9%,化合物整体回收率较之前有大幅提升. 值得注意的是,PFASs和OPFRs中回收率一直低于40%的PFDA、EHDPP、TCP等化合物,经过方案4处理后效果得到明显改善,回收率和相对标准偏差分别为53.6%—138%和0.01%—16.0%.
-
本研究采用内标法定量,使用甲醇和异辛烷将“1.2”中标准品进行稀释,分别配制mPAEs、PFASs、OPFRs及PBDEs混合溶液,然后依次稀释成9个系列浓度(2.0、5.0、10.0、20.0、50.0、100.0、200.0、500.0、1000.0 ng·mL−1). 考虑到样品中较高的检出浓度,PAEs标曲浓度为5.0、10.0、20.0、50.0、100.0、200.0、500.0、1000.0、2000.0、3000.0、4000.0、5000.0 ng·mL−1. 所配标准曲线在仪器最佳条件下检测,以待测物与对应内标峰面积比值Y对其质量浓度比值X进行分析,各目标化合物在相应浓度范围有良好线性关系,相关系数(correlation coefficient, R)均大于0.995. 按照“1.5”中方法计算每种化合物的方法定量限和检出限. PBDEs、OPFRs、PAEs、mPAEs和PFASs的检出限在0.042—364.7 ng·g−1之间,详见表4.
-
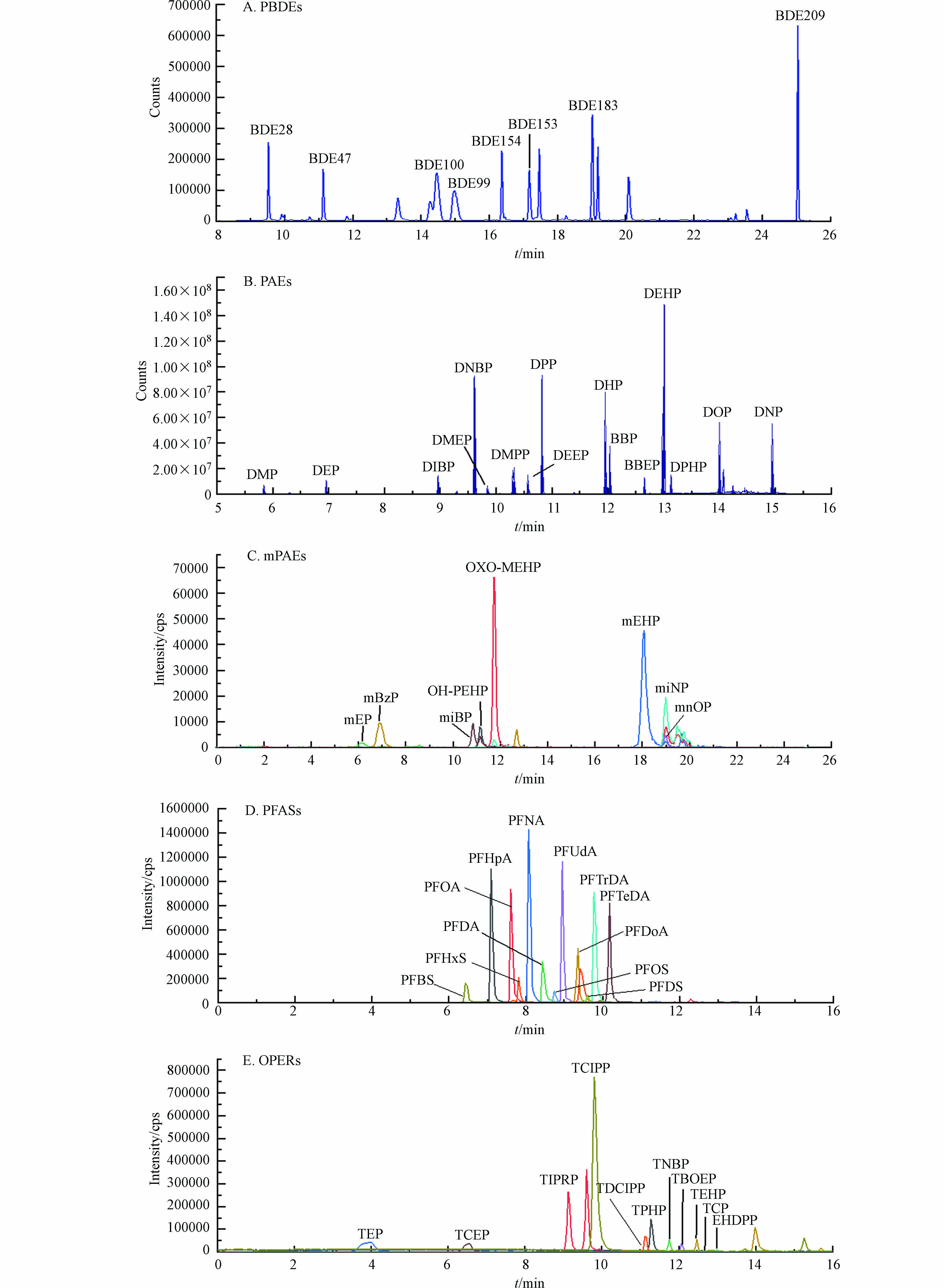
准确度采用目标化合物在头发样品中的加标回收率确定,精密度用平行样品之间的相对标准偏差(RSD)表示,使用同一标曲点每日重复测定3次且连续测定3 d获得的日内/间精密度评价方法的稳定性. 头发样品中5类化合物的基质加标回收率、相对标准差结果及样品基质加标色谱图如表5及图3所示. 经方案4处理后,5类化合物回收率及相对标准偏差均在可接受范围. 其中PBDEs回收率范围为:96. 4%—127%(RSD<4%);OPFRs:54. 7%—138%(RSD<7%);PFASs:53.6%—98.2%(RSD<10%);PAEs:88.3%—126%(RSD<16%);mPAEs:97.2%—133%(RSD<15%),所有化合物日内/间精密度均<20%,结果表明该前处理方法和操作过程适合用于头发中此5类污染物的分析.
-
将本研究建立的前处理方法用于检测广州市10例普通男性头发样品,结果显示5类EOCs在头发中均有检出(表6). PBDEs中主要检出污染物为BDE 209,检出率为100%,浓度在1.09 —36.6 ng·g−1 之间. OPFRs和PAEs检出污染物种类最多,其中TPHP、TEHP、EHDPP、TCEP、TCIPP、 DMP、DEP、DIBP、DNBP、DEHP在所有样品中均有检出,检出率为100%,含量介于2.69 —4951 ng·g−1之间. mEHP和miBP是mPAEs中最主要检出的两种化合物,检出率为100%,浓度分别为27.0—298 ng·g−1和15.0—38.6 ng·g−1. PFASs中主要检出的是PFOS和PFUdA,检出率分别为100%和90%,含量范围分别为1.40—17.9 ng·g−1和nd—0.58 ng·g−1. 头发主要检出污染物种类与之前报道相一致,其中 PBDEs和OPFRs检出浓度水平与广州居民头发的检出含量类似(2.61—56.86 ng·g−1、nd—287 ng·g−1)[47— 48];PAEs和mPAEs的浓度与重庆城市居民及希腊孕妇的报道相似(9.22—5890 ng·g−1、1.10—412.9 ng·g−1)[34, 49],而 PFASs检出浓度水平明显高于深圳居民(<0.03—1.60 ng·g−1)[24]. 值得注意的是,包括DMPP、DHP、TIPRP、PFBS和mnOP在内的24种目标物在所有样品中均未检出,表明这些污染物受试者日常生活中的暴露程度可能相对较低.
此外,为进一步验证研磨处理能否使头发中的污染物完全释放,本研究参考Tang[50]等的研究方法,将上述10例样品采用硝酸消解处理,液液提取后过弗罗里硅土小柱净化,上机后分析. 结果显示PFASs的回收率非常差,13C12-PFOA同位素内标回收率不足30%,而mPAEs同位素内标几乎全部损失. 同时发现PBDEs和OPFRs浓度与采用研磨处理后的水平相当(表6),进一步表明采用该方法对头发样品进行前处理能够准确反映人体中5类EOCs的暴露水平.
-
本文在现有研究基础上对头发样品前处理条件进行优化,建立了EtAC : HEX : ACE : ACN(1 : 1 : 1 : 1, V/V/V/V)混合溶液超声提取、C18和无水Na2SO4分散固相萃取填料净化分析头发中5类新型有机污染物的方法,结果显示15种PAEs、12种PFASs、11种OPFRs、8种mPAEs及8种PBDEs共54种EOCs的回收率在53.6%—138%之间. 采用该方法对广州10例普通男性头发样本进行分析,结果显示5类污染物在头发中均有检出,其中PFOS、DMP、DEP、DINP、DNBP、DEHP、miBP、mEHP、TPHP、TEHP、EHDPP、TCEP、TCIPP及BDE 209是最主要的污染物,检出率为100%,浓度范围在1.09— 4951 ng·g−1之间. 另外还将此结果与头发硝酸消解处理后的浓度水平进行了对比,表明该前处理方法可用于分析头发中的PBDEs、OPFRs、PFASs、PAEs和mPAEs类污染物. 本文建立的前处理方法仅需0.1 g样品和少量有机溶剂即可获得良好回收率和精密度,灵敏度高且简单快速,能同时有效检测头发中多种痕量新型有机污染物,可为人体多种有机污染物长期暴露研究提供技术参考.
头发中多种新型有机污染物检测方法的建立
The establishment of a new method for the detection of emerging organic contaminants in hair
-
摘要: 本研究基于超声提取-分散固相萃取技术,建立了同时分析头发中多溴联苯醚(PBDEs)、有机磷系阻燃剂(OPFRs)、全氟及多氟烷基化合物(PFASs)、邻苯二甲酸酯(PAEs)及其代谢物(mPAEs)等5类有机污染物的前处理方法. 头发样品(0.1 g)研磨成粉/絮状后经4 mL正己烷 : 丙酮 : 乙酸乙酯 : 乙腈(1 : 1 : 1 : 1,V/V/V/V)混合溶液提取3次,加入20 mg无水硫酸钠(Na2SO4)和100 mg十八烷基硅烷键合硅胶(C18)净化除杂,氮吹浓缩后分别采用GC-MS、GC-MS/MS和LC-MS/MS进行分析. 实验采用内标法定量,所有目标化合物在其相应的质量浓度范围内线性关系良好,相关性系数大于0.995;5类化合物检出限介于0.042—364.7 ng·g−1,加标回收率在53.6%—138%之间,相对标准差及日内/间精密度均小于20%. 采用该方法对广州市10例男性头发进行了检测,所有样品均检出全氟辛烷磺酸(PFOS)、邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二异丁酯(DIBP)、邻苯二甲酸二丁酯(DNBP)、邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸单异丁酯(miBP)、邻苯二甲酸单(2-乙基己基)酯(mEHP)、磷酸三苯酯(TPHP)、磷酸三(2-乙基己基)酯(TEHP)、2-乙基己基二苯基磷酸酯(EHDPP)、磷酸三(2-氯乙基)酯(TCEP)、磷酸三(2-氯丙基)酯(TCIPP)及十溴联苯醚(BDE 209),检出浓度介于1.09 —4951 ng·g−1之间. 该方法简单安全,有较高灵敏度和精确度,仅用少量样品和有机溶剂即可同步分析头发多种痕量新型有机污染物,可为人体多种有机污染物长期暴露研究提供技术参考.Abstract: In this study, a pretreatment method was established for the simultaneous analysis of polybrominated diphenyl ethers (PBDEs), organophosphorus flame retardants (OPFRs), perfluorinated and polyfluorinated alkyl compounds (PFASs), phthalate esters (PAEs) and their metabolites (mPAEs) in human hair based on ultrasonic extraction-dispersed solid phase extraction. Hair sample (0.1 g) was ground into powder/flocculent and then extracted with 4 mL hexane: acetone: ethyl acetate: acetonitrile (1:1:1:1, V/V/V/V) for three times, and 20 mg anhydrous sodium sulfate (Na2SO4) and 100 mg octadecyl bonded silica (C18) were added to purify and remove impurities. The extract was concentrated and reconstituted, and the target chemicals were analyzed by using GC-MS, GC-MS/MS and LC-MS/MS, respectively. The linearity of individual target chemicals was good in the corresponding concentration range, with correlation coefficient higher than 0.995. The detection limits of the target chemicals were 0.042—364.7 ng·g−1, the recoveries were 53.6%—138%, and the relative standard deviation and the intraday and interday precision were less than 20%. The developed method was applied to analyze target chemicals in 10 male hair samples. Perfluorooctane sulfonic acid (PFOS), dimethyl phthalate (DMP), diethyl phthalate (DEP), di-iso-butyl phthalate (DIBP), di-N-butyl phthalate (DNBP), dis(2-ethyl)hexyl phthalate (DEHP), mono-isobutyl phthalate (miBP), mono-(2-ethylhexyl) phthalate (mEHP), triphenyl phosphate (TPHP), tri2-ethylhexyl phosphate (TEHP), 2-ethylhexyl diphenyl phosphate (EHDPP), tri (2-chloroethyl) phosphate (TCEP), tri (2-chloropropyl) phosphate (TCIPP) and decabromodiphenyl ether (BDE 209) were detected in all samples, with concentrations as 1.09—4951 ng·g−1. Only a small amount of hair sample and low volume of organic solvents were needed to simultaneously analyze a variety of trace emerging organic contaminants in hair, which can provide technical support for the study of long-term exposure to a variety of organic pollutants in human body.
-
新型有机污染物(emerging organic contaminants, EOCs)指环境中新出现或最近引起关注,可能对生态系统和人体健康产生风险,管理措施不足或尚未纳入管理的有机污染物[1-4]. 主要包括药品和个人护理品(pharmaceuticals and personal care products, PPCP)、阻燃剂(flame retardant)、塑化剂(plasticizers)、杀虫剂,激素、表面活性剂等[3,5]. 这些EOCs在日常生活和工业生产中被频繁使用并广泛存在,如多溴联苯醚(polybrominated diphenyl ethers, PBDEs)是一种典型的溴代阻燃剂,具有阻燃效果好、生产成本低等特点,曾是应用最广泛的阻燃剂[6]. 近些年研究发现其具有环境持久性、生物累积性和生物毒性,目前已在全球范围内被禁用,并逐渐被有机磷酸酯阻燃剂(organophosphate flame retardants, OPFRs)取代[6—7]. 邻苯二甲酸酯(phthalic acid esters, PAEs)具有可塑性、耐久性,能够提高材料强度和透明度等优点[7—8],是一种常用的塑料添加剂,进入人体后经代谢转化可形成单酯或单酯的氧化产物即邻苯二甲酸酯代谢物(phthalate metabolites,mPAEs). 全氟及多氟烷基化合物(per-fluorinatedand polyfluoroalkyl compounds,PFASs)具有化学及热稳定性[9]、高表面活性及疏水疏油性[10]等特点,结构中含有极其稳定的C—F键,不易发生热解、光解、水解和生物降解,具有较强的生物蓄积性[11]. 上述化合物常以非化学键或直接添加的形式在塑料、建材、食品包装材料、电子设备、玩具、化妆品、农药、纸张、地毯、纺织品、家具等产品中被广泛使用[9,12—15],因而容易在产品生产、使用及回收处理过程经磨损、挥发等途径释放到环境中[16]. 目前已在土壤[17]、水体[18]、室内灰尘[19]等环境介质以及鱼[20]、蛋[21]等日常食品中被广泛检出,并可通过食物摄入、呼吸吸入和皮肤接触等途径进入人体,如血液、尿液、母乳、指甲等人体样品中已有关于PBDEs、PFASs、OPFRs、PAEs以及mPAEs检出的报道[22—26]. 同时研究发现这些EOCs能够导致人体内分泌紊乱,具有神经毒性、生殖毒性、内分泌毒性和致癌性等[27—28].
相较于血液、尿液、母乳等传统生物基质,头发具有采集方便、易储存、非侵入性采样、易被采集对象接纳等优点,常做为生物监测材料用于法医、毒品、重金属及有机污染物等研究,反映人体长期暴露情况. 尽管目前已有多篇文献报道了关于头发中EOCs检测方法[11, 29—31],但能够同时分析头发中多种EOCs的研究较为缺乏. 现有文献多采用硝酸消解的方法检测头发中的PBDEs、OPFRs和PAEs等污染物[6, 32—34],PFASs则多使用碱消解[35]. 两种消解方式存在费时、耗费溶剂、缺乏安全性等缺点. 此外有研究显示,酸/碱消解破坏头发结构的同时释放的一些内源性物质可能会影响头发中目标污染物如PFASs[11]的检测,具有一定局限性;相比之下,头发研磨后经有机溶剂萃取,能够更准确的反映头发中PFASs的污染水平[11, 36-37],然而该方法是否同样适用于其他种类的EOCs目前还缺少相关的文献报道.
因此,本研究在以往研究的基础上,通过优化有机萃取溶剂和分散固相萃取剂种类,建立了仅用少量头发样品(0.1 g)和有机溶剂即可同时检测头发中15种PAEs、12种PFASs、11种OPFRs、8种mPAEs及8种PBDEs共5大类54种EOCs的前处理方法,该方法节约溶剂且更为安全快速,同时采用本研究建立的前处理方法,分析了广州市10例普通男性头发中5类有机污染物的浓度水平.
1. 材料与方法(Materials and methods)
1.1 材料、试剂与仪器
材料与试剂:离心管(目盛付,日本),色谱级乙酸铵(CH3COONH4)、甲酸(HCOOH)、乙腈(ACN)、乙酸乙酯(EtAC)、甲基叔丁基醚(MTBE)、异辛烷(ISO)、正己烷(HEX)、二氯甲烷(DCM)和丙酮(ACE),无水硫酸镁(MgSO4)、无水硫酸钠(Na2SO4)、N-丙基乙二胺(PSA)、十八烷基硅烷键合硅胶(C18)和石墨化炭黑(GCB)(上海安谱实验科技股份有限公司,中国),甲醇(MEOH)(默克,德国).
仪器:AB SCIEX API 4000三重四极杆质谱仪(AB SCIEX, 美国);Agilent 7890B气相色谱仪、Agilent 1260液相色谱仪、Agilent 5977A质谱仪、Agilent 5975C质谱仪、DB-5HT毛细管柱(15 m×0.25 mm i.d., 0.10 μm)、DB-5MS毛细管柱(30 m×0.25 mm i.d., 0.25 μm)、Poroshell 120EC-C18(2.1 mm×100 mm, 2.7 μm)(安捷伦,美国);Kinetex EVO-C18100 A色谱柱(2.1 mm×100 mm, 5 μm),Kinetex×2.6 μm Bipheny l00 A(2.1 mm×100 mm)(Phenomenex,美国). 分析天平(上海安亭电子仪器厂,中国),氮吹仪(柏林河西路,美国),Milli-Q超纯水系统(默克,德国),涡旋振荡器(特朗纳,美国),冷冻干燥机(SP Scientific,美国),Eppendorf 5810低速冷冻离心机(Eppendorf,比利时). KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司,中国),行星式球磨仪(弗卡斯实验仪器有限公司,中国).
1.2 标准品
PBDEs、PAEs、mPAEs化合物标准品(AccuStandard,美国),PFASs化合物标准品(wellington,加拿大),OPFRs化合物标准品(CIL(Cambridge Isotope Laboratorie),美国)及对应内标标准品信息见表1.
表 1 目标化合物及内标标准品信息Table 1. The information of target chemicals and internal standards目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards PAEs PFASs OPFRs mPAEs PBDEs 邻苯二甲酸二甲酯(DMP) d4-邻苯二甲酸二丁酯(d4-DNBP) 全氟庚酸(PFHpA) 13C12-全氟辛酸(MPFOA) 磷酸三苯酯(TPHP) d15-磷酸三苯酯(d15-TPHP) 邻苯二甲酸单(2-乙基-5-羟基己基)酯(5OH-MEHP) 13C4-邻苯二甲酸单2-乙基-5-羟基己基酯(13C4-5OH-mEHP) 2,4,4-三溴联苯醚(BDE28) 2,3',4,4',5-五溴联苯醚(BDE118) 邻苯二甲酸二乙酯(DEP) 全氟辛酸(PFOA) 磷酸三异丙酯(TIPRP) d18-三(2-氯丙基)磷酸酯(d18-TCIPP) 邻苯二甲酸单(2-乙氧-5-氧己基)酯(5Oxo-MEHP) 邻苯二甲酸单(2-乙氧-5-氧己基)酯-13C4,(5Oxo-MEHP-13C4) 2,2',4,4'-四溴联苯醚(BDE47) 邻苯二甲酸二异丁酯(DIBP) 全氟壬酸(PFNA) 磷酸三乙酯(TEP) d12-三(2-氯乙基)磷酸酯(d12-TCEP) 邻苯二甲酸单(2-乙基己基)酯(mEHP) 邻苯二甲酸单(2-乙基己基)酯-13C4(mEHP-13C4) 2,2',4,4',5-五溴联苯醚(BDE99) 邻苯二甲酸二丁酯(DNBP) 全氟癸酸(PFDA) 磷酸三丁酯(TNBP) d15-磷酸三苯酯(d15-TPHP) 邻苯二甲酸单乙酯(mEP) 13C4-邻苯二甲酸单乙酯(13C4-mEP) 2,2',4,4',6-五溴联苯醚(BDE100) 邻苯二甲酸二甲氧乙酯(DMEP) 全氟十一烷酸(PFUdA) 13C12-全氟辛烷磺酸(MPFOS) 磷酸三(2-丁氧乙基)酯(TBOEP) 邻苯二甲酸单辛基乙酯(mnOP) d4-邻苯二甲酸单辛酯(d4-mnOP) 2,2',4,4',5,5'-六溴联苯醚(BDE153) 2,2',3,3',4,4'-六溴联苯醚(BDE128) 邻苯二甲酸二-4-甲基-2-戊基酯(DMPP) 全氟十二烷酸(PFDoA) 磷酸三2-乙基己基酯(TEHP) 邻苯二甲酸单苄基酯(mBzP) 13C4-邻苯二甲酸单苄基酯(13C4-mBzP) 2,2',4,4',5,6'-六溴联苯醚(BDE154) 邻苯二甲酸双-2-乙氧基乙酯(DEEP) 全氟十三烷酸(PFTrDA) 13C12-全氟辛酸(MPFOA) 2-乙基己基二苯基磷酸酯(EHDPP) 邻苯二甲酸单异壬酯(minP) d4-邻苯二甲酸单辛酯(d4-mnOP) 2,2',3,4,4',5',6-七溴联苯醚(BDE183) 邻苯二甲酸二戊酯(DPP) 全氟十四烷酸(PFTeDA) 磷酸三(2-氯乙基)酯(TCEP) d12-三(2-氯乙基)磷酸酯(d12-TCEP) 邻苯二甲酸单异丁酯(miBP) 13C4-邻苯二甲酸单正丁酯(13C4-mnBP) 十溴联苯醚(BDE209) 13C12-十溴联苯醚(13C12-BDE209) 邻苯二甲酸二己酯(DHP) 全氟丁烷磺酸盐(PFBS) 13C12-全氟辛烷磺酸(MPFOS) 磷酸三(2-氯丙基)酯(TCIPP) d18-三(2-氯丙基)磷酸酯(d18-TCIPP) 邻苯二甲酸丁苄酯(BBP) 全氟己烷磺酸盐(PFHxS) 三(1,3-二氯-2-丙基)磷酸酯(TDCIPP) d15-三(1,3-二氯-2-丙基)磷酸酯(d15-TDCIPP) 邻苯二甲酸二(2-丁氧基)乙酯(BBEP) 全氟辛烷磺酸(PFOS) 磷酸三甲苯酯(TCP) 邻苯二甲酸二(2-乙基)己酯(DEHP) 全氟癸烷磺酸盐(PFDS) 邻苯二甲酸二苯酯(DPHP) 邻苯二甲酸二正辛酯(DOP) 邻苯二甲酸二壬酯(DNP) 1.3 样本采集与前处理
以广州市年龄在18—40岁,且近期无烫染发行为的男性作为研究对象,志愿者在了解本次研究目的并签署知情同意书后,贴近头皮采集全部头发样品,铝箔纸包裹编号后放入密实袋,干燥阴凉处保存,每份样品大于5 g. 采集后的头发置于锥形瓶, Milli-Q水振荡清洗两遍,去除头发表面附着的灰尘等外部污染物,进行冷冻干燥. 实验前用HEX洗过的不锈钢剪刀将其剪短至0.5—1 cm. 采用行星式球磨仪将头发样品充分研磨成粉/絮状. 取0.1 g研磨头发于离心管加入1mL EtAC及20 μL各类目标物的同位素内标(OPFRs、PFASs、mPAEs的内标及13C12-BDE 209的质量浓度为100 ng·mL−1,BDE 118、BDE 128的质量浓度为200 ng·mL−1,PAEs 内标的质量浓度为500 ng·mL−1),通风橱静置过夜使溶剂挥发. 然后加入HEX、ACE、ACN及EtAC(1:1:1:1, V/V/V/V)的混合溶液4 mL,2000 r·min−1涡旋4 min, 20 ℃ 超声20 min,4000 r·min−1离心15 min取上清,重复3次. 上清液氮吹浓缩至1 mL后加入 20 mg 无水Na2SO4和100 mg C18进行净化. 1200 r·min−1涡旋7 min、3500 r·min−1离心15 min,转移上清液至干净的玻璃管中,氮吹近干后200 μL MEOH复溶,-20 ℃下静置4—6 h冷冻沉淀除杂,上清液待GC-MS、GC-MS/MS和LC-MS/MS检测分析.
1.4 仪器分析
PBDEs和PAEs分别采用气相色谱-质谱联用仪(GC-MS)和三重四极杆气相色谱质谱联用仪(GC-MS/MS)进行分析. PBDEs:负化学离子源(NCI),DB-5HT色谱柱(15 m×0.25 mm i.d., 0.10 μm)分离. 起始温度110 °C,保留5 min,20 °C·min−1升至200 °C,保持4.5 min,10 °C·min−1升至310 °C,保持15 min. PAEs:DB-5MS毛细管柱(30 m × 0.25 mm i.d., 0.25 μm),进样口温度290℃,传输线温度150 ℃;载气为氦气,流速1 mL·min−1;起始温度90 ℃,15 °C·min−1的速率升至310 ℃,保持5 min. 溶剂延迟5 min,EI源,电子轰击能量70 eV,多重反应监测模式(MRM);离子源温度230 ℃,四极杆温度150 ℃. 不分流进样且进样量均为1 μL.
OPFRs、PFASs、mPAEs使用Agilent 1260液相色谱仪、AB SCIEX API 4000+ MS/MS三重四极杆串联质谱仪分析(LC-MS/MS),色谱柱分别为:Kinetex 2.6 μm Biphenyl 100 A(2.1 mm×100 mm)、Poroshell 120 EC-C18(4.6 mm× 100 mm, 2.7 μm)、Kinetex EVO-C18 100 A(2.1 mm × 100 mm,5 μm),均采用电喷雾电离源(ESI)及多反应监测模式(MRM),进样量5 μL,其余仪器分析条件见表2.
表 2 OPFRs、PFASs及mPAEs的液相色谱和质谱参数Table 2. Liquid chromatography and mass spectrometry parameters of OPFRs, PFASs and mPAEs分析条件Analytical Conditions OPFRs PFASs mPAEs 色谱条件(流动相、洗脱梯度) Chromatographic conditions(Mobile phase, elution gradient) A:甲醇,B:0.01 mol·L−1乙酸铵溶液;0—0.1 min:65% B0.1—9 min:65%—5% B9—13 min:5%—0% B13—14 min:0% B14—15.1 min:0%—65% B15.1—20 min:65% B柱温40 ℃,流速250 μL·min−1 A:乙腈,B:0.01 mol·L−1乙酸铵溶液;0—1 min:20% A1—8 min:20%—100% A8—12.5 min:100% A12.5—13 min:100%—20% A13—18 min:20% A柱温50 ℃,流速300 μL·min−1 A:乙腈,B:0.1%甲酸水溶液,0—12 min:15%—45% A12—15 min:45% A15—19 min:45%—98% A19-21 min:98% A21—21.1 min:98%—15% A21.1-25 min:15% A柱温40 ℃,流速300 μL·min−1 质谱条件Mass spectrometry conditions 正离子扫描方式;毛细管电压:4000 V;气体(N2)温度:550 ℃ 负离子扫描方式,离子喷雾电压为-4500 V,离子源温度为450℃ 负离子扫描方式,离子喷雾电压4000 V,气体(N2)温度350℃ 1.5 质量保证与质量控制(QAQC)
所有玻璃器材使用前均采用碱液(pH>11)浸泡4 h以上,经自来水及超纯水冲洗并用烘箱烘干,再在400 ℃的马弗炉中焙烧4 h,使用前经DCM和HEX淋洗吹干. 方法定量限(limit of quantification,LOQ)和方法检出限(limit of detection,LOD)为空白样品中目标化合物浓度的均值加10倍或者3倍标准差,空白未检出时定义为10倍或者3倍信噪比. 实验采用内标法定量,设置空白、基质、空白加标和基质加标等4组实验且每组3个重复,用空白加标和基质加标浓度减去空白和基质的平均浓度计算回收率和相对标准差.
2. 结果与讨论(Results and discussion)
2.1 前处理条件优化
2.1.1 分散固相萃取剂的选择
现有研究中,EtAC、HEX、ACE、MTBE常用作OPFRs、PAEs、PAFSs和PBDEs的提取剂或洗脱剂[38—42] ,本研究在以往研究基础上首先采用ACE、HEX和MTBE对头发中污染物进行提取[16]. 分散固相萃取剂参考Zafeiraki [21]和熊仕茂[43]对OPFRs和PFASs的净化条件,具体如表3中方案1所示. 另有文献指出,研磨处理可提高头发样品中污染物的提取效率[11,37,44],故本研究在进行EOCs提取前将所有头发充分研磨成粉/絮状.
表 3 有机提取溶剂和分散固相萃取填料的4种前处理方案Table 3. Four pretreatment schemes of organic extraction solvent and dispersed solid phase extraction filler方案Scheme 有机提取溶剂Organic extraction solvent 分散固相萃取剂Disperse solid phase extractant 1 ACE,HEX,MTBE 无水MgSO4,PSA,C18 2 ACE,HEX,MTBE 无水Na2SO4,C18 3 EtAC,HEX,MTBE 4 EtAC,HEX,ACN,ACE 头发样品经方案1处理后,PBDEs、OPFRs和PAEs三类污染物均有较好效果,回收率和相对标准偏差分别介于40%—129%和0.1%—21.4%之间. 而PFASs中仅PFHxS、PFOS和PFDS的回收率在60%以上,其余几种化合物空白和基质加标的回收率小于7%,损失较为严重. 为进一步探究分散固相萃取填料对PFASs的影响,溶剂加标后分别采用MgSO4、PSA、C18和GCB净化,结果如图1所示. PFASs的回收率整体呈现C18>GCB>PSA>MgSO4的趋势. 其中经MgSO4处理后,8种全氟烷酸的回收率均低于50%,推测MgSO4可能对PFASs类污染物具有较强的吸附效应,因此回收率相对差. MgSO4作为干燥剂可吸收溶液中的微量水分[38, 45],考虑到可能存在的吸附作用,后续实验改用无水Na2SO4. C18一般用于去除脂肪等非极性杂质[38],研究结果显示其对大多数化合物的影响最小[46],因此实验选用无水Na2SO4和C18作为净化填料.
2.1.2 有机萃取溶剂的优化
确定净化填料后,进一步对有机萃取溶剂展开优化. Alves等[22]分别比较了乙酸乙酯、异丙醇、四氢呋喃/异丙醇的(50:50, V/V)对PFASs的提取效果,发现乙酸乙酯效果最好(回收率69.0%—141%之间). 此外乙酸乙酯常作为OPFRs优良的提取剂或洗脱剂,能够获得较好的回收效果[41],故本研究分别对比了ACE+HEX+MTBE(方案2)和EtAC+HEX+MTBE(方案3)对5类污染物的提取效率. 结果显示,经方案2处理后,EHDPP、PFHpA和PFOA的回收率较差,回收率在29.6%—42.8%之间;而方案3处理后EHDPP、PFBS的回收率在21.4%—48.2%之间,两种方案均存在一定的缺陷.
综合以上实验结果,考虑到mPAEs属于亲水性化合物,因此进一步采用EtAC+HEX+ACE+ ACN(方案4)作为提取剂,无水Na2SO4和C18作为净化剂对头发进行前处理,结果如图2所示. PBDEs、PFASs、OPFRs、PAEs和mPAEs基质加标回收率在53.6%—138%之间,RSD:0.01%—18.9%,化合物整体回收率较之前有大幅提升. 值得注意的是,PFASs和OPFRs中回收率一直低于40%的PFDA、EHDPP、TCP等化合物,经过方案4处理后效果得到明显改善,回收率和相对标准偏差分别为53.6%—138%和0.01%—16.0%.
2.2 方法学验证
2.2.1 标准曲线和检出限
本研究采用内标法定量,使用甲醇和异辛烷将“1.2”中标准品进行稀释,分别配制mPAEs、PFASs、OPFRs及PBDEs混合溶液,然后依次稀释成9个系列浓度(2.0、5.0、10.0、20.0、50.0、100.0、200.0、500.0、1000.0 ng·mL−1). 考虑到样品中较高的检出浓度,PAEs标曲浓度为5.0、10.0、20.0、50.0、100.0、200.0、500.0、1000.0、2000.0、3000.0、4000.0、5000.0 ng·mL−1. 所配标准曲线在仪器最佳条件下检测,以待测物与对应内标峰面积比值Y对其质量浓度比值X进行分析,各目标化合物在相应浓度范围有良好线性关系,相关系数(correlation coefficient, R)均大于0.995. 按照“1.5”中方法计算每种化合物的方法定量限和检出限. PBDEs、OPFRs、PAEs、mPAEs和PFASs的检出限在0.042—364.7 ng·g−1之间,详见表4.
表 4 目标化合物相关系数(R)、定量限(LOQ)及检出限(LOD)(ng·g−1)Table 4. Correlation coefficient (R), Limit of Quantification (LOQ) and Limit of Detection (LOD) of target chemicals目标物Target chemicals 相关系数(R) 定量限(LOQ) 检出限(LOD) 目标物Target chemicals 相关系数(R) 定量限(LOQ) 检出限(LOD) PAEs PFASs DMP 0.999 20.98 6.294 PFHpA 0.997 2.429 0.729 DEP 0.999 32.35 9.705 PFOA 0.998 1.788 0.537 DIBP 0.995 1215 364.7 PFNA 0.997 1.208 0.362 DNBP 0.998 856.0 256.8 PFDA 0.997 0.816 0.245 DMEP 0.998 15.11 4.533 PFUdA 0.996 0.668 0.200 DMPP 0.999 1.996 0.599 PFDoA 0.999 0.344 0.103 DEEP 0.997 17.29 5.186 PFTrDA 0.997 1.098 0.329 DPP 0.997 0.581 0.174 PFTeDA 0.997 1.457 0.437 DHP 0.999 0.297 0.089 PFBS 0.999 0.152 0.045 BBP 0.999 0.690 0.207 PFHxS 0.998 0.140 0.042 BBEP 0.999 1.129 0.339 PFOS 0.999 0.377 0.113 DEHP 0.997 1074 322.2 PFDS 0.997 0.457 0.137 DPHP 0.999 0.159 0.048 DOP 0.999 0.629 0.189 DNP 0.996 12.89 3.866 OPFRs mPAEs TPHP 0.995 1.044 0.313 5OH-MEHP 0.998 3.249 0.975 TIPRP 0.998 0.187 0.056 5Oxo-MEHP 0.998 0.146 0.044 TEP 0.999 0.574 0.172 mEHP 0.998 48.16 14.45 TNBP 0.995 17.12 5.135 mEP 0.999 2.874 0.862 TBOEP 0.997 1.280 0.384 mnOP 0.998 0.574 0.172 TEHP 0.999 4.726 1.575 mBzP 0.998 0.315 0.095 EHDPP 0.996 3.822 1.147 miNP 0.998 0.465 0.139 TCEP 0.999 12.44 3.731 miBP 0.997 21.79 6.538 TCIPP 0.998 6.327 1.898 TDCIPP 0.999 32.51 9.752 TCP 0.998 22.59 6.776 PBDEs PBDEs BDE 28 0.997 1.546 0.464 BDE 153 0.999 0.513 0.154 BDE 47 0.996 7.813 2.344 BDE 154 0.999 4.673 1.402 BDE 99 0.999 2.179 0.654 BDE 183 0.999 3.419 1.026 BDE 100 0.999 1.783 0.535 BDE 209 0.999 1.506 0.452 2.2.2 准确度和精密度
准确度采用目标化合物在头发样品中的加标回收率确定,精密度用平行样品之间的相对标准偏差(RSD)表示,使用同一标曲点每日重复测定3次且连续测定3 d获得的日内/间精密度评价方法的稳定性. 头发样品中5类化合物的基质加标回收率、相对标准差结果及样品基质加标色谱图如表5及图3所示. 经方案4处理后,5类化合物回收率及相对标准偏差均在可接受范围. 其中PBDEs回收率范围为:96. 4%—127%(RSD<4%);OPFRs:54. 7%—138%(RSD<7%);PFASs:53.6%—98.2%(RSD<10%);PAEs:88.3%—126%(RSD<16%);mPAEs:97.2%—133%(RSD<15%),所有化合物日内/间精密度均<20%,结果表明该前处理方法和操作过程适合用于头发中此5类污染物的分析.
表 5 目标化合物的基质加标回收率±相对标准差及精密度(%)Table 5. Matrix spiked recoveries, relative standard deviations and precisions of target chemicals目标物Target chemicals 回收率/%(Rec.±RSD)Recoveries 日内精密度/%Intraday precisions 日间精密度/%Interday precisions 目标物Target chemicals 回收率/%(Rec.±RSD)Recoveries 日内精密度/%Intraday precisions 日间精密度/%Interday precisions PAEs PFASs DMP 91.0±0.47 2.19 3.86 PFHpA 53.6±0.94 10.4 11.1 DEP 93.1±0.50 1.99 2.63 PFOA 61.4±2.19 9.75 11.5 DIBP 106±1.11 2.58 9.14 PFNA 76.6±0.08 4.90 5.51 DNBP 126±16.0 1.87 2.41 PFDA 71.1±0.30 3.55 11.7 DMEP 98.5±4.04 3.43 9.66 PFUdA 69.8±0.01 1.95 2.98 DMPP 98.9±1.45 2.11 15.5 PFDoA 74.7±6.78 1.47 3.09 DEEP 96.2±3.85 5.09 13.7 PFTrDA 58.6±3.37 2.02 3.01 DPP 89.1±1.99 4.12 13.3 PFTeDA 74.4±8.36 2.69 2.47 DHP 105±3.70 7.89 14.3 PFBS 98.2±9.26 2.93 3.58 BBP 107±4.10 5.72 13.9 PFHxS 84.7±0.51 4.38 4.23 BBEP 102±0.45 3.34 10.1 PFOS 84.1±0.12 3.11 2.86 DEHP 88.3±4.70 4.01 3.91 PFDS 86.3±1.00 3.96 3.75 DPHP 133±3.67 7.12 14.1 DOP 116±5.20 17.1 14.6 DNP 93.5±0.44 17.7 16.7 mPAEs OPFRs 5OH-MEHP 104±2.47 2.77 7.42 TPHP 138±1.71 3.53 6.07 5Oxo-MEHP 127±1.30 3.08 11.2 TIPRP 120±1.93 2.59 1.31 mEHP 122±3.21 4.84 7.23 TEP 87.4±3.52 5.88 3.16 mEP 106±12.4 8.24 9.32 TNBP 86.8±9.29 6.24 4.64 mnOP 97.2±2.20 5.07 8.89 TBOEP 69.8±2.41 3.42 4.23 mBzP 107±0.81 3.72 8.37 TEHP 132±6.31 3.25 5.90 miNP 133±0.72 2.44 2.00 EHDPP 54.7±0.42 5.40 10.4 miBP 104±12.6 6.22 6.88 TCEP 83.3±1.18 3.27 5.85 TCIPP 101±1.60 2.22 0.66 TDCIPP 65.2±2.04 1.53 1.20 TCP 67.7±8.31 2.16 0.64 PBDEs PBDEs BDE 28 127±0.47 2.07 5.76 BDE 153 105±1.85 5.91 10.2 BDE 47 104±0.45 0.66 5.66 BDE 154 104±1.97 4.28 9.02 BDE 99 111±1.68 0.89 4.94 BDE 183 98.4±0.38 5.41 8.02 BDE 100 112±3.82 4.58 6.26 BDE 209 96.4±0.36 0.18 0.12 2.3 头发样品分析及验证
将本研究建立的前处理方法用于检测广州市10例普通男性头发样品,结果显示5类EOCs在头发中均有检出(表6). PBDEs中主要检出污染物为BDE 209,检出率为100%,浓度在1.09 —36.6 ng·g−1 之间. OPFRs和PAEs检出污染物种类最多,其中TPHP、TEHP、EHDPP、TCEP、TCIPP、 DMP、DEP、DIBP、DNBP、DEHP在所有样品中均有检出,检出率为100%,含量介于2.69 —4951 ng·g−1之间. mEHP和miBP是mPAEs中最主要检出的两种化合物,检出率为100%,浓度分别为27.0—298 ng·g−1和15.0—38.6 ng·g−1. PFASs中主要检出的是PFOS和PFUdA,检出率分别为100%和90%,含量范围分别为1.40—17.9 ng·g−1和nd—0.58 ng·g−1. 头发主要检出污染物种类与之前报道相一致,其中 PBDEs和OPFRs检出浓度水平与广州居民头发的检出含量类似(2.61—56.86 ng·g−1、nd—287 ng·g−1)[47— 48];PAEs和mPAEs的浓度与重庆城市居民及希腊孕妇的报道相似(9.22—5890 ng·g−1、1.10—412.9 ng·g−1)[34, 49],而 PFASs检出浓度水平明显高于深圳居民(<0.03—1.60 ng·g−1)[24]. 值得注意的是,包括DMPP、DHP、TIPRP、PFBS和mnOP在内的24种目标物在所有样品中均未检出,表明这些污染物受试者日常生活中的暴露程度可能相对较低.
表 6 经研磨和消解处理后测得的头发样品中EOCs的检出率和浓度范围Table 6. Detection frequency and concentration range of EOCs detected by hair samples after grinding and digestion化合物Chemicals 研磨Grind 消解Digestion 检出率/%Detection frequency 浓度范围/(ng·g−1)Concentration range 检出率/%Detection frequency 浓度范围/(ng·g−1)Concentration range OPFRs TPHP 100 6.32—332 100 20.9—476 TIPRP 0 nd 0 nd TEP 0 nd 0 nd TNBP 30 nd—7.85 55 nd—7.37 TBOEP 60 nd—33.5 33 nd—2.54 TEHP 100 2.69—30.3 100 3.63—30.2 EHDPP 100 8.14—176 100 16.2—174 TCEP 100 6.38—36.6 100 4.04—44.7 TCIPP 100 14.9—132 100 1.38—48.0 TDCIPP 80 nd—390 66 nd—177 TCP 0 nd 0 nd PBDEs BDE 28 0 nd 0 nd BDE 47 0 nd 0 nd BDE 99 0 nd 0 nd BDE 100 0 nd 0 nd BDE 153 0 nd 0 nd BDE 154 0 nd 0 nd BDE 183 0 nd 0 nd BDE 209 100 1.09—36.6 100 0.57—41.4 PFASs PFHpA 30 nd—2.04 0 nd PFOA 70 nd—2.47 0 nd PFNA 60 nd—1.05 0 nd PFDA 30 nd—0.36 0 nd PFUdA 90 nd—0.58 0 nd PFDoA 70 nd—0.24 0 nd PFTrDA 10 nd—0.47 0 nd PFTeDA 30 nd—0.08 0 nd PFBS 0 nd 0 nd PFHxS 0 nd 0 nd PFOS 100 1.40—17.9 0 nd PFDS 0 nd 0 nd PAEs DMP 100 63.9—181 na na DEP 100 127—2593 na na DIBP 100 804—4823 na na DNBP 100 1074—4402 na na DMEP 0 nd na na DMPP 0 nd na na DEEP 0 nd na na DPP 20 nd—334 na na DHP 0 nd na na BBP 0 nd na na BBEP 0 nd na na DEHP 100 326—4951 na na DPHP 20 nd—1.50 na na DOP 0 nd na na DNP 0 nd na na mPAEs 5OH-MEHP 60 nd—4.53 0 nd 5Oxo-MEHP 0 nd 0 nd mEHP 100 27.0—298 0 nd mEP 30 nd—260 0 nd mnOP 0 nd 0 nd mBzP 0 nd 0 nd miNP 0 nd 0 nd miBP 100 15.0—38.6 0 nd 注:nd 未检出;na 未获得. Note: nd, not detected, na, not available. 此外,为进一步验证研磨处理能否使头发中的污染物完全释放,本研究参考Tang[50]等的研究方法,将上述10例样品采用硝酸消解处理,液液提取后过弗罗里硅土小柱净化,上机后分析. 结果显示PFASs的回收率非常差,13C12-PFOA同位素内标回收率不足30%,而mPAEs同位素内标几乎全部损失. 同时发现PBDEs和OPFRs浓度与采用研磨处理后的水平相当(表6),进一步表明采用该方法对头发样品进行前处理能够准确反映人体中5类EOCs的暴露水平.
3. 结论(Conclusion)
本文在现有研究基础上对头发样品前处理条件进行优化,建立了EtAC : HEX : ACE : ACN(1 : 1 : 1 : 1, V/V/V/V)混合溶液超声提取、C18和无水Na2SO4分散固相萃取填料净化分析头发中5类新型有机污染物的方法,结果显示15种PAEs、12种PFASs、11种OPFRs、8种mPAEs及8种PBDEs共54种EOCs的回收率在53.6%—138%之间. 采用该方法对广州10例普通男性头发样本进行分析,结果显示5类污染物在头发中均有检出,其中PFOS、DMP、DEP、DINP、DNBP、DEHP、miBP、mEHP、TPHP、TEHP、EHDPP、TCEP、TCIPP及BDE 209是最主要的污染物,检出率为100%,浓度范围在1.09— 4951 ng·g−1之间. 另外还将此结果与头发硝酸消解处理后的浓度水平进行了对比,表明该前处理方法可用于分析头发中的PBDEs、OPFRs、PFASs、PAEs和mPAEs类污染物. 本文建立的前处理方法仅需0.1 g样品和少量有机溶剂即可获得良好回收率和精密度,灵敏度高且简单快速,能同时有效检测头发中多种痕量新型有机污染物,可为人体多种有机污染物长期暴露研究提供技术参考.
-
表 1 目标化合物及内标标准品信息
Table 1. The information of target chemicals and internal standards
目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards 目标化合物Target chemicals 内标Internal standards PAEs PFASs OPFRs mPAEs PBDEs 邻苯二甲酸二甲酯(DMP) d4-邻苯二甲酸二丁酯(d4-DNBP) 全氟庚酸(PFHpA) 13C12-全氟辛酸(MPFOA) 磷酸三苯酯(TPHP) d15-磷酸三苯酯(d15-TPHP) 邻苯二甲酸单(2-乙基-5-羟基己基)酯(5OH-MEHP) 13C4-邻苯二甲酸单2-乙基-5-羟基己基酯(13C4-5OH-mEHP) 2,4,4-三溴联苯醚(BDE28) 2,3',4,4',5-五溴联苯醚(BDE118) 邻苯二甲酸二乙酯(DEP) 全氟辛酸(PFOA) 磷酸三异丙酯(TIPRP) d18-三(2-氯丙基)磷酸酯(d18-TCIPP) 邻苯二甲酸单(2-乙氧-5-氧己基)酯(5Oxo-MEHP) 邻苯二甲酸单(2-乙氧-5-氧己基)酯-13C4,(5Oxo-MEHP-13C4) 2,2',4,4'-四溴联苯醚(BDE47) 邻苯二甲酸二异丁酯(DIBP) 全氟壬酸(PFNA) 磷酸三乙酯(TEP) d12-三(2-氯乙基)磷酸酯(d12-TCEP) 邻苯二甲酸单(2-乙基己基)酯(mEHP) 邻苯二甲酸单(2-乙基己基)酯-13C4(mEHP-13C4) 2,2',4,4',5-五溴联苯醚(BDE99) 邻苯二甲酸二丁酯(DNBP) 全氟癸酸(PFDA) 磷酸三丁酯(TNBP) d15-磷酸三苯酯(d15-TPHP) 邻苯二甲酸单乙酯(mEP) 13C4-邻苯二甲酸单乙酯(13C4-mEP) 2,2',4,4',6-五溴联苯醚(BDE100) 邻苯二甲酸二甲氧乙酯(DMEP) 全氟十一烷酸(PFUdA) 13C12-全氟辛烷磺酸(MPFOS) 磷酸三(2-丁氧乙基)酯(TBOEP) 邻苯二甲酸单辛基乙酯(mnOP) d4-邻苯二甲酸单辛酯(d4-mnOP) 2,2',4,4',5,5'-六溴联苯醚(BDE153) 2,2',3,3',4,4'-六溴联苯醚(BDE128) 邻苯二甲酸二-4-甲基-2-戊基酯(DMPP) 全氟十二烷酸(PFDoA) 磷酸三2-乙基己基酯(TEHP) 邻苯二甲酸单苄基酯(mBzP) 13C4-邻苯二甲酸单苄基酯(13C4-mBzP) 2,2',4,4',5,6'-六溴联苯醚(BDE154) 邻苯二甲酸双-2-乙氧基乙酯(DEEP) 全氟十三烷酸(PFTrDA) 13C12-全氟辛酸(MPFOA) 2-乙基己基二苯基磷酸酯(EHDPP) 邻苯二甲酸单异壬酯(minP) d4-邻苯二甲酸单辛酯(d4-mnOP) 2,2',3,4,4',5',6-七溴联苯醚(BDE183) 邻苯二甲酸二戊酯(DPP) 全氟十四烷酸(PFTeDA) 磷酸三(2-氯乙基)酯(TCEP) d12-三(2-氯乙基)磷酸酯(d12-TCEP) 邻苯二甲酸单异丁酯(miBP) 13C4-邻苯二甲酸单正丁酯(13C4-mnBP) 十溴联苯醚(BDE209) 13C12-十溴联苯醚(13C12-BDE209) 邻苯二甲酸二己酯(DHP) 全氟丁烷磺酸盐(PFBS) 13C12-全氟辛烷磺酸(MPFOS) 磷酸三(2-氯丙基)酯(TCIPP) d18-三(2-氯丙基)磷酸酯(d18-TCIPP) 邻苯二甲酸丁苄酯(BBP) 全氟己烷磺酸盐(PFHxS) 三(1,3-二氯-2-丙基)磷酸酯(TDCIPP) d15-三(1,3-二氯-2-丙基)磷酸酯(d15-TDCIPP) 邻苯二甲酸二(2-丁氧基)乙酯(BBEP) 全氟辛烷磺酸(PFOS) 磷酸三甲苯酯(TCP) 邻苯二甲酸二(2-乙基)己酯(DEHP) 全氟癸烷磺酸盐(PFDS) 邻苯二甲酸二苯酯(DPHP) 邻苯二甲酸二正辛酯(DOP) 邻苯二甲酸二壬酯(DNP) 表 2 OPFRs、PFASs及mPAEs的液相色谱和质谱参数
Table 2. Liquid chromatography and mass spectrometry parameters of OPFRs, PFASs and mPAEs
分析条件Analytical Conditions OPFRs PFASs mPAEs 色谱条件(流动相、洗脱梯度) Chromatographic conditions(Mobile phase, elution gradient) A:甲醇,B:0.01 mol·L−1乙酸铵溶液;0—0.1 min:65% B0.1—9 min:65%—5% B9—13 min:5%—0% B13—14 min:0% B14—15.1 min:0%—65% B15.1—20 min:65% B柱温40 ℃,流速250 μL·min−1 A:乙腈,B:0.01 mol·L−1乙酸铵溶液;0—1 min:20% A1—8 min:20%—100% A8—12.5 min:100% A12.5—13 min:100%—20% A13—18 min:20% A柱温50 ℃,流速300 μL·min−1 A:乙腈,B:0.1%甲酸水溶液,0—12 min:15%—45% A12—15 min:45% A15—19 min:45%—98% A19-21 min:98% A21—21.1 min:98%—15% A21.1-25 min:15% A柱温40 ℃,流速300 μL·min−1 质谱条件Mass spectrometry conditions 正离子扫描方式;毛细管电压:4000 V;气体(N2)温度:550 ℃ 负离子扫描方式,离子喷雾电压为-4500 V,离子源温度为450℃ 负离子扫描方式,离子喷雾电压4000 V,气体(N2)温度350℃ 表 3 有机提取溶剂和分散固相萃取填料的4种前处理方案
Table 3. Four pretreatment schemes of organic extraction solvent and dispersed solid phase extraction filler
方案Scheme 有机提取溶剂Organic extraction solvent 分散固相萃取剂Disperse solid phase extractant 1 ACE,HEX,MTBE 无水MgSO4,PSA,C18 2 ACE,HEX,MTBE 无水Na2SO4,C18 3 EtAC,HEX,MTBE 4 EtAC,HEX,ACN,ACE 表 4 目标化合物相关系数(R)、定量限(LOQ)及检出限(LOD)(ng·g−1)
Table 4. Correlation coefficient (R), Limit of Quantification (LOQ) and Limit of Detection (LOD) of target chemicals
目标物Target chemicals 相关系数(R) 定量限(LOQ) 检出限(LOD) 目标物Target chemicals 相关系数(R) 定量限(LOQ) 检出限(LOD) PAEs PFASs DMP 0.999 20.98 6.294 PFHpA 0.997 2.429 0.729 DEP 0.999 32.35 9.705 PFOA 0.998 1.788 0.537 DIBP 0.995 1215 364.7 PFNA 0.997 1.208 0.362 DNBP 0.998 856.0 256.8 PFDA 0.997 0.816 0.245 DMEP 0.998 15.11 4.533 PFUdA 0.996 0.668 0.200 DMPP 0.999 1.996 0.599 PFDoA 0.999 0.344 0.103 DEEP 0.997 17.29 5.186 PFTrDA 0.997 1.098 0.329 DPP 0.997 0.581 0.174 PFTeDA 0.997 1.457 0.437 DHP 0.999 0.297 0.089 PFBS 0.999 0.152 0.045 BBP 0.999 0.690 0.207 PFHxS 0.998 0.140 0.042 BBEP 0.999 1.129 0.339 PFOS 0.999 0.377 0.113 DEHP 0.997 1074 322.2 PFDS 0.997 0.457 0.137 DPHP 0.999 0.159 0.048 DOP 0.999 0.629 0.189 DNP 0.996 12.89 3.866 OPFRs mPAEs TPHP 0.995 1.044 0.313 5OH-MEHP 0.998 3.249 0.975 TIPRP 0.998 0.187 0.056 5Oxo-MEHP 0.998 0.146 0.044 TEP 0.999 0.574 0.172 mEHP 0.998 48.16 14.45 TNBP 0.995 17.12 5.135 mEP 0.999 2.874 0.862 TBOEP 0.997 1.280 0.384 mnOP 0.998 0.574 0.172 TEHP 0.999 4.726 1.575 mBzP 0.998 0.315 0.095 EHDPP 0.996 3.822 1.147 miNP 0.998 0.465 0.139 TCEP 0.999 12.44 3.731 miBP 0.997 21.79 6.538 TCIPP 0.998 6.327 1.898 TDCIPP 0.999 32.51 9.752 TCP 0.998 22.59 6.776 PBDEs PBDEs BDE 28 0.997 1.546 0.464 BDE 153 0.999 0.513 0.154 BDE 47 0.996 7.813 2.344 BDE 154 0.999 4.673 1.402 BDE 99 0.999 2.179 0.654 BDE 183 0.999 3.419 1.026 BDE 100 0.999 1.783 0.535 BDE 209 0.999 1.506 0.452 表 5 目标化合物的基质加标回收率±相对标准差及精密度(%)
Table 5. Matrix spiked recoveries, relative standard deviations and precisions of target chemicals
目标物Target chemicals 回收率/%(Rec.±RSD)Recoveries 日内精密度/%Intraday precisions 日间精密度/%Interday precisions 目标物Target chemicals 回收率/%(Rec.±RSD)Recoveries 日内精密度/%Intraday precisions 日间精密度/%Interday precisions PAEs PFASs DMP 91.0±0.47 2.19 3.86 PFHpA 53.6±0.94 10.4 11.1 DEP 93.1±0.50 1.99 2.63 PFOA 61.4±2.19 9.75 11.5 DIBP 106±1.11 2.58 9.14 PFNA 76.6±0.08 4.90 5.51 DNBP 126±16.0 1.87 2.41 PFDA 71.1±0.30 3.55 11.7 DMEP 98.5±4.04 3.43 9.66 PFUdA 69.8±0.01 1.95 2.98 DMPP 98.9±1.45 2.11 15.5 PFDoA 74.7±6.78 1.47 3.09 DEEP 96.2±3.85 5.09 13.7 PFTrDA 58.6±3.37 2.02 3.01 DPP 89.1±1.99 4.12 13.3 PFTeDA 74.4±8.36 2.69 2.47 DHP 105±3.70 7.89 14.3 PFBS 98.2±9.26 2.93 3.58 BBP 107±4.10 5.72 13.9 PFHxS 84.7±0.51 4.38 4.23 BBEP 102±0.45 3.34 10.1 PFOS 84.1±0.12 3.11 2.86 DEHP 88.3±4.70 4.01 3.91 PFDS 86.3±1.00 3.96 3.75 DPHP 133±3.67 7.12 14.1 DOP 116±5.20 17.1 14.6 DNP 93.5±0.44 17.7 16.7 mPAEs OPFRs 5OH-MEHP 104±2.47 2.77 7.42 TPHP 138±1.71 3.53 6.07 5Oxo-MEHP 127±1.30 3.08 11.2 TIPRP 120±1.93 2.59 1.31 mEHP 122±3.21 4.84 7.23 TEP 87.4±3.52 5.88 3.16 mEP 106±12.4 8.24 9.32 TNBP 86.8±9.29 6.24 4.64 mnOP 97.2±2.20 5.07 8.89 TBOEP 69.8±2.41 3.42 4.23 mBzP 107±0.81 3.72 8.37 TEHP 132±6.31 3.25 5.90 miNP 133±0.72 2.44 2.00 EHDPP 54.7±0.42 5.40 10.4 miBP 104±12.6 6.22 6.88 TCEP 83.3±1.18 3.27 5.85 TCIPP 101±1.60 2.22 0.66 TDCIPP 65.2±2.04 1.53 1.20 TCP 67.7±8.31 2.16 0.64 PBDEs PBDEs BDE 28 127±0.47 2.07 5.76 BDE 153 105±1.85 5.91 10.2 BDE 47 104±0.45 0.66 5.66 BDE 154 104±1.97 4.28 9.02 BDE 99 111±1.68 0.89 4.94 BDE 183 98.4±0.38 5.41 8.02 BDE 100 112±3.82 4.58 6.26 BDE 209 96.4±0.36 0.18 0.12 表 6 经研磨和消解处理后测得的头发样品中EOCs的检出率和浓度范围
Table 6. Detection frequency and concentration range of EOCs detected by hair samples after grinding and digestion
化合物Chemicals 研磨Grind 消解Digestion 检出率/%Detection frequency 浓度范围/(ng·g−1)Concentration range 检出率/%Detection frequency 浓度范围/(ng·g−1)Concentration range OPFRs TPHP 100 6.32—332 100 20.9—476 TIPRP 0 nd 0 nd TEP 0 nd 0 nd TNBP 30 nd—7.85 55 nd—7.37 TBOEP 60 nd—33.5 33 nd—2.54 TEHP 100 2.69—30.3 100 3.63—30.2 EHDPP 100 8.14—176 100 16.2—174 TCEP 100 6.38—36.6 100 4.04—44.7 TCIPP 100 14.9—132 100 1.38—48.0 TDCIPP 80 nd—390 66 nd—177 TCP 0 nd 0 nd PBDEs BDE 28 0 nd 0 nd BDE 47 0 nd 0 nd BDE 99 0 nd 0 nd BDE 100 0 nd 0 nd BDE 153 0 nd 0 nd BDE 154 0 nd 0 nd BDE 183 0 nd 0 nd BDE 209 100 1.09—36.6 100 0.57—41.4 PFASs PFHpA 30 nd—2.04 0 nd PFOA 70 nd—2.47 0 nd PFNA 60 nd—1.05 0 nd PFDA 30 nd—0.36 0 nd PFUdA 90 nd—0.58 0 nd PFDoA 70 nd—0.24 0 nd PFTrDA 10 nd—0.47 0 nd PFTeDA 30 nd—0.08 0 nd PFBS 0 nd 0 nd PFHxS 0 nd 0 nd PFOS 100 1.40—17.9 0 nd PFDS 0 nd 0 nd PAEs DMP 100 63.9—181 na na DEP 100 127—2593 na na DIBP 100 804—4823 na na DNBP 100 1074—4402 na na DMEP 0 nd na na DMPP 0 nd na na DEEP 0 nd na na DPP 20 nd—334 na na DHP 0 nd na na BBP 0 nd na na BBEP 0 nd na na DEHP 100 326—4951 na na DPHP 20 nd—1.50 na na DOP 0 nd na na DNP 0 nd na na mPAEs 5OH-MEHP 60 nd—4.53 0 nd 5Oxo-MEHP 0 nd 0 nd mEHP 100 27.0—298 0 nd mEP 30 nd—260 0 nd mnOP 0 nd 0 nd mBzP 0 nd 0 nd miNP 0 nd 0 nd miBP 100 15.0—38.6 0 nd 注:nd 未检出;na 未获得. Note: nd, not detected, na, not available. -
[1] PAL A, GIN K Y H, LIN A Y C, et al. Impacts of emerging organic contaminants on freshwater resources: Review of recent occurrences, sources, fate and effects [J]. Science of the Total Environment, 2010, 408(24): 6062-6069. doi: 10.1016/j.scitotenv.2010.09.026 [2] LIU B, ZHANG S G, CHANG C C. Emerging pollutants - part II: Treatment [J]. Water Environment Research:a Research Publication of the Water Environment Federation, 2017, 89(10): 1829-1865. doi: 10.2175/106143017X15023776270674 [3] GARCÍA J, GARCÍA-GALÁN M J, DAY J W, et al. A review of emerging organic contaminants (EOCs), antibiotic resistant bacteria (ARB), and antibiotic resistance genes (ARGs) in the environment: Increasing removal with wetlands and reducing environmental impacts [J]. Bioresource Technology, 2020, 307: 123228. doi: 10.1016/j.biortech.2020.123228 [4] ZHONG M M, WANG T L, ZHAO W X, et al. Emerging organic contaminants in Chinese surface water: Identification of priority pollutants [J]. Engineering, 2022, 11: 111-125. doi: 10.1016/j.eng.2020.12.023 [5] ZENG Y Q, PAN W J, DING N, et al. Brominated flame retardants in home dust and its contribution to brominated flame retardants bioaccumulation in children hair [J]. Journal of Environmental Science and Health. Part A, Toxic/Hazardous Substances & Environmental Engineering, 2020, 55(13): 1528-1533. [6] LIU L Y, HE K, HITES R A, et al. Hair and nails as noninvasive biomarkers of human exposure to brominated and organophosphate flame retardants [J]. Environmental Science & Technology, 2016, 50(6): 3065-3073. [7] KATSIKANTAMI I, SIFAKIS S, TZATZARAKIS M N, et al. A global assessment of phthalates burden and related links to health effects [J]. Environment International, 2016, 97: 212-236. doi: 10.1016/j.envint.2016.09.013 [8] ZHANG Y, JIAO Y Q, LI Z X, et al. Hazards of phthalates (PAEs) exposure: A review of aquatic animal toxicology studies [J]. Science of the Total Environment, 2021, 771: 145418. doi: 10.1016/j.scitotenv.2021.145418 [9] HOUDE M, MARTIN J W, LETCHER R J, et al. Biological monitoring of polyfluoroalkyl substances: A review [J]. Environmental Science & Technology, 2006, 40(11): 3463-3473. [10] 徐方萍. 传统和新型全氟化合物在室内灰尘和孕妇血浆中污染特征研究[D]. 广州: 暨南大学, 2020. XU F P. Pollution characteristics of legacy and emerging per- and polyfluoroalkyl substances in indoor dust and pregnancy women plasma[D]. Guangzhou: Jinan University, 2020(in Chinese).
[11] LI J G, GUO F F, WANG Y X, et al. Development of extraction methods for the analysis of perfluorinated compounds in human hair and nail by high performance liquid chromatography tandem mass spectrometry [J]. Journal of Chromatography A, 2012, 1219: 54-60. doi: 10.1016/j.chroma.2011.11.015 [12] LIEW Z, GOUDARZI H, OULHOTE Y. Developmental exposures to perfluoroalkyl substances (PFASs): An update of associated health outcomes [J]. Current Environmental Health Reports, 2018, 5(1): 1-19. doi: 10.1007/s40572-018-0173-4 [13] ZHANG W Z, ZHENG X W, GU P, et al. Distribution and risk assessment of phthalates in water and sediment of the Pearl River Delta [J]. Environmental Science and Pollution Research International, 2020, 27(11): 12550-12565. doi: 10.1007/s11356-019-06819-y [14] PENG F J, HARDY E M, BERANGER R, et al. Human exposure to PCBs, PBDEs and bisphenols revealed by hair analysis: A comparison between two adult female populations in China and France [J]. Environmental Pollution, 2020, 267: 115425. doi: 10.1016/j.envpol.2020.115425 [15] 王晓伟, 刘景富, 阴永光. 有机磷酸酯阻燃剂污染现状与研究进展 [J]. 化学进展, 2010, 22(10): 1983-1992. WANG X W, LIU J F, YIN Y G. The pollution status and research progress on organophosphate ester flame retardants [J]. Progress in Chemistry, 2010, 22(10): 1983-1992(in Chinese).
[16] 李珺琪. 北京大学生暴露于室内灰尘中有机阻燃剂状况的研究[D]. 北京: 中央民族大学, 2019. LI J Q. Study on the exposure of Beijing college students to organic flame retardants in indoor dust[D]. Beijing: Central University for Nationalities, 2019(in Chinese).
[17] CHOU T H, OU M H, WU T Y, et al. Temporal and spatial surveys of polybromodiphenyl ethers (PBDEs) contamination of soil near a factory using PBDEs in northern Taiwan [J]. Chemosphere, 2019, 236: 124117. doi: 10.1016/j.chemosphere.2019.06.087 [18] LI B B, HU L X, YANG Y Y, et al. Contamination profiles and health risks of PFASs in groundwater of the Maozhou River Basin [J]. Environmental Pollution, 2020, 260: 113996. doi: 10.1016/j.envpol.2020.113996 [19] HE C, WANG X Y, THAI P, et al. Organophosphate and brominated flame retardants in Australian indoor environments: Levels, sources, and preliminary assessment of human exposure [J]. Environmental Pollution, 2018, 235: 670-679. doi: 10.1016/j.envpol.2017.12.017 [20] XU Y Y, WENG R, LU Y S, et al. Evaluation of phthalic Acid esters in fish samples using gas chromatography tandem mass spectrometry with simplified QuEChERS technique [J]. Food Analytical Methods, 2018, 11(12): 3293-3303. doi: 10.1007/s12161-018-1313-z [21] ZAFEIRAKI E, COSTOPOULOU D, VASSILIADOU I, et al. Perfluoroalkylated substances (PFASs) in home and commercially produced chicken eggs from the Netherlands and Greece [J]. Chemosphere, 2016, 144: 2106-2112. doi: 10.1016/j.chemosphere.2015.10.105 [22] ALVES A, JACOBS G, VANERMEN G, et al. New approach for assessing human perfluoroalkyl exposure via hair [J]. Talanta, 2015, 144: 574-583. doi: 10.1016/j.talanta.2015.07.009 [23] CHEN Z J, LIU H Y, CHENG Z, et al. Polybrominated diphenyl ethers (PBDEs) in human samples of mother-newborn pairs in South China and their placental transfer characteristics [J]. Environment International, 2014, 73: 77-84. doi: 10.1016/j.envint.2014.07.002 [24] WANG Y X, ZHONG Y X, LI J G, et al. Occurrence of perfluoroalkyl substances in matched human serum, urine, hair and nail [J]. Journal of Environmental Sciences, 2018, 67: 191-197. doi: 10.1016/j.jes.2017.08.017 [25] LI J H, LI Q, LI J F, et al. Simultaneous determination of poly- and perfluoroalkyl substances and organophosphorus flame retardants in serum by ultra-performance liquid chromatography/tandem mass spectrometry [J]. Rapid Communications in Mass Spectrometry:RCM, 2022, 36(14): e9312. [26] CHEN J A, LIU H J, QIU Z Q, et al. Analysis of di-n-butyl phthalate and other organic pollutants in Chongqing women undergoing parturition [J]. Environmental Pollution, 2008, 156(3): 849-853. doi: 10.1016/j.envpol.2008.05.019 [27] 李树飞, 杜美玲, 王开亮, 等. 待产孕妇血清中PAEs暴露水平及其与胎儿生长发育的相关性研究 [J]. 中国妇幼保健, 2013, 28(25): 4194-4197. doi: 10.7620/zgfybj.j.issn.1001-4411.2013.25.45 LI S F, DU M L, WANG K L, et al. Study on the correlation between exposure level of PAEs in serum of predelivery women and growth and development of fetuses [J]. Maternal and Child Health Care of China, 2013, 28(25): 4194-4197(in Chinese). doi: 10.7620/zgfybj.j.issn.1001-4411.2013.25.45
[28] 崔恒威, 严浩轩, 陈丽梅. 多溴二苯醚的生殖发育毒性 [J]. 卫生研究, 2021, 50(3): 510-514. doi: 10.19813/j.cnki.weishengyanjiu.2021.03.028 CUI H W, YAN H X, CHEN L M. Reproductive and developmental toxicity of polybrominated diphenyl ethers [J]. Journal of Hygiene Research, 2021, 50(3): 510-514(in Chinese). doi: 10.19813/j.cnki.weishengyanjiu.2021.03.028
[29] MAMMANA S B, ABRAHAM E C, CAMARGO A B, et al. Enzymatic digestion coupled to surfactant-assisted dispersive liquid-liquid microextraction: A mild approach for determining polybrominated diphenyl ethers in human hair sample [J]. ChemistrySelect, 2020, 5(7): 2179-2184. doi: 10.1002/slct.201904795 [30] MARTINEZ G, NIU J, TAKSER L, et al. A review on the analytical procedures of halogenated flame retardants by gas chromatography coupled with single quadrupole mass spectrometry and their levels in human samples [J]. Environmental Pollution, 2021, 285: 117476. doi: 10.1016/j.envpol.2021.117476 [31] YIN S S, BEEN F, LIU W P, et al. Hair as an alternative matrix to monitor human exposure to plasticizers - Development of a liquid chromatography - tandem mass spectrometry method [J]. Journal of Chromatography B, 2019, 1104: 94-101. doi: 10.1016/j.jchromb.2018.09.031 [32] LIANG S, XU F, TANG W B, et al. Brominated flame retardants in the hair and serum samples from an e-waste recycling area in southeastern China: The possibility of using hair for biomonitoring [J]. Environmental Science and Pollution Research, 2016, 23(15): 14889-14897. doi: 10.1007/s11356-016-6491-x [33] TADEO J L, SANCHEZ-BRUNETE C, MIGUEL E. Determination of polybrominated diphenyl ethers in human hair by gas chromatography-mass spectrometry [J]. Talanta, 2009, 78(1): 138-143. doi: 10.1016/j.talanta.2008.10.054 [34] HE M J, LU J F, MA J Y, et al. Organophosphate esters and phthalate esters in human hair from rural and urban areas, Chongqing, China: Concentrations, composition profiles and sources in comparison to street dust [J]. Environmental Pollution, 2018, 237: 143-153. doi: 10.1016/j.envpol.2018.02.040 [35] 高倍. 头发指甲作为人类全氟化合物暴露评价指示物的研究[D]. 大连: 大连理工大学, 2014. GAO B. Human hair and nail As bioindicator of exposure to perfluoroalkyl acids[D]. Dalian: Dalian University of Technology, 2014(in Chinese).
[36] RUAN Y F, LALWANI D, KWOK K Y, et al. Assessing exposure to legacy and emerging per- and polyfluoroalkyl substances via hair - The first nationwide survey in India [J]. Chemosphere, 2019, 229: 366-373. doi: 10.1016/j.chemosphere.2019.04.195 [37] WANG Y, SHI Y L, VESTERGREN R, et al. Using hair, nail and urine samples for human exposure assessment of legacy and emerging per- and polyfluoroalkyl substances [J]. Science of the Total Environment, 2018, 636: 383-391. doi: 10.1016/j.scitotenv.2018.04.279 [38] GAO Y, ZHANG Q H, LI X M, et al. Simultaneous determination of legacy and emerging per- and polyfluoroalkyl substances in fish by QuEChERS coupled with ultrahigh performance liquid chromatography tandem mass spectrometry [J]. Analytical Methods, 2018, 10(47): 5715-5722. doi: 10.1039/C8AY01478G [39] MARTÍN J, MÖDER M, GAUDL A, et al. Multi-class method for biomonitoring of hair samples using gas chromatography-mass spectrometry [J]. Analytical and Bioanalytical Chemistry, 2015, 407(29): 8725-8734. doi: 10.1007/s00216-015-9026-2 [40] LIN M Q, TANG J, MA S T, et al. Simultaneous determination of polybrominated diphenyl ethers, polycyclic aromatic hydrocarbons and their hydroxylated metabolites in human hair: A potential methodology to distinguish external from internal exposure [J]. Analyst, 2019, 144(24): 7227-7235. doi: 10.1039/C9AN01359H [41] KUCHARSKA A, COVACI A, VANERMEN G, et al. Development of a broad spectrum method for measuring flame retardants - Overcoming the challenges of non-invasive human biomonitoring studies [J]. Analytical and Bioanalytical Chemistry, 2014, 406(26): 6665-6675. doi: 10.1007/s00216-014-8106-z [42] 唐斌, 蔡凤珊, 王美欢, 等. 室内灰尘和空气中有机磷系阻燃剂和塑化剂的赋存、分配和暴露风险评估[C]//. 2020中国环境科学学会科学技术年会论文集(第一卷). 南京, 2020∶1078—1084. [43] 熊仕茂, 朱晓辉, 蔡凤珊, 等. 灰尘中有机磷系阻燃剂及其降解产物检测方法的建立 [J]. 环境化学, 2019, 38(11): 2457-2466. XIONG S M, ZHU X H, CAI F S, et al. Establishment of detection method for organic phosphorus flame retardants and their degradation products in dust [J]. Environmental Chemistry, 2019, 38(11): 2457-2466(in Chinese).
[44] 任梦圆, 贾晓倩, 王盈, 等. 北京市海淀区孕妇膳食频率与头发中邻苯二甲酸酯水平的关联研究 [J]. 中国生育健康杂志, 2021, 32(2): 101-105. REN M Y, JIA X Q, WANG Y, et al. Association between food frequency and hair concentration of phthalates among pregnant women in Haidian District, Beijing [J]. Chinese Journal of Reproductive Health, 2021, 32(2): 101-105(in Chinese).
[45] TAN H H, GU Y P, LIU S H, et al. Rapid residue determination of cyenopyrafen in Citrus peel, pulp, and whole fruit using ultra-performance liquid chromatography/tandem mass spectrometry [J]. Food Analytical Methods, 2018, 11(8): 2123-2130. doi: 10.1007/s12161-018-1197-y [46] LOCKWOOD T E, TALEBI M, MINETT A, et al. Micro solid-phase extraction for the analysis of per- and polyfluoroalkyl substances in environmental waters [J]. Journal of Chromatography A, 2019, 1604: 460495. doi: 10.1016/j.chroma.2019.460495 [47] ZHENG J, LUO X J, YUAN J G, et al. Levels and sources of brominated flame retardants in human hair from urban, e-waste, and rural areas in South China [J]. Environmental Pollution, 2011, 159(12): 3706-3713. doi: 10.1016/j.envpol.2011.07.009 [48] QIAO L, ZHENG X B, ZHENG J, et al. Legacy and currently used organic contaminants in human hair and hand wipes of female E-waste dismantling workers and workplace dust in South China [J]. Environmental Science & Technology, 2019, 53(5): 2820-2829. [49] KATSIKANTAMI I, TZATZARAKIS M N, KARZI V, et al. Biomonitoring of bisphenols A and S and phthalate metabolites in hair from pregnant women in Crete [J]. Science of the Total Environment, 2020, 712: 135651. doi: 10.1016/j.scitotenv.2019.135651 [50] TANG B, XIONG S M, ZHENG J, et al. Analysis of polybrominated diphenyl ethers, hexabromocyclododecanes, and legacy and emerging phosphorus flame retardants in human hair [J]. Chemosphere, 2021, 262: 127807. doi: 10.1016/j.chemosphere.2020.127807 -




 DownLoad:
DownLoad: