-
水体的富营养化加剧了蓝藻水华的频繁爆发。这不但影响水体景观效果,还会释放藻毒素,严重威胁水生态系统的稳定和公共卫生安全[1]。在众多藻毒素中,微囊藻毒素(microcystins, MCs)是一种具有显著肝脏毒性的七肽环状毒素,是世界各地水体中最为常见且危害最大的藻毒素。微囊藻毒素-LR(MC-LR)是MCs单体中分布最广毒性最强的一类,世界卫生组织(WHO)规定其在饮用水中最高含量不得超过1.0 µg·L−1[2]。鱼腥藻毒素(anatoxin, ANTXs)是一类毒性大、活性高的神经毒素,不慎接触会导致人和动物迅速中毒死亡。鱼腥藻毒素-a(ANTX-a)是鱼腥藻毒素中含量最高的一种单体,饮用水中最大安全剂量为3.0 µg·L−1[3]。在蓝藻水华频发水域,70%以上监测水体中都同时检测到MCs与ANTXs,表明两种毒素时空共存已普遍存在,且MCs或ANTXs浓度通常在1—100 µg·L−1,极端状况下会在短时间内高达1000 µg·L−1以上[4]。这些藻毒素通过灌溉、溢流、打捞堆放、堆沤还田(特别是蓝藻堆肥后施入农田)等途径进入农田系统[5-6]。研究发现,MCs被农作物吸收积累后,不仅影响农作物生长发育,如降低光合效率、破坏激素平衡、抑制抗氧化酶活性等[7-8],也会在植物可食部分积累并通过食物链传递威胁人体健康[9-10]。在调查35种农作物暴露于MCs的结果显示,MCs残留量最高的是生菜(Lactuca sativa)、欧芹(Petroselinum crispum)、茴香(Foeniculum vulgare)和卷心菜(Brassica oleracea)等蔬菜,其次是玉米(Zea mays)、胡萝卜(Daucus carota)和小麦(Hordeum vulgare)等作物[11]。因而关于藻毒素的植物毒理学研究近年来也备受关注。然而已有研究大多集中在MCs对植物生理生化代谢的影响,关于ANTXs的研究多集中在水生植物[12],关于MCs和ANTXs对植物的复合影响却鲜有报道。农作物在人类膳食结构中占有重要地位,如能明确MCs和ANTXs对农作物的复合作用机制,将为客观评价藻毒素的生态风险提供新依据,也为保障食品安全提供新的数据。
活性氧(reactive oxygen species, ROS)是植物有氧代谢中具有很强毒性的副产物,主要包括过氧化氢(H2O2)、超氧阴离子(O2·-)、羟基自由基(·OH)等[13]。作为信号分子,逆境迫使植物细胞中积累大量ROS以诱导防御基因的表达,进而调控植物对逆境的适应性。同时大量积累的ROS会引发氧化损伤,甚至导致细胞死亡[14]。因此,逆境下植物维持胞内ROS稳态是提高植物耐受性的重要机制之一。例如,MCs胁迫下水稻(Oryza sativa)中抗氧化酶清除ROS的能力强于黄瓜(Cucumis sativus),这也是水稻耐受MCs胁迫能力强于黄瓜的主要因素[8]。基于ROS水平与植物耐受环境胁迫机制的密切关系,从活性氧稳态(即产生与清除间的平衡)的角度去理解MCs和ANTXs对植物生长影响的复合作用特征,可为清晰植物耐受蓝藻毒素胁迫的适应机制提供新数据。鉴于此,本文选取广泛种植的生菜(Lactuca sativa)为研究对象,以调控活性氧生成与去除的重要酶类为切入点,探究MCs与ANTXs对生菜中活性氧稳态影响的内在机制,为客观评价蓝藻毒素的生态风险提供新的数据。
-
本研究所采用的MCs和ANTXs均提取自蓝藻细胞。用于提取微囊藻毒素(MCs)的新鲜蓝藻打捞自无锡太湖,提取与分析方法参照文献[9]。通过酶联免疫(ELISA)测定总MCs浓度,再通过高效液相色谱(HPLC)确定各MC变体占比(其中MC-LR、MC-RR和MC-YR分别占62.66%、28.48%和0.68%)。产生ANTXs的水华鱼腥藻(FACHB-1255)采购自中国科学院淡水藻种库(FACHB),提取与分析方法参照文献[15]。同样通过ELISA测定总ANTXs浓度,再通过HPLC确定ANTXs各变体占比(ANTX-a: HANTX-a=76.4%:23.6%)。
-
将籽粒饱满的生菜(Lactuca sativa L.)种子用0.1% HgCl2去离子水浸泡4 h,在黑暗中发芽(温度20 ℃;相对湿度70%)。待生菜长出两片真叶后移入含有营养液的5 L周转箱进行培养(每箱6株),培养条件为光强为350 µmol·m−2·s−2(日/夜:14 h/10 h),温度为25 ℃/18 ℃(日/夜),相对湿度80%。营养液每7 天更换1次,培养30 d后处理。参考自然水体中MCs与ANTXs出现频率较高的环境浓度范围, 将培养成熟的生菜移至含不同浓度MCs、ANTXs及MCs+ANTXs的营养液中进行处理。实验对照(CK,营养液中无藻毒素),单一MCs处理(营养液中MCs浓度分别为5 µg·L−1和100 µg·L−1),单一ANTXs处理(营养液中ANTXs浓度分别为5 µg·L−1和100 µg·L−1)和MCs+ANTXs复合处理(营养液中MCs和ANTXs浓度为(5+5) µg·L−1和(100+100) µg·L−1。每处理重复3次,处理7 d后收获。
-
采用电子天平测量生菜生物量。参考张清航等[16]的方法测定植物体内MDA含量,采用硫酸钛法测定H2O2含量[17]和羟氨氧化法测定O2·−含量[18]。参照关美艳[19]的方法测定NADPH氧化酶活性。采用Zhang等[20]的方法进行LsRbohA引物设计和扩增程序,基因相对表达量采用2−ΔΔCT法进行计算。采用FRAP法测定植株的总抗氧化能力[21]。SOD和CAT活性的测定参考顾艳芳等[22]的方法并稍作改动。MCs和ANTXs对生菜的复合影响作用使用Abotts公式[23]进行具体评估。
其中,A是单一MCs引起生菜指标的抑制程度;B是单一ANTXs引起生菜指标的抑制程度;C是MCs+ANTXs复合处理引起生菜指标的抑制程度;Cexp是预期抑制率;RI为抑制比率。
-
所有数据均以3次独立试验的平均值±标准误差(Mean±SD)表示。采用Levene检验分析各组方差的同质性,组间差异通过LSD检验的单因素方差进行评估(P<0.05)。
-
实验中以生物量(FW)表征生菜生长情况,以丙二醛(MDA)含量衡量植物氧化损伤程度[24],结合ROS中重要成员H2O2和O2·−含量变化,探究MCs与ANTXs对生菜中ROS稳态的影响。如表1所示,与CK相比,低浓度(5 µg·L−1)MCs、ANTXs及MCs+ANTXs((5+5) µg·L−1)复合处理分别促进生菜生物量增加75.3%、85.6%和63.3% (P<0.05),其中MCs+ANTXs((5+5) µg·L−1)组生物量低于单一MCs(5 µg·L−1)或ANTXs(5 µg·L−1)。同时,低浓度(5 µg·L−1)MCs或ANTXs对叶片中MDA、H2O2和O2·−含量无显著影响(P>0.05),其中MCs+ANTXs(5+5) µg·L−1复合处理诱导H2O2和O2·−含量小幅上升且MDA含量略高于CK(P<0.05)。综上结果可知,低浓度MCs、ANTXs及MCs+ANTXs复合处理促进生菜生长,呈现Hormesis效应。这种低浓度毒素促进作用可能与刺激植物体内生长促进型激素(生长素IAA、玉米素ZT和赤霉素GA3)含量升高有关[25]。此外,低浓度毒素未引起生菜活性氧大量积累,也未引起脂膜过氧化损伤,表明此时毒素胁迫强度未超出生菜的自调节范围,这也可能是生菜生长仍能正常进行的又一原因。与低浓度处理不同,高浓度(100 µg·L−1)MCs与MCs+ANTXs(100+100) µg·L−1复合处理降低生菜生物量达27.7%、5.1%和16.8%(P<0.05),其中高浓度(100 µg·L−1)ANTXs对生菜生物量无明显影响(P>0.05),这可能与毒素本身的理化性质,如分子量、作用方式以及毒性差异等原因有关[26]。Ariel等[12]发现ANTX-a浓度高达5000 µg·L−1时才会严重抑制品藻的生长。高浓度MCs、ANTXs及MCs+ANTX处理导致叶片中MDA、H2O2和O2·−含量显著增加(P<0.05),其中MDA、H2O2和O2·−含量增幅排序为MCs>MCs+ANTXs>ANTXs。以上结果说明100 µg·L−1MCs或ANTXs诱导了ROS含量升高而导致脂膜损伤,这可能是导致高浓度MCs和MCs+ANTX抑制生菜生长的原因之一。其中高浓度MCs+ANTXs抑制生菜生长的程度低于单一MCs,可能与MCs+ANTXs诱导生菜中产生ROS含量低于单一MCs有关。前期研究也发现MCs对植物细胞中ROS平衡的影响程度受MCs浓度、暴露时间以及植物种类等因素调节,可以反映植物耐受MCs的能力[8]。结合生物量、ROS水平和MDA分析,生菜能够耐受低浓度(5 µg·L−1)毒素胁迫,但不能耐受高浓度(100 µg·L−1)胁迫,且对高浓度MCs+ANTXs复合胁迫的耐受性强于单一MCs却弱于单一ANTXs,这可能与维持细胞内活性氧稳定的能力有关。
-
质膜上的NADPH氧化酶是植物细胞活性氧产生的主要酶之一[27],它能够将O2催化成O2·−,因此可用来表征植物ROS生成能力[28]。LsRbohA是编码生菜NADPH氧化酶的关键基因。与CK相比,低浓度(5 µg·L−1)MCs或ANTXs处理对生菜叶片中NADPH氧化酶活性及LsRbohA相对表达量均无显著影响(P>0.05)(图1),MCs+ANTXs复合处理显著提高了NADPH氧化酶活性,LsRbohA的相对表达量上调137.8%(P<0.05)。这表明低浓度MCs或ANTXs对生菜叶中ROS的生成无影响,这是生菜叶片中ROS维持稳态的原因之一。而低浓度(5+5) µg·L−1MCs+ANTXs复合下生菜叶片中LsRbohA表达量的上调可能是NADPH氧化酶活性上升的原因之一。结合生菜生物量、ROS含量和MDA含量(表1)分析可知,低浓度MCs+ANTXs复合处理通过促进NADPH氧化酶活性诱导ROS生成增多,促使防御系统及时对外界环境变化做出适应性应激,避免氧化损伤而不影响植物生长[29]。高浓度MCs、ANTXs和MCs+ANTXs复合处理显著上调LsRbohA表达272%—657%,且诱导NADPH氧化酶活性上升(P<0.05),其中酶活性增幅排序为MCs>MCs+ANTXs>ANTXs。表明高浓度(100 µg·L−1)MCs、ANTXs和MCs+ANTXs复合处理下生菜叶片中LsRbohA表达量大幅上升,合成酶蛋白增多,这可能是NADPH氧化酶活性上升的原因之一。NADPH氧化酶催化生成大量ROS,促发防御系统应激,但仍无法抵御高浓度毒素的伤害,最终引起氧化损伤而抑制生长(表1)。Pérez等[30]也发现,NADPH氧化酶是植物响应非生物胁迫下初始ROS升高的主要原因之一。同时H2O2可以诱导NADPH氧化酶基因Rboh表达[28],这是植物遭受非生物逆境的威胁时,信号分子H2O2启动一系列抗逆相关基因表达来缓解或抵御非生物逆境胁迫对植物造成的危害[31-32]。因而本实验中高浓度MCs+ANTXs复合处理下生菜NADPH氧化酶活性高于单一ANTXs却低于MCs, 这可能是MCs+ANTXs处理组生菜中ROS含量高于单一ANTXs而低于单一MCs的主要因素之一。
-
植物细胞中ROS平衡也受抗氧化系统的调节。SOD作为植物抗氧化系统的第一道防线,将胁迫诱导的过量O2·−歧化为H2O2和O2。H2O2在第二道防线CAT的催化下分解为H2O和O2。考虑到植物拥有众多抗氧化酶类和非酶类,将抗氧化酶活性与总抗氧化能力(FRAP)结合能更全面地反映植物细胞清除ROS的能力[21]。如图2所示,与CK相比,低浓度(5 µg·L−1)MCs、ANTXs和MCs+ANTXs(5+5) µg·L−1复合处理显著提高生菜的FRAP (P<0.05),促进SOD活性上升(除单一ANTXs处理组外),而对CAT活性无显著影响(P>0.05)。表明低浓度毒素处理组诱导SOD活性和FRAP上升,维持胞内ROS稳定。低浓度毒素处理下第二道防线的CAT未应激启动再次证实,该强度胁迫未超出生菜耐受范围。高浓度(100 µg·L−1)MCs、ANTXs和MCs+ANTXs显著促进生菜叶片中的SOD和CAT活性上升(P<0.05),增幅排序为MCs>MCs+ANTXs>ANTXs。生菜叶片的FRAP变化却不尽一致,在100 µg·L−1 MCs处理下降低(P<0.05),在100 µg·L−1 ANTXs处理下上升(P<0.05),而在MCs+ANTXs(100+100) µg·L−1处理下无显著变化(P>0.05)。结合FW、MDA和ROS含量变化(表1)分析发现,高浓度(100 µg·L−1)毒素促发SOD和CAT活性升高不足以清除过量生成的ROS,胞内ROS稳态被破坏,氧化损伤发生,这也是生长受抑制的原因之一。不同高浓度毒素处理下生菜FRAP变化不一致,这可能是由于植物体内抗氧化酶类和非酶类对不同毒素胁迫的响应程度有差异。例如酸雨胁迫下水稻幼苗SOD、CAT和脱氢抗坏血酸还原酶(DHAR)活性增加,而抗坏血酸过氧化物酶(APX)和谷胱甘肽还原酶(GR)活性降低[33-34]。此外,酚类和类黄酮物质也属于植物的非酶抗氧化剂防御系统的成员,其含量或状态变化也会影响细胞总抗氧化能力[35]。因此,生菜叶中SOD、CAT和FRAP对高浓度(100 µg·L−1)MCs、ANTXs和MCs+ANTXs处理响应存在差异,其中较高的SOD和CAT活性及FRAP有助于缓解高浓度毒素诱导的ROS过量积累,对维持ROS稳态有利,这也许是MCs+ANTXs组ROS含量高于单一ANTXs而低于单一MCs的又一原因。
-
两种不同污染物对受试生物的影响可能呈现独立作用、协同作用、加和作用或者拮抗作用。为客观评价MCs和ANTXs对生菜活性氧稳态的复合影响,分析了MCs+ANTXs对生菜ROS稳态相关指标复合影响的特征(表2)。当RI值>1时,呈现协同效应;RI=1,呈现加和效应;RI<1,则呈现拮抗效应[36]。
如表2所示,MCs+ANTXs(5+5) µg·L−1对MDA含量、H2O2、NADPH氧化酶与CAT活性抑制比率RI值均显著>1,呈现协同效应;而MCs+ANTXs(100+100) µg·L−1对MDA含量、H2O2、NADP氧化酶与CAT活性抑制比率RI值均显著<1,呈现拮抗效应。表明随着MCs和ANTXs浓度升高,两者间复合作用特征由协同作用转为拮抗作用。Wang等[36]研究发现低浓度MC-LR和多环芳烃(菲)对浮萍生长和抗氧化系统产生协同作用,而高浓度呈现拮抗或加和作用。因此,MCs与ANTXs对生菜生长与ROS稳态的复合作用特征受毒素浓度的影响。其中,MCs+ANTXs(100+100) µg·L−1对以上所有参数的抑制比率(RI)均<1,表明高浓度MCs+ANTXs对生菜复合作用特征主要呈拮抗效应,这与Li等研究结果一致[37],他们也发现MC-LR和ANTX-a对苦草生长和蛋白质的复合作用呈现拮抗效应。这与MCs或ANTXs进入细胞存在竞争有关,也可能与铜绿微囊藻与水华鱼腥藻之间存在竞争关系有关。例如在共培养的条件下,水华鱼腥藻对铜绿微囊藻有显著的抑制作用[38]。以上可以推测,水体中一定浓度的ANTXs可以减轻MCs对生菜的氧化伤害。
-
(1)低浓度(5 µg·L−1)MCs、ANTXs与MCs+ANTXs诱导生菜中SOD活性和总抗氧化能力(FRAP)上升,利于维持ROS平衡,避免了氧化损伤,促进生物量增加63.3%—85.6%,表明低浓度(5 µg·L−1)MCs、ANTXs和MCs+ANTXs对生菜生长有利。
(2)高浓度(100 µg·L−1)MCs、ANTXs与MCs+ANTXs上调生菜叶片中LsRbohA表达并提高NADPH氧化酶活性,生成大量ROS促发防御系统应激,而SOD和CAT活性的上升不足以清除大量ROS,诱发氧化损伤而抑制生菜生长,降幅为MCs(27.7%)>MCs+ANTXs(16.8%)>ANTXs(5.1%)。
(3)复合特征分析发现,MCs+ANTXs(5+5) µg·L−1对MDA含量、H2O2、NADP氧化酶与CAT活性影响呈现协同效应,而MCs+ANTXs(100+100) µg·L−1则呈现拮抗效应。表明MCs+ANTXs对生菜复合作用受毒素浓度的影响,高浓度ANTXs共存在一定程度上减轻了MCs对生菜的氧化伤害。
微囊藻毒素与鱼腥藻毒素对生菜活性氧稳态的复合影响
Compound effects of microcystin and anatoxin on homeostasis of reactive oxygen species in lettuce
-
摘要: 水体富营养化导致水体中蓝藻毒素浓度高于安全值。为客观评价灌溉水中蓝藻毒素的生态风险,本研究探析了微囊藻毒素(MCs)和鱼腥藻毒素(ANTXs)对生菜生长和活性氧(ROS)稳态的复合影响。采用5 µg·L−1或100 µg·L−1MCs、ANTXs和MCs+ANTXs((5+5) µg·L−1或(100+100) µg·L−1)处理生菜7 d后发现,低浓度(5 µg·L−1)MCs、ANTXs或MCs+ANTXs促进生菜鲜重增加63.3%—85.6%,可能是低浓度毒素诱导SOD活性和总抗氧化能力(FRAP)上升以维持H2O2和O2·−平衡进而避免氧化损伤。高浓度(100 µg·L−1)MCs、ANTXs或MCs+ANTXs抑制生菜生长,降幅为MCs(27.7%)>MCs+ANTXs(16.8%)>ANTXs(5.1%)。同时,MDA、H2O2和O2·−含量、NADPH氧化酶活性及LsRbohA表达量、SOD和CAT活性均升高,增幅为MCs>MCs+ANTXs>ANTXs,而FRAP变化不一致。推测高浓度藻毒素上调LsRbohA表达有助于增强NADPH氧化酶活性,生成的ROS增多以刺激防御应激,而SOD和CAT活性上升不足以维持ROS稳定,导致氧化损伤而抑制生长。进一步分析MCs+ANTXs对生菜中ROS稳态复合影响的作用特征发现,MCs+ANTXs(5+5) µg·L−1对MDA、H2O2、NADP氧化酶与CAT活性影响呈现协同效应,在MCs+ANTXs(100+100) µg·L−1处理下呈拮抗效应,表明MCs和ANTXs对生菜ROS稳态的复合影响受毒素浓度的调控,一定浓度的ANTXs共存减轻了MCs对生菜的氧化伤害,为指导灌溉安全提供新的理论依据。Abstract: The eutrophication of water leads to the increase of cyanobacteria toxin concentration in water. To objectively evaluate the ecological risk of cyanobacteria toxins in irrigation water, we studied compound effects of microcystin (MCs) and anatoxin (ANTXs) on growth and homeostasis of reactive oxygen species (ROS) in lettuce. After Hydroponic lettuce being treated with MCs (5 µg·L−1 or 100 µg·L−1), ANTXs (5 µg·L−1 or 100 µg·L−1) and MCs+ANTXs (5+5) µg·L−1 or (100+100) µg·L−1 for 7 d, we found that low concentration (5 µg·L−1) of MCs, ANTXs or MCs+ANTXs increased fresh weight of lettuce by 63.3%—85.6%, indicating that the increase of SOD activity and total antioxidant capacity (FRAP) induced by low concentration of toxin can maintain H2O2 and O2·− balance and then avoid oxidative damage. However, high concentration (100 µg·L−1) of MCs, ANTXs or MCs+ANTXs inhibited lettuce growth, and the decreased degree of each treatment was MCs(27.7%)>MCs+ANTXs(16.8%)>ANTXs(5.1%). Meanwhile, MDA, H2O2 and O2·− contents, NADPH oxidase activity and LsRbohA expression, SOD and CAT activities were increased with the order for increased degree as MCs>MCs+ANTXs>ANTXs. In addition, FRAP showed different change among treatments. These results indicate that high concentration treatments up-regulated LsRbohA expression for contributing to enhancing NADPH oxidase activity to produce more ROS for stimulating defense systems. While the increase in SOD and CAT activities was not enough to maintain the stability of ROS, resulting in oxidative damage and inhibition on growth. Furthermore, characteristic analysis of compound effects of MCs+ANTXs on ROS homeostasis in lettuce showed that MCs+ANTXs (5+5) µg·L−1 posed synergistic effects on MDA and H2O2 contents as well as NADPH oxidase and CAT activities in lettuce whereas MCs+ANTXs (100+100) µg·L−1 showed antagonistic effects on them. It can be included that compound effects of MCs and ANTXs on homeostasis of ROS in lettuce was dependent on their concentrations, and the coexistence of ANTXs at a certain concentration could reduce the oxidative damage caused by MCs to lettuce, providing a new theoretical basis for guiding the safety of irrigation water.
-
Key words:
- microcystins /
- anatoxin /
- NADPH oxidase /
- antioxidant enzymes /
- reactive oxygen species /
- lettuce
-
底泥是湖泊及其流域中重金属等污染物的重要归宿和蓄积库,底泥中的重金属形态和分布不仅能够反映自然和人类活动对湖泊的影响,也反映底泥对水体生态系统的威胁[1-3]。重金属在底泥的垂向分布与水平分布研究同样重要,它们在底泥某层位中的分布可反映某一历史时段内湖泊流域自然和人为活动所造成的重金属流失与污染强度 [4]。重金属是相对保守的物质,具有潜在危害性,一般认为底泥中重金属的毒性几乎与总量无关,而与间隙水中可生物利用的金属组分相关,间隙水中重金属离子浓度与底泥中重金属形态关系紧密[5-6]。底泥中重金属形态主要为金属可交换态、碳酸盐结合态、铁锰氧化物结合态、有机质及硫化物结合态和残渣晶格态,它们各自表现出不同的物理化学稳定性、生物可利用性及潜在生态毒害性 [7-8]。重金属的可交换态最易被生物利用,毒性最强,碳酸盐结合态也较易重新释放进入水相,因而可以用底泥中金属可交换态及碳酸盐结合态重金属占重金属总量的百分数来评价底泥中重金属的稳定程度 [6, 9]。
南四湖是我国华北平原上面积最大的淡水湖,湖泊面积1266 km2,自北向南依次由南阳、独山、昭阳和微山4个湖串联而成,平均水深约1.46 m。作为华东最重要的煤炭能源基地,南四湖周边地区的城市发电、民用煤燃烧,造纸、食品、化工、医药等行业企业的迅速发展,以及航运交通等方面的影响,南四湖近20年来底泥中Hg、Pb 、Cd和As的含量呈快速增长趋势,尤其是Hg和Pb的污染最为严重 [10-11]。底泥典型重金属对环境的危害除了与其总量有关外,更大程度上取决于其在环境系统中的形态和分布,其元素赋存形态是判断底泥中重金属的毒性响应以及生态风险的重要指标[3, 8]。作为南水北调东线工程最重要的输水通道和京杭大运河最重要的航运路段,对南四湖底泥典型重金属污染物的形态和污染程度进行分析评价具有重要意义[3]。然而,目前针对南四湖不同湖区底泥重金属污染研究多集中在总量水平分布上,而对其形态和垂向分布研究则较少[3, 12]。
本文以南四湖4个湖区为研究对象,在探讨4种典型重金属元素(Pb、Cd 、Hg 、As)主要生物有效形态垂向分布特征的基础上,对其表层底泥(0—4 cm)重金属污染程度、潜在生态风险性及稳定性进行评价,揭示南四湖近年来的重金属污染状况,为其水环境保护和底泥污染治理提供参考依据。
1. 材料与方法(Materials and Methods)
1.1 采样点布设
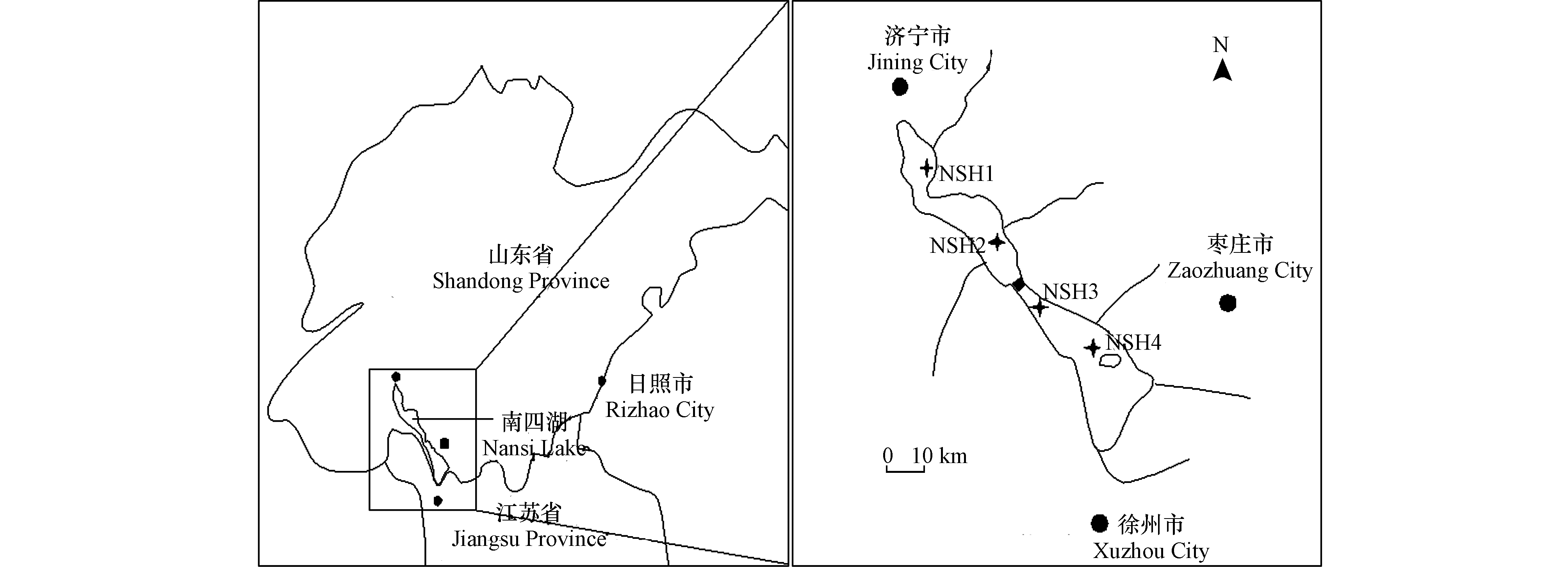
为充分反映南四湖不同湖区底泥性质的差异,结合现场环境条件,在南阳、独山、昭阳和微山等4个湖区的湖心分别设置代表性采样点,采样点布设应避免航运船只扰动及人工养殖的影响,具体采样点见图1。4个采样点位置及经纬度从北向南依次为:南阳湖区(NSH1,35°9′5.64″N,116°39′39″E)、独山湖区(NSH2,35°2′13.08″N,116°50′31.8″E)、昭阳湖区(NSH3,34°50′12.96″N,117°2′8.5″E)和微山湖区(NSH4,34°41′16.26″N,117°13′18.3″E)。
1.2 底泥的采集与预处理
2015年1月采集底泥样品,ϕ85 mm×600 mm有机玻璃管的柱状采样器每点采集3根平行样,上部用原样点水样注满后两端用橡皮塞塞紧,垂直放置,小心带回实验室[3]。在室内按10 cm以内间距为2 cm和10 cm以下间距为5 cm进行切样,自然风干至恒重,研磨后过100目筛备用。
1.3 底泥重金属形态分析
用Tessier分级提取法对底泥重金属进行形态含量分析[13],本文主要分析生物效应较强的3种形态:金属可交换态、碳酸盐结合态和铁锰氧化物结合态。因通过分级提取重金属各形态含量总和往往与实际总量有差异,本文采用三酸提取法对相应重金属总量进行一次性提取[14]。用电感耦合等离子体发射光谱仪(ICP-OES VISTA-MPX,美国Varian公司)检测重金属Pb、Cd、Hg和As总量及各形态含量。ICP-OES 工作前采用双内标Rh 和Re 对分析信号进行校正,RSD 在3%以下,测定前验证标准曲线,每种元素的线性相关系数达到0.9999以上,每批样品做1个平行空白和2个标准参考物质,全程采用空白样品进行对照,用以验证数据的准确性[15]。ICP-OES 测定Pb、Cd、Hg、As 等4种元素的检出限分别为0.01、0.01、0.02、0.05 μg·L−1。
1.4 重金属污染评价方法
底泥重金属污染评价方法很多,地积累指数法[16]与潜在生态危害指数法[17]因简单易行而被广泛应用[3]。地积累指数法能直观的判定重金属污染级别,但该法侧重单一金属元素,潜在生态危害指数法能够综合反映底泥中重金属对生态环境的影响,但其生物毒性加权系数存在主观性,因此将地积累指数(Igeo)和生态危害指数(RI)相互补充进行风险评价更为合理[3, 5]。
南四湖流域原为黄河泛滥平原,本文综合考虑黄河干流底泥和南四湖流域未受污染土壤的化学元素含量选取湖泊底泥中元素分析的环境背景值[3, 18]。参照相关研究,各重金属生物毒性响应因子分别为: Pb5、 Cd30、 Hg30、As10[3, 19]。
2. 结果与讨论(Results and Discussion)
2.1 底泥重金属形态的垂向分布
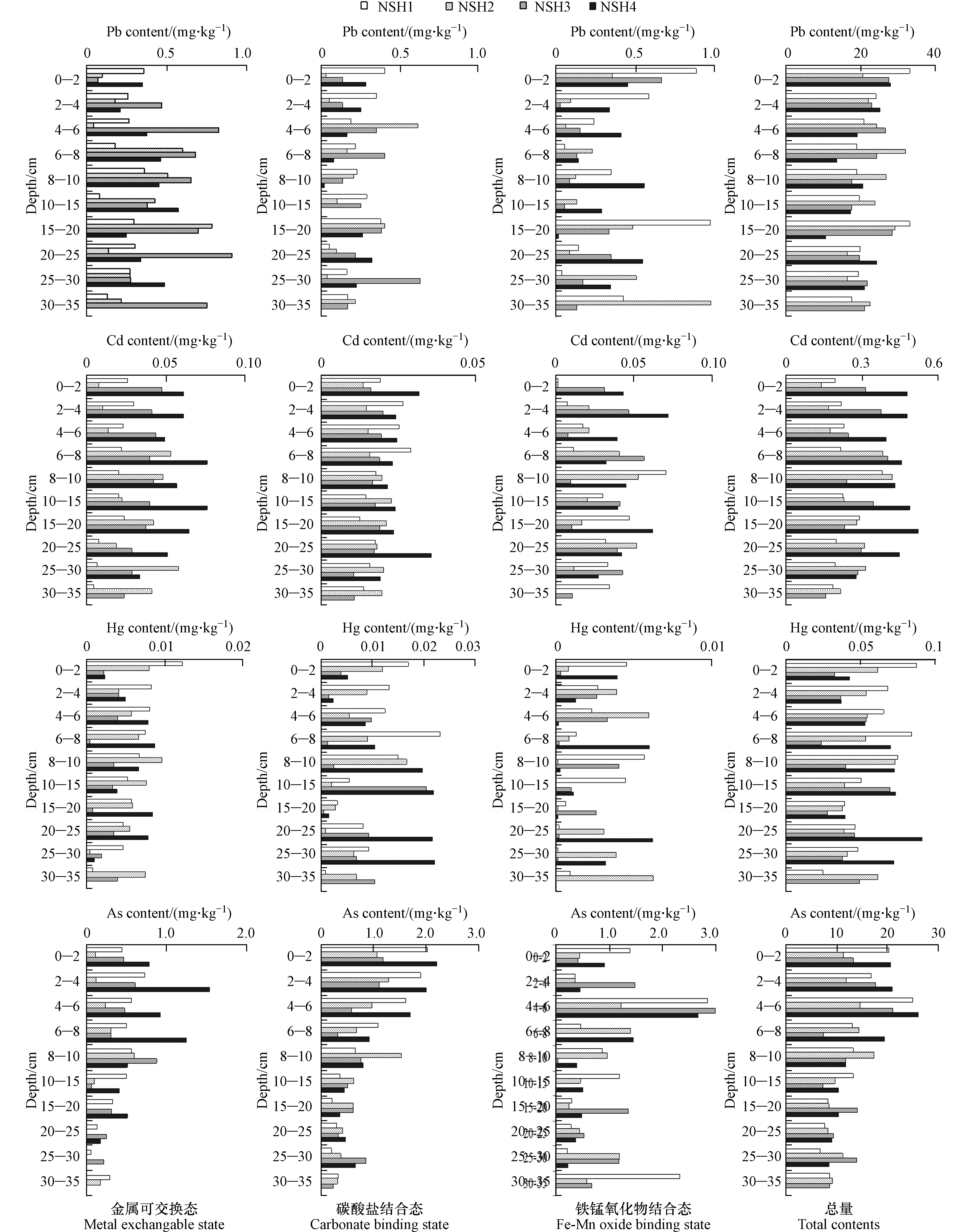
底泥重金属中的金属可交换态和碳酸盐结合态因其生物有效性大,能够更直接的反映底泥重金属的赋存现状与风险;铁锰氧化物比表面积大,吸附重金属能力强,在特定年份受铁锰浓度及重金属污染影响而沉积在相应层次中,铁锰氧化物结合态能反映出沉积各层对应年份的外源污染状况[20-21]。南四湖4个湖区采样点底泥典型重金属Pb、Cd、Hg、As的金属可交换态、碳酸盐结合态和铁锰氧化物结合态含量及总量的垂向分布见图2。重金属在底泥的垂向分布特征可反映某一历史时段内湖泊流域自然和人为活动所造成的重金属流失与污染强度,由图2可见,南四湖的4个湖区不同采样点典型重金属形态与含量在垂向分布上差异较大,各元素各形态未表现出一致的变化规律,说明各湖区采样点典型重金属近年来的污染状况亦有所差异。
4个湖区采样点Pb的金属可交换态、碳酸盐结合态、铁锰氧化物结合态含量较低,且差异不大,都在1 mg·kg−1的范围内波动,各形态仅占Pb总量的2%左右,底泥Pb的潜在风险相对较小。垂向上,南阳湖区采样点Pb的3种形态和总量有较为一致的变化趋势,即随深度增加呈波动下降,但存在15—20 cm处的相对高值,表明南阳湖区Pb在该层年份污染较重,而且近几年污染未有明显降低,南四湖东部地区是我国重要的煤田能源基地,煤炭燃烧过程和冶金、电镀等工业产生的大量废水是底泥Pb的主要来源[22]。独山湖和昭阳湖采样点表层底泥Pb的金属可交换态与碳酸盐结合态含量较底层明显降低,Pb的总量在表层亦表现出降低趋势,表明近几年这两个湖区Pb污染有所降低;微山湖采样点Pb各形态垂向分布较为复杂,可交换态随深度增加而增加,碳酸盐结合态和铁锰氧化物结合态随深度波动较大,无明显规律,从总量上看,微山湖表层底泥Pb含量有增加趋势。总体上,随着近几年南四湖的综合治理,独山湖和昭阳湖底泥Pb污染有所降低,南阳湖和微山湖降低不明显,但南四湖底泥Pb的含量总体不高,污染风险相对较低。
南四湖各湖区采样点Cd的金属可交换态占比较高,约占总量的15%左右,说明底泥Cd具有较高的释放风险,研究表明,冶金、电镀等工业产生的大量废水和湖区周边农药与化肥的大量使用等是南四湖底泥Cd 的主要来源[22]。垂向上,各湖区差异明显,南阳湖、昭阳湖、微山湖的金属可交换态及碳酸盐结合态有随深度增加呈波动下降的趋势,而独山湖表层6 cm内该赋存形态含量明显小于下层,表明独山湖表层底泥Cd的生物有效性明显降低。铁锰氧化物结合态变化趋势可以看出,南阳湖、独山湖表层赋存含量明显小于深层底泥,表明这两个区域当前污染状况有所好转,而微山湖、昭阳湖则相反,近年表现出一定程度的污染,且波动性大。总量上,南阳湖、独山湖、昭阳湖Cd含量峰值出现在6—8 cm,微山湖Cd含量峰值出现在15—20 cm,4个湖区表层0—2 cm含量均略小于2—4 cm,这一现象也见于以上3种结合态,表明近几年湖区外源Cd污染负荷有降低趋势。
南四湖各湖区样点底泥Hg的金属可交换态和碳酸盐结合态占总量的比例在20%以上,底泥中Hg的迁移性较强,具有较大的释放风险,值得关注。垂向上,南阳湖采样点Hg的金属可交换态及碳酸盐结合态呈现出随深度增加而减小的趋势,铁锰氧化物结合态15 cm以上含量也明显高于下层,表明该湖区近几年Hg污染没有得到缓解;独山湖金属交换态与碳酸盐结合态有较为一致的变化趋势,即8—10 cm含量最高;昭阳湖三形态垂向分布规律不明显,整体各赋存形态含量要小于其他湖区。微山湖采样点金属交换态与碳酸盐结合态表层含量均较下层低,该湖区近年Hg污染有所降低。总量上,南阳湖、独山湖Hg均有随深度增大而波动减小的趋势,微山湖则相反,昭阳湖不明显,总体上,南阳湖底泥Hg污染较为严重,且近几年未见明显好转,而独山湖、昭阳湖和微山湖Hg污染有降低趋势。南阳湖位于南四湖最北段,靠近济宁市区,除城区煤炭燃烧产生大量Hg外,城区生活污水和工业废水的大量排放应亦是其Hg含量增加的主要原因[22]。
南四湖各湖区采样点As的垂向分布特征明显,除独山湖外,其他湖区金属可交换态及碳酸盐结合态均有随深度增加而呈波动减小的趋势;独山湖三种形态含量在6—8 cm层出现峰值,采样点位该层As污染曾经较重,这和当时地方大力发展水产养殖,鱼类饵料中含有微量的As有关,该湖区禁渔后,As污染有所好转,这从总量的垂向分布中亦能得到验证。总量上,虽然4个湖区采样点As有随深度增加而波动递减,但As污染峰值均出现在2—8 cm区间,说明近几年南四湖各湖区As污染开始逐步降低。
2.2 表层底泥重金属的分布与污染风险评价
表层底泥对上覆水影响最为直接,研究表明,风力等动力扰动对底泥理化指标的影响主要集中在表层0—3 cm[23-24]。本研究选择0—4 cm深度的表层底泥作为分析对象,即取0—2 cm和2—4 cm底泥重金属含量的平均值,具体结果见表1。从表1可见,Pb、Cd、Hg、As的4种重金属在4个湖区的含量分别为21.31—28.46、0.16—0.50、0.037—0.079和12.91—20.81 mg·kg−1,对比《土壤环境质量 农用地土壤污染风险管控标准(GB15618—2018)》,4种重金属含量均低于该标准水田风险筛选值(6.5<pH<7.5)。根据底泥富集系数法[25]对4种重金属进行污染程度评价,4种重金属的富集系数均大于1,4个湖区采样点底泥均受到不同程度的重金属污染,Cd和Hg富集最明显,其次为As和Pb。4个湖区采样点Cd富集系数均在2以上,其中以微山湖污染最为突出,富集系数达到6.44,为显著污染,其次是昭阳湖、南阳湖和微山湖,富集系数依次为3.95、3.03和2.07,均为中度污染。4个湖区采样点Hg污染程度也较重,富集系数均在2以上,污染大小顺序为南阳湖>独山湖>微山湖>昭阳湖,南阳湖富集系数为5.26,为显著污染。各采样点As污染程度由高到低依次为微山湖、南阳湖、昭阳湖和独山湖,微山湖富集系数为2.78,为中度污染。南阳湖Pb的富集最明显,富集系数为1.9,然后依次是微山湖、昭阳湖和独山湖,均为无—弱污染等级。总体上,底泥富集系数法显示,南四湖底泥典型重金属Hg、Cd、As和Pb均有一定程度污染,污染较重的区域为南阳湖和微山湖,独山湖和昭阳湖相对较轻,这与刘良等的研究结果一致[11]。
表 1 南四湖表层底泥(0—4 cm)重金属含量及富集系数Table 1. Heavy metal contents and enrichment factors in surface sediments (0—4 cm) of Nansi Lake项目 Project Pb Cd Hg As 南阳湖 含量/(mg·kg−1) 28.46±4.17 0.23±0.01 0.079±0.011 18.64±2.01 富集系数 1.90 3.03 5.26 2.49 污染程度 无—弱污染 中度污染 显著污染 中度污染 独山湖 含量/(mg·kg−1) 21.31±0.89 0.16±0.02 0.058±0.007 12.91±0.29 富集系数 1.42 2.07 3.87 1.72 污染程度 无—弱污染 中度污染 中度污染 无—弱污染 昭阳湖 含量/(mg·kg−1) 25.14±3.86 0.30±0.03 0.037±0.019 15.50±1.84 富集系数 1.68 3.95 2.43 2.07 污染程度 无—弱污染 中度污染 中度污染 中度污染 微山湖 含量/(mg·kg−1) 26.51±1.28 0.50±0.01 0.041±0.003 20.81±3.02 富集系数 1.77 6.44 2.72 2.78 污染程度 无—弱污染 显著污染 中度污染 中度污染 农用地土壤污染风险管控标准值(水田,6.5<pH<7.5) 140 0.6 0.6 25 环境背景值/(mg ·kg−1) 15 0.077 0.015 7.5 注:富集系数为底泥重金属含量同环境背景值的比值. Note: Enrichment coefficient is the ratio of sediment heavy metal contents to environmental background values. 通过相关公式[26]计算出的南四湖各采样点表层底泥(0—4 cm)重金属地积累指数Igeo和潜在生态风险因子Ei、生态风险指数RI结果见表2。由表2看出,根据地积累指数Igeo进行评价,南四湖4个湖区表层底泥普遍受到Hg、Cd、As污染,Pb相对较轻。昭阳湖和微山湖Cd污染较重,分别达到中等污染和中-强污染等级,其中微山湖最严重,南阳湖和独山湖Cd污染相对较轻,为轻-中等级。南阳湖Hg污染最为突出。As在4个湖区均为轻-中污染水平,独山湖最轻。Pb污染独山湖最轻,其他3个湖区均为轻-中污染等级,其中南阳湖最重。
表 2 南四湖表层底泥(0—4 cm)重金属地积累指数Igeo及潜在生态风险指数RITable 2. The index of geoaccumulation (Igeo) and potential ecological risk index (RI) of heavy metals in surface sediments (0—4 cm) of Nansi Lake区域District 潜在生态风险因子EiPotential ecological risk index Ei RI 地积累指数IgeoIndex of geoaccumulation Igeo Pb Cd Hg As Pb Cd Hg As 南阳湖 9.49 80.93 156.44 24.85 272.97 0.34 0.85 1.80 0.73 轻微 强 强 轻微 重污染 轻—中 轻—中 中 轻—中 独山湖 7.10 59.88 115.40 15.61 199.09 −0.08 0.41 1.36 0.06 轻微 中 强 轻微 中等污染 无 轻—中 中 轻—中 昭阳湖 8.38 134.61 69.15 20.67 233.88 0.16 1.58 0.62 0.46 轻微 强 中 轻微 中等污染 轻—中 中 轻—中 轻—中 微山湖 8.84 186.95 80.41 27.75 304.99 0.24 2.05 0.84 0.89 轻微 很强 强 轻微 重污染 轻—中 中—强 轻—中 轻—中 从潜在生态风险因子评价可以看出,4种元素在4个湖区的污染风险等级与地积累指数法得到的污染等级较为接近,但因引入了生物毒性响应因子,生物毒性较强的元素污染风险等级较地积累指数法的污染等级高,说明潜在生态危害指数法更注重污染对生态的危害,同时,生物毒性加权系数亦具有一定的主观性。从表2中Ei看出,4个湖区采样点都明显受到Hg和Cd的污染,为中—强污染风险等级,As、Pb相对较轻,为轻微生态污染风险等级。具体来看,南阳湖区Hg污染风险最强,微山湖Cd污染风险最强,均达到很强等级。从潜在生态风险指数RI看,南阳湖、微山湖达到了重污染生态风险等级,其中Hg和Cd分别是最主要的生态风险贡献因子,昭阳湖、独山湖为中等污染生态风险强度,各湖区污染风险强度大小顺序表现为:微山湖>南阳湖>昭阳湖>独山湖。这与孟祥华等[10]和刘良等[11]的研究基本一致,但也有差异,主要在于微山湖重金属Cd污染因子的贡献加大。另外,底泥中重金属元素各形态组成差异较大,各形态迁移转化能力不同,评价时综合考虑以上因素,才能对其生态风险做出更科学的评价[27],由各湖区底泥Pb、Cd、Hg、As的形态分析得知,南阳湖和独山湖区Cd和Hg的金属可交换态、碳酸盐结合态、铁锰氧化物结合态含量占比分别高达36%和33%,具有较高的迁移性,存在生态风险相对较大,应予以重视。
2.3 底泥重金属稳定度评价
底泥中重金属的形态分布不是一成不变的,它们会随着周围环境条件的变化,如:水体温度、pH、底泥有机质和外源重金属等的改变而发生转化[6]。基于重金属可交换态最易被生物利用,毒性最强,碳酸盐结合态也较易重新释放进入水相的特点,很多学者用底泥中金属可交换态及碳酸盐结合态重金属占重金属总量的百分数来评价底泥中重金属的稳定程度[6, 9]。本文采用该法得到的南四湖各湖区表层0—4 cm底泥重金属的稳定度(SAC)见表3。由表3看出,Pb、Cd、Hg、As等4种重金属元素的稳定度差异较大,Hg、Cd、As的稳定性较小,Pb相对比较稳定。结合表1重金属富集系数及表2重金属污染评价发现,重金属的稳定性评价与总量污染评价有一定相关性,但并不一致,如微山湖Cd富集系数为6.44,南阳湖为3.03,微山湖Cd污染要明显重于南阳湖,但其稳定度(18.6%)却明显小于南阳湖(25.0%),说明南阳湖底泥Cd中金属可交换态和碳酸盐结合态占比更高、更活跃,对湖泊水环境的变化更敏感,释放风险亦更大 [28]。4个湖区Pb虽然受到一定程度的污染,但考虑到稳定度,其二次释放潜力较小,潜在生态危害并不高。Hg在南阳湖采样点最不稳定,稳定度大小顺序为昭阳湖>微山湖>独山湖>南阳湖。4个湖区各采样点As稳定度均为中等稳定,大小顺序为昭阳湖>独山湖>南阳湖>微山湖,其中,微山湖最不稳定。
表 3 南四湖各采样点表层底泥(0—4 cm)重金属稳定程度Table 3. The stable risks of heavy metals in surface sediment (0—4 cm) of Nansi Lake区域District Pb Cd Hg As 南阳湖 SAC 2.4% 25.0% 32.7% 13.6% 分级 稳定 中等稳定 不稳定 中等稳定 独山湖 SAC 0.8% 14.9% 28.6% 11.0% 分级 极稳定 中等稳定 中等稳定 中等稳定 昭阳湖 SAC 1.6% 18.1% 16.9% 10.9% 分级 稳定 中等稳定 中等稳定 中等稳定 微山湖 SAC 2.1% 18.6% 18.6% 15.7% 分级 稳定 中等稳定 中等稳定 中等稳定 3. 结论(Conclusion)
(1)底泥富集系数法显示,典型重金属Pb、Cd、Hg、As在南四湖4个湖区表层底泥(0—4 cm)中富集系数均大于1,均受到不同程度的污染,其中,Cd、Hg富集最为明显,其次为As和Pb,4个湖区采样点表层底泥污染较重的为南阳湖和微山湖,独山湖和昭阳湖相对较轻。
(2)南四湖4个湖区采样点Pb的金属可交换态、碳酸盐结合态、铁锰氧化物结合态含量较低,在1 mg·kg−1的范围内波动,约占Pb总量的2%左右,潜在风险较小,Cd的金属可交换态占比较高,约占总量的15%左右,Hg的金属可交换态和碳酸盐结合态占总量的比例在20%以上,Hg和Cd的潜在风险较大。垂向分布上,4个湖区各重金属形态差异较大,无明显规律,有的随深度增加而波动下降,如As在南阳湖、昭阳湖和微山湖的垂向分布,总体上,除南阳湖表层底泥Hg含量外,其他湖区采样点表层底泥Cd、Hg、As含量均下降,近几年南四湖各湖区重金属污染有降低趋势。
(3)地积累指数评价结果显示,南四湖4个湖区采样点表层底泥普遍受到Hg、Cd、As污染,Pb污染相对较轻。微山湖Cd污染最重,南阳湖Hg污染最为突出,As在4个湖区均为轻—中污染水平,独山湖污染最轻。从潜在生态风险指数RI看出,南阳湖、微山湖为重污染生态风险强度,昭阳湖、独山湖为中等污染风险强度,污染风险程度大小顺序为:微山湖>南阳湖>昭阳湖>独山湖。
(4)南四湖各采样点表层底泥Pb、Cd、Hg、As的稳定度差异较大,其中,Hg、Cd、As稳定性较小,Pb最为稳定。4个湖区Cd均为中等稳定,稳定度大小顺序为独山湖>昭阳湖>微山湖>南阳湖。Hg在南阳湖最不稳定,各湖区大小顺序为昭阳湖>微山湖>独山湖>南阳湖。As的稳定度大小为昭阳湖>独山湖>南阳湖>微山湖。综合比较,南阳湖区底泥Hg污染应引起足够重视。
-
表 1 MCs和ANTXs对生菜生物量、MDA、H2O2和O2·-含量的复合影响
Table 1. Combined effects of MCs and ANTXs on biomass and contents of MDA, H2O2 and O2·- in lettuce leaves
处理组Treatments 浓度/(µg·L−1)Concentration FW/g MDA/(µmol·g−1 FW) H2O2/(µg·g−1 FW) O2·−/(µg·g−1 FW) CK 0 20.772±1.292c 0.74±0.06d 6.27±0.74e 4.18±0.07c MCs 5 36.415±1.290a 0.75±0.06d 5.50±0.44e 4.25±0.14c 100 15.093±0.791d 1.57±0.13a 15.83±0.66a 10.71±0.98a ANTXs 5 38.552±0.888a 0.73±0.12d 5.47±0.29e 4.86±0.11c 100 19.720±1.764c 1.24±0.10b 10.06±0.61c 8.57±0.53b MCs+ANTX 5+5 33.913±1.158b 0.89±0.03c 8.83±1.00d 4.78±0.26c 100+100 17.283±0.983d 1.37±0.08b 11.31±0.47b 8.97±0.49b 注:不同字母表示各处理组间差异显著(P<0.05). Note: Different letters represent significant differences between treatments (P<0.05). 表 2 MCs和ANTXs对生菜ROS稳态影响的复合作用特征分析
Table 2. Characteristic analysis on combined effects of MCs and ANTXs on homeostasis of ROS in lettuce
指标Index MCs/(µg·L−1) A/% ANTXs/(µg·L−1) B/% MCs+ANTXs/(µg·L−1) C/% Cexp/% RI FW 5 −75.31 5 −85.60 5+5 −63.27 −225.36 0.28* 100 27.34 100 5.06 100+100 16.80 31.02 0.54* MDA 5 −2.22 5 1.31 5+5 −28.44 −0.88 32.44* 100 −113.39 100 −68.59 100+100 −85.52 −259.74 0.33* H2O2 5 12.24 5 12.77 5+5 −40.95 23.45 −1.75* 100 −152.58 100 −60.54 100+100 −80.44 −305.49 0.26* O2·− 5 −1.63 5 −16.11 5+5 −14.13 −18.01 0.79* 100 −155.90 100 −104.75 100+100 −114.31 −423.96 0.27* NADPH 5 5.25 5 1.38 5+5 −8.09 6.56 −1.23* 100 −81.90 100 −45.44 100+100 −62.80 −164.55 0.38* SOD 5 −20.59 5 −4.22 5+5 −16.42 −25.67 0.64* 100 −94.40 100 −32.65 100+100 −76.28 −157.86 0.48* CAT 5 2.18 5 1.72 5+5 −4.43 3.87 −1.15* 100 −66.98 100 −18.99 100+100 −49.37 −98.69 0.50* FRAP 5 −70.13 5 −86.76 5+5 −87.78 −217.73 0.40* 100 26.41 100 −17.14 100+100 11.89 13.80 0.86* 注:数据为平均值±标准误差,*代表与1之间的显著性(P<0.05). Note: The data is denoted as mean±standard deviation, * represents the significance between RI and 1 (P<0.05). -
[1] ZHANG Y F, LIANG J, ZENG G M, et al. How climate change and eutrophication interact with microplastic pollution and sediment resuspension in shallow lakes: A review [J]. The Science of the Total Environment, 2020, 705: 135979. doi: 10.1016/j.scitotenv.2019.135979 [2] INGRID C, MARTIN W. Toxic cyanobacteria in water: A guide to their public health consequences, monitoring and management [M]. CRC Press, 2021. [3] RELLÁN S, OSSWALD J, SAKER M, et al. First detection of anatoxin-a in human and animal dietary supplements containing cyanobacteria [J]. Food and Chemical Toxicology, 2009, 47(9): 2189-2195. doi: 10.1016/j.fct.2009.06.004 [4] SVIRČEV Z, LALIĆ D, BOJADŽIJA SAVIĆ G, et al. Global geographical and historical overview of cyanotoxin distribution and cyanobacterial poisonings [J]. Archives of Toxicology, 2019, 93(9): 2429-2481. doi: 10.1007/s00204-019-02524-4 [5] CHEN W, JIA Y L, LI E H, et al. Soil-based treatments of mechanically collected cyanobacterial blooms from Lake Taihu: Efficiencies and potential risks [J]. Environmental Science & Technology, 2012, 46(24): 13370-13376. [6] AI Y H, LEE S, LEE J. Drinking water treatment residuals from cyanobacteria bloom-affected areas: Investigation of potential impact on agricultural land application [J]. The Science of the Total Environment, 2020, 706: 135756. doi: 10.1016/j.scitotenv.2019.135756 [7] LIANG C J, WANG W M, WANG Y. Effect of irrigation with microcystins-contaminated water on growth, yield and grain quality of rice (Oryza sativa) [J]. Environmental Earth Sciences, 2016, 75(6): 1-10. [8] GU Y F, LIANG C J. Responses of antioxidative enzymes and gene expression in Oryza sativa L and Cucumis sativus L seedlings to microcystins stress [J]. Ecotoxicology and Environmental Safety, 2020, 193: 110351. doi: 10.1016/j.ecoenv.2020.110351 [9] ZHU J Z, REN X Q, LIU H Y, et al. Effect of irrigation with microcystins-contaminated water on growth and fruit quality of Cucumis sativus L. and the health risk [J]. Agricultural Water Management, 2018, 204: 91-99. doi: 10.1016/j.agwat.2018.04.011 [10] LIANG C J, MA X D, LIU H Y. Effect of microcystins at different rice growth stages on its yield, quality, and safety [J]. Environmental Science and Pollution Research, 2021, 28(11): 13942-13954. doi: 10.1007/s11356-020-11642-x [11] ZHANG Y Y, WHALEN J K, SAUVÉ S. Phytotoxicity and bioconcentration of microcystins in agricultural plants: Meta-analysis and risk assessment [J]. Environmental Pollution, 2021, 272: 115966. doi: 10.1016/j.envpol.2020.115966 [12] KAMINSKI A, BOBER B, CHRAPUSTA E, et al. Phytoremediation of anatoxin-a by aquatic macrophyte Lemna trisulca L [J]. Chemosphere, 2014, 112: 305-310. doi: 10.1016/j.chemosphere.2014.04.064 [13] LIN Y F, LIN H T, ZHANG S, et al. The role of active oxygen metabolism in hydrogen peroxide-induced pericarp browning of harvested longan fruit [J]. Postharvest Biology and Technology, 2014, 96: 42-48. doi: 10.1016/j.postharvbio.2014.05.001 [14] 孙亮亮. 镧对拟南芥种子萌发和早期根系发育影响的生理与分子机制研究[D]. 太谷: 山西农业大学, 2018. SUN L L. Physiological and molecular mechanisms of La on seed germination and early root development of Arabidopsis thaliana[D]. Taigu: Shanxi Agricultural University, 2018(in Chinese).
[15] MARTENS S. Handbook of cyanobacterial monitoring and cyanotoxin analysis [J]. Advances in Oceanography and Limnology, 2017, 8(2): 242. [16] 张清航, 张永涛. 植物体内丙二醛(MDA)含量对干旱的响应 [J]. 林业勘查设计, 2019(1): 110-112. doi: 10.3969/j.issn.1673-4505.2019.01.052 ZHANG Q H, ZHANG Y T. Study on response to drought stress of MDA content in plants [J]. Forest Investigation Design, 2019(1): 110-112(in Chinese). doi: 10.3969/j.issn.1673-4505.2019.01.052
[17] 曹翠玲, 麻鹏达. 植物生理学教学实验指导[M]. 杨凌: 西北农林科技大学出版社, 2016. CAO C L, MA P D. Experimental Study on plant Physiology teaching [M]. Yangling: Northwest A&F University Press, 2016(in Chinese).
[18] KUMAR A, PRASAD M N V, MOHAN MURALI ACHARY V, et al. Elucidation of lead-induced oxidative stress in Talinum triangulare roots by analysis of antioxidant responses and DNA damage at cellular level [J]. Environmental Science and Pollution Research, 2013, 20(7): 4551-4561. doi: 10.1007/s11356-012-1354-6 [19] 关美艳. 一氧化氮清除系统在拟南芥应答镉胁迫过程中的作用及其机制[D]. 杭州: 浙江大学, 2018. GUAN M Y. The mechanisms of nitric oxide scavenging systems in regulating Arabidopsis response to cadmium stress[D]. Hangzhou: Zhejiang University, 2018(in Chinese).
[20] ZHANG B J, BU J J, LIANG C J. Regulation of nitrogen and phosphorus absorption by plasma membrane H+ ATPase in rice roots under simulated acid rain [J]. International Journal of Environmental Science and Technology, 2017, 14(1): 101-112. doi: 10.1007/s13762-016-1125-x [21] STOJNIĆ S, KOVAČEVIĆ B, KEBERT M, et al. Genetic differentiation in functional traits among wild cherry (Prunus avium L. ) half-sib lines [J]. Journal of Forestry Research, 2022, 33(3): 991-1003. doi: 10.1007/s11676-021-01390-0 [22] 顾艳芳, 邓媛, 梁婵娟. 微囊藻毒素对黄瓜幼苗抗氧化酶及其同工酶的影响 [J]. 环境化学, 2020, 39(12): 3402-3409. GU Y F, DENG Y, LIANG C J. Effect of microcystins on antioxidative enzymes activities and isozymes pattern in cucumber seedlings [J]. Environmental Chemistry, 2020, 39(12): 3402-3409(in Chinese).
[23] CAO Q, STEINMAN A D, WAN X, et al. Combined toxicity of microcystin-LR and copper on lettuce (Lactuca sativa L. ) [J]. Chemosphere, 2018, 206: 474-482. doi: 10.1016/j.chemosphere.2018.05.051 [24] RASTOGI R P, SINHA R P, INCHAROENSAKDI A. The cyanotoxin-microcystins: Current overview [J]. Reviews in Environmental Science and Bio/Technology, 2014, 13(2): 215-249. doi: 10.1007/s11157-014-9334-6 [25] LIANG C J, LIU H Y. Response of hormone in rice seedlings to irrigation contaminated with cyanobacterial extract containing microcystins [J]. Chemosphere, 2020, 256: 127157. doi: 10.1016/j.chemosphere.2020.127157 [26] CHRISTENSEN V G, KHAN E. Freshwater neurotoxins and concerns for human, animal, and ecosystem health: A review of anatoxin-a and saxitoxin [J]. The Science of the Total Environment, 2020, 736: 139515. doi: 10.1016/j.scitotenv.2020.139515 [27] 杨颖丽, 安黎哲, 张立新. NaCl对小麦根质膜NADPH氧化酶活性的影响 [J]. 西北植物学报, 2006, 26(12): 2463-2467. doi: 10.3321/j.issn:1000-4025.2006.12.010 YANG Y L, AN L Z, ZHANG L X. NaCl effect on plasmalemma NADPH oxidase activity of wheat roots [J]. Acta Botanica Boreali-Occidentalia Sinica, 2006, 26(12): 2463-2467(in Chinese). doi: 10.3321/j.issn:1000-4025.2006.12.010
[28] 张腾国, 赖晶, 李萍, 等. 不同处理下油菜RbohA、RbohD基因的表达特性分析 [J]. 生态学杂志, 2019, 38(1): 173-180. doi: 10.13292/j.1000-4890.201901.024 ZHANG T G, LAI J, LI P, et al. Expression analysis of RbohA and RbohD genes in Brassica campestris under different treatments [J]. Chinese Journal of Ecology, 2019, 38(1): 173-180(in Chinese). doi: 10.13292/j.1000-4890.201901.024
[29] ZHANG J Z, WANG L H, ZHOU Q, et al. Reactive oxygen species initiate a protective response in plant roots to stress induced by environmental bisphenol A [J]. Ecotoxicology and Environmental Safety, 2018, 154: 197-205. doi: 10.1016/j.ecoenv.2018.02.020 [30] PÉREZ-CHACA M V, RODRÍGUEZ-SERRANO M, MOLINA A S, et al. Cadmium induces two waves of reactive oxygen species in Glycine max (L. ) roots [J]. Plant, Cell & Environment, 2014, 37(7): 1672-1687. [31] SHABIR H, VINAY K, VARSHA S, et al. Phytohormones and their metabolic engineering for abiotic stress tolerance in crop plants [J]. Crop Journal, 2016, 4(3): 162-176. doi: 10.1016/j.cj.2016.01.010 [32] 朱婷婷, 王彦霞, 裴丽丽, 等. 植物蛋白激酶与作物非生物胁迫抗性的研究 [J]. 植物遗传资源学报, 2017, 18(4): 763-770. doi: 10.13430/j.cnki.jpgr.2017.04.020 ZHU T T, WANG Y X, PEI L L, et al. Research progress of plant protein kinase and abiotic stress resistance [J]. Journal of Plant Genetic Resources, 2017, 18(4): 763-770(in Chinese). doi: 10.13430/j.cnki.jpgr.2017.04.020
[33] LIANG C J, ZHANG Y Q, REN X Q. Calcium regulates antioxidative isozyme activity for enhancing rice adaption to acid rain stress [J]. Plant Science, 2021, 306: 110876. doi: 10.1016/j.plantsci.2021.110876 [34] MA Y J, REN X Q, LIANG C J. Exogenous Ca2+ enhances antioxidant defense in rice to simulated acid rain by regulating ascorbate peroxidase and glutathione reductase [J]. Planta, 2021, 254(2): 41-44. doi: 10.1007/s00425-021-03679-0 [35] CHRISTINE H F, GRAHAM N. Redox sensing and signalling associated with reactive oxygen in chloroplasts, peroxisomes and mitochondria [J]. Physiologia Plantarum, 2003, 119(3): 355-364. doi: 10.1034/j.1399-3054.2003.00223.x [36] WANG Z, ZHANG J Q, LI E H, et al. Combined toxic effects and mechanisms of microsystin-LR and copper on Vallisneria Natans (Lour. ) Hara seedlings [J]. Journal of Hazardous Materials, 2017, 328: 108-116. doi: 10.1016/j.jhazmat.2016.12.059 [37] LI Q, GU P, ZHANG C, et al. Combined toxic effects of anatoxin-a and microcystin-LR on submerged macrophytes and biofilms [J]. Journal of Hazardous Materials, 2020, 389: 122053. doi: 10.1016/j.jhazmat.2020.122053 [38] 张雪薇. 铜绿微囊藻与水华鱼腥藻种间竞争机制的初步研究[D]. 南京: 南京大学, 2012. ZHANG X W. The preliminary study of the mechanism of competition between Microcystis aeruginosa and Anabaena flos-aquae[D]. Nanjing: Nanjing University, 2012(in Chinese).
-




 下载:
下载: