-
近年来,人类内分泌相关疾病的发病率不断增加引发了人们对环境内分泌干扰物(environmental endocrine disruptors,EDCs)的关注,如人体内分泌紊乱[1]、儿童肥胖[2]等。EDCs的影响可以通过该物质对雌激素受体 (estrogen receptor, ER)的激动作用来评估[3]。
对人类雌激素受体有激动作用的雌激素可以分为三类:天然雌激素(雌酮、雌二醇、雌三醇等);合成雌激素(双酚A);以及植物雌激素(金雀异黄酮、β-谷甾醇、豆甾醇等)[4]。目前大量研究已从人体血液、尿液中检测出了天然雌激素[5-7]、合成雌激素[8-9]以及植物雌激素[10-12]。还有研究检测了人从水体环境接触雌激素的风险[13]以及从中草药[14]、豆浆[15]等通过食用摄入雌激素的风险。
雌激素对ER的激动作用可以通过相对结合亲和力 (relative binding affinity, RBA)的数据进行评估,有研究通过实验确定了部分雌激素的雌激素受体相对结合亲和力 [16]。对于部分没有实验数据的物质,一些研究通过分子对接[17]或者使用QSAR建模[18]预测了雌激素受体相对结合亲和力。
本研究对雌激素进行了3D-QSAR计算,得到具有较好预测能力的CoMFA(q2=0.721,r2=0.925)和CoMSIA(q2=0.824,r2=0.961)模型。并通过使用CoMFA和CoMSIA模型预测了部分雌激素的RBA。对我国各地区的鸡饲料和鸡肉样品中的天然雌激素(雌酮、雌二醇、雌三醇等)、合成雌激素(双酚A)、植物雌激素(金雀异黄酮、β-谷甾醇、豆甾醇等)的水平进行了检测,在饲料以及肉样品中均有不同程度检出雌激素。最后利用QSAR模型预测的RBA对全国范围的鸡肉样品进行了雌激素风险评估。
-
β-谷甾醇标准品、柚皮素标准品、豆甾醇标准品、大豆苷标准品,购自ANPEL公司;香豆素标准品,购自Dr公司;香芹酚(≥95%)、麝香草酚(≥99%),购自CNW公司;金雀异黄酮(96.0%),购自TCI公司;8种激素类混标(GB31660.2-2019),购自ANPEL公司;硅烷化试剂BSTFA:TMCS=99:1,购自REGIS公司;SPE填料LC-C18(40—63 μm)、PSA(40—63 μm),购自CNW公司。
鸡饲料样品于各地购买后空运至实验室,并于室温下密封保存;鸡肉样品于各地购买后冷冻空运至实验室,并于−40 ℃冰箱保存。鸡饲料及鸡肉样品的采样点设置在我国东北地区、华北地区、华中地区、华东地区、东南地区、西南地区具有代表性的城市,分别是哈尔滨、北京、西安、上海、广州和成都.
-
采用QuEChERS法进行样品处理,在进行衍生化后进样。饲料及鸡肉用粉碎机粉碎后,作为样品待测,在室温下密封保存。处理时称取2.0 g左右样品,加入50 mL聚乙烯离心管中,向离心管中加入10 mL超纯水,于涡旋混合器上混合1 min。向离心管中加入10mL 1%乙酸+乙酸乙酯,再于涡旋混合器上混合1 min,在摇床振荡混合90 min。向振荡后的样品中加入4.0 g无水硫酸钠和1.0 g氯化钠萃取盐,于涡旋混合器上混合1 min。将离心管置于离心机中,以4000 r·min−1的转速离心10 min后,取约8 mL上清液于15 mL离心管中。向离心管中加入100 mg C18、50 mg PSA和200 mg无水硫酸钠,于涡旋混合器上混合1 min。在4 ℃冰箱静置过夜后,取5 mL上清液至10 mL样品瓶中,40 ℃氮吹至干,用100 μL BSTFA-TMCS衍生化试剂衍生处理后,转移至2 mL样品瓶中上机测定[19]。
-
使用日本岛津GCMS-QP2010气相色谱质谱联用仪进行分析,进样器为岛津AOC-6000多功能自动进样器,使用的色谱柱是Rtx-5ms气相色谱柱(30 m×0.25 mm,0.25 μm)。进样量为1 μL,电子能量70 eV,离子源温度230 ℃,进样器温度程序如下:初始温度50 °C,以8 ℃·s−1的速率升温至220 °C,保持2 min;之后以10 ℃·s−1的速率升温至280 °C,保持16 min。载气流速1 mL·min−1,扫描模式为选择离子(SIM)模式。
-
相对结合亲和力(relative binding affinity, RBA) 是通过比较测试化学品与雌二醇的IC50(抑制浓度的一半)来计算的。
其中,
ICE250 指的是雌二醇在生物测定中对ER结合产生50%抑制作用的浓度,IC50 指的是测试化学品在生物测定中对ER结合产生50%抑制作用的浓度。在本研究中,使用相对结合亲和力的对数 (log RBA)来衡量结合亲和力,活性数据来自美国EPA[20]。物质结构数据来自PubChem[21],经MarvinSketch软件处理后导入Sybyl-X 2.1.1进行QSAR计算.
-
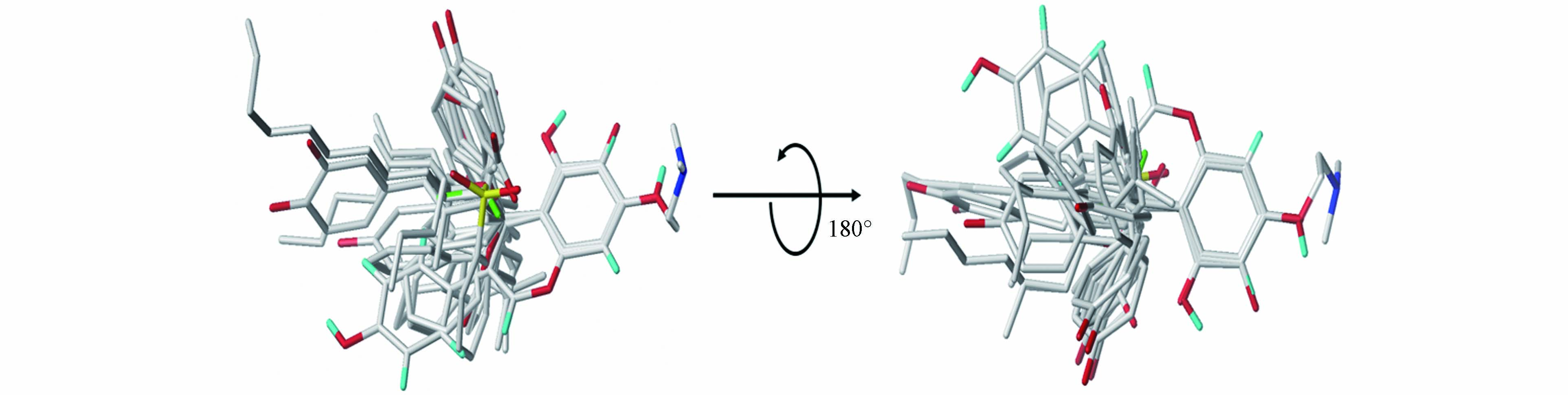
本研究首先在PubChem中搜索了1000多种雌激素结构相似化合物,其中65种化合物具有RBA实验值。从这65种化合物中选取29个能够较好分子叠合的化合物进行3D-QSAR研究,以RBA的对数表征生物活性,建立了CoMFA与CoMSIA模型。构建三维定量构效关系模型时,选用p-Cresol作为模板分子,将所有分子的苯环作为公共结构,进行分子的叠合。训练集中化合物与模板分子叠合后的构象如下图1所示。
对分子叠合后构象进行CoMFA和CoMSIA建模分析得出的各项数据如表1所示。CoMFA模型的交叉验证相关系数(q2)为0.721,非交叉验证相关系数(r2)为0.925, F检验值为64.977,说明CoMFA模型较为可靠。CoMFA立体场(S)贡献率为56.6%,静电场(E)为43.4%,因此立体场和静电场对RBA活性都有着重要的影响。CoMSIA模型的q2和r2分别是0.824和0.961, F检验值为113.157,说明CoMSIA模型较为可靠。CoMSIA模型中贡献率最高的是氢键供体场,为29.4%,空间场、静电场、疏水场、氢键受体场贡献值接近,均在16%—20%之间,因此应该综合考虑各分子场的影响。
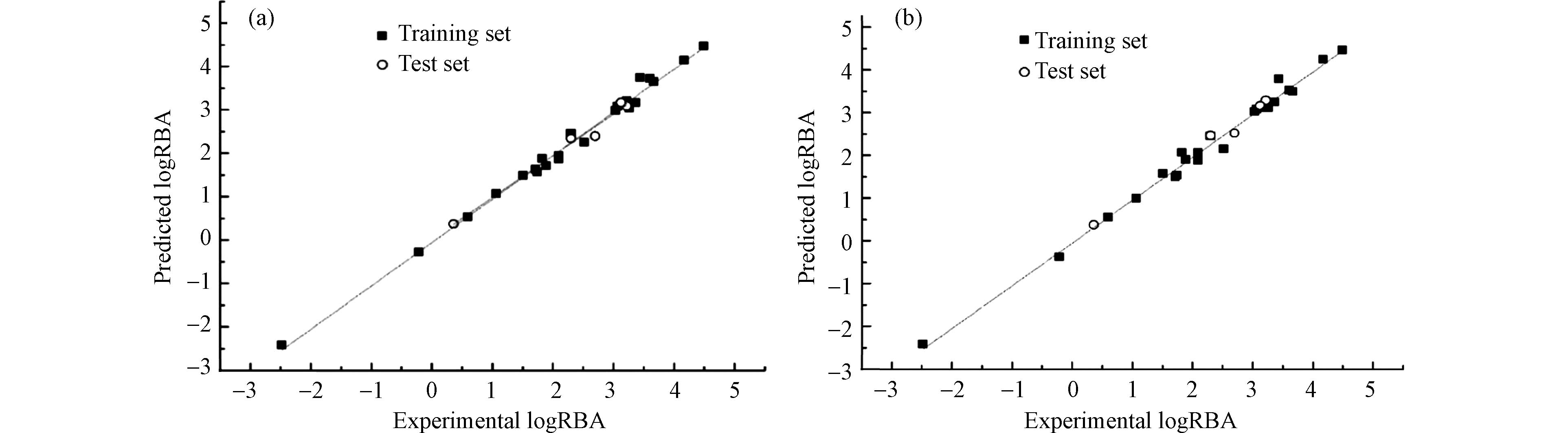
对CoMFA和CoMSIA模型预测得到的lgRBA值与RBA的实验值进行了相关性分析,得到r2分别为0.991和0.989,说明CoMFA和CoMSIA模型均具有较为良好的预测能力(图2)。
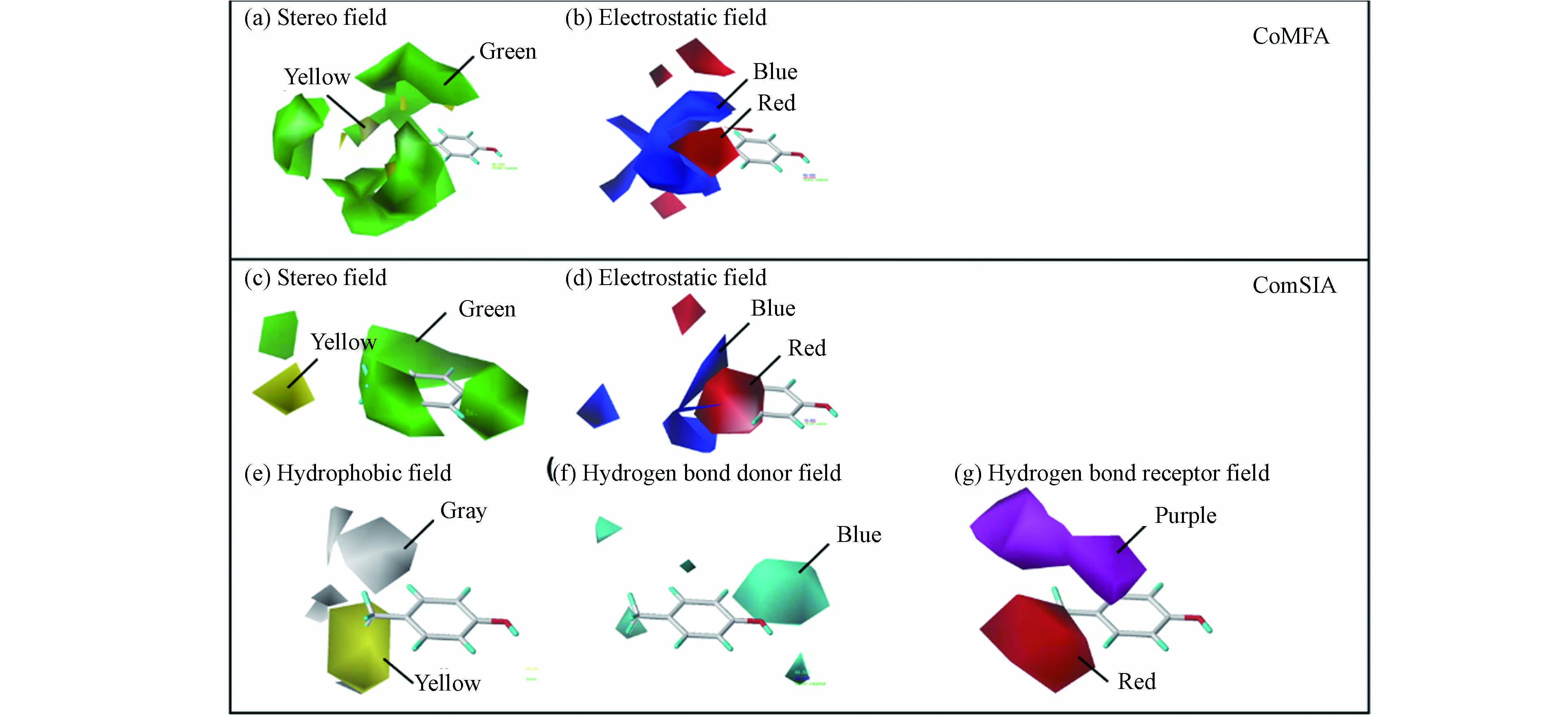
以模板分子对甲酚绘制了CoMFA和CoMSIA等值线图(图3)。CoMFA模型仅计算立体场和电子场,如图3a和b所示,a代表立体场,b代表静电场,等势线截断比为80% : 20%。立体场中,黄色代表体积增大,分子的RBA值降低;绿色代表体积增大,分子的RBA值增大。电子场中,在红色处添加带负电的基团,分子的RBA值增大;在蓝色处添加带负电的基团,分子的RBA值降低。CoMSIA模型除立体场与电子场外,还计算了疏水场、氢键供体场和氢键受体场,如图3c、d、e、f和g所示,c代表立体场,d代表静电场,e代表疏水场,f代表氢键供体场,g代表氢键受体场,等势线截断比为80% : 20%。疏水场中,黄色表示引入疏水性基团,分子的RBA值增大;灰色代表引入疏水性基团,分子的RBA值降低。氢键供体场中,蓝色代表增加氢键供体,分子的RBA值增大。氢键受体场中,紫色代表增加氢键受体,分子的RBA值增大;红色代表减少氢键受体,分子的RBA值增大。
使用该模型得到所检测的13种雌激素的RBA预测值如表2。从表2数据可知,在预测己烯雌酚、17β-雌二醇、17α-乙炔雌二醇等RBA值较高的天然雌激素时,模型预测结果较不理想,因此该模型不适用于预测RBA值较高的天然雌激素,对RBA值较低的部分植物雌激素有一定预测能力。为了使评估所用数据更为可靠,具有RBA实验值的雌激素使用实验值;无RBA实验值的雌激素使用CoMSIA预测值,因为CoMFA模型的总体预测能力略低于CoMSIA模型,β-谷甾醇的CoMSIA预测值出现了不符合常理的负值,因此使用CoMFA预测值。
-
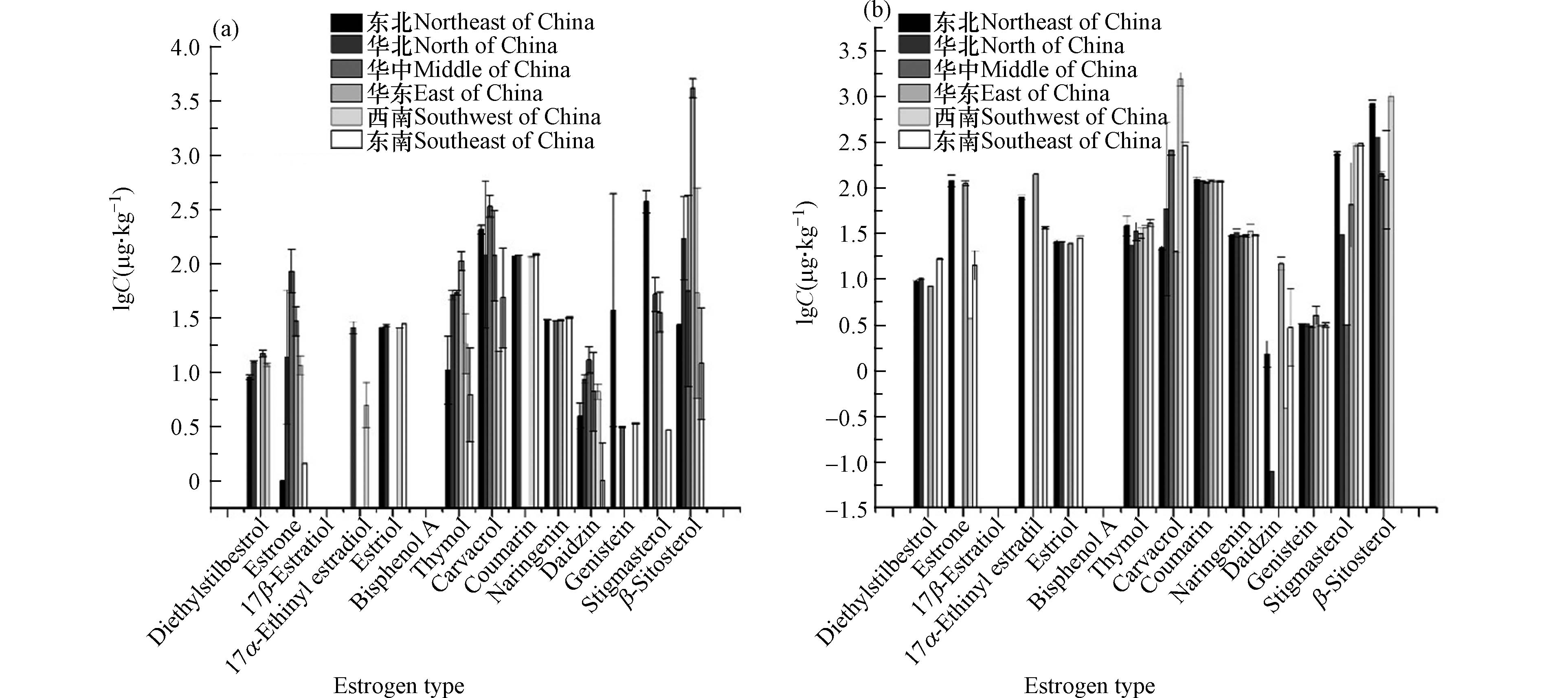
在代表我国东北地区、华北地区、华中地区、华东地区、东南地区、西南地区的鸡饲料以及鸡肉样品中均有不同程度检出天然雌激素以及植物雌激素(图4)。其中植物雌激素在鸡饲料和鸡肉中检出率较高,为69%和84%;天然雌激素在鸡饲料和鸡肉中检出率较低,为53%和50%,合成雌激素在鸡饲料和鸡肉中均未检出。利用饲料和肉中植物雌激素浓度计算得出,植物雌激素从鸡饲料到鸡肉中的生物富集系数(Biocon Centration Factor,BCF)为0.98—19.7。
-
从《2020中国卫生健康统计年鉴》中的城乡居民膳食结构以及城乡居民每人每日食物摄入量得到鸡肉的每日摄入量数据为89.7 g;参照标准人定义(体重63 kg,年龄18—45岁,从事轻体力劳动的成年男性),算出各雌激素每日暴露量如表3[21]。
一般来说,雌激素作用效应是由其浓度和雌激素效力决定的,这可以用雌激素当量(Estrogen equivalence quotient, EEQ)反映[22],计算公式如下:
其中,
RBAi 表示某个雌激素的相对结合亲和力,Ci 是鸡肉中该雌激素的浓度。各雌激素对总雌激素效应的贡献如图5。由图5可以看到,鸡饲料和鸡肉中植物雌激素所贡献的雌激素效应总量都与天然雌激素相当,因此植物雌激素的雌激素效应不可忽视。
鸡肉中雌激素风险指数的计算,参照食品中化学物质风险评估的原则和方法,计算公式如下:
其中,
RI 为环境雌激素的风险指数,E 为环境雌激素的每日暴露量,ADI 为环境雌激素的每日容许摄入量。若RI≤1 ,则说明该雌激素的暴露风险在可接受范围内;若RI>1 ,则说明该雌激素有健康风险。欧洲食品安全局(EPSA)以及世界卫生组织(WHO)给出了部分雌激素的日容许摄入量(Acceptable daily intake, ADI),17β-雌二醇为0.05 μg·kg−1·d−1,双酚A为50 μg·kg−1·d−1。其他未给出ADI的物质可通过使用EEQ转化为雌二醇当量进行估算。
通过计算得出各物质雌激素风险指数(Risk index, RI)如表4所示。由表4数据可见,东北地区的己烯雌酚和西南地区的香芹酚RI>1,值得引起重视;其余大部分地区的鸡肉可以安全食用。
-
本文以logRBA表征生物活性,对雌激素进行了3D-QSAR计算,得到具有较好预测能力的CoMFA(q2=0.721,r2=0.925)和CoMSIA(q2=0.824,r2=0.961)模型,并以此模型预测出了部分雌激素的RBA。
对代表我国东北地区、华北地区、华中地区、华东地区、东南地区、西南地区的鸡饲料以及鸡肉样品中的雌激素含量进行了检测。结果显示,植物雌激素在鸡饲料和鸡肉中检出率较高,为69%和84%;天然雌激素在鸡饲料和肌肉中检出率较低,为53%和50%,合成雌激素在鸡饲料和鸡肉中均未检出。同时通过计算得出植物雌激素从鸡饲料到鸡肉中的平均残留率为71.4%。
通过计算鸡肉中雌激素的每日暴露量以及使用雌激素的日容许摄入量,对全国范围内各地区鸡肉进行了雌激素风险评估。结果显示鸡饲料和鸡肉中植物雌激素所贡献的雌激素效应都与天然雌激素相当,因此植物雌激素的雌激素效应不可忽视。其中香芹酚、己烯雌酚、17α-乙炔雌二醇的EEQ最高,值得引起重视。各地区鸡肉的雌激素风险指数显示,东北地区的己烯雌酚和西南地区的香芹酚RI>1,值得引起重视;其余大部分地区的鸡肉可以安全食用。
雌激素的3D-QSAR模型构建及其在饲料与鸡肉中含量的测定以及对人体的影响
3D-QSAR predicts the endocrine disrupting effect of estrogen and measures and evaluates the effect of estrogen in chicken feed and chicken on the human body
-
摘要: 雌激素对人体有显著的内分泌干扰效应。本文以雌激素受体相对亲和力(relative binding affinity, RBA)作为生物活性,对雌激素进行了三维定量构效关系(3D-QSAR)计算,得到具有较好预测能力的CoMFA(交叉验证相关系数q2=0.721,非交叉验证相关系数r2=0.925)和CoMSIA(q2=0.824,r2=0.961)模型。并对国内各地区鸡肉进行了雌激素含量检测与雌激素效应评估。植物雌激素在鸡饲料和鸡肉中检出率为69%和84%;天然雌激素在鸡饲料和鸡肉中检出率为53%和50%。检测及评估结果显示绝大部分鸡肉可以安全食用,但鸡肉中含有的己烯雌酚、17α-乙炔雌二醇以及香芹酚所具有的雌激素效应值得引起重视。Abstract: Estrogen has a significant endocrine disrupting effect on the human body. In this paper, the relative binding affinity (RBA) was used as the biological activity, and the three-dimensional quantitative structure-activity relationship (3D-QSAR) calculation of estrogen was carried out. CoMFA (q2=0.721, r2=0.925) and CoMSIA (q2=0.824, r2=0.961) models with good predictive ability are obtained. The detection rates of phytoestrogens in chicken feed and chicken were 69% and 84%; the detection rates of natural estrogens in chicken feed and chicken were 53% and 50%. The results show that most chickens are safe to eat, but the estrogenic effects of diethylstilbestrol, 17α-ethinyl estradiol and carvacrol in chicken are worthy of attention.
-
Key words:
- Estrogen /
- phytoestrogens /
- 3D-QSAR /
- hormonal effects /
- evaluation
-
表 1 CoMFA和CoMSIA模型的统计参数
Table 1. Statistical parameters of CoMFA and CoMSIA models
模型Models PLS statictics ONCa q2 b Es c r2 d F e P f rp2 g CoMFA 6 0.721 0.450 0.925 64.977 0.000 0.991 CoMSIA 6 0.824 0.323 0.961 113.157 0.000 0.989 Contributions S h E i H j D k A l CoMFA 0.566 0.434 — - — CoMSIA 0.180 0.191 0.164 0.294 0.171 a 最佳主成分数. b 留一法 (LOO) 交叉验证相关系数. c 估计标准误差. d 非交叉验证相关系数. e F检验值. f r2的概率. g 测试集的预测相关系数. h 空间场. i 静电场. j H疏水场. k 氢键供体场. l 氢键受体场. a Optimum number of components. b Leave-one-out (LOO) cross-validated correlation coefficient. c Standard error of estimate. d Noncross-validated correlation coefficient. e F-test value. f Probability of r2. g Predicted correlation coefficient for the test set. h Steric field. i Electrostatic field. j Hydrophobic field. k H-bond donor field. l H-bond acceptor field. 表 2 13种雌激素的RBA实验值与预测值
Table 2. RBA experimental and predicted values of 13 estrogen
物质名称Compounds RBA 实验值Experimental value CoMFA CoMSIA 己烯雌酚 398.107 3.969 4.305 雌酮 7.244 2.034 2.433 17β-雌二醇 100 2.511 2.789 17α-乙炔雌二醇 100 1.98 2.435 雌三醇 9.772 1.878 2.663 双酚A 0.008 1.861 1.871 麝香草酚 — 9.747 3.645 香芹酚 — 4.022 4.133 香豆素 — 8.886 4.569 柚皮素 0.007 9.283 1.179 大豆苷 — 8.886 4.569 金雀异黄酮 0.437 0.368 0.374 豆甾醇 — 0.862 1.057 β-谷甾醇 — 0.484 -0.087 表 3 各地区鸡肉中雌激素每日暴露量(μg·kg−1·d−1)
Table 3. Daily exposure to estrogen in chicken meat in various regions
物质名称Compounds 东北 华北 华中 华东 西南 东南 己烯雌酚 0.013382 N.D. N.D. N.D. N.D. N.D. 雌酮 0.17143 N.D. N.D. N.D. N.D. 0.021743 17β-雌二醇 N.D. N.D. N.D. N.D. N.D. N.D. 17α-乙炔雌二醇 0.112584 N.D. N.D. N.D. N.D. 0.052181 雌三醇 0.037081 N.D. N.D. N.D. N.D. N.D. 双酚A N.D. N.D. N.D. N.D. N.D. N.D. 麝香草酚 0.056508 0.033633 0.048733 0.045679 0.052643 0.058782 香芹酚 0.031307 0.633206 0.372618 0.028756 2.245922 0.417594 香豆素 0.175107 0.17087 0.162316 0.167872 0.167255 0.167619 柚皮素 0.04352 0.046175 0.042312 0.042596 0.049038 0.04333 大豆苷 0.002276 N.D. N.D. 0.01428 N.D. 0.006006 金雀异黄酮 0.004643 N.D. 0.004314 0.005906 N.D. 0.004468 豆甾醇 0.340804 N.D. 0.000487 0.138105 0.416443 0.43459 β-谷甾醇 1.193188 N.D. 0.201398 0.355421 1.434338 N.D. N.D.,未检出 N.D., not detected. 表 4 各地区鸡肉中雌激素风险指数(RI)
Table 4. Estrogen risk index (RI) in chicken meat by region
物质名称Compounds 东北 华北 华中 华东 西南 东南 己烯雌酚 1.065483 N.D. N.D. N.D. N.D. N.D. 雌酮 0.248368 N.D. N.D. N.D. N.D. 0.031501 17β-雌二醇 N.D. N.D. N.D. N.D. N.D. N.D. 17α-乙炔雌二醇 0.011258 N.D. N.D. N.D. N.D. 0.005218 雌三醇 0.072472 N.D. N.D. N.D. N.D. N.D. 双酚A N.D. N.D. N.D. N.D. N.D. N.D. 麝香草酚 0.041194 0.024518 0.035526 0.0333 0.038377 0.042852 香芹酚 0.025879 0.523408 0.308006 0.02377 1.856479 0.345183 香豆素 0.160013 0.156141 0.148325 0.153401 0.152838 0.15317 柚皮素 6.09×10−5 6.46×10−5 5.92×10−5 5.96×10−5 6.87×10−5 6.07×10−5 大豆苷 0.00208 N.D. N.D. 0.013049 N.D. 0.005488 金雀异黄酮 0.000406 N.D. 0.000377 0.000516 N.D. 0.00039 豆甾醇 0.072046 N.D. 0.000103 0.029195 0.088036 0.091872 β-谷甾醇 0.115501 N.D. 0.019495 0.034405 0.138844 N.D. N.D.,未检出 N.D., not detected. -
[1] BOBERG J, MANDRUP K R, JACOBSEN P R, et al. Endocrine disrupting effects in rats perinatally exposed to a dietary relevant mixture of phytoestrogens [J]. Reproductive Toxicology, 2013, 40: 41-51. doi: 10.1016/j.reprotox.2013.05.014 [2] HERAS-GONZÁLEZ L, LATORRE J A, MARTINEZ-BEBIA M, et al. The relationship of obesity with lifestyle and dietary exposure to endocrine-disrupting chemicals [J]. Food and Chemical Toxicology, 2020, 136: 110983. doi: 10.1016/j.fct.2019.110983 [3] EMARA Y, FANTKE P, JUDSON R, et al. Integrating endocrine-related health effects into comparative human toxicity characterization [J]. Science of the Total Environment, 2021, 762: 143874. doi: 10.1016/j.scitotenv.2020.143874 [4] FLECK S C, CHURCHWELL M I, DOERGE D R, et al. Urine and serum biomonitoring of exposure to environmental estrogens II: Soy isoflavones and Zearalenone in pregnant women [J]. Food and Chemical Toxicology, 2016, 95: 19-27. doi: 10.1016/j.fct.2016.05.021 [5] ROBLES J, MARCOS J, RENAU N, et al. Quantifying endogenous androgens, estrogens, pregnenolone and progesterone metabolites in human urine by gas chromatography tandem mass spectrometry [J]. Talanta, 2017, 169: 20-29. doi: 10.1016/j.talanta.2017.03.032 [6] HUANG J, SUN J H, CHEN Y H, et al. Analysis of multiplex endogenous estrogen metabolites in human urine using ultra-fast liquid chromatography-tandem mass spectrometry: A case study for breast cancer [J]. Analytica Chimica Acta, 2012, 711: 60-68. doi: 10.1016/j.aca.2011.10.058 [7] ADLERCREUTZ H, KIURU P, RASKU S, et al. An isotope dilution gas chromatographic-mass spectrometric method for the simultaneous assay of estrogens and phytoestrogens in urine [J]. The Journal of Steroid Biochemistry and Molecular Biology, 2004, 92(5): 399-411. doi: 10.1016/j.jsbmb.2004.10.015 [8] FOSTER W G, KUBWABO C, KOSARAC I, et al. Free bisphenol A (BPA), BPA-Glucuronide (BPA-G), and total BPA concentrations in maternal serum and urine during pregnancy and umbilical cord blood at delivery [J]. Emerging Contaminants, 2019, 5: 279-287. doi: 10.1016/j.emcon.2019.08.002 [9] LACROIX M Z, PUEL S, COLLET S H, et al. Simultaneous quantification of bisphenol A and its glucuronide metabolite (BPA-G) in plasma and urine: Applicability to toxicokinetic investigations [J]. Talanta, 2011, 85(4): 2053-2059. doi: 10.1016/j.talanta.2011.07.040 [10] MUSTAFA A M, MALINTAN N T, SEELAN S, et al. Phytoestrogens levels determination in the cord blood from Malaysia rural and urban populations [J]. Toxicology and Applied Pharmacology, 2007, 222(1): 25-32. doi: 10.1016/j.taap.2007.03.014 [11] PRASAIN J K, ARABSHAHI A, MOORE D R II, et al. Simultaneous determination of 11 phytoestrogens in human serum using a 2 Min liquid chromatography/tandem mass spectrometry method [J]. Journal of Chromatography B, 2010, 878(13/14): 994-1002. [12] WYNS C, BOLCA S, DE KEUKELEIRE D, et al. Development of a high-throughput LC/APCI-MS method for the determination of thirteen phytoestrogens including gut microbial metabolites in human urine and serum [J]. Journal of Chromatography. B, Analytical Technologies in the Biomedical and Life Sciences, 2010, 878(13/14): 949-956. [13] 王亮, 毛茜慧, 袁守军, 等. 气相色谱-质谱联用法同时测定污水中对羟基苯甲酸酯和甾体雌激素 [J]. 环境化学, 2016, 35(1): 49-56. doi: 10.7524/j.issn.0254-6108.2016.01.2015081901 WANG L, MAO Q H, YUAN S J, et al. Simultaneous determination of parabens and steroid estrogens in sewage water using gas chromatography-mass spectrometry [J]. Environmental Chemistry, 2016, 35(1): 49-56(in Chinese). doi: 10.7524/j.issn.0254-6108.2016.01.2015081901
[14] LEE S H, JUNG B H, KIM S Y, et al. Determination of phytoestrogens in traditional medicinal herbs using gas chromatography-mass spectrometry [J]. The Journal of Nutritional Biochemistry, 2004, 15(8): 452-460. doi: 10.1016/j.jnutbio.2004.01.007 [15] BENEDETTI B, di CARRO M, MIRASOLE C, et al. Fast derivatization procedure for the analysis of phytoestrogens in soy milk by gas chromatography tandem mass spectrometry [J]. Microchemical Journal, 2018, 137: 62-70. doi: 10.1016/j.microc.2017.09.023 [16] GRAY S L, LACKEY B R. Optimizing a recombinant estrogen receptor binding assay for analysis of herbal extracts [J]. Journal of Herbal Medicine, 2019, 15: 100252. doi: 10.1016/j.hermed.2018.12.002 [17] COTTERILL J V, PALAZZOLO L, RIDGWAY C, et al. Predicting estrogen receptor binding of chemicals using a suite of in silico methods - Complementary approaches of (Q)SAR, molecular docking and molecular dynamics [J]. Toxicology and Applied Pharmacology, 2019, 378: 114630. doi: 10.1016/j.taap.2019.114630 [18] 蒙延娟, 易忠胜, 艾芳婷, 等. 基于对接的植物激素3D-QSAR和分子动力学模拟 [J]. 环境化学, 2014, 33(6): 880-890. doi: 10.7524/j.issn.0254-6108.2014.06.016 MENG Y J, YI Z S, AI F T, et al. 3D QSAR study of phytoestrogens: A combined molecular dockingand molecular dynamics simulation [J]. Environmental Chemistry, 2014, 33(6): 880-890(in Chinese). doi: 10.7524/j.issn.0254-6108.2014.06.016
[19] 胡海山, 赵淑娥, 芦慧, 等. QuEChERS-超高效液相色谱法快速测定果蔬中4种植物激素残留 [J]. 食品安全质量检测学报, 2019, 10(10): 2995-2999. doi: 10.3969/j.issn.2095-0381.2019.10.026 HU H S, ZHAO S E, LU H, et al. Rapid determination of 4 kinds of phytohormone residues in fruits and vegetables by QuEChERS-ultra performance liquid chromatography [J]. Journal of Food Safety & Quality, 2019, 10(10): 2995-2999(in Chinese). doi: 10.3969/j.issn.2095-0381.2019.10.026
[20] CompTox, U. S. Environmental Protection Agency [DB]. [2021-10-5] [21] 赵娜娜, 应力, 孙方云, 等. 温州市食品环境雌激素污染状况及风险评估 [J]. 温州医科大学学报, 2014, 44(3): 173-176. doi: 10.3969/j.issn.2095-9400.2014.03.005 ZHAO N N, YING L, SUN F Y, et al. Contamination levels of environmental estrogens in foods and risk assessment in Wenzhou [J]. Journal of Wenzhou Medical University, 2014, 44(3): 173-176(in Chinese). doi: 10.3969/j.issn.2095-9400.2014.03.005
[22] TANG Z, WAN Y P, LIU Z H, et al. Twelve natural estrogens in urines of swine and cattle: Concentration profiles and importance of eight less-studied [J]. Science of the Total Environment, 2022, 803: 150042. doi: 10.1016/j.scitotenv.2021.150042 -




 下载:
下载: