-
碘是合成甲状腺激素的必要微量元素,碘元素对于强健体魄和促进能量代谢等有重大作用[1]。研究表明,碘摄入过少或过多都会对身心健康造成危害[2-3]。碘缺乏会引起地方性克汀病等疾病,但碘过量也会导致甲状腺肿大、甲状腺肿瘤等疾病[4-5]。20世纪,缺碘问题日益突出,到1995年,我国基本实现了“全民食盐加碘”[6],随着食盐加碘的实施及人们生活水平的提高,部分地区碘过量的问题逐渐凸显,水源性高碘甲状腺肿时常发生,这已经成为了公共卫生问题[7]。1980年我国在沧州发现了水源性高碘甲状腺肿 [8],之后,诸多学者对高碘地下水进行研究,碘不易富集形成矿物,易与有机质形成络合物[9]。我国高碘地区大多分布在冲积平原区和盆地中心,其松散的沉积环境及其富含的有机质,有利于形成高碘地下水[10]。由于浅层水与中层水之间的垂向水力交替作用,造成了中层地下水中碘的富集[11]。盆地中下部黏土层原生地质有利于碘的富集[12]。弱碱性以及偏还原的环境有助于碘从沉积物释放到地下水中[13]。蒸发浓缩作用和有机质降解作用[14]等过程均使得碘在水体发生富集。地下水水动力条件也会影响碘的迁移富集 [15]。
本文通过对喀什地区地下水碘含量的空间分布特征进行研究,以期明确研究区内地下水碘的来源和形成机制,揭示不同水文地球化学过程对地下水中碘富集的影响。旨在对当地饮水安全提供科学依据,对于预防因缺碘或高碘引起的病症具有一定的现实意义。
-
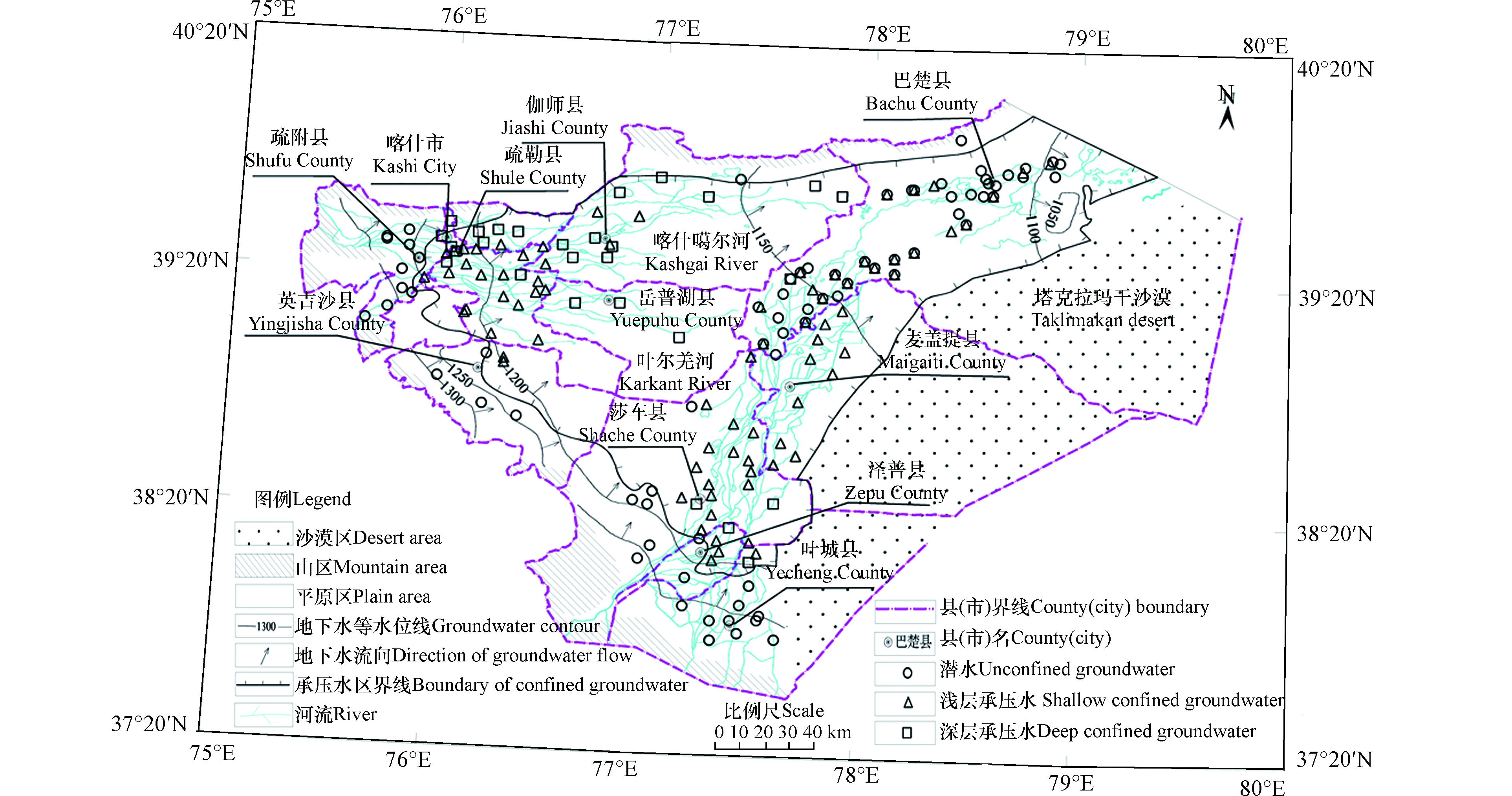
喀什地区位于新疆维吾尔自治区西南部,地势由西南向东北倾斜,西、北、南三面环山,东部向塔克拉玛干沙漠敞开的独特地形条件,形成了三角洲半封闭盆地[16]。地理坐标为75°00'—80°00'E,37°20'—40°20'N(图1),喀什地区干旱少雨,春夏有较多风沙天气,冬季气温较低,属暖温带大陆性干旱气候。研究区多年平均降水量65 mm,年平均蒸发量2100 mm,蒸降比约为32:1[17]。
单一结构潜水主要分布于研究区上游的山前倾斜冲洪积平原区,以砂砾石、粗砂为主,主要受大气降水入渗及山前侧渗等方式进行补给,水流交替条件较好。多层结构潜水-承压水分布于中下游河流冲积平原区,该含水层介质颗粒较细,以亚砂土和黏土为主,地势较为平坦,水平方向上受上游的侧向补给,垂直方向上通过地面径流、灌溉用水等方式进行补给[18]。地下水总体流向自西南向东北流动(图1)。地下水排泄方式以开采、蒸发及向下游侧向流出为主[19]。
-
地下水水样严格按《地下水环境监测技术规范(HJ/T164—2004)》进行采集、保存和送检,采样时间为2014—2017年,共采集183组地下水样,其中潜水(井深7—170 m)、浅层承压水(井深≤80 m)、深层承压水采样点(井深100—220 m)分别为76、78、29组(图1)。水样测试由新疆地矿局第二水文地质工程地质大队实验室完成,现场测定pH和水温等,实验室测定K+、Na+、Ca2+、Mg2+、Cl−、SO42−、HCO3−、I−和TDS等指标,K+、Na+和Fe采用火焰原子吸收分光光度法测定,Ca2+、Mg2+、HCO3−采用乙二胺四乙酸二钠滴定法测定,Cl−采用硝酸银容量法测定,SO42−采用硫酸钡比浊法测定,除Fe的检测下限为0.03 mg·L−1,其他指标检测下限均为0.05 mg·L−1;I−用高浓度碘化物比色法测试,I−的检测下限为0.02 mg·L−1;TDS用干燥称重法测定,检出限为0.10 mg·L−1。
-
利用SPSS软件进行组分含量描述性统计分析和因子分析,运用Grapher软件绘制Piper三线图和Gibbs图,确定水化学类型及主控因素,运用PHREEQC软件计算矿物饱和指数(SI),计算氯碱指数,明确影响碘富集的因素。
-
研究区地下水pH值范围在6.4 —8.7,整体呈弱碱性;地下水中阳离子以Na+和Ca2+为主,阴离子以SO42−和Cl−为主(表1)。水样中TDS为214.0—14548.0 mg·L−1,均值为2725.7 mg·L−1。在潜水中淡水(TDS<1 g·L−1)、微咸水(TDS为1—3 g·L−1)、咸水(TDS为3—10 g·L−1)和盐水(TDS为10—50 g·L−1)分别占总水样的23.7%、31.6%、43.4%和1.3%,在浅层承压水中分别占总水样的20.5%、39.7%、38.5%和1.3%,在深层承压水中分别占总水样的27.6%、51.7%、17.2%和3.5%。
研究区潜水、浅层承压水和深层承压水I−含量变化范围分别为ND—350.0 μg·L−1、ND—1460.0 μg·L−1和ND—220.0 μg·L−1,依据《碘缺乏病(IDD)病区划分标准(GB16005—2009)》和《水源性高碘地区和高碘病区的划定(GB/T19380—2016)》,研究区地下水分为缺碘水(≤20 μg·L−1)139组水样、适碘水(20—150 μg·L−1)33组水样、高碘水(150—300 μg·L−1)7组水样和超高碘水(>300 μg·L−1)4组水样,潜水中缺碘水、适碘水、高碘水和超高碘水占比分别为88.2%、9.2%、1.3%和1.3%,浅层承压水中缺碘水、适碘水、高碘水和超高碘水占比分别为69.2%、20.5%、6.4%和3.9%,深层承压水中缺碘水、适碘水和高碘水占比分别为62.1%、34.5%和3.4%。综上所述,喀什地区地下水缺碘水和适碘水所占比重较大,部分地下水为高碘水和超高碘水。从缺碘水来看潜水占比均高于承压水,从高碘水和超高碘水来看潜水占比低于承压水,表明潜水中碘对人体健康存在潜在危险,承压水更利于碘的富集。
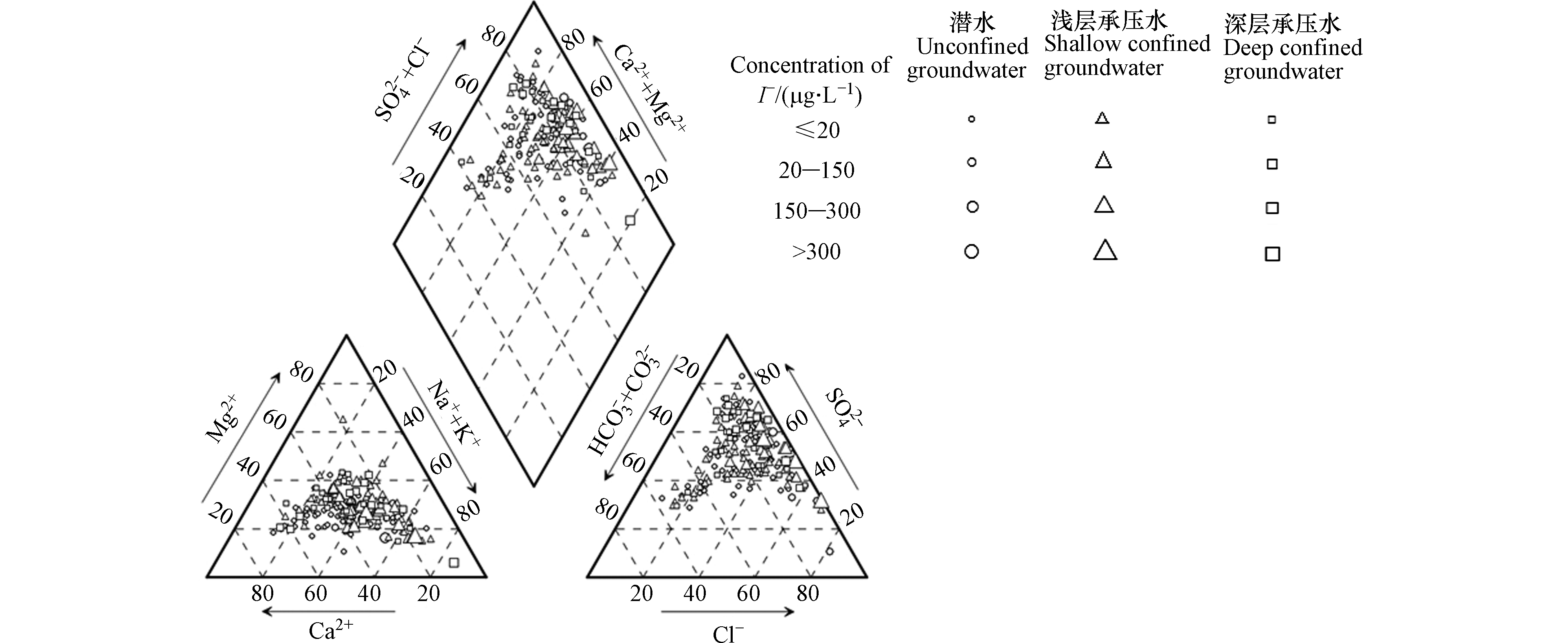
从Piper三线图(图2)中可以看出,研究区I−含量不同其水化学环境也有差异,缺碘区地下水化学类型以SO4·Cl-Na·Ca·Mg(18.0%)和SO4·Cl-Na·Ca(13.7%)为主,适碘区地下水化学类型主要为SO4·Cl-Na·Ca·Mg型(24.2%),高碘区地下水化学类型主要以SO4·Cl-Na(50.0%)和SO4·Cl-Na·Ca型(33.3%)为主,超高碘区地下水化学类型主要为SO4·Cl-Na型(25.0%)。随着碘含量的增加,地下水中Ca2+和Mg2+减少,是因为蒸发浓缩作用使溶解度小的钙、镁等重碳酸盐在水中达到饱和而率先析出。
-
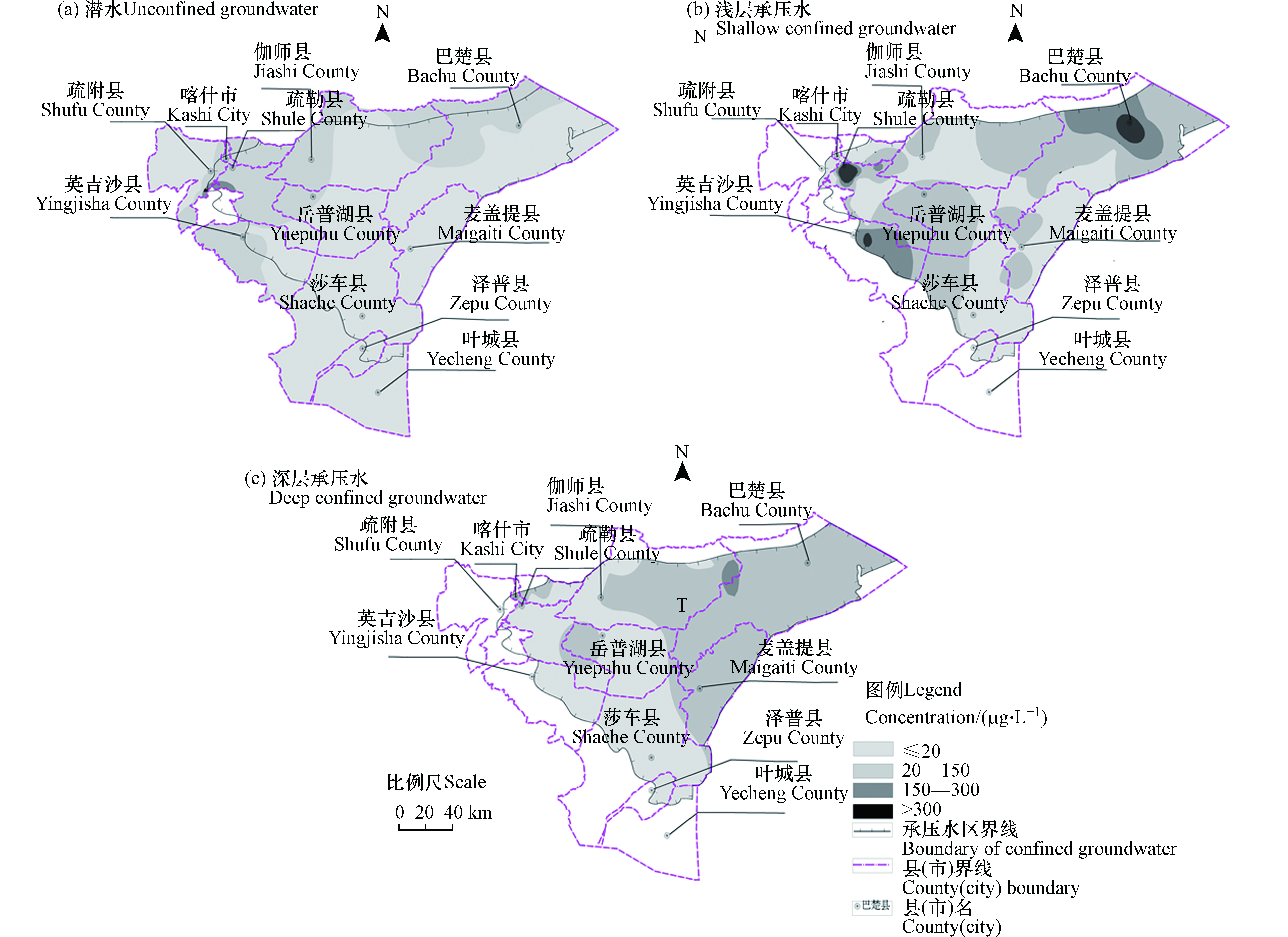
采用MAPGIS软件绘制潜水、浅层承压水和深层承压水中I−含量空间分区图来分析碘的水平分布特征,潜水中大部分为缺碘水(图3a),喀什噶尔河流域平原区中下游和英吉沙县西部等部分区域为适碘水,极少数为高碘水和超高碘水;浅层承压水中高碘水和超高碘水主要分布在巴楚县北部、喀什市西南部、英吉沙县东部,缺碘水分布在伽师县中部、莎车县东部、麦盖提县东北部,其余为适碘水(图3b);深层承压水中碘的分布呈现分带性,缺碘水主要分布在喀什噶尔河流域和叶尔羌河流域上部,而适碘水分布在其下部,另有少量高碘水分布(图3c)。
-
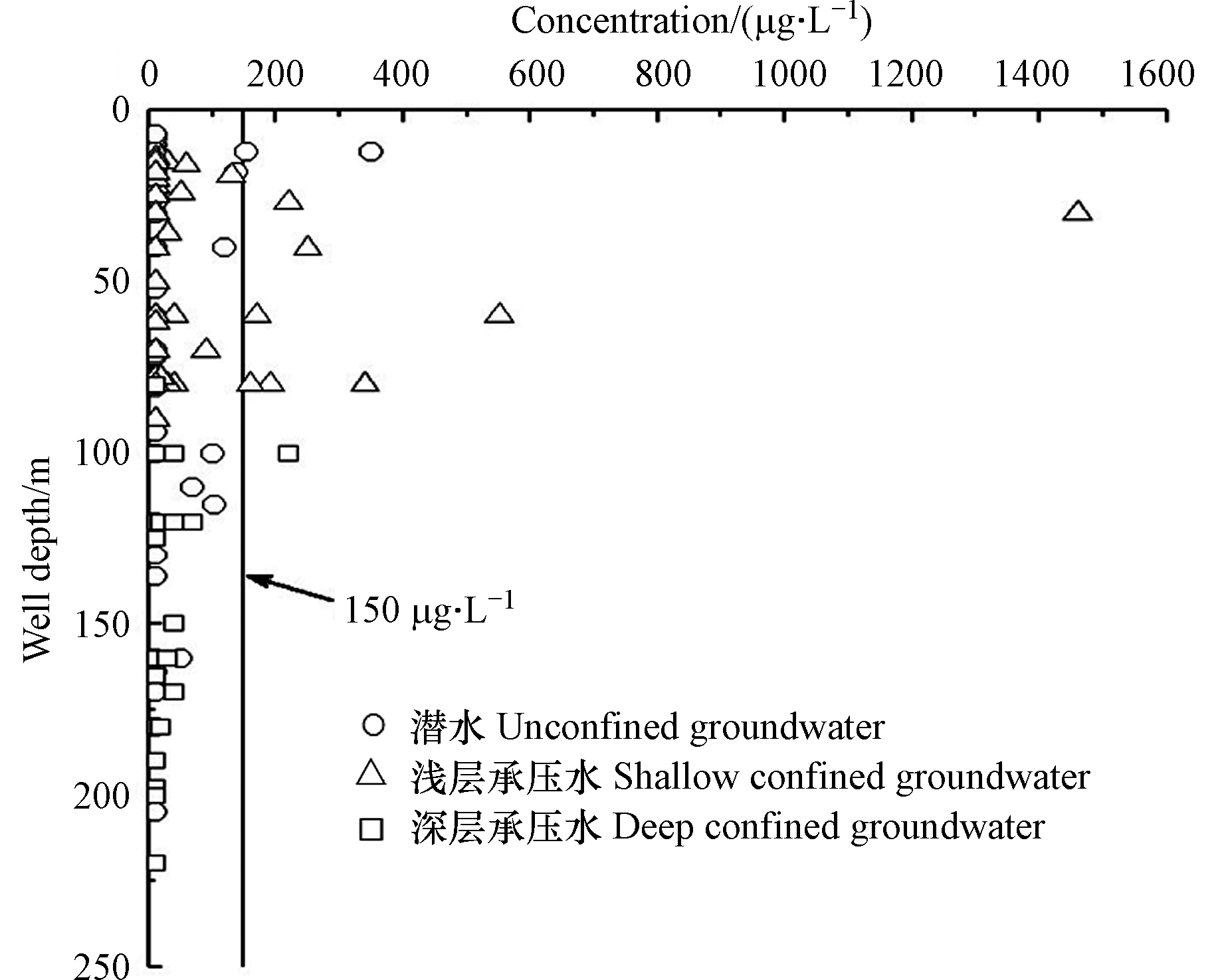
从研究区井深与I−含量关系(图4)可以看出,地下水水样的井深越大,高碘水和超高碘水所占比例越小,大多数水样的井深都<100 m,超过100 m的地下水均为缺碘水或者适碘水。垂直方向上,随着井深的增加,I−含量为先增加后减少的趋势。潜水中缺碘水(≤20 μg·L−1)的水样占比88.2%,其原因可能是山前倾斜冲洪积平原大多为潜水,该区干旱少雨,埋深较浅的潜水受蒸发岩矿物的溶滤作用,同时碘在流动较快的潜水携带下易流失,使得潜水中碘缺乏[20]。183组水样中,有11组水样I−含量>150 μg·L−1,其中,有8组水样为浅层承压水,2组为潜水,1组为深层承压水。浅层承压水中的高碘水和超高碘水远多于深层承压水,降雨的冲刷淋滤作用可使表层土壤中的碘随着地下水垂直运动作用下渗至浅层承压水中,最终使浅层地下水I−浓度较高[21]。高碘水和超高碘水垂向分布为浅层承压水>潜水>深层承压水。
-
选取研究区地下水11项指标运用SPSS软件对183组水样进行因子分析,采用主成分分析分别提取出公共因子3个(F1、F2和F3),并利用最大方差法计算旋转因子载荷。碘在F1、F2和F3中载荷分别为0.733、-0.307和-0.235,表明因子F1对碘富集影响较大。
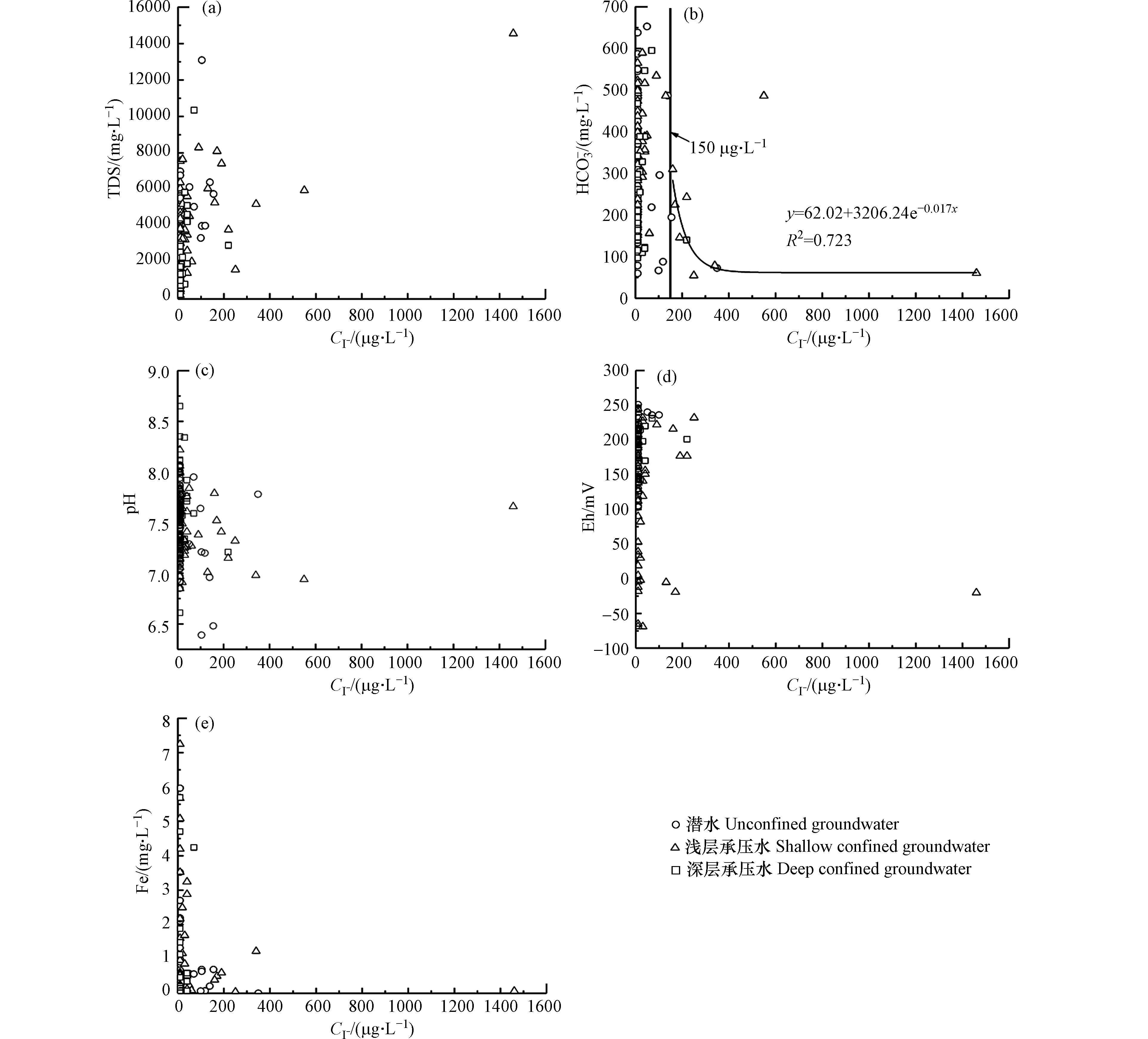
从旋转因子载荷矩阵(表2)可以看出,F1中因子载荷较高的指标为TDS、SO42−、Ca2+、Mg2+、Na+、Cl−和I−,均与F1呈正相关,且7个指标在主因子F1上的载荷均>0.75(强相关),F1因子贡献率为53.366%。地下水中的Ca2+、Mg2+主要来源于含钙镁碳酸盐的溶解,SO42−主要来源于石膏等硫酸盐的溶解,Na+和Cl−主要来源于岩盐的溶解[22],另外,当地下水位埋藏较浅时,在强烈的蒸发作用下,易形成高TDS水有利于碘的富集(图5a)。
F2中因子载荷较高的指标为HCO3−、pH和Eh,当I−含量大于150 μg·L−1时,I−随着HCO3−增大有减少趋势(图5b),表明HCO3−对I−含量的影响较大,一方面HCO3−主要来源于如方解石和白云石等含碳酸盐矿物的风化溶解;另一方面HCO3−和I−在沉积物上有竞争吸附作用[23]。研究区地下水呈中至弱碱性,pH大致范围为6.39—9.93,而高碘和超高碘地下水pH范围大约在6.48—7.79之间(图5c),说明pH在控制地下水系统中碘的分布方面有非常重要的作用,在弱碱性条件下,黏土和铁氧化物表面带有负电荷,负电荷和I−相斥,使得地下水中I−含量增加 [24]。样品的氧化还原电位为−69—260 mV(图5d),表现出弱还原状态(−50—70 mV)和氧化状态(>70 mV)。在氧化条件下,碘形态以IO3−为主,还伴有一定量的I−[25]。在还原条件下,IO3−被还原为I−,导致I−在地下水中富集[26]。
F3中因子载荷较高的指标为Fe,Fe对I−含量也有影响(图5e),在还原环境中,溶解性增强,伴随着铁氧化物的还原性溶解,赋存在其表面的I−也会进入地下水中[12]。
-
研究区有着较大的蒸降比,使得地下水通过入渗-蒸发的垂向交替运动促使碘富集。山前冲洪积平原,含水层岩性为砂砾石或粗砂,地势起伏显著,水力梯度较大,碘容易迁移,因此,多为缺碘水或适碘水[27]。中下游河流冲积平原,含水层岩性为细沙、黏土与亚砂土两层,地势较为平缓,地下径流迟缓,水力梯度相对较小,减缓了地下水中碘的移运,使地下水中碘得到富集。
-
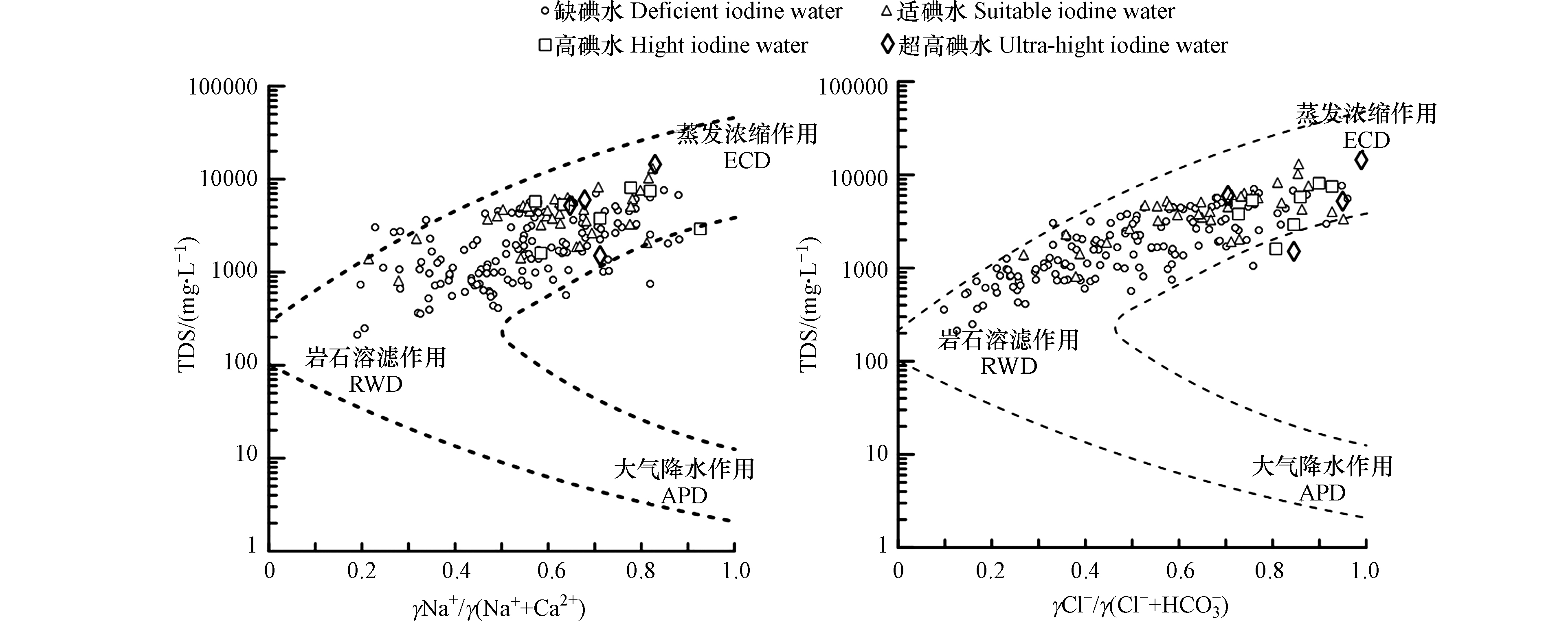
Gibbs图可以定性判断大气降水、岩石溶滤和蒸发浓缩对水化学组分的影响程度[28],当TDS值较小且阴阳离子以HCO3−和Ca2+为主,表明主要受岩石溶滤作用;当TDS以及Cl−、Na+较高时,表明主要受蒸发浓缩作用[29],由图6可看出,TDS集中在110—10000 mg·L−1,γNa+/γ(Na++Ca2+)集中在0.2—0.9,而γCl−/γ(Cl−+HCO3−)集中在0.2—1.0,主要分布在图形的中部以及右上方,表明蒸发浓缩和岩石溶滤对水化学组分影响较大。大多数缺碘水和部分适碘水主要位于山前倾斜平原补给区,受到岩石溶滤作用,该区域径流条件较好,蒸发较弱,易形成以溶滤作用为主的低TDS水,地下水中的I−在溶滤作用下溶滤淋失,使得该区域碘含量较少。而高碘水和超高碘水主要位于细土平原蒸发区,受到蒸发浓缩作用,研究区蒸发极限一般为地下水埋深5 m左右[30],该区11个高碘水和超高碘水水样中有7个样点地下水埋深小于5 m,直接受到蒸发浓缩作用的影响;4个样点地下水埋深介于5—10 m之间,降雨或农业灌溉使得埋深较浅、易受蒸发浓缩作用的潜水垂直下渗,间接影响埋深为5—10 m的地下水化学组分的形成,地下水中的I−在蒸发浓缩作用下易于富集。部分采样点落在Gibbs图之外,可能还受到阳离子交换作用的影响。
-
矿物饱和指数可判别矿物溶解或沉淀趋势,当水中矿物SI<0时,水溶液处于未饱和(矿物溶解);当SI>0时,水溶液处于饱和(矿物沉淀),当SI=0时,水溶液处于平衡[31]。运用PHREEQC软件计算矿物饱和指数可知(表3),方解石、白云石的SI范围分布为−0.77—1.94、−1.63—3.62,SI值大于0的水样占比均为90.7%,白云石和方解石难溶于水,但当地下水中有CO2时,有一定量的矿物会溶于水[32],使得地下水中Ca2+、Mg2+含量增加;当有盐类参与时,碘的吸附作用按K+>Na+>Mg2+>Ca2+和SO42−>Cl−的顺序逐步增强,随着Mg2+和Ca2+含量的增加,碘的吸附作用减弱,解吸作用增强[26]。研究区白云石和方解石发生沉淀,Mg2+和Ca2+相应减少,碘的解吸作用减弱,碘含量减少。石膏、岩盐的SI范围分布为 −1.93— −0.01和−8.36— −3.42其SI值皆小于0,说明石膏和岩盐处于溶解状态,矿物发生溶解,有利于地下水中碘的增加。
-
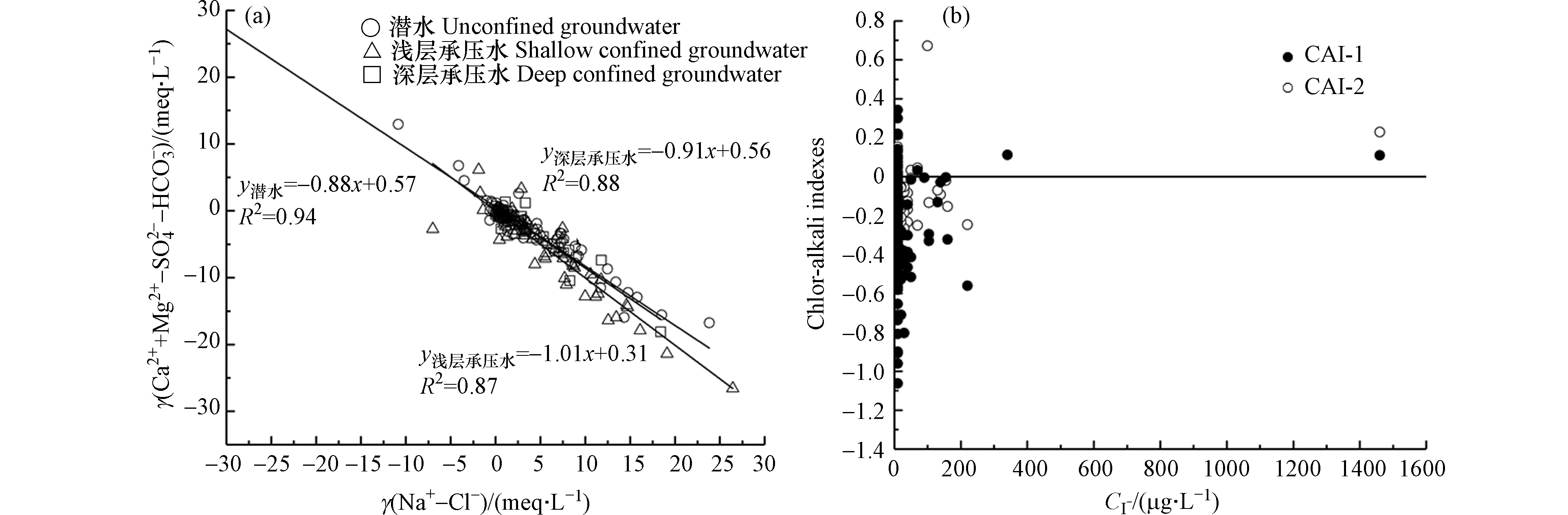
当γ(Ca2++Mg2+-SO42−-HCO3−)与γ(Na+-Cl−)的比值接近−1,表示发生了阳离子交换作用 [33]。由(图7a)可以看出潜水直线斜率为-0.88,R2=0.94;浅层承压水直线斜率为−1.01,R2=0.87;深层承压水直线斜率为−0.91,R2=0.88,说明研究区水样阳离子交换强弱为浅层承压水>深层承压水>潜水,因为承压含水层的地下水动力条件差,沉积物颗粒较细,使得阳离子交换更加明显。
利用氯碱指数(CAI-1和CAI-2)进一步分析阳离子交换作用发生的强度和方向[22],若(CAI-1和CAI-2)均为负值,表明地下水中Ca2+、Mg2+与颗粒物上的Na+发生离子交换,使得地下水中Na+含量升高,Ca2+、Mg2+含量降低[34];若两者均为正值,则反之。如(图7b)所示,绝大部分采样点CAI-1和CAI-2 均小于0,表明发生了反向阳离子交换作用,氯碱指数减小,阳离子交换作用增强,I−含量增加。
-
(1)喀什地区缺碘水和适碘水占比高于高碘水和超高碘水。缺碘水和适碘水水化学类型主要为SO4·Cl-Na·Ca·Mg型,高碘水和超高碘水水化学类型主要为SO4·Cl-Na型。水平向上缺碘水分布在喀什噶尔河流域平原区上部和叶尔羌河流域平原区上部,而适碘水分布在其下部,高碘水和超高碘水分布在巴楚县北部和英吉沙县等部分区域。垂直方向上随着井深的增加,I−含量总体上有先增加后减少的趋势,高碘水和超高碘水的垂向分布为浅层承压水>潜水>深层承压水。
(2)偏碱性、偏还原性地下水环境使得更多的I−被释放到地下水中,有利于碘的富集;地形坡度平缓、地下水动力条件差等条件减缓了地下水的移运;强烈的蒸发浓缩作用、岩盐等矿物溶解和阳离子交换作用易形成以Na+和Cl−为主的高矿化度水,进而促进地下水中碘的富集。
新疆喀什地区地下水碘的分布特征及成因分析
Distribution characteristics and cause analysis of iodine in groundwater in Kashi Prefecture, Xinjiang
-
摘要: 本文以新疆喀什地区183组地下水水质资料为基础,运用Piper三线图、因子分析、Gibbs图、饱和指数、离子比值等方法来分析地下水碘的分布特征及成因。结果表明,研究区地下水碘的匮乏与富集并存,I−含量范围为未检出—1460.0 μg·L−1;在碱性、偏还原性和富含有机质的水环境中,矿物中的碘容易以I−的形式进入到地下水中,沿地下水流向,I−逐渐从山前倾斜冲洪积平原区,向中下游河流冲积平原区富集;研究区地下水中碘主要受强烈的蒸发浓缩作用、阳离子交换作用和矿物溶解沉淀的影响。Abstract: Based on the test results of 183 groups of groundwater quality in Kashi prefecture of Xinjiang, Piper trilinear diagram, factor analysis, Gibbs diagram, saturation index and ion ratio were used to analyze the distribution characteristics and causes of groundwater iodine. The results showed that iodine deficiency and iodine enrichment coexist in groundwater. The range of I− varied from undetected to 1460.0 μg·L−1. Alkaline, partially reductive and organic-rich environment was likely to cause the iodine occured on minerals to enter the groundwater in the form of I−. Along the flow of groundwater, the I− gradually accumulated from the mountain front alluvial plain to the river alluvial plain of the middle and lower reaches. In addition, the iodine in groundwater was mainly affected by strong evaporation and concentration, cation exchange, mineral dissolution and precipitation.
-
Key words:
- groundwater /
- iodine /
- factor analysis /
- Kashi Prefecture
-
农村生活污水作为面源污染的主要来源,具有氮磷营养素较高、分散、面广、量少、不易收集、管理水平低等特点[1-2],是导致河流、湖泊富营养化的重要原因[3-4]。因此,为提高农村生活污水处理率、研究开发投资成本低、工艺设备操作简单、低能高效、运行维护方便且适用于农村污水处理设备具有重要意义。
近年来,生物膜法凭借剩余污泥量少、抗冲击负荷能力强、运行管理方便等特点,已在水处理中被大量运用[5-6],生物滤池利用生物膜的过滤、絮凝及生物氧化作用,能够有效地去除水中引起水体富营养化的氮磷元素[7]。多级生物滤池通过设置两级及以上独立的缺氧、好氧段来进行污水处理,具有抗冲击负荷能力强、充分利用原水碳源、较好地有机物降解和脱氮等能力[8-9]。填料作为生物滤池重要的组成部分,其结构、空隙率和亲水性等属性对生物膜的生长、结构和更新均具有显著影响[10-12]。相比于其他填料,聚氨酯填料(海绵)具有寿命长、损耗低(年损耗5%)、不易堵塞、氧利用率高等优点,其独特的多孔结构可使微生物在流动状态下自动聚集于载体内部,形成三维固定化生物膜,避免了流体剪切力对微生物冲刷剥离的影响,在其外表面实现亚硝化反应,在内部实现亚硝酸盐的反硝化,不仅有简单的物理吸附,还有正、负电荷的引力。此外,聚氨酯海绵填料市售价格为860~1 200元·m−3,价格低廉,故其在水处理中受到了重视,但也存在着生物亲和性不足等缺点[13-19]。为此,本研究将改性后的海绵作为填料,构建了4级斜板生物填料滤池,并对该处理系统的硝化液回流比参数进行了考察,采用高通量测序技术分析处理池中生物膜微生物生长分布情况,为该污水处理系统的达标稳定运行提供理论依据。本研究可为实际工程中工艺结构及参数的选取提供参考,有着重要的现实意义。
1. 实验材料与装置
1.1 实验材料
1)填料。本研究使用的聚氨酯发泡海绵材料购买于江苏常州市某公司,堆积比重为26 kg·m−3,孔隙率为96.20%,整张填料的尺寸为1.00 m×2.00 m×0.02 m,将填料裁剪为0.37 m×0.15 m×0.02 m大小的尺寸,采用化学氧化-壳聚糖接枝[20-21]改性方法获得的改性聚氨酯填料以备用。
2)实验用水。根据现场调研及相关资料查阅,按照浙江省农村地区生活污水水质特征,本研究采用稀释加药法配制了实验用进水,即取一定体积的原水(北京科技大学校区内的生活污水)稀释,稀释后降低的浓度差采用乙酸钠、葡萄糖、氯化铵和磷酸氢二钾进行添加,使进水中的COD、氨氮、TP和SS浓度达到模拟农村生活污水的设计浓度值,设计浓度值见表1。出水水质需要达到浙江省《农村生活污水处理设施水污染物排放标准》(DB 33/973-2015)一级标准,其中pH的标准限值为6~9,其他主要监测指标及浓度见表1。
表 1 进/出水水质Table 1. Water quality of inlet / outlet进出水浓度 COD/(mg·L−1) 氨氮/(mg·L−1) TP/(mg·L−1) SS/(mg·L−1) 进水设计浓度 250~350 33~40 3.2~3.8 60~100 出水浓度标准 ≤60 ≤15 ≤2 ≤20 1.2 污水处理装置系统
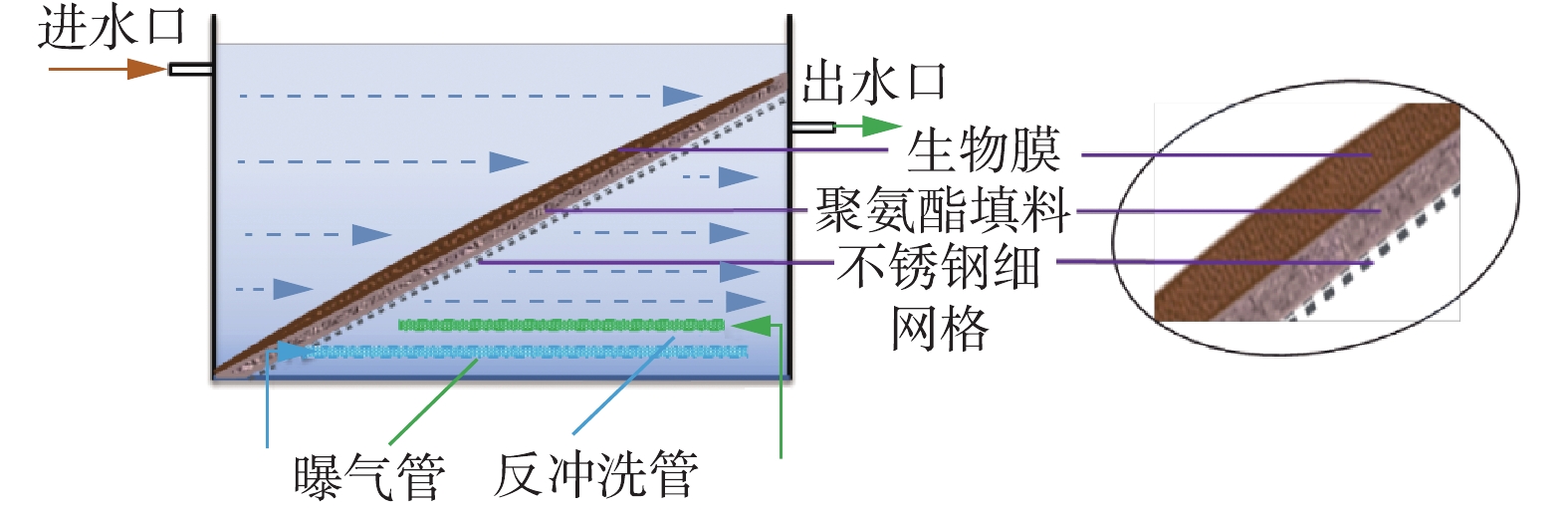
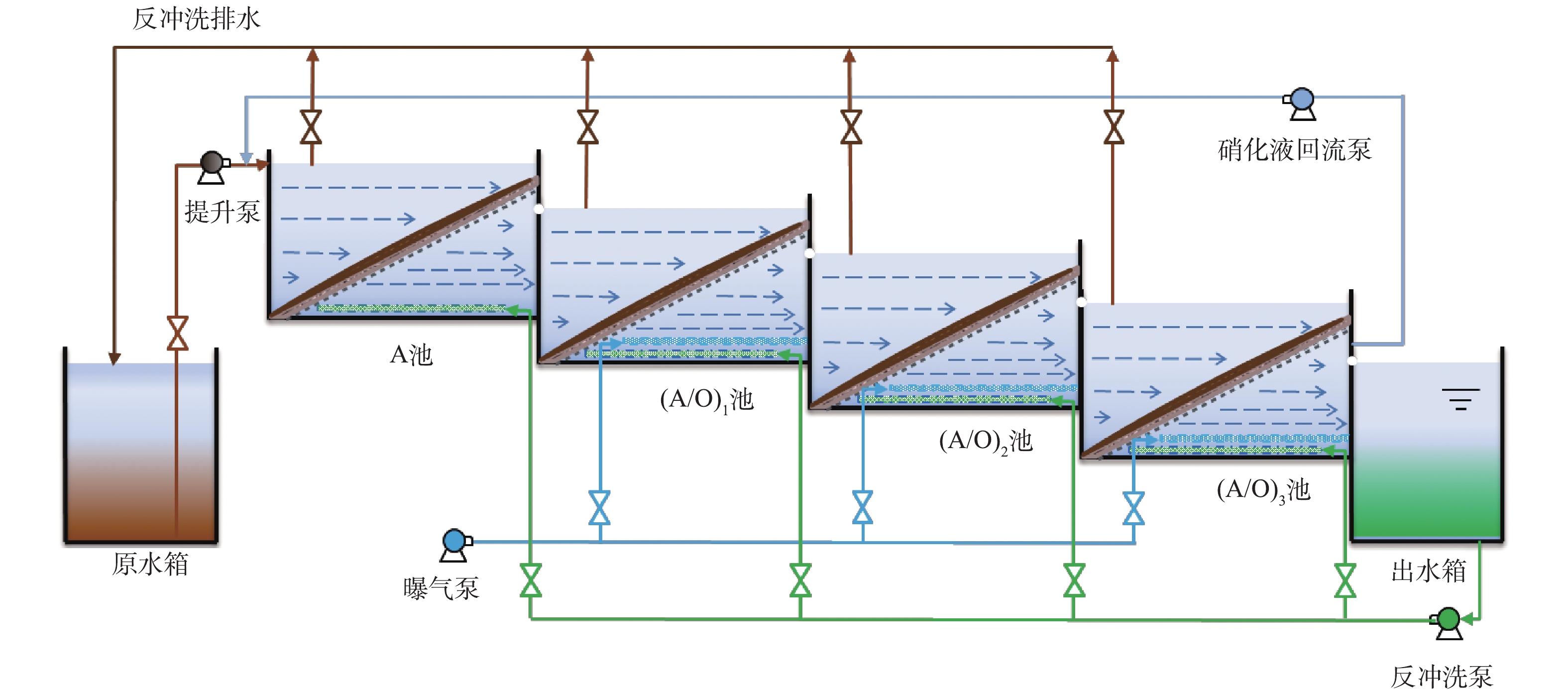
本研究实验装置如图1和图2所示。在笔者前期工作的基础上,确定了该系统由4个斜板生物滤池串联构成,运行时,第1个池体不进行曝气,后3个池体进行曝气,将其分别记为A、(A/O)1、(A/O)2、(A/O)3。
1)单池结构。单个斜板生物滤池的尺寸为0.30 m×0.15 m×0.25 m,有效容积为10.10 L,主要由进出水管、斜板式生物填料、不锈钢支撑网、曝气系统、反冲洗系统、回流液系统等构成。为防止因水流冲击造成填料的变形和移动,生物膜填料平铺在不锈钢支撑网上并以36°角进行固定,同时采用弹性压条将斜板填料与四周池壁缝隙处进行压实,防止在进水过程中造成壁流效应。斜板填料固定好后的尺寸为0.37 m×0.15 m×0.02 m,填充率约为11%,其将水池分割为上下2个相对独立的部分,可在一个处理池中同时创造好氧和缺氧的条件,这样每个A/O池均可视为一个局部的A/O系统,使同步硝化反硝化成为可能,这也是该处理系统的优势之一。
2)运行参数。实验系统采用前段单点进水,单个滤池水力负荷为1.40 m3·(m2·d)−1,进水流量约为(24±1) L·d−1,废水在每一级池体内的水力停留时间约为10 h,系统总体停留时间约为40 h。A/O池斜板填料下方好氧区溶解氧浓度控制在(2.0±0.2) mg·L−1,控制斜板上方缺氧区溶解氧浓度≤0.50 mg·L−1,第一个A池不曝气。为达到脱氮的目标,本研究将A/O池处理后的混合液通过回流泵回流至A池,利用A池中的反硝化菌将回流混合液中亚硝态氮和硝态氮转化成氮气[22],将硝化液回流比分别设为0、50%、100%、200%。
3)填料反冲洗。该污水处理系统进水开始运行初期主要依靠填料的机械截留和过滤作用来去除污水中的悬浮物质,随着水处理的进行,斜板填料截留的悬浮物质增多,逐渐形成一个生物膜,起到截留、吸收、降解有机物及氮、磷等污染物的作用[23]。随着系统运行,生物膜增厚,填料膜两侧压头损失逐渐增大。在实验阶段每12 d对填料进行1次水反冲洗,反冲洗时填料上老化的生物膜随着冲洗水而脱落并随反冲洗水排出系统,达到净化滤层的目的,同时减少了滤料两侧压差。
1.3 微生物群落分析
为了研究4级填料生物滤池污水处理系统的细菌群落,利于系统的操作和优化,将最优条件下的斜板生物膜样品在干冰冷冻条件下送至生工生物工程(上海)股份有限公司,采用基于16S rRNA基因V3~V4区高通量测序[24-25]分析生物膜中细菌的种类及多样性,在97%的分类水平上,通过应用Mothur软件计算各样品的Alpha多样性[26],用RDP Classifier方法与Green Gene数据库进行物种注释分析[27]。
2. 结果与讨论
对于污水处理系统,在不同回流比条件下分别进行了12 d的运行实验,每2 d检测1次进出水COD、氨氮、TN、TP水质。本实验装置系统对于SS的去除主要来自于四个池体内斜板填料的机械截留过滤作用,在初期摸索实验阶段得知,当实验进水SS浓度为60~100 mg·L−1时,出水中SS浓度均在10 mg·L−1以下,随着运行时间的延长,出水SS浓度会进一步降低到5 mg·L−1,满足DB 33/973-2015一级标准对SS的要求,由于该指标基本不受回流比的影响,在本文中不做详细分析。
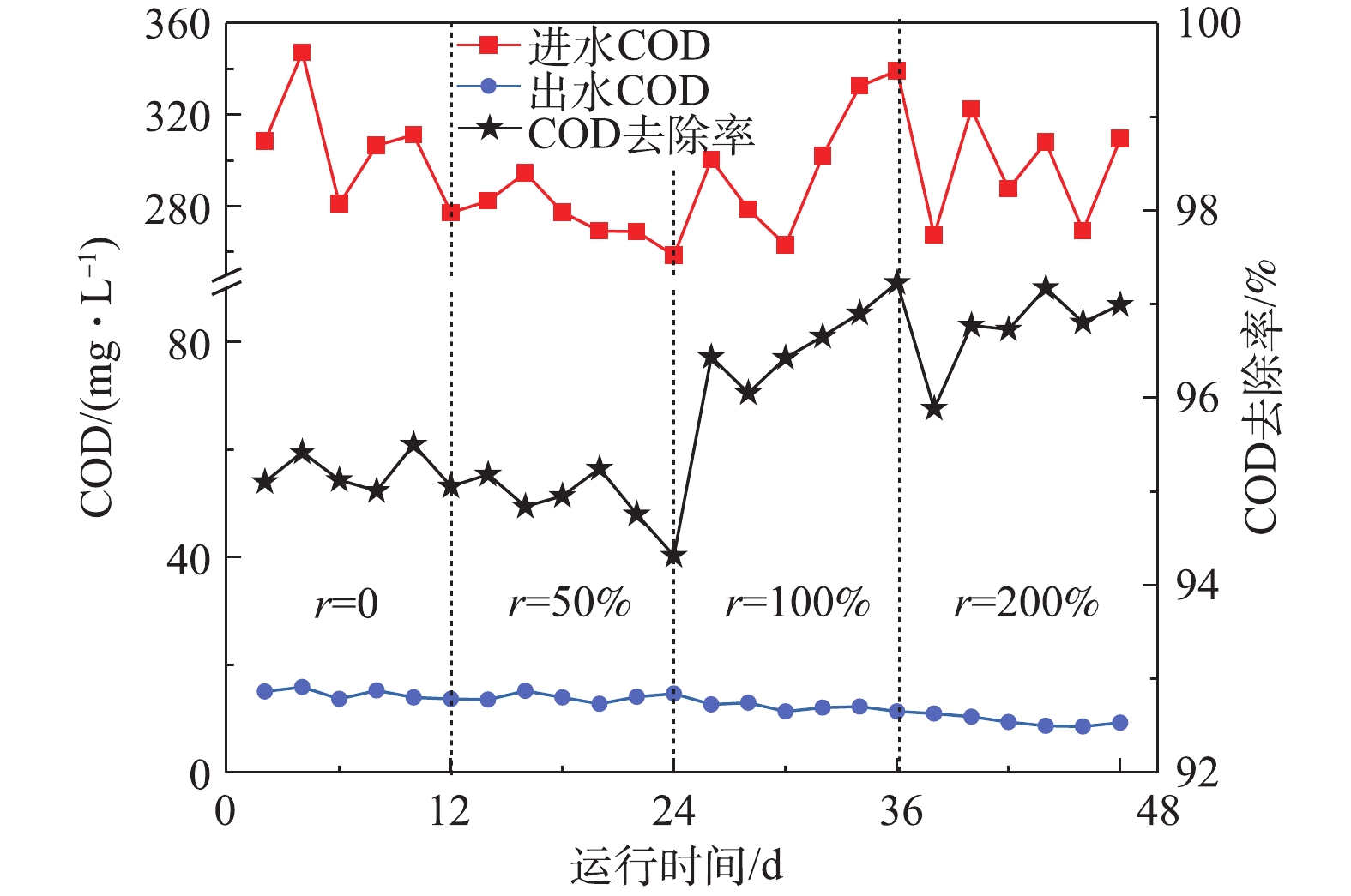
2.1 对COD的去除效果
由图3可知,回流比从0逐渐增大到200%时,COD去除率逐渐升高并趋于平稳,平均出水COD由14.62 mg·L−1降低到9.57 mg·L−1,达到DB 33/973-2015一级排放标准,由此可见,改系统对有机物的去除率整体较高。这是由于A/O池作为污水处理系统的重要组成,在聚氨酯填料表面及内部生长的大量异养微生物的降解和吸收作用下,有机物被大量去除[28]。同时可以看到,回流比的增大促进了有机污染物的降解,这是由于回流比的增加使水力剪切作用加大,加快了生物膜的脱落和更新,提高了传质效果,同时反硝化细菌利用回流液中的硝酸盐作为电子受体,以有机污染物作为碳源来进行反硝化作用,促进了COD的去除。剩余的COD没有被微生物利用,其原因可能是难降解的有机物以及微生物通过内源呼吸的产物是微生物较难利用的碳源。
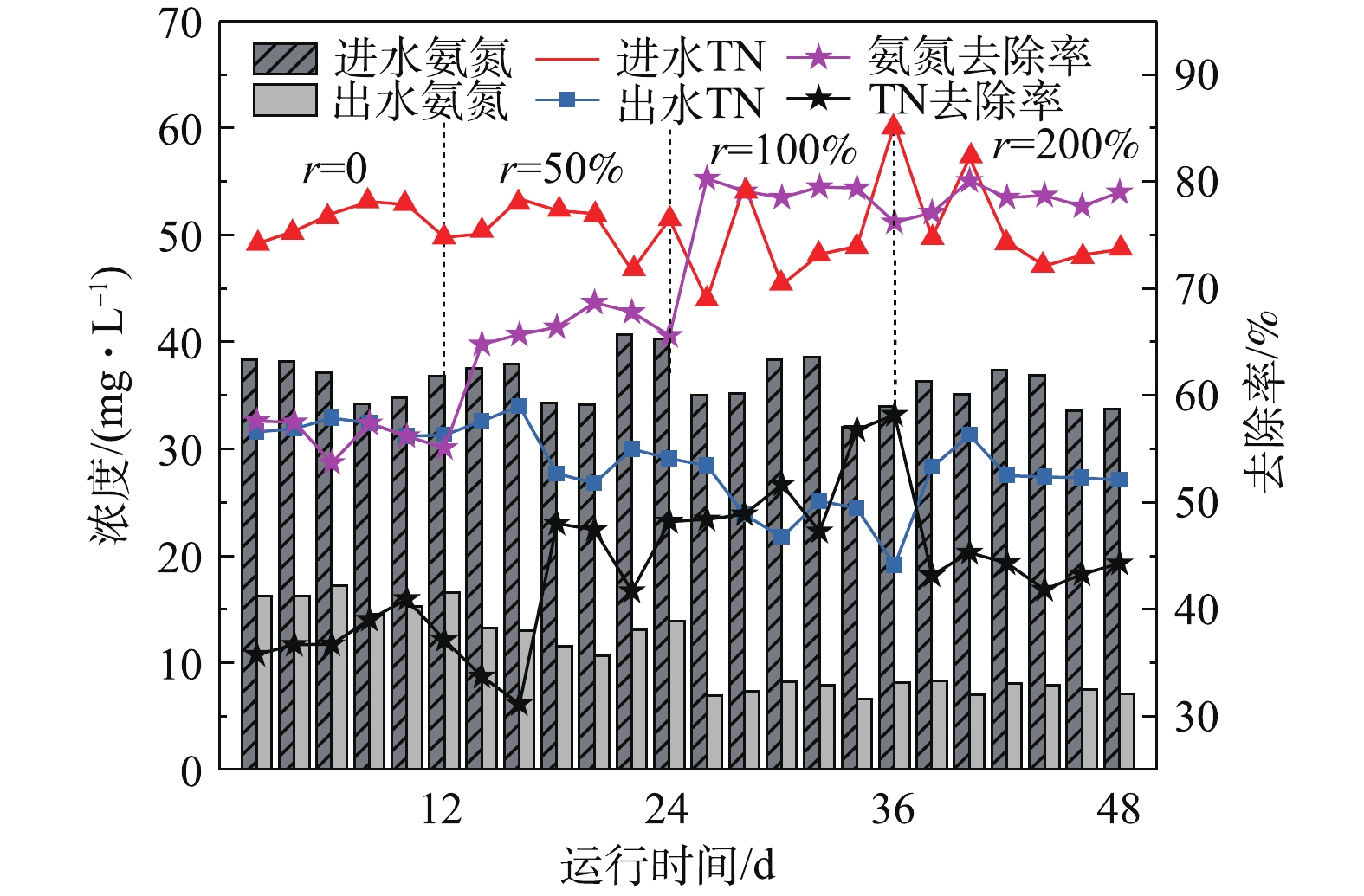
2.2 对氮元素的去除效果
处理系统在不同回流比下对氨氮和TN的去除效果和去除率如图4所示。由图4可知,当回流比由0提高到100%时,氨氮的平均去除率由56.25%提高到78.83%;而当回流比继续增加到200%时,系统对氨氮去除率并没有持续增大,平均去除率为78.50%。污染物去除率的逐步升高是由于回流硝化液稀释了进水中的有机物浓度,使得A/O池内异养菌竞争力下降,硝化自养菌成为优势菌,这有利于硝化反应的进行,进而提高了氨氮的去除率。而当硝化液回流比超过100%时,回流液携带大量的溶解氧进入A池,破坏了缺氧环境,使得反硝化菌活性降低,对有机污染物的消耗降低,A/O段的有机负荷增大,自养硝化细菌与异养菌的竞争力减弱,降低氨氮去除率[29]。此外,回流比的增大导致系统的水力负荷增大,进水流速和水力剪切作用增大,使得一部分硝化菌脱落随出水流失。在这些因素的共同作用下,硝化液回流比从100%增加到200%时,氨氮去除率无明显增高。
TN的去除率随着回流比的增大呈先上升后下降的趋势,当回流比由0增大到100%时,TN的去除率明显上升且达到最高,由37.73%增大到51.89%,出水TN平均浓度由31.88 mg·L−1降低到23.79 mg·L−1。这是由于随着回流比增大,进入A池的硝化液量也相应增大,反硝化菌利用原水中的有机物作为碳源,将A/O池中回流的硝态氮作为电子受体进行反硝化反应来脱氮。当回流比继续增加到200%时,TN的去除率下降,其原因与氨氮去除率下降的原因相同,均是由于回流比的增大,使得更多的溶解氧进入A池,破坏了缺氧环境,从而降低了反硝化菌活性,进而导致反硝化脱氮作用减少。
2.3 对磷元素的去除效果
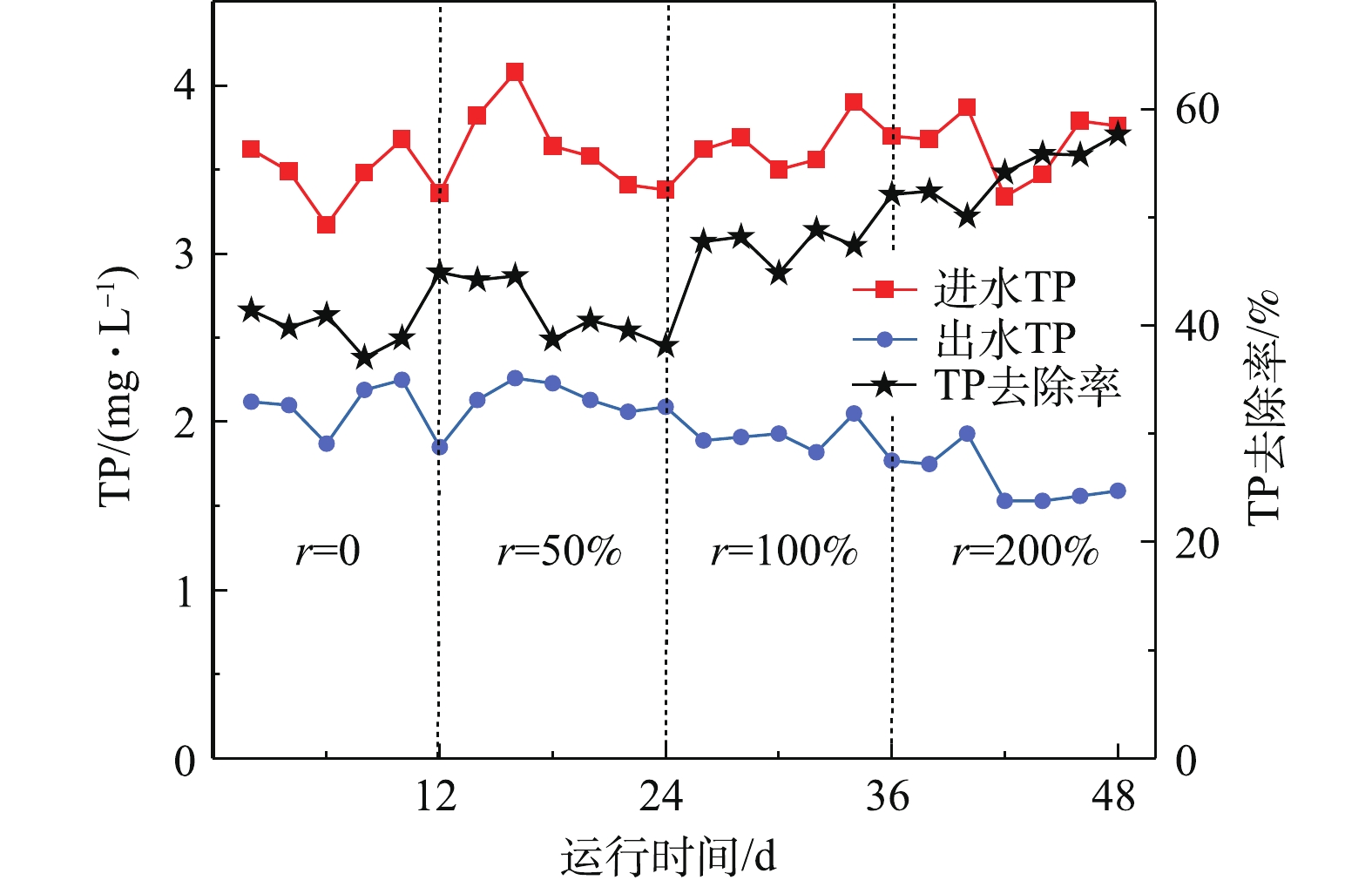
由图5可知,随着回流比的增加,有机负荷也随之增加,聚磷菌在A池获得充足的碳源,释磷量增多,在A/O池吸磷量也随着增加,磷的去除率升高,TP的平均去除率由40.52%提高到54.36%,出水TP平均浓度由2.06 mg·L−1减少到1.65 mg·L−1,当回流比大于等于100%时,出水TP达到DB33/973-2015一级标准。系统对TP的去除主要依靠聚磷菌(PAOs)在厌氧条件下释放磷,将易降解的有机物和挥发性脂肪酸VFA转化为聚羟基链烷酸(PHAs)的形式,污水进入A/O池后,聚磷菌以PHAs为电子供体在好氧状态下过量吸磷[30-31]。本研究在每一种工况结束后对填料进行水反冲洗,老化的生物膜最终随反冲洗水以富磷污泥的形式流出系统,实现脱磷的效果。
综上所述,该多级A/O填料滤池处理系统在回流比变化较大的情况下,综合对各污染物的去除效果确定回流比为100%是该系统的最优运行条件,出水水质均达到浙江省《农村生活污水处理设施水污染物排放标准》(DB33/973-2015)一级标准。
2.4 细菌群落多样性分析
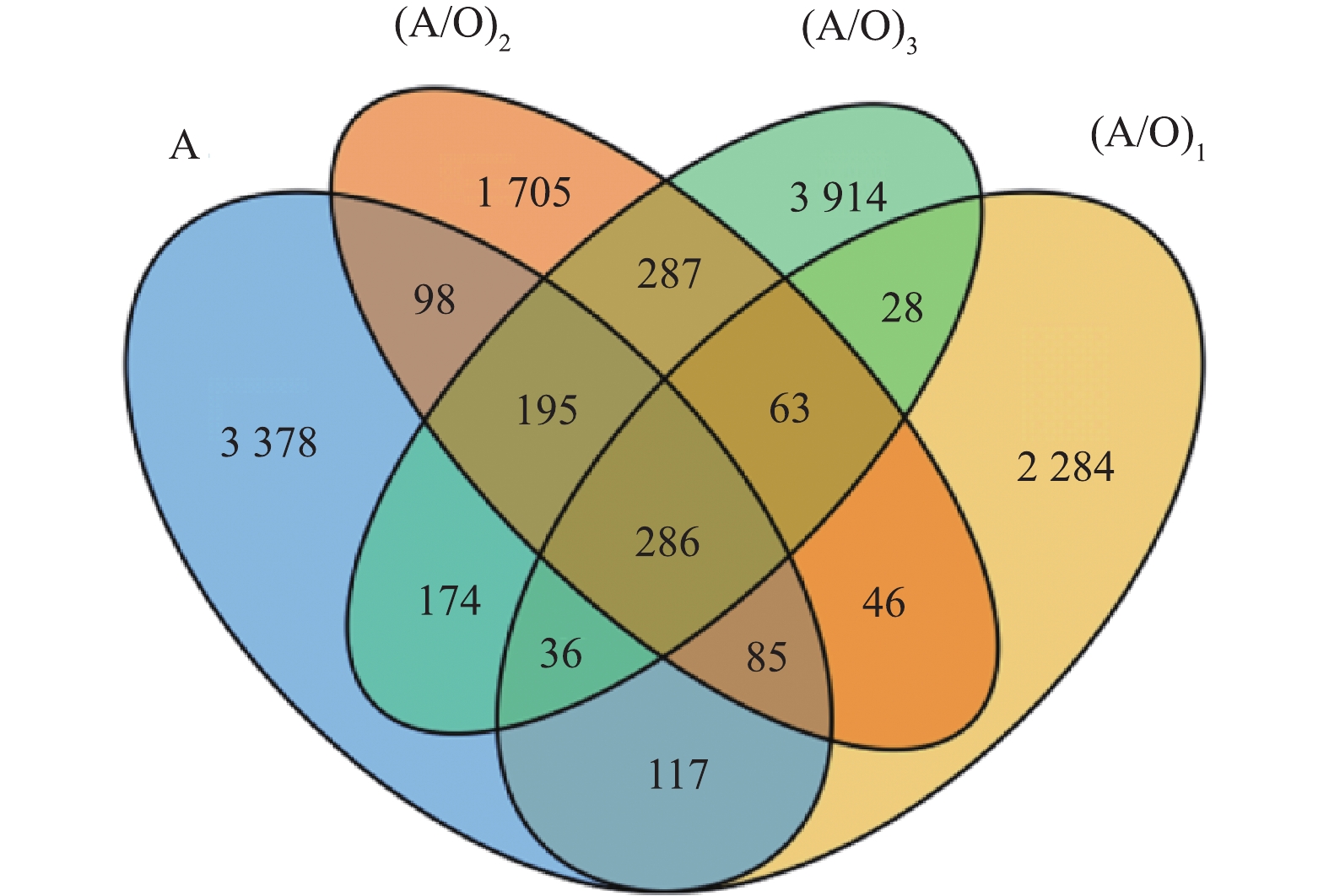
对4个斜板生物膜样品进行通量测序分析,得到有效序列信息后以97%的相似性将其聚类成为OTU[32],Veen图可以直观地展现样品的OTU组成的多样性、相似性及重叠情况。本实验4个生物膜样品属水平的Veen图如图6所示。4个池体的生物膜样品聚类得到的OTU总数目分别为4 369、2 945、2 765、4 983个,(A/O)3池物种种数最多[33]。2个处理池共同拥有的OTU个数越多时,其细菌组成的相似度越大,由图6可知,4个生物池内(A/O)2和(A/O)3池内细菌组成的相似度最大。A、(A/O)1、(A/O)2和(A/O)3生物膜样品特有的OTU数目分别是3 378、2 284、1 705、3 914个,各处理池之间共有OTU数目明显低于其各自特有的OTU数目。这说明各处理池在细菌群落组成上存在较大的差异,在一定程度上表明各处理池在处理系统中起着不同的作用。
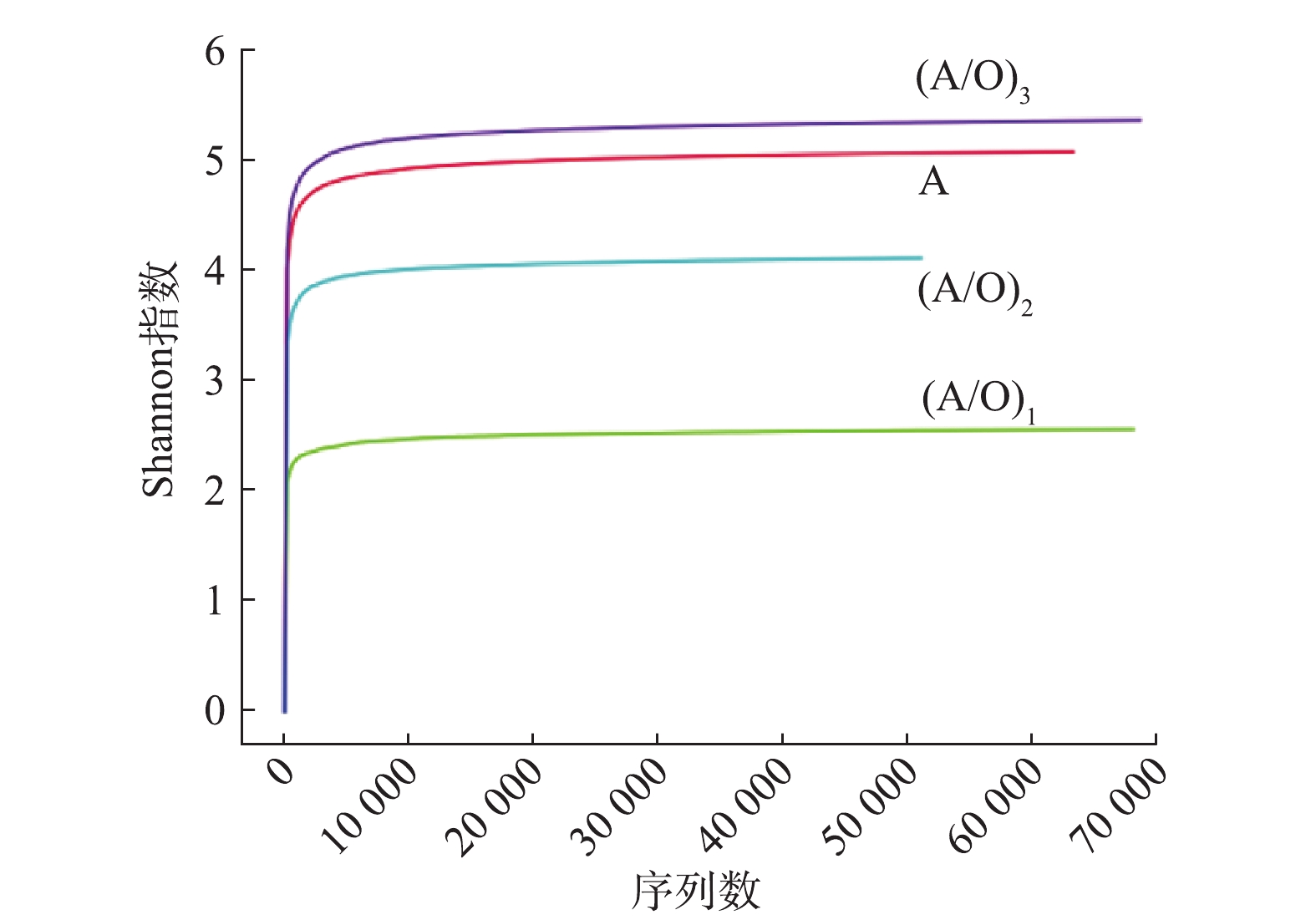
Alpha多样性包括覆盖率、ACE指数、Chao1指数及Simpson指数。Chao1指数和ACE指数可反应群落分布丰富度,其越大群落丰富度越高。Shannon指数越大,群落多样性越高,Simpson指数越大,群落多样性越低[34-35]。由表2中的ACE和Chao1指数可知,4个生物膜样品中细菌群落丰富度由大到小顺序排列依次是(A/O)1>(A/O)3>A>(A/O)2。Shannon指数表明各生物膜样品的细菌群落多样性由大到小是(A/O)3>A>(A/O)2>(A/O)1,Simpson指数也印证了这一点。(A/O)1样品的细菌群落多样性最低,这可能是由于进入(A/O)1池的污水中有机物浓度高、营养物质丰富,从而造成丝状菌大量繁殖,丝状菌与菌胶团细菌竞争营养物质和氧,导致池内溶解氧浓度大幅降低。最终,丝状菌成为优势菌,破坏了菌胶团的结构、减少了菌胶团细菌的多样性。由4个样品的文库覆盖率(coverage)可以看出,所有样本的样本序列的覆盖率为95%~96%,获取了绝大多数样本信息,能够很好地反映各样品的细菌群落组成。利用R语言工具制作Shannon稀疏曲线见图7。由图7可见,当序列数增加到10 000以上时,4个样本的Shannon稀疏曲线均趋向平坦,同样说明4个样本的测序数据量足够大,可以反映4个生物膜样本的绝大多数微生物的物种信息。
表 2 样品多样性及丰度指数统计Table 2. Sample diversity and abundance index statistics样本名称 OTU ACE Chao1 Shannon Simpson 覆盖率/% A 4 369 41 920.70 22 856.80 5.21 0.02 95 (A/O)1 2 945 72 636.75 27 675.05 2.63 0.25 96 (A/O)2 2 765 27 145.44 13 244.00 4.22 0.07 96 (A/O)3 4 983 55 977.55 26 508.83 5.50 0.02 95 2.5 各处理池细菌在门及属分类层面的分布规律
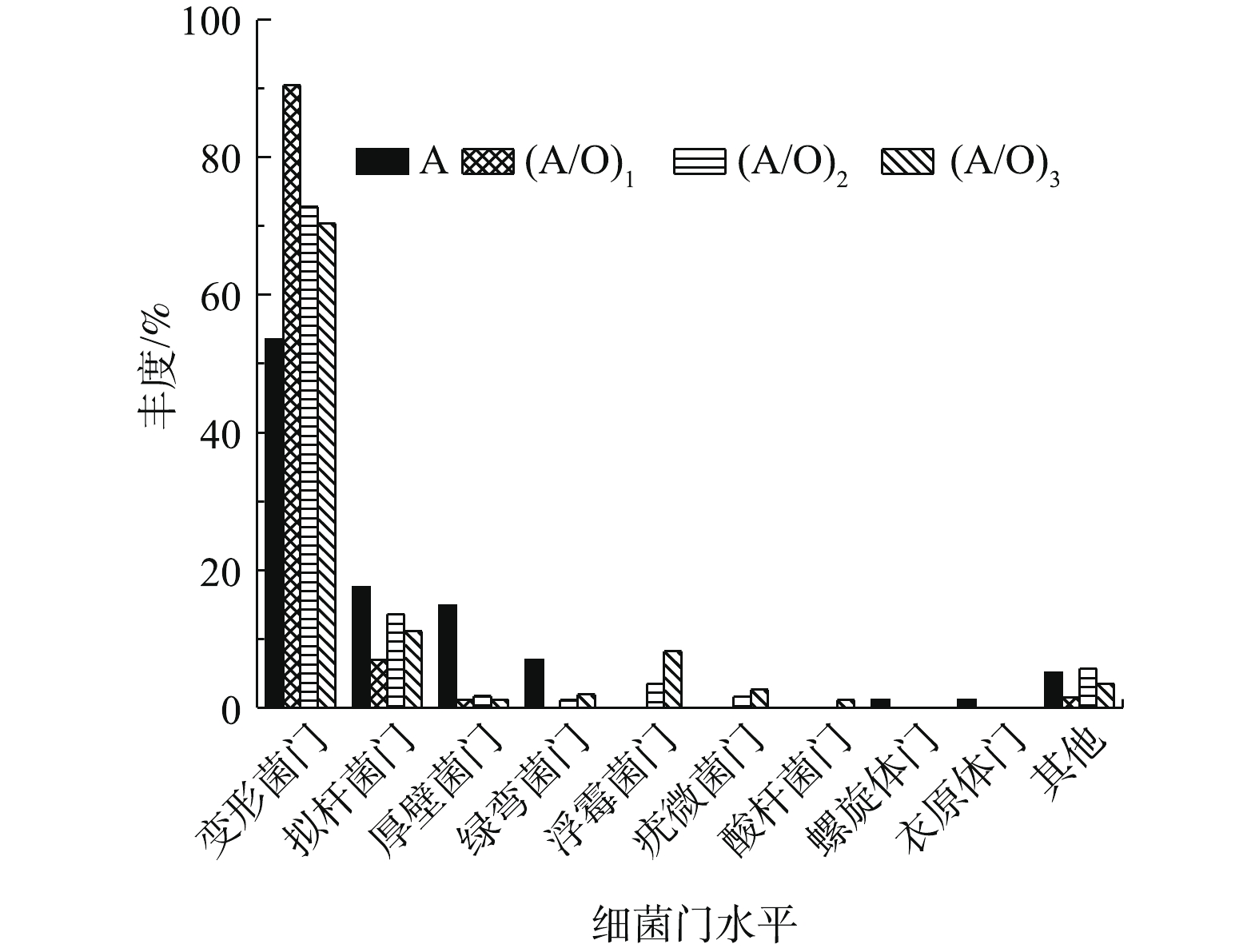
微生物作为生物废水处理工艺的核心,在降解和转化污染物过程中起着关键的作用[36-37]。4个生物膜样品的可操作分类单元(OTU)在门(phylum)水平上的细菌群落分布如图8所示。由图8可知,该处理系统主要存在变形菌门、拟杆菌门、厚壁菌门等门类群。变形菌门参与氨化、反硝化等生化过程,在生物脱氮、除磷及诸多污染物降解过程中起着重要的作用[38],其在各个池中占比最大,在A/O池中更是高达90.50%、72.80%和70.40%。考虑在A/O池内水中NH3-N进行硝化反应生成
NO−3 ,同时微生物进行生物代谢降解有机物供给聚磷菌能量,使其以PHAs为电子供体在好氧状态下过量吸磷,磷进入细胞组织,最后以富磷污泥的形式从系统中排出现除磷的去除;在A池中,拟杆菌门、厚壁菌门、绿弯菌门的占比情况分别为17.50%、14.80%和6.90%,相较于A/O池高。有研究[39-40]表明,该菌类对于污水中的碳水化合物、大分子有机物的降解具有重要的作用。例如,绿弯菌门中的厌氧绳菌科是典型的产氢产乙酸细菌,在厌氧或缺氧条件下较常见,厚壁菌门则可以进行反硝化脱氮反应,具有较强的氨化作用。可见,在A池中细菌主要以有机物为碳源将A/O池回流进来的NO−3 还原为N2释放,实现污水中氮的去除,期间,高分子有机物被分解为小分子,可降低后续生物处理的生物负荷并提高了生化性。此外,在A/O池中也存在有拟杆菌门、厚壁菌门等门类,这是因为每一个A/O池都兼具好氧池和缺氧池的部分功能。除以上几大门类外,还存在浮霉菌门、酸杆菌门等,但其占比相对较小。为进一步了解反应器在运行过程中细菌群落的演化,在属(genus)水平进一步进行细菌群落结构分析并对其功能菌属进行统计,统计结果如表3所示。由表3可见,优势菌属大多为反硝化菌、聚磷菌这类具有脱氮除磷作用的功能微生物,解释了水体N、P良好的去除作用。其中,硝化细菌主要有4个属,反硝化细菌主要有9个属,聚磷菌有3个属。有研究[41]表明,Nitrosomonas是亚硝化单胞菌属,是能够调节硝化过程中氨氮转变为亚硝酸盐氮的限速酶,起到控制硝化反应的作用。Nitrospira是硝化螺旋菌属,在处理系统中具有将亚硝酸盐还原为硝酸盐的能力,A/O池样品中该菌属的丰度值较高;Pseudomonas属于变形菌门,是常见的反硝化细菌,对废水生物脱氮、除磷均有重要意义,同时,Pseudomonas能够显著降低系统中的COD,其在A池中的含量最高,在其他A/O池的样品中的含量也较高,这也是系统对COD具有较高去除率的原因;除磷微生物主要有Acinetobacter[42]、Pseudomonas、Thiopseudomonas,其中以Acinetobacter细菌为主。
表 3 脱氮除磷功能菌及其丰度Table 3. Nitrogen and phosphorus removal bacteria and their abundances% 功能菌 A (A/O)1 (A/O)2 (A/O)3 Nitrospira(硝化) 0 0 0.02 0.44 Nitrobacter(硝化) 0 0 0 0.04 Nitrosomonas(硝化) 0 0 0.01 0.03 Nitrosospira(硝化) 0 0 0 0.01 Rosebaccilus(反硝化) 0.03 0 0.97 0.59 Pseudomonas(反硝化、聚磷) 0.25 0.15 0.04 0.08 Halothiobaccilus(反硝化) 0.3 0.01 0 0.01 Thiopseudomonas(反硝化、聚磷) 0.01 0 0.03 0.22 Cloacibaccilus(反硝化) 0.17 0 0.01 0 Acetanaerobacterium(反硝化) 0.15 0 0 0 Anaerobacterium(反硝化) 0.1 0 0 0 Thiobaccilus(反硝化) 0.01 0 0.01 0.01 Baccilus(反硝化) 0 0 0 0.01 Acinetobacter(聚磷) 0.43 6.91 1.3 0.55 3. 结论
1) 100%是该系统的最优硝化液回流比,在此条件下系统对COD、氨氮、TN、TP的综合去除率最高,包括SS指标均优于浙江省地方标准《农村生活污水处理设施水污染物排放标准》(DB 33/973-2015)一级标准。该系统具有较高的污染物去除率,同时具有流程简单、无辅助药剂添加等优势,具有良好的应用价值。
2)本研究所有样本的覆盖率为95%~96%,获取了绝大多数微生物的物种信息,保证了后续的微生物分析结果的准确性。不同生物膜样品共有的OTU数目远低于其特有的OTU,A/O池、A池在细菌群落组成上存在很大差异,发挥着不同的功能和作用。不同样品细菌群落丰富度由大到小排列依次为(A/O)1>(A/O)3>A>(A/O)2,细菌群落的多样性由大到小排列依次为(A/O)3>A>(A/O)2>(A/O)1。
3)在A/O池中,以变形菌门为主要门类群。在此,NH3-N进行硝化反应,聚磷菌在好氧状态下吸磷,有机物被降解;在A池中,拟杆菌门、厚壁菌门、绿弯菌门的占比较大,
NO−3 在此还原为N2释放;同时高分子有机物分解为小分子,降低后续生物处理的生物负荷。细菌属水平的统计结果为硝化菌、反硝化菌、聚磷菌等具有脱氮除磷作用的微生物,解释了系统稳定高效的的氮磷处理能力。 -
表 1 地下水化学指标特征参数统计表
Table 1. Statistical results of groundwater chemical Indexes characteristic
类型Type 潜水(n=76)Unconfined groundwater 浅层承压水(n=78)Shallow confined groundwater 深层承压水(n=29)Deep confined groundwater 指标Index 最小值Min 最大值Max 平均值Mean 中数Median 最小值Min 最大值Max 平均值Mean 中数Median 最小值Min 最大值Max 平均值Mean 中数Median K+ 4.2 120.4 24.5 18.6 3.8 101.6 27.0 20.5 1.6 46.9 13.9 10.5 Na+ 26.9 3537.2 466.2 296.6 10.2 3644.0 531.5 372.4 12.9 2348.0 384.6 213.6 Ca2+ 52.1 751.7 296.7 250.6 43.1 753.1 249.8 196.3 39.4 530.5 216.1 160.7 Mg2+ 18.2 410.3 136.4 113.1 11.0 479.4 155.0 126.1 16.2 571.5 136.4 87.7 Cl− 22.9 6568.4 598.2 354.6 15.8 5865.0 659.7 431.8 26.3 3501.0 457.6 230.5 SO42− 96.2 3175.8 1117.5 848.5 65.1 3734.0 1180.7 845.3 60.6 3034.0 1007.5 740.8 HCO3− 59.9 1106.2 322.7 291.7 54.6 589.5 324.8 306.9 97.2 595.0 250.4 210.1 TH 226.7 3566.1 1223.7 840.7 255.7 3278.0 1299.8 1117.5 35.0 3778.0 1126.6 847.5 TDS 354.8 13081.7 2826.0 2023.3 214.0 14548.0 2988.1 2249.6 249.3 10350.0 2362.9 1771.0 pH 6.4 9.9 7.5 7.4 6.9 8.2 7.5 7.5 6.6 8.7 7.7 7.7 I− ND 350.0 25.9 10.0 ND 1460.0 58.7 10.0 ND 220.0 24.5 10.0 Fe ND 6.0 0.6 0.2 ND 30.3 1.9 0.2 ND 26.5 3.5 0.2 Eh 103.0 251.0 187.7 205.0 −69.0 260.0 125.6 147.0 113.0 244.0 193.2 198.5 注:n为样品数;pH为无量纲;ND为未检出;I−单位为μg·L−1,Eh单位为mV,其余单位为mg·L−1. Note:n is sample number;pH is dimensionless;ND is not detected;unit of I− is μg·L−1;unit of Eh is mV;other units are mg·L−1. 表 2 水化学指标旋转因子载荷矩阵
Table 2. Rotation factor loading matrix of groundwater chemistry index
指标Index 因子载荷Factor loading F1 F2 F3 Na+ 0.952 0.055 −0.063 Ca2+ 0.864 0.294 0.162 Mg2+ 0.871 0.274 0.207 Cl− 0.944 −0.032 −0.091 SO42- 0.895 0.277 0.155 HCO3− 0.149 0.759 0.231 I− 0.733 −0.307 −0.235 TDS 0.979 0.165 0.044 Eh 0.066 −0.701 0.058 pH −0.203 −0.522 0.115 Fe 0.044 −0.033 0.935 特征值Eigenvalues 5.870 1.611 1.000 贡献率Contribution rate% 53.366 14.644 9.090 累计贡献率Cumulative contribution rate% 53.366 68.010 77.101 表 3 地下水矿物饱和指数计算
Table 3. Calculation of groundwater mineral saturation index
矿物指标Mineral index 潜水Unconfined groundwater 浅层承压水Shallow confined groundwater 深层承压水Deep confined groundwater 最小值Min 最大值Max 平均值Mean 最小值Min 最大值Max 平均值Mean 最小值Min 最大值Max 平均值Mean 方解石Calcite −0.32 1.94 0.55 −0.41 1.25 0.55 −0.77 1.32 0.55 白云石Dolomite −0.55 3.62 1.10 −0.83 2.54 1.22 −1.63 2.69 1.17 石膏Gypuum −1.75 −0.02 −0.66 −1.93 −0.01 −0.70 −1.93 −0.09 −0.77 盐岩Halite −7.79 −3.42 −5.70 −8.36 −3.46 −5.59 −8.04 −3.86 −5.90 -
[1] 王洋, 侯常春, 陈晓蓓, 等. 高碘对儿童健康影响的流行病学研究进展 [J]. 环境与健康杂志, 2015, 32(6): 560-563. WANG Y, HOU C C, CHEN X B, et al. Effects of excessive iodine intake on children's health: A review of recent epidemiological studies [J]. Journal of Environment and Health, 2015, 32(6): 560-563(in Chinese).
[2] 白超, 魏巍, 张丽, 等. 乌鲁木齐地区人群碘和硒营养状态与甲状腺癌相关性研究 [J]. 新疆医科大学学报, 2016, 39(9): 1183-1186. doi: 10.3969/j.issn.1009-5551.2016.09.027 BAI C, WEI W, ZHANG L, et al. Urumqi region population iodine and selenium nutrition status with thyroid cancer relevant research [J]. Journal of Xinjiang Medical University, 2016, 39(9): 1183-1186(in Chinese). doi: 10.3969/j.issn.1009-5551.2016.09.027
[3] 王敏, 庞绪贵, 高宗军, 等. 山东省黄河下游地区部分县市高碘型甲状腺肿与地质环境的关系 [J]. 中国地质, 2010, 37(3): 803-808. doi: 10.3969/j.issn.1000-3657.2010.03.037 WANG M, PANG X G, GAO Z J, et al. The relationship between the goiter induced by excessive iodine and the geological environment of several cities in the Lower Yellow River Basin of Shandong Province [J]. Geology in China, 2010, 37(3): 803-808(in Chinese). doi: 10.3969/j.issn.1000-3657.2010.03.037
[4] 李霞, 张丽. 天津市滨海新区高碘摄入与甲状腺肿瘤的相关性研究 [J]. 社区医学杂志, 2018, 16(11): 37-38. LI X, ZHANG L. Study on the correlation between high iodine intake and thyroid tumors in Tianjin Binhai New Area [J]. Journal of Community Medicine, 2018, 16(11): 37-38(in Chinese).
[5] 曹龄之, 谢建平, 彭小东, 等. 碘摄入量及富碘食物与甲状腺癌发病关系的Meta分析 [J]. 肿瘤防治研究, 2016, 43(7): 616-622. CAO L Z, XIE J P, PENG X D, et al. Association of iodine intake and iodine-enriched food with Risk of Thyroid cancer: A meta-analysis [J]. Cancer Research on Prevention and Treatment, 2016, 43(7): 616-622(in Chinese).
[6] 阎玉芹, 陈祖培, 舒延清. 全民食盐加碘4年来我国是否发生了高碘性甲状腺肿流行 [J]. 中国地方病学杂志, 2001, 20(3): 228-229. YAN Y Q, CHEN Z P, SHU Y Q. Study on the correlation between high iodine intake and thyroid tumors in Tianjin Binhai New Area [J]. Chinese Journal of Endemiology, 2001, 20(3): 228-229(in Chinese).
[7] 郭晓尉, 秦启亮, 边建朝, 等. 山东省水源性高碘地区分布现状与特征 [J]. 中国公共卫生, 2005, 21(4): 403-405. doi: 10.3321/j.issn:1001-0580.2005.04.011 GUO X W, QIN Q L, BIAN J C, et al. Distribution and characteristic of areas with high iodine concentration in drinking water in Shandong Province [J]. Chinese Journal of Public Health, 2005, 21(4): 403-405(in Chinese). doi: 10.3321/j.issn:1001-0580.2005.04.011
[8] 曾昭华. 地下水中碘的形成及其控制因素 [J]. 江苏地质, 1999, 18(2): 31-34,73. ZENG Z H. The formation of I and its control factors [J]. Jilin Geology, 1999, 18(2): 31-34,73(in Chinese).
[9] 吴飞, 王曾祺, 童秀娟, 等. 我国典型地区浅层高碘地下水分布特征及其赋存环境 [J]. 水资源与水工程学报, 2017, 28(2): 99-104. doi: 10.11705/j.issn.1672-643X.2017.02.17 WU F, WANG Z Q, TONG X J, et al. The distribution characteristics and storage environments of rich iodine in shallow groundwater of typical areas in China [J]. Journal of Water Resources and Water Engineering, 2017, 28(2): 99-104(in Chinese). doi: 10.11705/j.issn.1672-643X.2017.02.17
[10] 徐清, 刘晓端, 汤奇峰, 等. 山西晋中地区地下水高碘的地球化学特征研究 [J]. 中国地质, 2010, 37(3): 809-815. doi: 10.3969/j.issn.1000-3657.2010.03.038 XU Q, LIU X D, TANG Q F, et al. High iodic geochemical characteristics of the groundwater in central Shanxi Province [J]. Geology in China, 2010, 37(3): 809-815(in Chinese). doi: 10.3969/j.issn.1000-3657.2010.03.038
[11] 韩颖, 张宏民, 张永峰, 等. 大同盆地地下水高砷、氟、碘分布规律与 成因分析及质量区划 [J]. 中国地质调查, 2017, 4(1): 57-68. HAN Y, ZHANG H M, ZHANG Y F, et al. Distribution regularity, origin and quality division of high arsenic, fluorine and iodine contents in groundwater in Datong Basin [J]. Geological Survey of China, 2017, 4(1): 57-68(in Chinese).
[12] 薛肖斌, 李俊霞, 钱坤, 等. 华北平原原生富碘地下水系统中碘的迁移富集规律: 以石家庄-衡水-沧州剖面为例 [J]. 地球科学, 2018, 43(3): 910-921. XUE X B, LI J X, QIAN K, et al. Spatial distribution and mobilization of iodine in groundwater system of North China Plain: Taking hydrogeological section from Shijiazhuang, Hengshui to Cangzhou section as an example [J]. Earth Science, 2018, 43(3): 910-921(in Chinese).
[13] 张媛静, 张玉玺, 向小平, 等. 沧州地区地下水碘分布特征及其成因浅析 [J]. 地学前缘, 2014, 21(4): 59-65. doi: 10.13745/j.esf.2014.04.006 ZHANG Y J, ZHANG Y X, XIANG X P, et al. Distribution characteristics and cause analysis of iodine in groundwater of Cangzhou Region [J]. Earth Science Frontiers, 2014, 21(4): 59-65(in Chinese). doi: 10.13745/j.esf.2014.04.006
[14] 徐芬, 马腾, 石柳, 等. 内蒙古河套平原高碘地下水的水文地球化学特征 [J]. 水文地质工程地质, 2012, 39(5): 8-15. doi: 10.16030/j.cnki.issn.1000-3665.2012.05.020 XU F, MA T, SHI L, et al. Hydrogeochemical characteristics of high-iodine groundwater in the Hetao Plain’ Inner Mongolia [J]. Hydrogeology and Engineering Geology, 2012, 39(5): 8-15(in Chinese). doi: 10.16030/j.cnki.issn.1000-3665.2012.05.020
[15] 王雨婷, 李俊霞, 薛肖斌, 等. 华北平原与大同盆地原生高碘地下水赋存主控因素的异同 [J]. 地球科学, 2021, 46(1): 308-320. WANG Y T, LI J X, XUE X B, et al. Similarities and differences of main controlling factors of natural high iodine groundwater between North China Plain and Datong Basin [J]. Earth Science, 2021, 46(1): 308-320(in Chinese).
[16] 孙英, 周金龙, 乃尉华, 等. 新疆喀什噶尔河流域地表水水化学季节变化特征及成因分析 [J]. 干旱区资源与环境, 2019, 33(8): 128-134. doi: 10.13448/j.cnki.jalre.2019.238 SUN Y, ZHOU J L, NAI W H. Seasonal variation characteristics and causes of surface water chemistry in Kashgar River Basin, Xinjiang [J]. Journal of Arid Land Resources and Environment, 2019, 33(8): 128-134(in Chinese). doi: 10.13448/j.cnki.jalre.2019.238
[17] 陈劲松, 周金龙, 陈云飞, 等. 新疆喀什地区地下水氟的空间分布规律及其富集因素分析 [J]. 环境化学, 2020, 39(7): 1800-1808. doi: 10.7524/j.issn.0254-6108.2019042801 CHEN J S, ZHOU J L, CHEN Y F, et al. Spatial distribution and enrichment factors of groundwater fluoride in Kashgar Region, Xinjiang [J]. Environmental Chemistry, 2020, 39(7): 1800-1808(in Chinese). doi: 10.7524/j.issn.0254-6108.2019042801
[18] 曾妍妍, 周殷竹, 周金龙, 等. 新疆喀什地区西部地下水质量现状评价 [J]. 新疆农业大学学报, 2016, 39(2): 167-172. doi: 10.3969/j.issn.1007-8614.2016.02.015 ZENG Y Y, ZHOU Y Z, ZHOU J L, et al. Assessment of groundwater quality status in western Kashgar, Xinjiang [J]. Journal of Xinjiang Agricultural University, 2016, 39(2): 167-172(in Chinese). doi: 10.3969/j.issn.1007-8614.2016.02.015
[19] 纪媛媛, 李巧, 周金龙. 新疆喀什地区地下水质量与污染评价 [J]. 节水灌溉, 2014(1): 50-53,56. doi: 10.3969/j.issn.1007-4929.2014.01.014 JI Y Y, LI Q, ZHOU J L. Assessment of groundwater quality and pollution in Kashgar region of Xinjiang [J]. Water Saving Irrigation, 2014(1): 50-53,56(in Chinese). doi: 10.3969/j.issn.1007-4929.2014.01.014
[20] 於嘉闻, 周金龙, 曾妍妍, 等. 新疆喀什地区东部地下水“三氮”空间分布特征及影响因素 [J]. 环境化学, 2016, 35(11): 2402-2410. doi: 10.7524/j.issn.0254-6108.2016.11.2016040804 YU J W, ZHOU J L, ZENG Y Y, et al. Spatial distribution and influencing factors of “ three-nitrogen”in groundwater of the eastern area of Kashgar, Xinjiang [J]. Environmental Chemistry, 2016, 35(11): 2402-2410(in Chinese). doi: 10.7524/j.issn.0254-6108.2016.11.2016040804
[21] 王红太, 周金龙, 曾妍妍, 等. 新疆喀什地区饮用地下水碘分布及其富集因素分析 [J]. 新疆农业大学学报, 2019, 42(2): 145-150. doi: 10.3969/j.issn.1007-8614.2019.02.011 WANG H T, ZHOU J L, ZENG Y Y, et al. Spatial distribution and enrichment factors of iodine in drinking groundwater in Kashgar prefecture of Xinjiang [J]. Journal of Xinjiang Agricultural University, 2019, 42(2): 145-150(in Chinese). doi: 10.3969/j.issn.1007-8614.2019.02.011
[22] 徐雄, 肖培平, 孙艳亭, 等. 鲁西南黄河冲积平原地下水氟碘特征及成因分析 [J]. 生态与农村环境学报, 2020, 36(2): 186-192. doi: 10.19741/j.issn.1673-4831.2019.0274 XU X, XIAO P P, SUN Y T, et al. Study on the characteristics and physical causes of groundwater fluoride and iodide over the Yellow River alluvial plain in the southwest of Shandong Province [J]. Journal of Ecology and Rural Environment, 2020, 36(2): 186-192(in Chinese). doi: 10.19741/j.issn.1673-4831.2019.0274
[23] 钱会, 马致远. 水文地球化学[M]. 北京: 地质出版社, 2005: 45-46. QIAN H, MA Z Y. Hydrogeochemistry [M]. Beijing: Geological Publishing House, 2005: 45-46(in Chinese).
[24] LI J, WANG Y, XIE X, et al. Hydrogeochemistry of high iodine groundwater: a case study at the Datong Basin, northern China [J]. Environ Sci Process Impacts, 2013, 15(4): 848-859. [25] LI J, WANG Y, WEI G, et al. Iodine mobilization in groundwater system at Datong basin, China: Evidence from hydrochemistry and fluorescence characteristics [J]. Science of the Total Environment, 2014, 468-469(15): 738-745. [26] 王妍妍, 马腾, 董一慧, 等. 内陆盆地区高碘地下水的成因分析: 以内蒙古河套平原杭锦后旗为例 [J]. 地学前缘, 2014, 21(4): 66-73. WANG Y Y, MA T, DONG Y H, et al. The formation of inland-high-iodine groundwater: A case study in Hangjinhouqi, Hetao Plain [J]. Earth Science Frontiers, 2014, 21(4): 66-73(in Chinese).
[27] 陆徐荣, 杨磊, 陆华, 等. 江苏平原地区(淮河流域)潜水碘含量控制因素探讨 [J]. 地球学报, 2014, 35(2): 211-221. doi: 10.3975/cagsb.2014.02.13 LU X R, YANG L, LU H, et al. Discussion on the control factors of iodine content in groundwater in the Jiangsu Plain (Huaihe River Basin) [J]. Acta Geosciences, 2014, 35(2): 211-221(in Chinese). doi: 10.3975/cagsb.2014.02.13
[28] GIBBS R J. Mechanisms controlling world water chemistry [J]. Science, 1970, 170(3962): 1088-1090. [29] 雷米, 周金龙, 范薇, 等. 新疆阿克苏平原区地下水水化学演化特征 [J]. 地球与环境, 2020, 48(5): 602-611. doi: 10.14050/j.cnki.1672-9250.2020.48.069 LEI M, ZHOU J L, FAN W, et al. Hydrochemical evolution of groundwater in Aksu plain, Xinjiang [J]. Earth and Environment, 2020, 48(5): 602-611(in Chinese). doi: 10.14050/j.cnki.1672-9250.2020.48.069
[30] 孙英. 基于长系列和高频观测数据的干旱区潜水蒸发机理研究[D]. 乌鲁木齐: 新疆农业大学, 2019. SUN Y. Study on mechanism of phreatic evaporation in arid area based on long series and high frequency observation data[D] Urumqi: Xinjiang Agricultural University, 2019 (in Chinese).
[31] 孙英, 周金龙, 梁杏, 等. 塔里木盆地南缘浅层高碘地下水的分布及成因: 以新疆民丰县平原区为例 [J]. 地球科学, 2021, 46(8): 2999-3011. SUN Y, ZHOU J L, LIANG X, et al. The distribution and cause of formation of shallow high-iodine groundwater in the southern margin of the Tarim Basin: Taking the plain area of Minfeng County, Xinjiang as an example [J]. Earth Science, 2021, 46(8): 2999-3011(in Chinese).
[32] 张恒星, 张翼龙, 李政红, 等. 基于主导离子分类的呼和浩特盆地浅层地下水化学特征研究 [J]. 干旱区资源与环境, 2019, 33(4): 189-195. doi: 10.13448/j.cnki.jalre.2019.126 ZHANG H X, ZHANG Y L, LI Z H, et al. Chemical characteristics of shallow groundwater in Hohhot basin [J]. Journal of Arid Land Resources and Environment, 2019, 33(4): 189-195(in Chinese). doi: 10.13448/j.cnki.jalre.2019.126
[33] XIAO J, JIN Z D, WANG J, et al. Hydrochemical characteristics, controlling factors and solute sources of groundwater within the Tarim River Basin in the extreme arid region, NW Tibetan Plateau [J]. Quaternary International, 2015, 380-381(5): 237-246. [34] 孙一博, 王文科, 段磊, 等. 关中盆地浅层地下水地球化学的形成演化机制 [J]. 水文地质工程地质, 2014, 41(3): 29-35. doi: 10.16030/j.cnki.issn.1000-3665.2014.03.005 SUN Y B, WANG W K, DUAN L, et al. Geochemical evolution mechanisms of shallow groundwater in Guanzhong basin, China [J]. Hydrogeology and Engineering Geology, 2014, 41(3): 29-35(in Chinese). doi: 10.16030/j.cnki.issn.1000-3665.2014.03.005
-






 DownLoad:
DownLoad: