-
随着全球能源危机和环境污染威胁的日益加剧,寻找一种高效且无公害的环境治理技术是目前环境领域研究的热点[1-2]。自从1972年Fujishima首次发现在TiO2电极上水的光电化学反应将水分解为氢气和氧气以来,半导体光催化技术就以其绿色、可持续发展的优点引起了人们的广泛关注[3]。
在半导体光催化剂中,SrTiO3因为具有高化学稳定性和丰富的组成元素,被认为是一种很有前景的光催化剂[4]。此外,SrTiO3的导带和价带边缘具有较高的光化学稳定性和良好的生物相容性[5]。但由于SrTiO3具有较宽的禁带宽度(约为3.2 eV),导致其光吸收范围仅限于紫外光波段,严重降低了SrTiO3对太阳光的利用效率。此外,光生电子-空穴对复合速率快,量子效率低也是限制SrTiO3光催化性能的重要因素[6]。为了提高SrTiO3的光催化性能,科学研究人员开发了各种改性方法[7-9]。Qazi等[10]发现掺杂Cu后的SrTiO3,Cu+取代了Sr+,SrTiO3的带隙宽度从3.2 eV降低到2.96 eV,掺杂后的SrTiO3光催化活性大大提高。Atkinson等[11]通过溶胶-凝胶法合成了氮(N)掺杂的SrTiO3粉末,研究表明,由于结构、组织和形貌的协同作用,N掺杂使SrTiO3的带隙减小了1 eV左右。此外,利用S、Cr、Er和C3N4等多种材料,也提高了SrTiO3的光催化活性和化学稳定性[12-15]。目前还没有关于钨(W)和银(Ag)共掺杂SrTiO3的报道。
本文采用溶胶-凝胶法制备了W-Ag共掺杂SrTiO3纳米复合材料,以亚甲基蓝为目标污染物探究其光催化活性。并采用多种表征手段,探究W-Ag共掺杂SrTiO3样品光催化效率提升的机制。
-
酒石酸(C4H6O6),碳酸锶(SrCO3),钛酸丁酯(C16H36O4Ti),钨酸铵((NH4)10W12O41-xH2O),硝酸银(AgNO3),亚甲基蓝(MB)。所有试剂在本实验中均为分析级纯,无需进一步纯化。实验用水为蒸馏水。
-
溶胶凝胶法制备纯SrTiO3和W-Ag共掺杂SrTiO3粉末:取1.47 g碳酸锶与适量的酒石酸混合,加入20 mL蒸馏水,在水浴温度70 ℃的情况下均匀搅拌30 min,形成清澈透明的均匀溶液A。在磁力搅拌器持续搅拌的情况下,向溶液A中缓慢滴加3.4 mL钛酸丁酯,继续搅拌,直至形成透明的均质溶胶。将溶胶置于坩埚中,在烘箱中80 ℃的情况下烘干10 h,制得干凝胶。再将干凝胶置于马弗炉中,在700 ℃下煅烧2 h,冷却至室温,研磨后就制得了纯SrTiO3粉末。制备掺杂的SrTiO3粉末与上述步骤基本类似,只需在加入钛酸丁酯之前加入所需的钨酸铵和硝酸银试剂,其它步骤不变,就制备出了W-Ag共掺杂SrTiO3粉末。实验结果表明,SrTiO3中W和Ag的最佳摩尔比分别为2%和0.5%,此时样品光催化效果最佳。
-
使用D8 ADVANCE型X射线衍射仪表征SrTiO3材料的结晶性质。用扫描电子显微镜(SEM,ZEISS,Supra55)在200 kV下观察样品的结构形态。通过HITACHI的F-7000获得室温光致发光光谱(PL)。在Shimadzu UV-2550分光光度计上记录UV-Vis漫反射光谱(DRS)。利用ASAP 2020装置测量了样品的氮吸附-解吸等温线,以研究其(BET)表面积。使用ESCALAB 250型X-射线光电子能谱仪进行X射线光电子能谱(XPS)分析。
-
本研究以MB作为目标污染物,评价了W-Ag共掺杂SrTiO3样品的光催化活性。具体操作为:将0.1 g固体催化剂分散于100 mL MB溶液中。在光照前,将混合物在黑暗中搅拌30 min,进行避光吸附,以达到吸附-解吸平衡。将250 W高压汞灯作为模拟太阳光光源。每隔2 h,取5 mL反应溶液进行离心,取上层清液并测量其吸光度。通过计算MB水溶液在664 nm处的吸光度,考察纯SrTiO3和W-Ag共掺杂SrTiO3的光催化活性。
-
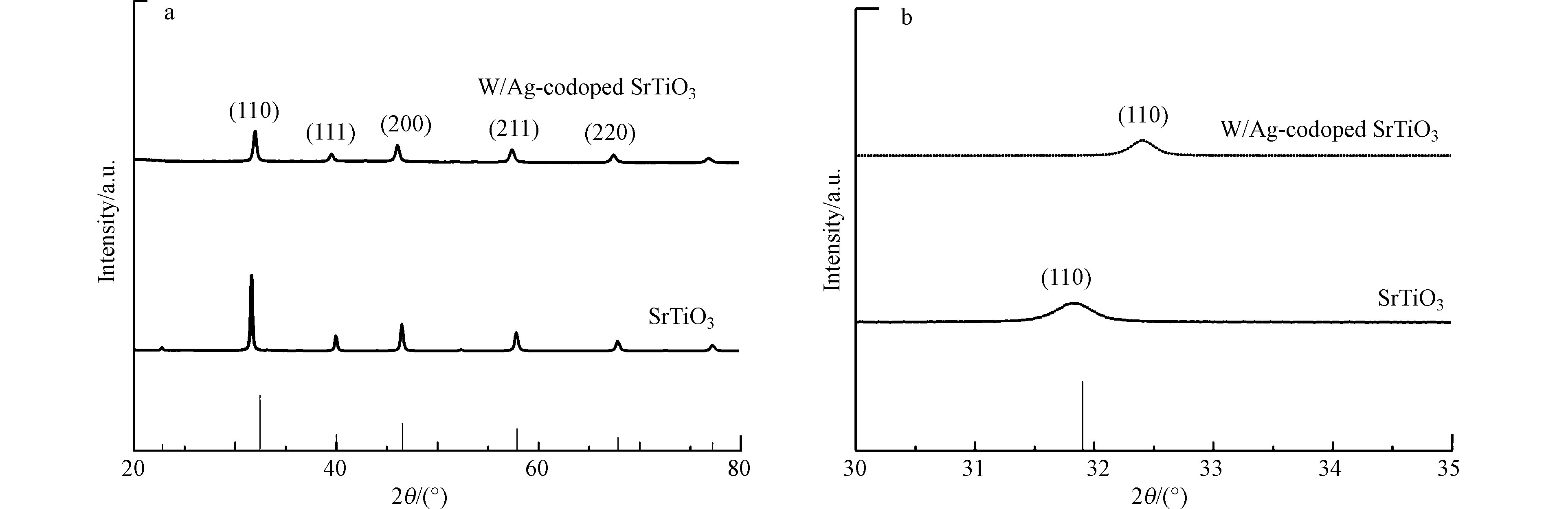
利用X射线衍射(XRD)分析了合成的纯SrTiO3和W-Ag共掺杂SrTiO3样品的晶体结构。如(图1)所示,衍射峰在2θ= 32.1°、39.6°、46.1°、57.2°和67.2°处分别对应SrTiO3标准卡(JCPDS No.35-0734)中(110)、(111)、(200)、(211)和(220)晶面,且没有观察到任何其他杂质峰。说明SrTiO3晶体是具有立方对称性的钙钛矿结构,且纯度和结晶度较高[16]。然而,图1中并没有观察到W和Ag峰,可能是W和Ag掺杂量过小,且均匀分散在SrTiO3晶格内。从图1(b)可以发现,与纯SrTiO3相比,W-Ag共掺杂SrTiO3的衍射峰强度降低且移动到了较高的衍射角区,根据Bragg公式,晶面间距变小,晶格收缩,晶体体积变小。这可能是由于W和Ag的离子半径小于Sr离子的半径,掺杂后使SrTiO3晶体尺寸减小[17]。一般来说,减小光催化剂的粒径可以缩短电荷载体的扩散路径,从而降低电子空穴对的复合几率,有助于提高光催化效率[18]。
-
用SEM对制备的样品进行结构和形貌表征。如图2a所示,纯SrTiO3样品呈现为类球状,且有明显的团聚现象,粒径约为50 nm。从图2b中可以看出,共掺杂样品显示出与纯SrTiO3样品相似的微观形貌特征,区别在于其粒径更小,约为40 nm左右(这与XRD显示的结果高度一致),同时改善了团聚现象。比表面积增加有利于晶体暴露出更多的活性位点,增加了电子-空穴的捕获阱,抑制了他们的复合,与污染物结合的更加充分,从而提高光催化剂的光催化活性。
-
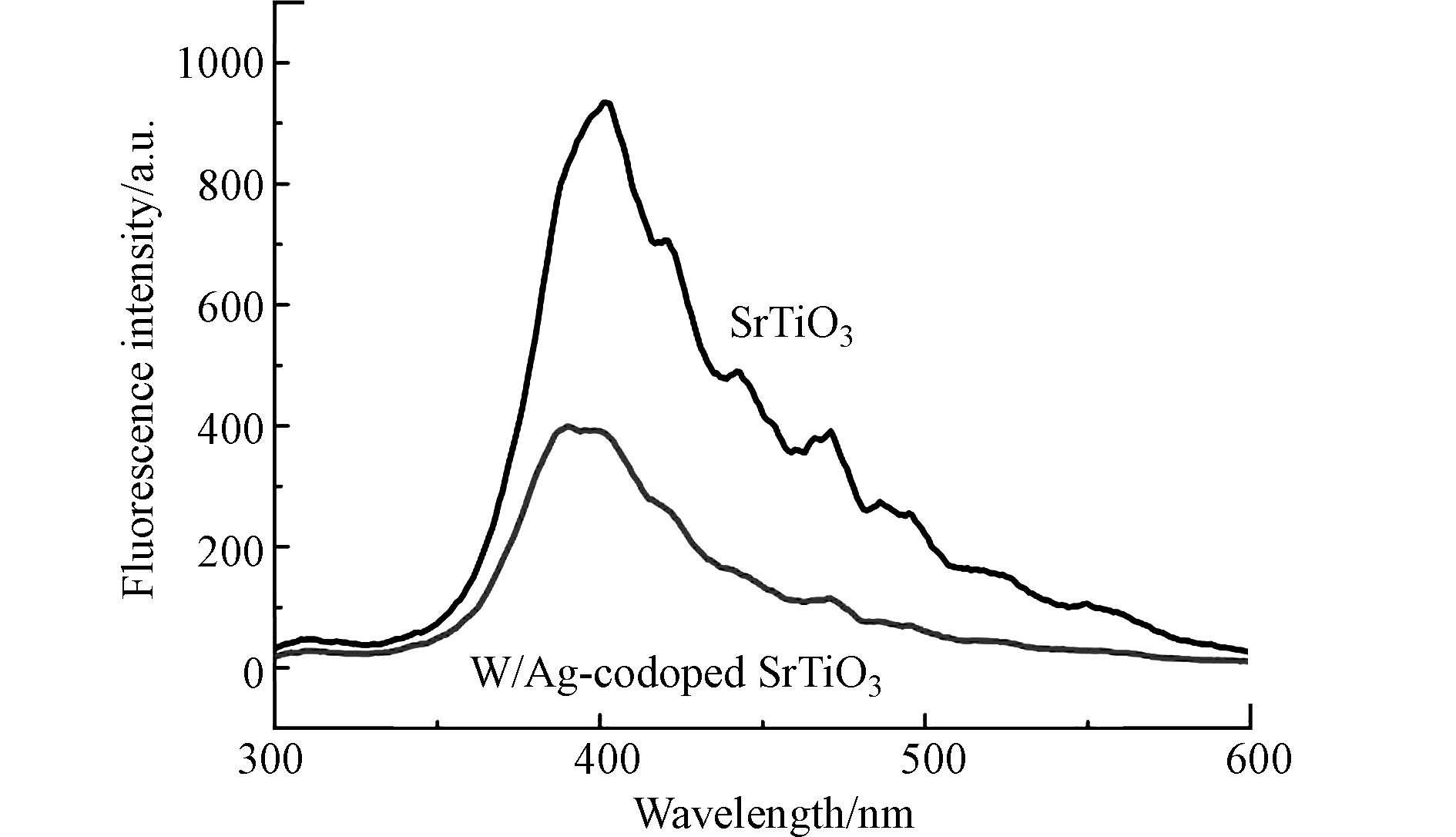
研究样品的电子-空穴对产生、分离和重组性质等光学性质,在室温下进行PL测量。其激发波长为365 nm。纯SrTiO3和W-Ag共掺杂SrTiO3样品的PL光谱如图3所示。与纯SrTiO3样品相比,W、Ag离子的掺杂使SrTiO3样品PL发生峰强度明显降低,这是由于W-Ag共掺杂SrTiO3抑制了光生电子-空穴对的复合,提高了光生载流子的分离效率[19]。降低电子-空穴对的复合速率更有利于电子空穴参与光催化反应,生成强氧化物质,从而提高光催化效率[20]。
-
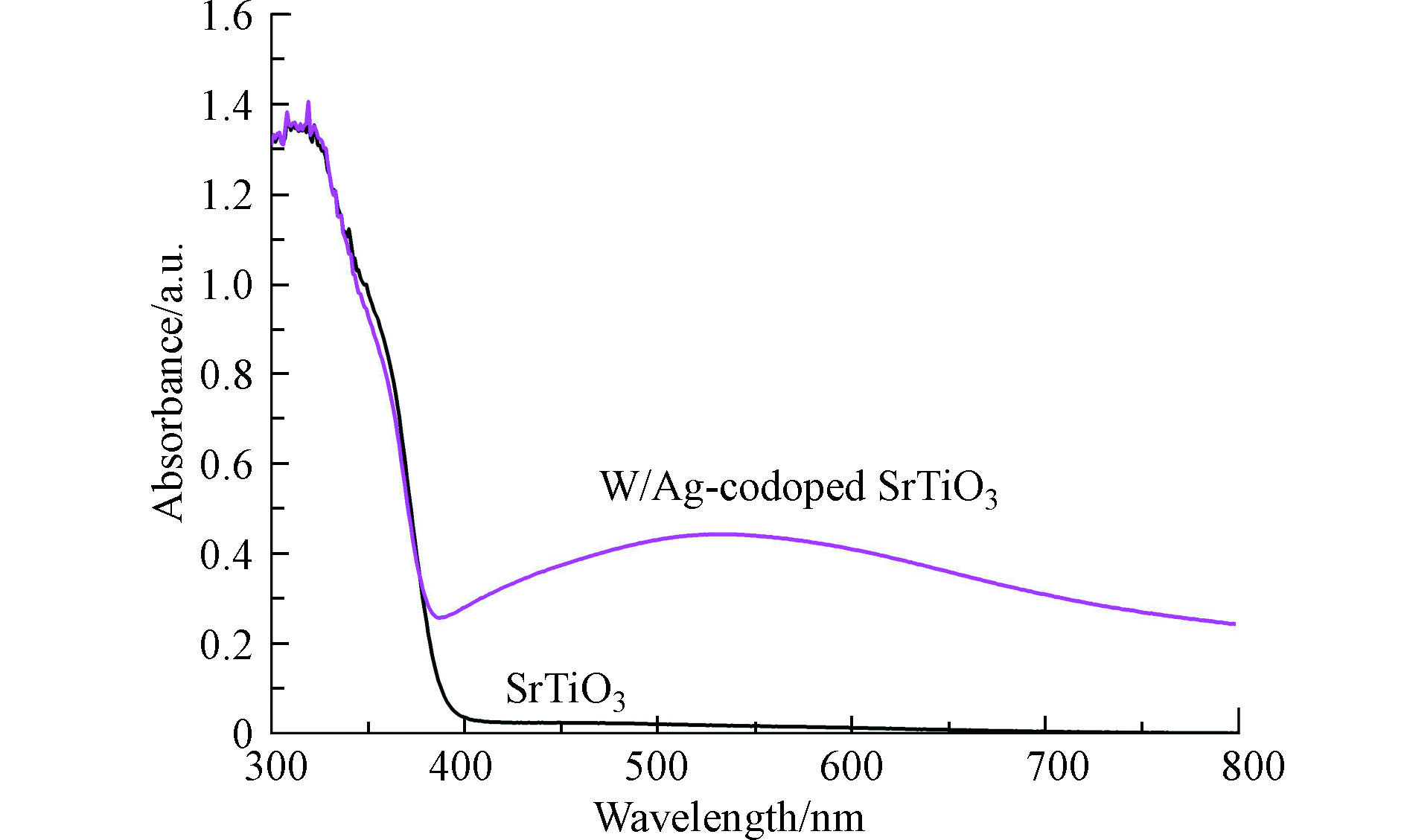
采用UV-vis DRS对纯SrTiO3和W-Ag共掺杂SrTiO3样品进行光学性能测试,如图4所示。纯SrTiO3样品在紫外区表现出明显的光吸收,这表明了纯SrTiO3仅由紫外光驱动的光催化活性,这可能与SrTiO3的带隙吸收有关[21]。对比掺杂后的SrTiO3可以发现,在紫外光波段显示出与纯SrTiO3几乎相同的光学吸收性质,但区别在于W-Ag共掺杂SrTiO3样品在可见光区具有明显的光吸收。可见光吸收增强的原因在于共掺杂在SrTiO3价带上方产生了缺陷能级,这表明了共掺杂可以有效提高SrTiO3的可见光响应[22]。
-
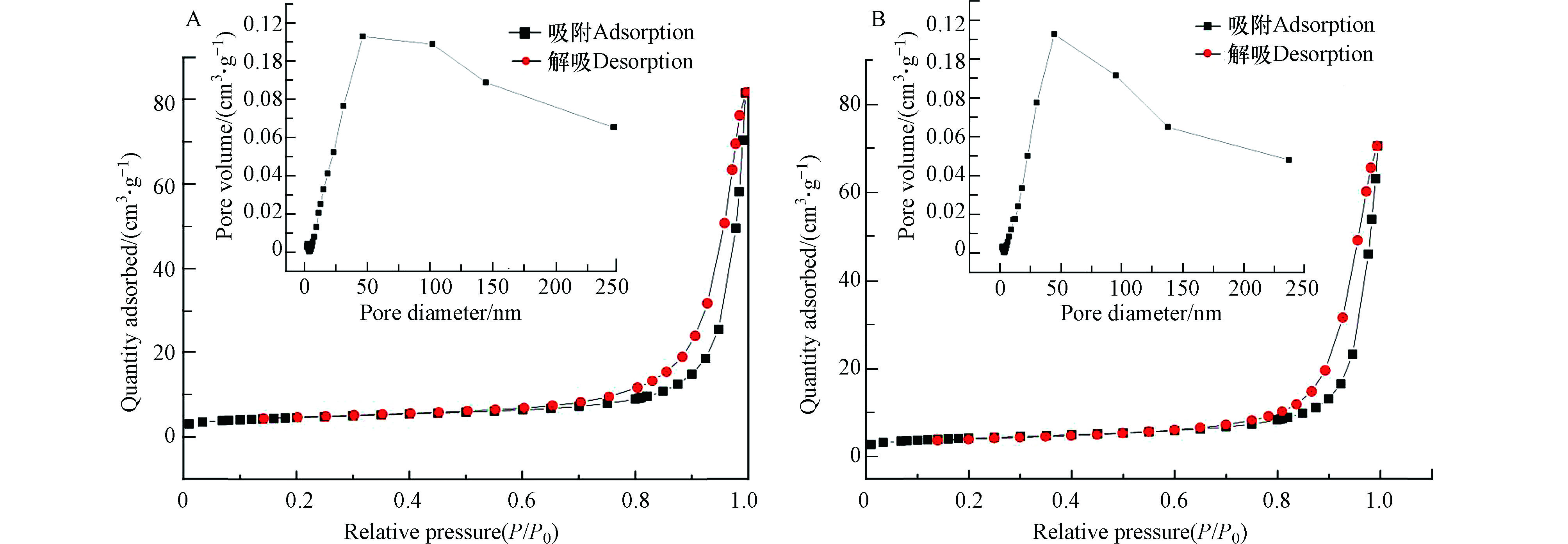
采用氮气吸附-解吸等温线分析纯SrTiO3和W-Ag共掺杂SrTiO3样品的BET表面积和孔径分布,如图5和表1所示。根据IUPAC分类,纯SrTiO3和W-Ag共掺杂SrTiO3样品具有IV型等温线,这是具有非常薄的H3滞回线的介孔材料的特征,其中解吸支向低压延伸,表明形成了狭缝形状的孔隙[23]。根据Barrett - Joyner - Halenda (BJH)模型分析,由等温线吸附支计算得到的多孔微球孔径分布较宽,约为10—200 nm,验证了样品为大孔、中孔结构。纯SrTiO3样品的BET表面积为15.200 m2·g−1,平均孔隙体积为0.086 cm3· g−1。对于W-Ag共掺杂SrTiO3样品,BET表面积为16.523 m2·g−1,平均孔隙体积为0.071 m3·g−1,这与SEM测定的结果高度一致。这些结果表明,W-Ag共掺杂SrTiO3样品比表面积增大,表面的活性中心随之增加,同时缩短了光生电子和空穴转移到样品表面的距离,从某种程度上也抑制了两种载流子的复合,氧化还原反应的效果增强,光催化活性得到提高。与此同时,提供了更多的吸附能力和表面活性。在W-Ag共掺杂后,由于离子的掺杂抑制了SrTiO3颗粒的团聚,因此SrTiO3的孔径相对减小。
-
为了确定W-Ag共掺杂SrTiO3样品的表面组成和价态,进行了XPS分析,如图6(a)所示。图6(a)中的XPS测量光谱表明存在Sr、Ti、W、Ag和O元素。C元素的存在可能是由于样品中残留的C或者是XPS设备中的污染造成的[24]。由图6(b)中观察到O 1s特征峰是不对称的,这表明样品中的表面氧存在两种以上的化学态,在533.24、531.68、529.23 eV处存在3个峰,分别为表面吸附氧、氧空位和晶格氧。相对于纯SrTiO3样品,W-Ag共掺杂SrTiO3样品中氧空位含量增加,且出现了表面吸附氧。其中空位氧和表面吸附氧的存在说明样品表面存在一定的表面缺陷以及羟基团,不同的氧缺陷浓度以及缺陷类型会影响光催化活性,而表面羟基的存在有利于捕获光生电子和空穴,抑制电子-空穴对的复合,有助于光催化活性的提高[25-26]。在图6(c)Sr 3d高分辨光谱中,出现132.41 eV和134.15 eV两个峰值,分别与Sr 3d5/2和Sr 3d3/2的结合能相关,意味着Sr在样品中仅以二价氧化态的形式存在[27]。图6(d)中的高分辨率光谱Ti 2p由Ti 2p1/2和Ti 2p3/2两个峰值组成,集中在463.63 eV和458.01 eV的结合能上,这是SrTiO3样品中Ti4+状态的特征,说明Ti+以+4价的形式存在。图中可以看出掺杂前后样品内部的Ti2p电子结合能没有明显变化,这证明少量金属W和Ag的掺杂不会改变Ti原子周围的宏观化学环境。由图6(e)可以发现,W 4f的峰值为35.55 eV和36.58eV,属于W6+氧化态,因此W以+6价的形式存在。由图6(f)可以观察到Ag 3d的峰值,373.07 eV和367.21 eV两处的能峰与Ag+相对应。以上结果说明W和Ag成功掺杂到了SrTiO3的晶格中,这也与XRD测定的结果一致。
-
纯SrTiO3和W-Ag共掺的SrTiO3样品降解MB的光催化活性和动力学如图7所示。为了排除MB溶液的自然降解,还在相同实验条件下,进行了单独光照实验。如图7(a)所示,在没有催化剂的情况下,MB的降解效率可以忽略不计,这表明MB溶液的降解效果均是由于光催化反应所提供。并且在相同的反应条件下,W-Ag共掺杂SrTiO3样品的光降解活性明显高于纯SrTiO3样品。W-Ag共掺杂SrTiO3样品在6 h内降解效率可达90.5%,而纯SrTiO3样品在6 h内降解效率仅为54.8%。如图7(b)所示,MB的降解遵循一级动力学方程[28-29]。降解速率常数k及其回归相关系数R2数据见表2,R2越接近1,降解过程,越高度符合准一级动力学模型。研究发现,W-Ag共掺杂SrTiO3样品的降解速率常数k值,几乎是纯SrTiO3的5倍。结果表明,在可见光条件下,W-Ag共掺杂可以大大提高SrTiO3的降解速率和光催化效率。
-
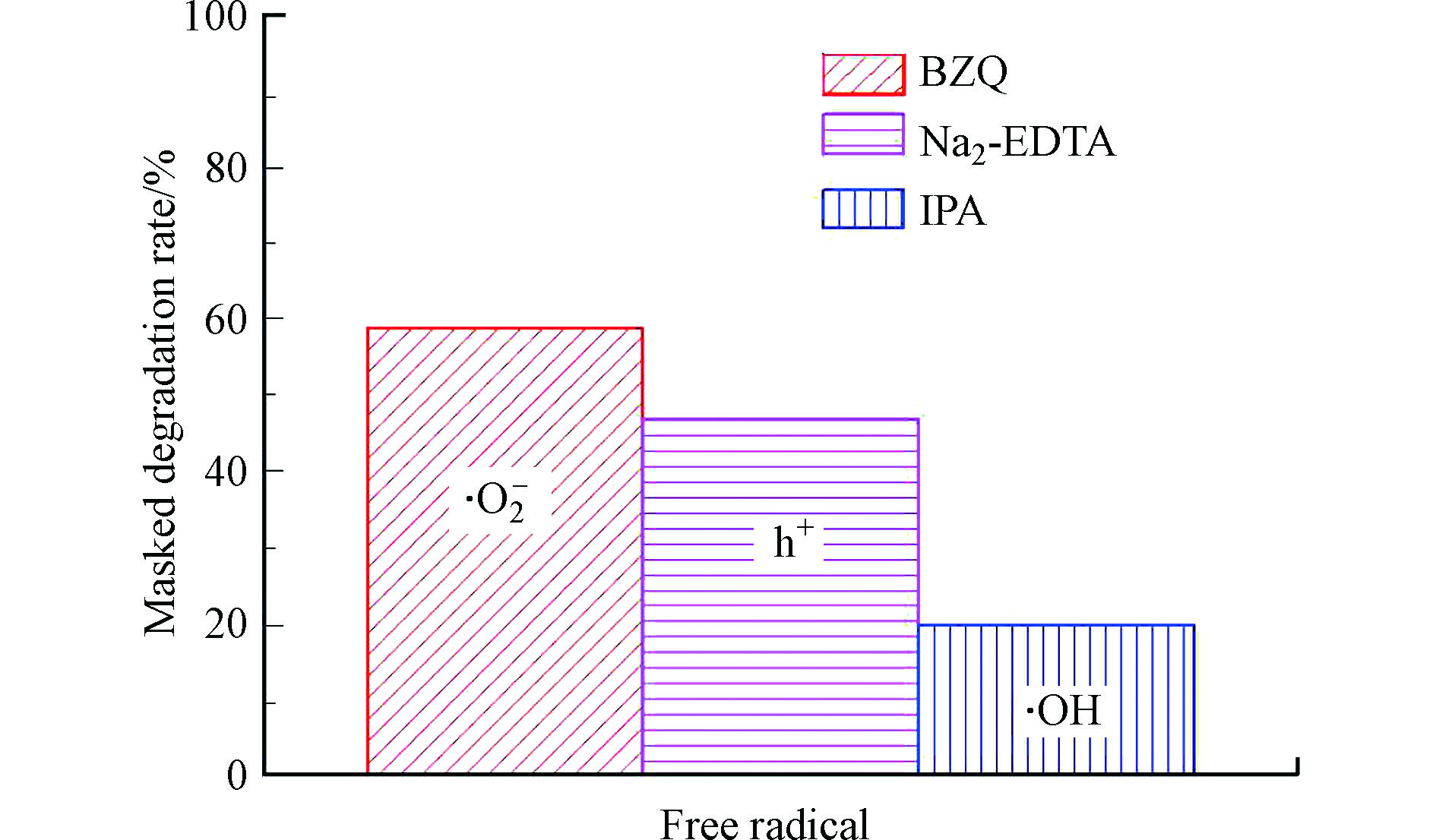
为了探索光催化机理,对W-Ag共掺杂SrTiO3复合催化剂进行自由基掩蔽实验。结果如图8所示。使用乙二胺四乙酸二钠(Na2-EDTA)、异丙醇(IPA)和对苯醌(BZQ),分别作为h+、·OH和·O2−的捕获剂。由图8可知,BZQ、Na2-EDTA、IPA和对降解实验的掩蔽率分别为58.77%、46.78%和19.62%,由此可知,光催化过程中起主要作用的是·O2−,其次为h+,而·OH对光催化效果影响较小。
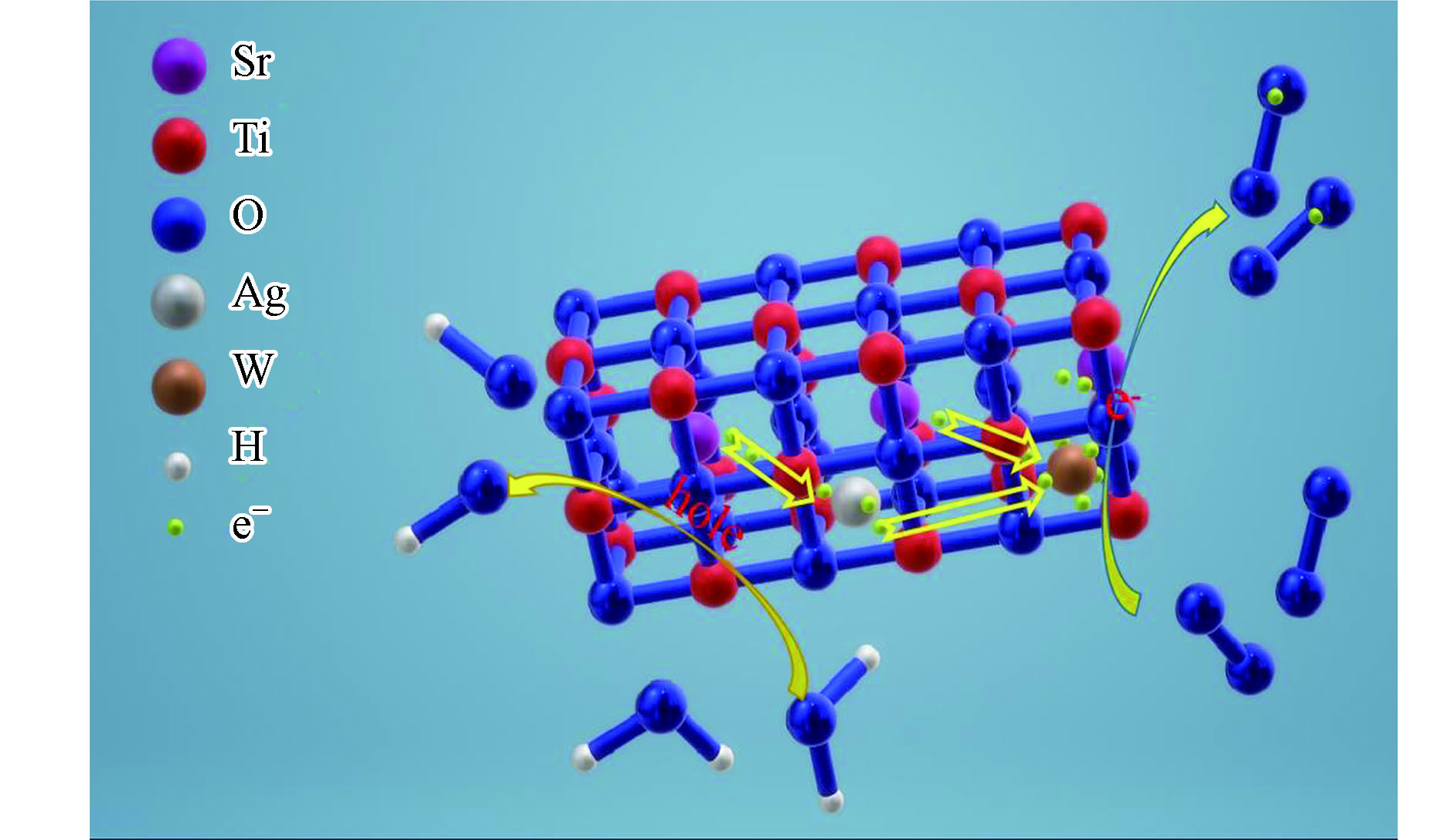
可以由Butler和Ginley模型[30]可知,SrTiO3的CB和VB分别为−1.2 eV和+2.1 eV。SrTiO3材料的价带电位(+2.1 eV)低于OH/·OH(+2.38 eV)和H2O/·OH(+ 2.72 eV)的还原电位,因此,SrTiO3材料的价带中的h+与OH−和H2O反应产生·OH的过程较为微弱。由·OH诱导的MB的降解也较为微弱。由于SrTiO3材料的导带电位(-1.2 eV)超过O2/·O2−(-0.33 eV)的氧化电位[31],SrTiO3的CB中的电子与周围的O2发生的反应强烈,从而进行强烈的光催化降解。W-Ag共掺杂SrTiO3复合材料对亚甲基蓝溶液可能的降解机制如图9所示。经光源照射后,在捕获中心中跃迁的电子与O2结合生成大量的·O2−,·O2−参与光催化降解反应。而电子跃迁后,留下的空穴与水分子反应生成·OH,·O2−和·OH共同作用于MB,直至分解。
-
(1) W和Ag掺杂使SrTiO3晶格发生畸变,降低其粒径尺寸,增大其比表面积,暴露更多的活性位点,提高其对污染物的吸附能力。
(2) W和Ag掺杂,在SrTiO3价带上方产生了缺陷能级,有效提高SrTiO3的可见光响应。
(3) W和Ag掺杂,增加SrTiO3氧空位和表面吸附氧的含量。有效抑制电子-空穴对的复合,提高其光催化活性。
(4)在模拟太阳光条件下,W-Ag共掺杂SrTiO3样品对MB的降解速率常数约为纯SrTiO3的5倍。
W-Ag共掺杂SrTiO3的制备及其光催化性能
Preparation and photocatalytic properties of W-Ag co-doped SrTiO3
-
摘要: 本研究采用溶胶-凝胶法制备W-Ag共掺杂SrTiO3,以亚甲基蓝(MB)为目标污染物,研究W-Ag共掺杂SrTiO3的光催化活性及其效率提升的机制。通过X射线衍射(XRD)、扫描电镜(SEM)、光致发光光谱分析(PL)、紫外-可见漫反射光谱(UV- vis DRS)、比表面积测试(BET)和X射线光电子能谱(XPS)对样品结构、组成和光学性能进行表征。结果表明,W和Ag成功掺入SrTiO3晶体结构中,并引起SrTiO3产生晶格畸变,粒径尺寸减小。相比纯SrTiO3比表面积15.200 m2·g−1,W-Ag共掺杂SrTiO3比表面积增大到16.523 m2·g−1,有利于活性位点的暴露。W和Ag的掺杂增加了SrTiO3晶格内氧空位和表面吸附氧含量,有效抑制电子-空穴对的复合。此外,在SrTiO3价带上方产生了缺陷能级,提高SrTiO3的可见光响应。因此,与纯SrTiO3相比,W-Ag共掺杂SrTiO3显示出了更强的光催化活性。在模拟太阳光条件下,相比纯SrTiO3在6 h内54.8%的降解效率,W-Ag共掺杂SrTiO3的降解效率可达到90.5%,而降解速率常数由0.0861 h−1增加到0.3895 h−1,几乎是纯SrTiO3的5倍。Abstract: In this paper, the novel W-Ag co-doped SrTiO3 samples were prepared by sol-gel method, the photocatalytic activity has been investigated for methylene blue degradation. Structure, composition and morphology of the as-prepared catalysts were characterized using several techniques including X-ray diffraction (XRD)、Scanning electron microscope (SEM)、Photoluminescence spectroscopy (PL)、Uv-visible diffuse reflectance (UV-vis DRS)、Specific surface area (BET) and X-ray photoelectron spectroscopy (XPS). The results show that the successful doping of W and Ag into SrTiO3 crystal lattice was achieved, and the dopants, and the distortion of SrTiO3 crystal lattice caused by doping resulted in the decrease of crystallite size of SrTiO3. W-Ag co-doped SrTiO3 sample has a surface area of about 16.523 m2·g−1, which is larger than that of pure SrTiO3 (15.200 m2·g−1). The relatively large specific surface area of W-Ag co-doped SrTiO3 sample provides a greater number of reactive sites for the photocatalytic process. Doping of W and Ag increases the oxygen vacancy concentration and surface absorbed oxygen, which suppress recombination rate of the photogenerated electron-hole pairs. Besides, the defect energy level is generated above valence band of SrTiO3, which improves its visible light response. So, W-Ag co-doped SrTiO3 show higher photocatalytic activity compared with pure SrTiO3. The photocatalytic degradation efficiency of W-Ag co-doped SrTiO3 to MB reaches 90.5% after 6 h under the simulated sunlight illumination, much higher than that of pure SrTiO3 (54.8%), and the degradation rate constant of MB for W-Ag co-doped SrTiO3 is 0.3895 h−1, which was almost 5 times as much as pure SrTiO3.
-
Key words:
- strontium titanate /
- simulated sunlight /
- doping /
- sol-gel process
-
药品和个人护理品类污染物(如内分泌干扰物、抗生素等)导致的水体污染问题是生态安全和人类身体健康的一大威胁[1-3]。基于过硫酸盐的高级氧化技术可通过产生羟基自由基(OH•)、硫酸根自由基(SO4•−)、单线态氧(1O2)等活性氧物种降解水中多种类型的有机污染物,在药、护品类污染物处理方面受到了广泛关注[1]。与过一硫酸盐(peroxymonosulfate,PMS)相比,过二硫酸盐(peroxydisulfate,PDS)价格低廉、水溶性好、稳定性高便于储存和运输,已被广泛用于催化降解有机污染物[1]。PDS可通过热活化、碱活化、金属离子催化、金属氧化物催化等多种方法活化,其中基于纳米金属氧化物(如Co3O4等)的异相催化由于催化剂价格低廉、反应条件温和、催化活性高等优点,是目前研究的一个重要方向[2]。然而,纳米尺寸的金属氧化物分散于水中易团聚,导致催化剂活性位点暴露有限,并且分散于水中的纳米催化剂还存在难以分离和回收的问题,极大地限制了其应用。
将金属氧化物纳米催化剂负载于活性炭、泡沫金属、矿物颗粒以及陶瓷膜等三维载体的表面,不仅可以有效缓解氧化物纳米颗粒的团聚问题,而且便于分离和回收,对纳米金属氧化物活化过硫酸盐降解有机物具有重要意义[4]。现阶段,金属氧化物主要通过浆料涂覆的方式负载于载体表面,合成方法简单但稳定性较差[5]。添加高分子粘结剂可增强其稳定性,但催化体系中引入导电性较差的高分子不利于过硫酸活化过程中电子的转移,同时添加粘结剂也可能会带来二次污染[6]。因此,亟需发展一种可将金属氧化物原位负载于三维载体表面的绿色合成方法。植物多酚如单宁酸(tannic acid,TA)普遍存在于植物的根、茎、叶及果实中,是一种价格低廉的生物质[7]。TA分子富含邻二酚羟基,具有较强的金属离子络合能力和优异的表面粘附性能,可与多种金属离子(Co2+、Fe2+、Cu2+等)在聚乙烯球、陶瓷、玻璃等不同载体表面配位形成金属-多酚配合物[7]。作为由金属离子和有机配体组成的复合物,金属-多酚配合物可进一步热解制成不同种类的金属氧化物,并且研究表明有机配体TA分解还会产生多孔结构而形成多孔结构的金属氧化物[8]。
基于TA分子的金属离子络合能力和表面粘附性能,本研究以具有稳定物理化学性质且价格低廉的气泡石为载体,通过在其表面包覆Co2+与TA的配合物,进一步热解将纳米尺寸的Co3O4原位负载于气泡石表面,制备易分离回收的负载型Co3O4催化剂,通过SEM、XRD、ICP等详细分析了负载型Co3O4的结构和组成。利用负载型Co3O4催化剂活化PDS降解水中的双酚A(bis-phenol A,BPA)、磺胺甲恶唑(sulfamethoxazole,SMX)等药、护品类有机污染物,分析了溶液初始pH、PDS浓度、催化剂投加量、共存化学组分等对有机物降解性能的影响,并通过电子顺磁共振分析、化学淬灭实验、光谱分析等手段深入分析了PDS的活化机制和有机物的降解机理。
1. 材料与方法
1.1 实验试剂
主要试剂包括六水合硝酸钴(Co(NO3)2·6H2O)、单宁酸(tannic acid)、双酚A(bisphenol A)、盐酸(HCl,1 mol·L−1)、过硫酸钠(sodium persulfate, Na2S2O8)、氢氧化钠(NaOH,1 mol·L−1)、叔丁醇(tert-butyl alcohol, TBA)、对苯醌(p-benzoquinone, BQ)、碳酸钠(Na2CO3)、氯化钠(NaCl)、硝酸钠(NaNO3)、硫酸钠(Na2SO4)、腐殖酸(HA)、甲醇、乙腈、无水乙醇等,所有试剂均为分析纯,实验用水为超纯水。
1.2 实验方法
1)负载型Co3O4的制备:将尺寸0.5 cm×0.5 cm×0.5 cm的气泡石颗粒置于Co(NO3)2与TA的混合溶液中,利用TA分子的表面粘附特性及其与Co2+的配位反应,在气泡石颗粒表面形成Co-TA包覆层,进一步在空气气氛下焙烧制得负载于气泡石表面的Co3O4催化剂。具体步骤如下:将5 g Co(NO3)2和10 g TA依次溶解于250 mL纯水,然后加入30 g气泡石载体搅拌30 min,加入5 mL氨水后继续搅拌1 h,将修饰后的气泡石用纯水反复清洗。重复上述负载步骤4次后,制得负载有Co-TA配合物的气泡石颗粒,充分干燥后将其置于马弗炉中在400 °C下焙烧2 h (升温速率设置为2 ℃·min−1),即制得负载型Co3O4催化剂。
2)材料表征:通过场发射扫描电子显微镜(Hitachi, S-4800)分析负载型Co3O4的形貌与元素组成,利用Rigaku Ultimate IV型X射线衍射(XRD)表征其晶体结构,借助X射线光电子能谱(XPS)研究催化剂反应前后各元素的化学价态,采用电感耦合等离子体发射光谱仪(ICP, NexION 350D)测定浸出钴离子的浓度以及气泡石颗粒表面Co3O4的负载量。ATR-FTIR测试以超纯水为背景,将PDS与Co3O4纳米催化剂的混合物滴至ATR附件晶体表面,在400~3000 cm−1内至少扫描3次,扫描分辨率为4 cm−1。
3)BPA降解实验:本研究通过催化降解BPA评价负载型Co3O4活化PDS的性能。室温条件下,配制50 mL 0.04 mmol·L−1的BPA溶液,加入3.0 g负载型Co3O4催化剂和0.5 mL 40 mmol·L−1的PDS溶液,然后于特定时间取1 mL水样与0.5 mL甲醇混合以终止反应,进一步用0.22 μm微孔滤膜过滤后,通过高效液相色谱仪测定BPA的浓度,流动相为水和乙腈的混合溶液,两者的体积比为1:1,流速为1 mL·min−1。
2. 结果与讨论
2.1 负载型Co3O4催化剂的表征
图1为气泡石载体负载Co3O4前后的照片及其表面Co3O4纳米催化剂的微观结构。如图1(a)所示,气泡石表面粗糙呈白色,负载Co3O4后变为灰褐色(图1(b)),表明Co3O4纳米催化剂成功负载于其表面。通过SEM表征了气泡石表面Co3O4纳米催化剂的微观结构,如图1(c)所示,气泡石光滑的表面存在大量的纳米颗粒团簇,进一步表明Co3O4纳米催化剂的成功负载。纳米团簇的高倍SEM图表明Co3O4纳米催化剂呈多孔结构(图1(d)),这可能是Co-TA配合物中有机组分TA分解导致的。多孔结构利于催化位点的充分暴露,利于PDS的活化和有机污染物的降解[9]。
图2(a)为Co-TA焙烧衍生粉体Co3O4及气泡石负载Co3O4的XRD谱图。粉体催化剂在2θ为31.27°、36.85°、44.8°、59.35°、65.23°的衍射峰分别对应于立方相Co3O4的(220)、(311)、(400)、(511)和(440)晶面(JCPDS-no.42-1467)。气泡石的XRD图谱表明其主要成分为SiO2 (JCPDS-no.78-2315);SiO2化学性质稳定,便于在复杂环境中使用。气泡石表面负载催化剂后,在2θ为31.27°、44.81°检测到了属于Co3O4的衍射峰,分别对应于立方相Co3O4的(220)和(400)晶面,进一步表明Co3O4成功负载于气泡石表面。通过热重分析研究了Co-TA配合物的热分解过程。如图2(b)所示,Co-TA配合物的残余质量在20~400 °C内持续降低,这主要归咎配合物表面水分子的脱附以及有机配体TA的氧化分解[10]。DTA分析表明Co-TA分解过程中在380 °C出现了明显的吸热峰,表明Co-TA热解生成了新的固相。400 °C后配合物的质量损失保持不变,表明Co-TA中的有机配体在400 °C下完全分解,因此本研究将负载型Co3O4催化剂的合成温度设定为400 °C。通过ICP-MS分析了气泡石表面Co3O4的负载量,结果表明每克气泡石表面负载有1.25 mg的Co3O4纳米颗粒。
2.2 负载型Co3O4的催化性能研究
在反应温度为(25±1) °C、负载型Co3O4投加量60 g·L−1(即0.075 g·L−1 Co3O4纳米颗粒)、BPA初始浓度为0.04 mmol·L−1、PDS初始浓度为0.4 mmol·L−1和pH为7的条件下测试了负载型Co3O4活化PDS降解BPA的性能。如图3(a)所示,PDS氧化降解BPA的能力有限,120 min内BPA的去除率仅为9%,同时负载型Co3O4仅吸附了4.8%的BPA。负载型Co3O4活化PDS可有效降解BPA,120 min内BPA的去除率达到了100%。BPA的降解遵循拟一级反应动力学,反应动力学常数为0.04 min−1 (图3(b))。ICP分析表明催化反应结束后溶液中Co2+的质量浓度为0.55 mg·L−1,低于地表水环境质量标准(GB 3838-2002D)规定的标准(1.0 mg·L−1),表明负载型Co3O4具有良好的稳定性。溶出的Co2+在相同实验条件下催化PDS仅降解了11%的BPA,表明负载型Co3O4主要通过异相催化反应降解有机物[10]。图3(b)反映了负载型Co3O4活化PDS降解不同类型有机物的性能,苯酚(Phenol)、对乙酰氨基酚(AAP)、磺胺甲恶唑(SMX)均可被有效去除,相同反应条件下120 min内的去除率分别为78.2%、93.6%、67.3%,对应的反应动力学常数分别为0.01、0.02、0.01 min−1(图3(d))。以上结果表明负载型Co3O4活化PDS可催化降解不同类型的药、护品类有机污染物。
2.3 实验因素的影响
图4(a)反映了溶液初始pH分别为3、5、7、9、11时,负载型Co3O4活化PDS降解BPA的性能。在pH=3~9内,BPA均可得到有效去除,120 min内BPA的去除率均达到100%,同时反应速率也并未受到显著影响;然而,当pH提升至11时,BPA的降解受到抑制,120 min内BPA的去除率降低了24.4%,反应速率也由中性时的0.04 min−1降至0.01 min−1,这可能是由于碱性条件下OH•的氧化还原电位降低所致[11]。图4(b)为不同PDS投加量下,负载型Co3O4对BPA的催化降解性能。当PDS浓度由0.1 mmol·L−1增加到0.4 mmol·L−1时,BPA的去除率从20.9%增加到98.2%,反应速率也由0.002 min−1提升至0.03 min−1。增加PDS的浓度可增加活性氧物种的生成量,进而促进有机物的催化降解[12]。然而,进一步增加PDS的浓度至0.8 mmol·L−1和1.6 mmol·L−1时,BPA的降解性能并未得到进一步提升。这可能是由于负载型Co3O4的催化位点有限,不能完全活化反应体系中的PDS[13]。增加催化剂的投加量可提供更多的催化位点而充分活化PDS,进而产生更多的活性氧物种而显著提升有机物的降解效率[14]。如图4(c)所示,在BPA溶液体积为50 mL的情况下,当负载型Co3O4催化剂的投加量由1.5 g增加至3.0 g时,BPA的降解速率由0.02 min−1提高至0.037 min−1,当催化剂的投加量进一步增加至6.0 g时,BPA在60 min即可被完全去除,降解速率达0.039 min−1。这表明增加负载型Co3O4的剂量可显著提升PDS的有效利用率。
为考察水中常见无机阴离子对负载型Co3O4活化PDS降解有机物性能的影响,研究了Cl−、NO3−、CO32−对BPA去除效率和降解速率的影响。如图4(d)所示,在负载型Co3O4/PDS体系中加入10 mmol·L−1 Cl−并未降低BPA的去除效率,同样加入10 mmol·L−1的NO3−也未影响BPA的去除。Co3O4活化PDS降解有机物主要有2种途径:一种是基于SO4•−和OH•的自由基氧化;另一种是基于单线态氧(1O2)的非自由基氧化[15]。在自由基途径中,Cl−、NO3−等无机阴离子会竞争消耗强氧化性的SO4•−和OH•,进而抑制有机污染物的降解[16-18]。在本研究中,Cl−和NO3−对BPA的去除影响较弱,表明自由基氧化不是Co3O4活化PDS降解有机物的主要途径。然而,向反应体系中添加10 mmol·L−1的CO32−可显著抑制BPA的去除,同样反应条件下BPA仅去除了16.64%,同时反应速率由0.04 min−1降低至了0.001 min−1。CO32−是一种常用的1O2淬灭剂,其对BPA降解的显著抑制表明负载型Co3O4活化PDS降解有机物是1O2主导的非自由途径[19]。除了无机阴离子,天然有机物如腐殖酸(HA)也是一种常见的水体背景成分[6]。在10 mg·L−1 HA存在的情况下,负载型Co3O4催化降解有机物的效率也未受到显著影响,进一步说明本反应体系中有机物的降解为非自由基途径[20]。综上所述,负载型Co3O4/PDS体系不仅能够在较宽的pH范围内降解有机物,而且对无机阴离子和腐殖酸等常见的水体背景成分具有较强的抗干扰能力,因此,有着较强的应用潜力。
2.4 活性氧物种鉴定
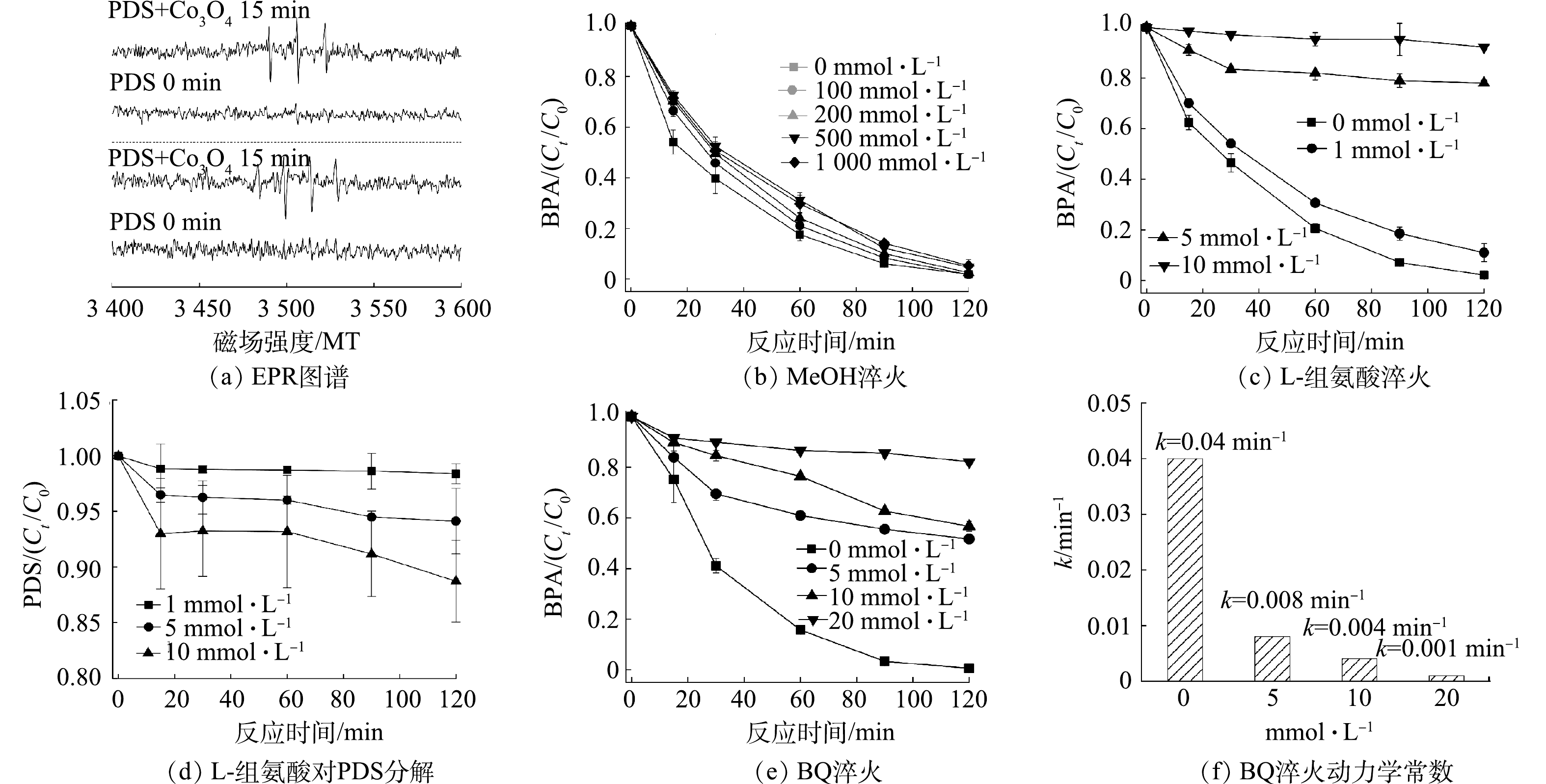
为明确负载型Co3O4活化PDS降解有机物的机理,通过EPR鉴定分析了该体系产生的活性氧的种类。如图5(a)所示,当仅有PDS时,以DMPO为自旋捕获剂未检测到任何信号,而当加入负载型Co3O4催化剂后,EPR谱图观测到了峰强度为1: 2 : 2 : 1的特征峰,这是催化产生的OH•被DMPO捕获所致,表明负载型Co3O4活化PDS产生了OH•[21]。此外,以TEMP为1O2捕获剂还检测到了TEMP-1O2的特征峰,因此,负载型Co3O4活化PDS也产生了1O2[22]。进一步通过化学淬灭实验判别了反应体系中OH•和1O2对BPA降解的贡献。图5(b)反映了不同浓度MeOH的淬灭效果,可以看出MeOH对BPA的降解影响有限,在1 000 mmol·L−1 MeOH存在的情况下,BPA的去除率仍高达94.7%。MeOH可与SO4•−和OH•快速反应,反应速率常数分别为k 分别为 2.5×107 (mol·s)−1和9.7×108 (mol·s)−1,是常用的自由基淬灭剂;MeOH对负载型Co3O4/PDS有限的淬灭能力表明该体系降解有机物的过程中,自由基的氧化作用有限[7]。然而,L-组氨酸可显著抑制BPA的降解,如图5(c)所示,1 mmol·L−1的组氨酸使得BPA的降解率由100%降低至89%;当L-组氨酸的浓度增加至5 mmol·L−1时,BPA的去除率进一步降低至21.98%,反应速率也由0.04 min−1降低至0.002 min−1。L-组氨酸具有一定的还原性,可能会消耗PDS而降低负载型Co3O4催化降解BPA的能力[23]。为排除L-组氨酸消耗PDS对淬灭实验的干扰,研究了不同浓度L-组氨酸对PDS的降解效率。如图5(d)所示,L-组氨酸分解PDS的能力有限,例如5 mmol·L−1的L-组氨酸在120 min内仅分解了5.8%的PDS。因此,L-组氨酸对负载型Co3O4/PDS降解BPA的抑制作用主要归咎于其对活性氧物种的淬灭,而L-组氨酸是常用的1O2淬灭剂,这表明负载型Co3O4活化PDS降解有机物是以1O2为主导的非自由基氧化途径。过渡金属氧化物活化PDS产生1O2已被广泛报道,有研究表明,O2•−是1O2生成的重要中间体(
2O2·−+2H2O→21O2+2OH−+H2O2 2.5 PDS活化机理研究
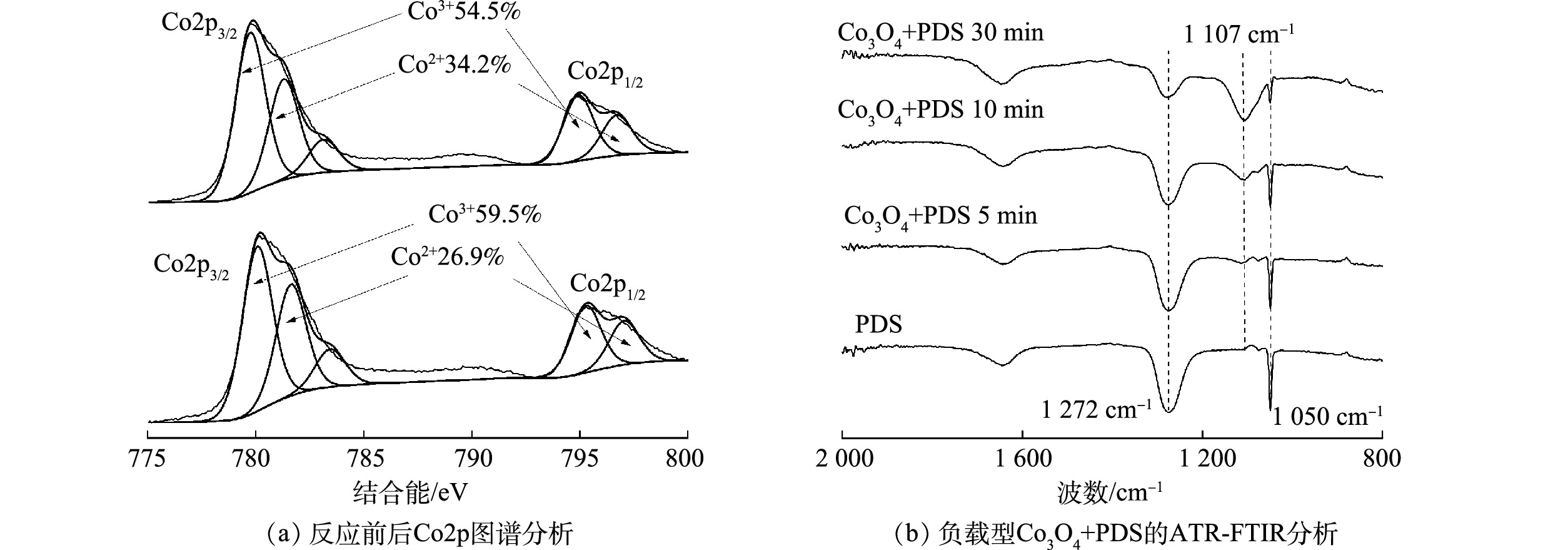
过渡金属氧化物主要通过金属离子的价态循环活化过硫酸盐[26]。为解析负载型多孔Co3O4活化PDS的机理,通过XPS分析了Co3O4中Co元素的价态及其反应前后含量的变化。如图6(a)所示,Co2p在794.9 eV和779.7 eV的特征峰分别对应于Co2p1/2和Co2p3/2,而Co2p3/2的高分辨XPS谱图拟合结果表明,781.2 eV和779.7 eV处的峰分别对应于Co2+和Co3+,所占比例分别为34.2%和54.5%。反应后,Co3O4表面Co2+、Co3+比例变化表明Co3+/Co2+的氧化还原参与了PDS的活化[27]。进一步通过原位ATR-FTIR分析研究了PDS分子在负载型Co3O4表面的反应机理。如图6(b)所示,在1 050 cm−1和1 272 cm−1处检测到PDS振动峰,加入Co3O4催化剂后在其表面观测到了PDS的特征峰的位置并且未发生偏移,表明PDS吸附于Co3O4催化剂的表面。此外,在Co3O4/PDS体系中还观测到了SO42‒的特征峰(1 107 cm−1),表明Co3O4活化PDS产生了SO42‒;随着反应时间的增加PDS特征峰的强度逐渐降低,而SO42‒特征峰的强度逐渐增加,表明PDS在Co3O4催化剂表面持续分解[1]。
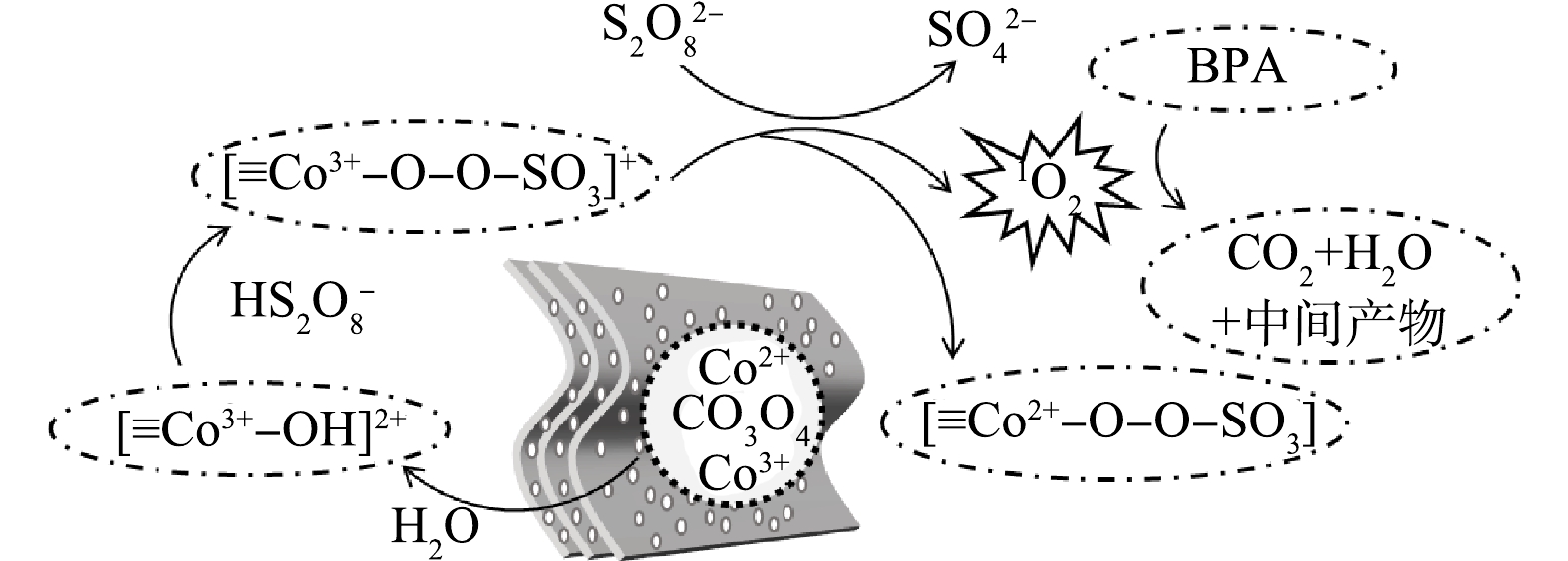
金属氧化物(MOx)活化过硫酸盐时,吸附于其表面的水分子会解离形成MOx-OH[19]。因此,结合XPS和ATR-FTIR分析,提出了负载型Co3O4活化PDS降解BPA的可能反应机理(图7)。首先,PDS分子通过氢键与[≡Co3+—OH]2+结合形成[≡Co3+—O—O—SO3]+络合物(式(1)),该络合物具有较高的氧化电势,还原PDS分子生成O2•−,同时Co3+被还原为Co2+形成中间态[≡Co2+—OH] (式(2)),随之生成的O2•−进一步反应生成1O2 (式(3))。中间态[≡Co2+—O—O—SO3]通过内电子转移被氧化为≡Co3+—OH,同时生成少量的自由基(式(4))。如上所述,负载型Co3O4/PDS体系中自由基对有机物的降解贡献有限,因此1O2进一步氧化有机物将其分解为中间产物或者H2O和CO2 (式(5))。本研究中,负载型Co3O4有效活化PDS主要有2点原因,一是负载型Co3O4避免了纳米催化剂的团聚,可暴露更多的活性位点而提升催化效率;另一方面,Co-TA配合物热解会产生富含氧缺陷的Co3O4[28],而氧缺陷可有效提升PDS分子在Co3O4表面的吸附,也会提升内电子催化PDS的效能。
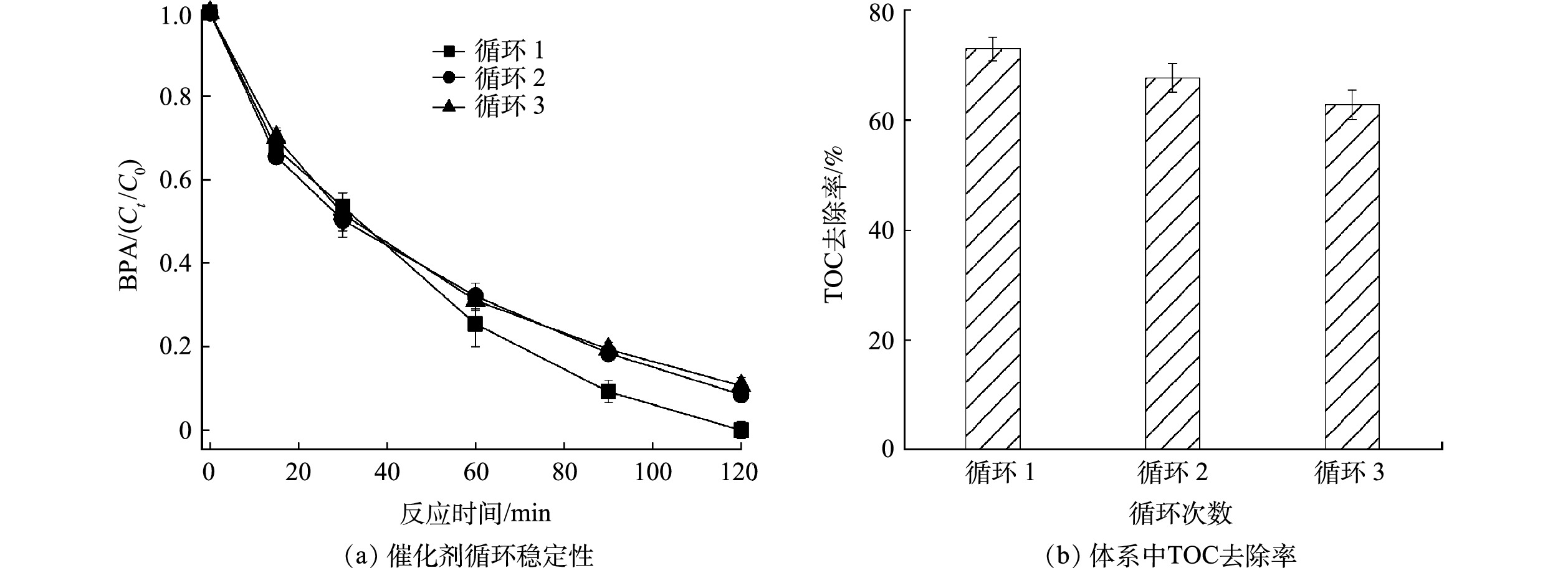
2[≡Co3+−OH]2++HS2O8−→2[≡Co3+−O−O−SO3]++3H+ (1) 2[≡Co3+−O−O−SO3]++4H2O+S2O82−→2[≡Co2+−OH]+4SO42−+2O2·−+6H+ (2) 2O2·−+2H2O→21O2+2OH−+H2O2 (3) [≡Co2+−O−O−SO3]+H2O→≡Co3+−OH+SO4·−+OH· (4) 1O2+有机物→H2O+CO2+中间产物 (5) 催化剂的稳定性是衡量其实际应用潜力的一个重要因素,本研究通过循环降解实验研究了负载型Co3O4的稳定性。如图8(a)所示,3次循环后负载型Co3O4对BPA的去除率仍保持在89%,表明负载型Co3O4具有良好的稳定性。循环降解过程中催化活性的轻微降低可能是BPA的降解产物堵塞活性位点导致的[10]。此外,XRD分析表明循环使用后负载型Co3O4的晶相没有明显变化(图2(a)),进一步说明负载型Co3O4具有良好的稳定性。负载型Co3O4可有效矿化BPA(图8(b)),TOC去除率高达73%,而且3次循环后TOC的去除率仍高达63%,表明负载型Co3O4可持续稳定地处理水中酚类有机污染物。
3. 结论
1)基于植物多酚的界面配位原理,通过在三维矿物载体表面原位负载Co3O4纳米颗粒制得了易分离回收的负载型Co3O4催化剂,比Co3O4粉体催化剂展现出更优异的催化活性和良好的稳定性。
2)负载型Co3O4催化剂活化PDS可高效降解BPA、SMX、AAP等多种类型的药、护品类有机污染物,中性条件下,负载型Co3O4投加量为60 g·L−1(即0.075 g·L−1 Co3O4纳米颗粒),在BPA/PDS摩尔比为1:10的情况下可在120 min内将BPA完全降解。
3)负载型Co3O4主要通过内电子转移活化PDS,降解有机物时自由基氧化的作用有限,主要是1O2主导的非自由基氧化途径,对无机阴离子和腐殖酸等水体背景成分有着较强的抗干扰能力,在实际水体处理方面展现出广阔的应用前景。
-
图 7 (a)纯SrTiO3和W-Ag共掺杂SrTiO3样品降解MB的光催化活性比较,(b)纯SrTiO3和W-Ag共掺杂SrTiO3样品的相应一级动力学图
Figure 7. (a) Comparison of photocatalytic activity of pure and W-Ag-codoped SrTiO3 samples for the degradation of MB in aqueous solution and (b) the corresponding first-order kinetics plot of pure and W-Ag-codoped SrTiO3 samples
表 1 SrTiO3、W-Ag共掺杂SrTiO3的孔性质
Table 1. Pore properties of SrTiO3 and W-Ag co-doped SrTiO3
样品Sample 比表面/(m2 ·g−1)Specific surface area 孔容/(cm3 ·g−1)Pore volume 平均孔径/nmAverage aperture SrTiO3 15.200 0.086 21.129 W-Ag共掺杂SrTiO3 16.523 0.071 19.920 表 2 掺杂对SrTiO3催化降解动力学参数的影响
Table 2. Effect of doping on kinetic parameters of catalytic degradation of SrTiO3
k/h−1 R2 纯 SrTiO3 0.0861 0.9481 W-Ag共掺杂SrTiO3 0.3895 0.9415 -
[1] NORVIU K W, YU J K, CHI Y, et al. Effect of adding Au nanoparticles to TiO2 films on crystallization, phase transformation, and hotocatalysis [J]. Journal of Materials Research, 2018, 33(4): 467-481. doi: 10.1557/jmr.2018.16 [2] 齐中, 王熙, 李来胜, 等. 基于水热法制备的TiO2/MOS2复合光催化剂及其光催化制氢活性 [J]. 环境化学, 2016, 35(5): 1027-1034. doi: 10.7524/j.issn.0254-6108.2016.05.2015112403 QI Z, WANG X, LI L S. Development of TiO2 /MoS2 by hydrothermal method for photocatalytic hydrogen generation under solar light [J]. Environmental Chemistry, 2016, 35(5): 1027-1034(in Chinese). doi: 10.7524/j.issn.0254-6108.2016.05.2015112403
[3] 赵真艺, 沈鑫怡, 陈定宁, 等. NH2-nFe3O4@ZnO@Ce磁性复合材料的制备及其对三氯酚污染物的光催化降解 [J]. 环境化学, 2020, 39(3): 643-652. doi: 10.7524/j.issn.0254-6108.2019080501 ZHAO Z Y, SHEN X Y, CHEN D N, et al. Preparation of NH2-nFe3O4@ZnO@Ce magnetic composite and its photocatalytic degradation of trichlorophenol [J]. Environmental Chemistry, 2020, 39(3): 643-652(in Chinese). doi: 10.7524/j.issn.0254-6108.2019080501
[4] GU L, WEI H H, PENG Z J, et al. Defects enhanced photocatalytic performances in SrTiO3 using laser-melting treatment [J]. Journal of Materials Research, 2016, 32(4): 748-756. [5] TAN H Q, ZHAO Z, ZHU W B, et al. Oxygen vacancyenhanced photocatalytic activity of pervoskite SrTiO3 [J]. Acs Appl Mater Interfaces, 2014, 21: 19184-19190. [6] FU X, LI H, LV R, et al. Synthesis of Mn2+ doped ZnS quantum dots/ZIF-8 composite and its applications as a fluorescent probe for sensing Co2+ and dichromate [J]. Journal of Solid State Chemistry, 2018, 264: 26-35. [7] JIANG J Z, JIA Y S, WANG Y B, et al. Insight into efficient photocatalytic elimination of tetracycline over SrTiO3(La, Cr) under visible-light irradiation: The relationship of doping and performance [J]. Applied Surface Science, 2019, 486: 93-101. doi: 10.1016/j.apsusc.2019.04.261 [8] JIN S W, SHU Y, QI W Z, et al. Influences of the factors on photocatalysis of fluorine-doped SrTiO3 made by mechanochemical [J]. Solid State Ionics, 2004, 172: 191-195. doi: 10.1016/j.ssi.2004.05.016 [9] SHAH Z H, GE Y, YE W, et al. Visible light activation of SrTiO3 by loading Ag/AgX (X = Cl, Br) for highly efficient plasmon-enhanced photocatalysis [J]. Materials Chemistry and Physics, 2017, 198: 36-73. [10] RAHMAN I Q, AHMAD M, MISRA S K, et al. Efficient degradation of methylene blue dye over highly reactive Cu doped strontium titanate (SrTiO3) nanoparticles photocatalyst under visible light [J]. Journal of Nanoence & Nanotechnology, 2012, 12: 7181-7186. [11] ATKINSON I, PARVULESCU V, PANDELE CUSU J, et al. Influence of preparation method and nitrogen (N) doping on properties and photo-catalytic activity of mesoporous SrTiO3 [J]. Journal of Photochemistry & Photobiology A Chemistry, 2018, 368: 12-41. [12] ZHANG C, JIA Y, JING Y, et al. DFT study on electronic structure and optical properties of N-doped, S-doped, and N/S co-doped SrTiO3 [J]. Physica B:Condensed Matter, 2012, 407: 4649-4654. doi: 10.1016/j.physb.2012.08.038 [13] YANG D, ZHAO X, ZOU X, et al. Removing Cr (Ⅵ) in water via visible-light photocatalytic reduction over Cr-doped SrTiO3 nanoplates [J]. Chemosphere, 2019, 215: 586-594. doi: 10.1016/j.chemosphere.2018.10.068 [14] ZhOU D D, ZHAI P P, HU G T, et al. Upconversion luminescence and enhanced photocatalytic hydrogen production for Er3+ doped SrTiO3 nanopaeticles [J]. Chemical Physics Letters, 2018, 711: 77-85. doi: 10.1016/j.cplett.2018.09.024 [15] LUO Y, DEG B, PU Y, et al. Interfacial coupling effects in g-C3N4/SrTiO3 nanocomposites with enhanced H2 evolution under visible light irradiation [J]. Applied Catalysis B:Environmental, 2019, 247: 1-25. doi: 10.1016/j.apcatb.2019.01.089 [16] SHAH Z H, GE Y, YE W, et al. Visible light activation of SrTiO3 by loading Ag/AgX (X = Cl, Br) for highly efficient plasmon-enhanced photocatalysis [J]. Materials Chemistry and Physics, 2017, 198: 73-78. doi: 10.1016/j.matchemphys.2017.05.002 [17] ANITHA B G, DEVI L G. Study of reaction dynamics of photocatalytic degradation of 4-Chlorophenol using SrTiO3, sulfur doped SrTiO3, silver metallized SrTiO3 and silver metallized sulfur doped SrTiO3 catalysts: Detailed analysis of kinetic results [J]. Surfaces and Interfaces, 2019, 16: 50-58. doi: 10.1016/j.surfin.2019.04.009 [18] KAVITHA V, MAHALINGAM P, JEYANTHINATH M, et al. Optical and structural properties of ungsten-doped barium strontium titanate [J]. Materials Today:Proceedings, 2019, 11: 1-4. doi: 10.1016/j.matpr.2018.12.097 [19] KAVIYARASAN K, VINOTHV, et al. Photocatalytic and photoelectrocatalytic performance of sonochemically synthesized Cu2O@TiO2 Heterojunction Nanocomposites [J]. Ultrasonics Sonochemistry, 2019, 51: 223-246. doi: 10.1016/j.ultsonch.2018.10.022 [20] WU G L, XIAO L S, GUO L S, et al. Fabrication and excellent visible-light-driven photodegradation activity for antibiotics of SrTiO3 nanocube coated CdS microsphere heterojunctions [J]. RSC Advances, 2016, 24: 19878-19902. [21] DUAN C L, SONG J L, WANGB Y, et al. Lactic acid assisted solvothermal synthesis of BiOClxI1–x solid solutions as excellent visible light photocatalysts [J]. Chemical Research in Chinese Universities, 2019, 236: 326-334. [22] HWANG D W, KIM H G, LEE J S, et al. Photocatalytic hydrogen production from water over M-Doped La2Ti2O7 (M = Cr, Fe) under visible light irradiation [J]. Journal of Physical Chemistry B, 2015, 109: 2093-2102. [23] GUAN X J, GUO L J, et al. Cocatalytic effect of SrTiO3 on Ag3PO4 toward enhanced photocatalytic water oxidation [J]. ACS Catalysis, 2014, 4: 3020-3027. doi: 10.1021/cs5005079 [24] LIU R R, JI Z J, WANG J, et al. Solvothermal synthesized Ag-decorated TiO2/sepiolite composite with enhanced UV–vis and visible light photocatalytic activity [J]. Microporous and Mesoporous Materials, 2018, 266: 268-275. doi: 10.1016/j.micromeso.2018.03.009 [25] DING J F, LONG G Y, LUO Y, et al. Photocatalytic reductive dechlorination of 2-chlorodibenzo-p-dioxin by Pd modified g-C3N4 photocatalysts under UV–vis irradiation: Efficacy, kinetics and mechanism [J]. Journal of Hazardous Materials, 2018, 355: 74-106. doi: 10.1016/j.jhazmat.2018.05.014 [26] WANG P, JIA C C J, LI J, et al. Ti3+-doped TiO2(B)/anatase spheres prepared using thioglycolic acid towards super photocatalysis performance [J]. Journal of Alloys and Compounds, 2018, 780: 660-690. [27] NG J W, XU S P, ZHANG X W, et al. Hybridized Nanowires and Cubes: A Novel Architecture of a Heterojunctioned TiO2/SrTiO3 Thin Film for Efficient Water Splitting [J]. Advanced Functional Materials, 2010, 20: 4287-4295. doi: 10.1002/adfm.201000931 [28] SHEN H F, WEI H Y, PAN Z D, et al. Preparation and characterization of SrTiO3-Ag/AgCl hybrid composite with promoted plasmonic visible light excited photocatalysis [J]. Applied Surface Science, 2017, 423: 403-446. doi: 10.1016/j.apsusc.2017.06.023 [29] HU C C, HUANG H X, LIN Y F, et al. Decoration of SrTiO3 nanofibers by BiOI for photocatalytic methyl orange degradation under visible light irradiation [J]. Journal of the Taiwan Institute of Chemical Engineers, 2019, 96: 264-273. doi: 10.1016/j.jtice.2018.11.020 [30] AKHUNDI A, AZIZ H A. Ternary g-C3N4/ZnO/AgCl nanocomposites: Synergistic collaboration on visible-light-driven activity in photodegradation of an organic pollutant [J]. Applied Surface Science, 2015, 358: 261-269. doi: 10.1016/j.apsusc.2015.08.149 [31] WAN S, OU M, ZHONG Q, et al. Z-scheme CaIn2S4/Ag3PO4 nanocomposite with superior photocatalytic NO removal performance: Fabrication, characterization and mechanistic study [J]. New Journal of Chemistry, 2018, 42(1): 318-326. doi: 10.1039/C7NJ03588H -






 下载:
下载: