-
在各种类型的废水排放要求中,总氮(total nitrogen,TN)通常都是一个严格管控的指标,因为过量的氮元素会引起水体的富营养化,危害人类健康和环境生态安全。废水总氮的去除主要包括氨态氮(NH4+-N)的氧化和硝酸盐态氮(NO3−-N)的还原过程,在传统的生物反硝化过程中,硝酸盐态氮的去除比氨氮的氧化更为困难[1],并且很难将氨态氮降低至足够低的水平(<1 mg·L−1)。因此,开发一种将废水中总氮处理至较低水平的技术,以实现直接排放至天然水体,具有重要意义。
去除水中硝酸盐氮的最常见处理方法是离子交换法[2]、电渗析[3]和反渗透法[4],这些方法会产生浓缩的废盐水,可能会造成二次处理问题。相比之下,电化学处理因其便利性、低投资成本和环境友好性而受到越来越多的关注,尤其是可能实现最终产物仅为无害的氮气[5]。自MONICA等[6]在1980年报道,通过电化学过程可以有效地去除与海水混合的生活废水中的氨和有机污染物,之后电化学过程就开始被广泛应用于去除各种废水中的氮元素,如制革厂、发电厂、市政及垃圾填埋场废水等。然而,电化学技术应用于天然水体的研究较少,原因是不同于电解质丰富的工业废水,天然水体的电导率普遍较低,对于含有总溶解固体小于100 mg·L−1的饮用水源,电导率仅在50~500 µS·cm−1,相当于离子强度约为0.002 5 mol·L−1,远低于大多数研究中使用的离子强度[7]。水质电导率对电催化活性有直接影响,因为其决定了回路内电子输送所需的外加电流和电解槽所需的电压[8-9],电导率越低意味着溶液电阻高,电催化效率会因此降低[10],进而导致运行成本显着增加[11]。有研究[12]表明,通过添加硫酸钠等支持电解质解决了水体电导率低的问题。然而从应用的角度来看,添加额外的药剂会导致运营成本的大幅增加,尤其是清淤尾水等大宗废水,甚至还可能导致二次污染。YANG等[13]设计了一种流通阳极膜反应器系统,利用管状Ti4O7陶瓷膜作为阳极,从低电导率(178~832 µS·cm−1)废水中去除抗生素,证明了电化学反应器通过优化结构改善传质可以高效去除低电导率水体中的污染物。实际上,电导率低的废水普遍存在,但很少有针对电导率低的真实废水进行相关动力学的研究,目前的相关研究主要集中在电极的材料选择和制备工艺的创新[14],而真正的工程实践中需要进一步评估多个因素的综合影响,尤其是关键操作参数的动力学规律,将为工程应用提供指导。
本研究针对清淤尾水总氮不达标的问题,利用除氮电解器的电化学氧化还原作用,将废水中NH4+-N和NO3−-N分别在阳极、阴极发生氧化和还原反应,生成氮气进而被脱除。首先,本研究利用极化曲线研究了泡沫铜阴极和Ti/IrO2阳极的工作电位和耐腐蚀性,然后在普通单室电解池中研究了支持电解质、电流密度和电导率对模拟废水中氨氮氧化的影响和去除动力学,对于废水电导率低的问题,通过改进电解池结构利用流动池增强传质,降低低电导率水质的欧姆压降,最后对水库坝前淤积泥水进行顺序电解处理,实现在80 min TN去除率达到95%以上。
-
实验所用溶液由硝酸钾(KNO3,≥99.0%)、氯化铵(NH4Cl,≥99.0%)、无水硫酸钠(Na2SO4,≥99.0%)和超纯水制备。所有化学品均为分析级化学品。
-
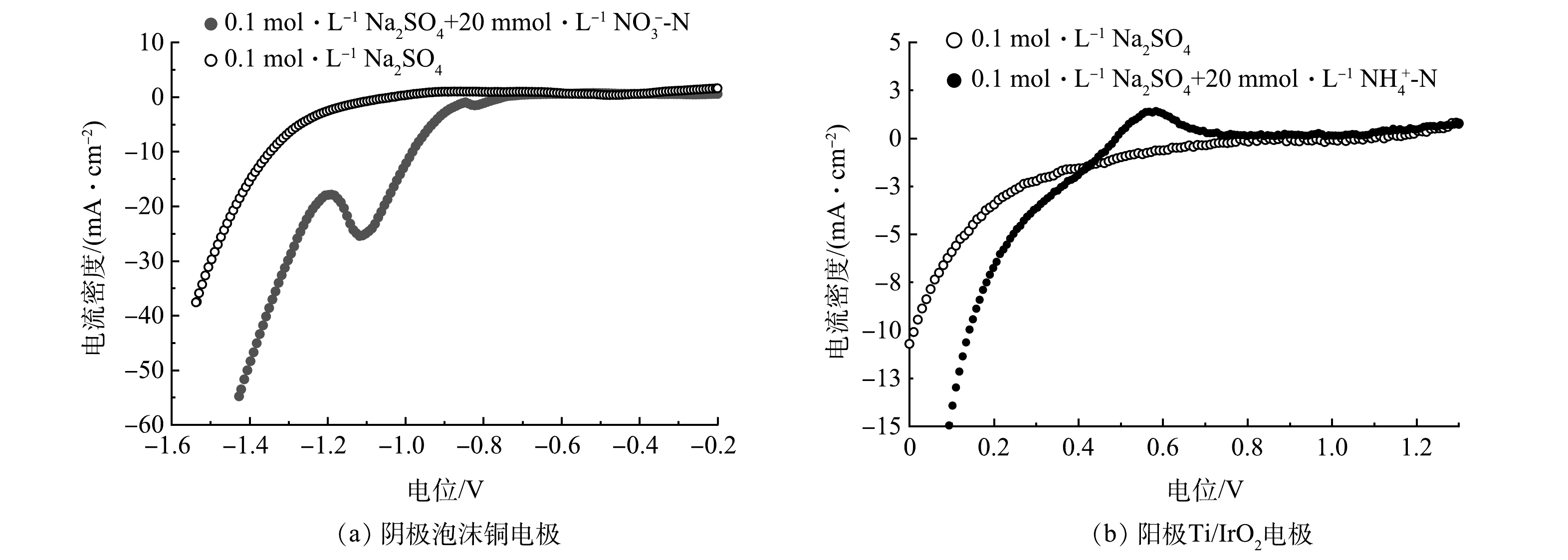
电化学测试旨在研究体系的氧化还原电位,通常通过H型电解槽中的三电极系统进行,循环伏安法(CV)或线性扫描伏安法(LSV)可用于初步评估电解液中催化剂对反应物的催化活性,例如,在硝酸盐氮存在下电流密度的增加归因于还原产物的产生。在每个对应电位下,可以根据计算获得相应的硝酸盐转化率、选择性等。因此,可以根据极化曲线选择最佳电位,从而获得最优的电化学性能,此外,不同催化剂的最佳电位应接近硝酸盐电还原的理论电位,因此可以有效避免能耗损失[15]。本实验构建的三电极体系在室温下进行,使用电化学工作站(科斯特,CS310)供应直流电,使用铂片(2 cm×2 cm)和饱和甘汞电极分别作为对电极和参比电极。阴极线性扫描伏安曲线分别在0.1 mol·L−1 Na2SO4、0.1 mol·L−1 Na2SO4+20 mmol·L−1 NO3−-N溶液中进行测试,工作电极为泡沫铜(1 cm×1 cm);阳极线性扫描伏安曲线在0.1 mol·L−1 Na2SO4和0.1 mol·L−1 Na2SO4+20 mmol·L−1 NH4+-N溶液中进行,工作电极为Ti/IrO2(1 cm×1 cm),扫描速率为10 mV·s−1。其中,阴极NO3−-N和阳极NH4+-N分别由NaNO3和(NH4)2SO4提供氮源。
电解实验使用了传统单室电解槽处理模拟废水中氨氮,获得动力学参数。单次处理量为35 mL,阳极板材料为Ti/IrO2,阴极板材料为泡沫铜,面积均为3 cm×3 cm。使用(NH4)2SO4控制溶液中氨氮的浓度,Na2SO4或NaCl溶于去离子水作为支撑电解质并控制电导率,根据天然水体的电导率范围,配置200~1 000 µS·cm−1的含氨溶液,在5~50 mA·cm−2的电流密度下进行电解,分析废水中氨、亚硝酸盐、硝酸盐、总氮的浓度变化。使用流动池处理时,阴阳极室溶液由蠕动泵进行持续输送,流量为20 mL·min−1。
水质氮元素的检测方法为:NH4+-N质量浓度采用纳氏试剂分光光度法(HJ 535-2009),NO3− -N采用紫外分光光度法(GB 3838-2002),N2含量利用元素质量守恒进行计算。
能耗(electrical energy)根据式(1)进行计算。
式中:E为能耗,kWh·m−3;U为电压,V;I为电流,A;t为反应时间,h;
C0 为初始氨氮质量浓度,g·m−3;Ct 为反应t时间氨氮的质量浓度,g·m−3;V为处理废水的体积,m−3。 -
在实际的电解工艺中,通常根据实测的极化曲线来确定合适的工艺参数。如图1(a)所示,线性扫描伏安法(LSV)在泡沫铜阴极的−1.0 V(vs RHE)附近出现一个明显的还原峰,在工作电位更负于−1.0 V时,硝态氮可以被有效还原[16],而泡沫铜阴极的析氢过电位为−1.2 V,因此析氢副反应在硝酸还原反应之后发生。Ti/IrO2阳极在Na2SO4溶液中的LSV曲线如图1(b)所示,背景溶液加入NH4+-N后,在+0.6 V左右观察到明显的氧化峰,与报道的工作电位一致[17],表明在Ti/IrO2阳极的工作电位更高于+0.6 V时NH4+-N可以有效地氧化为N2。
标准情况下,阳极氨氮氧化反应如式(2)[18]所示,阴极硝酸盐态氮还原反应过程可以由式(3)表示,总反应过程如式(4)所示。
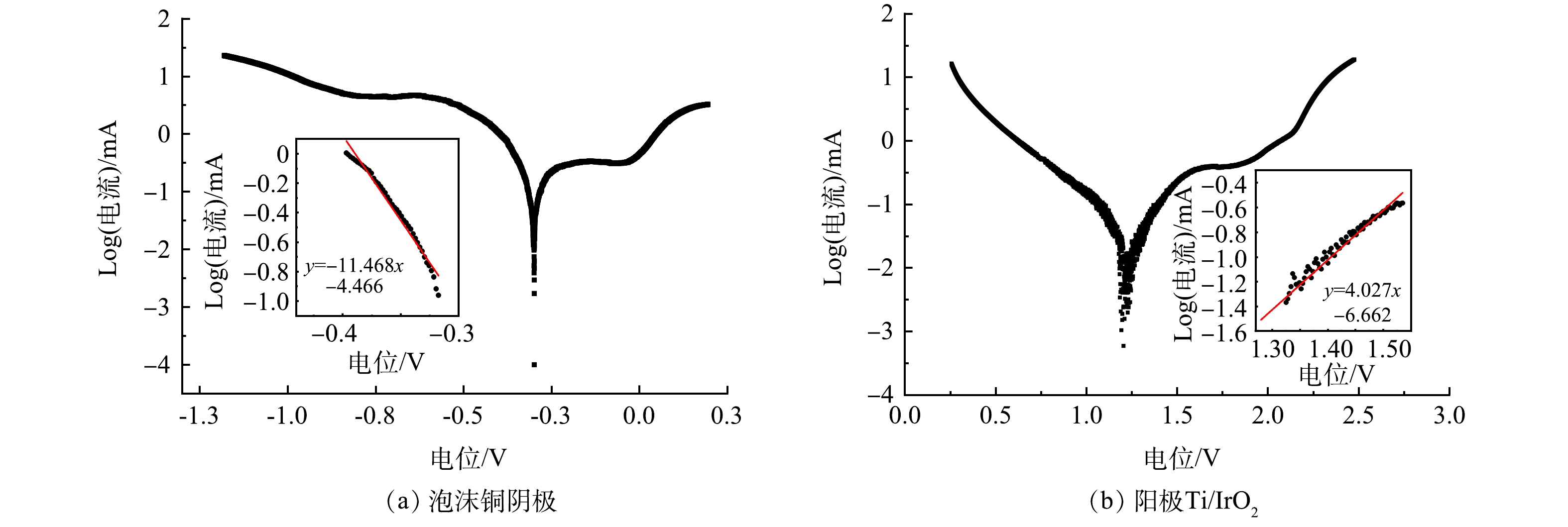
通过Tafel极化测试研究阴极泡沫铜和阳极Ti/IrO2的电化学腐蚀行为,如图2(a),泡沫铜阴极在0.1 mol·L−1 Na2SO4+20 mmol·L−1 NO3−-N溶液的阴极曲线中具有−0.40~−0.30 V的线性区域,其Tafel斜率约为11.468 mV·decade−1,如图2(b)所示,Ti/IrO2阳极在0.1 mol·L−1 Na2SO4+20 mmol·L−1 NH4+-N溶液阳极曲线中具有在1.35~1.50 V的线性区域,其Tafel斜率约为4.027 mV·decade−1。由以上动电位极化曲线中可以得到腐蚀电位和腐蚀电流的值,泡沫铜阴极和Ti/IrO2阳极的腐蚀电流分别为15.57×10−3 mA和11.73×10−3 mA,泡沫铜阴极的腐蚀电位为+0.289 V,Ti/IrO2阳极有相对高的腐蚀电位为+1.221 V,预计该组合极板在TN的电化学去除中可以有较长的使用寿命。
-
1) 支持电解质对于氨氮氧化的影响。天然水体中可能含有各种离子,对于模拟废水的支持电解质的选取,首先分别使用Na2SO4和NaCl配置等电导率的溶液,对比其对于氨氮氧化是否有影响。使用5 mA·cm−2进行恒电流电解实验,表1列出了通过2 h电化学氧化以两种钠盐作为基础电解质的除氨结果。使用Na2SO4作为支持电解质时,在低初始氨约为20 mg·L−1和不同电导率(200和400 µS·cm−1)情况下,2 h内氨浓度没有显著变化(变化幅度小于0.05%),亚硝酸盐氮(NO2−-N)和硝酸盐氮(NO3−-N)均小于氮元素的检测限值0.003 mg·L−1和0.080 mg·L−1,这可能是由于溶液中导电离子浓度较低的情况下,阳极直接氨氧化和羟基自由基间接氧化去除率太慢。在NaCl作为支持电解质氨氮浓度在同样水平的情况下,在电导率为200 µS·cm−1时,2 h内氨氮略有减少,期间产生NO3−-N和NO2−-N的浓度均较低,前者低于检测限,后者在2 h电化学氧化过程中的浓度由0变化至0.028 mg·L−1。添加NaCl增加电导率至400 µS·cm−1时,氨氮氧化速率明显提高,从原本的20.319 mg·L−1降至7.324 mg·L−1,此时的阳极氧化氨氮的机制可以理解为3种机制的共同作用,分别为:直接氧化、羟基自由基间接氧化以及Cl·/ClO·间接氧化。其中Cl·/ClO·来自于NaCl,通电2 h后溶液中63.96%的NH4+-N得以氧化,且基本以氮气的形式从溶液中脱除。Cl·/ClO·间接氧化具体的反应机制可以通过式(5)~式(8)进行解释[19]。
通过本实验可知,废水中Cl−的存在会引入由ClO·带来的额外间接氧化作用,进而大大增强氨氮的氧化。但在实际废水中,尤其是离子浓度有限的天然水体中,不一定能够提供足够的Cl−,因此,后续实验中选择Na2SO4作为支持电解质。
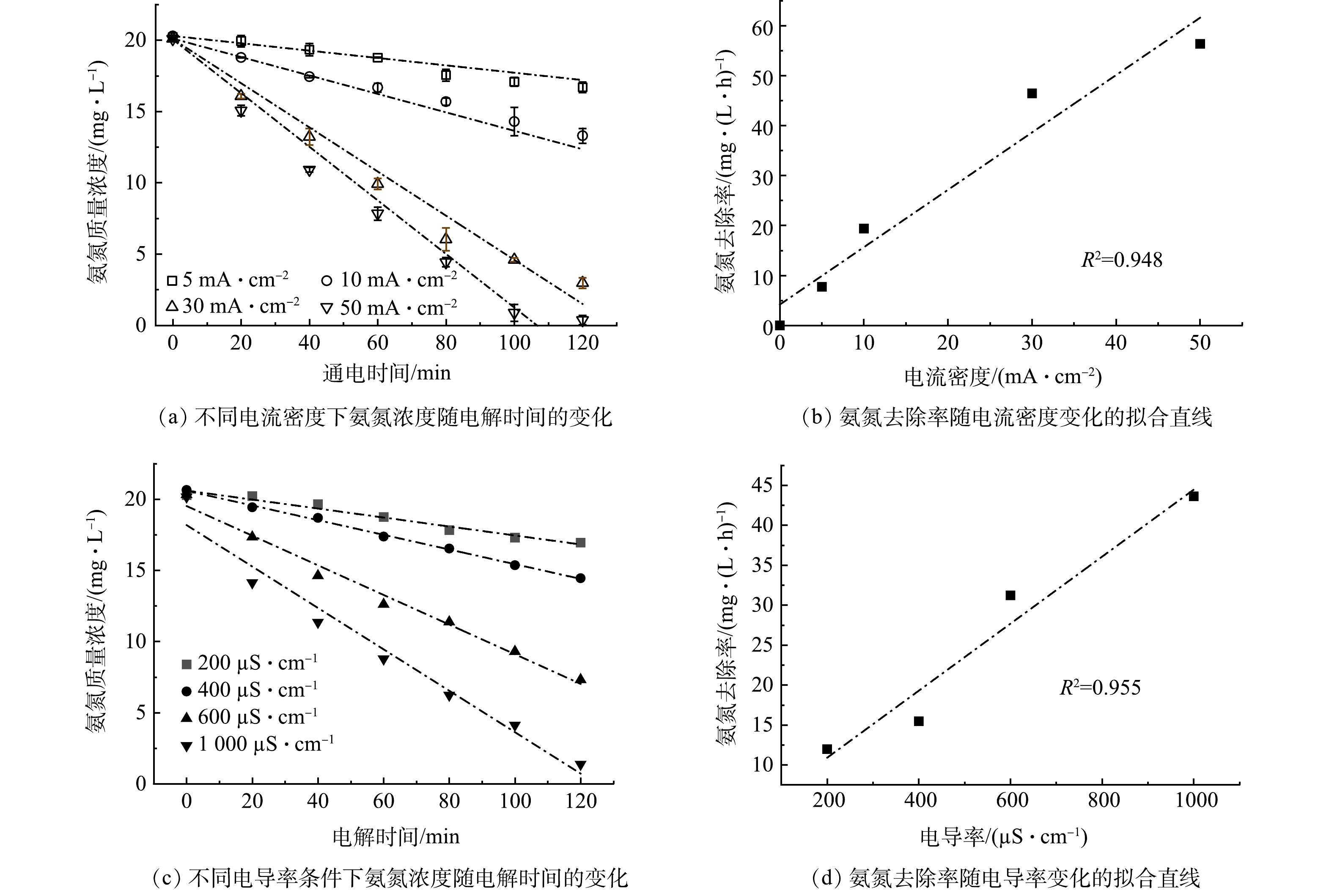
2) 电流密度、电导率对于氨氮氧化的影响。图3(a)为电导率为500 µS·cm−1模拟废水在不同电流密度处理条件下,废水中氨氮的质量浓度随时间的变化情况,图3(c)为配置的不同电导率模拟废水在施加电流密度为15 mA·cm−2时氨氮浓度随电解时间的变化情况。由图3(b)和图3(d)的拟合直线可知,氨氮氧化速率随电流密度和电导率的变化均遵循伪零级动力学过程,在其他条件不变的情况下,单独增加电流密度或废水的电导率均能够有效提升氨氮的氧化速率。
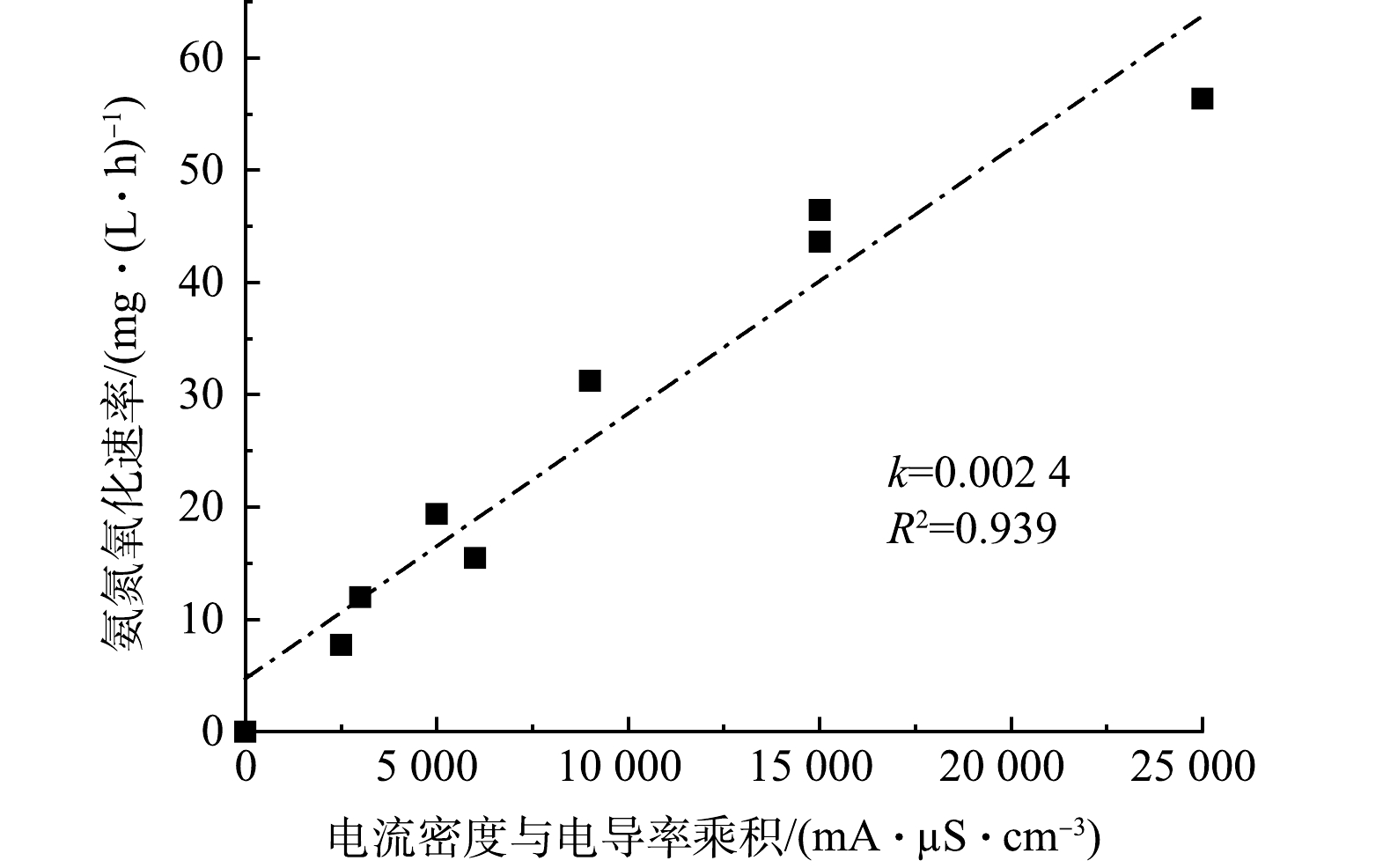
综合考虑电导率和电流密度对氨氮氧化速率的共同影响,由图4中可以看出,氨氧化速率与电导率和电流密度的乘积成正比,斜率为0.002 4,R2为0.939。因此,该影响的伪零级动力学常数如式(9)所示。
式中:σ为电导率,µS·cm−1,电导率为200~
1000 µS·cm−1;i为电流密度,mA·cm−2,模型的应用电流密度为5~50 mA·cm−2。 -
1)流动池参数优化。传统的平板电解槽由阴极和阳极两个水平并列且相通的腔室组成,电极板分别浸入至两极室内,由于结构简单、操作方便通常作为水处理的基础结构。但由于腔室结构不紧凑,浸没在废水中的电极表面会形成一个分界层[20],分界层的存在大大限制了污染物至电极板的传质过程,极大影响污染物的降解效率,更难应用于电导率低的废水。为克服传质限制,有研究通过改进电解槽构型,设计了具有电解液与极板紧密接触特征的流通式反应器。有研究[21]表明,具有高效传质的流通式反应器系统比传统电解槽系统报告的最高传质高出1~2个数量级,得益于优异的传质能力,氧化动力学能实现提高至10倍,降低90%的电能成本。SIMOES等[22]研究表明,极窄电极间隙的流通式反应器实现了传质的增强,反应速率常数比传统电解槽高2倍。GONZAGA等[23]研究表明,具有极窄电极间间隙的流通式反应器提高传质效率进而节约了污染物的降解能耗。
本研究通过改进电解池构型以减小两极板之间的间距,同时使用蠕动泵使得电解液以一定的流速缓慢经过电极表面与电极充分接触,两极室中间使用Nafion117膜使两极室分隔,分别发生还原、氧化反应,其示意图如图5所示。极板间距由改变垫片厚度进行调整,本次实验两极板距离约为8 mm。
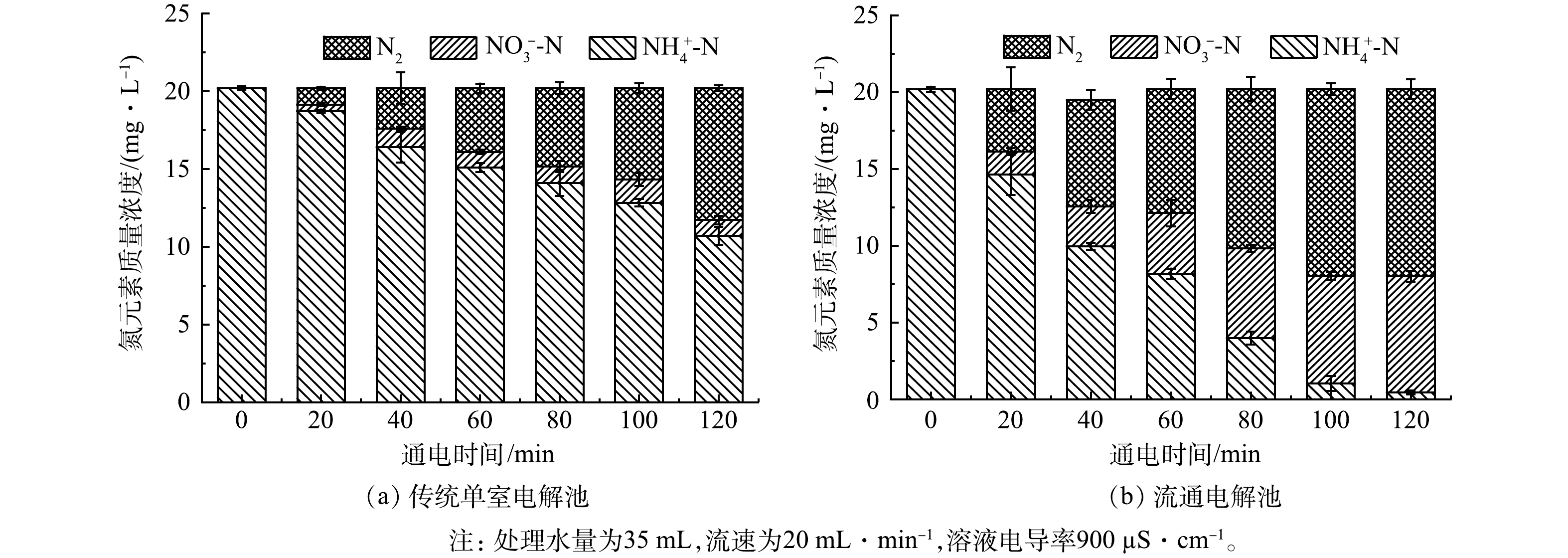
由图6可以看出,当电导率为900 µS·cm−1时,2种电解池的氨氮去除率相比于表2所列在电导率为400 µS·cm−1及以下时均有明显的提升,这也印证了上一部分电导率对于氨氮氧化速率影响的结果。但由于电解过程中废水的电导率低,普通单室电解槽的欧姆压降较大,维持恒电流电解需要很大的电压(维持30 mA·cm−2的电流密度需要电压持续在12 V以上),随之而来的是电能消耗过大,不利于实际应用。而同等条件下,流动池仅需2.17 V的峰值电压,此外,电解2 h后,单室电解槽的氨氮去除率仅在46.45%,而流动电解池氨氮去除率可达97.78%。
如表2所示,本研究所使用的流通式电解池的电能消耗仅为单室槽的16.217%(按照能耗的均值计算),同时也优于已报道的添加电解质、使用固体聚合物电解质和微流控电解工艺的平均能耗。已有研究[13]表明,添加电解质的能耗最高,每降解1个对数阶污染物能耗为6~38 kWh·m−3,微流控反应器系统和固体聚合物电解质系统的电能消耗分别为3.8~35.0 kWh·m−3和2.0~10.2 kWh·m−3。
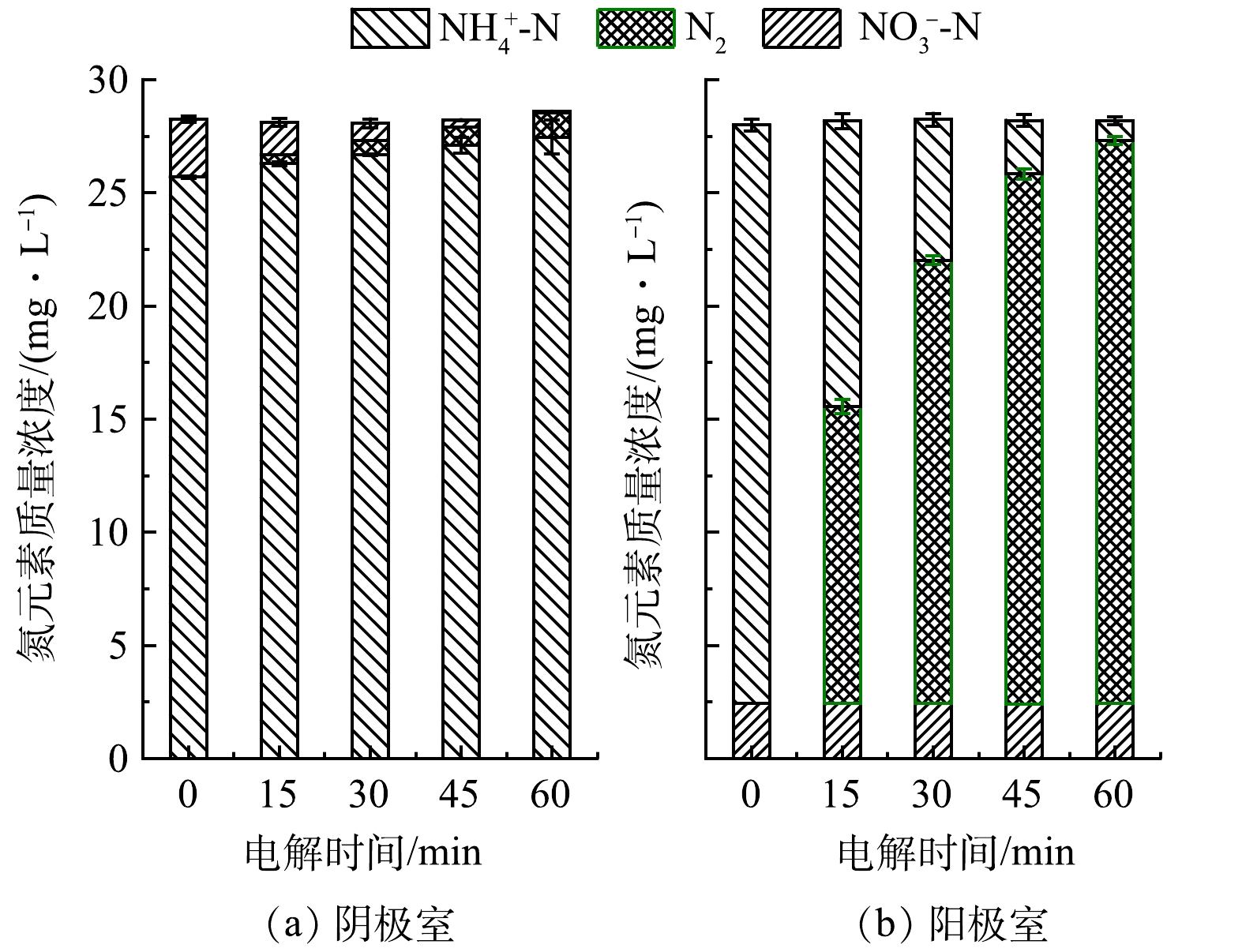
2)顺序电解法去除清淤尾水总氮。本实验废水取自宜昌天福庙水库坝前淤积处,样品为清淤泵吸取的底泥水混合物,过滤后取上清液通入电解器。样品含氨氮25.733 mg·L−1,硝酸盐态氮1.829 mg·L−1,总氮为28.174 mg·L−1,电导率为832 µS·cm−1。不同于模拟废水,真实废水往往存在氨氮和硝酸盐氮共存的现象,单独的氧化还原反应可能会产生含氮副产物,导致体系中TN去除不完全。电解过程中分别对阴阳极室出水进行氮含量测定,结果如图7所示。如图7(b)所示,在阳极室电解过程中,60 min后NH4+-N的去除率达96.63%,几乎全部转化为N2。而从图7(a)可以看出,在通电60 min内,在NO3−-N浓度降低的同时伴随着N2的增加,然而同时也观察到NH4+-N的浓度有轻微的上升,这是硝酸盐态的过度还原导致的。有研究[30]发现,废水中NO3−-N在阴极即使选择性生成主要还原产物N2,但同时仍然会有一部分NO3−-N会不可避免地被还原为NH3-N/NH4+-N(约为20%),这与本研究的实验结果一致。这种现象被称作过度还原,而过度还原产生的副产物NH4+-N仍然会积累在阴极水体中,造成TN含量不达标。
因此,本研究对比了2种电解路线,即单独电解和顺序电解。单独电解是阴、阳极室反应独立发生,顺序电解为使废水顺序通入阳极室和阴极室,依次发生NH4+-N氧化和NO3− -N还原反应,重点是利用阳极和阴极反应的协同作用,提高全局效率从而实现目标污染物的彻底去除,这一反应路线在有机废水的降解中也有报道[31]。
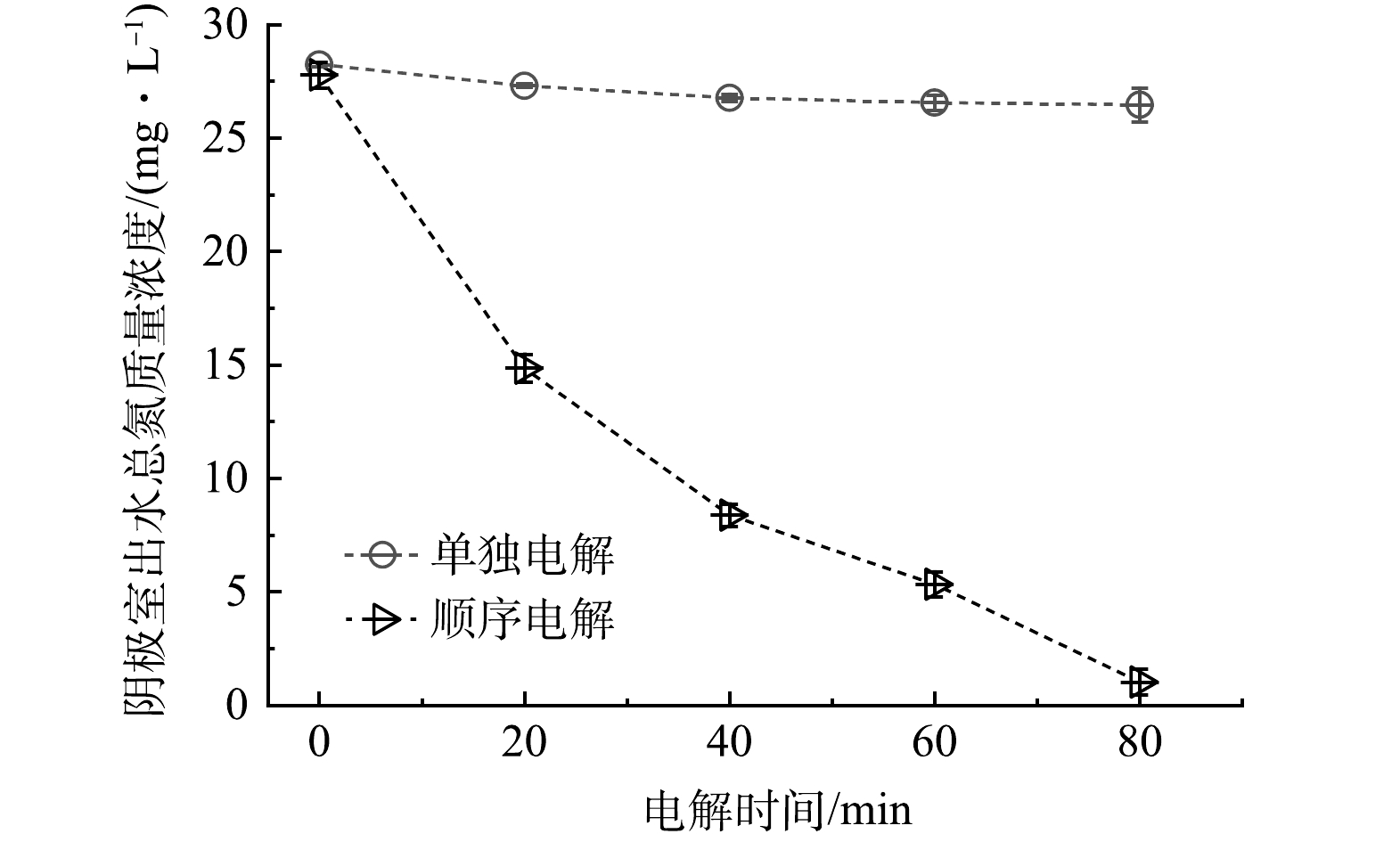
由于顺序电解的最终出水端为阴极室,因此,对2种工艺的阴极出水进行比较。如图8所示,对于单独电解而言,阴极室内脱去的总氮量非常有限。这是由于以下2点原因:首先,原废水中硝酸盐态氮的含量水平较低,其转化为氮气的量有限;其次,正如在图7(a)中讨论的,一部分硝酸盐氮还被过度还原为氨氮继续积累在废水中。相比而言,顺序电解的对于总氮的去除率可达95.33%,其作用机理为:阳极活性涂层与废水中NH4+-N反应迅速转化为N2和少量NO3−-N;阴极将少量的NO3−-N(水体中原本存在的NO3−-N加上前一步过量氧化生成的NO3−-N)还原为N2。顺序电解总氮质量浓度在80 min后降至0.919 mg·L−1,根据我国《地表水环境质量标准》(GB 3838-2002)可知处理后该水质总氮水平介于地表水Ⅲ类至Ⅱ类水质之间,远低于我国《城镇污水处理厂污染物排放标准》(GB 18918-2002)中一级A标准中规定的控制浓度。事实证明,顺序电解工艺能够将低电导率尾水中的总氮转化为氮气,该转化基于在第一阶段阳极反应中将氨氮氧化为氮气和硝酸盐态氮,并在第二阶段阴极反应中将产生的硝酸盐态氮还原成氮气。使用耦合还原和氧化处理工艺可以实现电子的最佳利用,从而节省电能消耗。然而,本研究也发现,在实验结束时,废水中总氮仍然存在少量残留,这可能是反应不彻底或反应中间产物积累所致。理论上,当溶液体系中离子的氧化/还原反应电位低于电解系统所施加的电压时,副反应的发生不可避免,实际废水中杂质离子成分和浓度复杂多样,将除氮电解器广泛应用于真实废水,还要求研究人员进一步对电化学氮循环过程中中间产物的反应途径和生成机理进行完善。
-
本研究针对低电导率清淤尾水的彻底脱氮需求,利用电化学工艺研究了NO3−-N和NH4+-N同时向N2的转化。
1)首先针对低电导率尾水进行了相关动力学的研究,发现电流密度在5~50 mA·cm−2,电导率在200~
1000 µS·cm−1时,氨氮的氧化遵循伪零级动力学,氨氧化速率与电导率和电流密度的乘积成正比,斜率为0.002 4,R2为0.939;使用模拟废水在选择支持电解质的时候发现,废水中如果存在一定的Cl−,会引入由ClO·带来的额外间接氧化作用,进而增强氨氮的氧化;2)为改善低电导率尾水电解时能耗较高的问题,本研究使用的流动电解池可以有效减少极板之间的欧姆降压、增强废水与电极之间的传质,进而使电能消耗相比于传统单室电解槽降低83.783%。
3)将废水依次通过阳极室、阴极室进行顺序电解可以有效避免单独电解导致的过度反应生成含氮副产物的现象。以湖北宜昌天福庙水库坝前淤积泥水混合物为研究对象,过滤后进行顺序电解80 min后总氮含量由28.174 mg·L−1降至0.919 mg·L−1,出水总氮和氨氮浓度远低于我国《城镇污水处理厂污染物排放标准》(GB 18918-2002)中一级A标准中规定的控制浓度,在我国《地表水环境质量标准》(GB 3838-2002)中地表水Ⅲ~Ⅱ类水质之间。
除氮电解器应用于低电导率清淤尾水的性能研究
Performance of a denitrifying electrolyzer applied to low-conductivity dredging tailwater
-
摘要: 为解决清淤尾水总氮超标的问题,本研究开发的除氮电解器使用泡沫铜电极作为阴极,Ti/IrO2作为阳极,利用电化学作用将废水中的NH4+-N和NO3−-N分别在阳极和阴极发生氧化和还原反应,最终生成氮气脱除。首先利用电化学测试极化曲线研究了阴阳两极的工作电位区间和耐腐蚀性,然后在普通单室电解池中研究了支持电解质、电流密度和电导率对模拟废水中氨氮氧化的影响和去除动力学,认为当电流密度在5~50 mA·cm−2,电导率在200~1 000 µS·cm−1时,氨氮的氧化遵循伪零级动力学。为改善低电导率尾水电解时能耗较高的问题,本研究改进电解池构型使用的流通式电解池压缩了两极板之间的间距,有效减少了欧姆降压,相比于单室电解槽每降低一个数量级的氨氮节省83.783%的能耗。最后,为解决过度反应导致副产物的问题,该研究采取了顺序电解的反应路线,并应用于真实清淤废水的处理,实现在80 min内总氮浓度由28.174 mg·L−1降至0.919 mg·L−1,去除率达到95%以上,出水总氮和氨氮浓度远低于我国《城镇污水处理厂污染物排放标准》(GB 18918-2002)中一级A标准中规定的控制浓度,介于我国《地表水环境质量标准》(GB 3838-2002)中地表水Ⅲ类至Ⅱ类水质之间。本研究证明了除氮电解器对于低电导率废水的适用性,为废水的深度脱氮提供了新的思路。Abstract: To address the over standard issue of total nitrogen in dredging tailwater, a nitrogen removal electrolyzer that employs a copper foam electrode as the cathode and Ti/IrO2 as the anode was developed in this study. This system utilizes electrochemical redox reactions to oxidize NH4+-N at the anode and reduce NO3−-N at the cathode, ultimately converting them into nitrogen gas for removal. Initially, the electrochemical polarization curves were used to investigate the working potential ranges and corrosion resistance of both electrodes. Subsequently, the effects of supporting electrolytes, current density, and conductivity on ammonia nitrogen oxidation in simulated wastewater and its removal kinetics were studied in a conventional single-chamber electrolytic cell. The results demonstrated that ammonia nitrogen oxidation followed pseudo-zero-order kinetics at the current density of 5~50 mA·cm−2 and the conductivity of 200~1 000 µS·cm−1. To mitigate the high energy consumption associated with electrolyzing tailwater of low conductivity, the electrolytic cell configuration was improved by using a flow-through electrolytic cell that compresses the distance between the two electrode plates, effectively reducing ohmic voltage drop. Compared to a single-chamber electrolytic cell, this improvement saved 83.783% of energy consumption for each order of magnitude reduction in ammonia nitrogen. Finally, to address the issue of byproducts resulting from overreaction, a "sequential electrolysis" reaction route was adopted and used to the treatment of actual dredging wastewater. Within 80 minutes, the total nitrogen concentration decreased from 28.174 mg·L−1 to 0.919 mg·L−1, achieving a removal rate of over 95%. The concentrations of total nitrogen and ammonia nitrogen in the effluent were far below the control concentrations specified in the Grade 1A standard of China's "Discharge Standard of Pollutants for Municipal Wastewater Treatment Plants" (GB 18918-2002) and fell between the water quality standards for Class III to Class II surface water in the "Environmental Quality Standards for Surface Water" (GB 3838-2002) in China. This study demonstrates the applicability of the nitrogen removal electrolyzer for low-conductivity wastewater and provides a new approach for advanced nitrogen removal from wastewater.
-
为响应“碳达峰、碳中和”国家战略,加快建立污水处理行业的低碳核算和评价标准体系,协同推进污水处理厂减污降碳,并引导污水处理厂实现精细化管理与低碳运行,特制定团体标准《污水处理厂低碳运行评价技术规范》 (T/CAEPI 49—2022) 。该标准基于《2006 IPCC国家温室气体清单指南》 (IPCC即联合国政府间气候变化专门委员会,全称Intergovernmental Panel on Climate Change) ,从直接碳排放和间接碳排放两方面详细阐述了碳排放强度核算内容和步骤,最后梳理了污水处理厂低碳运行评价的基本条件及内容,以期为相关行业从业人员理解标准、落实标准提供参考。此标准由中国环境保护产业协会批准,经中国环保产业协会城镇污水处理分会组织制定,以中国人民大学为主要起草单位,于2022年6月6日发布,并于2022年7月1日起正式实施。
1. 标准制订的背景
污水处理行业是区域经济发展的重要引擎,其碳排放量约占全社会总碳排放的1%~3%[1]。到2030年,全球污水处理行业的CH4和N2O逸散量将分别超过6亿吨和1亿吨二氧化碳当量 (CO2-eq),约占非二氧化碳总排放量的4.5%,是重要的碳排放源[2]。因此,应率先将“低碳”贯穿到污水处理的发展理念、发展方式、产业结构、增长动力、效益评价等各环节中。目前,污水处理低碳发展面临诸多现实问题:对温室气体减排措施的研究不够深入,基础数据不足,监测手段缺乏,且实现污水处理行业碳减排的路径不够明确等。因此,亟需加强对污水处理碳排放的核算与评价,以促进减污降碳的进一步发展,其中指定相关规范性文件是污水处理行业低碳发展的重要保障。
国际上已发布了多项碳排放核算政策与标准,其中,基于“碳足迹”对温室气体核算的包括ISO 19694《固定源排放—确定能量密集型行业的温室气体排放》系列标准、ISO 14067:2013《温室气体—产品碳足迹—量化与沟通的规则与指南》等,基于排放因子法的核算标准有《IPCC 2006年国家温室气体清单指南 2019修订版》。国内也已发布多项温室气体排放核算标准,包括国家标准《工业企业温室气体排放核算和报告通则》 (GB/T 32150-2015) 和12项针对具体行业的标准 (GB/T 32151.1~12) 。然而,不同行业的温室气体排放核算方法仍存在差异,污水处理行业缺少统一的碳核算方法和评价标准,并缺乏相关低碳建设、运营的理论指导,难以科学全面地评价污水处理厂低碳运行水平,污水处理的节能减排仍停留在经验层面。
《污水处理厂低碳运行评价技术规范》 (T/CAEPI 49—2022) 的制订可填补我国污水处理领域低碳核算和低碳运行评价标准的空白,完善我国低碳评价方法体系,在提标改造的同时实现减污降碳,为后续行业标准,以及国家标准、低碳认定细则的编制提供参考。
2. 标准的制定原则与科学方法
2.1 标准编制的基础与方法
1) 编制的政策、文件和标准依据。《污水处理厂低碳运行评价技术规范》 (T/CAEPI 49-2022) 以习近平总书记生态文明建设理念为指导,以《2030年前碳达峰行动方案》、《国家适应气候变化战略2035》、《减污降碳协同增效实施方案》、《城镇污水处理厂运营质量评价标准》 (CJJ/T228-2014) 、《温室气体核算体系》和《温室气体——第一部:企业层面上温室气体排放和去除量化报告指南》 (ISO 14064-1:2018) 等国家和地方有关文件为依据。
2) 标准的制订目标、基本原则。该标准的制订目标与减污降碳的目标紧密结合,旨在完善污水处理行业评价指标体系,指导污水处理厂低碳运行和实现碳减排目标。该标准制订的基本原则为:与国家和地方相关环境标准和污染物排放标准相协调的同时,从全局出发,兼顾全社会与全行业的综合效益,广泛调动各方积极性,综合分析实施标准的技术经济可行性,充分考虑标准使用要求,使该标准具有可操作性。
3) 标准制订的方法和过程。在该标准制订过程中充分调查研究、广泛征求意见,并依靠系统的和科学的分析方法,考虑区域环境的特点和与现有标准的衔接,以提高标准的整体性、系统性和可行性。根据低碳运行评价内容的需要,该标准引用了密切相关的现行标准作为该标准的延伸技术规定,引用文件的管理规定和技术要求视为该标准的一部分。
2.2 核算边界
核算边界是重要的碳排放核算与评价依据。在时间边界上,污水处理厂运行包括污水进入污水处理厂的粗格栅后,经过一系列的一级处理、二级处理和三级处理后排出的过程。此过程包括去除污水中固体污染物质、有机污染物以及难降解有机和无机污染物等。具体在空间边界的体现,即污水在上述处理过程中厂界内各具体构筑物,因此,本标准的空间边界不包括办公区和污泥深度处理区 (即污泥脱水外的过程) 。
本标准以城市污水处理厂为主,不包括工业污水处理厂和汇入较多工业污水的城镇污水处理厂。根据城镇污水处理厂的碳排放活动,确定以下6种碳排放类型:1) 全生命周期各个阶段直接燃烧消耗化石燃料的直接碳排放;2) 污水处理厂内各处理构筑物及传输过程由微生物为主产生并排放的CH4,N2O和非生源性CO2直接碳排放;3) 全生命周期各个阶段化石燃料生产电能、热能等过程产生的间接碳排放;4) 全生命周期所消耗材料,主要为化学药剂生产产生的间接碳排放;5) 运输材料过程所产生的直接碳排放;6) 资源、能源等回收形成的碳补偿。
3. 标准的主要内容
标准内容主要分为碳排放强度核算与低碳运行评价两部分。碳排放强度核算可分为直接碳排放核算和间接碳排放核算。评价指标体系分为定量评价和定性评价。定量评价是以碳排放核算为基础的评价;定性评价是对设施设备低碳改造、优化运行、低碳建设、监测与核算等低碳行为的评价。
3.1 碳排放强度的核算内容
3.1.1 核算公式
根据IPCC排放因子法[3]计算污水处理厂N2O、CH4和CO2的排放强度,计算公式见式 (1) 。
温室气体排放强度=活动数据×排放因子×全球变暖潜能值(GWP100) (1) 式中:活动数据是污水处理过程中排放的温室气体和生产或消费活动的活动量,如污水处理构筑物产生的温室气体、化石燃料的消耗量、净购入的电量、化学药品的消耗量、净购入的热量等;排放因子是与活动水平数据对应的系数,表征单位生产或消费活动量的温室气体排放系数。排放因子与全球变暖潜能值GWP100参考自《IPCC 2006年国家温室气体清单指南 2019修订版》[3]。
3.1.2 直接碳排放强度
直接碳排放为污水生物处理单元产生的N2O排放、CH4排放和化石燃料燃烧产生的CO2排放,如公式 (2) 所示。计算出的温室气体排放量乘相应气体的 GWP100,即为该气体直接碳排放强度值。IPCC认为污水处理厂由生物分解产生的CO2归为生源性碳,因此产生的CO2不纳入碳排放的计算[3]。
Ed=EN2O+ECH4+ECO2 (2) 式中:碳排放强度单位为kg∙m−3,是以CO2排放当量计,即每方水排放碳强度为多少千克CO2-eq,本文所有碳排放强度皆为此单位,后不再赘述;
Ed EN2O ECH4 ECO2 3.1.3 间接碳排放强度
间接碳排放强度按公式 (3) 计算,包括电力、热力等能耗碳排放和化学药剂 (碳源、除磷药剂、脱水药剂、消毒药剂等) 消耗的物耗碳排放。
Ei=Ee+Eh+Ec (3) 式中:
Ei Ee Eh Ec 3.2 污水处理厂的低碳运行评价
3.2.1 评价基本条件
该标准主要适用于城镇污水处理厂碳排放核算和低碳运行水平的评价,进行核算与评价的污水处理厂应满足如下5个基本条件。1) 符合其他污染物排放标准,无超标现象。2) 评价周期为一年,一般从每年的1月1日至12月31日计,取日平均值,以避免一年中不同季节、不同月份或一天中不同时间的温度、湿度及其它因素引起的碳排放差异。3) 污水处理厂需完成环保验收才能参与评价,且要投产1年以上,以保证污水处理厂运行数据的准确性和有效性。4) 污水处理厂平均水量负荷率应该大于设计处理水量的50%,工业废水进水比例应小于10%;污水处理厂设计处理水量与实际处理水量差距过大,造成基础建设、设备采购、运行成本等方面碳排放增加,造成资源的浪费,也与低碳相悖。工业废水的汇入对城镇污水处理厂运行有一定影响,若出水需达标则则需要增加碳排放例如电耗或药剂,因此工业废水进水比例应小于10%。5) 监测、运行与样品采集、记录过程中均要遵循现行的标准和工艺运行管理原则。化验监测、日常化验检测项目及周期应遵循国家现行标准和工艺运行管理需要的原则。此外,污水处理厂应完整并准确记录工艺运行参数和能耗物耗等数据。规范样品的采集、化验、记录过程,确保核算与评价结果的准确性。
3.2.2 低碳运行评价指标体系
根据文献资料与实践调研分析,评价指标体系分为定量评价指标和定性评价指标两大类,细分为二级评价指标体系 (表1) 。定量评价指标包括一级指标 (评价碳排放强度) 、二级指标 (直接碳排放修正强度、间接碳排放修正强度) 。定性评价指标包括一级指标 (低碳行为) 、二级指标 (设施设备低碳改造、优化运行、低碳建设、监测与核算) 。
表 1 污水处理厂低碳运行评价指标体系Table 1. Low-carbon operation evaluation index system of sewage treatment plant分类 一级指标 二级指标 其他指标与系数 定量评价 评价碳排放强度 (EP) 直接碳排放修正强度 (Edc) 直接碳排放强度 (Ed) 总氮去除率修正系数 (k1) 间接碳排放修正强度 (Eic) 间接碳排放强度 (Ei) 处理规模修正系数 (k2) 耗氧污染物削减量修正系数 (k3) 出水排放标准修正系数 (k4) 臭气控制程度修正系数 (k5) 定性评价 低碳行为 设施设备低碳改造 优化运行 低碳建设 监测与核算 3.2.3 评价碳排放强度
(1) 碳排放修正强度分数
针对污水处理过程的差异性,该标准提出归一化的碳排放评价方法。碳排放修正强度是对由于总氮去除率、处理规模、耗氧污染物削减量、出水排放标准以及臭气控制程度等因素导致的客观碳排放差异进行修正后的碳排放强度。为了避免不同污水处理厂的处理规模、总氮去除率、出水排放标准、耗氧污染物削减量和除臭程度差异的情况,确保污水处理厂低碳运行评价的有效性、合理性和公平性,在评价指标中提出了修正系数,用于碳排放强度的修正。修正系数是基于污水处理厂运行过程中上述因素对单位污水处理碳排放的影响系数。该标准确定了用于修正碳排放强度的5项修正系数,分别为总氮去除率修正系数k1、处理规模修正系数k2、耗氧污染物削减量修正系数k3、出水排放标准修正系数k4和臭气控制程度修正系数k5。
1) 总氮去除率修正系数k1。总氮去除率修正系数k1的提出是基于总氮去除率对直接碳排放的影响。污水处理厂的总氮去除率 (ηTN) 越高,N2O排放因子越低[4],直接碳排放强度越低。因此,采用总氮去除率修正系数k1修正直接碳排放强度。
2) 处理规模修正系数k2。处理规模修正系数k2的提出是基于处理水量对电耗的影响。当处理规模较小时,吨水电耗较高;当处理规模较大时会呈现出一定的规模效应,吨水电耗较小。
3) 耗氧污染物削减量修正系数k3。进水水质常见指标包括COD、BOD5、SS、NH4+-N、TN和TP这6项。其中,进水COD (或BOD5) 和NH4+-N (或TN) 的降解和转化需要消耗大量氧气,会直接增加电耗;TN的去除还可能需要外加碳源,增加药耗;TP的去除需要化学除磷药剂,同样会增加药耗。因此,耗氧污染物削减量修正系数k3的提出是基于污染物削减量对间接碳排放强度的影响。
4) 出水排放标准修正系数k4。现行出水排放标准主要为一级A、一级B或者地方标准,基于此,该标准将出水排放标准划分为高于一级A、一级A和低于一级A三档,高于一级A又分为COD限值为40 mg∙L−1和COD限值小于等于30 mg∙L−1两档。出水排放标准是出水水质的区分,也是污水处理工艺的区分。当出水排放标准执行一级A或高于一级A时,必定会有深度处理单元,这会进一步增加污水处理厂的电耗、物耗,也会增加直接碳排放。因此,本标准规定出水排放标准修正系数k4主要用于间接碳排放强度的修正。
5) 臭气控制程度修正系数k5。目前,部分污水处理厂增加了除臭设施设备,该部分主要会增加电耗。因此,臭气控制程度修正系数k5用于修正间接碳排放强度。无除臭指对污水处理厂各工艺单元产生的臭气未进行收集处理,部分除臭指对污水处理厂部分工艺单元的臭气进行收集处理,全部除臭指对全部工艺单元的臭气进行收集处理,包括加盖和地下式2种方式。
(2) 碳排放修正强度计算
该标准碳排放修正强度是基于总氮去除率修正系数、处理规模修正系数、耗氧污染物削减量修正系数、出水排放标准修正系数和臭气控制程度修正系数这5项修正系数对碳排放强度进行修正。
Ep=Edc+Eic (4) Edc=EN2O×k1+ECH4+ECO2 (5) Eic=[Ee×(k2⋅k5)+Eh+Ec]⋅k3⋅k4 (6) 式中:
EP Eic Edc EN2O k1 ECH4 ECO2 Ee Eh Ec k2 k3 k4 k5 3.2.4 低碳行为鼓励
该标准对污水处理厂低碳行为进行了界定,对开展污水处理设施设备低碳改造、全流程工艺单元的优化运行管理、低碳建设、温室气体监测与低碳运行核算等低碳行为进行加分鼓励。其中,设施设备主要体现在集约化、自动化、绿色高效等方面。优化运行则包括用电分区计量与评估、化学药剂优选与精准投加、生物处理系统优化调控。低碳建设包括采用污泥稳定化技术和清洁能源技术。温室气体监测与低碳运行核算包括污水处理厂开展重点温室气体 (CH4、N2O) 的现场监测并形成相关监测报告、实际碳排放核算并编制相关报告和低碳运行评价并形成年度报告。
3.2.5 低碳运行评价规则
评价分数是碳排放修正强度分数和低碳行为鼓励分数两部分的加权之和。经专家组评议,考虑现阶段污水处理行业的低碳行为占污水处理厂碳减排比重,将碳排放修正强度分数权重值定为0.8,低碳行为鼓励分数权重值定为0.2。根据分级需要及污水处理厂低碳运行评价总分数,将污水处理厂低碳运行等级分为一级、二级和三级,分别代表污水处理厂低碳运行水平优秀、良好和一般。
3.2.6 评价流程
污水处理厂低碳运行评价流程包括资料收集、资料核查、数据核算和等级评定4个部分,如图1所示。根据运行数据,经过甄别、计算和修正得到评价碳排放强度分数。根据低碳行为资料,经过数据合适、现场核查、低碳行为认证得到低碳行为鼓励分数,最终得出评价总分数并进行等级评。监管层面的低碳行为认证由监管部门专门成立的机构进行材料认定,污水处理厂内部的评价由本厂专门负责低碳运行评价的部门认证。认证过程包括认证委托、文件评审、初始现场核查、认证结果评价与批准等。评价过程应保证数据的真实性、准确性与完整性。
4. 案例展示
按照《污水处理厂低碳运行评价技术规范》 (T/CAEPI 49—2022) 附录D表D.1、D.2和D.3要求,收集A、B、C污水处理厂2021年1月1日—2021年12月30日每日运行数据 (日平均值) ,收集台账详见表2和表3。根据规范内公式计算得出污水处理厂低碳运行评价等级,如表4所示。
表 2 污水处理厂低碳运行评价资料收集表1Table 2. Data collection table 1 for low-carbon operation evaluation of sewage treatment plant污水处理厂 设计进水水量/ (m3∙d−1) 工业废水进水比例/% 排放限值 (COD) / (mg∙L−1) 型式 除臭程度 日进水水量/ (m3∙d−1) 进水COD/(mg∙L−1) 进水BOD5/ (mg∙L−1) 进水氨氮/ (mg∙L−1) 进水总氮/ (mg∙L−1) 出水COD/ (mg∙L−1) 出水BOD5/ (mg∙L−1) 出水氨氮/ (mg∙L−1) 出水总氮/ (mg∙L−1) 污泥产量/ (kg∙d−1) 脱水污泥含水率/% CH4回收体积/ (m3∙d−1) A 50 000 5.0 30 地下式 有除臭电耗 18 938 299 137 45 50 16 2.0 0.80 7.0 14 78 0 B 70 000 0 30 地上式 有除臭电耗 53 569 236 103 38 42 17 2.0 0.71 8.0 56 218 79 0 C 40 000 10 30 地上式 有除臭电耗 22 417 140 68 26 35 16 2.0 0.62 6.0 26 74 0 表 3 污水处理厂低碳运行评价资料收集表2Table 3. Data collection table 2 for low-carbon operation evaluation of sewage treatment plant污水处理厂 用于生产的外购总耗电量/ (kW·h∙d−1) 每日热能消耗量 (折合为标准煤量) / (kg∙d−1) 每日化石燃料种类及其使用量(折合为标准煤量)/ (kg∙d−1) 每日化学药剂种类和纯品重量/ (kg∙d−1) A 15 813 0 0 乙酸钠878、聚丙烯酰胺27、聚合硫酸铝141、次氯酸钠644 B 24 788 0 0 除磷剂188、次氯酸钠1 744、聚丙烯酰胺49、碳源805 C 6 158 0 0 乙酸钠395、PAM聚丙烯酰胺17、聚合氯化铝169、次氯酸钠756 表 4 污水处理厂低碳运行评价等级计算表Table 4. Calculation table of low-carbon operation evaluation grade of sewage treatment plant污水处理厂 总氮去除率修正系数k1 处理规模修正系数k2 耗氧污染物削减量修正系数k3 出水排放标准修正系数k4 臭气控制程度修正系数k5 直接碳排放修正强度Edc/(kg∙m−3) 间接碳排放修正强度Eic/(kg∙m−3) 评价碳排放强度Ep/ (kg∙m−3) 评价碳排放强度分数F1 低碳行为鼓励分数F2 低碳运行评价总分数F 评价等级 A 0.003 5 0.95 0.80 0.64 0.90 0.065 0.35 0.41 63 61 63 三级 B 0.007 4 1.00 0.97 0.64 0.95 0.087 0.24 0.33 75 80 76 二级 C 0.006 6 0.95 1.05 0.64 0.95 0.063 0.19 0.25 86 84 86 一级 5. 评述
污水处理厂的碳排放核算主要是依据IPCC排放因子法,而污水处理厂的低碳运行评价内容则是首次提出。评价标准制定过程主要是将不同的污水处理厂低碳运行水平受不同运行情况 (例如水量、进水水质和排放标准等) 进行类似归一化处理。低碳行为的鼓励是对污水处理厂低碳工作的定性评价指标,旨在对污水处理厂现有低碳工作的肯定,以及鼓励污水处理厂在后续设计、运行和改造过程中补充低碳行为,以获得更高的低碳等级。权重的比例对污水处理厂低碳运行评价结果影响较大,因此,该比例的确定由标准评审专家集体讨论最终确定。
标准后续可完善的内容包括如下4点。1) 基于现有的IPCC排放因子法的样本数较少,未有针对我国的特定排放因子,各省也未根据本省情况制定温室气体排放因子。从行业的角度,化工行业也尚未对污水处理行业常用的大部分化学试剂排放因子进行确定。2) 基于IPCC排放因子法的计算方法具备较高的可操作性,除了未考虑不同地域、也未考虑不同处理工艺的影响,是污水处理厂未获得实测数据结果的替代方法。3) 污水处理厂的污泥处理处置方式包括外运、填埋、厌氧堆肥、热水解、脱水干化后焚烧、焚烧后作为建筑材料等,污泥处理处置情况不同导致的碳排放情况差异较大,目前也无相关标准可参考,因此,污水处理厂低碳运行评价不包括污泥处理处置的碳排放核算与评价。4) 根据低碳发展的需要,污水处理行业仍需完善一系列低碳标准,如污水处理行业低碳建设、污水处理厂温室气体 (N2O和CH4) 监测的标准和核算方法学、污水处理厂低碳管理标准以及报告要求等。
6. 结语
《污水处理厂低碳运行评价技术规范》 (T/CAEPI 49—2022) 作为我国首部污水处理领域低碳团体标准,对污水处理厂的低碳时代有开创性的意义。低碳运行评价是实现污水处理行业减污降碳的重要途径之一,是推动资源循环利用和低碳发展的重要措施。《污水处理厂低碳运行评价技术规范》 (T/CAEPI 49—2022) 规定了污水处理厂低碳运行评价的分级及其基本依据。该团体标准的制定、颁布和实施,对规范污水处理厂低碳运行评价工作,指导污水处理厂开展低碳工作,促进资源合理利用具有积极意义。今后需进一步做好该标准的宣贯工作,加强实施和减污降碳的落实推广工作,充分发挥标准的规范和引领作用。
-
表 1 在5 mA·cm−2恒电流密度条件下电解2 h内氮元素的质量浓度变化
Table 1. Changes in nitrogen mass concentration during 2 hours of electrolysis at a constant current of 5 mA·cm−2
电解时间/min 氮元素质量浓度/(mg·L−1) 200 µS·cm−1 Na2SO4 400 µS·cm−1 Na2SO4 200 µS·cm−1 NaCl 400 µS·cm−1 NaCl NH4+-N NO2−-N NO3−-N NH4+-N NO2−-N NO3−-N NH4+-N NO2−-N NO3−-N NH4+-N NO2−-N NO3−-N 0 19.84 BD BD 19.78 BD BD 20.288 BD BD 20.319 BD BD 20 19.84 BD BD 19.77 BD BD 20.219 BD BD 17.339 BD BD 40 19.84 BD BD 19.81 BD BD 19.647 BD BD 14.623 BD 0.051 60 19.84 BD BD 19.77 BD BD 18.754 BD BD 12.615 BD 0.070 80 19.84 BD BD 19.78 BD BD 17.833 0.023 BD 11.380 BD 0.124 100 19.84 BD BD 19.78 BD BD 17.299 0.026 BD 9.300 BD 0.203 120 19.84 BD BD 19.78 BD BD 16.951 0.028 BD 7.324 BD 0.241 注:BD表示低于检出限。 表 2 不同废水处理工艺/系统能耗对比
Table 2. Comparison of energy consumption of different wastewater treatment processes/systems
工艺或系统 污染物 浓度 能耗 /(kWh·m−3) 参考文献 单室电解槽 总氮 28.174 mg·L−1 15.9~43.323 本研究 流动池反应器 0.6~10.781 本研究 添加额外电解质 四环素 1 µmol·L−1 28 [24] 磺胺二甲氧嘧啶 1 µmol·L−1 38 左氧氟沙星 1 384 μmol·L−1 25 [25] 诺氟沙星 313 μmol·L−1 6.5~8.5 [26] 固体电解质系统 苯甲酸 200 μmol·L−1 35 [27] 特丁津 0.4~17.4 μmol·L−1 3.8~19.0 [28] 微流控系统 苯甲酸 200 μmol·L−1 4.6~10.2 [27] 敌草隆 43 μmol·L−1 2.0 [29] -
[1] ZHAO H. Nitrogen removal from wastewater plant secondary effluent in a compound natural treatment system[J]. Ecological Engineering, 2013, 57: 361-365. doi: 10.1016/j.ecoleng.2013.04.026 [2] SAMATYA S, KABAY N, YÜKSEL Ü, et al. Removal of nitrate from aqueous solution by nitrate selective ion exchange resins[J]. Reactive and Functional Polymers, 2006, 66(11): 1206-1214. doi: 10.1016/j.reactfunctpolym.2006.03.009 [3] EL MIDAOUI A, ELHANNOUNI F, TAKY M, et al. Optimization of nitrate removal operation from ground water by electrodialysis[J]. Separation and Purification Technology, 2002, 29(3): 235-244. doi: 10.1016/S1383-5866(02)00092-8 [4] SCHOEMAN J J, STEYN A. Nitrate removal with reverse osmosis in a rural area in South Africa[J]. Desalination, 2003, 155(1): 15-26. doi: 10.1016/S0011-9164(03)00235-2 [5] CHEN G. Electrochemical technologies in wastewater treatment[J]. Separation and Purification Technology, 2004, 38(1): 11-41. doi: 10.1016/j.seppur.2003.10.006 [6] MONICA M D, AGOSTIANO A, CEGLIE A. An electrochemical sewage treatment process[J]. Journal of Applied Electrochemistry, 1980, 10(4): 527-533. doi: 10.1007/BF00614086 [7] GARCIA-SEGURA S, NIENHAUSER A B, FAJARDO A S, et al. Disparities between experimental and environmental conditions: Research steps toward making electrochemical water treatment a reality[J]. Current Opinion in Electrochemistry, 2020, 22: 9-16. doi: 10.1016/j.coelec.2020.03.001 [8] MOREIRA F C, BOAVENTURA R A R, BRILLAS E, et al. Electrochemical advanced oxidation processes: A review on their application to synthetic and real wastewaters[J]. Applied Catalysis B: Environmental, 2017, 202: 217-261. doi: 10.1016/j.apcatb.2016.08.037 [9] GARCIA-SEGURA S. Electrochemical oxidation remediation of real wastewater effluents: A review[J]. Process Safety and Environmental Protection, 2018, 113: 48-67. doi: 10.1016/j.psep.2017.09.014 [10] XU H, MA Y, CHEN J, et al. Electrocatalytic reduction of nitrate: A step towards a sustainable nitrogen cycle[J]. Chemical Society Reviews, 2022, 51(7): 2710-2758. doi: 10.1039/D1CS00857A [11] ZOU X, XIE J, WANG C, et al. Electrochemical nitrate reduction to produce ammonia integrated into wastewater treatment: Investigations and challenges[J]. Chinese Chemical Letters, 2023, 34(6): 107908. doi: 10.1016/j.cclet.2022.107908 [12] ELENI T, THEODORA V, ALEXANDROS K, et al. Anodic oxidation of textile dyehouse effluents on boron-doped diamond electrode[J]. Journal of Hazardous Materials, 2012, 207-208: 91-96. doi: 10.1016/j.jhazmat.2011.03.107 [13] YANG K , LIN H , FENG X W , et al. Energy-efficient removal of trace antibiotics from low-conductivity water using a Ti4O7 reactive electrochemical ceramic membrane: Matrix effects and implications for byproduct formation[J]. Water Research, 2022, 224: 119047. [14] GABRIAL A, ANA S. FAJARDO, et al. Enabling circular economy by N-recovery: Electrocatalytic reduction of nitrate with cobalt hydroxide nanocomposites on copper foam treating low conductivity groundwater effluents[J]. Science of the Total Environment, 2023, 887: 163938. doi: 10.1016/j.scitotenv.2023.163938 [15] WANG Y T , WANG C , LI M, et al. Nitrate electroreduction: mechanism insight, in situ characterization, performance evaluation, and challenges[J]. Chemical Society Reviews, 2021, 50: 6720-6733. [16] LAN H, LIU X, LIU H, et al. Efficient nitrate reduction in a fluidized electrochemical reactor promoted by Pd–Sn/AC particles[J]. Catalysis Letters, 2016, 146(1): 91-99. doi: 10.1007/s10562-015-1615-3 [17] BUNCE N J, BEJAN D. Mechanism of electrochemical oxidation of ammonia[J]. Electrochimica Acta, 2011, 56(24): 8085-8093. doi: 10.1016/j.electacta.2011.07.078 [18] HAND S, CUSICK R D. Electrochemical disinfection in water and wastewater treatment: Identifying impacts of water quality and operating conditions on performance[J]. Environmental Science & Technology, 2021, 55(6): 3470-3482. [19] ZHOU C, BAI J, ZHANG Y, et al. Novel 3D Pd-Cu(OH)2/CF cathode for rapid reduction of nitrate-N and simultaneous total nitrogen removal from wastewater[J]. Journal of Hazardous Materials, 2021, 401: 123232. doi: 10.1016/j.jhazmat.2020.123232 [20] LI J, YIN M, WANG Y, et al. Improvement of the conventional flat plate electrode: Application of filtered Pd@Ti electrode in the removal of toxic chlorinated PPCPs[J]. Separation and Purification Technology, 2024, 329: 125120. doi: 10.1016/j.seppur.2023.125120 [21] TRELLU C, COETSIER C, ROUCH J C, et al. Mineralization of organic pollutants by anodic oxidation using reactive electrochemical membrane synthesized from carbothermal reduction of TiO2[J]. Water Research, 2018, 131: 310-319. doi: 10.1016/j.watres.2017.12.070 [22] SIMÕES A J A, DÓRIA A R, VIEIRA D S, et al. Electrochemical degradation of ciprofloxacin using a coupled 3D anode to a microfluidic flow-through reactor[J]. Journal of Water Process Engineering, 2023, 51: 103443. doi: 10.1016/j.jwpe.2022.103443 [23] GONZAGA I M D, DÓRIA A R, MORATALLA A, et al. Electrochemical systems equipped with 2D and 3D microwave-made anodes for the highly efficient degradation of antibiotics in urine[J]. Electrochimica Acta, 2021, 392: 139012. doi: 10.1016/j.electacta.2021.139012 [24] WANG B, SHI H, HABTESELASSIE, et al. Simultaneous removal of multidrug-resistant Salmonella enterica serotype typhimurium, antibiotics and antibiotic resistance genes from water by electrooxidation on a Magnéli phase Ti4O7 anode[J]. Chemical Engineering Journal, 2021, 407: 127134-127141. doi: 10.1016/j.cej.2020.127134 [25] XIA Y, DAI Q. Electrochemical degradation of antibiotic levofloxacin by PbO2 electrode: Kinetics, energy demands and reaction pathways[J]. Chemosphere, 2018, 205: 215-222. doi: 10.1016/j.chemosphere.2018.04.103 [26] CARNEIRO J F, AQUINO J M, SILVA BF, et al. Comparing the electrochemical degradation of the fluoroquinolone antibiotics norfloxacin and ciprofloxacin using distinct electrolytes and a BDD anode: evolution of main oxidation byproducts and toxicity[J]. Journal of Environmental Chemical Engineering, 2020, 8(6): 104433-104442. doi: 10.1016/j.jece.2020.104433 [27] MENG X, CHEN Z, WANG C, et al. Development of a three-dimensional electrochemical system using a blue TiO2/SnO2-Sb2O3 anode for treating low-ionic-strength wastewater[J]. Environmental Science & Technology, 2019, 53(23): 13784-13793. [28] KLIDI N, CLEMATIS D, CARPANESE M P, et al. Electrochemical oxidation of crystal violet using a BDD anode with a solid polymer electrolyte[J]. Separation and Purification Technology, 2018, 208: 178-183. [29] KHONGTHON W, JOVANOVIC G, YOKOCHI A, et al. Degradation of diuron via an electrochemical advanced oxidation process in a microscale-based reactor[J]. Chemical Engineering Journal, 2016, 292: 298-307. doi: 10.1016/j.cej.2016.02.042 [30] ZHANG Y, LI J, BAI J, et al. Extremely efficient decomposition of ammonia N to N2 using ClO · from reactions of HO · and HOCl generated in Situ on a novel bifacial photoelectroanode[J]. Environmental Science & Technology, 2019, 53(12): 6945-6953. [31] MARTÍNEZ-HUITLE C A, RODRIGO M A, SIRÉS I, et al. Single and coupled electrochemical processes and reactors for the abatement of organic water pollutants: A critical review[J]. Chemical Reviews, 2015, 115(24): 13362-13407. doi: 10.1021/acs.chemrev.5b00361 -












 DownLoad:
DownLoad: