-
溶解性有机物(dissloved organic matter, DOM)是粒径小于0.45 μm的异质混合物,是废水中的主要成分之一[1]。DOM难以通过常规污水处理手段去除[2],且DOM的存在会对污水中其他污染物的降解产生影响。WANG等[3]研究发现,DOM会对污水中扑米酮的高级氧化降解产生影响,进而显著影响高级氧化性能;LIN等[4]发现,小分子量的DOM会促进2,4,4′-三氯联苯的降解。相较于城镇生活污水和其他工业废水,制药污水呈现出高盐度、高毒性和可生物降解性差等特征,成分更为复杂[5]。处理过程中,制药污水中DOM更容易影响处理过程,对水中污染物的去除产生影响[6]。因此,深入了解制药污水各个阶段DOM组成及其变化情况对于污水处理厂稳定运行具有重要意义。
常规评价DOM的指标主要为溶解性有机碳(dissolved organic carbon, DOC)[7]。然而,仅用单一数值指标无法表征DOM种类及其变化情况。为了解决这个问题,研究人员使用超高分辨率质谱识别DOM组成和确定分子量[2]、尺寸排阻色谱明确DOM分子量分布情况[8]、树脂柱分离确定DOM腐殖化程度[9]等。这些方法虽然可以精确表征DOM自身特性,但存在着实验过程复杂、实验耗材昂贵、操作要求高、分析时间长等不足,无法满足工业现场即时监测表征的需要。近年来,越来越多的研究使用三维荧光光谱-平行因子分析及紫外-可见吸收光谱快速表征水体DOM[10-11]。三维荧光光谱-平行因子分析(3DEEMs-PARAFAC)可以全方位识别和解析污水中DOM组分及其组分变化情况,但对于DOM分子量变化情况、DOM芳香性表征较为困难[12]。紫外-可见吸收光谱(UV-Vis)是较为成熟的光谱分析方法,具有分析速度快、操作简单等优势。UV-Vis虽在DOM组分解析方面存在困难,但结合DOC指标可以快速表征水体DOM芳香化程度、分子量大小等3DEEMs-PARAFAC方法无法提供的指标[13]。2种方法的结合使用可以一定程度上替代复杂繁琐的传统检测方法,详细、准确、快速地表征制药污水处理过程中DOM变化情况,进而从污水分子层面监测污水处理厂运行情况。
本研究对某制药工业园区中集中污水处理厂全处理流程进行采样,运用3DEEMs-PARAFAC方法和UV-Vis吸收光谱对污水处理厂全处理流程和不同处理单元DOM种类、分子量、腐殖化程度等进行表征,明确DOM变化情况,为监测污水处理厂运行情况,保证运行稳定和日后改进污水处理工艺提供可借鉴的技术方法。
-
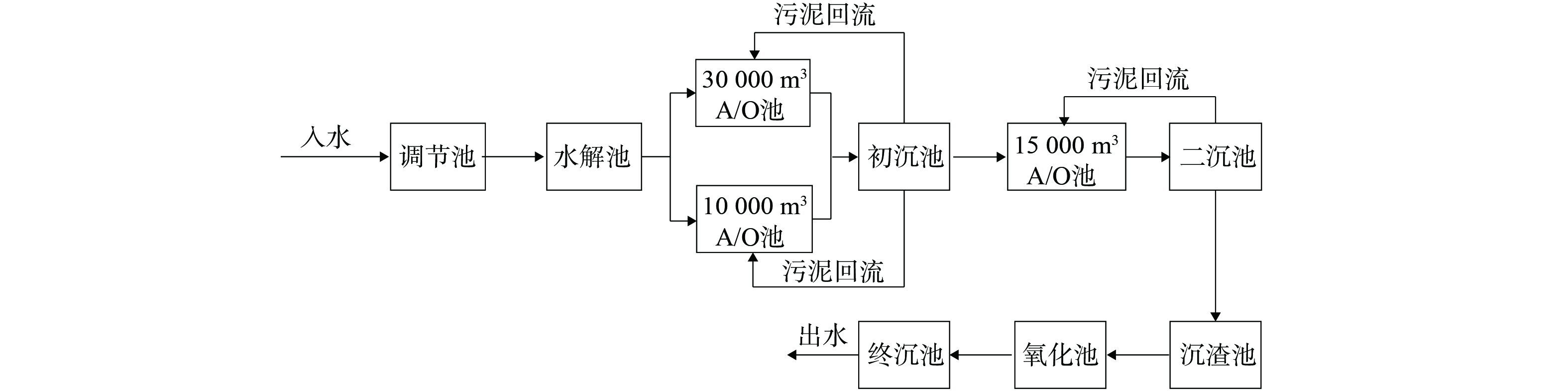
某制药园区集中污水处理厂采用如图1所示处理工艺处理园区所产生制药废水,经处理后排入园区污水管网。经了解,该制药污水处理厂主要承接制药园区内青霉素、维生素K2、辅酶Q10等药品生产工艺废水,整体水质呈现出高毒性、生物降解性差等特点。不同工艺段产生的污水于调节池混合后再进行下一步处理。本研究在制药污水处理厂调节池、水解池、10 000 m3 A/O池、30 000 m3 A/O池、15 000 m3 A/O池、初沉池、二沉池、沉渣池、氧化池、终沉池等工艺段取样,并采集出水水样。3个生化处理池在好氧段进行取样,使用0.45 μm滤膜过滤,低温保存,于48 h之内完成相关指标检测。
-
测定采集水样pH、化学需氧量(COD)、总氮(TN)、氨氮(NH3-N)、溶解性有机碳(DOC)等水质指标。pH使用pH计(PHSJ-4F,中国上海仪电科学仪器股份有限公司)测量;COD测定采用快速消解分光光度法(HJ/T399-2007)[14];TN测定使用碱性过硫酸钾消解紫外分光光度法(HJ636-2012)[15];NH3-N测定采用纳氏试剂分光光度法(HJ535-2009)[16];DOC使用总有机碳分析仪(TOC-L,日本株式会社岛津制作所)测定。
-
使用荧光分光光度计(F-7000,日本株式会社日立制作所)对水样进行三维荧光扫描。设置参数如下:激发波长(Ex)200~450 nm,发射波长(Em)250~600 nm,狭缝宽度5 nm,扫描速度12 000 nm·min−1。预实验发现直接扫描水样超出仪器量程,无法获取水样三维荧光光谱。使用Milli-Q超纯水对各水样进行稀释处理后至仪器量程范围内再进行测量,每个样品重复扫描3遍。扫描完成后,发现谱图中存在强烈的散射,以Milli-Q超纯水为参比扣除拉曼散射,采用drEEM工具箱中扣除散射命令去除瑞利散射,Delanuay三角内插法补全因扣除瑞利散射而产生的缺失空白值[17],高斯平滑去除谱图中随机噪声干扰。
-
使用紫外-可见分光光度计(DR6000,美国哈希公司),以Milli-Q超纯水作为参比对采集水样进行扫描,扫描范围190~800 nm,间隔1 nm。为去除扫描过程中水体存在的细小悬浮物造成的散射现象,采用式1和式2进行修正[18]。
式中:
α′(λ) 为波长λ处未经校正的DOM吸收系数,m−1;D(λ) 是波长λ处的吸光度;r是光学单元的路径长度,m;α(λ) 是给定波长λ处经校正散射的吸收系数,m−1。 -
平行因子分析(PARAFAC)方法的原理是将形成三相阵列X,样品为N种荧光成分的混合物的激发-发射矩阵(EEM)数据分解为3组线性项和1组残差项,其原理见式3[19]。
式中:xijk表示样本i在发射波长j和激发波长k处的荧光强度;ain与样品i中组分n的浓度成正比;bjn与发射波长j处的发射量子产率成正比;ckn与激发波长k处的吸收系数成正比;eijk表示分解误差项。
-
采用MATLABR2018a中DOMfluor工具箱对处理后荧光数据进行PARAFAC分析,运用残差平方和、半分法检验等方法确定组分数量;OpenFluor在线数据库(www.openfluor.lablicate.com)明确组分成分[20]。使用IBM SPSS Statistics 25.0软件进行相关性分析,R Studio进行相关性热图绘制;其余绘图使用Origin 2019b软件完成。
-
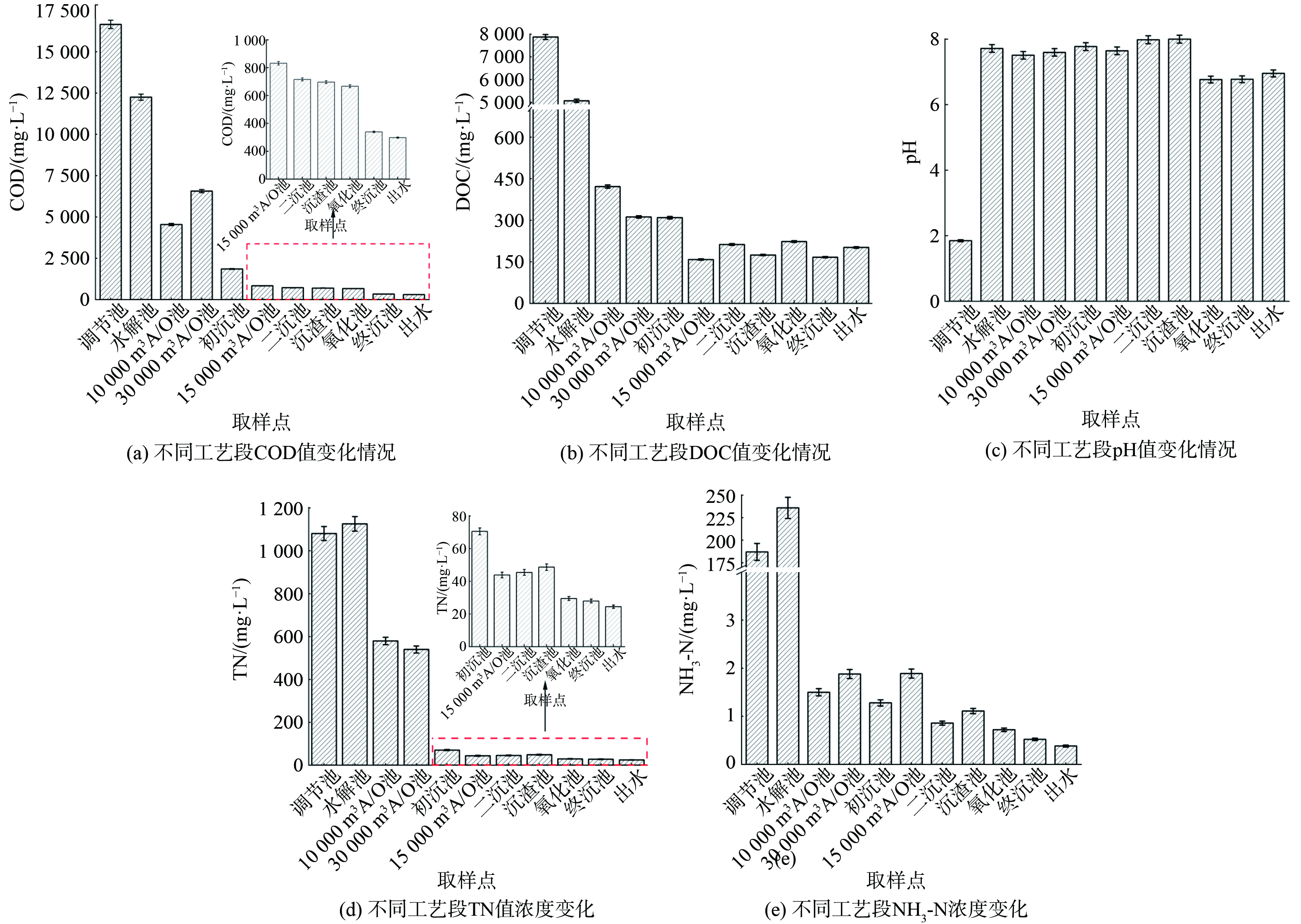
该制药污水处理厂各个流程水质参数如图2所示。pH值除调节池较低外,其余工艺段均稳定在6~8之间。总的来看,COD、TN、NH3-N和DOC随着污水处理的进行呈现显著下降的趋势。污水经过前面3个生化处理池处理后,TN、NH3-N、COD和DOC去除率均在95%以上,说明该污水处理厂生化处理池中生物活性较高,处理效果好。比较并联10 000 m3 A/O池和30 000 m3 A/O池水质指标,TN和NH3-N数值接近,说明脱氮效果基本一致;COD值10 000 m3 A/O池低于30 000 m3 A/O池。综合来看,说明10 000 m3 A/O池对有机物处理效果要优于30 000 m3 A/O池。
-
图3为该制药废水处理厂各个处理流程水样的三维荧光光谱。明显看出,经并联生化处理池处理后,水样三维荧光光谱发生较大改变。未生化处理之前,2个荧光峰主要位于Ex/Em=230(270)/350 nm区域;生化处理后,荧光峰位置改变,位于Ex/Em=200~250/350~450 nm和Ex/Em=300~350/400~450 nm 2个区域。
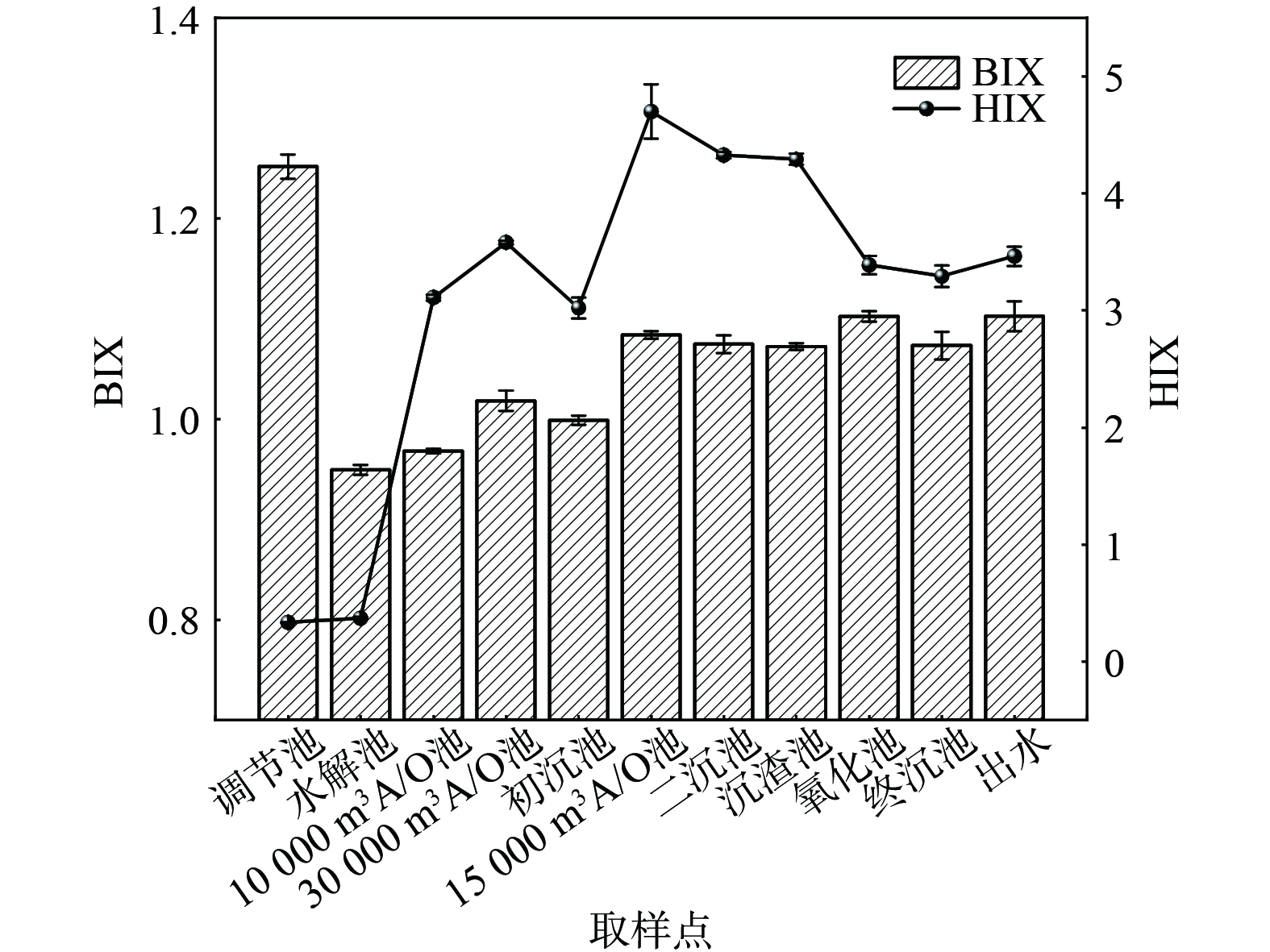
依据三维荧光光谱数据,计算各个样品的腐殖化指数(HIX)和生物源指数(BIX)。HIX是固定激发波长254 nm,发射波长435~480 nm之间荧光强度积分和300~345 nm之间荧光强度积分比值,用来表征水体DOM腐殖化程度,HIX<4腐殖化程度低,HIX>4腐殖化程度高[21]。BIX是Ex=310 nm,Em=380 nm和430 nm处荧光强度比值,用来表征DOM自生源在水中贡献,BIX>1.0说明DOM来自内生源,0.8<BIX<1.0说明内生源对DOM贡献较大,0.6<BIX<0.8则说明内生源贡献较小[22]。由各处理流程水样三维荧光光谱计算得到BIX和HIX,计算结果见图4。计算发现,各个处理流程BIX指数介于0.95~1.25之间,说明污水中绝大多数DOM来源于内生源,与外界干扰无关。HIX指数经生化处理后增长迅速,在15 000 m3 A/O池最高,间接说明生化处理使得污水中腐殖质类物质增加;HIX指数经深度氧化处理流程后下降到分界值以下,降低了水体的腐殖化程度。
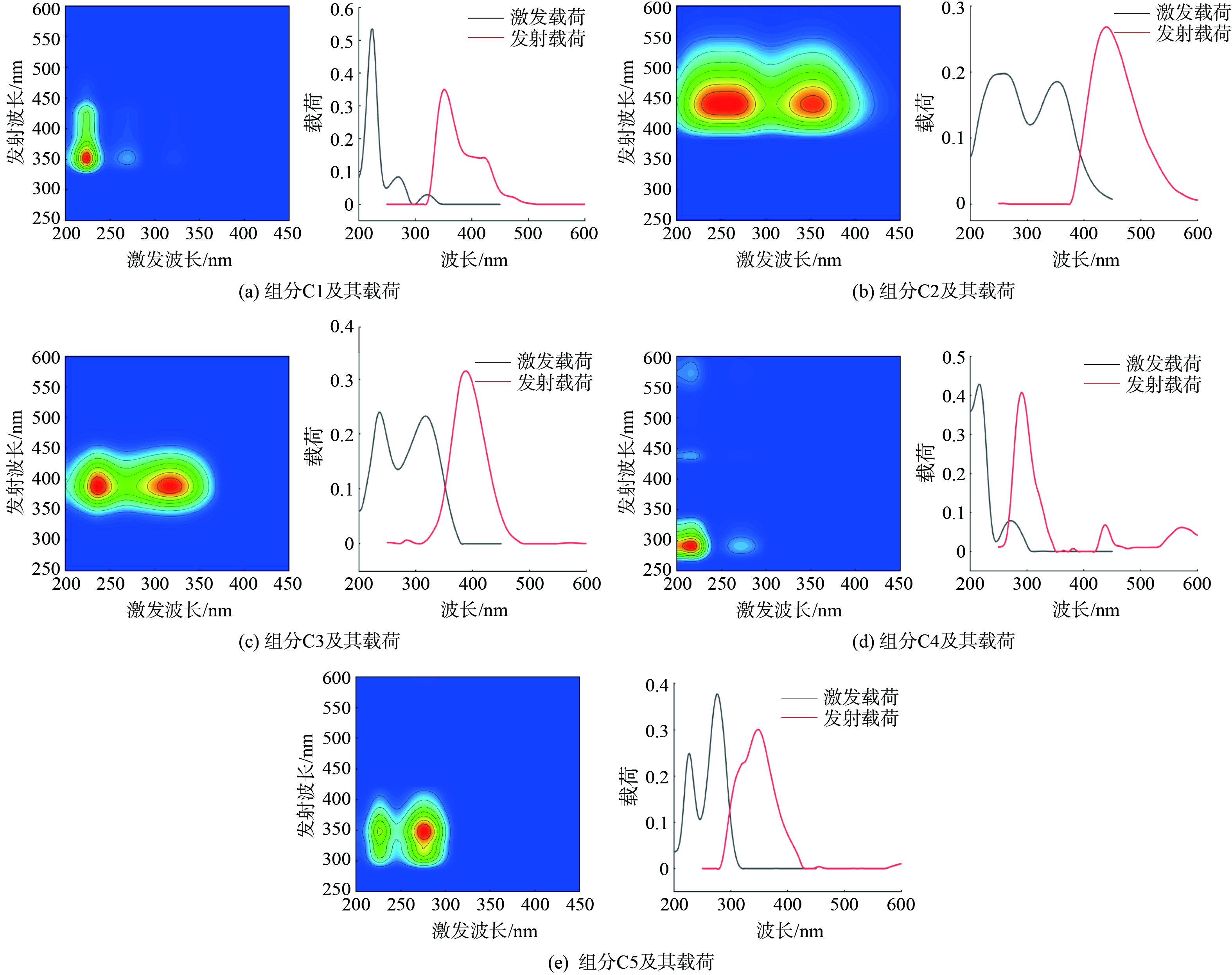
图5是经PARAFAC算法从荧光数据集中识别出来的5种大分子组分三维荧光光谱及其对应载荷。与数据库数据进行数据对比时Ex和Em相似性得分均设置为0.95。表1列举了5类大分子组分对比结果。由对比结果可知,水样中含有类腐殖质和类蛋白类荧光基团,C2和C3组分分别为类腐殖酸物质和类富里酸物质;类蛋白组分C4和C5分别为类酪氨酸物质和类色氨酸物质;未在数据库中检索到C1组分,但C1组分与调节池和水解池三维荧光光谱高度相似,故组分C1可能与制药污水中独特的荧光发光组分高度相关。梁月清等 [29]研究了某工业园区污水处理厂各处理工艺DOM变化情况,其DOM组分特征为腐殖质样和类蛋白样,与本研究高度相似。
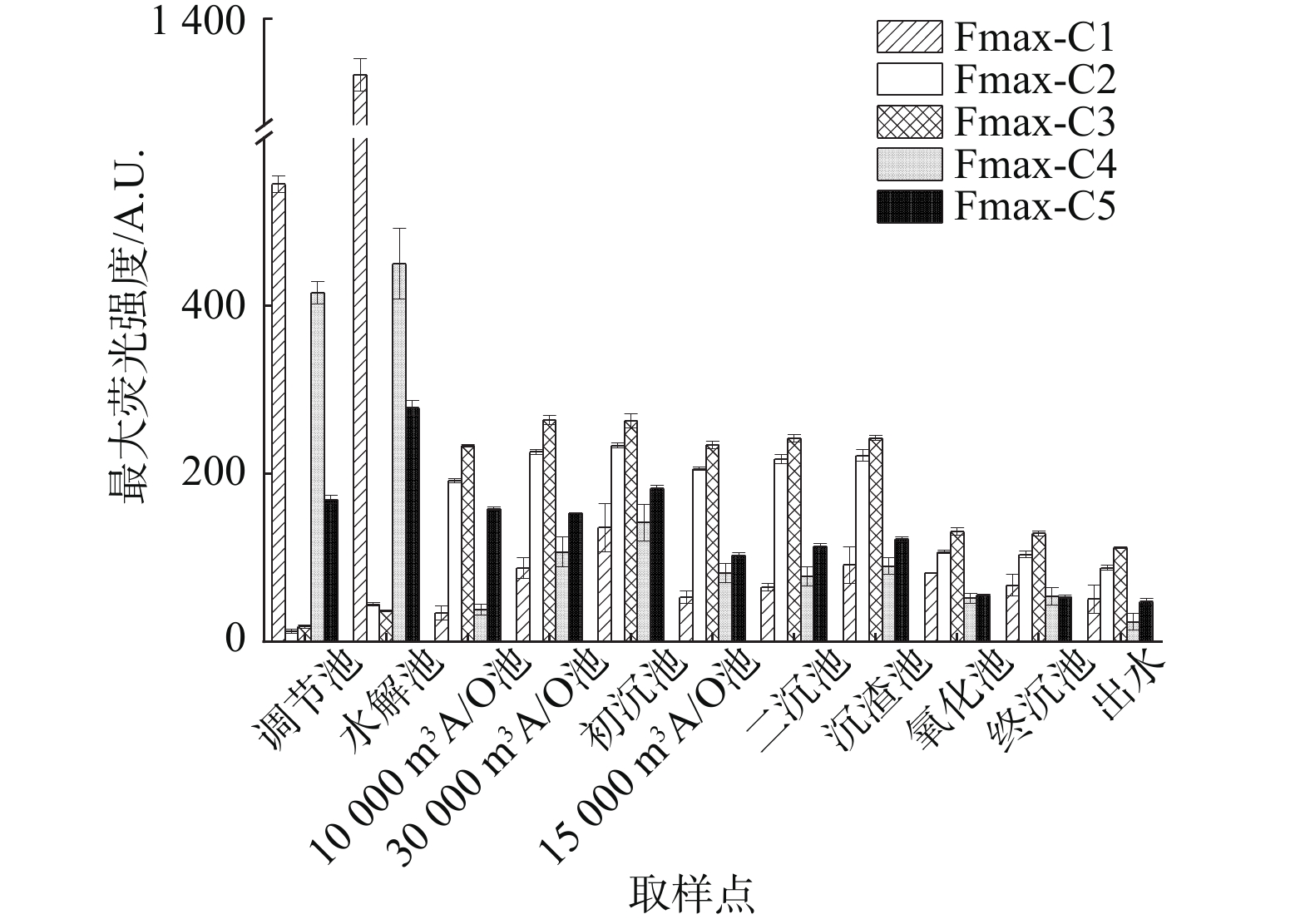
污水处理每个阶段,其DOM组分可能相近,但组分强度会发生变化[30]。图6展示了制药废水在每个处理阶段解析出来的5组分最大荧光强度(Fmax)及其变化情况。与调节池Fmax值相比,C1组分Fmax值在水解池急剧上升,经生化处理过后Fmax值大幅度下降,说明物化处理会使得污水中某些物质转变为独特的荧光发光组分,而微生物会有效地去除这类独特的有机组分。C2和C3两种腐殖质成分则与C1变化趋势相反,经生化处理后,水样中C2和C3组分Fmax大幅升高,深度氧化处理后C2和C3组分Fmax略微降低,与HIX指数变化趋势一致。有的研究发现污水经生化处理后出现新的腐殖质物质,并且原有腐殖质荧光峰呈现增强的趋势[31]。李胜楠等[32]对制药废水三维荧光光谱分析,发现制药废水经生化处理后二级出水DOM主要为腐殖质类物质。经生化处理后水中腐殖质升高可能的原因是污水中含有的糖类与类蛋白质类物质在微生物的作用下发生美拉德反应,生成腐殖质类大分子物质,从而导致污水经生化处理后腐殖质含量上升[33]。生化处理后的深度氧化工艺使得部分腐殖质物质转变为其他可溶性发色物质,表现出腐殖质组分Fmax值降低。类蛋白组分C4和C5的Fmax值在物化处理阶段小幅度提升,经生化处理后数值下降并保持一定程度的稳定,深度氧化处理后数值进一步下降并保持稳定。可能的原因是物化处理导致大分子物质水解为类蛋白类小分子物质使得类蛋白组分上升[6];生化处理过程中微生物自身作用使得类蛋白组分下降,一定程度上印证了生化反应中美拉德反应的发生;最后的深度氧化处理导致类蛋白物质变为分子量更小的物质,使得类蛋白Fmax值下降。
-
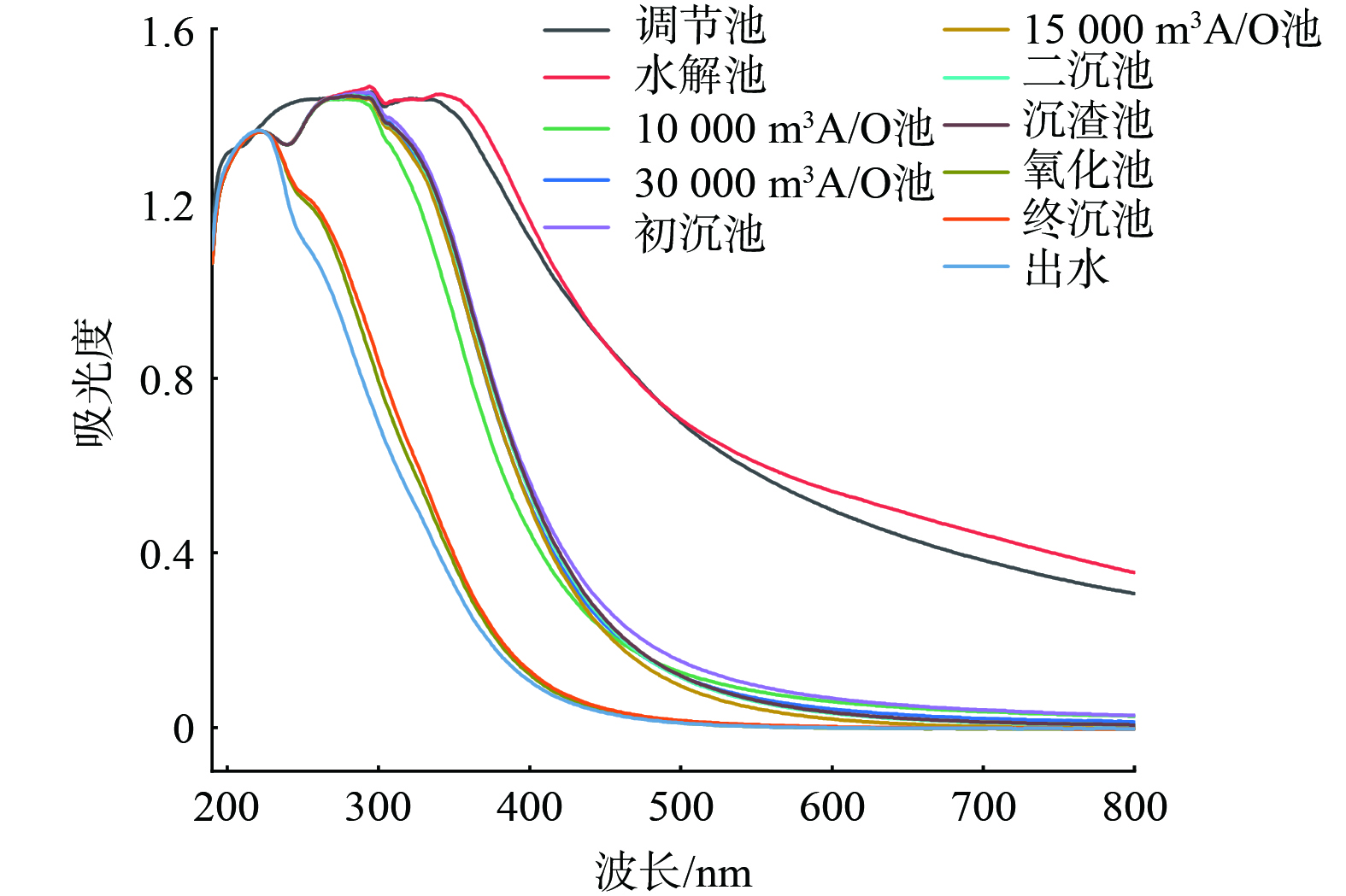
UV-Vis根据不同波段DOM的吸光度可以解析出DOM芳香化程度、分子量大小等三维荧光光谱较难提供的信息。制药污水处理各工艺段水样原始UV-Vis光谱见图7。由图7可知,不同处理工艺水样吸光度均表现出先上升后下降的趋势。随着污水过程的推进,水样吸收光谱逐渐蓝移。氧化池、终沉池和出水水样变化基本一致,吸收峰在220 nm附近;调节池和水解池吸收光谱大致相同,在200 nm至400 nm处存在多个吸收峰,表明存在多种物质,水样中有大量的发色团物质重叠,进一步验证和说明了进水水质的复杂性;其余处理部分水样吸收光谱在220 nm和270 nm附近有2个较为明显的吸收峰。由荧光解析结果推断,270 nm附近吸收峰可能是水样中腐殖质类物质吸收产生;220 nm处紫外吸收峰是有可能是蛋白质类物质特征吸收峰。
依据UV-Vis吸收光谱及校正公式,计算250 nm吸光度和365 nm吸光度比值(E2/E3),表征DOM分子量变化,值越高DOM分子量越小[34];254 nm吸收系数与DOC比值(SUVA254)表征DOM芳香化程度,数值越高DOM芳香性越高[35];300 nm吸光度和400 nm吸光度比值(E3/E4)表征DOM腐殖化程度,比值小于3.5时腐殖酸为主,大于3.5富里酸占主要部分[36]。GAO等[37]选用SUVA254、E2/E3和E3/E4指标对制革废水处理过程中DOM芳香性、分子量和腐殖化程度进行表征;KOU等[38]利用SUVA254指标表征石化废水处理厂处理过程中污水芳香性变化;YU等[39]利用SUVA254、E2/E3和E3/E4 3项紫外-可见吸收光谱计算指标揭示了污水经膜生物反应器和纳滤之后DOM芳香性、分子量和腐殖化程度变化情况。
图8展现了不同工艺段SUA254变化情况。经前2个并联A/O池生化处理后SUVA254数值急剧升高,在随后15 000 m3 A/O池中达到极大值,经氧化池深度氧化后数值下降。这表明污水生化处理过程中DOM芳香性加强,深度氧化处理导致DOM芳香性减弱。造成这种现象可能的原因是大分子有机污染物在微生物作用下转变为含有大量不饱和键有机物,导致数值升高[40];同时生化处理使得DOC浓度从水解池(5 066±71.0) mg·L−1大幅度下降到初沉池(309.1±4.3) mg·L−1,而254 nm处吸收系数同DOC数值超过90%大幅下降相比变化不大,在数值计算层面表现出经生化处理后SUVA254数值大幅度升高。深度氧化过程使得苯环打开,有机物中不饱和键减少,从而导致数值下降[41]。同时注意到二沉池、沉渣池和终沉池SUVA254数值极不稳定,可能与污泥自身吸附解吸有机物、长距离管道运输等因素导致DOC浓度变化有关。
图9展示了E2/E3和E3/E4比值变化情况。E2/E3和E3/E4在氧化池深度氧化均表现出突变升高。水样经过氧化池深度氧化处理之后,腐殖质中大量腐殖酸转变为富里酸,同时DOM分子质量减少,这说明深度氧化处理工艺把分子量较大的腐殖酸氧化为分子量更小、结构更为简单的富里酸,同时把其他大分子DOM氧化为分子量较小的物质。除了氧化池阶段数值突变升高之外,注意到E2/E3数值在生化处理过程中小幅升高,E3/E4数值大幅升高,间接说明生化处理过程中腐殖质的生成和大分子物质降解为小分子物质。生化处理和深度氧化处理两阶段处理中比值的升高,与前文Fmax值变化情况相互验证,间接证明了生化处理过程中发生美拉德反应从而产生腐殖质的可能性。
-
对解析出的5组分大分子有机物同检测各项水质指标进行相关性分析,分析结果见图10。C1组分与C4组分(r=0.91, p<0.001)呈现出极为显著正相关,同C5组分(r=0.79, p<0.01)呈现出显著正相关,而C4、C5组分主要是类蛋白质组分,结合Fmax值变化情况,推测未解析出成分的C1组分可能与蛋白质类物质及其衍生物高度同源。类腐殖酸组分C2和类富里酸组分C3与水样DOC均呈现显著负相关,一定情况下可以使用C2和C3组分Fmax值快速判断污水处理过程中DOC变化情况。C4组分与NH3-N(r=0.97, p<0.001)和TN(r=0.86, p<0.001)呈现出极显著正相关,故可以利用C4组分Fmax值变化趋势快速了解污水处理过程中污水氮含量变化情况。SUVA254数值与TN和C4组分呈现出高度负相关,在不便得到C4组分Fmax值情况下,可以使用SUVA254数值表征水体氮含量变化。注意到同为类蛋白组分的类色氨酸C5组分除与C4组分有显著正相关(r=0.80, p<0.01)外,与其他指标之间相关性均不如组分C4显著。研究表明类酪氨酸组分与微生物自身活动相关,类色氨酸组分可以指示水体中游离蛋白质物质[42]。微生物自身活动对水体相关污染物的去除至关重要[43]。微生物自身活动可能是组分C4和C5相关性差异的原因。
-
1) 3DEEMs-PARAFAC方法解析出制药污水中主要含有5类大分子DOM组分,其中组分C2和C3为类腐殖质组分,C4和C5为类蛋白质组分,C1虽未明确具体成分,但经分析发现与类蛋白质组分高度相关。
2) 紫外-可见吸收光谱表明,生化处理过程中DOM芳香性、DOM腐殖化程度升高;深度氧化处理后小分子DOM物质占比增加。随着处理工艺的进行,DOM分子量逐渐降低。
3) 相关性分析表明,可以使用C4组分Fmax值和SUVA254值快速表征污水在处理过程中含氮量变化,类腐殖质C2和C3组分Fmax值表征DOC变化情况。
4) 三维荧光光谱-平行因子分析和紫外-可见吸收光谱可以一定程度上替代超高分辨率质谱、尺寸排阻色谱、树脂柱分离等方法对制药污水处理过程中DOM特征变化进行快速表征。
基于三维荧光光谱-平行因子分析及紫外-可见吸收光谱对制药污水不同处理工艺单元溶解性有机物特征分析
Characterization of dissolved organic matter in pharmaceutical wastewater treatment process units based on three-dimensional fluorescence spectroscopy-parallel factor analysis and ultraviolet-visible absorption spectroscopy
-
摘要: 利用三维荧光光谱-平行因子分析法和紫外-可见吸收光谱2种技术方法对某制药园区污水处理厂处理过程中污水溶解性有机物种类、分子量、腐殖化程度等进行表征,同时对解析出的溶解性有机物组分和水质指标进行相关性分析。三维荧光光谱-平行因子分析法解析出5类大分子溶解性有机物,组分C1是制药污水中特征污染物,组分C2和C3属于类腐殖质物质,组分C4和C5为类蛋白质物质。紫外-可见吸收光谱表明,处理过程中溶解性有机物分子量逐渐降低,腐殖化程度呈现先上升后下降的趋势。相关性分析表明,组分C4和SUVA254数值可以快速推断污水处理过程中氮含量变化情况,组分C2和C3可以推断污水溶解性有机碳变化情况。本研究技术方法和结果可以为监测污水处理厂运行情况和日后改进污水处理工艺提供支持。Abstract: The types, molecular weights, and humification degree of dissolved organic matter in wastewater treatment process of a pharmaceutical park were characterized by three-dimensional fluorescence spectroscopy-parallel factor analysis and ultraviolet-visible absorption spectroscopy. Meanwhile, the correlations between the dissolved organic matter fractions and water quality indicators were analyzed. Therefore, five types of macromolecular dissolved organic matter were tested by three-dimensional fluorescence spectroscopy-parallel factor analysis, which component C1 was the characteristic pollutant in pharmaceutical wastewater, and components C2 and C3 were humus-like substances, as well as components C4 and C5 were protein-like substances. Subsequently, ultraviolet-visible absorption spectra showed that the molecular weight of dissolved organic matter decreased gradually during the treatment, and the humification degree increased first and then decreased. Furthermore, the correlation analysis indicated that the values of components C4 and SUVA254 could quickly infer the change of nitrogen content in wastewater treatment process, and components C2 and C3 could predict the changes of dissolved organic carbon in sewage. Hence, the technical approach and results of this study could provide supports for monitoring the operation of wastewater treatment plants and improving the wastewater treatment process in the future.
-
溶解性有机物(dissloved organic matter, DOM)是粒径小于0.45 μm的异质混合物,是废水中的主要成分之一[1]。DOM难以通过常规污水处理手段去除[2],且DOM的存在会对污水中其他污染物的降解产生影响。WANG等[3]研究发现,DOM会对污水中扑米酮的高级氧化降解产生影响,进而显著影响高级氧化性能;LIN等[4]发现,小分子量的DOM会促进2,4,4′-三氯联苯的降解。相较于城镇生活污水和其他工业废水,制药污水呈现出高盐度、高毒性和可生物降解性差等特征,成分更为复杂[5]。处理过程中,制药污水中DOM更容易影响处理过程,对水中污染物的去除产生影响[6]。因此,深入了解制药污水各个阶段DOM组成及其变化情况对于污水处理厂稳定运行具有重要意义。
常规评价DOM的指标主要为溶解性有机碳(dissolved organic carbon, DOC)[7]。然而,仅用单一数值指标无法表征DOM种类及其变化情况。为了解决这个问题,研究人员使用超高分辨率质谱识别DOM组成和确定分子量[2]、尺寸排阻色谱明确DOM分子量分布情况[8]、树脂柱分离确定DOM腐殖化程度[9]等。这些方法虽然可以精确表征DOM自身特性,但存在着实验过程复杂、实验耗材昂贵、操作要求高、分析时间长等不足,无法满足工业现场即时监测表征的需要。近年来,越来越多的研究使用三维荧光光谱-平行因子分析及紫外-可见吸收光谱快速表征水体DOM[10-11]。三维荧光光谱-平行因子分析(3DEEMs-PARAFAC)可以全方位识别和解析污水中DOM组分及其组分变化情况,但对于DOM分子量变化情况、DOM芳香性表征较为困难[12]。紫外-可见吸收光谱(UV-Vis)是较为成熟的光谱分析方法,具有分析速度快、操作简单等优势。UV-Vis虽在DOM组分解析方面存在困难,但结合DOC指标可以快速表征水体DOM芳香化程度、分子量大小等3DEEMs-PARAFAC方法无法提供的指标[13]。2种方法的结合使用可以一定程度上替代复杂繁琐的传统检测方法,详细、准确、快速地表征制药污水处理过程中DOM变化情况,进而从污水分子层面监测污水处理厂运行情况。
本研究对某制药工业园区中集中污水处理厂全处理流程进行采样,运用3DEEMs-PARAFAC方法和UV-Vis吸收光谱对污水处理厂全处理流程和不同处理单元DOM种类、分子量、腐殖化程度等进行表征,明确DOM变化情况,为监测污水处理厂运行情况,保证运行稳定和日后改进污水处理工艺提供可借鉴的技术方法。
1. 材料与方法
1.1 样品采集
某制药园区集中污水处理厂采用如图1所示处理工艺处理园区所产生制药废水,经处理后排入园区污水管网。经了解,该制药污水处理厂主要承接制药园区内青霉素、维生素K2、辅酶Q10等药品生产工艺废水,整体水质呈现出高毒性、生物降解性差等特点。不同工艺段产生的污水于调节池混合后再进行下一步处理。本研究在制药污水处理厂调节池、水解池、10 000 m3 A/O池、30 000 m3 A/O池、15 000 m3 A/O池、初沉池、二沉池、沉渣池、氧化池、终沉池等工艺段取样,并采集出水水样。3个生化处理池在好氧段进行取样,使用0.45 μm滤膜过滤,低温保存,于48 h之内完成相关指标检测。
1.2 常规指标测定方法
测定采集水样pH、化学需氧量(COD)、总氮(TN)、氨氮(NH3-N)、溶解性有机碳(DOC)等水质指标。pH使用pH计(PHSJ-4F,中国上海仪电科学仪器股份有限公司)测量;COD测定采用快速消解分光光度法(HJ/T399-2007)[14];TN测定使用碱性过硫酸钾消解紫外分光光度法(HJ636-2012)[15];NH3-N测定采用纳氏试剂分光光度法(HJ535-2009)[16];DOC使用总有机碳分析仪(TOC-L,日本株式会社岛津制作所)测定。
1.3 三维荧光光谱测定方法
使用荧光分光光度计(F-7000,日本株式会社日立制作所)对水样进行三维荧光扫描。设置参数如下:激发波长(Ex)200~450 nm,发射波长(Em)250~600 nm,狭缝宽度5 nm,扫描速度12 000 nm·min−1。预实验发现直接扫描水样超出仪器量程,无法获取水样三维荧光光谱。使用Milli-Q超纯水对各水样进行稀释处理后至仪器量程范围内再进行测量,每个样品重复扫描3遍。扫描完成后,发现谱图中存在强烈的散射,以Milli-Q超纯水为参比扣除拉曼散射,采用drEEM工具箱中扣除散射命令去除瑞利散射,Delanuay三角内插法补全因扣除瑞利散射而产生的缺失空白值[17],高斯平滑去除谱图中随机噪声干扰。
1.4 分析方法
使用紫外-可见分光光度计(DR6000,美国哈希公司),以Milli-Q超纯水作为参比对采集水样进行扫描,扫描范围190~800 nm,间隔1 nm。为去除扫描过程中水体存在的细小悬浮物造成的散射现象,采用式1和式2进行修正[18]。
stringUtils.convertMath(!{formula.content}) (1) stringUtils.convertMath(!{formula.content}) (2) 式中:
α′(λ) D(λ) α(λ) 1.5 平行因子分析方法
平行因子分析(PARAFAC)方法的原理是将形成三相阵列X,样品为N种荧光成分的混合物的激发-发射矩阵(EEM)数据分解为3组线性项和1组残差项,其原理见式3[19]。
stringUtils.convertMath(!{formula.content}) (3) 式中:xijk表示样本i在发射波长j和激发波长k处的荧光强度;ain与样品i中组分n的浓度成正比;bjn与发射波长j处的发射量子产率成正比;ckn与激发波长k处的吸收系数成正比;eijk表示分解误差项。
1.6 数据统计与分析
采用MATLABR2018a中DOMfluor工具箱对处理后荧光数据进行PARAFAC分析,运用残差平方和、半分法检验等方法确定组分数量;OpenFluor在线数据库(www.openfluor.lablicate.com)明确组分成分[20]。使用IBM SPSS Statistics 25.0软件进行相关性分析,R Studio进行相关性热图绘制;其余绘图使用Origin 2019b软件完成。
2. 结果与讨论
2.1 污水处理厂不同处理单元常规污染物处理效果分析
该制药污水处理厂各个流程水质参数如图2所示。pH值除调节池较低外,其余工艺段均稳定在6~8之间。总的来看,COD、TN、NH3-N和DOC随着污水处理的进行呈现显著下降的趋势。污水经过前面3个生化处理池处理后,TN、NH3-N、COD和DOC去除率均在95%以上,说明该污水处理厂生化处理池中生物活性较高,处理效果好。比较并联10 000 m3 A/O池和30 000 m3 A/O池水质指标,TN和NH3-N数值接近,说明脱氮效果基本一致;COD值10 000 m3 A/O池低于30 000 m3 A/O池。综合来看,说明10 000 m3 A/O池对有机物处理效果要优于30 000 m3 A/O池。
2.2 制药污水三维荧光光谱及PARAFAC解析
图3为该制药废水处理厂各个处理流程水样的三维荧光光谱。明显看出,经并联生化处理池处理后,水样三维荧光光谱发生较大改变。未生化处理之前,2个荧光峰主要位于Ex/Em=230(270)/350 nm区域;生化处理后,荧光峰位置改变,位于Ex/Em=200~250/350~450 nm和Ex/Em=300~350/400~450 nm 2个区域。
依据三维荧光光谱数据,计算各个样品的腐殖化指数(HIX)和生物源指数(BIX)。HIX是固定激发波长254 nm,发射波长435~480 nm之间荧光强度积分和300~345 nm之间荧光强度积分比值,用来表征水体DOM腐殖化程度,HIX<4腐殖化程度低,HIX>4腐殖化程度高[21]。BIX是Ex=310 nm,Em=380 nm和430 nm处荧光强度比值,用来表征DOM自生源在水中贡献,BIX>1.0说明DOM来自内生源,0.8<BIX<1.0说明内生源对DOM贡献较大,0.6<BIX<0.8则说明内生源贡献较小[22]。由各处理流程水样三维荧光光谱计算得到BIX和HIX,计算结果见图4。计算发现,各个处理流程BIX指数介于0.95~1.25之间,说明污水中绝大多数DOM来源于内生源,与外界干扰无关。HIX指数经生化处理后增长迅速,在15 000 m3 A/O池最高,间接说明生化处理使得污水中腐殖质类物质增加;HIX指数经深度氧化处理流程后下降到分界值以下,降低了水体的腐殖化程度。
图5是经PARAFAC算法从荧光数据集中识别出来的5种大分子组分三维荧光光谱及其对应载荷。与数据库数据进行数据对比时Ex和Em相似性得分均设置为0.95。表1列举了5类大分子组分对比结果。由对比结果可知,水样中含有类腐殖质和类蛋白类荧光基团,C2和C3组分分别为类腐殖酸物质和类富里酸物质;类蛋白组分C4和C5分别为类酪氨酸物质和类色氨酸物质;未在数据库中检索到C1组分,但C1组分与调节池和水解池三维荧光光谱高度相似,故组分C1可能与制药污水中独特的荧光发光组分高度相关。梁月清等 [29]研究了某工业园区污水处理厂各处理工艺DOM变化情况,其DOM组分特征为腐殖质样和类蛋白样,与本研究高度相似。
表 1 5组分对应的大分子物质Table 1. Macromolecules corresponding to 5 components污水处理每个阶段,其DOM组分可能相近,但组分强度会发生变化[30]。图6展示了制药废水在每个处理阶段解析出来的5组分最大荧光强度(Fmax)及其变化情况。与调节池Fmax值相比,C1组分Fmax值在水解池急剧上升,经生化处理过后Fmax值大幅度下降,说明物化处理会使得污水中某些物质转变为独特的荧光发光组分,而微生物会有效地去除这类独特的有机组分。C2和C3两种腐殖质成分则与C1变化趋势相反,经生化处理后,水样中C2和C3组分Fmax大幅升高,深度氧化处理后C2和C3组分Fmax略微降低,与HIX指数变化趋势一致。有的研究发现污水经生化处理后出现新的腐殖质物质,并且原有腐殖质荧光峰呈现增强的趋势[31]。李胜楠等[32]对制药废水三维荧光光谱分析,发现制药废水经生化处理后二级出水DOM主要为腐殖质类物质。经生化处理后水中腐殖质升高可能的原因是污水中含有的糖类与类蛋白质类物质在微生物的作用下发生美拉德反应,生成腐殖质类大分子物质,从而导致污水经生化处理后腐殖质含量上升[33]。生化处理后的深度氧化工艺使得部分腐殖质物质转变为其他可溶性发色物质,表现出腐殖质组分Fmax值降低。类蛋白组分C4和C5的Fmax值在物化处理阶段小幅度提升,经生化处理后数值下降并保持一定程度的稳定,深度氧化处理后数值进一步下降并保持稳定。可能的原因是物化处理导致大分子物质水解为类蛋白类小分子物质使得类蛋白组分上升[6];生化处理过程中微生物自身作用使得类蛋白组分下降,一定程度上印证了生化反应中美拉德反应的发生;最后的深度氧化处理导致类蛋白物质变为分子量更小的物质,使得类蛋白Fmax值下降。
2.3 制药污水紫外-可见吸收光谱分析
UV-Vis根据不同波段DOM的吸光度可以解析出DOM芳香化程度、分子量大小等三维荧光光谱较难提供的信息。制药污水处理各工艺段水样原始UV-Vis光谱见图7。由图7可知,不同处理工艺水样吸光度均表现出先上升后下降的趋势。随着污水过程的推进,水样吸收光谱逐渐蓝移。氧化池、终沉池和出水水样变化基本一致,吸收峰在220 nm附近;调节池和水解池吸收光谱大致相同,在200 nm至400 nm处存在多个吸收峰,表明存在多种物质,水样中有大量的发色团物质重叠,进一步验证和说明了进水水质的复杂性;其余处理部分水样吸收光谱在220 nm和270 nm附近有2个较为明显的吸收峰。由荧光解析结果推断,270 nm附近吸收峰可能是水样中腐殖质类物质吸收产生;220 nm处紫外吸收峰是有可能是蛋白质类物质特征吸收峰。
依据UV-Vis吸收光谱及校正公式,计算250 nm吸光度和365 nm吸光度比值(E2/E3),表征DOM分子量变化,值越高DOM分子量越小[34];254 nm吸收系数与DOC比值(SUVA254)表征DOM芳香化程度,数值越高DOM芳香性越高[35];300 nm吸光度和400 nm吸光度比值(E3/E4)表征DOM腐殖化程度,比值小于3.5时腐殖酸为主,大于3.5富里酸占主要部分[36]。GAO等[37]选用SUVA254、E2/E3和E3/E4指标对制革废水处理过程中DOM芳香性、分子量和腐殖化程度进行表征;KOU等[38]利用SUVA254指标表征石化废水处理厂处理过程中污水芳香性变化;YU等[39]利用SUVA254、E2/E3和E3/E4 3项紫外-可见吸收光谱计算指标揭示了污水经膜生物反应器和纳滤之后DOM芳香性、分子量和腐殖化程度变化情况。
图8展现了不同工艺段SUA254变化情况。经前2个并联A/O池生化处理后SUVA254数值急剧升高,在随后15 000 m3 A/O池中达到极大值,经氧化池深度氧化后数值下降。这表明污水生化处理过程中DOM芳香性加强,深度氧化处理导致DOM芳香性减弱。造成这种现象可能的原因是大分子有机污染物在微生物作用下转变为含有大量不饱和键有机物,导致数值升高[40];同时生化处理使得DOC浓度从水解池(5 066±71.0) mg·L−1大幅度下降到初沉池(309.1±4.3) mg·L−1,而254 nm处吸收系数同DOC数值超过90%大幅下降相比变化不大,在数值计算层面表现出经生化处理后SUVA254数值大幅度升高。深度氧化过程使得苯环打开,有机物中不饱和键减少,从而导致数值下降[41]。同时注意到二沉池、沉渣池和终沉池SUVA254数值极不稳定,可能与污泥自身吸附解吸有机物、长距离管道运输等因素导致DOC浓度变化有关。
图9展示了E2/E3和E3/E4比值变化情况。E2/E3和E3/E4在氧化池深度氧化均表现出突变升高。水样经过氧化池深度氧化处理之后,腐殖质中大量腐殖酸转变为富里酸,同时DOM分子质量减少,这说明深度氧化处理工艺把分子量较大的腐殖酸氧化为分子量更小、结构更为简单的富里酸,同时把其他大分子DOM氧化为分子量较小的物质。除了氧化池阶段数值突变升高之外,注意到E2/E3数值在生化处理过程中小幅升高,E3/E4数值大幅升高,间接说明生化处理过程中腐殖质的生成和大分子物质降解为小分子物质。生化处理和深度氧化处理两阶段处理中比值的升高,与前文Fmax值变化情况相互验证,间接证明了生化处理过程中发生美拉德反应从而产生腐殖质的可能性。
2.4 制药污水各指标相关性分析
对解析出的5组分大分子有机物同检测各项水质指标进行相关性分析,分析结果见图10。C1组分与C4组分(r=0.91, p<0.001)呈现出极为显著正相关,同C5组分(r=0.79, p<0.01)呈现出显著正相关,而C4、C5组分主要是类蛋白质组分,结合Fmax值变化情况,推测未解析出成分的C1组分可能与蛋白质类物质及其衍生物高度同源。类腐殖酸组分C2和类富里酸组分C3与水样DOC均呈现显著负相关,一定情况下可以使用C2和C3组分Fmax值快速判断污水处理过程中DOC变化情况。C4组分与NH3-N(r=0.97, p<0.001)和TN(r=0.86, p<0.001)呈现出极显著正相关,故可以利用C4组分Fmax值变化趋势快速了解污水处理过程中污水氮含量变化情况。SUVA254数值与TN和C4组分呈现出高度负相关,在不便得到C4组分Fmax值情况下,可以使用SUVA254数值表征水体氮含量变化。注意到同为类蛋白组分的类色氨酸C5组分除与C4组分有显著正相关(r=0.80, p<0.01)外,与其他指标之间相关性均不如组分C4显著。研究表明类酪氨酸组分与微生物自身活动相关,类色氨酸组分可以指示水体中游离蛋白质物质[42]。微生物自身活动对水体相关污染物的去除至关重要[43]。微生物自身活动可能是组分C4和C5相关性差异的原因。
3. 结论
1) 3DEEMs-PARAFAC方法解析出制药污水中主要含有5类大分子DOM组分,其中组分C2和C3为类腐殖质组分,C4和C5为类蛋白质组分,C1虽未明确具体成分,但经分析发现与类蛋白质组分高度相关。
2) 紫外-可见吸收光谱表明,生化处理过程中DOM芳香性、DOM腐殖化程度升高;深度氧化处理后小分子DOM物质占比增加。随着处理工艺的进行,DOM分子量逐渐降低。
3) 相关性分析表明,可以使用C4组分Fmax值和SUVA254值快速表征污水在处理过程中含氮量变化,类腐殖质C2和C3组分Fmax值表征DOC变化情况。
4) 三维荧光光谱-平行因子分析和紫外-可见吸收光谱可以一定程度上替代超高分辨率质谱、尺寸排阻色谱、树脂柱分离等方法对制药污水处理过程中DOM特征变化进行快速表征。
-
-
[1] WANG J, LIU D, YU H, et al. Insight into suppression of dibutyl phthalate on DOM removal during municipal sewage treatment using fluorescence spectroscopy with PARAFAC and moving-window 2D-COS[J]. Science of the Total Environment, 2023, 878: 163210. doi: 10.1016/j.scitotenv.2023.163210 [2] GAN S, WU P, SONG Y, et al. Non-targeted characterization of dissolved organic matter from a wastewater treatment plant by FT-ICR-MS: A case study of hospital sewage[J]. Journal of Water Process Engineering, 2022, 48: 102834. doi: 10.1016/j.jwpe.2022.102834 [3] WANG Y, COUET M, GUTIERREZ L, et al. Impact of DOM source and character on the degradation of primidone by UV/chlorine: Reaction kinetics and disinfection by-product formation[J]. Water Research, 2020, 172: 115463. doi: 10.1016/j.watres.2019.115463 [4] LIN Z R, ZHAO L, DONG Y H. Effects of low molecular weight organic acids and fulvic acid on 2, 4, 4′-trichlorobiphenyl degradation and hydroxyl radical formation in a goethite-catalyzed Fenton-like reaction[J]. Chemical Engineering Journal, 2017, 326: 201-209. doi: 10.1016/j.cej.2017.05.112 [5] ZHANG J, DENG Y, SHI W, et al. Advanced treatment of pharmaceutical wastewater with foam fractionation coupled with heterogeneous Fenton[J]. Journal of Water Process Engineering, 2023, 54: 104052. doi: 10.1016/j.jwpe.2023.104052 [6] WEN L, YANG F, LI X, et al. Composition of dissolved organic matter (DOM) in wastewater treatment plants influent affects the efficiency of carbon and nitrogen removal[J]. Science of the Total Environment, 2023, 857: 159541. doi: 10.1016/j.scitotenv.2022.159541 [7] WU F C, KOTHAWALA D N, EVANS R D, et al. Relationships between DOC concentration, molecular size and fluorescence properties of DOM in a stream[J]. Applied Geochemistry, 2007, 22(8): 1659-1667. doi: 10.1016/j.apgeochem.2007.03.024 [8] OLGA E. TRUBETSKAYA, OLGA M. SELIVANOVA, VADIM V. Rogachevsky, et al. Transmission electron microscopy of electrophoretic humic acids fractions obtained by coupling size exclusion chromatography-polyacrylamide gel electrophoresis: The next step to understanding structural organization of soil humic matter[J]. Microchemical Journal, 2023, 193: 109177. doi: 10.1016/j.microc.2023.109177 [9] PATRICK BREZONIK, PAUL R. BLOOM, RACHEL L. SLEIGHTER, et al. Chemical differences of aquatic humic substances extracted by XAD-8 and DEAE-cellulose[J]. Journal of Environmental Chemical Engineering, 2015, 3(4): 2982-2990. doi: 10.1016/j.jece.2015.03.004 [10] QIAN F, HE M, WU J, et al. Insight into removal of dissolved organic matter in post pharmaceutical wastewater by coagulation-UV/H2O2[J]. Journal of Environmental Sciences, 2019, 76: 329-338. doi: 10.1016/j.jes.2018.05.025 [11] FENG X, SUN D. Degradation characteristics of refractory organic matter in naproxen pharmaceutical secondary effluent using vacuum ultraviolet-ozone treatment[J]. Journal of Hazardous Materials, 2023, 459: 132056. doi: 10.1016/j.jhazmat.2023.132056 [12] ZHANG J, SONG F, LI T, et al. Simulated photo-degradation of dissolved organic matter in lakes revealed by three-dimensional excitation-emission matrix with regional integration and parallel factor analysis[J]. Journal of Environmental Sciences, 2020, 90: 310-320. doi: 10.1016/j.jes.2019.11.019 [13] 张家胜, 孟凡生, 梁朱明, 等. 七虎林河流域上游溶解性有机质光谱特性分析[J]. 中国环境监测, 2023, 39(1): 137-145. doi: 10.19316/j.issn.1002-6002.2023.01.15 [14] 中华人民共和国国家环境保护总局, 国家环境保护总局科技标准司. 水质 化学需氧量的测定 快速消解分光光度法: HJ/T 399-2007[S]. 北京: 中国环境科学出版社, 2008. [15] 中华人民共和国环境保护部, 环境保护部科技标准司. 水质 总氮的测定 碱性过硫酸钾消解紫外分光光度法: HJ 636-2012[S]. 北京: 中国环境科学出版社, 2012. [16] 中华人民共和国环境保护部, 环境保护部科技标准司. 水质 氨氮的测定 纳氏试剂分光光度法: HJ 535-2009[S]. 北京: 中国环境科学出版社, 2010. [17] HE Q, XIAO Q, FAN J, et al. Excitation-emission matrix fluorescence spectra of chromophoric dissolved organic matter reflected the composition and origination of dissolved organic carbon in Lijiang River, Southwest China[J]. Journal of Hydrology, 2021, 598: 126240. doi: 10.1016/j.jhydrol.2021.126240 [18] ZHOU Q, ZHANG Y, LI K, et al. Seasonal and spatial distributions of euphotic zone and long-term variations in water transparency in a clear oligotrophic Lake Fuxian, China[J]. Journal of Environmental Sciences, 2018, 72: 185-197. doi: 10.1016/j.jes.2018.01.005 [19] LI Y, ZHANG Y, LI Z, et al. Characterization of colored dissolved organic matter in the northeastern South China Sea using EEMs-PARAFAC and absorption spectroscopy[J]. Journal of Sea Research, 2022, 180: 102159. doi: 10.1016/j.seares.2021.102159 [20] XIE L, GUAN W, ZOU L, et al. Composition, variation and contribution of chromophoric dissolved organic matter in Laizhou Bay estuaries, North China[J]. Marine Environmental Research, 2023: 106102. [21] OHNO T. Fluorescence inner-filtering correction for determining the humification index of dissolved organic matter[J]. Environmental Science & Technology, 2002, 36(4): 742-746. [22] HANSEN A M, KRAUS T E C, PELLERIN B A, et al. Optical properties of dissolved organic matter (DOM) : Effects of biological and photolytic degradation[J]. Limnology and Oceanography, 2016, 61(3): 1015-1032. doi: 10.1002/lno.10270 [23] YANG L, CHEN W, ZHUANG W E, et al. Characterization and bioavailability of rainwater dissolved organic matter at the southeast coast of China using absorption spectroscopy and fluorescence EEM-PARAFAC[J]. Estuarine, Coastal and Shelf Science, 2019, 217: 45-55. doi: 10.1016/j.ecss.2018.11.002 [24] PELEATO N M, SIDHU B S, LEGGE R L, et al. Investigation of ozone and peroxone impacts on natural organic matter character and biofiltration performance using fluorescence spectroscopy[J]. Chemosphere, 2017, 172: 225-233. doi: 10.1016/j.chemosphere.2016.12.118 [25] VARDHARAJULA S, ZULFIKAR ALI S, GROVER M, et al. Drought-tolerant plant growth promoting Bacillus spp. : effect on growth, osmolytes, and antioxidant status of maize under drought stress[J]. Journal of Plant Interactions, 2011, 6(1): 1-14. doi: 10.1080/17429145.2010.535178 [26] GAMRANI M, EERT J, WILLIAMS W J, et al. A river of terrestrial dissolved organic matter in the upper waters of the central Arctic Ocean[J]. Deep Sea Research Part I: Oceanographic Research Papers, 2023, 196: 104016. doi: 10.1016/j.dsr.2023.104016 [27] WHEELER K I, LEVIA D F, HUDSON J E. Tracking senescence-induced patterns in leaf litter leachate using parallel factor analysis (PARAFAC) modeling and self-organizing maps[J]. Journal of Geophysical Research: Biogeosciences, 2017, 122(9): 2233-2250. [28] OSBURN C L, HANDSEL L T, MIKAN M P, et al. Fluorescence tracking of dissolved and particulate organic matter quality in a river-dominated estuary[J]. Environmental Science & Technology, 2012, 46(16): 8628-8636. [29] 梁月清, 刘会来, 崔康平, 等. 基于三维荧光光谱-平行因子分析法的工业园区污水溶解性有机物溯源与归趋[J]. 环境工程学报, 2022, 16(4): 1238-1247. doi: 10.12030/j.cjee.202201093 [30] ZHANG R, XIAO R, WANG F, et al. Direct discharge of sewage to natural water through illicitly connected urban stormwater systems: An overlooked source of dissolved organic matter[J]. Science of the Total Environment, 2023, 890: 164248. doi: 10.1016/j.scitotenv.2023.164248 [31] HE H, LUO N, HUANG B, et al. Optical characteristics and cytotoxicity of dissolved organic matter in the effluent and sludge from typical sewage treatment processes[J]. Science of the Total Environment, 2020, 725: 138381. doi: 10.1016/j.scitotenv.2020.138381 [32] 李胜楠, 耿金菊, 李珏纯, 等. 制药废水二级出水中溶解性有机物混凝去除特性研究[J]. 环境科学学报, 2019, 39(10): 3364-3373. doi: 10.13671/j.hjkxxb.2019.0274 [33] 郝晓地, 周鹏, 曹亚莉. 污水处理中腐殖质的来源及其演变过程[J]. 环境工程学报, 2017, 11(1): 1-11. doi: 10.12030/j.cjee.201606072 [34] CHEN B, HUANG W, MA S, et al. Characterization of chromophoric dissolved organic matter in the littoral zones of Eutrophic Lakes Taihu and Hongze during the algal bloom season[J]. Water, 2018, 10(7): 861. doi: 10.3390/w10070861 [35] WEISHAAR J L, AIKEN G R, BERGAMASCHI B A, et al. Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon[J]. Environmental Science & Technology, 2003, 37(20): 4702-4708. [36] KORSHIN G V, BENJAMIN M M, SLETTEN R S. Adsorption of natural organic matter (NOM) on iron oxide: effects on NOM composition and formation of organo-halide compounds during chlorination[J]. Water Research, 1997, 31(7): 1643-1650. doi: 10.1016/S0043-1354(97)00007-9 [37] GAO X X, WANG Y W, AN Y C, et al. Molecular insights into the dissolved organic matter of leather wastewater in leather industrial park wastewater treatment plant[J]. Science of the Total Environment, 2023, 882: 163174. doi: 10.1016/j.scitotenv.2023.163174 [38] KOU Y, JIANG J, YANG B, et al. Transformation of dissolved organic matter at a full-scale petrochemical wastewater treatment plant[J]. Journal of Environmental Management, 2023, 329: 117021. doi: 10.1016/j.jenvman.2022.117021 [39] YU J, HUO R, LIU W, et al. Chemodiversity transformation of organic matters in a full scale MBR-NF wastewater reclamation plant[J]. Science of the Total Environment, 2023, 903: 166246. doi: 10.1016/j.scitotenv.2023.166246 [40] QIU J, LI T, Lü F, et al. Molecular behavior and interactions with microbes during anaerobic degradation of bio-derived DOM in waste leachate[J]. Journal of Environmental Sciences, 2023, 126: 174-183. doi: 10.1016/j.jes.2022.04.015 [41] HU Q, WANG R, ZHANG Y, et al. Formation of halogenated macromolecular organics induced by Br- and I- during plasma oxidation/chlorination of DOM: Highlighting competitive mechanisms[J]. Water Research, 2023, 229: 119513. doi: 10.1016/j.watres.2022.119513 [42] 牛天浩, 周振, 胡大龙, 等. 污水处理厂污泥水溶解性有机物的光谱特性分析[J]. 环境科学, 2016, 37(4): 1460-1466. doi: 10.13227/j.hjkx.2016.04.034 [43] LI C, WU K, CHEN L, et al. Advanced treatment of low-pollution and poor biodegradability sewage by combined process[J]. Journal of Cleaner Production, 2023, 414: 137366. doi: 10.1016/j.jclepro.2023.137366 期刊类型引用(6)
1. 余羿琼,周翠红,冯书耕,张明玉,王梦涵. 外源性物质对消化沼液中DOM光谱特征的影响. 环境工程学报. 2025(02): 364-372 .  本站查看
本站查看
2. 袁尧森,李恩泽,吕宏洲,宋一朋,杨成立,李娟娟. 喷雾干燥法在高盐有机废水中无机盐回收和有机质分解的应用研究. 无机盐工业. 2024(08): 83-91 .  百度学术
百度学术
3. 徐鏊雪,聂明华,晏彩霞,汪王宇,邓思维,丁明军. 基于PARAFAC及SOM的鄱阳湖湿地植物生物炭不同分子量DOM光谱特征分析. 环境科学学报. 2024(08): 393-404 .  百度学术
百度学术
4. 周津羽,李强,章通行,周振超,帅馨怡,林泽俊,陈红. 反渗透膜水处理工艺预处理技术对溶解性有机质去除效果探究. 环境科学学报. 2024(08): 190-197 .  百度学术
百度学术
5. 郭蓉蓉,张永,刘淑刚,薛彦,李志成,陈爽. 臭氧-活性炭深度处理在饮用水厂除嗅的应用. 石油化工应用. 2024(08): 86-91 .  百度学术
百度学术
6. 王宗星,刘昊,闫海虎,符家科,李德鑫,刘承照. 基于紫外-可见吸收光谱的排水管网污染溯源分析. 水上安全. 2024(21): 58-60 .  百度学术
百度学术
其他类型引用(5)
-






 下载:
下载: