-
厨余垃圾是指居民日常生活及食品加工、单位供餐、饮食服务等活动中产生的垃圾[1]。相比其他各类垃圾,厨余垃圾富含蛋白质、淀粉等有机物以及氮、磷、钾等各种营养元素,开发利用价值较大,但也因此易腐烂脏臭,致病菌、蚊虫等容易滋生繁殖[2]。随着城镇化发展和垃圾分类政策的实施,厨余垃圾的精细化、高值化利用成为研究热点。
目前,厨余垃圾资源化处理的主要技术有厌氧消化产能和好氧发酵制肥。其中,厌氧消化和好氧堆肥技术成熟,但处理工艺复杂、处理周期长达30~40 d、运维成本高、产品附加值低,难以实现厨余垃圾的全量资源化。厨余垃圾制备液态有机肥是好氧发酵制肥技术的新突破,它利用微生物、酶的作用,通过微环境调控可以在短时间实现厨余垃圾固相、液相的全降解,并转化为易于作物吸收利用的液态有机肥。利用厨余垃圾制备的液态有机肥富含可溶性糖、游离氨基酸等作物直接吸收利用的小分子物质[3],对作物生长具有良好的调节效果,能够提高作物产量和品质[4-5]。然而厨余垃圾中富含的纤维素、半纤维素、木质素相互缠绕交联,形成难降解的大分子物质,成为制约厨余垃圾快速液化的关键,也限制了腐殖质前体物的生成,使液态有机肥产品肥效差,市场化困难。有研究表明,通过热水解工艺可以打破木质纤维素的结构交联,不同热水解温度下有不同的热水解机制,在较低温度下 (<121 ℃) 胞外聚合物的溶解占主导地位,而在较高温度下 (>121 ℃) 下细胞破裂比例升高,胞内成分得到释放,因此较高的温度有利于大分子有机物的分解和营养物质的释放,同时促进腐殖质的生成。多数研究报告显示,厨余垃圾最佳热水解温度为160~180 ℃,处理时间是30~60 min,此时能产生最高的有机物和营养物质,但温度高于180 ℃可能会产生更多的难降解化合物并降低微生物的降解性能,同时较高的温度还会增加工艺能耗和运行成本。因此,本研究选取低温90 ℃和高温170 ℃的热水解温度进行比较。腐殖质是土壤矿质元素的活化剂和保肥剂,可以降低环境毒性,修复受损土壤,促进植物生长,调节土壤酸碱性[6-7]。ZHU等[8]发现热水解加速了木质纤维素的降解和腐殖质的产生,使堆肥过程中嗜热细菌的相对丰度增加。GAO等[9]通过评价水解前后营养物质的释放和腐殖质的合成,证明了厨余垃圾热水解产生的水解液的肥料潜力。但是在厨余垃圾制备液态有机肥的过程中,存在易降解有机物水解酸化与大分子物质 (蛋白质、淀粉、脂肪等) 降解转化不同步的问题,为此笔者团队前期开展了厨余垃圾降解功能菌剂的筛选与复配,发现抗酸化复合菌剂与米曲霉联用可实现易腐有机物与难降解有机物的同步转化[10-13]。在厨余垃圾高效降解转化的基础上,如何实现厨余垃圾定向腐殖化,提高厨余垃圾液态有机肥的产品附加值,成为研究难点。
近年来,学者们指出腐殖质前体物主要包括多酚、羧酸、氨基酸,多糖和还原糖,前体物的产生与细菌的活动密切相关,微生物通过降解有机物从而释放前体物,随着微生物的生长,它们开始通过次生代谢途径将前体物聚合,如莽草酸和丙二酸途径。最终前体物在酶的作用下聚合或自动形成腐殖质[14-15]。但值得注意的是,这些前体物也是微生物活动的能源,容易在微生物的作用下矿化成CO2,造成前体物的浪费[16]。因此,腐殖质形成和微生物生长繁殖之间存在底物竞争,影响腐殖质形成效率,难以实现厨余垃圾的定向腐殖化[17]。美拉德反应作为氨基酸和还原糖之间缩合的化学反应,这是氨基酸和还原糖合成腐殖质的主要途径,在非生物过程中,可以通过MnO2催化并促进腐殖质的合成,提高腐殖化效率[18]。其机理是,由于MnO2具有氧化性,其可以破坏酚类的物质的苯环结构,释放自由电子,增加反应体系内的活性基团,进而通过酚类和还原糖、氨基酸的缩合形成腐殖质[19]。此外,QI等[20]发现,在富含木质纤维素的材料中MnO2的存在加速了有机组分的降解,同时通过驱动官能团浓度的变化增加了腐殖质浓度,加速有机废弃物向高品质产品的转化。一方面,因为MnO2吸收电子变成Mn2+,这是各种代谢酶最重要的辅助因子之一,因此MnO2可以作为酶启动子刺激酶活性,刺激细菌分解并利用有机物;另一方面,引入 MnO2进入系统也可能改变微生物多样性,因为锰结核内部存在丰富多样的原核生物群落[21]。然而,关于MnO2在大分子有机物质的降解以及催化糖类物质和氨基酸缩合形成腐殖质的研究鲜有报道[17]。
为实现厨余垃圾定向腐殖化制备高品质液态有机肥,本研究在不同热水解温度下研究热水解对厨余垃圾中腐殖质前体物的影响,通过添加自主筛选的抗酸化复合菌剂和米曲霉,开展MnO2强化厨余垃圾快速定向腐殖化的研究;通过解析肥料化过程中腐殖质类、蛋白质类和糖类物质的转化规律,探究MnO2强化厨余垃圾定向腐殖化的作用机制,以期为厨余垃圾全量化和高值化利用提供参考。
-
厨余垃圾原料取自北京某大学食堂,按照菜叶60%、餐厨25%、果皮15%重量比进行配制,将厨余垃圾混合破碎,过20目 (0.850 mm) 筛后置于4 ℃冰箱备用[22]。厨余垃圾的基本理化指标为:含水率86.05%、有机质质量分数为93.75%、pH为5.9、溶解性化学需氧量 (SCOD) 为18 048 mg·L−1、总碳为45.93%、总氮为0.568%。
抗酸化复合菌剂是以餐厨垃圾堆肥酸化抑制期样品为菌源,采用自行设计的、模拟餐厨垃圾堆肥酸化环境的限制性培养基,以迅速降解小分子有机酸 (主要是乙酸、丙酸、丁酸和乳酸) 、提高pH为筛选指标,通过长时间连续继代培养和驯化,获得一组菌群结构稳定的有机酸降解复合菌系。该复合菌系主要由2种假单胞菌、2种芽孢杆菌、1种未培养的Dysgonomonas、1种唾液乳杆菌和1种Aeribacillus pallidus组成。值得注意的是,这7种优势菌群都是细菌。其中,假单胞菌属和芽孢杆菌属都是乙酸和丙酸代谢途径关键酶来源菌株,推测其他3种微生物可能在菌系耐酸性及适应厨余垃圾堆肥环境方面发挥重要作用,这有待于进一步的研究[23]。实验所用米曲霉CGMCC 3.4427购于中国微生物菌种保藏管理委员会普通微生物中心。
-
将平板培养的米曲霉收集至无菌瓶中,稀释后置于4 ℃冰箱保存备用,将1 mL孢子悬浮液接种到50 g餐厨垃圾中,38 ℃下培养48 h,获得富酶产物。
-
厨余垃圾热水解在反应釜内进行,温度控制在3个水平 (0 (CK) 、90和170 ℃) ,处理时间1 h。热水解反应结束后冷却至室温,测定产物的pH、SCOD、总固体(TS)、有机质、总碳、总氮、可溶性蛋白质、游离氨基酸、可溶性糖、还原糖、腐殖酸、富里酸。所有试验组和对照组均在相同条件下设计平行试验。
热水解后去除厨余垃圾表面浮油,随后取热水解后的厨余垃圾250 g,与去离子水按照质量比1∶1混合,分装至4个锥形瓶中,灭菌后接种6%抗酸化复合菌剂,实验组投加0.5% MnO2,48 h后加入6%米曲霉酶源产物,置于磁力搅拌器中,在40 ℃下恒温培养7 d。前3 d每隔12 h取样,后4 d每隔24 h取样测定SCOD、可溶性蛋白质、游离氨基酸、还原糖、可溶性糖、腐殖酸和富里酸指标。
-
有机质采用灼烧法[24]测定;总碳和总氮使用元素分析仪检测;可溶性蛋白浓度采用凯氏定氮法[10]测定;游离氨基酸浓度采用茚三酮比色法测定[25];还原糖采用3,5二硝基水杨酸法 (DNS法) 测定[26];可溶性糖采用蒽酮法测定[27]。
腐殖酸、富里酸提取和测定采用ZHOU等[28]的方法进行:将干燥的样品 (10 g) 与50 mL 0.1 mol·L−1 NaOH+0.1 mol·L−1 Na4P2O7·10 H2O混合溶液按1∶10的比例均匀混合, 将混合物在25 °C摇动持续24 h后,以11 000 r·min−1离心15 min,通过0.45 μm Millipore 膜过滤上清液,所得的澄清液为腐殖质溶液;此后,用6 mol·L−1 HCl将腐殖质溶液的pH调节至1.5,将酸性溶液以11 000 r·min−1离心15 min,上清液为富里酸,沉淀物为腐殖酸。
-
1) 热水解后pH和SCOD变化情况。在不同热水解温度下厨余垃圾理化指标的变化情况如表1所示,经过热水解处理后,含固率下降,这是因为热水解会增强固相中脂肪、碳水化合物、蛋白质的溶解。随着热水解温度的增加有机质质量分数逐渐上升,在90和170 ℃分别增加了0.37%和1.33%。经过热水解后,厨余垃圾的pH明显降低,且温度越高,pH越低,这是因为在热水解过程中有机酸从厨余垃圾中的固相连续释放到液相中。因此,在一定程度上,pH的降低反映了热水解反应的程度。SCOD反映了溶解性有机物的质量分数,90~170 ℃的热水解条件下,部分大分子有机物在热化学作用下发生解聚,细胞发生破裂,从而释放溶解性有机物[28]。很明显,由表1可知,随着加热温度的增加,SCOD 质量分数变化很大,温度越高,SCOD形成速率越快,说明随着热水解温度的提高,体系内有机物质量分数越高。经过热水解后总碳、总氮的质量分数均有上升,在90 ℃时达到最大值,而在170 ℃热水解后总氮的质量分数明显降低,主要有2个方面的原因:首先,热水解期间产生的氨基酸将通过脱氨或脱羧反应进一步降解[29];其次当温度高于160 ℃时,葡萄糖和氨基酸之间可能会发生美拉德反应,产生棕色的含氮杂环和其他含氮聚合物,例如类黑素是葡萄糖和甘氨酸混合物转化产生的棕色产品[30-31]。因此,随着热水解温度升高,总氮质量分数逐渐降低。
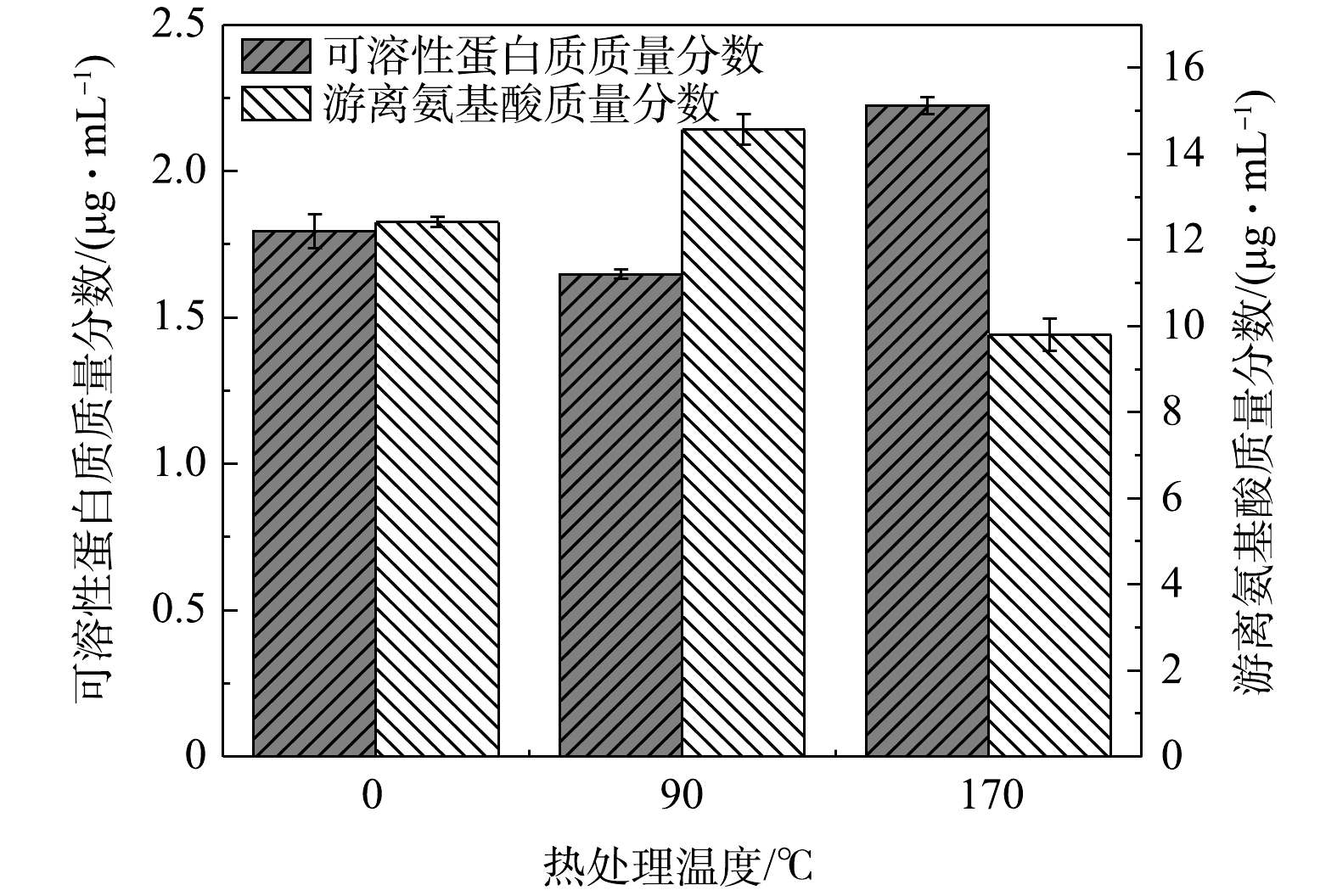
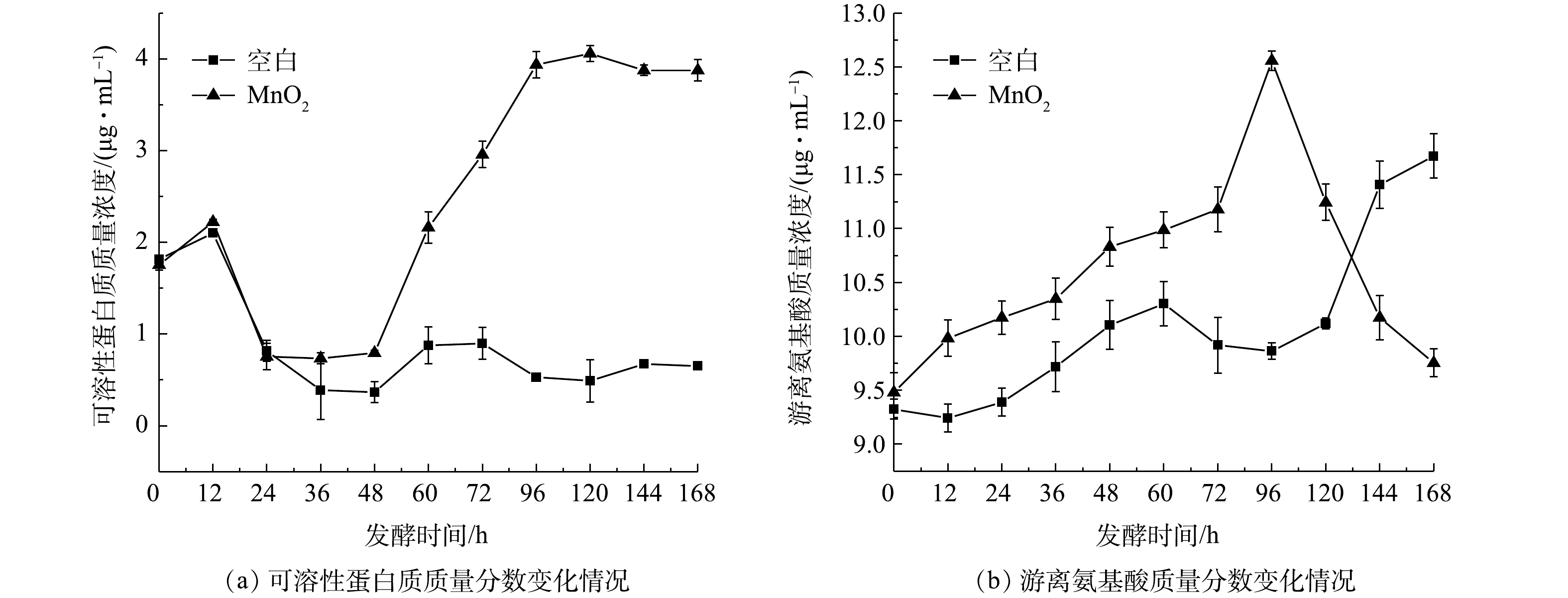
2) 热水解后可溶性蛋白质与游离氨基酸质量分数变化。可溶性蛋白质与游离氨基酸的变化情况如图1所示,随着热水解温度的升高,90 ℃热水解后液相中的蛋白质相较对照组降低了11%,这是因为随着温度的升高,会导致蛋白质变性和凝结,降低蛋白质的比例;而在170 ℃下,液相中的蛋白质质量分数达到最大值,为2.2 ug·mL−1,相较对照组提高了22%。这是因为,随着热水解温度的升高,粗蛋白会进一步水化,并因遇水膨胀而逐渐变成胶体溶液[28]。因此,在170 ℃的温度下固相中的蛋白质会溶解到液相中,从而使液相中的蛋白质质量分数升高。氨基酸的质量分数在90 ℃预处理温度下最高,达到了14.6 ug·mL−1,相较对照组提高了17.7%,这是因为鸡蛋、肉类、豆制品等食品中的蛋白质在热水解过程中也可以转化为氨基酸;而在170 ℃热水解后氨基酸的质量分数明显降低,这与前文提到的总氮质量分数变化情况一致。
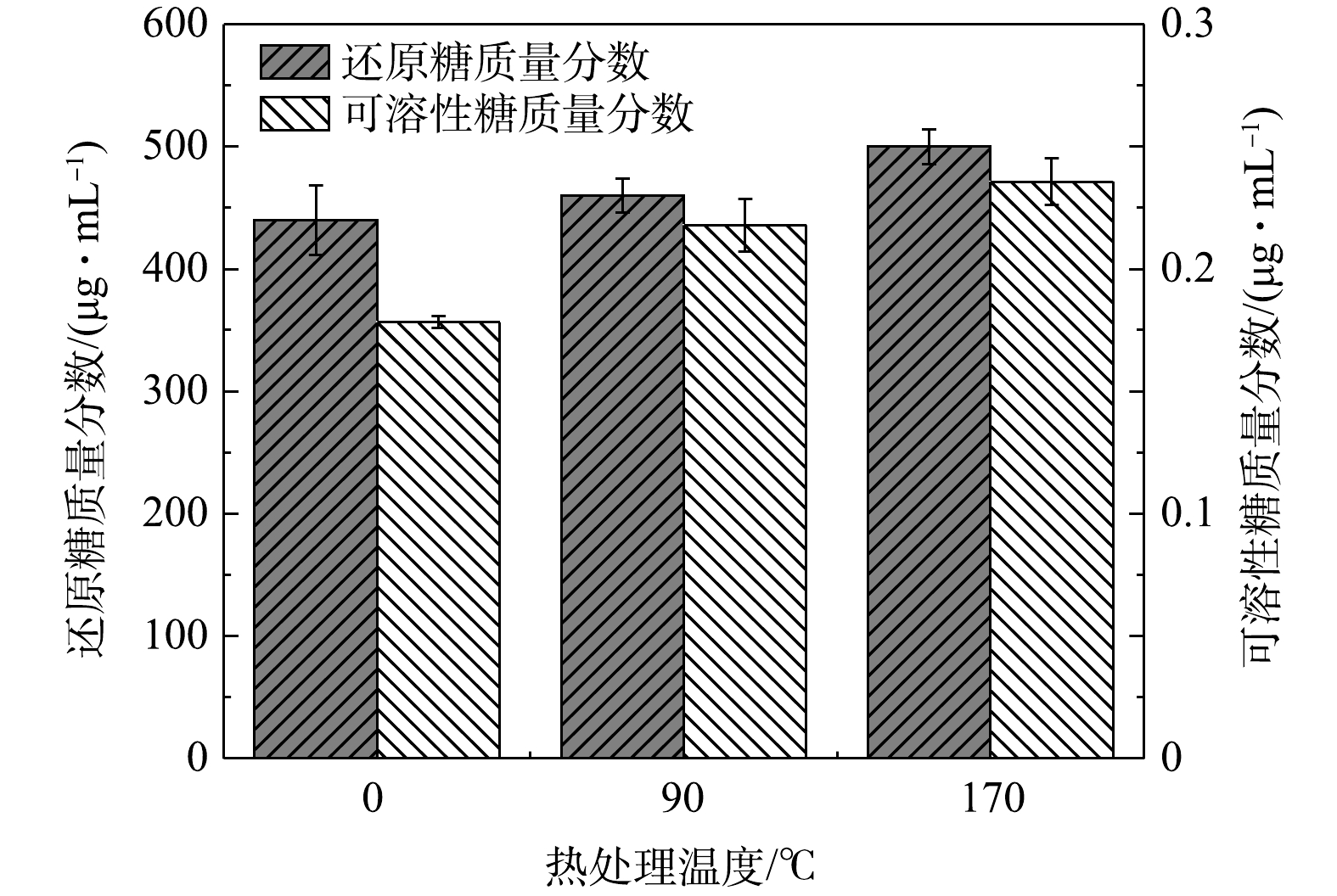
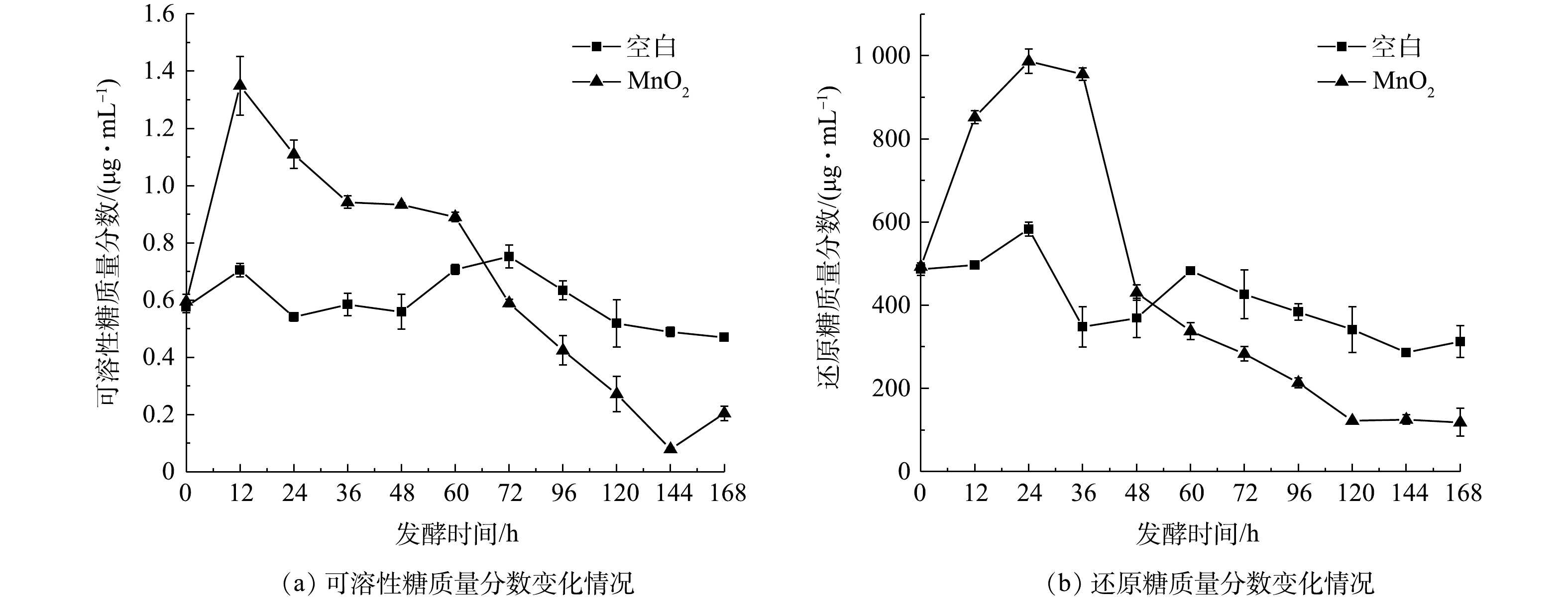
3) 热水解后还原糖和可溶性糖的变化情况。还原糖是指具有还原性的糖类,主要有葡萄糖、果糖、半乳糖、乳糖、麦芽糖等;可溶性糖包括绝大部分的单糖、双糖、多糖。在厨余垃圾热水解的过程中,还原糖和可溶性糖的质量分数变化如图2所示,随着热水解温度的升高,还原糖和可溶性糖的质量分数明显增加,在90和170 ℃热水解后还原糖质量分数分别升高至460、500 ug·mL−1,相较对照组分别提高了5%和12%,可溶性糖的质量分数在170 ℃热水解下达到了最大值为0.24 ug·mL−1,可溶性糖的转化率高达33%。这是由于厨余垃圾中富含碳水化合物,其热解过程中产生大量的可溶性糖,导致固相中可溶性糖的质量分数明显提高。同时,随着热水解温度的提高,加速了固相中碳水化合物的分解,一部分糖类物质向液相中转化,导致液相中的糖类物质明显增加,并且随着热水解的进行,液相中的多糖类物进一步分解为葡萄糖、果糖等可溶性糖,这也就解释了热水解后液相中还原性糖明显增加的原因。
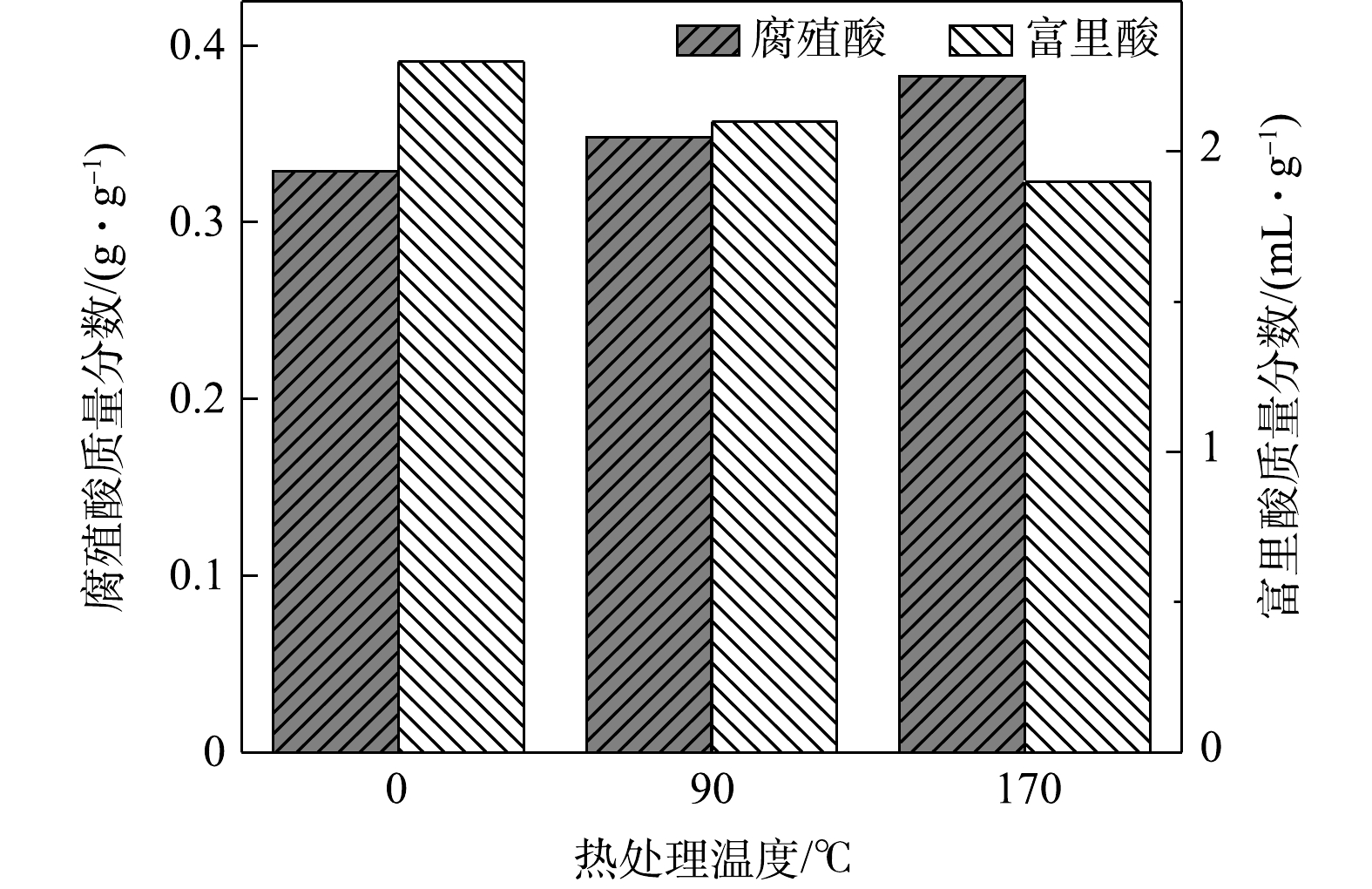
4) 热水解后腐殖酸和富里酸的变化情况。热水解过程中腐殖酸和富里酸的质量分数变化如图3所示,随着热水解温度升高腐殖酸的质量分数有明显的提高,在90、170 ℃下腐殖酸质量分数分别为0.35和0.38 g·g−1,较对照组分别提高了6%和15%。这是因为,当处理温度超过160 ℃时,厨余垃圾颜色变黑,厨余垃圾中的氨基酸和糖类物质发生美拉德反应,产生可以在植物代谢过程中刺激根系生长并促进根系萌生的含氮聚合物腐殖酸[32]。而富里酸的质量分数则呈现相反的趋势,随着热水解温度的升高,富里酸的质量分数逐渐降低,在90、170 ℃热水解下质量分数为2.1和1.9 mL·g−1,较对照组分别降低了8%和17%。这是因为,富里酸的分子量较低,经常转化为更高芳香化的腐殖酸,从而导致腐殖酸质量分数增加而富里酸的质量分数降低[33]。
-
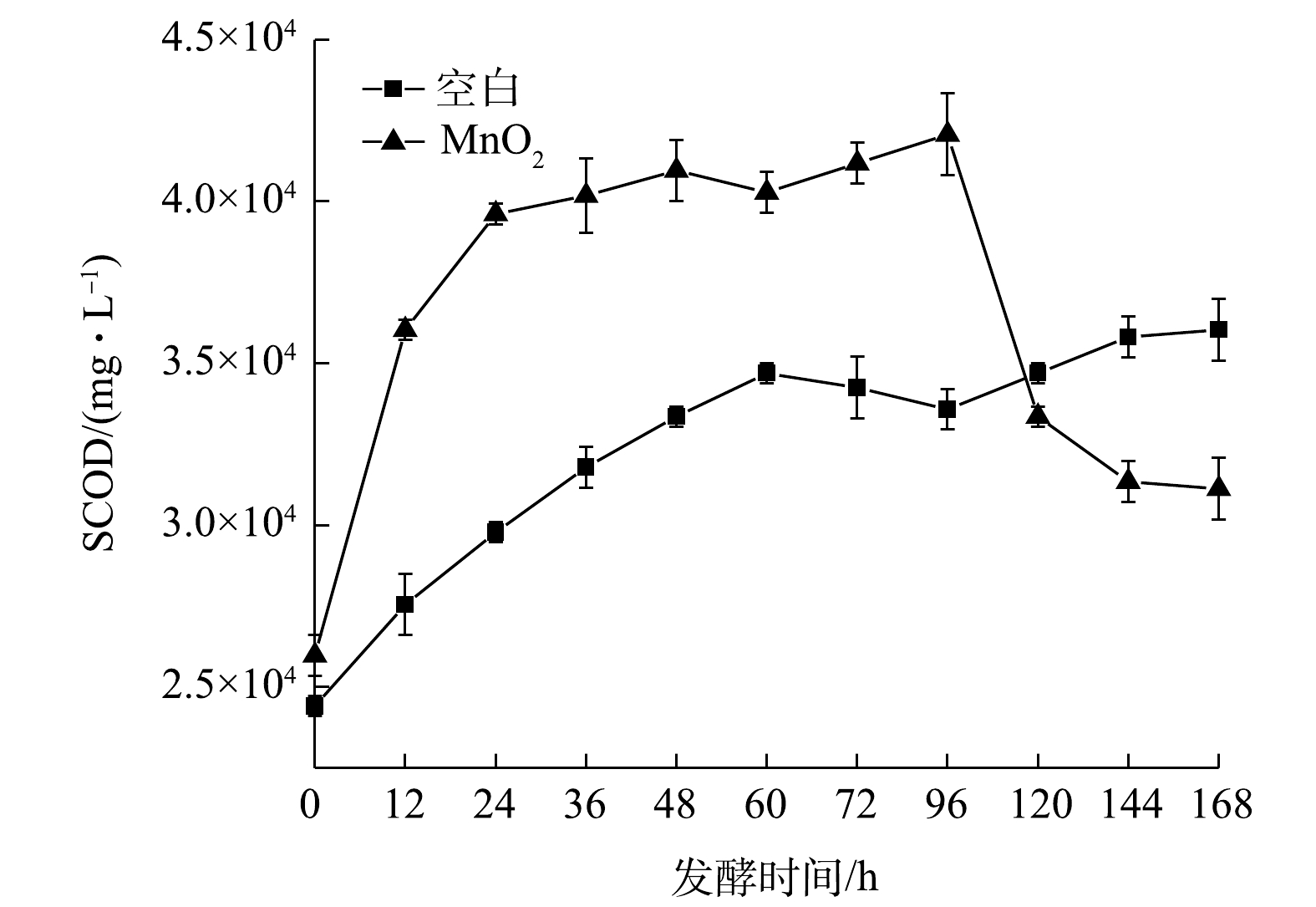
1) 添加MnO2对SCOD的影响。厨余垃圾制备液态有机肥过程中,易降解有机物水解与大分子物质(蛋白质、淀粉、脂肪等)降解转化不同步[13],是限制其高值化的关键限速步骤。SCOD的转化情况可以反映有机物的降解效果。加入MnO2后SCOD的变化情况如图4所示,可以看出加入MnO2后SCOD质量分数明显升高,0~96 h整体呈现上升的趋势,从25 975 mg·L−1上升至最大值42 073 mg·L−1,相较空白组提高了20%,此时大部分大分子有机物降解为小分子可溶性有机物,MnO2的加入可能作为生物活性活化剂刺激细菌的活性,从而导致有机物的剧烈降解[19]。随后,在96~168 h在微生物的作用下SCOD的值持续降低至31 118 mg·L−1,下降了26%,并且低于空白组13.6%。这是因为,此时微生物可以利用小分子的可溶性有机物进行细胞增殖。与对照组相比,加入MnO2后可能促进了微生物对小分子有机物的吸收,从而促进微生物的生长和繁殖[34]。
2) 添加MnO2对可溶性蛋白质和游离氨基酸的影响。厨余垃圾制备液态有机肥过程中可溶性蛋白质变化情况如图5(a)所示,在发酵周期内,空白组和加入MnO2的实验组有明显差异,加入MnO2 48 h后可溶性蛋白的质量分数迅速升高,在96 h达到最大值4.1 ug·mL−1,是空白组的10倍,这可能是因为加入MnO2后增加了蛋白质的在液相中的溶解度,促进了蛋白质的溶解,使厨余垃圾中的蛋白质从固相分解并转移到液相中[35]。
游离氨基酸的质量分数变化情况如图5(b)所示,在0~96 h持续上升,加入MnO2后其质量分数明显高于空白组,在96 h达到最大值12.56 ug·mL−1,相较空白组提高了27.3%。这是因为,加入MnO2后,Mn4+会吸收电子,转化为Mn2+,这是各种代谢酶重要的辅助因子之一[36]。因此,MnO2可以作为酶促剂刺激酶活性,此时功能微生物将厨余垃圾中的蛋白质降解为游离氨基酸,增加了小分子可溶物质的质量分数。在96 h之后,游离氨基酸的质量分数迅速降低,在168 h降至最低9.75 ug·mL−1,降低了22%。这是因为,游离氨基酸是腐殖质形成的重要前体物,其他腐殖质前体物需要与氨基化合物结合才能完成腐殖质的形成[19],因此游离氨基酸质量分数的降低可能是由于其参与形成腐殖质结构所致。
3) 添加MnO2对可溶性糖和还原糖的影响。可溶性糖质量分数的变化情况如图6(a)所示,在发酵期间,加入MnO2实验组和空白组有明显的差异,空白组在发酵周期内可溶性糖的变化不明显,其质量分数均在0.4~0.8 ug·mL−1,而加入MnO2 12 h后由于厨余垃圾中淀粉等大分子有机物的降解转化,导致可溶性糖的质量分数从0.5 ug·mL−1升高到1.4 ug·mL−1,然而随着好氧发酵的进行,可溶性糖的质量分数迅速下降,在168 h内其质量分数降低了93%,这可能是因为,加入MnO2后微生物的活性提高,可溶性糖作为微生物能量供给站不断被微生物利用,一部分为微生物的生长繁殖提供能量,另一部分被降解为还原糖,为美拉德反应提供前体[17]。
还原糖的变化情况如图6(b)所示,发酵周期的前24 h空白组和实验组的还原糖的质量分数由于多糖等大分子有机质的分解迅速上升,均在24 h达到最大值,分别为583和986 ug·mL−1,加入MnO2后质量分数提高了69%,表明加入MnO2后刺激了微生物的活性,从而促进了厨余垃圾中的大分子有机物的降解。而在24 h之后还原糖的质量分数迅速降低,空白组和实验组分别降低至312和118 ug·mL−1,降低了46.4%和88%。这是因为,还原糖作为微生物的直接能源很容易直接被微生物利用矿化成CO2 [37];同时,还原糖还是腐殖质合成重要的前体物质,可以通过美拉德反应形成腐殖质,从而导致还原糖质量分数大幅下降。在反应后期实验组还原糖的质量分数明显低于空白组这是因为Mn4+的存在,会催化糖类物质的脱水、氧化、以及芳香族官能团等活性集团的衍生,从而促进了糖类物质的美拉德反应,最终形成腐殖质。
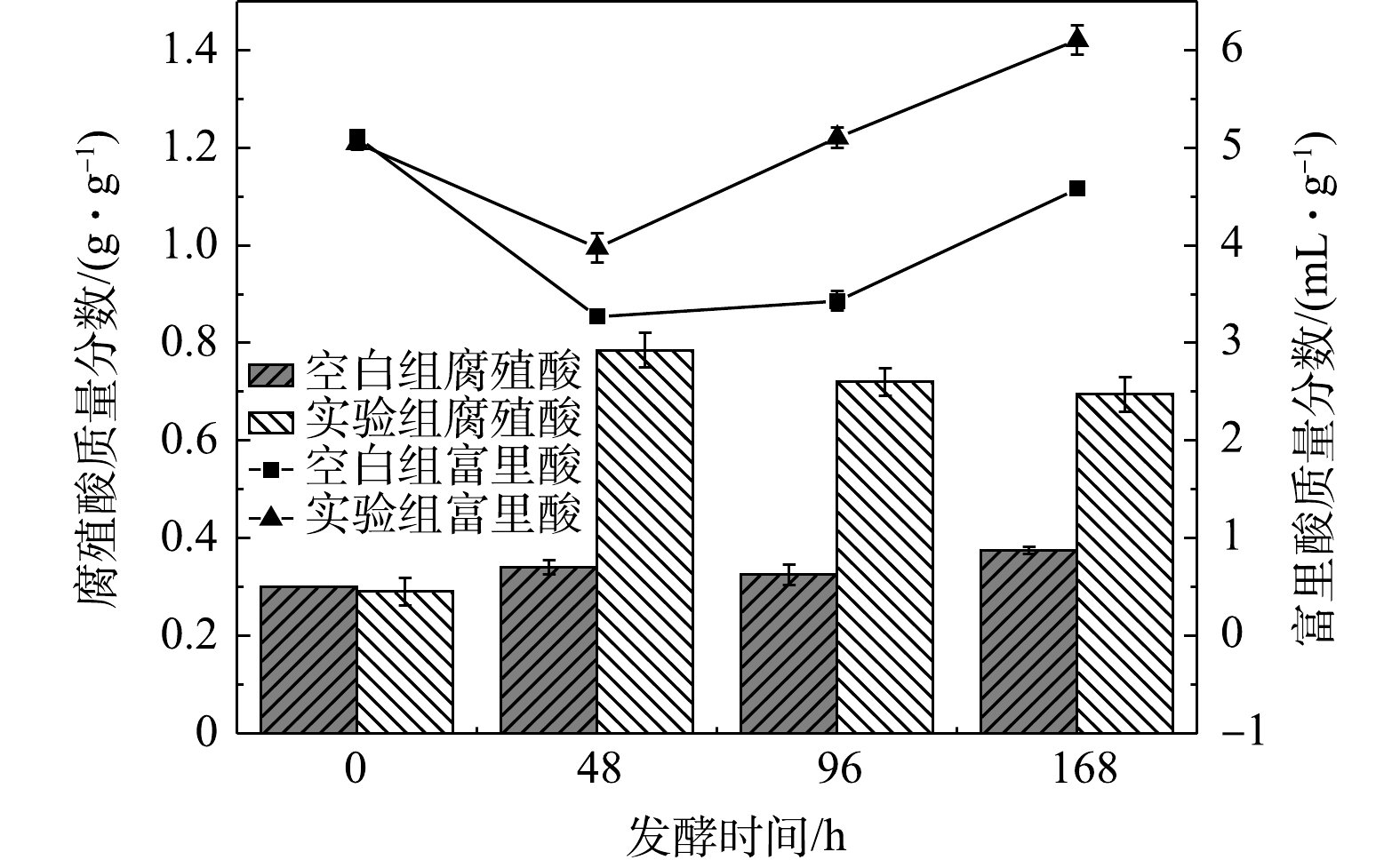
3) 添加MnO2对腐殖酸和富里酸的影响。分别选取0、48、96、168 h4个时间测定厨余垃圾中的腐殖酸和富里酸质量分数,如图7所示,在48 h时空白组和实验组富里酸的质量分数分别从5.08 mL·g−1下降至3.27和3.98 mL·g−1。而空白组和实验组的腐殖酸质量分数均有不同程度的上升,其中空白组的上升并不明显,从0.3 g·g−1上升至0.34 g·g−1,实验组的腐殖酸质量分数却提高1倍从0.3 g·g−1上升至0.79 g·g−1,这可能是因为腐殖酸和富里酸之间相互转化,而加入MnO2促进了两者之间的转化。48 h后,实验组的腐殖酸和富里酸的质量分数明显高于空白组,在168 h腐殖酸的质量分数为0.70 g·g−1,较空白组提高了85%,富里酸的质量分数为6.117 mL·g−1,较空白组提高了33%,这表明MnO2可以明显促进腐殖酸和富里酸的产生。这是因为厨余垃圾中含有丰富的木质纤维素,在发酵过程中降解为碳水化合物,此后,形成的碳水化合物可以通过酸催化水解或脱水反应产生大量的腐殖酸[38]。此外,MnO2作为酶促进剂可以加速木质纤维素等大分子有机质的降解,进而提供了丰富的前体物,例如还原糖、氨基酸、酚类等[20];同时由于MnO2的氧化性,从酚类中吸收电子,增加了美拉德反应中的活性集团,进而通过前体物的缩合促进了腐殖质类物质的产生[21]。
-
1) 最佳的热水解温度为170 ℃,此时可产生最高的有机物和营养物质,其中可溶性蛋白质和还原糖质量分数分别提高了22%和12%,并且经170 ℃热水解后能促进体系内腐殖酸的合成,与热水解前相比腐殖酸的质量分数提高了15%。
2) 在发酵前期 (24 h) 加入MnO2后能明显提高腐殖质合成前体物的质量分数,还原糖质量分数提高了69%,游离氨基酸的质量分数提高了27.3%。
3) 在发酵结束时,还原糖和游离氨基酸的质量分数分别降低了88%和22%,而腐殖酸和富里酸质量分数分别提高了85%和33%。表明MnO2能定向催化氨基酸和还原糖之间的美拉德反应,促进腐殖质的合成。
二氧化锰对厨余垃圾制备液体肥中腐殖质形成的影响
Effect of manganese dioxide on humus formation in liquid fertilizers prepared from food waste
-
摘要: 厨余垃圾全量化制备液态有机肥是其高值资源化利用的重要途径之一。厨余垃圾中腐殖质合成前体物的释放与定向腐殖化是制备高品质液态有机肥的技术难题。通过厨余垃圾热水解 (90和170 ℃) 破坏大分子木质纤维素结构,探究厨余垃圾中蛋白质、氨基酸、可溶性糖等腐殖质合成前体物的转化规律,通过添加二氧化锰 (MnO2) 与功能微生物 (抗酸化复合菌剂和米曲霉酶源产物) 协同定向腐殖化,阐明MnO2强化厨余垃圾定向腐殖化制备液态有机肥的作用机制。结果表明,厨余垃圾在170 ℃热水解1 h效果最佳,液相中可溶性蛋白质和还原糖质量分数与热水解前相比分别提高了22%和12%。添加MnO2后,发酵前期 (24 h) 还原糖质量分数提高了69%,96 h游离氨基酸的质量分数提高了27.3%,进一步提高了厨余垃圾中腐殖质合成前体物的释放。随着腐殖化反应的进行,发酵结束时 (168 h) 还原糖和游离氨基酸的质量分数分别降低了88%和22%,腐殖酸和富里酸质量分数分别提高了85%和33%。可见,热水解联合MnO2催化,可明显促进腐殖质合成前体物的生成和发酵后期的定向腐殖化。该研究结果可为厨余垃圾全量化制备液态有机肥提供参考。Abstract: The preparation of liquid organic fertilizers from food waste in full quantification is one of the most important ways of its high-value resource utilization. The release and directed humification of humus synthetic precursors in food waste is a technical challenge for the preparation of high quality liquid organic fertilizers. In this study, in order to achieve targeted humification of food waste thermal hydrolysis, functional microbial enhancement, and the addition of manganese dioxide (MnO2) catalysis were performed, The thermal hydrolysis under different conditions (90 and 170 ℃) was first performed, and then the anti-acidification compound bacterial agents, enzyme-derived products of Aspergillus oryzae and MnO2 was added. The mechanism of MnO2-enhanced targeted humification of food waste to produce liquid organic fertilizers was investigated. The results showed that food waste was subjected to the targeted humification at 170 ℃. The results showed that the highest efficiency was achieved by thermal hydrolysis of food waste at 170 ℃ for 1 h. The mass of soluble protein and reducing sugar in the liquid phase increased by 22% and 12% than that before thermal hydrolysis, respectively. The addition of MnO2 increased the mass of reducing sugars by 69% at the first stage of fermentation (24 h) and the mass of free amino acids by 27.3% at 96 h. This further enhanced the release of precursors for humus synthesis from food waste. As the humification reaction proceeded, the mass of reducing sugars and free amino acids decreased by 88% and 22% at the end of fermentation (168 h), and the contents of humic and fulvic acids increased by 85% and 33%, respectively. Thermal hydrolysis in combination with MnO2 catalysis significantly promoted the production of precursors for humus synthesis and targeted humification in the later stages of fermentation. This study may provide technical support for the preparation of liquid organic fertiliser from food waste in a fully quantified form.
-
Key words:
- food waste /
- manganese dioxide /
- humification /
- thermal hydrolysis /
- liquid organic fertilizer
-
厨余垃圾是指居民日常生活及食品加工、单位供餐、饮食服务等活动中产生的垃圾[1]。相比其他各类垃圾,厨余垃圾富含蛋白质、淀粉等有机物以及氮、磷、钾等各种营养元素,开发利用价值较大,但也因此易腐烂脏臭,致病菌、蚊虫等容易滋生繁殖[2]。随着城镇化发展和垃圾分类政策的实施,厨余垃圾的精细化、高值化利用成为研究热点。
目前,厨余垃圾资源化处理的主要技术有厌氧消化产能和好氧发酵制肥。其中,厌氧消化和好氧堆肥技术成熟,但处理工艺复杂、处理周期长达30~40 d、运维成本高、产品附加值低,难以实现厨余垃圾的全量资源化。厨余垃圾制备液态有机肥是好氧发酵制肥技术的新突破,它利用微生物、酶的作用,通过微环境调控可以在短时间实现厨余垃圾固相、液相的全降解,并转化为易于作物吸收利用的液态有机肥。利用厨余垃圾制备的液态有机肥富含可溶性糖、游离氨基酸等作物直接吸收利用的小分子物质[3],对作物生长具有良好的调节效果,能够提高作物产量和品质[4-5]。然而厨余垃圾中富含的纤维素、半纤维素、木质素相互缠绕交联,形成难降解的大分子物质,成为制约厨余垃圾快速液化的关键,也限制了腐殖质前体物的生成,使液态有机肥产品肥效差,市场化困难。有研究表明,通过热水解工艺可以打破木质纤维素的结构交联,不同热水解温度下有不同的热水解机制,在较低温度下 (<121 ℃) 胞外聚合物的溶解占主导地位,而在较高温度下 (>121 ℃) 下细胞破裂比例升高,胞内成分得到释放,因此较高的温度有利于大分子有机物的分解和营养物质的释放,同时促进腐殖质的生成。多数研究报告显示,厨余垃圾最佳热水解温度为160~180 ℃,处理时间是30~60 min,此时能产生最高的有机物和营养物质,但温度高于180 ℃可能会产生更多的难降解化合物并降低微生物的降解性能,同时较高的温度还会增加工艺能耗和运行成本。因此,本研究选取低温90 ℃和高温170 ℃的热水解温度进行比较。腐殖质是土壤矿质元素的活化剂和保肥剂,可以降低环境毒性,修复受损土壤,促进植物生长,调节土壤酸碱性[6-7]。ZHU等[8]发现热水解加速了木质纤维素的降解和腐殖质的产生,使堆肥过程中嗜热细菌的相对丰度增加。GAO等[9]通过评价水解前后营养物质的释放和腐殖质的合成,证明了厨余垃圾热水解产生的水解液的肥料潜力。但是在厨余垃圾制备液态有机肥的过程中,存在易降解有机物水解酸化与大分子物质 (蛋白质、淀粉、脂肪等) 降解转化不同步的问题,为此笔者团队前期开展了厨余垃圾降解功能菌剂的筛选与复配,发现抗酸化复合菌剂与米曲霉联用可实现易腐有机物与难降解有机物的同步转化[10-13]。在厨余垃圾高效降解转化的基础上,如何实现厨余垃圾定向腐殖化,提高厨余垃圾液态有机肥的产品附加值,成为研究难点。
近年来,学者们指出腐殖质前体物主要包括多酚、羧酸、氨基酸,多糖和还原糖,前体物的产生与细菌的活动密切相关,微生物通过降解有机物从而释放前体物,随着微生物的生长,它们开始通过次生代谢途径将前体物聚合,如莽草酸和丙二酸途径。最终前体物在酶的作用下聚合或自动形成腐殖质[14-15]。但值得注意的是,这些前体物也是微生物活动的能源,容易在微生物的作用下矿化成CO2,造成前体物的浪费[16]。因此,腐殖质形成和微生物生长繁殖之间存在底物竞争,影响腐殖质形成效率,难以实现厨余垃圾的定向腐殖化[17]。美拉德反应作为氨基酸和还原糖之间缩合的化学反应,这是氨基酸和还原糖合成腐殖质的主要途径,在非生物过程中,可以通过MnO2催化并促进腐殖质的合成,提高腐殖化效率[18]。其机理是,由于MnO2具有氧化性,其可以破坏酚类的物质的苯环结构,释放自由电子,增加反应体系内的活性基团,进而通过酚类和还原糖、氨基酸的缩合形成腐殖质[19]。此外,QI等[20]发现,在富含木质纤维素的材料中MnO2的存在加速了有机组分的降解,同时通过驱动官能团浓度的变化增加了腐殖质浓度,加速有机废弃物向高品质产品的转化。一方面,因为MnO2吸收电子变成Mn2+,这是各种代谢酶最重要的辅助因子之一,因此MnO2可以作为酶启动子刺激酶活性,刺激细菌分解并利用有机物;另一方面,引入 MnO2进入系统也可能改变微生物多样性,因为锰结核内部存在丰富多样的原核生物群落[21]。然而,关于MnO2在大分子有机物质的降解以及催化糖类物质和氨基酸缩合形成腐殖质的研究鲜有报道[17]。
为实现厨余垃圾定向腐殖化制备高品质液态有机肥,本研究在不同热水解温度下研究热水解对厨余垃圾中腐殖质前体物的影响,通过添加自主筛选的抗酸化复合菌剂和米曲霉,开展MnO2强化厨余垃圾快速定向腐殖化的研究;通过解析肥料化过程中腐殖质类、蛋白质类和糖类物质的转化规律,探究MnO2强化厨余垃圾定向腐殖化的作用机制,以期为厨余垃圾全量化和高值化利用提供参考。
1. 材料与方法
1.1 实验原料
厨余垃圾原料取自北京某大学食堂,按照菜叶60%、餐厨25%、果皮15%重量比进行配制,将厨余垃圾混合破碎,过20目 (0.850 mm) 筛后置于4 ℃冰箱备用[22]。厨余垃圾的基本理化指标为:含水率86.05%、有机质质量分数为93.75%、pH为5.9、溶解性化学需氧量 (SCOD) 为18 048 mg·L−1、总碳为45.93%、总氮为0.568%。
抗酸化复合菌剂是以餐厨垃圾堆肥酸化抑制期样品为菌源,采用自行设计的、模拟餐厨垃圾堆肥酸化环境的限制性培养基,以迅速降解小分子有机酸 (主要是乙酸、丙酸、丁酸和乳酸) 、提高pH为筛选指标,通过长时间连续继代培养和驯化,获得一组菌群结构稳定的有机酸降解复合菌系。该复合菌系主要由2种假单胞菌、2种芽孢杆菌、1种未培养的Dysgonomonas、1种唾液乳杆菌和1种Aeribacillus pallidus组成。值得注意的是,这7种优势菌群都是细菌。其中,假单胞菌属和芽孢杆菌属都是乙酸和丙酸代谢途径关键酶来源菌株,推测其他3种微生物可能在菌系耐酸性及适应厨余垃圾堆肥环境方面发挥重要作用,这有待于进一步的研究[23]。实验所用米曲霉CGMCC 3.4427购于中国微生物菌种保藏管理委员会普通微生物中心。
1.2 酶源产物制备
将平板培养的米曲霉收集至无菌瓶中,稀释后置于4 ℃冰箱保存备用,将1 mL孢子悬浮液接种到50 g餐厨垃圾中,38 ℃下培养48 h,获得富酶产物。
1.3 实验设计
厨余垃圾热水解在反应釜内进行,温度控制在3个水平 (0 (CK) 、90和170 ℃) ,处理时间1 h。热水解反应结束后冷却至室温,测定产物的pH、SCOD、总固体(TS)、有机质、总碳、总氮、可溶性蛋白质、游离氨基酸、可溶性糖、还原糖、腐殖酸、富里酸。所有试验组和对照组均在相同条件下设计平行试验。
热水解后去除厨余垃圾表面浮油,随后取热水解后的厨余垃圾250 g,与去离子水按照质量比1∶1混合,分装至4个锥形瓶中,灭菌后接种6%抗酸化复合菌剂,实验组投加0.5% MnO2,48 h后加入6%米曲霉酶源产物,置于磁力搅拌器中,在40 ℃下恒温培养7 d。前3 d每隔12 h取样,后4 d每隔24 h取样测定SCOD、可溶性蛋白质、游离氨基酸、还原糖、可溶性糖、腐殖酸和富里酸指标。
1.4 分析方法
有机质采用灼烧法[24]测定;总碳和总氮使用元素分析仪检测;可溶性蛋白浓度采用凯氏定氮法[10]测定;游离氨基酸浓度采用茚三酮比色法测定[25];还原糖采用3,5二硝基水杨酸法 (DNS法) 测定[26];可溶性糖采用蒽酮法测定[27]。
腐殖酸、富里酸提取和测定采用ZHOU等[28]的方法进行:将干燥的样品 (10 g) 与50 mL 0.1 mol·L−1 NaOH+0.1 mol·L−1 Na4P2O7·10 H2O混合溶液按1∶10的比例均匀混合, 将混合物在25 °C摇动持续24 h后,以11 000 r·min−1离心15 min,通过0.45 μm Millipore 膜过滤上清液,所得的澄清液为腐殖质溶液;此后,用6 mol·L−1 HCl将腐殖质溶液的pH调节至1.5,将酸性溶液以11 000 r·min−1离心15 min,上清液为富里酸,沉淀物为腐殖酸。
2. 结果与讨论
2.1 厨余垃圾热水解条件优化
1) 热水解后pH和SCOD变化情况。在不同热水解温度下厨余垃圾理化指标的变化情况如表1所示,经过热水解处理后,含固率下降,这是因为热水解会增强固相中脂肪、碳水化合物、蛋白质的溶解。随着热水解温度的增加有机质质量分数逐渐上升,在90和170 ℃分别增加了0.37%和1.33%。经过热水解后,厨余垃圾的pH明显降低,且温度越高,pH越低,这是因为在热水解过程中有机酸从厨余垃圾中的固相连续释放到液相中。因此,在一定程度上,pH的降低反映了热水解反应的程度。SCOD反映了溶解性有机物的质量分数,90~170 ℃的热水解条件下,部分大分子有机物在热化学作用下发生解聚,细胞发生破裂,从而释放溶解性有机物[28]。很明显,由表1可知,随着加热温度的增加,SCOD 质量分数变化很大,温度越高,SCOD形成速率越快,说明随着热水解温度的提高,体系内有机物质量分数越高。经过热水解后总碳、总氮的质量分数均有上升,在90 ℃时达到最大值,而在170 ℃热水解后总氮的质量分数明显降低,主要有2个方面的原因:首先,热水解期间产生的氨基酸将通过脱氨或脱羧反应进一步降解[29];其次当温度高于160 ℃时,葡萄糖和氨基酸之间可能会发生美拉德反应,产生棕色的含氮杂环和其他含氮聚合物,例如类黑素是葡萄糖和甘氨酸混合物转化产生的棕色产品[30-31]。因此,随着热水解温度升高,总氮质量分数逐渐降低。
表 1 不同热水解温度下理化指标变化情况Table 1. Changes of physical and chemical indexes under different thermal hydrolysis temperatures处理组 TS/% 含水率/% 有机质/% pH SCOD/(mg·L−1) 总碳/% 总氮/% CK 13.95 86.05 93.75 5.9 18 048 45.93 0.568 90 ℃ 12.75 87.25 94.12 5.5 24 308 46.77 0.614 170 ℃ 11.95 88.05 95.08 5.2 28 780 46.2 0.567 2) 热水解后可溶性蛋白质与游离氨基酸质量分数变化。可溶性蛋白质与游离氨基酸的变化情况如图1所示,随着热水解温度的升高,90 ℃热水解后液相中的蛋白质相较对照组降低了11%,这是因为随着温度的升高,会导致蛋白质变性和凝结,降低蛋白质的比例;而在170 ℃下,液相中的蛋白质质量分数达到最大值,为2.2 ug·mL−1,相较对照组提高了22%。这是因为,随着热水解温度的升高,粗蛋白会进一步水化,并因遇水膨胀而逐渐变成胶体溶液[28]。因此,在170 ℃的温度下固相中的蛋白质会溶解到液相中,从而使液相中的蛋白质质量分数升高。氨基酸的质量分数在90 ℃预处理温度下最高,达到了14.6 ug·mL−1,相较对照组提高了17.7%,这是因为鸡蛋、肉类、豆制品等食品中的蛋白质在热水解过程中也可以转化为氨基酸;而在170 ℃热水解后氨基酸的质量分数明显降低,这与前文提到的总氮质量分数变化情况一致。
3) 热水解后还原糖和可溶性糖的变化情况。还原糖是指具有还原性的糖类,主要有葡萄糖、果糖、半乳糖、乳糖、麦芽糖等;可溶性糖包括绝大部分的单糖、双糖、多糖。在厨余垃圾热水解的过程中,还原糖和可溶性糖的质量分数变化如图2所示,随着热水解温度的升高,还原糖和可溶性糖的质量分数明显增加,在90和170 ℃热水解后还原糖质量分数分别升高至460、500 ug·mL−1,相较对照组分别提高了5%和12%,可溶性糖的质量分数在170 ℃热水解下达到了最大值为0.24 ug·mL−1,可溶性糖的转化率高达33%。这是由于厨余垃圾中富含碳水化合物,其热解过程中产生大量的可溶性糖,导致固相中可溶性糖的质量分数明显提高。同时,随着热水解温度的提高,加速了固相中碳水化合物的分解,一部分糖类物质向液相中转化,导致液相中的糖类物质明显增加,并且随着热水解的进行,液相中的多糖类物进一步分解为葡萄糖、果糖等可溶性糖,这也就解释了热水解后液相中还原性糖明显增加的原因。
4) 热水解后腐殖酸和富里酸的变化情况。热水解过程中腐殖酸和富里酸的质量分数变化如图3所示,随着热水解温度升高腐殖酸的质量分数有明显的提高,在90、170 ℃下腐殖酸质量分数分别为0.35和0.38 g·g−1,较对照组分别提高了6%和15%。这是因为,当处理温度超过160 ℃时,厨余垃圾颜色变黑,厨余垃圾中的氨基酸和糖类物质发生美拉德反应,产生可以在植物代谢过程中刺激根系生长并促进根系萌生的含氮聚合物腐殖酸[32]。而富里酸的质量分数则呈现相反的趋势,随着热水解温度的升高,富里酸的质量分数逐渐降低,在90、170 ℃热水解下质量分数为2.1和1.9 mL·g−1,较对照组分别降低了8%和17%。这是因为,富里酸的分子量较低,经常转化为更高芳香化的腐殖酸,从而导致腐殖酸质量分数增加而富里酸的质量分数降低[33]。
2.2 添加MnO2对厨余垃圾制备液态有机肥的影响
1) 添加MnO2对SCOD的影响。厨余垃圾制备液态有机肥过程中,易降解有机物水解与大分子物质(蛋白质、淀粉、脂肪等)降解转化不同步[13],是限制其高值化的关键限速步骤。SCOD的转化情况可以反映有机物的降解效果。加入MnO2后SCOD的变化情况如图4所示,可以看出加入MnO2后SCOD质量分数明显升高,0~96 h整体呈现上升的趋势,从25 975 mg·L−1上升至最大值42 073 mg·L−1,相较空白组提高了20%,此时大部分大分子有机物降解为小分子可溶性有机物,MnO2的加入可能作为生物活性活化剂刺激细菌的活性,从而导致有机物的剧烈降解[19]。随后,在96~168 h在微生物的作用下SCOD的值持续降低至31 118 mg·L−1,下降了26%,并且低于空白组13.6%。这是因为,此时微生物可以利用小分子的可溶性有机物进行细胞增殖。与对照组相比,加入MnO2后可能促进了微生物对小分子有机物的吸收,从而促进微生物的生长和繁殖[34]。
2) 添加MnO2对可溶性蛋白质和游离氨基酸的影响。厨余垃圾制备液态有机肥过程中可溶性蛋白质变化情况如图5(a)所示,在发酵周期内,空白组和加入MnO2的实验组有明显差异,加入MnO2 48 h后可溶性蛋白的质量分数迅速升高,在96 h达到最大值4.1 ug·mL−1,是空白组的10倍,这可能是因为加入MnO2后增加了蛋白质的在液相中的溶解度,促进了蛋白质的溶解,使厨余垃圾中的蛋白质从固相分解并转移到液相中[35]。
游离氨基酸的质量分数变化情况如图5(b)所示,在0~96 h持续上升,加入MnO2后其质量分数明显高于空白组,在96 h达到最大值12.56 ug·mL−1,相较空白组提高了27.3%。这是因为,加入MnO2后,Mn4+会吸收电子,转化为Mn2+,这是各种代谢酶重要的辅助因子之一[36]。因此,MnO2可以作为酶促剂刺激酶活性,此时功能微生物将厨余垃圾中的蛋白质降解为游离氨基酸,增加了小分子可溶物质的质量分数。在96 h之后,游离氨基酸的质量分数迅速降低,在168 h降至最低9.75 ug·mL−1,降低了22%。这是因为,游离氨基酸是腐殖质形成的重要前体物,其他腐殖质前体物需要与氨基化合物结合才能完成腐殖质的形成[19],因此游离氨基酸质量分数的降低可能是由于其参与形成腐殖质结构所致。
3) 添加MnO2对可溶性糖和还原糖的影响。可溶性糖质量分数的变化情况如图6(a)所示,在发酵期间,加入MnO2实验组和空白组有明显的差异,空白组在发酵周期内可溶性糖的变化不明显,其质量分数均在0.4~0.8 ug·mL−1,而加入MnO2 12 h后由于厨余垃圾中淀粉等大分子有机物的降解转化,导致可溶性糖的质量分数从0.5 ug·mL−1升高到1.4 ug·mL−1,然而随着好氧发酵的进行,可溶性糖的质量分数迅速下降,在168 h内其质量分数降低了93%,这可能是因为,加入MnO2后微生物的活性提高,可溶性糖作为微生物能量供给站不断被微生物利用,一部分为微生物的生长繁殖提供能量,另一部分被降解为还原糖,为美拉德反应提供前体[17]。
还原糖的变化情况如图6(b)所示,发酵周期的前24 h空白组和实验组的还原糖的质量分数由于多糖等大分子有机质的分解迅速上升,均在24 h达到最大值,分别为583和986 ug·mL−1,加入MnO2后质量分数提高了69%,表明加入MnO2后刺激了微生物的活性,从而促进了厨余垃圾中的大分子有机物的降解。而在24 h之后还原糖的质量分数迅速降低,空白组和实验组分别降低至312和118 ug·mL−1,降低了46.4%和88%。这是因为,还原糖作为微生物的直接能源很容易直接被微生物利用矿化成CO2 [37];同时,还原糖还是腐殖质合成重要的前体物质,可以通过美拉德反应形成腐殖质,从而导致还原糖质量分数大幅下降。在反应后期实验组还原糖的质量分数明显低于空白组这是因为Mn4+的存在,会催化糖类物质的脱水、氧化、以及芳香族官能团等活性集团的衍生,从而促进了糖类物质的美拉德反应,最终形成腐殖质。
3) 添加MnO2对腐殖酸和富里酸的影响。分别选取0、48、96、168 h4个时间测定厨余垃圾中的腐殖酸和富里酸质量分数,如图7所示,在48 h时空白组和实验组富里酸的质量分数分别从5.08 mL·g−1下降至3.27和3.98 mL·g−1。而空白组和实验组的腐殖酸质量分数均有不同程度的上升,其中空白组的上升并不明显,从0.3 g·g−1上升至0.34 g·g−1,实验组的腐殖酸质量分数却提高1倍从0.3 g·g−1上升至0.79 g·g−1,这可能是因为腐殖酸和富里酸之间相互转化,而加入MnO2促进了两者之间的转化。48 h后,实验组的腐殖酸和富里酸的质量分数明显高于空白组,在168 h腐殖酸的质量分数为0.70 g·g−1,较空白组提高了85%,富里酸的质量分数为6.117 mL·g−1,较空白组提高了33%,这表明MnO2可以明显促进腐殖酸和富里酸的产生。这是因为厨余垃圾中含有丰富的木质纤维素,在发酵过程中降解为碳水化合物,此后,形成的碳水化合物可以通过酸催化水解或脱水反应产生大量的腐殖酸[38]。此外,MnO2作为酶促进剂可以加速木质纤维素等大分子有机质的降解,进而提供了丰富的前体物,例如还原糖、氨基酸、酚类等[20];同时由于MnO2的氧化性,从酚类中吸收电子,增加了美拉德反应中的活性集团,进而通过前体物的缩合促进了腐殖质类物质的产生[21]。
3. 结论
1) 最佳的热水解温度为170 ℃,此时可产生最高的有机物和营养物质,其中可溶性蛋白质和还原糖质量分数分别提高了22%和12%,并且经170 ℃热水解后能促进体系内腐殖酸的合成,与热水解前相比腐殖酸的质量分数提高了15%。
2) 在发酵前期 (24 h) 加入MnO2后能明显提高腐殖质合成前体物的质量分数,还原糖质量分数提高了69%,游离氨基酸的质量分数提高了27.3%。
3) 在发酵结束时,还原糖和游离氨基酸的质量分数分别降低了88%和22%,而腐殖酸和富里酸质量分数分别提高了85%和33%。表明MnO2能定向催化氨基酸和还原糖之间的美拉德反应,促进腐殖质的合成。
-
表 1 不同热水解温度下理化指标变化情况
Table 1. Changes of physical and chemical indexes under different thermal hydrolysis temperatures
处理组 TS/% 含水率/% 有机质/% pH SCOD/(mg·L−1) 总碳/% 总氮/% CK 13.95 86.05 93.75 5.9 18 048 45.93 0.568 90 ℃ 12.75 87.25 94.12 5.5 24 308 46.77 0.614 170 ℃ 11.95 88.05 95.08 5.2 28 780 46.2 0.567 -
[1] 靳晨曦, 孙士强, 盛维杰, 等. 中国厨余垃圾处理技术及资源化方案选择[J]. 中国环境科学, 2022, 42(3): 1240-1251. doi: 10.3969/j.issn.1000-6923.2022.03.029 [2] 邓俊. 餐厨垃圾无害化处理与资源化利用现状及发展趋势[J]. 环境工程技术学报, 2019, 9(6): 637-642. doi: 10.12153/j.issn.1674-991X.2019.05.300 [3] 汪家春, 陈雅琳, 杨睿倩. 冬虫夏草口服液游离氨基酸和微量元素的分析比较[J]. 生物技术通讯, 2013, 24(3): 393-397. doi: 10.3969/j.issn.1009-0002.2013.03.023 [4] 刘晓佩, 李鸣晓, 戴昕, 等. 不同菌剂制备餐厨垃圾液态有机肥过程物质转化规律研究[J]. 环境工程技术学报, 2021, 11(4): 750-755. doi: 10.12153/j.issn.1674-991X.20200229 [5] 熊湖, 郑顺林, 龚静, 等. 液态有机肥对酚酸胁迫下马铃薯生长发育和土壤酶活性影响[J]. 水土保持学报, 2019, 33(3): 254-259. [6] YANG Y N, LI H. Recovering humic substances from the dewatering effluent of thermally treated sludge and its performance as an organic fertilizer[J]. Frontiers of Environmental Science & Engineering, 2016, 10(3): 578-584. [7] PAN C N, ZHAO Y, ZHAO L, et al. Modified montmorillonite and illite adjusted the preference of biotic and abiotic pathways of humus formation during chicken manure composting[J]. Bioresource Technology, 2021, 319: 1-10. [8] ZHU N, GAO J, LIANG D, et al. Thermal pretreatment enhances the degradation and humification of lignocellulose by stimulating thermophilic bacteria during dairy manure composting[J]. Bioresource Technology, 2021, 319: 1-9. [9] GAO S, LU D, QIAN T, et al. Thermal hydrolyzed food waste liquor as liquid organic fertilizer[J]. Science of the Total Environment, 2021, 775: 1-9. [10] 贾璇, 李雪琪, 刘晓佩, 等. 米曲霉协同抗酸化菌剂制备餐厨垃圾氨基酸液态肥[J]. 环境科学研究, 2022, 35(7): 1707-1714. doi: 10.13198/j.issn.1001-6929.2022.03.05 [11] SONG C H, LI M X, JIA X, et al. Comparison of bacterial community structure and dynamics during the thermophilic composting of different types of solid wastes: anaerobic digestion residue, pig manure and chicken manure[J]. Microbial Biotechnology, 2014, 7(5): 424-433. doi: 10.1111/1751-7915.12131 [12] SONG C H, LI M X, WEI Z M, et al. Effect of inoculation with multiple composite microorganisms on characteristics of humic fractions and bacterial community structure during biogas residue and livestock manure co-composting[J]. Journal of Chemical Technology and Biotechnology, 2016, 91(1): 155-164. doi: 10.1002/jctb.4554 [13] LIN J, ZUO J E, GAN L L, et al. Effects of mixture ratio on anaerobic co-digestion with fruit and vegetable waste and food waste of China[J]. Journal of Environmental Sciences, 2011, 23(8): 1403-1408. doi: 10.1016/S1001-0742(10)60572-4 [14] WU J, ZHAO Y, QI H, et al. Identifying the key factors that affect the formation of humic substance during different materials composting[J]. Bioresource Technology, 2017, 244: 1193-1196. doi: 10.1016/j.biortech.2017.08.100 [15] WU J, ZHAO Y, ZHAO W, et al. Effect of precursors combined with bacteria communities on the formation of humic substances during different materials composting[J]. Bioresource Technology, 2017, 226: 191-199. doi: 10.1016/j.biortech.2016.12.031 [16] WEI Y Q, ZHAO Y, ZHAO X Y, et al. Roles of different humin and heavy-metal resistant bacteria from composting on heavy metal removal[J]. Bioresource Technology, 2020, 296: 1-37. [17] WU J, ZHAO Y, WANG F, et al. Identifying the action ways of function materials in catalyzing organic waste transformation into humus during chicken manure composting[J]. Bioresource Technology, 2020, 303: 1-10. [18] 依胜男, 芦晶, 逄晓阳, 等. 热处理对牛乳美拉德反应程度及挥发性成分的影响[J]. 食品科学, 2021, 42(14): 9-15. doi: 10.7506/spkx1002-6630-20200622-295 [19] WU J, QI H, HUANG X, et al. How does manganese dioxide affect humus formation during bio-composting of chicken manure and corn straw?[J]. Bioresource Technology, 2018, 269: 169-178. doi: 10.1016/j.biortech.2018.08.079 [20] QI H, ZHAO Y, ZHAO X, et al. Effect of manganese dioxide on the formation of humin during different agricultural organic wastes compostable environments: It is meaningful carbon sequestration[J]. Bioresource Technology, 2020, 299: 1-8. [21] HARDIE A G, DYNES J J, KOZAK L M, et al. The role of glucose in abiotic humification pathways as catalyzed by birnessite[J]. Journal of Molecular Catalysis A:Chemical, 2009, 308(1): 114-126. [22] JIA X, XI B, LI M, et al. Metaproteomic analysis of the relationship between microbial community phylogeny, function and metabolic activity during biohydrogen-methane coproduction under short-term hydrothermal pretreatment from food waste[J]. Bioresource Technology, 2017, 245(Pt A): 1030-1039. [23] SONG C, LI M, QI H, et al. Impact of anti-acidification microbial consortium on carbohydrate metabolism of key microbes during food waste composting[J]. Bioresource Technology, 2018, 259: 1-9. doi: 10.1016/j.biortech.2018.03.022 [24] GILCREAS F W. Future of standard methods for the examination of water and wastewater[J]. Health laboratory science, 1967, 4(3): 137-141. [25] LIE S, EUROPEAN BREWERY CONVENTION A C. The EBC-ninhydrin method for determination of free alpha amino nitrogen[J]. Journal of the Institute of Brewing, 1973, 79(1): 37-41. doi: 10.1002/j.2050-0416.1973.tb03495.x [26] 王欢, 卢红梅, 张义明, 等. 固态发酵食醋中还原糖、总糖浓度测定[J]. 中国酿造, 2011(9): 172-175. doi: 10.3969/j.issn.0254-5071.2011.09.048 [27] 张述伟, 宗营杰, 方春燕, 等. 蒽酮比色法快速测定大麦叶片中可溶性糖浓度的优化[J]. 食品研究与开发, 2020, 41(7): 196-200. doi: 10.12161/j.issn.1005-6521.2020.07.033 [28] ZHOU Y, SELVAM A, WONG J W. Evaluation of humic substances during co-composting of food waste, sawdust and Chinese medicinal herbal residues[J]. Bioresource Technology, 2014, 168: 229-234. doi: 10.1016/j.biortech.2014.05.070 [29] JIN Y, LI Y, LI J. Influence of thermal pretreatment on physical and chemical properties of kitchen waste and the efficiency of anaerobic digestion[J]. Journal of Environmental Management, 2016, 180: 291-300. doi: 10.1016/j.jenvman.2016.05.047 [30] PAVLOVIC I, KNEZ Z, SKERGET M. Hydrothermal reactions of agricultural a nd food processing wastes in sub- and supercritical water: a review of fundamentals, mechanisms, and state of research[J]. Journal of Agricultural and Food Chemistry, 2013, 61(34): 8003-8025. doi: 10.1021/jf401008a [31] DWYER J, STARRENBURG D, TAIT S, et al. Decreasing activated sludge thermal hydrolysis temperature reduces product colour, without decreasing degradability[J]. Water Research, 2008, 42(18): 4699-4709. doi: 10.1016/j.watres.2008.08.019 [32] PETERSON A A, LACHANCE R P, TESTER J W. Kinetic Evidence of the Maillard Reaction in Hydrothermal Biomass Processing: Glucose−Glycine Interactions in High-Temperature, High-Pressure Water[J]. Industrial & Engineering Chemistry Research, 2010, 49(5): 2107-2117. [33] ATIYEH R M, LEE S, EDWARDS C A, et al. The influence of humic acids derived from earthworm-processed organic wastes on plant growth[J]. Bioresource Technology, 2002, 84(1): 7-14. doi: 10.1016/S0960-8524(02)00017-2 [34] 刘厶瑶, 李玉双, 侯永侠, 等. 富里酸对土壤中DnBP的降解及微生物活性的影响[J]. 农业环境科学学报, 2020, 39(2): 313-320. doi: 10.11654/jaes.2019-0887 [35] 咸芳. 餐厨垃圾高效处理复合微生物菌剂的研究[D]. 吉林: 吉林大学, 2009. [36] ZHAO M X, YAN Q, RUAN W Q, et al. Enhancement of substrate solubilization and hydrogen production from kitchen wastes by pH pretreatment[J]. Environmental Technology, 2011, 32(2): 119-125. doi: 10.1080/09593330.2010.482596 [37] EWERT J, GLüCK C, STRASDEIT H, et al. Influence of the metal ion on the enzyme activity and kinetics of PepA from Lactobacillus delbrueckii[J]. Enzyme and Microbial Technology, 2018, 110: 69-78. doi: 10.1016/j.enzmictec.2017.10.002 [38] WEI Y, ZHAO Y, ZHAO X, et al. Roles of different humin and heavy-metal resistant bacteria from composting on heavy metal removal[J]. Bioresource Technology, 2020, 296: 1-37. 期刊类型引用(2)
1. 张雷,Zakia Manzoor,汪魏,王雨,刘凯月,Fahim Ullah,徐佰青. 矿物催化氧化聚合绿色合成腐殖酸. 当代化工. 2025(01): 1-8 .  百度学术
百度学术
2. 王辉辉,王雪梅,李子富,靳晓辉,胡亚伟. 高固体条件下黑水添加对厨余垃圾厌氧发酵的影响. 环境工程学报. 2024(01): 237-244 .  本站查看
本站查看
其他类型引用(1)
-






 DownLoad:
DownLoad: