-
近年来,随着新能源产业的迅速发展,锂电池的产量大幅度增加,废旧锂电池也随之大量产生[1]。在锂电池湿法回收过程中,通常采用黄铁矾法实现其中铁元素的脱除,进而产生铁矾渣固体废弃物[2]。铁矾渣主要成分黄钠铁矾 (NaFe3(SO4)2(OH)6) 是一种硫酸盐复盐,通常含有少量的镍钴锰等重金属元素,直接填埋潜在环境风险较大。利用铁矾渣为原料烧制陶粒产品是一种可以固定重金属元素,实现资源化利用的有效途径。但由于其含硫较高,高温过程易分解产生SO2,存在着后续环境处理成本较高的问题[3-6]。
目前,高温固硫的研究主要集中在高温反应中固硫和烟气脱硫[7-9]方面。在高温反应中,固硫是在高温烧结前采取措施减少高温过程含硫物质的分解[10],主要技术手段是在高温过程前或者高温过程中添加一定量的固硫剂,使高温时产生的气态硫化物与固硫剂中的有效成分 (CaO、MgO等) 发生反应,使其转变成硫酸盐等形式留在渣中,进而有效减少SO2和SO3的释放,从而达到固硫的效果。其反应温度一般控制在800~1 250 ℃,常用固硫剂有钙基固硫剂、钠基固硫剂和镁基固硫剂[11-13]。烟气脱硫是利用固相吸收剂、水或碱性溶液与含硫烟气充分接触,生成对应的硫酸盐等化合物,从而减少烟气中SO2的排放,目前此方法存在脱硫设备易腐蚀且副产石膏量大[14-17]的问题。陶粒通常在900~1 300 ℃烧制形成[18],然而黄钠铁矾在高温过程中易分解产生SO2,如式(1)所示[19],该过程会提高后端脱硫处理成本。因此,通过研究在陶粒的烧制过程中添加固硫剂降低生产过程中SO2的排放可有效减小后续脱硫设备规模,以降低生产成本。
通过对不同的固硫剂在高温下可能的反应进行热力学模拟,筛选出高温过程对铁矾渣可能存在固硫效果的Ca/Na/Mg基固硫剂,并利用铁矾渣-固硫剂混合焙烧的实验方式验证固硫剂在1 100 ℃条件下焙烧对铁矾渣的固硫效果,以筛选出固硫效果较佳的固硫剂,从而进一步验证固硫剂掺量对陶粒密度、吸水率和抗压强度的影响。同时,通过XRD和TG-FTIR分析,明确不同烧成反应物的矿相、反应热力学和气相产物的变化,从而明确固硫机理。对固硫陶粒进行了毒性浸出分析,检验其环境安全性。
-
本研究制备陶粒的主要原料包括页岩、铁矾渣和含碳化硅废料分别来自湖南某锂电回收企业和陶瓷企业;固硫剂筛选考察实验分别采用碳酸钙 (CaCO3、氧化钙 (CaO) 、氢氧化钙 (Ca(OH)2) 、硅酸钙 (CaSiO3) 、碳酸钠 (Na2CO3) 、碳酸氢钠 (NaHCO3) 、氢氧化钠 (NaOH) 、硅酸钠 (Na2SiO3) 、偏铝酸钠 (NaAlO2) 、氧化镁 (MgO) 和氢氧化镁 (Mg(OH)2) ,均为分析纯。
主要使用的设备及分析仪器:X 射线衍射仪 (Smartlab,日本株式会社理学公司);X射线荧光光谱仪(AXIOS,荷兰帕纳科公司);烧结炉 (佛山市科顺龙电控有限公司);万能试验机 (E100,济南试金集团有限公司);热重红外联用 (TENSOR III,德国布鲁克公司;STA449 F5,德国耐驰公司)。
-
1) 固硫率的计算方法。固硫率采用硫质量守恒的算法,根据XRF测定焙烧前样品硫的质量分数,称取一定质量的样品,将称取质量的样品进行焙烧后再次称重,并对焙烧后的样品测定硫的质量分数具体计算如式 (2)~式 (3)所示。
式中:Xn为硫残留率;X*为固硫率;XT为未添加固硫剂的样品硫残留率;xn为烧制样品含硫质量分数;mn为烧制样品质量,g;xns为未烧样品含硫质量分数;mns为未烧样品质量,g。
2) 混合焙烧实验。称取一定量的铁矾渣,经过对铁矾渣硫含量的计算,分别按照摩尔比Ca/S=2.35、Na/S=2.35和Mg/S=2.35称取相应物质的质量,将称取的各物质利用球磨机充分混合5 min后称重,计算出混合物体系含硫质量分数,取一定量混合物在1 100 ℃的条件下灼烧30 min后再次称重,根据式 (2)~式 (3)计算固硫率,最终固硫率取3次稳定实验结果的平均值。
3) 陶粒配方及制备方法。将页岩、铁矾渣和碳化硅废料原料在 (105±2) ℃烘干至恒重,经破碎和球磨机球磨30 min后过100目 (150 μm) 标准筛,按照页岩和铁矾渣的质量分数为92.5%和7.5%,在页岩和铁矾渣总质量基础上掺加0.8%含碳化硅废料,利用球磨机混合5 min后加入适量水,利用成球设备制备生料球。将滚好的生料球在 (105±2) ℃烘干至恒重后,在500 ℃下预热30 min得到陶粒熟料,预热好的陶粒熟料直接放入1 100 ℃的电炉中烧制一定时间后取出冷却。
4) 陶粒物理性能测试方法。抗压强度采取一种已经报道的方法[20],将陶粒样品垂直放置于压力机承压板之间,以一定升压速度施加载荷,压至破坏时得到破坏荷载Pc,每组样品测试10颗陶粒,取其平均值,得到陶粒的强度S。测试方法原理如式(4)所示。
式中:S为陶粒的单颗粒强度,MPa;Pc为陶粒破坏时的荷载,N;X为陶粒在起始受力时与压力机承压板接触点间的垂直距离,mm。
陶粒的表观密度和吸水率按照《轻集料及其试验方法》[21]测定。
-
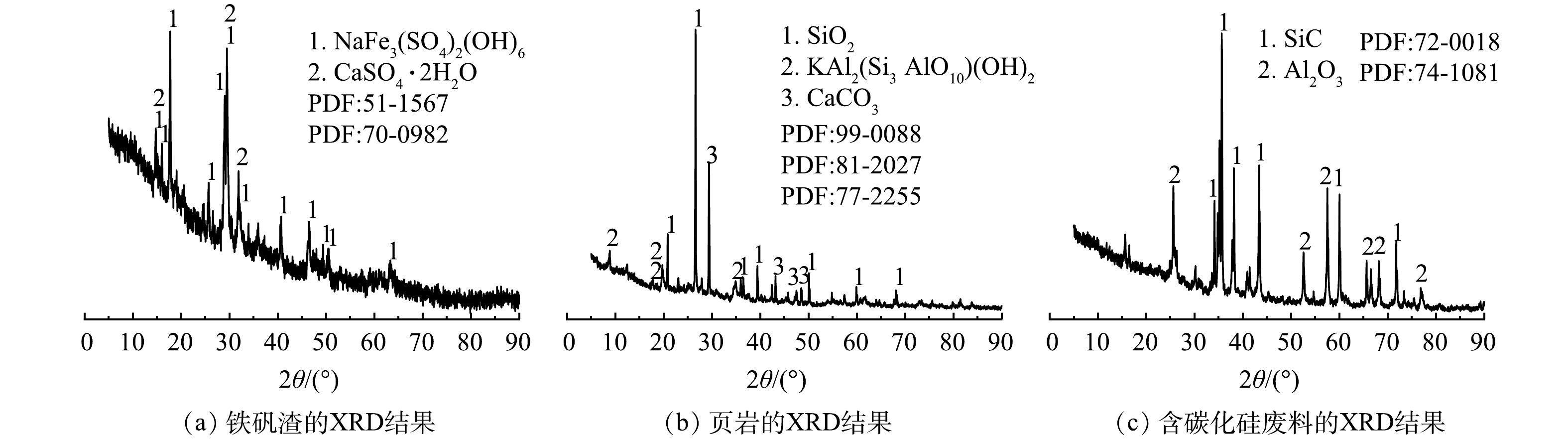
将烘干至恒重的原料进行XRD和XRF测试。所使用的原料主要化学成分如表1所示,由表可知,铁矾渣中硫、铁、铝和钠含量较高,其中同时含有镍、钴、锰和铜等金属元素,烧失率为22.60%;页岩富含铝、硅、钙等元素,其中SiO2、Al2O3和CaO的质量分数分别为53.79%、18.04%和11.93%,烧失率为14.60%;陶粒成孔剂采用含有碳化硅成分的电子陶瓷行业研磨抛光产生的废料,其中Al2O3和SiC的质量分数分别为49.41%和43.34%,烧失率为2.80%。由图1可知,铁矾渣主要矿相为黄钠铁矾 (NaFe3(SO4)2(OH)6) 和CaSO4·2H2O,根据铁矾渣产生过程推测含铝物相为无定型的氢氧化铝;页岩的主要矿相成分是白云母石,石英和方解石;含碳化硅废料的主要矿相是碳化硅和氧化铝。
-
常用固硫剂有很多种,碱金属固硫剂是其中最重要的一类,其中钙基应用最为广泛[7, 22-25],部分研究人员利用富含碱金属氧化物的固废作为固硫剂对反应产生二氧化硫进行固定[9, 26],结合文献和理论分析,通过对钙基固硫剂,钠基固硫剂和镁基固硫剂3类可能具有固硫效果的固硫剂进行理论和实验验证。其中,钙基固硫剂选择CaCO3、CaO、Ca(OH)2和CaSiO3,钠基固硫剂选择Na2CO3、NaHCO3、NaOH、Na2SiO3和NaAlO2,镁基固硫剂选择MgO和Mg(OH)2。
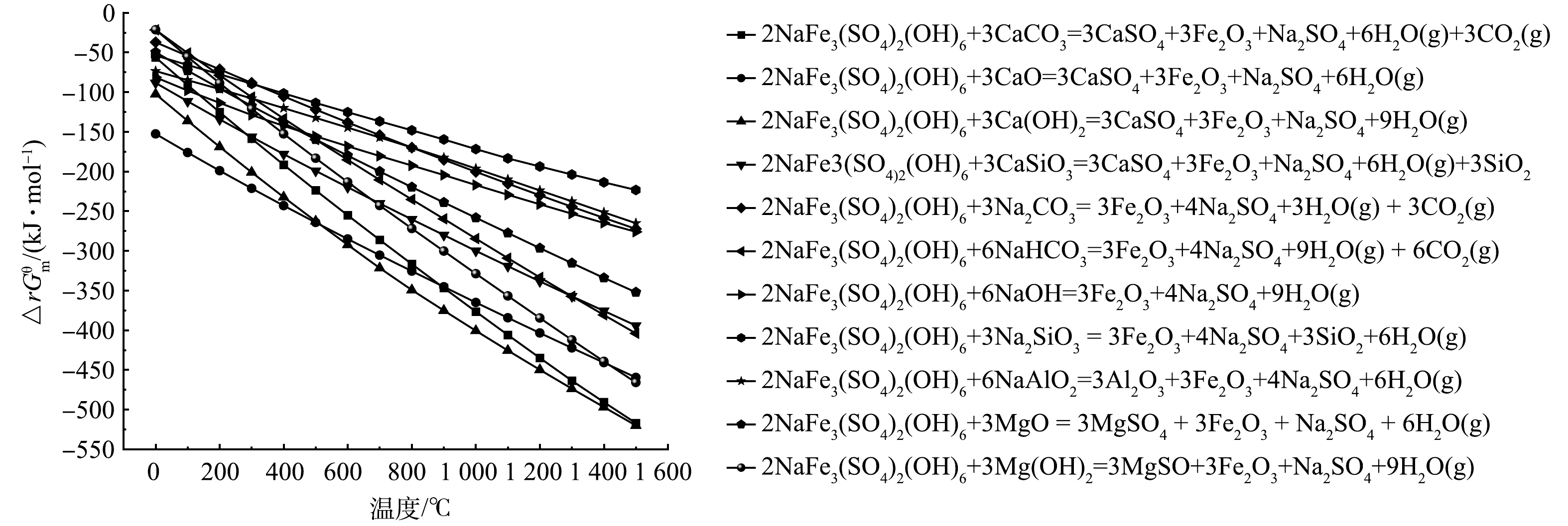
本研究铁矾渣中主要成分是黄钠铁矾,是受热分解产生二氧化硫的主要物质,利用HSC 6.0对各种固硫剂与黄钠铁矾可能发生的反应进行热力学模拟计算,可能发生的固硫反应在不同温度下反应的吉布斯自由能结果如图2所示。
模拟结果如图2所示,理论上,所有固硫剂在温度范围内△rGθm<0,即1 500 ℃以下选择的固硫剂均有可能发生固硫反应,且反应温度越高,△rGθm越小,反应趋向于正向发生。
以不同固硫剂与黄钠铁矾在高温下反应热力学计算结果为依据,进铁矾渣和固硫剂混合焙烧实验,并按照式 (2) 和式 (3) 所述方式进行固硫率计算,结果见表2。除9、10和11组外,其余固硫剂在1 100 ℃实验条件下均有固硫效果,其中添加钙基固硫剂1、2、3和4组的固硫率均大于75%,相较于钠基固硫剂的有更好的固硫效果;而添加钠基固硫剂的5、6、7和8组的固硫率均低于70%,其中Na2SiO3的固硫率最高为68.36%;添加NaAlO2、MgO和Mg(OH)2固硫率低于0,即促进了硫的排放。后续实验选择固硫率最高的CaO作为铁矾渣轻质固硫陶粒的系统实验用固硫剂。
-
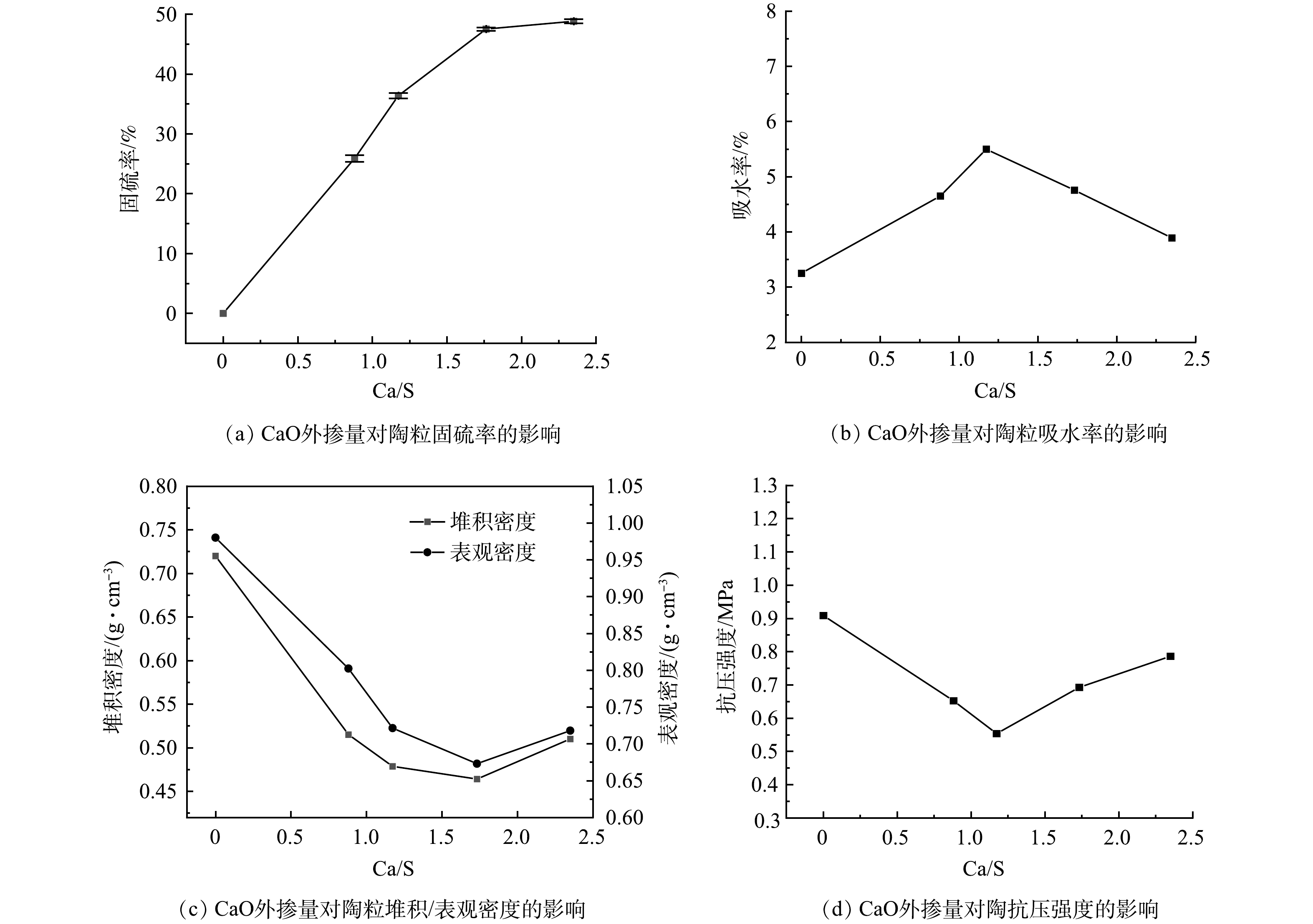
采用CaO作为陶粒的固硫剂,根据体系不同Ca/S (摩尔比) 外掺固硫剂制备铁矾渣固硫陶粒。图3(a)~图3(d)分别是CaO外掺量对陶粒固硫率、吸水率、堆积/表观密度、和抗压强度的影响,其中外掺Ca/S的摩尔比为0.88、1.17、1.76和2.35。由图3(a)可知,随着CaO掺加量的增加,固硫率增大,当Ca/S为2.35时,固硫率达到48.8%,当Ca/S小于1.76时,固硫率上升较为明显,当Ca/S大于1.76时,固硫率基本保持恒定。由图3(b)~图3(d)可知,铁矾渣固硫轻质陶粒的吸水率随着CaO的掺加量增加呈现先增加后减小的趋势,抗压强度、堆积密度和表观密度均表现出先减小后增大的趋势;当Ca/S达到1.17后,吸水率达到最高为5.50%,抗压强度达到最低0.55 MPa,堆积密度为0.48 g·cm−3,表观密度为0.72 g·cm−3。
图4为不同CaO掺量下的陶粒截面照片。由图可知,随着CaO掺量的增加截面孔数明显减少,同时截面孔径不断增大。其主要原因可能是,由于CaO掺量的增加,即碱金属氧化物的占比增加,导致陶粒烧制过程中,在较低的温度即可达到熔融状态。因此,在相同的温度的条件下,熔融的液相表面张力降低,内部更易形成气泡,导致陶粒内部孔隙变多;当气泡达到一定数量,距离表面较近的气泡较大且容易破裂,易形成更多的开孔,从而导致吸水率的增加,堆积密度、表观密度和强度降低。但随着CaO掺量的继续增加,陶粒表面熔融相张力更低,更易形成平滑的玻璃相表面,封闭了表面的孔道,导致吸水率降低;同时,内部熔融相在烧结过程中难以包裹产生的气体,即陶粒内部和表面过熔,孔结构被破坏,导致堆积密度、表观密度和抗压强度的提高[27-29]。
-
1) XRD结果分析。图5为不同掺加CaO固硫陶粒和未掺加固硫剂的陶粒的XRD结果,Ca/S摩尔比分别为0.88、1.18、1.76和2.35。由图5可知,陶粒中主要矿相特征峰有SiO2、CaO·Al2O3·2SiO2、CaSO4和K2O·Al2O3·6SiO2,固硫陶粒的主要矿相种类基本一致;随着CaO掺量的增加,当Ca/S摩尔比达到1.76时,出现了明显的K2SO4特征峰,且Ca/S摩尔比怎加到2.35时特征峰明显增强,同时SiO2的峰也逐渐增强。这说明,CaO的增加,使体系中产生了更多的K2SO4和SiO2。
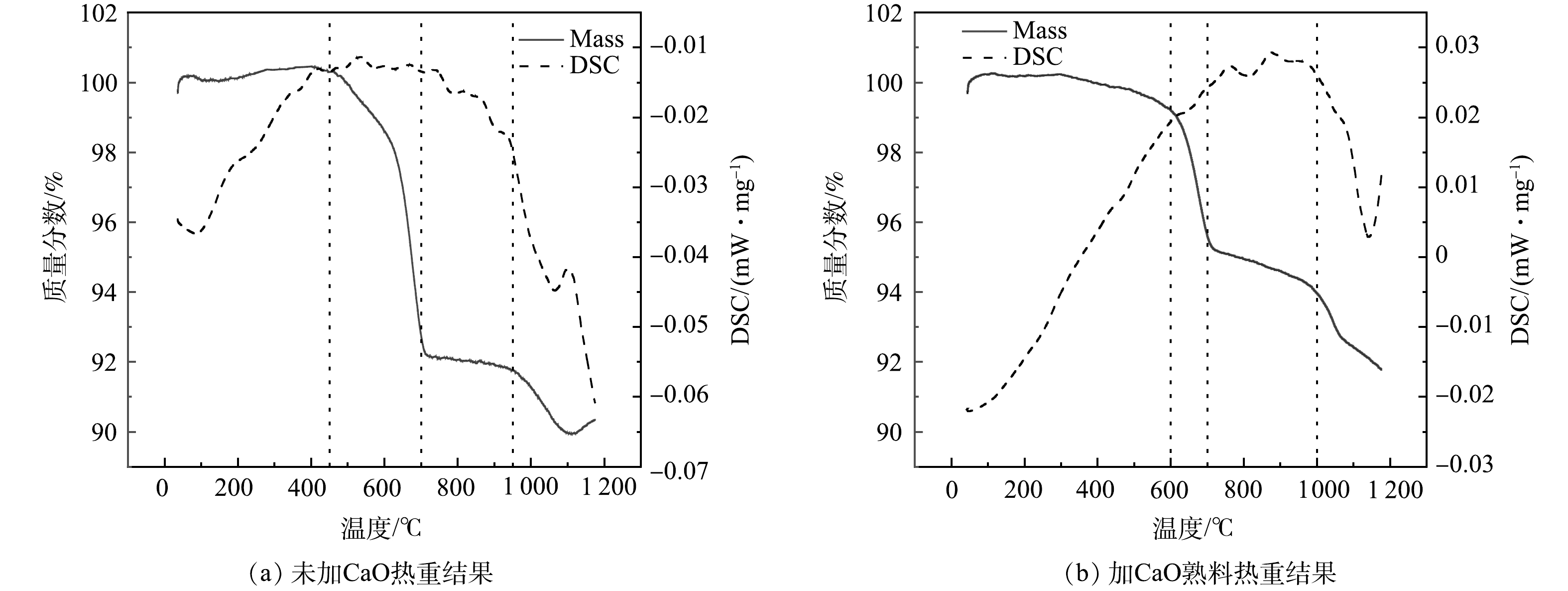
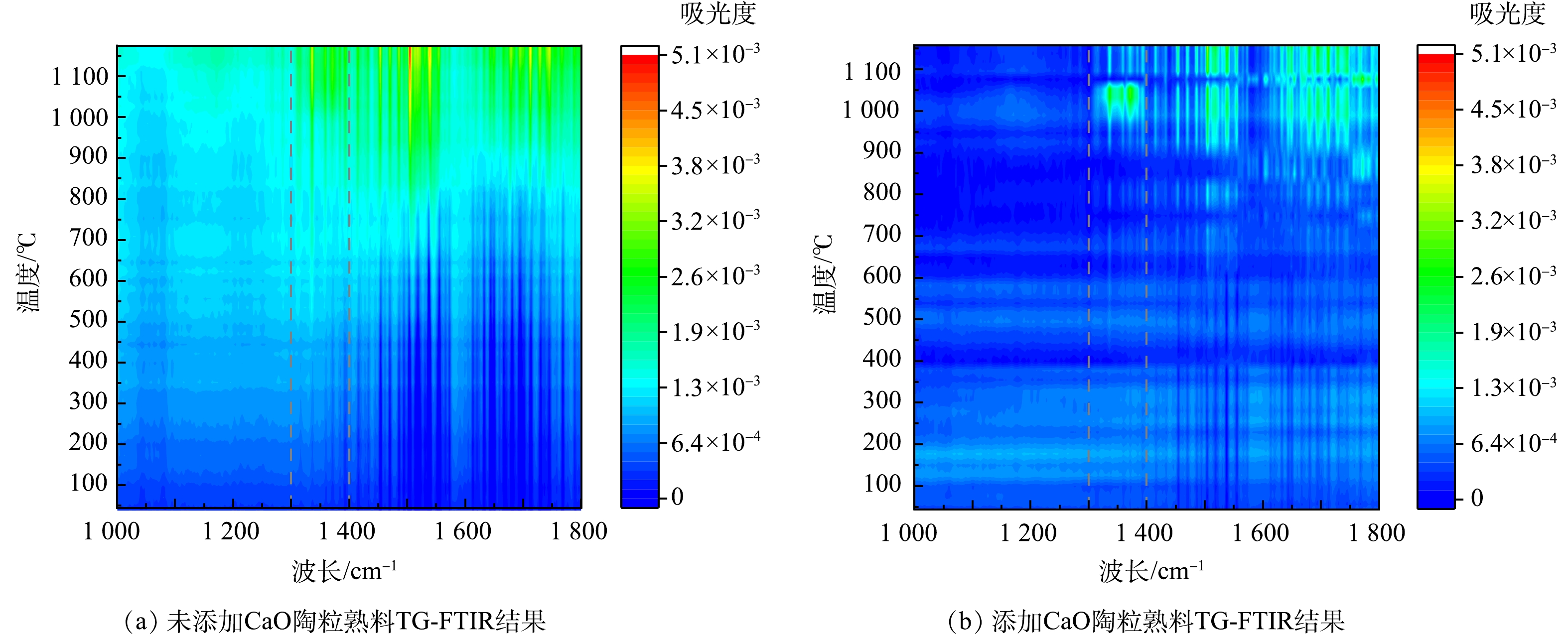
2) TG-DSC-FTIR分析。图6和7所示分别为利用TG-DSC-FTIR研究未掺加CaO的陶粒熟料及添加CaO且Ca/S=2.35的陶粒熟料在常温至1 200 ℃的质量损失变化规律,对固硫陶粒熟料升温过程产生的气体进行红外分析。由图6(a)可知,在温度上升过程中,2次失重分别在450和950 ℃附近发生;随着温度升高,失重速度逐渐增加,陶粒烧制过程中总共失重达到了超过10%。由图6(b)可知,添加CaO后,2次失重分别在600和1 000 ℃左右发生,整个过程总失重不超过7%;在1 100~1 150 ℃范围内,失重由3%降低至2%以下。二氧化硫所对应的红外波长范围是1 300~1 400 cm−1附近,不同体系下存在偏移。根据图7加固硫剂熟料产生气体红外结果可知,CaO的加入有效的提高了分解产生SO2的温度,在0~1 000 ℃的升温过程中,当未加入CaO的样品达到在500 ℃附近开始有SO2产出,达到800 ℃时SO2产生量增加,并随着温度升高逐渐加强,结果与热失重结果相对应。加入CaO的样品主要在1 000 ℃后产生SO2,相较于未掺加CaO的结果,吸光度在1 100~1 150 ℃温度明显降低。可见,CaO的加入,SO2的溢出量在升温过程减少,硫元素在升温过程中被有效固定下来。
有研究表明,钾长石可在高温过程与CaSO4反应转化成其他含钙矿相并生成K2SO4[30-31],因此推测陶粒的固硫机理如下:首先NaFe3(SO4)2(OH)6与CaO反应,生成相应的固硫产物CaSO4;生成的CaSO4可继续和陶粒中的K2O·Al2O3·6SiO2反应,生成了CaO·Al2O3·2SiO2和K2SO4,并且随着CaO的增加,K2SO4特征峰逐渐增强,体系中K2SO4含量的增加印证了这一观点,反应方程式如式式 (5)~式 (6)所示:
-
采用《固体废物浸出毒性浸出方法醋酸缓冲溶液法》[32]的方法对原料及固硫陶粒进行毒性浸出实验,实验对象包括铁矾渣、页岩及Ca/S=2.35掺加量CaO的固硫陶粒,并根据《危险废物鉴别标准浸出毒性鉴别》[33]中规定的鉴别浸出毒性,结果如表3所示。
如表3所示,铁矾渣中浸出的可被检测元素有Ni、Co、Mn、Cu、Zn和Cr。Ni、Co和Mn的浸出量分别达到了19.819、12.580和5.715 mg·L−1,其中Ni超过标准近4倍,浸出量较高。页岩中检出元素有Ni、Co、Mn、Cu、Zn、Cr、Se和Cd,其中Mn的浸出量较高,达到15.143 mg·L−1。固硫陶粒的检出元素的浸出浓度低于铁矾渣和页岩检出元素的浸出浓度,并且小于《危险废物鉴别标准浸出毒性鉴别》[33]所规定的元素浓度,对环境没有污染风险。
-
1) 固硫剂验证实验中,钙基固硫剂相较于钠基固硫剂对铁矾渣有更好的固硫效果,其中氧化钙的固硫率较优;固硫陶粒实验中,当固硫剂掺加量达到Ca/S=2.35,固硫率达到48.8%。
2) 由于固硫剂添加导致碱金属含量增加,熔融温度降低烧制过程中陶粒性能发生改变,其中吸水率和抗压强度先增加后减少,堆积密度和表观密度先减少后增加;固硫陶粒毒性浸出符合《GB 5085.3-2007危险废物鉴别标准浸出毒性鉴别》中的规定,无环境污染风险。
3) 固硫剂可有效提高SO2开始分解的温度,并减少反应失重;CaO反应过程中与黄钠铁矾发生反应生成CaSO4,部分CaSO4会和K2O·Al2O3·6SiO2继续反应,生成钙长石和K2SO4。
利用铁矾渣制备轻质固硫陶粒
Preparation of Light Sulfur Retention Ceramsite from Jarosite Residues
-
摘要: 铁矾渣是锂电回收过程黄铁矾法除铁产生的废渣,高温条件下易分解产生二氧化硫。通过在铁矾渣中添加固硫剂制备固硫陶粒是实现铁矾渣合理利用的有效途径。通过计算高温环境下不同氧化物吉布斯自由能,并结合固硫剂铁矾渣混合焙烧实验,确定固硫效果较优的氧化钙作为固硫陶粒的固硫剂;同时,考察固硫剂掺量对固硫陶粒的固硫效果及性能的影响。结果表明,随着固硫剂掺量增加固硫率上升,固硫陶粒的吸水率和抗压强度先增加后减少,堆积密度和表观密度先减少后增加。当Ca/S 比为 2.35时,固硫陶粒的固硫率达到最高48.8%,吸水率为3.89%,抗压强度为0.79 MPa,表观密度和堆积密度分别为0.72 g·cm-3和0.51 g·cm-3。通过XRD和TG-DSC-FTIR分析固硫机理,发现硫酸盐通过与固硫剂相互作用形成了分解温度更高的CaSO4和K2SO4。固硫陶粒的毒性浸出实验结果符合国家标准。本研究结果可为铁矾渣的高值环保利用的相关研究提供参考。Abstract: Jarosite residues is the waste residue produced by iron removal in jarosite method in the process of lithium-ion batteries recovery, and it decomposes to sulfur dioxide easily at high temperatures. The rational and effective way to utilize jarosite residues is to prepare sulfur retention ceramsite by adding sulfur retention agent. Through the thermodynamic calculation of different oxides, and combined with mixed calcination experiment of sulfur retention agent with jarosite residues, CaO was chosen as the sulfur retention agent in the paper. The effect of the amount of sulfur retention agent on sulfur retention efficiency and properties of ceramsite were investigated. Results showed that the increase of the amount of sulfur retention agent led to an increase in sulfur retention efficiency, an increase and then decrease trend in water absorption rate and compressive strength, and the reverse trend in bulk density and apparent density. Under Ca/S of 2.35, the sulfur retention rate could reach to the highest of 48.8%, with the water absorption rate of 3.89%, the compressive strength of 0.79 MPa, and the apparent and bulk densities of 0.72 g·cm−3 and 0.51 g·cm−3, respectively. XRD and TG-DSC-FTIR were used to further investigate the mechanism of sulfur retention. It was found that CaSO4 and K2SO4 with higher decomposition temperature were formed by the interaction of sulfate with sulfur retention agent. The result of toxicity leaching meet the national standard. This study provided a reference for further research on the high-value and environmental protection applications of jarosite residues.
-
近年来,随着新能源产业的迅速发展,锂电池的产量大幅度增加,废旧锂电池也随之大量产生[1]。在锂电池湿法回收过程中,通常采用黄铁矾法实现其中铁元素的脱除,进而产生铁矾渣固体废弃物[2]。铁矾渣主要成分黄钠铁矾 (NaFe3(SO4)2(OH)6) 是一种硫酸盐复盐,通常含有少量的镍钴锰等重金属元素,直接填埋潜在环境风险较大。利用铁矾渣为原料烧制陶粒产品是一种可以固定重金属元素,实现资源化利用的有效途径。但由于其含硫较高,高温过程易分解产生SO2,存在着后续环境处理成本较高的问题[3-6]。
目前,高温固硫的研究主要集中在高温反应中固硫和烟气脱硫[7-9]方面。在高温反应中,固硫是在高温烧结前采取措施减少高温过程含硫物质的分解[10],主要技术手段是在高温过程前或者高温过程中添加一定量的固硫剂,使高温时产生的气态硫化物与固硫剂中的有效成分 (CaO、MgO等) 发生反应,使其转变成硫酸盐等形式留在渣中,进而有效减少SO2和SO3的释放,从而达到固硫的效果。其反应温度一般控制在800~1 250 ℃,常用固硫剂有钙基固硫剂、钠基固硫剂和镁基固硫剂[11-13]。烟气脱硫是利用固相吸收剂、水或碱性溶液与含硫烟气充分接触,生成对应的硫酸盐等化合物,从而减少烟气中SO2的排放,目前此方法存在脱硫设备易腐蚀且副产石膏量大[14-17]的问题。陶粒通常在900~1 300 ℃烧制形成[18],然而黄钠铁矾在高温过程中易分解产生SO2,如式(1)所示[19],该过程会提高后端脱硫处理成本。因此,通过研究在陶粒的烧制过程中添加固硫剂降低生产过程中SO2的排放可有效减小后续脱硫设备规模,以降低生产成本。
4NaFe3(SO4)2(OH)6→2Na2SO4+6Fe2O3+6SO2↑+3O2↑+12H2O↑ (1) 通过对不同的固硫剂在高温下可能的反应进行热力学模拟,筛选出高温过程对铁矾渣可能存在固硫效果的Ca/Na/Mg基固硫剂,并利用铁矾渣-固硫剂混合焙烧的实验方式验证固硫剂在1 100 ℃条件下焙烧对铁矾渣的固硫效果,以筛选出固硫效果较佳的固硫剂,从而进一步验证固硫剂掺量对陶粒密度、吸水率和抗压强度的影响。同时,通过XRD和TG-FTIR分析,明确不同烧成反应物的矿相、反应热力学和气相产物的变化,从而明确固硫机理。对固硫陶粒进行了毒性浸出分析,检验其环境安全性。
1. 材料与方法
1.1 原料及仪器
本研究制备陶粒的主要原料包括页岩、铁矾渣和含碳化硅废料分别来自湖南某锂电回收企业和陶瓷企业;固硫剂筛选考察实验分别采用碳酸钙 (CaCO3、氧化钙 (CaO) 、氢氧化钙 (Ca(OH)2) 、硅酸钙 (CaSiO3) 、碳酸钠 (Na2CO3) 、碳酸氢钠 (NaHCO3) 、氢氧化钠 (NaOH) 、硅酸钠 (Na2SiO3) 、偏铝酸钠 (NaAlO2) 、氧化镁 (MgO) 和氢氧化镁 (Mg(OH)2) ,均为分析纯。
主要使用的设备及分析仪器:X 射线衍射仪 (Smartlab,日本株式会社理学公司);X射线荧光光谱仪(AXIOS,荷兰帕纳科公司);烧结炉 (佛山市科顺龙电控有限公司);万能试验机 (E100,济南试金集团有限公司);热重红外联用 (TENSOR III,德国布鲁克公司;STA449 F5,德国耐驰公司)。
1.2 实验及固硫率计算方法
1) 固硫率的计算方法。固硫率采用硫质量守恒的算法,根据XRF测定焙烧前样品硫的质量分数,称取一定质量的样品,将称取质量的样品进行焙烧后再次称重,并对焙烧后的样品测定硫的质量分数具体计算如式 (2)~式 (3)所示。
Xn=xn∗mnxns∗mns (2) X∗=Xn−XT1−XT (3) 式中:Xn为硫残留率;X*为固硫率;XT为未添加固硫剂的样品硫残留率;xn为烧制样品含硫质量分数;mn为烧制样品质量,g;xns为未烧样品含硫质量分数;mns为未烧样品质量,g。
2) 混合焙烧实验。称取一定量的铁矾渣,经过对铁矾渣硫含量的计算,分别按照摩尔比Ca/S=2.35、Na/S=2.35和Mg/S=2.35称取相应物质的质量,将称取的各物质利用球磨机充分混合5 min后称重,计算出混合物体系含硫质量分数,取一定量混合物在1 100 ℃的条件下灼烧30 min后再次称重,根据式 (2)~式 (3)计算固硫率,最终固硫率取3次稳定实验结果的平均值。
3) 陶粒配方及制备方法。将页岩、铁矾渣和碳化硅废料原料在 (105±2) ℃烘干至恒重,经破碎和球磨机球磨30 min后过100目 (150 μm) 标准筛,按照页岩和铁矾渣的质量分数为92.5%和7.5%,在页岩和铁矾渣总质量基础上掺加0.8%含碳化硅废料,利用球磨机混合5 min后加入适量水,利用成球设备制备生料球。将滚好的生料球在 (105±2) ℃烘干至恒重后,在500 ℃下预热30 min得到陶粒熟料,预热好的陶粒熟料直接放入1 100 ℃的电炉中烧制一定时间后取出冷却。
4) 陶粒物理性能测试方法。抗压强度采取一种已经报道的方法[20],将陶粒样品垂直放置于压力机承压板之间,以一定升压速度施加载荷,压至破坏时得到破坏荷载Pc,每组样品测试10颗陶粒,取其平均值,得到陶粒的强度S。测试方法原理如式(4)所示。
S=2.8PcπX2 (4) 式中:S为陶粒的单颗粒强度,MPa;Pc为陶粒破坏时的荷载,N;X为陶粒在起始受力时与压力机承压板接触点间的垂直距离,mm。
陶粒的表观密度和吸水率按照《轻集料及其试验方法》[21]测定。
2. 结果与讨论
2.1 原料的化学成分及矿相结构
将烘干至恒重的原料进行XRD和XRF测试。所使用的原料主要化学成分如表1所示,由表可知,铁矾渣中硫、铁、铝和钠含量较高,其中同时含有镍、钴、锰和铜等金属元素,烧失率为22.60%;页岩富含铝、硅、钙等元素,其中SiO2、Al2O3和CaO的质量分数分别为53.79%、18.04%和11.93%,烧失率为14.60%;陶粒成孔剂采用含有碳化硅成分的电子陶瓷行业研磨抛光产生的废料,其中Al2O3和SiC的质量分数分别为49.41%和43.34%,烧失率为2.80%。由图1可知,铁矾渣主要矿相为黄钠铁矾 (NaFe3(SO4)2(OH)6) 和CaSO4·2H2O,根据铁矾渣产生过程推测含铝物相为无定型的氢氧化铝;页岩的主要矿相成分是白云母石,石英和方解石;含碳化硅废料的主要矿相是碳化硅和氧化铝。
表 1 原料化学成分Table 1. Chemical composition of raw materials% (质量分数) 供试原料 SO3 Fe2O3 Al2O3 Na2O CaO NiO SiO2 Co3O4 TiO2 MnO K2O SiC LOI 铁矾渣 26.82 26.55 20.28 11.96 6.95 1.21 0.60 0.58 0.44 0.27 — — 22.60 页岩 0.11 7.78 18.04 0.30 11.93 — 53.79 — 0.78 0.13 3.47 — 14.60 含碳化硅废料 0.08 0.61 49.41 0.18 0.35 — — 0.15 — 0.16 43.34 2.80 2.2 固硫剂筛选及效果验证
常用固硫剂有很多种,碱金属固硫剂是其中最重要的一类,其中钙基应用最为广泛[7, 22-25],部分研究人员利用富含碱金属氧化物的固废作为固硫剂对反应产生二氧化硫进行固定[9, 26],结合文献和理论分析,通过对钙基固硫剂,钠基固硫剂和镁基固硫剂3类可能具有固硫效果的固硫剂进行理论和实验验证。其中,钙基固硫剂选择CaCO3、CaO、Ca(OH)2和CaSiO3,钠基固硫剂选择Na2CO3、NaHCO3、NaOH、Na2SiO3和NaAlO2,镁基固硫剂选择MgO和Mg(OH)2。
本研究铁矾渣中主要成分是黄钠铁矾,是受热分解产生二氧化硫的主要物质,利用HSC 6.0对各种固硫剂与黄钠铁矾可能发生的反应进行热力学模拟计算,可能发生的固硫反应在不同温度下反应的吉布斯自由能结果如图2所示。
模拟结果如图2所示,理论上,所有固硫剂在温度范围内△rGθm<0,即1 500 ℃以下选择的固硫剂均有可能发生固硫反应,且反应温度越高,△rGθm越小,反应趋向于正向发生。
以不同固硫剂与黄钠铁矾在高温下反应热力学计算结果为依据,进铁矾渣和固硫剂混合焙烧实验,并按照式 (2) 和式 (3) 所述方式进行固硫率计算,结果见表2。除9、10和11组外,其余固硫剂在1 100 ℃实验条件下均有固硫效果,其中添加钙基固硫剂1、2、3和4组的固硫率均大于75%,相较于钠基固硫剂的有更好的固硫效果;而添加钠基固硫剂的5、6、7和8组的固硫率均低于70%,其中Na2SiO3的固硫率最高为68.36%;添加NaAlO2、MgO和Mg(OH)2固硫率低于0,即促进了硫的排放。后续实验选择固硫率最高的CaO作为铁矾渣轻质固硫陶粒的系统实验用固硫剂。
表 2 固硫率的实验结果Table 2. Experimental results of sulfur-retention rate组别 固硫剂 硫残留率/% 固硫率/% 对照 未添加 71.21 — 1 CaCO3 93.89 78.78 2 CaO 99.99 99.97 3 Ca(OH)2 96.09 86.41 4 CaSiO3 99.90 99.66 5 Na2CO3 85.87 50.92 6 NaHCO3 88.80 61.11 7 NaOH 85.06 48.09 8 Na2SiO3 90.89 68.36 9 NaAlO2 69.57 -5.71 10 MgO 63.34 -27.34 11 Mg(OH)2 45.47 -89.42 2.3 固硫陶粒的固硫率及工艺条件优化
采用CaO作为陶粒的固硫剂,根据体系不同Ca/S (摩尔比) 外掺固硫剂制备铁矾渣固硫陶粒。图3(a)~图3(d)分别是CaO外掺量对陶粒固硫率、吸水率、堆积/表观密度、和抗压强度的影响,其中外掺Ca/S的摩尔比为0.88、1.17、1.76和2.35。由图3(a)可知,随着CaO掺加量的增加,固硫率增大,当Ca/S为2.35时,固硫率达到48.8%,当Ca/S小于1.76时,固硫率上升较为明显,当Ca/S大于1.76时,固硫率基本保持恒定。由图3(b)~图3(d)可知,铁矾渣固硫轻质陶粒的吸水率随着CaO的掺加量增加呈现先增加后减小的趋势,抗压强度、堆积密度和表观密度均表现出先减小后增大的趋势;当Ca/S达到1.17后,吸水率达到最高为5.50%,抗压强度达到最低0.55 MPa,堆积密度为0.48 g·cm−3,表观密度为0.72 g·cm−3。
图4为不同CaO掺量下的陶粒截面照片。由图可知,随着CaO掺量的增加截面孔数明显减少,同时截面孔径不断增大。其主要原因可能是,由于CaO掺量的增加,即碱金属氧化物的占比增加,导致陶粒烧制过程中,在较低的温度即可达到熔融状态。因此,在相同的温度的条件下,熔融的液相表面张力降低,内部更易形成气泡,导致陶粒内部孔隙变多;当气泡达到一定数量,距离表面较近的气泡较大且容易破裂,易形成更多的开孔,从而导致吸水率的增加,堆积密度、表观密度和强度降低。但随着CaO掺量的继续增加,陶粒表面熔融相张力更低,更易形成平滑的玻璃相表面,封闭了表面的孔道,导致吸水率降低;同时,内部熔融相在烧结过程中难以包裹产生的气体,即陶粒内部和表面过熔,孔结构被破坏,导致堆积密度、表观密度和抗压强度的提高[27-29]。
2.4 固硫机理研究
1) XRD结果分析。图5为不同掺加CaO固硫陶粒和未掺加固硫剂的陶粒的XRD结果,Ca/S摩尔比分别为0.88、1.18、1.76和2.35。由图5可知,陶粒中主要矿相特征峰有SiO2、CaO·Al2O3·2SiO2、CaSO4和K2O·Al2O3·6SiO2,固硫陶粒的主要矿相种类基本一致;随着CaO掺量的增加,当Ca/S摩尔比达到1.76时,出现了明显的K2SO4特征峰,且Ca/S摩尔比怎加到2.35时特征峰明显增强,同时SiO2的峰也逐渐增强。这说明,CaO的增加,使体系中产生了更多的K2SO4和SiO2。
2) TG-DSC-FTIR分析。图6和7所示分别为利用TG-DSC-FTIR研究未掺加CaO的陶粒熟料及添加CaO且Ca/S=2.35的陶粒熟料在常温至1 200 ℃的质量损失变化规律,对固硫陶粒熟料升温过程产生的气体进行红外分析。由图6(a)可知,在温度上升过程中,2次失重分别在450和950 ℃附近发生;随着温度升高,失重速度逐渐增加,陶粒烧制过程中总共失重达到了超过10%。由图6(b)可知,添加CaO后,2次失重分别在600和1 000 ℃左右发生,整个过程总失重不超过7%;在1 100~1 150 ℃范围内,失重由3%降低至2%以下。二氧化硫所对应的红外波长范围是1 300~1 400 cm−1附近,不同体系下存在偏移。根据图7加固硫剂熟料产生气体红外结果可知,CaO的加入有效的提高了分解产生SO2的温度,在0~1 000 ℃的升温过程中,当未加入CaO的样品达到在500 ℃附近开始有SO2产出,达到800 ℃时SO2产生量增加,并随着温度升高逐渐加强,结果与热失重结果相对应。加入CaO的样品主要在1 000 ℃后产生SO2,相较于未掺加CaO的结果,吸光度在1 100~1 150 ℃温度明显降低。可见,CaO的加入,SO2的溢出量在升温过程减少,硫元素在升温过程中被有效固定下来。
有研究表明,钾长石可在高温过程与CaSO4反应转化成其他含钙矿相并生成K2SO4[30-31],因此推测陶粒的固硫机理如下:首先NaFe3(SO4)2(OH)6与CaO反应,生成相应的固硫产物CaSO4;生成的CaSO4可继续和陶粒中的K2O·Al2O3·6SiO2反应,生成了CaO·Al2O3·2SiO2和K2SO4,并且随着CaO的增加,K2SO4特征峰逐渐增强,体系中K2SO4含量的增加印证了这一观点,反应方程式如式式 (5)~式 (6)所示:
2NaFe3(SO4)2(OH)6+3CaO=3CaSO4+3Fe2O3+Na2SO4+6H2O↑ (5) K2O·Al2O3·6SiO2+CaSO4=K2SO4+CaO·Al2O3·2SiO2+4SiO2 (6) 2.5 毒性浸出分析
采用《固体废物浸出毒性浸出方法醋酸缓冲溶液法》[32]的方法对原料及固硫陶粒进行毒性浸出实验,实验对象包括铁矾渣、页岩及Ca/S=2.35掺加量CaO的固硫陶粒,并根据《危险废物鉴别标准浸出毒性鉴别》[33]中规定的鉴别浸出毒性,结果如表3所示。
表 3 浸出毒性测试结果(Ni/Co/Mn/Cu/Zn/Cr/Se/Cd/Pb/Ag/Ti/Zr)Table 3. Test results of extraction toxicity (Ni/Co/Mn/Cu/Zn/Cr/Se/Cd/Pb/Ag/Ti/Zr)mg·L−1 被检元素 检测样品 GB5085.3-2007 铁矾渣 页岩 陶粒 固硫陶粒 Ni 19.819 0.083 0.008 0.010 5 Co 12.580 0.035 0.007 0.008 * Mn 5.715 15.143 0.051 0.046 * Cu 0.181 0.001 0.000 0.107 100 Zn 0.054 0.014 0.003 0.050 100 Cr 0.011 0.017 0.000 0.005 5 Se — 0.098 0.000 0.042 1 Cd — 0.009 0.000 0.000 1 Pb — — — — 5 Ag — — — — 5 Ti — — — — * Zr — — — — * 注:GB 5085.3—2007未规定的数据以“*”表示;数据未检出以“—”表示。 如表3所示,铁矾渣中浸出的可被检测元素有Ni、Co、Mn、Cu、Zn和Cr。Ni、Co和Mn的浸出量分别达到了19.819、12.580和5.715 mg·L−1,其中Ni超过标准近4倍,浸出量较高。页岩中检出元素有Ni、Co、Mn、Cu、Zn、Cr、Se和Cd,其中Mn的浸出量较高,达到15.143 mg·L−1。固硫陶粒的检出元素的浸出浓度低于铁矾渣和页岩检出元素的浸出浓度,并且小于《危险废物鉴别标准浸出毒性鉴别》[33]所规定的元素浓度,对环境没有污染风险。
3. 结论
1) 固硫剂验证实验中,钙基固硫剂相较于钠基固硫剂对铁矾渣有更好的固硫效果,其中氧化钙的固硫率较优;固硫陶粒实验中,当固硫剂掺加量达到Ca/S=2.35,固硫率达到48.8%。
2) 由于固硫剂添加导致碱金属含量增加,熔融温度降低烧制过程中陶粒性能发生改变,其中吸水率和抗压强度先增加后减少,堆积密度和表观密度先减少后增加;固硫陶粒毒性浸出符合《GB 5085.3-2007危险废物鉴别标准浸出毒性鉴别》中的规定,无环境污染风险。
3) 固硫剂可有效提高SO2开始分解的温度,并减少反应失重;CaO反应过程中与黄钠铁矾发生反应生成CaSO4,部分CaSO4会和K2O·Al2O3·6SiO2继续反应,生成钙长石和K2SO4。
-
表 1 原料化学成分
Table 1. Chemical composition of raw materials
% (质量分数) 供试原料 SO3 Fe2O3 Al2O3 Na2O CaO NiO SiO2 Co3O4 TiO2 MnO K2O SiC LOI 铁矾渣 26.82 26.55 20.28 11.96 6.95 1.21 0.60 0.58 0.44 0.27 — — 22.60 页岩 0.11 7.78 18.04 0.30 11.93 — 53.79 — 0.78 0.13 3.47 — 14.60 含碳化硅废料 0.08 0.61 49.41 0.18 0.35 — — 0.15 — 0.16 43.34 2.80 表 2 固硫率的实验结果
Table 2. Experimental results of sulfur-retention rate
组别 固硫剂 硫残留率/% 固硫率/% 对照 未添加 71.21 — 1 CaCO3 93.89 78.78 2 CaO 99.99 99.97 3 Ca(OH)2 96.09 86.41 4 CaSiO3 99.90 99.66 5 Na2CO3 85.87 50.92 6 NaHCO3 88.80 61.11 7 NaOH 85.06 48.09 8 Na2SiO3 90.89 68.36 9 NaAlO2 69.57 -5.71 10 MgO 63.34 -27.34 11 Mg(OH)2 45.47 -89.42 表 3 浸出毒性测试结果(Ni/Co/Mn/Cu/Zn/Cr/Se/Cd/Pb/Ag/Ti/Zr)
Table 3. Test results of extraction toxicity (Ni/Co/Mn/Cu/Zn/Cr/Se/Cd/Pb/Ag/Ti/Zr)
mg·L−1 被检元素 检测样品 GB5085.3-2007 铁矾渣 页岩 陶粒 固硫陶粒 Ni 19.819 0.083 0.008 0.010 5 Co 12.580 0.035 0.007 0.008 * Mn 5.715 15.143 0.051 0.046 * Cu 0.181 0.001 0.000 0.107 100 Zn 0.054 0.014 0.003 0.050 100 Cr 0.011 0.017 0.000 0.005 5 Se — 0.098 0.000 0.042 1 Cd — 0.009 0.000 0.000 1 Pb — — — — 5 Ag — — — — 5 Ti — — — — * Zr — — — — * 注:GB 5085.3—2007未规定的数据以“*”表示;数据未检出以“—”表示。 -
[1] TAO R, XING P, LI H Q, et al. Full-component pyrolysis coupled with reduction of cathode material for recovery of spent LiNiXCoYMnZO2 lithium-ion batteries[J]. ACS Sustainable Chemistry & Engineering, 2021, 9(18): 6318-6328. [2] 陈欢, 张银亮, 谭群英, 等. 废旧电池回收过程中硫酸镍钴锰溶液除铁铝工艺研究[J]. 湿法冶金, 2018, 37(6): 482-486. doi: 10.13355/j.cnki.sfyj.2018.06.011 [3] MUKUNA P M, MAMOOKHO E M, ESTHER T A. Characterization, leachate characteristics and compressive strength of jarosite/clay/fly ash bricks[J]. Materials Today:Proceedings, 2018, 5(9): 17802-17811. doi: 10.1016/j.matpr.2018.06.105 [4] ASOKAN P, VIJAY KUMAR T, RAVI P, et al. Recycling marble wastes and jarosite wastes into sustainable hybrid composite materials and validation through response surface methodology[J]. Journal of Cleaner Production, 2019, 240(10): 118249.1-118249.18. [5] 刘明坤, 孙振华, 李少鹏, 等. 工业副产铁矾渣资源化利用研究进展[J]. 材料导报, 2022, 36(16): 163-171. doi: 10.11896/cldb.20100089 [6] 吕娟, 黄利华, 滕德亮, 等. 相对湿度对钙基脱硫剂干法烟气脱硫效率的影响[J]. 环境工程学报, 2020, 14(6): 1563-1569. doi: 10.12030/j.cjee.201908108 [7] 薛文雯. 金属氧化物和复合钙基固硫剂对煤热解及半焦燃烧固硫的影响[D]. 呼和浩特: 内蒙古大学, 2019. [8] 于清航. 煤粉工业锅炉钙基灰循环烟气脱硫技术研究[D]. 北京: 中国矿业大学(北京), 2018. [9] 韩瑞. 氧化钙固硫/储热过程反应活性和稳定性的强化方法及机制[D]. 哈尔滨: 哈尔滨工业大学, 2019. [10] 王瑞, 刘自勇, 王琪, 等. CO2辅助好氧菌煤炭脱硫工艺的实验[J]. 化工进展, 2021, 40(1): 526-533. [11] 魏宁. 钙基固硫剂固硫机理及固硫效果影响因素研究论文[D]. 西安: 西安科技大学, 2012. [12] 罗金平. 钙基固硫过程中无机矿物转化及可资源化矿物形成[D]. 武汉: 武汉理工大学, 2004. [13] 张威. 添加剂对燃煤高温固硫的促进作用研究[D]. 沈阳: 东北大学, 2008. [14] 冯强, 杜蓉, 王鑫羽. 镍冶炼企业环集烟气二氧化硫治理可行性分析[J]. 甘肃冶金, 2021, 43(2): 27-29. doi: 10.3969/j.issn.1672-4461.2021.02.009 [15] 孟子衡. 低温烟气钢渣联合脱硫脱硝过程强化工艺与机理研究[D]. 中国科学院大学(中国科学院过程工程研究所), 2020. [16] 吕丽娜. 基于石灰石石膏湿法烟气脱硫技术的脱硫添加剂研究[D]. 上海: 华东理工大学, 2016. [17] 李蔷薇. 燃煤烟气SO2/CO2吸收过程反应动力学研究[D]. 北京: 华北电力大学(北京), 2016. [18] 陈美玲, 颜家保, 胡杰, 等. 钢渣污泥陶粒催化剂催化臭氧深度处理炼油废水[J]. 环境工程学报, 2019, 13(6): 1299-1304. doi: 10.12030/j.cjee.201812152 [19] 胡明, 虎训, 邵哲如, 等. 铁矾渣热分解行为及焙烧脱硫机理研究[J]. 有色金属(冶炼部分), 2018(4): 32-38. [20] 林佳佳, 邹晓燕, 王玉, 等. 污泥辅助飞灰水热-热解处置产物制备陶粒[J]. 环境工程学报, 2021, 15(8): 2730-2739. doi: 10.12030/j.cjee.202105070 [21] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. 轻集料及其试验方法 第二部分: 轻集料试验方法: GB/T 17431.2-2010[S]. 北京: 中国标准出版社, 2011. [22] 闫旭东, 郝志强, 刘守军, 等. 钠基固硫剂在低阶煤中的固硫机理研究[J]. 高校化学工程学报, 2018, 32(1): 237-242. [23] 杨巧文, 赵昕伟, 陈思, 等. 燃煤高温固硫机理及影响因素研究[J]. 新型工业化, 2015, 5(6): 41-46. doi: 10.3969/j.issn.2095-6649.2015.06.07 [24] 王晋麟. 燃中固硫方法提高烧结砖生产的脱硫效果探讨[J]. 墙材革新与建筑节能, 2017(6): 27-31. doi: 10.3969/j.issn.1006-9135.2017.06.025 [25] GOU X, LIU Y B, LIU S J, et al. Study on sulfur-fixation effects of cement raw meal during pulverized coal combustion under different atmospheres[J]. Fuel, 2020, 270: 117484-117495. doi: 10.1016/j.fuel.2020.117484 [26] 刘伟, 徐东耀, 陈佐会, 等. 新型固硫剂的研发与应用研究[J]. 矿业科学学报, 2018, 3(4): 398-405. doi: 10.19606/j.cnki.jmst.2018.04.012 [27] ZOU J L, XU G R, LI G B. Ceramsite obtained from water and wastewater sludge and its characteristics affected by Fe2O3, CaO, and MgO[J]. Journal of Hazardous Materials, 2009, 165(1-3): 995-1001. doi: 10.1016/j.jhazmat.2008.10.113 [28] XU G R, LIU M W, LI G B. Stabilization of heavy metals in lightweight aggregate made from sewage sludge and river sediment[J]. Journal of Hazardous Materials, 2013, 260(1): 74-81. [29] QIN J, CUI C, CUI X Y, et al. Preparation and characterization of ceramsite from lime mud and coal fly ash[J]. Construction and Building Materials, 2015, 95: 10-17. doi: 10.1016/j.conbuildmat.2015.07.106 [30] 夏举佩, 任雪姣, 李国斌. 钾长石-硫酸钙-氧化钙热反应制备可溶性钾机理研究[J]. 北京工业大学学报, 2014, 11(40): 1735-1740. doi: 10.11936/bjutxb2014111735 [31] 宋一涵, 李洪枚, 马淑花, 等. 钾长石提钾及制备复合肥料的研究进展[J]. 过程工程学报, 2018, 18(2): 241-257. doi: 10.12034/j.issn.1009-606X.217285 [32] 中华人民共和国国家环境保护总局, 中国国家标准化管理委员会. 固体废物浸出毒性浸出方法醋酸缓冲溶液法: HJ/T 300-2007 [S]. 北京: 中国环境科学出版社, 2007. [33] 中华人民共和国国家环境保护总局, 中国国家标准化管理委员会. 危险废物鉴别标准 浸出毒性鉴别: GB 5085.3-2007[S]. 北京: 中国环境科学出版社, 2007. -




 DownLoad:
DownLoad: