-
挥发性有机物(VOCs)的高灵敏在线监测在大气污染过程监测与溯源、化工园区VOCs溯源与突发事件应急监测以及痕量毒品和炸药的安检等多个领域均起到重要作用[1-2]。尤其在环境领域,VOCs不仅作为室内室外污染中的一次污染物,危害人体健康,还可在大气光氧化条件下产生灰霾和臭氧等二次污染[3-4]。另外,一些VOCs具有极低的嗅阈值,较低的空气浓度即可对人体嗅觉感官造成强烈刺激,引发臭味污染问题。在我国,恶臭投诉事件相当频繁,仅次于噪声的投诉事件,排在第二位,且呈逐年递增的趋势[5-7]。因此,发展VOCs高灵敏在线监测技术对大气污染防控、减少环境污染事件对社会的负面影响具有重要意义。
近年来,质谱技术的飞速发展为VOCs的高灵敏在线监测提供了一种有效的技术手段。目前,用于VOCs直接、在线监测的VOC质谱仪主要包括基于电子电离(EI)、化学电离(CI)和单光子电离(SPI)技术的单质谱[8-14]。其中,发展较成熟的高灵敏VOC质谱为质子转移质谱(PTR-MS),属于化学电离质谱的一种。该仪器可以检测体积分数为10−12量级的VOCs[15-19],已被很多国际一流团队用于实验室及外场VOCs的直接在线测量。与CI相比,SPI属于一种特别的软电离技术[20],它最大的特点是电离方式简单:任何电离能(IE)低于光子能量的原子或分子都会在真空紫外(VUV)灯的辐照下直接电离,生成一个带正电荷的待测物阳离子。SPI具有分子离子产率高、碎片少、质谱简洁、线性动态范围较宽、对极性和非极性有机物都适用等独特优势,非常适合实际VOCs混合样品的直接、在线监测[21]。
在SPI-MS中,VUV光源的产生方式和光子通量对仪器的适用性和检测灵敏度至关重要[21]。大型VUV光源(如同步辐射光源[22-25]和基于激光器的光源[26-27])可以实现高光束密度,但是由于其成本高、体积大和操作复杂等原因,只能用于实验室研究。为了满足常规监测仪器的需要,SPI相关的监测仪器通常使用体积小、携带方便的VUV灯作为SPI光源。常用的VUV灯主要包括直流放电灯和射频放电灯,分别使用直流或射频放电激发低压Kr气产生10 eV的VUV光[28]。然而,目前使用较广泛的商用VUV灯的光子通量约为1011 s−1[29-30],导致SPI离子源的电离效率以及相应的SPI-MS的检测灵敏度较低,成为阻碍SPI-MS发展为高灵敏商用VOC质谱仪的主要因素之一。
为了提高SPI-MS的检测性能,众多研究者在发展新型光电离源方面开展了大量工作。已有研究[31-34]表明,研制新型VUV灯,提高光子通量,是提升SPI-MS检测性能的一种途径。MUHIBERGER等[32-35]开发了一系列电子束激发稀有气体灯,光子通量达到了1013~1016 s−1,将电子束激发稀有气体灯与小型飞行时间质谱(TOFMS)或四级杆质谱(QMS)联用,能够在线检测体积分数为10−9以上的气态有机物。另外一种提升SPI-MS检测灵敏度的途径是增加SPI离子源内的压力[36-39],由此衍生出的技术包括低压光电离(LPPI)和高压光电离(HPPI)技术,相应的电离区压力为几十~几千Pa。SUN等[40]和LI等[41]使用光子通量为1014 s−1的射频VUV灯研制了1台低气压SPI-TOFMS,离子源内气压为500~1 000 Pa,在检测体积分数为10−9的气相苯系物时,10 s内的信号强度可达到5 000,有效提升了SPI-MS的检测灵敏度。然而,该仪器是概念型样机,体积较大,难以用于外场实地VOCs的在线监测。
本研究在已有研究的基础上,基于高通量射频VUV灯、低气压光电离离子源和飞行时间质谱技术,研制出1台紧凑型高灵敏SPI-TOFMS,用苯标准气体对SPI-TOFMS的检测灵敏度、检测限、检测精确度和准确度进行性能测试,考察SPI-TOFMS在农药污染场地异味气体检测中的应用效果,验证SPI-TOFMS在实地VOCs混合物快速检测上的优势及定量能力,以期为环境科学与工程领域涉及的VOCs高灵敏在线监测提供技术支撑。
-
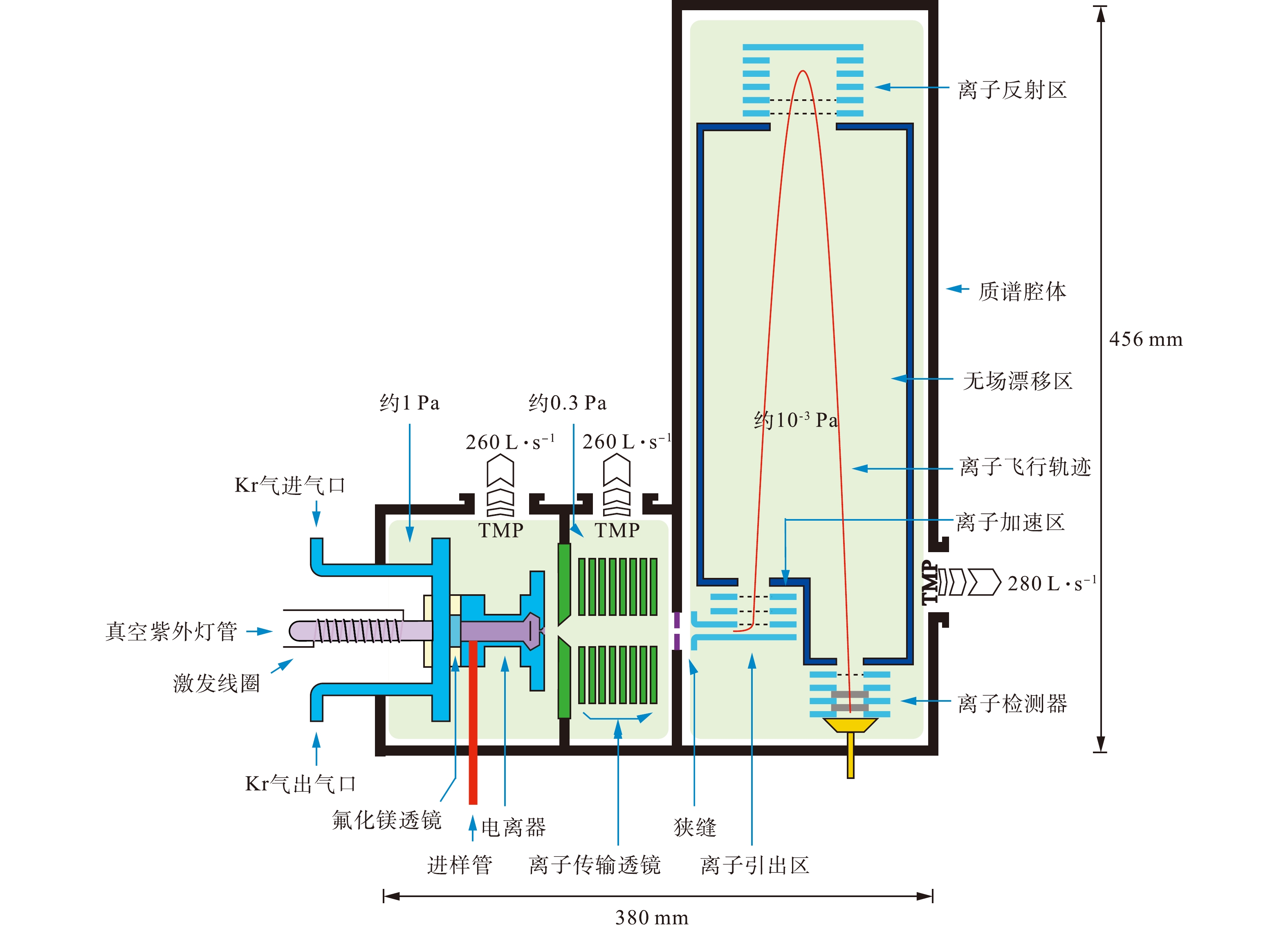
高灵敏SPI-TOFMS装置结构如图1所示。该仪器主要由真空系统、进样系统、VUV光电离源、离子传输系统、垂直引入反射式飞行时间质量分析器和数据采集系统组成。整台仪器设计紧凑,主体部分长度为456 mm,宽度为380 mm。样品分子在VUV灯照射下发生单光子电离产生离子,被离子源的加速电压加速后,通过离子传输系统进入垂直引入反射式飞行时间质量分析器,通过无场飞行区后,到达微通道板离子检测器,最终被数据采集系统收集并进行质谱分析。离子反射区和离子引出区的电极设计和工作电压如图2所示。
-
真空系统分为束源室、差分室和TOF室三级差分系统,分别由3台分子泵维持真空,另外使用1台干泵为3台分子泵提供前级真空。1台干泵为ECODRY 40 plus干式真空泵(德国Leybold公司),抽速为40 m3·h−1;分子泵为1台Agilent TV 301 Navigator涡轮分子泵(美国Agilent公司,对N2抽速为280 L·s−1)和2台Pfeiffer HiPace 300涡轮分子泵(德国Pfeiffer公司,对N2抽速为260 L·s−1);真空规为1个Pfeiffer TPR270皮拉尼规(德国Pfeiffer公司)和2个Pfeiffer PKR361全量程真空规(德国Pfeiffer公司)。真空系统能够使仪器的真空度在进样前保持在2×10−5 Pa以下,进样时,束源室、差分室和TOF室的动态真空度分别约为1、0.3和1×10−3 Pa。
-
进样接口由直径为0.635 cm的不锈钢管将质谱仪与外界空气相连接,通过仪器负压将气相样品被动吸入仪器内。进样时,使用针阀控制进样流量,检测时流量通常为3.3 cm3·s−1。使用气体标定腔配制一定体积分数的样品气体。气体标定腔是一个体积为60 L的开口不锈钢圆筒,上端与一个特氟龙(Teflon)袋密封连接,以保证气体标定腔内维持1个大气压(101 325 Pa)。实验前,使用高纯氮将气体标定腔反复充放气来清洗气体标定腔,将其充气到一定体积。配制样品气体时,向气体标定腔内注射一定浓度的样品溶液,待其挥发完全,即得到一定浓度的气相样品。气体标定腔底部装有磁力搅拌风扇,使气相样品混合均匀;外部覆有加热衣,可调节气体标定腔的温度,便于样品溶液挥发。实验过程中的温度控制在65 ℃。
-
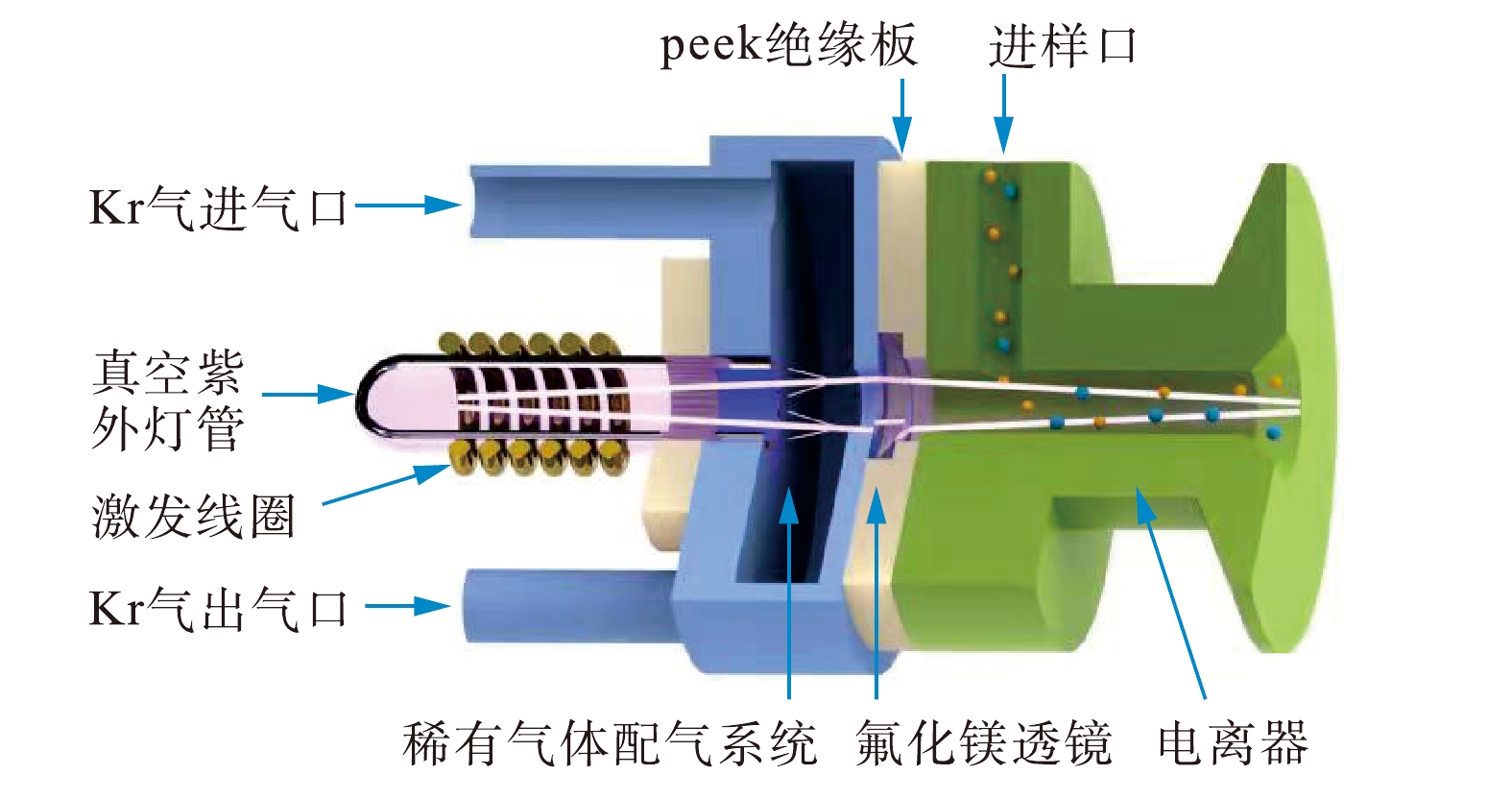
真空紫外单光子电离源由VUV灯和电离器组成,结构示意图如图3所示。VUV灯主要由放电石英灯管、线圈、Kr气配气系统、氟化镁窗片和射频电源组成。射频电源工作频率为13.56 MHz,正常工作功率为60 W。射频电源通过线圈激发惰性气体(5%的Kr气,He气作为缓冲气体)产生真空紫外光。石英灯管内Kr气的压力为250 Pa。真空紫外光穿过氟化镁窗片进入电离器中,光子通量达到6.6×1014 s−1·cm−2,光子能量为10.0 eV(80%)和10.6 eV(20%)。样品分析物通过进样系统进入到电离器中,此时离子源的工作压力为1 300 Pa,经VUV光照射发生单光子电离,产生的离子随后进入离子传输系统。
-
离子传输系统由1组与飞行时间质量分析器垂直装配的离子透镜组成。这种垂直装配的组成结构可以使离子传输系统与飞行时间质量分析器在不设置离子偏转装置的情况下,只需使用合适的加速电压匹配离子的入射动能即可使离子反射后落在检测区内,实现离子检测。离子透镜组由8片中空圆极板组成。给前后4片极板与中间4片极板施加不同的迁移电压,形成聚焦电场。聚焦电场将电离器输送来的离子聚焦为离子束,通过狭缝传输至飞行时间质量分析器。
-
飞行时间质量分析器为垂直加速V型反射式结构,包括离子引出区、离子加速区、无场漂移区、离子反射区和微通道板检测器5个部分,离子飞行距离为220 mm。离子通过狭缝进入质量分析器后,在脉冲引出场的作用下,进入离子加速区加速,漂移过后,进入离子反射区。离子经过减速、反转和加速3个阶段后,漂移飞行进入离子检测器。当离子撞击到微通道板后,产生的电流信号由数据采集系统采集记录。质量分析器在 m/z=182处的质量分辨率(m/Δm)约为500。
-
数据采集系统主要由脉冲/延时发生器、放大器、数据采集卡和计算机组成。微通道板检测器检测到的离子信号经过放大器放大20倍后,再用多通道数据采集卡(P7888,德国Fast ComTech公司)进行采集,每次采集时间为10 s。每次实验都会测量3次来保证数据的可重复性。
-
气态苯是一种常见的室内室外污染物,具有较大的光电离截面,常被用来表征光电离质谱的检测灵敏度,因此,本研究使用苯标准蒸汽测试仪器的灵敏度及检出限。用二氯甲烷将纯苯稀释416倍,制备成苯标准溶液。用微量进样器取1 μL苯溶液,注入到气体标定腔内,待挥发完全,经风扇混匀后,得到体积分数为10×10−9的气相苯。在灵敏度实验中,通过注入的次数来控制气体标定腔内苯的气体体积分数。
-
光通量是通过固定在距离灯出口73 mm处镀金的铜板测量的。将一个导流针放在金板的正上方,处于金板和灯之间并靠近金板的位置。当给导流针施加一个正直流电压时,导流针可以引导光电子离开镀金铜板表面,通过连接镀金铜板的皮安表(Keithley Instruments公司,6485型)可以测出此时产生的光电流。光电流转化成光子通量的计算方法如式(1)所示。
式中:Ф为单位面积内的光子通量,s−1·cm−2;Q为基本电荷,其数值为1.6×10−19 C;ε为光电子产率,数值为0.063;S为电离区入口的横截面积,cm2。
-
农药行业是异味污染的主要贡献者,特别是在废弃农药污染场地的修复再利用过程中,非常容易引起异味投诉。在本研究中,使用125 L的静态通量箱收集某废弃农药污染场地地面释放的异味气体0.5 h后,使用0.5 L的特氟龙袋采样,采用SPI-TOFMS对气袋内的VOCs进行直接检测。同时,将相同的静态通量箱内的气体用苏玛罐采样后,使用P&T GC-MS按照USEPA TO15-1999标准方法进行检测,将2种分析方法的结果进行对比分析[42]。
-
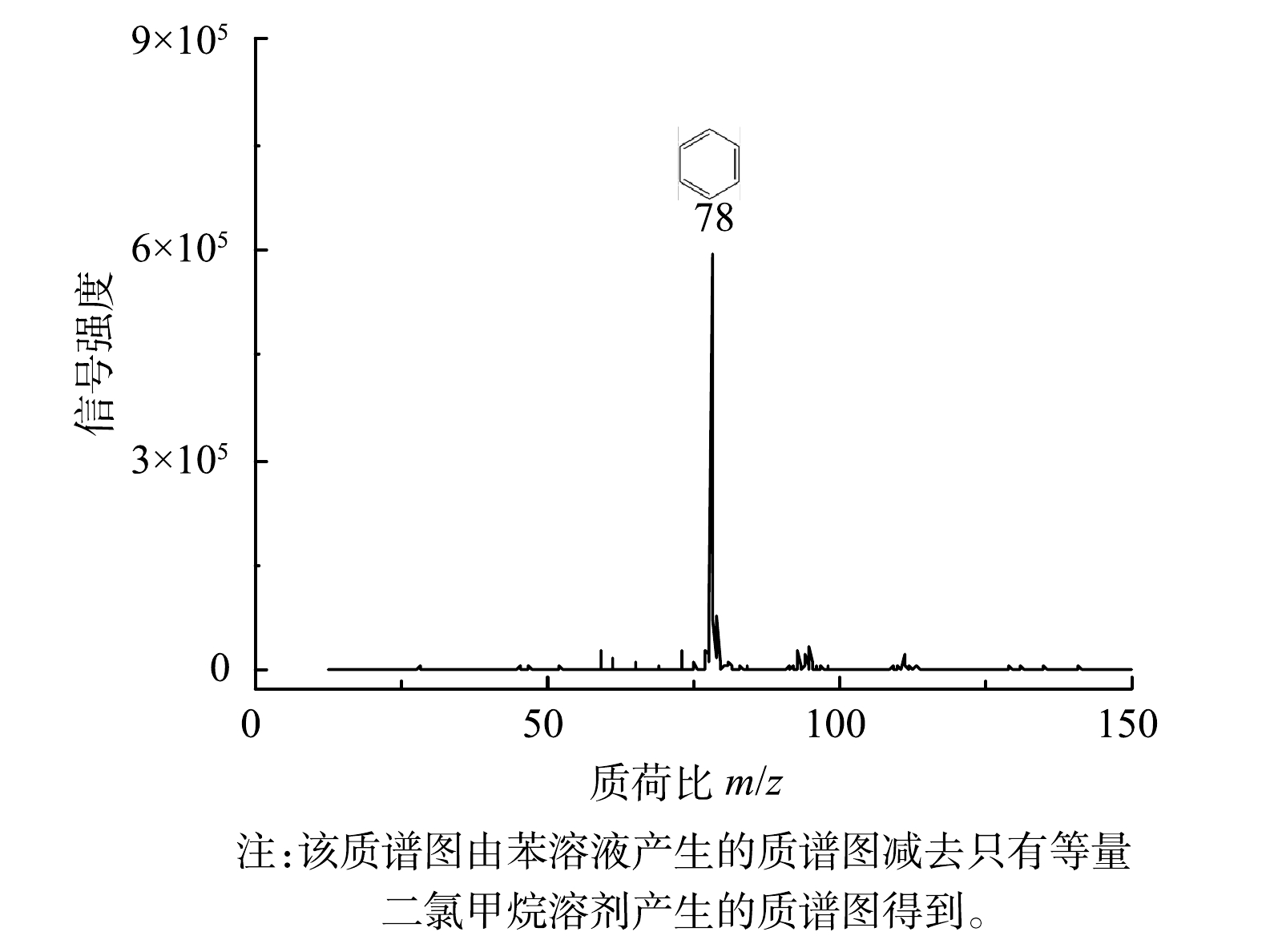
图4显示的是体积分数为10×10−9的苯在氮气中的SPI-TOFMS质谱图。由于配制苯标准溶液使用的溶剂是二氯甲烷,而当二氯甲烷存在时,SPI离子源内会产生大量的水合质子(H3O+)及其团簇离子((H2O)2H+、(H2O)3H+和(H2O)4H+),因此,为了得到简明的待测物质谱图,往往需要用待测物/二氯甲烷的质谱图减去等量纯二氯甲烷的质谱图(质谱背景)。由图4可以看出,减去二氯甲烷引起的质谱背景后,苯的SPI质谱图中只有m/z=78的母离子峰为主要特征峰。
-
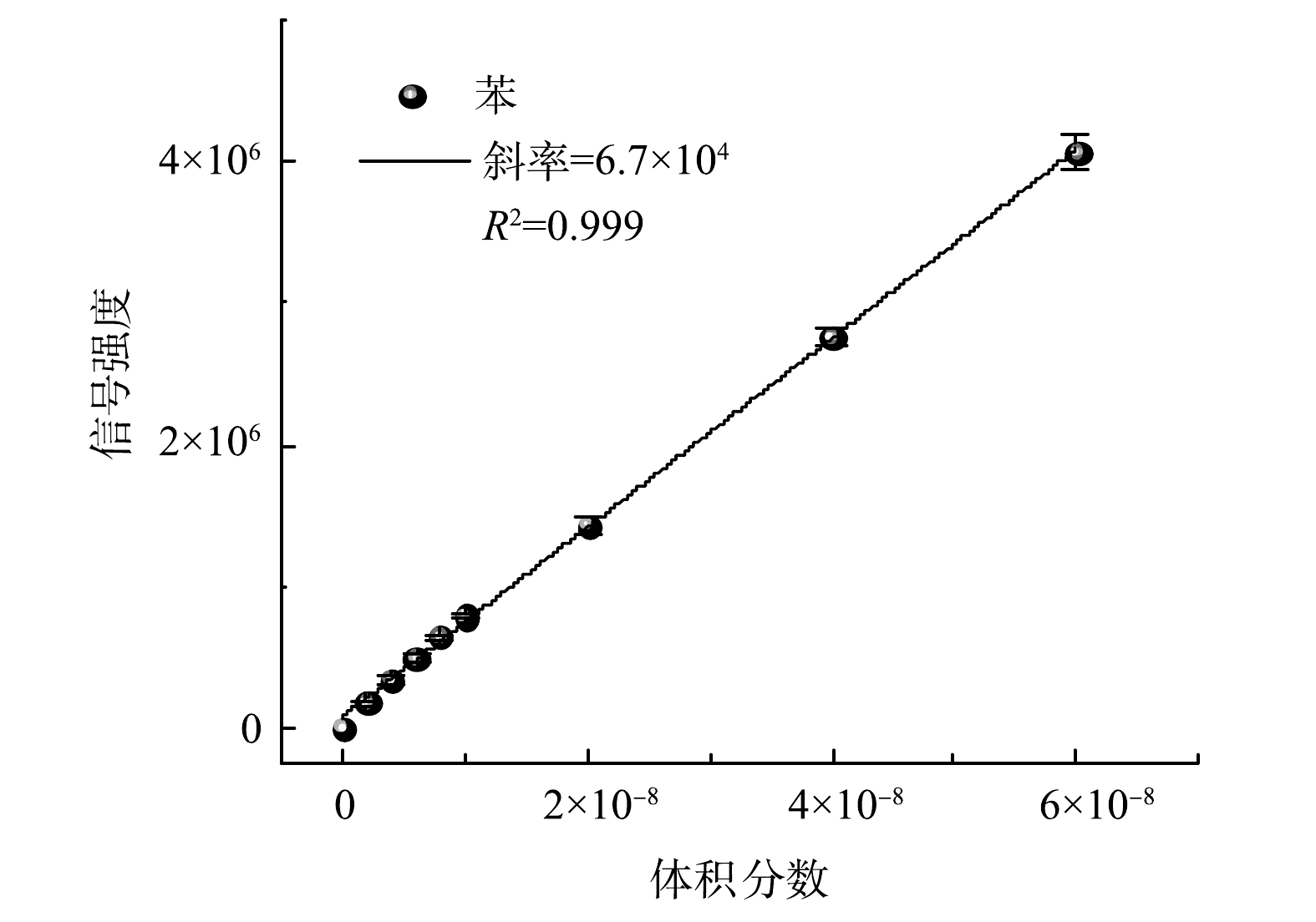
使用气体标定腔配制不同体积分数的苯,使用SPI-TOFMS获得不同体积分数下苯的信号强度。对分子离子信号强度(m/z=78)与气相苯的体积分数进行线性拟合,得到苯的灵敏度校正曲线。如图5所示,在体积分数为2×10−9~60×10−9时,线性拟合曲线的线性较好(R2=0.999)。由线性拟合的斜率可计算得到SPI-TOFMS对苯的检测灵敏度:体积分数为10−12的苯对应的信号强度为67±0.70(10 s检测时间)。目前已有研究[43]报道的灵敏度最高的PTR-MS对苯的检测灵敏度:体积分数为10−12的苯对应的信号强度为7左右(1 s检测时间)。因此,本文报道的紧凑型高灵敏SPI-TOFMS对苯的检测灵敏度与灵敏度最高的PTR-MS相当,且明显优于同类型SPI-MS。SPI-TOFMS对苯的检测限(LOD)的计算方法见式(2)。
式中:L为检测限;σ为质谱信号背景噪声的标准偏差,其数值为2.2;s为检测灵敏度。
在10 s采集时间内,仪器对苯的检测限(以体积分数计)为(0.09±0.00)×10−12。值得注意的是,SPI-TOFMS具有非常高的检测灵敏度,因此,在检测高浓度有机物时,因到达离子检测器的离子量过大,逐渐超出离子检测器对信号的线性响应范围,则信号强度与待测物浓度之间的线性度会有所下降(如本仪器对体积分数超过60×10−9的苯的线性度有所下降)。因此,该质谱技术适宜对环境空气中的低浓度痕量有机污染物进行在线监测。如果监测高浓度有机污染物,则需要预先对气体样品进行稀释处理,或者改变质谱内离子的迁移电压,人为降低仪器的检测灵敏度。
-
在本研究中,准确度表示在3次平行实验中,苯的3次测量值与其平均值的比值。为了方便讨论,本研究选取3个比值中与100%差值最大的一个数值作为准确度;精确度表示苯的3次测量值的标准偏差。如表1所示,由SPI-TOFMS对体积分数为2×10−9~60×10−9的苯的检测结果可以得出,在此体积分数范围内,SPI-TOFMS对苯的检测准确度为95%~109%;精确度的标准偏差总体上小于8%。由此可知,SPI-TOFMS在VOCs的直接在线检测方面具有良好的可靠性。
-
某农药污染场地释放的异味气体样品的SPI-TOFMS质谱图如图6所示,P&T GC-MS检测得到的化学组分如表2所示。可以看出,除了相对分子质量为26的乙炔,P&T GC-MS检测到的所有物质的相对分子质量(图6中以星号标记的质量峰)都能在SPI-TOFMS质谱图中看到。另外,除了P&T GC-MS检测到的这些质量峰外,在SPI-TOFMS质谱图中,还能观察到大量其他质量峰(除星号标记以外的质量峰),这些质量峰主要为未被P&T GC-MS检测到的物质。
结合农药企业的原料和产品信息,将SPI-TOFMS质谱(图6)中观察到的m/z为48、62、76、94和126的质量峰归为挥发性有机硫化合物。这些有机硫化合物分别为甲硫醇(m/z=48)、二甲基硫(m/z=62)、乙硫醇(m/z=62)、甲基乙基硫(m/z=76)、二甲基二硫(m/z=94)和二甲基三硫(m/z=126)。在这些可能的有机硫化合物中,只有二甲基二硫在P&T GC-MS中具有100%的检出率,二甲基二硫也是该农药污染地块释放的主要有机污染物。此外,还有一些含氮的异味物质没有被P&T GC-MS检测到。根据农药企业的原料和产品信息,将m/z为69、79、87、93、108和123的质谱峰归为吡咯烷、吡啶、乙基丙胺、苯胺、邻苯二胺和硝基苯。
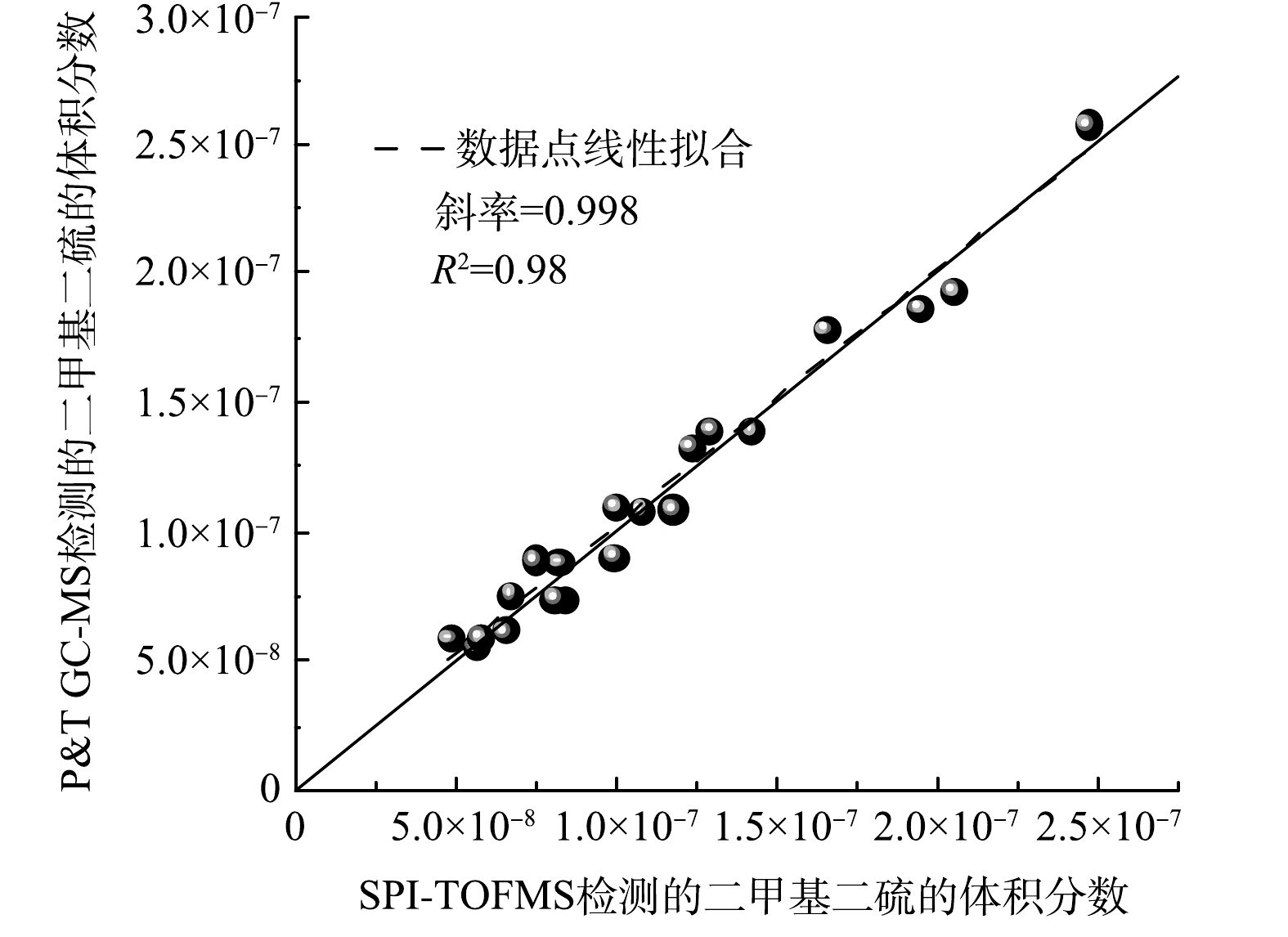
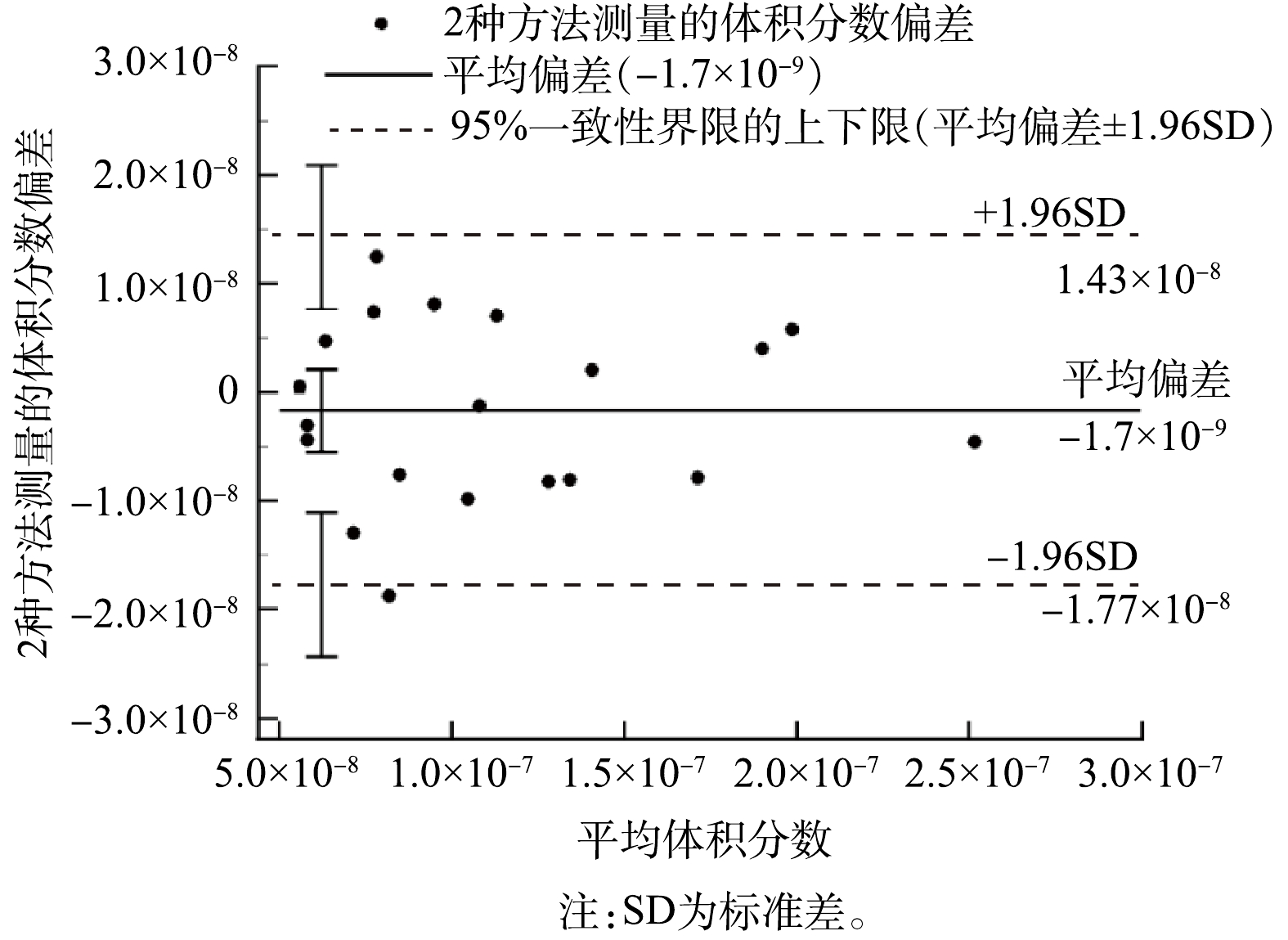
为了评价SPI-TOFMS的定量能力,分别用SPI-TOFMS和P&T GC-MS测定了20组体积分数为56×10−9~246×10−9的二甲基二硫样品。如图7所示,2种检测方法得到的二甲基二硫的体积分数呈良好的线性关系,斜率为0.998,R2=0.98。2种方法的一致性可通过Bland-Altman分析方法来评估[44-45]。如图8所示,SPI-TOFMS和P&T GC-MS分别测定的二甲基二硫体积分数在此范围内有较小的负偏差(−1.7×10−9),标准差(SD)为8.16×10−9,95%的一致性界限(平均偏差±1.96SD)为−17.7×10−9~14.3×10−9。这说明SPI-TOFMS与P&T GC-MS标准方法的定量结果具有较好的一致性,但相比之下,SPI-TOFMS的分析时间要短得多。这些结果表明,高灵敏SPI-TOFMS有助于快速、全面地筛查复杂的异味气体的化学组成和浓度范围,从而对国标方法难以检测的未知物质做进一步分析,最终获得异味气体所有组分信息。
-
1) 本研究研制的紧凑型高灵敏SPI-TOFMS可作为车载式仪器,直接、在线监测外场环境空气中的痕量VOCs。在10 s的检测时间内,该仪器对苯的检测限(以体积分数计)为0.09×10−12。
2) SPI-TOFMS对不同体积分数(2×10−9~60×10−9)的苯的检测准确度为95%~109%,检测精确度的标准偏差总体小于8%,表现出较好的检测稳定性和可靠性。
3) 在农药污染场地异味气体分析中,SPI-TOFMS可以在10 s的检测时间内检测到更多P&T GC-MS标准方法未能检测到的异味物质;SPI-TOFMS与P&T GC-MS 2种方法对异味样品主要成分(二甲基二硫)的定量分析结果具有良好的一致性。
紧凑型高灵敏真空紫外单光子电离飞行时间质谱仪的研制及其在污染场地异味分析中的应用
Development of a compact and highly sensitive vacuum ultraviolet single-photon-ionization time-of-flight mass spectrometer and its application in odorous analysis of a contaminated site
-
摘要: 真空紫外单光子电离质谱仪(SPI-MS)在挥发性有机物(VOCs)在线监测方面具有独特优势,然而目前常用的SPI-MS灵敏度普遍较低,限制了SPI-MS在环境监测领域的广泛应用。为了有效提高SPI-MS的检测灵敏度,达到实时在线监测环境中痕量VOCs的目的,采用自制的高通量真空紫外灯,结合低气压光电离技术和飞行时间质谱技术,研制了1台紧凑型高灵敏真空紫外单光子电离飞行时间质谱仪(SPI-TOFMS),并使用SPI-TOFMS和吹扫捕集气相色谱质谱(P&T GC-MS)标准方法对农药污染场地释放的异味气体进行了检测分析。结果表明:在10 s的检测时间内,该仪器对气态苯具有极高的检测灵敏度,检测限(以体积分数计)低至0.09×10−12,检测准确度为95%~109%,精确度的标准偏差小于8%;在农药场地异味气体分析中,SPI-TOFMS不仅在极短的检测时间内(10 s)检测到甲硫醇、二甲基硫和二甲基二硫等典型异味物质,还检测到更多未被P&T GC-MS标准方法检测到的异味物质,如吡咯烷、吡啶、乙基丙胺、苯胺、邻苯二胺和硝基苯等;SPI-TOFMS与P&T GC-MS 2种方法对异味样品主要成分(二甲基二硫)的定量分析结果具有良好的一致性。本研究研制的紧凑型SPI-TOFMS与同类型仪器相比,检测灵敏度有了大幅提高,可为实验室模拟研究及外场环境中痕量VOCs的实时在线监测提供一种高效的技术方法。Abstract: Vacuum ultraviolet single photon ionization mass spectrometer (SPI-MS) has unique advantages in on-line monitoring of volatile organic compounds (VOCs). However, the low sensitivity of the commonly used SPI-MS limits its wide application in environmental monitoring. In order to effectively improve the detection sensitivity of SPI-MS and realize the goal of real-time online monitoring of trace VOCs in the environment, a compact and highly sensitive vacuum ultraviolet single-photon-ionization time-of-flight mass spectrometer (SPI-TOFMS) was developed using a high-flux vacuum ultraviolet lamp combining with low-pressure photoionization technology and compact time-of-flight mass spectrometry. Then the SPI-TOFMS and purge-and-trap gas chromatography-mass spectrometry (P&T GC-MS) standard methods were used to analyze the gas phase samples of odorous substances released from the same pesticide site. The results show that the instrument exhibited an extremely high detection sensitivity toward gaseous benzene, the detection limit (in terms of volume ratio) was as low as 0.09 × 10−12 in 10 s acquisition time, the detection accuracy was 95%~109% with standard deviations less than 8%. In the analysis of odorous gas released from a pesticide site, the SPI-TOFMS could not only detect methanethiol, dimethyl sulfur, and dimethyl disulfide in a very short detection time (10 s), but also detect more odorous that cannot be detected by P&T GC-MS standard method, such as pyrrolidine, pyridine, ethyl propyl amine, aniline, o-phenylenediamine, and nitrobenzene. The SPI-TOFMS and P&T GC-MS had a good agreement on the quantitative analysis results of the main component of the odor substances (dimethyl disulfide) in the odor samples. The compact SPI-TOFMS developed in this study has a much higher detection sensitivity compared with other analogue instruments, which can provide an efficient technical method for laboratory simulation and real-time online monitoring of trace VOCs in the field environment monitoring.
-
铝盐类混凝剂在饮用水净化过程中的残余问题一直是混凝工艺面临的技术难题,受到广泛关注。过量摄入的铝会在人体中积累残留,从而形成一些潜在的健康问题,如引发阿尔茨海默症、导致体细胞及生殖细胞发生突变等[1-3]。
在水质净化过程中,经铝盐混凝处理后水中铝的含量会明显升高[4-5]。有研究[6]发现,溶解态铝是饮用水中总残余铝的主要组成部分。混凝剂容易以溶解态的单体或小聚合体的形式与溶解性有机物(DOM)中的羧基、酚基类活性基团络合形成有机络合态的铝,不易通过沉降、过滤等后续工艺去除而残留在饮用水中,该机理被认为是溶解性残余铝的主要成因[7-9]。铁盐也是一种常用混凝剂[10],其价格便宜,矾花易沉降,对DOM也有较好的去除效果[11]。但是铁盐过量使用可能造成出水的感官污染,而且极易腐蚀设备[12]。铁-铝盐混凝剂混合投加是在保证水质的同时,减少铝盐类混凝剂投加量和残余铝的常用工艺。
混凝过程非常复杂,不同种类的混凝剂对DOM中不同组分的去除能力存在差异,影响其分子量分布及特性[10]。此外,在铁-铝盐混合投加时,Fe3+离子同样可以与DOM中的羧基、酚基络合形成有机态的铁,Fe3+、Al3之间会形成竞争作用相互影响[13-15]。由于缺乏有效的表征手段,对混凝环境条件下DOM特性的变化以及其与Al3+、Fe3+之间相互作用机理认识不清,影响了工程应用。
最近的研究发现,可以用紫外-可见光谱法定量表征天然环境条件下DOM的水化学特性变化规律,结合非理想竞争吸附模型(NICA),可以从酸碱滴定过程中紫外-可见差分光谱参数(如DlnA400)的变化获得DOM中羧基、酚基类官能团数量、化学反应平衡常数等定量信息[16-18]。
本研究通过中试实验,在考察使用聚合氯化铝(PACl)和三氯化铁(FeCl3)不同混凝剂投加方案下的水质净化效果及在铝残余量的基础上,利用紫外-可见光谱法,揭示DOM的去除特性及残余铝形成与调控机制。为实际工程生产中的残余铝控制提供新的视角和理论指导。
1. 实验部分
1.1 中试实验
中试系统由混合池、混凝反应池、斜管沉淀池和石英砂滤池组成,设计流量为1 m3·h−1。原水通过增压泵被提升至混合池,与通过计量泵投加的混凝剂混合,混合池转速为300 r·min−1,停留时间为5 min。混合后原水进入混凝反应池中,池内设三级搅拌桨,转速分别为250、150、50 r·min−1,每级停留时间6.5 min。混凝出水进入斜管沉淀池,停留时间为40 min后进入石英砂滤池,滤池设计流速为10 m·h−1。
实验原水为中国北方某大型水厂水源。实验期间原水水质:浊度为1.314~1.865 NTU,pH为 8.10~8.38,DOC为 2.46~2.82 mg·L−1,UV254为 0.026 1~0.030 7 cm−1,溶解性残余铝为0 μg·L−1,溶解性残余铁为0 μg·L−1。
重点考察原水和滤池出水水质。浊度和pH分别采用浊度计(Hach turbidimeter 2100P)和pH计(Mettler Toledo S210 Seven Compact)测量。水样经过孔径为0.45 μm的微滤膜过滤后,溶解性有机碳(DOC)由碳分析仪(Shimadzu TOC-Vcsh)来测定;溶解性铝、铁浓度用电感耦合等离子体质谱仪(Element X Series,Thermo Scientific)测定;紫外-可见分光光谱采用紫外-可见分光光度计(Hitachi U-3900)测定。
1.2 试剂与药品
所用化学品均为试剂级,除非特别说明。所有溶液均使用Milli-Q水(18.2 MU,Millipore Corp,MA,USA)制备。混凝剂聚合氯化铝(PACl,Al2O3含量约为10%)、三氯化铁(FeCl3,总Fe含量约为40%)均为商用产品,由当地一家工厂(中国北京万水净水剂有限公司)提供。
1.3 光谱滴定方法
100 mL水样经孔径为0.45 μm的膜过滤去除水样中颗粒物后,利用阳离子交换树脂去除水样中的Ca2+、Mg2+等背景金属阳离子。利用HClO4将水样酸化至pH 3室温保存30 min。向样品中逐步滴加0.1 mol·L−1的NaOH使水样pH缓慢升高,在pH为 3~11内以0.5个pH为间隔(误差为 −0.05~0.05)取少量样品进行紫外-可见光光谱扫描,测量波长为200~600 nm。
1.4 数据处理
DOM的紫外-可见光谱滴定数据分析采用文献中的方法[17-18]。利用式(1)和式(2)分别计算线性差分光谱和差分对数转换光谱参数。
D(Aλ)=Aλ,i−Aλ,ref (1) D(lnAλ)=lnAλ,i−lnAλ,ref (2) 式中:D(Aλ)为线性差分光谱;D(lnAλ)为差分光谱对数转换光谱参数;Aλ, i为选定实验条件(i)在波长λ处测量的DOM吸光度;Aλ, ref为参考光谱在波长λ处测量的DOM吸光度(通常为pH=3时)。
光谱参数DlnA400通过式(2)计算后与修正的NICA模型结合,利用式(3)拟合定量DOM水解(脱质子)引起的光谱参数的变化规律。
D(lnAλ)=[D(lnAHAS)1+(pKHAS[H+])mHAS+D(lnALAS)1+(pKLAS[H+])mLAS]−[D(lnAHAS)1+(pKHAS[H+]ref)mHAS+D(lnALAS)1+(pKLAS[H+]ref)mLAS] (3) 式中:D(lnALAS)和D(lnAHAS)分别对应在波长λ处羧基类和酚基类官能团水解(脱质子)引起的吸光度最大变化,这2类官能团分别为低亲和质子活性位点(LAS)和高亲和质子活性位点(HAS);pKHAS和pKLAS是水解平衡常数;mLAS和mHAS为平衡常数的分布宽度指数[16-19]。值得指出的是,D(lnALAS)和D(lnAHAS)的数值代表单位水体中1 mg的DOC所含活性官能团的数量[16-19]。
2. 结果与讨论
2.1 不同混凝剂投加量下的水处理效果
本节研究了单独使用混凝剂PACl在低、中、高3种剂量(0.04、0.08、0.12 mmol·L−1,以Al3+计)时,以及同时投加0.01、0.02、0.03、0.04、0.05 mmol·L−1 (以Fe3+计,下同)FeCl3进行铁-铝盐混合混凝时的水质变化。滤池出水的浊度、DOC、溶解性残余铝和铁的浓度如图1所示。
当单独使用PACl时,DOC和浊度的去除效果随着铝盐投加量增加逐渐增加,在低、中、高3种剂量下,DOC去除率逐渐升高,分别为15.0%、25.4%、36.6% (原水DOC为2.66 mg·L−1),浊度分别为0.216、0.206、0.115 NTU (原水浊度为1.580 NTU);溶解性残余铝浓度轻微降低,分别为131、119、105 μg·L−1。
同时投加PACl和FeCl3时,DOC的去除效果会进一步提升,浊度去除效果有轻微改善,溶解性残余铝的浓度会随FeCl3投加量增加显著降低。由图1(a)和图1(b)中的数据可以看出,当铁-铝盐混合投加使用时,0.08 mmol·L−1 PACl + 0.03 mmol·L−1 FeCl3、0.04 mmol·L−1 PACl + 0.05 mmol·L−1 FeCl3这2种投加方案下的浊度和DOC去除效果均达到或超过单独使用高投加量的PACl时的水平。从图1(c)和图1(d)可知,在将混凝剂混合投加后,溶解性残余铝浓度显著降低,由PACl单独混凝的滤池出水中残余铝为105 μg·L−1分别降低到41 μg·L−1和21 μg·L−1;在不使用混凝剂FeCl3时,滤池出水中溶解性铁含量很低(<5 μg·L−1),当混凝剂FeCl3投加后溶解性铁浓度显著升高。
2.2 FeCl3对DOM特性的影响
为了探究DOM的特性与溶解性残余铝的内在联系,对水样进行紫外-可见光谱酸碱滴定。利用式(2)计算光谱参数D(lnA400),结合修正后的NICA模型拟合定量DOM水解(脱质子)引起的D(lnA400)光谱参数的变化规律,部分结果如图2所示。
不同混凝剂投加方案下的滤池出水对应的NICA模型拟合参数和DOM所含官能团计算结果如表1所示。通常使用CDOC·D(lnALAS)、CDOC·D(lnAHAS)的值分别计算单位水体中DOM含有的羧基类、酚基类官能团总量[16-18]。
表 1 不同混凝剂投加方案下滤池出水中DOM所含活性官能团计算结果Table 1. NICA model parameters of filtered water at different coagulant dosing schemesPACl/(mmol·L−1) FeCl3/(mmol·L−1) DOC/(mg·L−1) D(lnALAS) D(lnAHAS) mLAS mHAS pKLAS pKHAS R2 羧基类官能团总量 酚基类官能团总量 0 0 2.66 0.562 0.549 1.972 4.998 3.503 9.500 0.995 1.492 1.463 0.04 0 2.26 0.618 0.613 2.121 3.002 3.496 9.406 0.993 1.401 1.379 0.01 1.94 0.763 0.598 1.881 2.510 3.002 9.520 0.999 1.474 1.164 0.03 1.84 0.814 0.566 2.500 2.823 3.500 9.005 0.987 1.490 1.049 0.05 1.69 0.821 0.560 1.850 3.020 3.490 9.989 0.995 1.386 0.946 0.08 0 1.97 0.705 0.695 1.647 2.987 3.505 9.310 0.998 1.399 1.359 0.01 1.87 0.767 0.602 3.003 4.596 3.992 9.906 0.984 1.440 1.141 0.03 1.69 0.937 0.573 1.950 3.200 3.455 9.620 0.991 1.589 0.963 0.05 1.60 0.887 0.549 2.203 3.709 3.997 10.000 0.995 1.419 0.880 0.12 0 1.70 0.811 0.730 1.724 3.121 3.508 9.899 0.990 1.377 1.241 0.01 1.65 0.802 0.687 1.955 4.088 3.900 9.595 0.989 1.320 1.139 0.03 1.56 0.817 0.713 1.907 3.854 3.557 9.200 0.994 1.279 1.108 0.05 1.51 0.926 0.541 2.456 2.883 3.798 9.857 0.996 1.398 0.817 注:PACl和FeCl3的投加量均为0 mmol·L−1时即原水。 由表1可知,在单独使用铝盐混凝的过程中,随着PACl投加量的增加,活性官能团总量相较于原水不断减少。在高PACl投加量下,羧基类官能团总量累计减少约13.3%,酚基类官能团总量累计减少9.4%。
同时投加FeCl3时会使DOM中活性官能团总量进一步减少,其中羧基类官能团总量变化规律并不明显,酚基类官能团总量下降显著。在FeCl3的投加量为0.05 mmol·L−1时,低、中、高PACl投加量下酚基类官能团总量较未投加FeCl3时分别减少约31.4%、35.3%、38.4%。
将不同混凝剂投加条件下滤池出水中溶解性残余铝浓度与DOM中活性官能团总量作比较,结果如图3所示。滤池出水中的溶解性残余铝浓度与DOM中活性官能团总量相关(
R2总 =0.73),其中与酚基类官能团总量关系尤为密切(R2酚基 =0.85)。结合表1结果,可以推测正是由于FeCl3的加入改变了DOM特性及活性官能团总量,尤其是大幅减少了酚基类活性官能团总量,从而使溶解性残余铝浓度降低。2.3 Fe3+与Al3+竞争机制
为了进一步验证上述推测,探究Al3+与Fe3+和DOM络合时的竞争机制,分别用检测的铝、铁浓度和活性官能团总量之比表示不同混凝剂使用条件下产水中单位数量活性官能团络合的铝、铁的浓度,结果如图4所示。可以看出,单位数量活性官能团络合的铁浓度随着FeCl3的加入大幅上升,而单位数量活性官能团络合的铝浓度均随着FeCl3的加入显著下降,FeCl3强烈抑制了Al3+与DOM的络合,FeCl3剂量越高,抑制作用越明显。
由于目前尚没有方法能直接测量混凝条件下有机络合态铝、铁的浓度,使用水化学模型软件Visual Minteq 3.1(https://vminteq.lwr.kth.se/download/),基于NICA-Donnan模型[20]预测Fe3+、Al3+离子与腐殖酸(humic, HA)的络合分配机制。不同Al3+、Fe3+投加量下活性官能团络合的铝、铁浓度的模拟计算结果如图5所示。由于实际水源中DOM与HA的特性存在显著差异,而且混凝过程中Fe3+、Al3+离子易水解产生沉淀,模型计算时参数设置与实际混凝环境存在较大差异,仅提供了较低浓度条件下的计算数据作为参考。该结果也表明,DOM与Al3+、Fe3+的络合物中,酚基络合态的铝、铁是主要组成部分,其浓度远高于羧基络合态和静电层中的铝和铁,占总络合态铝、铁的比率均超过了77%;DOM对Fe3+的络合能力要显著强于Al3+,相同Fe3+、Al3+总浓度下Fe3+络合量是Al3+的2倍以上;在Fe3+、Al3+共存时,Fe3+强烈抑制了Al3+与DOM的络合过程,Fe3+投加量越大,抑制作用越明显,而Al3+对Fe3+与DOM络合过程影响较轻微。模型计算结果与实验结果基本一致。
3. 结论
1)铁-铝盐混凝剂混合投加工艺可以显著降低滤池出水的溶解性残余铝含量,同时能在减少混凝剂总使用量的情况下保证水处理效能。
2)溶解性残余铝与DOM的特性及活性官能团含量密切相关,尤其是酚基类官能团总量。在铁-铝盐混合投加时,FeCl3能显著提高酚基类官能团的去除效率,降低了滤池出水中溶解性残余铝的浓度。
3) Fe3+与DOM的络合能力显著强于Al3+。投加铁盐后,通过竞争络合位点,明显抑制了络合态有机铝的形成,而Al3+对Fe3与+DOM之间的络合过程影响轻微。
-
表 1 SPI-TOFMS对苯在不同体积分数下的精准度和准确度
Table 1. Accuracy and precision of SPI-TOFMS against benzene at different volume fractions
体积分数 准确度/% 精确度/% 2×10-9 95 5 4×10-9 109 8 6×10-9 95 4 8×10-9 104 3 10×10-9 98 2 20×10-9 96 4 40×10-9 102 2 60×10-9 97 3 表 2 P&T GC-MS检测的异味气体的化学组分
Table 2. List of the chemical composition of odorous gas identified by P&T GC-MS
序号 停留时间/min 化合物 相对分子质量 定量结果(以体积分数计) 1 17.721 丙酮 58.08 13.2×10−9 2 23.538 2-丁酮 72.11 3.65×10−9 3 20.850 二硫化碳 76.14 2.57×10−9 4 32.731 甲苯 92.14 1.54×10−9 5 36.910 乙苯 106.17 1.50×10−9 6 37.274 对二甲苯 106.17 7.71×10−9 7 38.254 邻二甲苯 106.17 2.43×10−9 8 18.274 三氯氟甲烷 137.37 0.863×10−9 9 20.265 二氯甲烷 84.93 19.2×10−9 10 29.464 三氯乙烯 131.39 2.47 × 10−9 11 34.862 四氯乙烯 165.82 97.1×10−9 12 14.753 丙烷 44.1 3.87×10−9 13 24.885 正己烷 86.18 3.19×10−9 14 34.422 正辛烷 114.23 1.21 × 10−9 15 38.560 壬烷 128.26 2.51 × 10−9 16 42.473 正癸烷 142.29 1.21 × 10−9 17 25.004 三氯甲烷 119.38 21.5×10−9 18 13.564 乙烷 30.07 1.70×10−9 19 22.470 乙炔 26.04 2.61×10−9 20 14.019 乙烯 28.06 1.75×10−9 21 19.815 二甲基硫 62.13 8.29×10−9 22 31.470 二甲基二硫 94.2 84.6×10−9 -
[1] GOUW J D, WARNEKE C. Measurements of volatile organic compounds in the earth’s atmosphere using proton-transfer-reaction mass spectrometry[J]. Mass Spectrometry Reviews, 2007, 26(2): 223-257. doi: 10.1002/mas.20119 [2] LINDINGER W, HANSEL A, JORDAN A. On-line monitoring of volatile organic compounds at pptv levels by means of proton-transfer-reaction mass spectrometry (PTR-MS) medical applications, food control and environmental research[J]. International Journal of Mass Spectrometry and Ion Processes, 1998, 173(3): 191-241. doi: 10.1016/S0168-1176(97)00281-4 [3] JANG M, CZOSCHKE N M, LEE S, et al. Heterogeneous atmospheric aerosol production by acid-catalyzed particle-phase reactions[J]. Science, 2002, 298(5594): 814-817. doi: 10.1126/science.1075798 [4] JANG M, CZOSCHKE N M, NORTHCROSS A L. Atmospheric organic aerosol production by heterogeneous acid-catalyzed reactions[J]. Chemphyschem, 2004, 5(11): 1646-1661. doi: 10.1002/cphc.200301077 [5] TANSEL B, INANLOO B. Odor impact zones around landfills: Delineation based on atmospheric conditions and land use characteristics[J]. Waste Management, 2019, 88: 39-47. doi: 10.1016/j.wasman.2019.03.028 [6] JIN P, GU Y G, SHI X, et al. Non-negligible greenhouse gases from urban sewer system[J]. Biotechnology for Biofuels, 2019, 12(1): 1-11. doi: 10.1186/s13068-018-1346-y [7] NIE E, ZHENG G, GAO D, et al. Emission characteristics of VOCs and potential ozone formation from a full-scale sewage sludge composting plant[J]. Science of the Total Environment, 2019, 659: 664-672. doi: 10.1016/j.scitotenv.2018.12.404 [8] EWING R G, WALTMAN M J, ATKINSON D A, et al. The vapor pressures of explosives[J]. Trends in Analytical Chemistry, 2013, 42: 35-48. doi: 10.1016/j.trac.2012.09.010 [9] QIN M R, CHEN Z M, SHEN H Q, et al. Impacts of heterogeneous reactions to atmospheric peroxides: Observations and budget analysis study[J]. Atmospheric Environment, 2018, 183: 144-153. doi: 10.1016/j.atmosenv.2018.04.005 [10] ZIMMERMANN R. Photo ionisation in mass spectrometry: Light, selectivity and molecular ions[J]. Analytical and Bioanalytical Chemistry, 2013, 405(22): 6901-6905. doi: 10.1007/s00216-013-7187-4 [11] SYAGE J A, CAI S S, LI J W, et al. Direct sampling of chemical weapons in water by photoionization mass spectrometry[J]. Analytical Chemistry, 2006, 78(9): 2967-2976. doi: 10.1021/ac0518506 [12] TSURUGA S, SUZUKI T, TAKATSUDO Y, et al. On-line monitoring system of P5CDF homologues in waste incineration plants using VUV-SPI-IT-TOFMS[J]. Environmental Science and Technology, 2007, 41(10): 3684-3688. doi: 10.1021/es0614924 [13] SARAJI-BOZORGZAD M, GEISSLER R, STREIBEL T, et al. Thermogravimetry coupled to single photon ionization quadrupole mass spectrometry: A tool to investigate the chemical signature of thermal decomposition of polymeric materials[J]. Analytical Chemistry, 2008, 80(9): 3393-3403. doi: 10.1021/ac702599y [14] FISCHER M, WOHLFAHRT S, VARGA J, et al. Evolved gas analysis by single photon ionization-mass spectrometry[J]. Journal of Thermal Analysis and Calorimetry, 2014, 116(3): 1461-1469. doi: 10.1007/s10973-014-3830-3 [15] YUAN B, KOSS A, WARNEKE C, et al. A high-resolution time-of-flight chemical ionization mass spectrometer utilizing hydronium ions (H3O+ ToF-CIMS) for measurements of volatile organic compounds in the atmosphere[J]. Atmospheric Measurement Techniques, 2016, 9(6): 2735-2752. doi: 10.5194/amt-9-2735-2016 [16] BLAKE R S, PATEL M, MONKS P S, et al. Aldehyde and ketone discrimination and quantification using two-stage proton transfer reaction mass spectrometry[J]. International Journal of Mass Spectrometry, 2008, 278(1): 15-19. doi: 10.1016/j.ijms.2008.07.010 [17] HANSEL A, JORDAN A, HOLZINGER R, et al. Proton transfer reaction mass spectrometry: On-line trace gas analysis at the ppb level[J]. International Journal of Mass Spectrometry and Ion Processes, 1995, 149-150: 609-619. doi: 10.1016/0168-1176(95)04294-U [18] LINDINGER W, HANSEL A, JORDAN A. Proton-transfer-reaction mass spectrometry (PTR-MS): On-line monitoring of volatile organic compounds at pptv levels[J]. Chemical Society Reviews, 1998, 27(5): 347-354. doi: 10.1039/a827347z [19] SULZER P, HARTUNGEN E, HANEL G, et al. A proton transfer reaction-quadrupole interface time-of-flight mass spectrometer (PTR-QiTOF): High speed due to extreme sensitivity[J]. International Journal of Mass Spectrometry, 2014, 368: 1-5. doi: 10.1016/j.ijms.2014.05.004 [20] HANLEY L, ZIMMERMANN R. Light and molecular ions: The emergence of vacuum UV single-photon ionization in MS[J]. Analytical Chemistry, 2009, 81(11): 4174-4182. doi: 10.1021/ac8013675 [21] HUA L, WU Q H, HOU K Y, et al. Single photon ionization and chemical ionization combined ion source based on a vacuum ultraviolet lamp for orthogonal acceleration time-of-flight mass spectrometry[J]. Analytical Chemistry, 2011, 83(13): 5309-5316. doi: 10.1021/ac200742r [22] GIULIANI A, GIORGETTA J L, RICAUD J P, et al. Atmospheric pressure photoionization using tunable VUV synchrotron radiation[J]. Nuclear Instruments and Methods in Physics Research, Section B:Beam Interactions with Materials and Atoms, 2012, 279: 114-117. [23] YAKIMOV S A, KNYAZ'KOV D A, BOL'SHOVA T A, et al. Investigation of the effect of ethanol additives on the structure of low-pressure ethylene flames by photoionization mass spectrometry[J]. Combustion, Explosion and Shock Waves, 2012, 48(5): 609-619. doi: 10.1134/S0010508212050127 [24] MILOSAVLJEVIC A R, NICOLAS C, GIL J F, et al. VUV synchrotron radiation: A new activation technique for tandem mass spectrometry[J]. Journal of Synchrotron Radiation, 2012, 19(2): 174-178. doi: 10.1107/S0909049512001057 [25] ZHOU Z Y, GUO H J, QI F. Recent developments in synchrotron vacuum ultraviolet photoionization coupled to mass spectrometry[J]. Trends in Analytical Chemistry, 2011, 30(9): 1400-1409. doi: 10.1016/j.trac.2011.05.007 [26] MULLEN C, IRWIN A, POND B V, et al. Detection of explosives and explosives-related compounds by single photon laser ionization time-of-flight mass spectrometry[J]. Analytical Chemistry, 2006, 78(11): 3807-3814. doi: 10.1021/ac060190h [27] STREIBEL T, WEH J, MITSCHKE S, et al. Thermal desorption/pyrolysis coupled with photoionization time-of-flight mass spectrometry for the analysis of molecular organic compounds and oligomeric and polymeric fractions in urban particulate matter[J]. Analytical Chemistry, 2006, 78(15): 5354-5361. doi: 10.1021/ac060227y [28] VAIKKINEN A, HAAPALA M, KERSTEN H, et al. Comparison of direct and alternating current vacuum ultraviolet lamps in atmospheric pressure photoionization[J]. Analytical Chemistry, 2012, 84(3): 1408-1415. doi: 10.1021/ac2024574 [29] WU Q H, HUA L, HOU K Y, et al. A combined single photon ionization and photoelectron ionization source for orthogonal acceleration time-of-flight mass spectrometer[J]. International Journal of Mass Spectrometry, 2010, 295(1/2): 60-64. [30] CHEN P, HOU K Y, HUA L, et al. Quasi-trapping chemical ionization source based on a commercial VUV lamp for time-of-flight mass spectrometry[J]. Analytical Chemistry, 2014, 86(3): 1332-1336. doi: 10.1021/ac403132k [31] LI A, CHEN M Z, GUO W F, et al. Detection of polycyclic aromatic hydrocarbons in a soil sample with photon ionization technique[J]. Applied Mechanics and Materials, 2013, 271: 112-115. [32] MUHLBERGER F, WIESER J, MOROZOV A, et al. Single-photon ionization quadrupole mass spectrometry with an electron beam pumped excimer light source[J]. Analytical Chemistry, 2005, 77(7): 2218-2226. doi: 10.1021/ac048319f [33] MUHLBERGER F, STREIBEL T, WIESER J, et al. Single photon ionization time-of-flight mass spectrometry with a pulsed electron beam pumped excimer VUV lamp for on-line gas analysis: Setup and first results on cigarette smoke and human breath[J]. Analytical Chemistry, 2005, 77(22): 7408-7414. doi: 10.1021/ac051194+ [34] MUHLBERGER F, WIESER J, ULRICH A, et al. Single photon ionization (SPI) via incoherent VUV-excimer light: Robust and compact time-of-flight mass spectrometer for on-line, real-time process gas analysis[J]. Analytical Chemistry, 2002, 74(15): 3790-3801. doi: 10.1021/ac0200825 [35] MUHLBERGER F, SARAJI-BOZORGZAD M, GONIN M, et al. Compact ultrafast orthogonal acceleration time-of-flight mass spectrometer for on-line gas analysis by electron impact ionization and soft single photon ionization using an electron beam pumped rare gas excimer lamp as VUV-light source[J]. Analytical Chemistry, 2007, 79(21): 8118-8124. doi: 10.1021/ac071217f [36] WANG Y, JIANG J C, HUA L, et al. High-pressure photon ionization source for TOFMS and its application for online breath analysis[J]. Analytical Chemistry, 2016, 88(18): 9047-9055. doi: 10.1021/acs.analchem.6b01707 [37] WAN N B, JIANG J C, HU F, et al. Nonuniform electric field-enhanced in-source declustering in high-pressure photoionization/photoionization-induced chemical ionization mass spectrometry for operando catalytic reaction monitoring[J]. Analytical Chemistry, 2021, 93(4): 2207-2214. doi: 10.1021/acs.analchem.0c04081 [38] LIU C Y, ZHU Y N, ZHOU Z Y, et al. Ultrasonic nebulization extraction/low pressure photoionization mass spectrometry for direct analysis of chemicals in matrices[J]. Analytica Chimica Acta, 2015, 891: 203-210. doi: 10.1016/j.aca.2015.08.010 [39] ZHU Z X, WANG J, QIU K Q, et al. Note: A novel vacuum ultraviolet light source assembly with aluminum-coated electrodes for enhancing the ionization efficiency of photoionization mass spectrometry[J]. Review of Scientific Instruments, 2014, 85(4): 046110. doi: 10.1063/1.4871796 [40] SUN W Q, SHU J N, ZHANG P, et al. Real-time monitoring of trace-level VOCs by an ultrasensitive lamp-based VUV photoionization mass spectrometer[J]. Atmospheric Measurement Techniques, 2015, 8(11): 4637-4643. doi: 10.5194/amt-8-4637-2015 [41] LI Z, XU C, SHU J N. Detection of sub-pptv benzene, toluene, and ethylbenzene via low-pressure photoionization mass spectrometry[J]. Analytica Chimica Acta, 2017, 964: 134-141. doi: 10.1016/j.aca.2017.01.065 [42] U. S. EPA. Method TO-15: Determination of volatile organic compounds in air collected in specially-prepared canisters ans analysed by gas chromatography mass spectrometry (GC/MS)[S]. U. S. EPA, 1999. [43] KRECHMER J, LOPEZ-HILFIKER F, KOSS A, et al. Evaluation of a new reagent-ion source and focusing ion-molecule reactor for use in proton-transfer-reaction mass spectrometry[J]. Analytical Chemistry, 2018, 90(20): 12011-12018. doi: 10.1021/acs.analchem.8b02641 [44] COWLEY N J, LAITENBERGER P, LIU B, et al. Evaluation of a new analyser for rapid measurement of blood propofol concentration during cardiac surgery[J]. Anaesthesia, 2012, 67(8): 870-874. doi: 10.1111/j.1365-2044.2012.07151.x [45] XIAO Y, WANG X, LI E Y, et al. Rapid determination of intraoperative blood propofol concentration in operating theatre by dopant-enhanced neutral release and negative photoionization ion mobility spectrometry[J]. Analytica Chimica Acta, 2020, 1098: 47-55. doi: 10.1016/j.aca.2019.11.011 -





 下载:
下载: