-
近年来,环渤海三省一市实施了大规模围填海,造成滨海滩涂湿地面积大幅锐减,水鸟生存空间被严重压缩,在此停歇、繁殖的水鸟种群数量呈下降趋势[1-2]。为扭转这一局面,我国各级政府也在积极开展针对滨海水鸟的湿地重建工作[3-6]。水生生物群落重建是湿地重建工程的重要内容,同时也是水鸟群落恢复的关键影响要素。科学、准确地评估水生生物重建效果是调整和改进重建方案的重要手段,对湿地生态重建实践具有重要指导意义[7-8]。然而,目前针对围海造陆区水生生物重建效果的评估研究相对较少,缺乏对重建成效和趋势的直观了解与判断[9]。
2019—2020年,天津港保税区临港经济区规划建设了临港湿地二期工程,除设计表流湿地外,还增设了生境恢复单元,通过物理生境改造和水生生物群落快速重建等措施,不仅构建了水鸟栖息觅食空间,还重建了鱼类、底栖动物等鸟类藉以生存的食物资源[1,5]。该工程一经建成,就吸引了数十种水鸟,在一定程度上证明了该湿地的栖息适宜性[5]。为进一步评估湿地重建成效,本研究以临港湿地二期水生生物群落为研究对象,通过对比生态重建前后浮游生物、底栖动物和鱼类群落结构变化,分析水生生物群落演变特征,探讨重建措施的成效,以期为北方滨海人工湿地重建和水鸟保护提供借鉴。
-
天津临港湿地二期工程坐落在天津滨海新区临港经济区西部、临港湿地一期南侧,占地约120 hm2,原是一片干涸的盐碱地,生物群落结构单一,食物链受损,生态系统十分脆弱[5]。为有效恢复湿地生态功能,维护生物多样性,临港湿地二期采用物理生境构造和水生生物快速重建相结合的方法(表1),构建了占地面积约50 hm2的生境恢复单元。在物理生境构造方面,通过微地形改造、水系连通等方法,构建了浅滩区、岛屿区、开放深水区等核心区,同时在核心区外围修建环流渠(外围区),引入人工湿地区净化水,在增加水体循环量的同时,还能减缓外界干扰[5]。在水生生物快速重建方面,针对临港湿地二期生态系统现状和所面临的压力,以及底栖动物和鱼类生物匮乏问题,以北大港湿地和临港湿地一期为参考湿地,通过湿地生物调查与生物多样性比选,确定重点恢复底栖动物和鱼类群落物种清单,采用生境改善、增殖放流等方式,恢复核心区乡土底栖动物群落和鱼类群落,修补和完善人工湿地受损食物链[1]。该项目于2020年6月完成物理生境构造,2020年10月开展水生生物投放工作,其中底栖动物和鱼类投放点位全部设置在核心区。
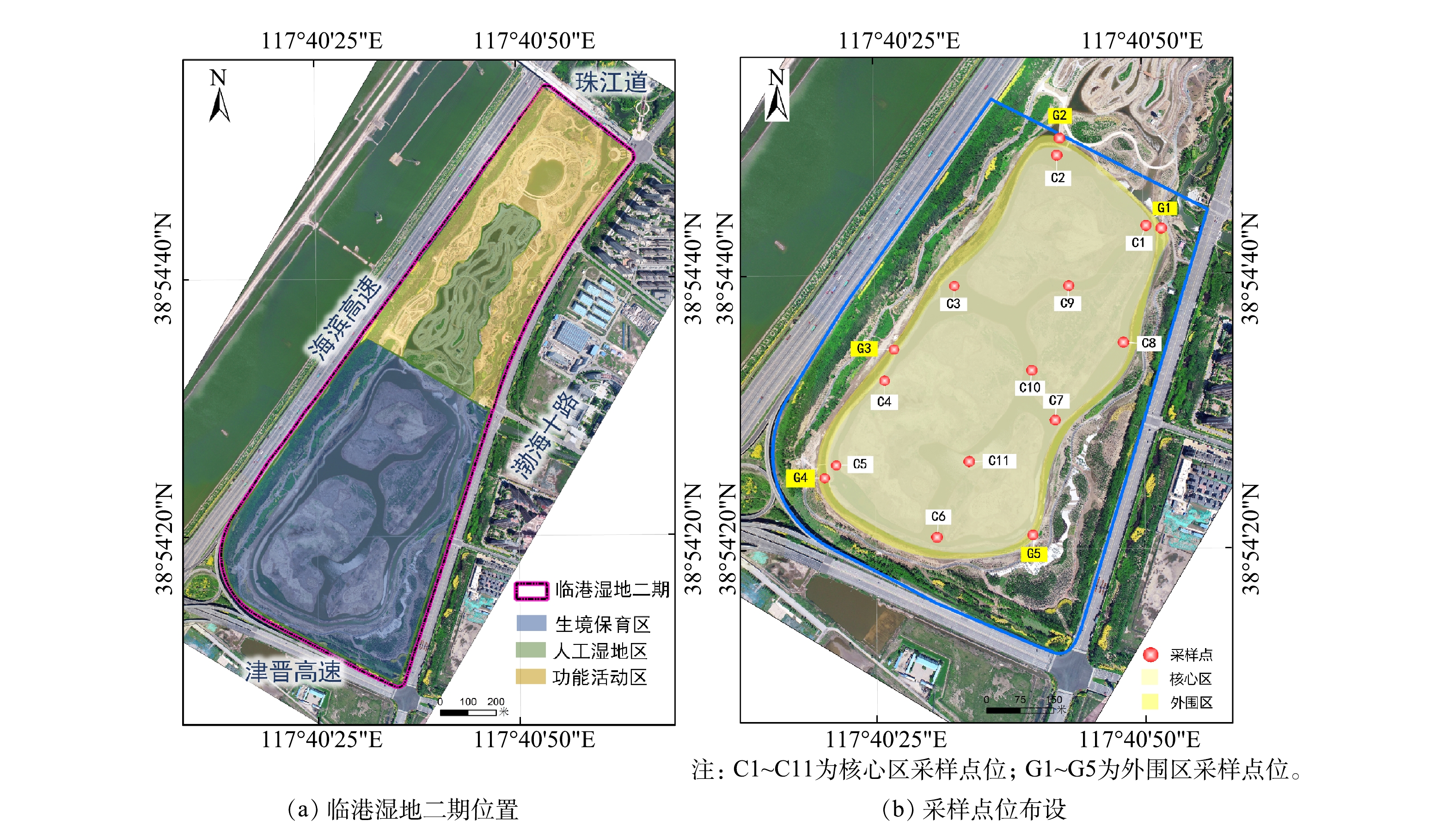
本研究以生境保育区为研究对象,在水生生物重建前(2020年9月)和重建后(2021年9月)分别开展了水生生物群落调查。2020年,设置核心区采样点位8个(C1~C8),外围区采样点位5个(G1~G5);2021年,在2020年采样点位的基础上,增设核心区中部监测点位3个(C9、C10、C11)。调查区域及点位布设见图1。其中:C1、C2、C5为鱼类增殖放流点位;C1、C2、C3、C5、C6、C7为底栖动物增殖放流点位。
-
1)调查方法[1]。浮游动植物和大型底栖动物样品采集、保存、处理和分析参照《淡水浮游生物研究方法》《湖泊生态调查观测与分析》中的方法。底栖动物采用直接称量法,计算其湿生物量。鱼类样品用地笼和刺网采集,每次放网时间为1 h。根据《中国动物志 鱼类》《天津鱼类志》等对采集的鱼类进行物种鉴定。按渔具渔法对每次的渔获物分类计数和称量。
2)数据处理。利用Shannon-Wiener多样性指数(
H′ ),对临港湿地二期的浮游生物(底栖动物)作出评价。计算方法见式(1)。式中:
Ni 为第i种浮游生物(底栖动物)个体数量;N 为个体总数量。 -
重建前后核心区内外浮游植物群落结构变化见图2。2020年,核心区共监测到浮游植物44种,外围区共监测到浮游植物48种。在丰度组成中,2个区域均是蓝藻、绿藻和硅藻含量最高。项目实施1年后,浮游植物种类有了较大提升,核心区浮游植物种类数量增加了30种,外围区增加了7种。在丰度组成中,核心区硅藻占比最高(43.2%),其次是绿藻(25.7%)、蓝藻(18.9%)、裸藻(1.3%)、隐藻(4.1%)、甲藻(4.1%)和金藻(2.7%),其中金藻和裸藻首次出现。在外围区,硅藻、绿藻、蓝藻种类数量最多,共占到总量的87.3%。2021年,核心区水域浮游植物平均密度和平均生物量分别为280×105个·L−1和10.3 mg·L−1,较2020年分别提升了63.2%和234%;外围区水域浮游植物平均密度和平均生物量分别为222×105个·L−1和3.31 mg·L−1,较2020年分别下降了60.7%和70.4%;2个区域呈现了相反的变化趋势。与重建前相比,核心区和外围区浮游植物Shannon-Wiener多样性指数分别下降了23%和15.2%。
-
重建前后核心区内外浮游动物群落结构变化见图3。2020年,核心区和外围区分别鉴定出浮游植物15种和17种。在种类组成方面,2个区域都是由轮虫类、桡足类和原生动物组成。项目实施1年后,2021核心区共监测到浮游动物17种,首次出现了枝角类物种;外围区共监测到浮游动物15种。在密度组成上,核心区和外围区均为原生动物占绝对优势,约占总量的95%以上。与2020年相比,核心区浮游动物密度增加了76.5%,外围区增加了24.7%。在生物量方面,核心区和外围区均为桡足类占绝对优势。与2020年相比,核心区浮游动物生物量减少了91.7%,外围区增加了15.7%。核心区生物量并未随着生物密度升高而增加,这从侧面反映出核心区水域浮游动物呈现轻质小型化趋势。与重建前相比,核心区和外围区浮游动物生物多样性指数分别增加了1.1%和270%。
-
重建前后核心区内外底栖动物群落结构变化见图4。2020年,核心区和外围区分别鉴定出大型底栖动物4种和9种,平均密度分别为740个·m−2和349个·m−2,平均生物量分别为3.21 g·m−2和0.60 g·m−2,优势种类均为摇蚊幼虫。2021年共采集到底栖动物28种(核心区20种,外围区18种),主要由昆虫类(摇蚊幼虫)、寡毛类(水丝蚓、尾鳃蚓)、甲壳类(虾蟹)、腹足类(螺类)、瓣鳃类(蚬)组成。底栖动物数量和生物量主要组成仍然是摇蚊幼虫类。与重建前相比,生物密度变化幅度不大,但生物量变化显著,其中核心区生物量减少了52%,外围区生物量增加了73.3%。生态修复1年后,核心区水体中底栖动物生物多样性存在一定的好转趋势,Shannon-Wiener多样性指数较2020年增长近7倍,而外围区生物多样性变化不大。
-
2020年,保育区刚刚通水不久,调查过程中未发现鱼类。2021年,核心区共采集到鱼类10种,除增殖放流存活品种(鲢、鳙、鲤、鲫、草鱼、团头鲂)外,还鉴定出4种野生杂鱼,其中,3种鉴定到种(翘嘴鲌、鮻、鲈),1种鉴定到属(鰕虎鱼属)。野生杂鱼的出现,可能是在湿地补水或夏汛水位涨时,湿地与外部河道的水交换所致。经统计,鲢鱼、鳙鱼质量约为300 g左右,鲤鱼、鲫鱼、团头鲂多为100~200 g,草鱼平均为700 g,较增殖放流鱼苗质量显著增加,鱼类群落恢复初见成效。虽然增殖放流点位均设置在核心区,但由于核心区和外围区存在水体交换,导致部分鱼类逃逸扩散进入了外围区。调查中发现,除团头鲂外,其他4种增殖放流种(鲢、鳙、鲤、鲫)均在外围区有检出。尽管如此,核心区与外围区鱼类群落结构不尽相同,核心区以底层分布鱼类占优势,鲫鱼的数量和质量最高,分别占渔获物总量的16.9%和21.3%;外围区中上层鱼类占优势,鳙的数量和质量最高,分别占渔获物总量的24.4%和33.0%。
-
临港二期湿地保育区经过1年的生态重建,整体生态环境正在逐步改善,残缺的水生生态系统也处于逐步恢复过程中。鱼类处于水生态系统食物链的较高端,本研究中增殖的先锋物种有鲢、鳙、草鱼、鲫、鲤、梭鱼、泥鳅、团头鲂,项目实施1年后,除泥鳅、梭鱼种群未恢复外,其他增殖鱼类均长势良好。泥鳅是底层鱼类,喜密集扎堆在20~30 cm浅水区[10],而临港保育区泥鳅增殖放流点为深水区,并非泥鳅生长的理想环境,这可能间接造成了泥鳅苗种死亡。梭鱼未成活的原因可能是在进入淡水培育前未经过充分淡化[11]。
作为湿地主要生物类群之一,浮游动物群落结构主要由水体中的有效营养成分、物理因子及鱼类捕食作用等因素决定[12]。生态重建工程实施前后水体均来自人工湿地区净化水,其有效营养成分、物理因子相对稳定,故浮游动物的组成变化主要受制于鱼类增殖放流影响。浮游动物是幼鱼阶段和一些滤食性鱼类成鱼阶段的主要饵料[13]。在核心区鱼类群落恢复初期,水体中以鱼苗和幼稚鱼为主,鱼类摄食相对旺盛,较快的新陈代谢率可消耗大量的浮游动物[14]。因此,浮游动物在持续而强烈的滤食和捕食压力下,生物量急剧减少,并且呈现出低生物量和小个体种类占优势的特征[14-15]。与此相反,外围区未设置增殖放流点,鱼苗和幼稚鱼数量远不及核心区,对浮游动物捕食压力相对较小,浮游动物生物量总体变化不大。
鱼类、浮游动物通过直接或间接捕食及对水体扰动等对浮游植物群落结构产生影响。在核心区,一方面,鱼类对浮游动物的强烈捕食降低了浮游植物被牧食的压力,有可能使其生态位得以扩展[14];另一方面,鱼类的活动能使上下水层的营养盐分更加均匀,而且还能够通过搅动将底泥中的营养物质释放出来,增加水体中的营养物质,促进浮游植物的生长繁殖[16]。在上述因素的综合作用下,核心区浮游植物数量和生物量显著增加。然而,对于外围区,优势种类鲢鳙等鱼类的滤食性作用可能导致水体中浮游植物向小型化发展[17],加之植食性浮游动物的选择性摄食,进而引起了浮游植物生物量的降低。
作为渔业资源和迁徙水鸟的食物来源,底栖动物群落长期生活在底泥中,具有区域性强、迁移能力弱等特点,在食物网的能量流动和物质循环中起着重要作用[18]。随着物理生境的改善和先锋物种的直接投加,核心区和外围区的底栖动物生物数量、密度和物种多样性均呈显著增加趋势,恢复迹象比较明显。在类群组成上,底栖动物群落以轻质化、小型化摇蚊幼虫为主。摇蚊幼虫采用自然恢复方式,从侧面反映出核心区和外围区的物理生境的适宜性。前期投放的大量底栖动物死亡,仅少部分得以生存,恢复进程较为缓慢。另外值得关注的是,项目竣工1年后,核心区内底栖动物生物量显著下降,而外围区显著上升,这与浮游动物的变化规律相似。考虑底栖动物是鲤、鲫等底层鱼类的优良天然饵料[19],核心区以底层鱼类占优势,而外围区以中上层鱼类为主,故核心区底栖动物受到底层鱼类下行效应的影响更为显著。国内也有研究者通过无鱼围栏内外底栖动物对比发现,放养鱼类的存在会对底栖动物的现存量产生负面影响[19]。
-
生态重建是个极其复杂的过程,因此,要达到更为成熟、稳定的状态,需要更长的时间和更多的调控措施。针对临港湿地二期水生生物群落恢复过程中存在的问题,提出如下建议。
1) 在鱼类重建方面,考虑到水生生物物种之间的相互关系,鱼苗投放阶段应避免或减少底层鱼类的投放,同时充分遵循鱼苗生态习性和适宜水域状况等因素,优化投放前处理、投放位置、投放方式等环节。在鱼类恢复初期,核心区应同步进行大型溞等常见且易于繁殖的浮游动物投放工作,以保障鱼类食物需求和生物群落结构稳定性。
2) 在底栖动物恢复方面,应更多地关注投放过程和投放后的长效管理,如优化人工投放的关键物种、个体大小、投放时间、投放方式等,辅助配合沉水植物恢复、底质改良等措施,以加快大型底栖动物群落恢复速度[18,20-21]。
3) 在综合评估结果、食物网和工程经验的基础上,有必要深入研究水生生物群落变化的影响机制,积极探索生态容量调控技术,以促进整体生态系统的良性发展。
-
1) 临港湿地二期采用物理生境构造和水生生物快速重建相结合的方法,经过近1年的生态恢复,鱼类的种类由重建前的未检出增加到10种,底栖动物数量由重建前的11种提高到重建后的28种,生物多样性明显提高,残缺的水生生态系统处于逐步恢复过程中。
2) 受鱼类增殖放流影响,核心区水域浮游动物呈低生物量和小个体种类占优势的特征,生物量减少了91.7%;外围区由于未设置增殖放流点,浮游动物生物量总体变化不大。鱼类、浮游动物群落结构的波动导致了水体系统中浮游植物群落结构的快速响应和结构变化。
3) 在恢复期间,底栖动物类群组成以自然恢复的轻质化、小型化摇蚊幼虫为主,人工投放的大型底栖动物恢复进程相对缓慢。受底层鱼类下行效应的影响,核心区底栖动物生物量减少了52%。
4) 针对临港湿地二期仍然面临着浮游生物群落结构稳定性差、大型底栖动物物种恢复缓慢、鱼类群落结构不完善等问题,针对性地提出了鱼类和底栖动物重建优化调控建议,以促进北方滨海人工湿地的重建并加强对水鸟的保护。
北方滨海人工湿地水生生物群落重建效果评估——以天津临港湿地二期生态重建工程为例
Evaluation on the ecological reconstruction of aquatic communities in the coastal constructed wetland of northern China: A case study of Tianjin Lingang constructed wetland (phase II)
-
摘要: 为准确评估滨海人工湿地生态重建成效,科学指导工程改进方案,以重建近1年的天津临港湿地二期生态重建工程为例,通过调查重建前(2020年)和重建后(2021年)湿地水生生物群落组成变化,评价湿地生物群落重建效果。结果表明:经过近1年的生态重建,鱼类群落和底栖动物群落均得到不同程度恢复;鱼类的种类由重建前的未检出增加到10种,除泥鳅、梭鱼等增殖先锋物种未得以恢复外,其他增殖鱼类均长势良好;随着物理生境改善和先锋物种的直接投加,底栖动物数量由重建前的11种提高到重建后的28种,生物多样性明显提高;在类群组成上,底栖动物群落以自然恢复的摇蚊幼虫为主,人工投放的大型底栖物种恢复进程相对缓慢;鱼类增殖放流加剧了对浮游动物的捕食压力,造成浮游动物生物量降低和个体减小,进而导致浮游植物群落的快速响应和结构变化。基于上述研究结果,提出了水生生物群落重建优化调控建议。本研究成果可为北方滨海人工湿地重建提供借鉴。Abstract: Tianjin Lingang Constructed Wetland (Phase II), a typical coastal constructed wetland in northern China, which has been reconstructed for nearly one year, was taken as a case study for the effect evaluation of aquatic community reconstruction that could serve as a guideline for further improvement of engineering scheme. The changes in aquatic community composition were investigated before (2020) and after (2021) the reconstruction. The results showed that the fish and Zoobenthos communities were restored to some extent. The number of fish species increased from 0 in 2020 to 10 in 2021. Most fishes exhibited impressive growth except that the pioneer species of Loach and Barracuda were not restored successfully. The number of Zoobenthos species increased from 11 to 28 and the biodiversity increased significantly with the improvement of physical habitat and the direct release of pioneer species. In addition. Chironomid larvae numerically dominated in the Zoobenthos community while the progress of artificially released macrobenthic species was relatively slow. The biomass of zooplankton exhibited an obvious downward trend and the species composition dominated by small individual species, probably a result of the fish proliferation at this site. Accordingly, the number and biomass of phytoplankton changed significantly due to the grazing pressure fluctuation. Based on the above research, some strategies for further regulation of aquatic community reconstruction were proposed. This work could provide a reference for wetland reconstruction in north China coastal area.
-
Key words:
- constructed wetland /
- ecological reconstruction /
- aquatic community /
- effect evaluation
-
近年来,环渤海三省一市实施了大规模围填海,造成滨海滩涂湿地面积大幅锐减,水鸟生存空间被严重压缩,在此停歇、繁殖的水鸟种群数量呈下降趋势[1-2]。为扭转这一局面,我国各级政府也在积极开展针对滨海水鸟的湿地重建工作[3-6]。水生生物群落重建是湿地重建工程的重要内容,同时也是水鸟群落恢复的关键影响要素。科学、准确地评估水生生物重建效果是调整和改进重建方案的重要手段,对湿地生态重建实践具有重要指导意义[7-8]。然而,目前针对围海造陆区水生生物重建效果的评估研究相对较少,缺乏对重建成效和趋势的直观了解与判断[9]。
2019—2020年,天津港保税区临港经济区规划建设了临港湿地二期工程,除设计表流湿地外,还增设了生境恢复单元,通过物理生境改造和水生生物群落快速重建等措施,不仅构建了水鸟栖息觅食空间,还重建了鱼类、底栖动物等鸟类藉以生存的食物资源[1,5]。该工程一经建成,就吸引了数十种水鸟,在一定程度上证明了该湿地的栖息适宜性[5]。为进一步评估湿地重建成效,本研究以临港湿地二期水生生物群落为研究对象,通过对比生态重建前后浮游生物、底栖动物和鱼类群落结构变化,分析水生生物群落演变特征,探讨重建措施的成效,以期为北方滨海人工湿地重建和水鸟保护提供借鉴。
1. 研究区域与方法
1.1 研究区域与样点布设
天津临港湿地二期工程坐落在天津滨海新区临港经济区西部、临港湿地一期南侧,占地约120 hm2,原是一片干涸的盐碱地,生物群落结构单一,食物链受损,生态系统十分脆弱[5]。为有效恢复湿地生态功能,维护生物多样性,临港湿地二期采用物理生境构造和水生生物快速重建相结合的方法(表1),构建了占地面积约50 hm2的生境恢复单元。在物理生境构造方面,通过微地形改造、水系连通等方法,构建了浅滩区、岛屿区、开放深水区等核心区,同时在核心区外围修建环流渠(外围区),引入人工湿地区净化水,在增加水体循环量的同时,还能减缓外界干扰[5]。在水生生物快速重建方面,针对临港湿地二期生态系统现状和所面临的压力,以及底栖动物和鱼类生物匮乏问题,以北大港湿地和临港湿地一期为参考湿地,通过湿地生物调查与生物多样性比选,确定重点恢复底栖动物和鱼类群落物种清单,采用生境改善、增殖放流等方式,恢复核心区乡土底栖动物群落和鱼类群落,修补和完善人工湿地受损食物链[1]。该项目于2020年6月完成物理生境构造,2020年10月开展水生生物投放工作,其中底栖动物和鱼类投放点位全部设置在核心区。
表 1 临港湿地二期生态重建工程Table 1. Ecological reconstruction projects of Lingang constructed wetland (phase II)类别 重建项目 重建具体措施 物理生境构造 微地形改造 营建4个面积共计22×104 m2的浅滩,水位控制在15 cm以下;在浅滩内部构建10个集中分布的不同形态的小型岛屿;浅滩外围深挖沟渠,形成深水区,提高保育区内部连通性和整合度 水系连通 在湿地保育区核心区外围建设环流渠(外围区),引入人工湿地区净化水,形成环流,对湿地保育区核心区进行生态补水 水生生物重建 底栖动物重建 摇蚊幼虫类以自然恢复为主,虾蟹类、寡毛类和单壳类以人工投放为主,在核心区设置放流点位6处,每处投放总量的1/6,累计投放量280×104个 鱼类重建 鱼类群落重建先锋种包括鲢、鳙、草鱼、团头鲂、鲫、泥鳅、梭鱼、鲤鱼,在核心区设置鱼类放流点3处,每处投放总量的1/3,累计投放34 000尾 本研究以生境保育区为研究对象,在水生生物重建前(2020年9月)和重建后(2021年9月)分别开展了水生生物群落调查。2020年,设置核心区采样点位8个(C1~C8),外围区采样点位5个(G1~G5);2021年,在2020年采样点位的基础上,增设核心区中部监测点位3个(C9、C10、C11)。调查区域及点位布设见图1。其中:C1、C2、C5为鱼类增殖放流点位;C1、C2、C3、C5、C6、C7为底栖动物增殖放流点位。
1.2 研究方法
1)调查方法[1]。浮游动植物和大型底栖动物样品采集、保存、处理和分析参照《淡水浮游生物研究方法》《湖泊生态调查观测与分析》中的方法。底栖动物采用直接称量法,计算其湿生物量。鱼类样品用地笼和刺网采集,每次放网时间为1 h。根据《中国动物志 鱼类》《天津鱼类志》等对采集的鱼类进行物种鉴定。按渔具渔法对每次的渔获物分类计数和称量。
2)数据处理。利用Shannon-Wiener多样性指数(
H′ H′=−∑(Ni/N)log2(Ni/N) (1) 式中:
Ni N 2. 结果与分析
2.1 浮游植物群落
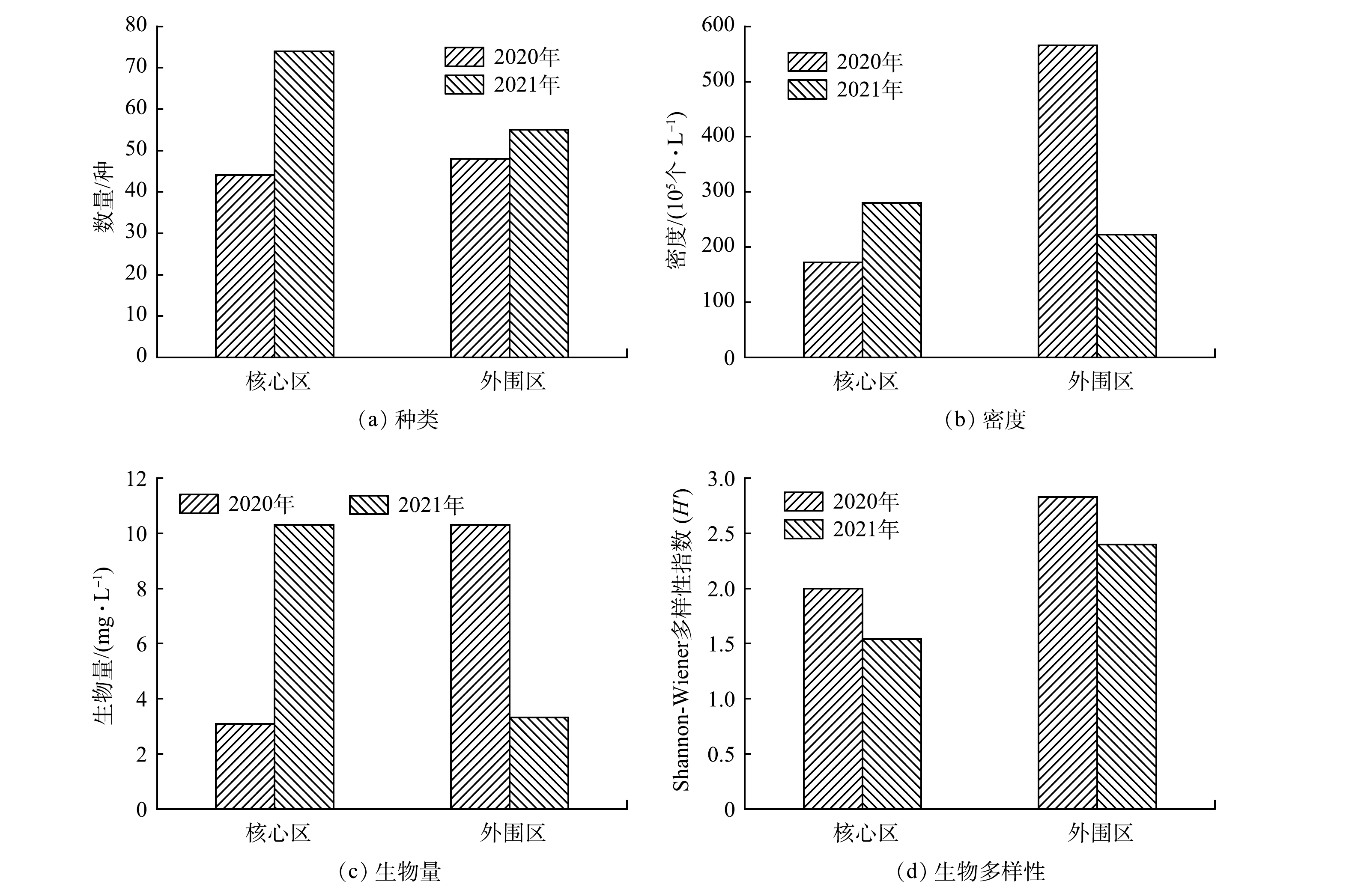
重建前后核心区内外浮游植物群落结构变化见图2。2020年,核心区共监测到浮游植物44种,外围区共监测到浮游植物48种。在丰度组成中,2个区域均是蓝藻、绿藻和硅藻含量最高。项目实施1年后,浮游植物种类有了较大提升,核心区浮游植物种类数量增加了30种,外围区增加了7种。在丰度组成中,核心区硅藻占比最高(43.2%),其次是绿藻(25.7%)、蓝藻(18.9%)、裸藻(1.3%)、隐藻(4.1%)、甲藻(4.1%)和金藻(2.7%),其中金藻和裸藻首次出现。在外围区,硅藻、绿藻、蓝藻种类数量最多,共占到总量的87.3%。2021年,核心区水域浮游植物平均密度和平均生物量分别为280×105个·L−1和10.3 mg·L−1,较2020年分别提升了63.2%和234%;外围区水域浮游植物平均密度和平均生物量分别为222×105个·L−1和3.31 mg·L−1,较2020年分别下降了60.7%和70.4%;2个区域呈现了相反的变化趋势。与重建前相比,核心区和外围区浮游植物Shannon-Wiener多样性指数分别下降了23%和15.2%。
2.2 浮游动物群落
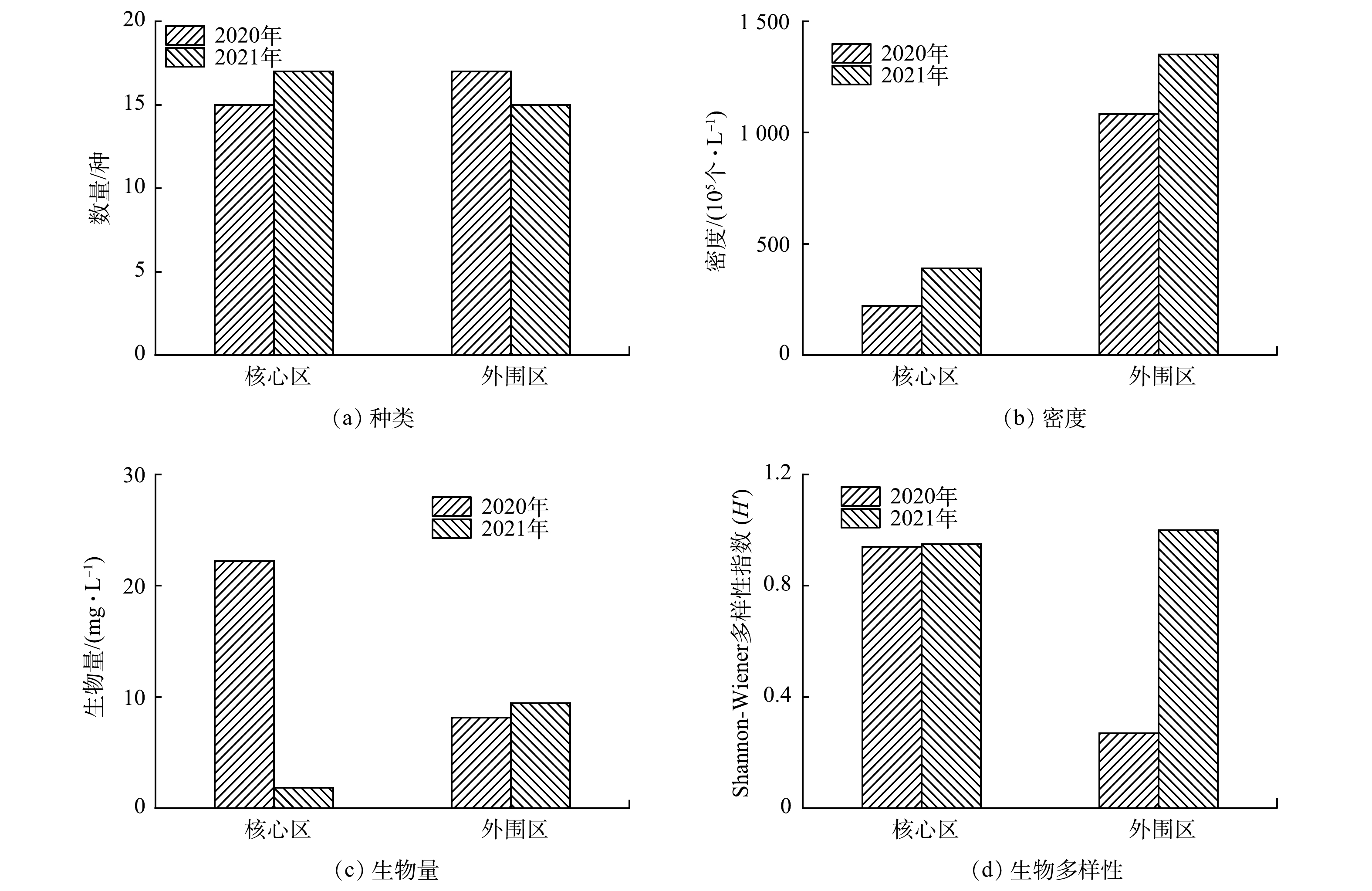
重建前后核心区内外浮游动物群落结构变化见图3。2020年,核心区和外围区分别鉴定出浮游植物15种和17种。在种类组成方面,2个区域都是由轮虫类、桡足类和原生动物组成。项目实施1年后,2021核心区共监测到浮游动物17种,首次出现了枝角类物种;外围区共监测到浮游动物15种。在密度组成上,核心区和外围区均为原生动物占绝对优势,约占总量的95%以上。与2020年相比,核心区浮游动物密度增加了76.5%,外围区增加了24.7%。在生物量方面,核心区和外围区均为桡足类占绝对优势。与2020年相比,核心区浮游动物生物量减少了91.7%,外围区增加了15.7%。核心区生物量并未随着生物密度升高而增加,这从侧面反映出核心区水域浮游动物呈现轻质小型化趋势。与重建前相比,核心区和外围区浮游动物生物多样性指数分别增加了1.1%和270%。
2.3 底栖动物群落
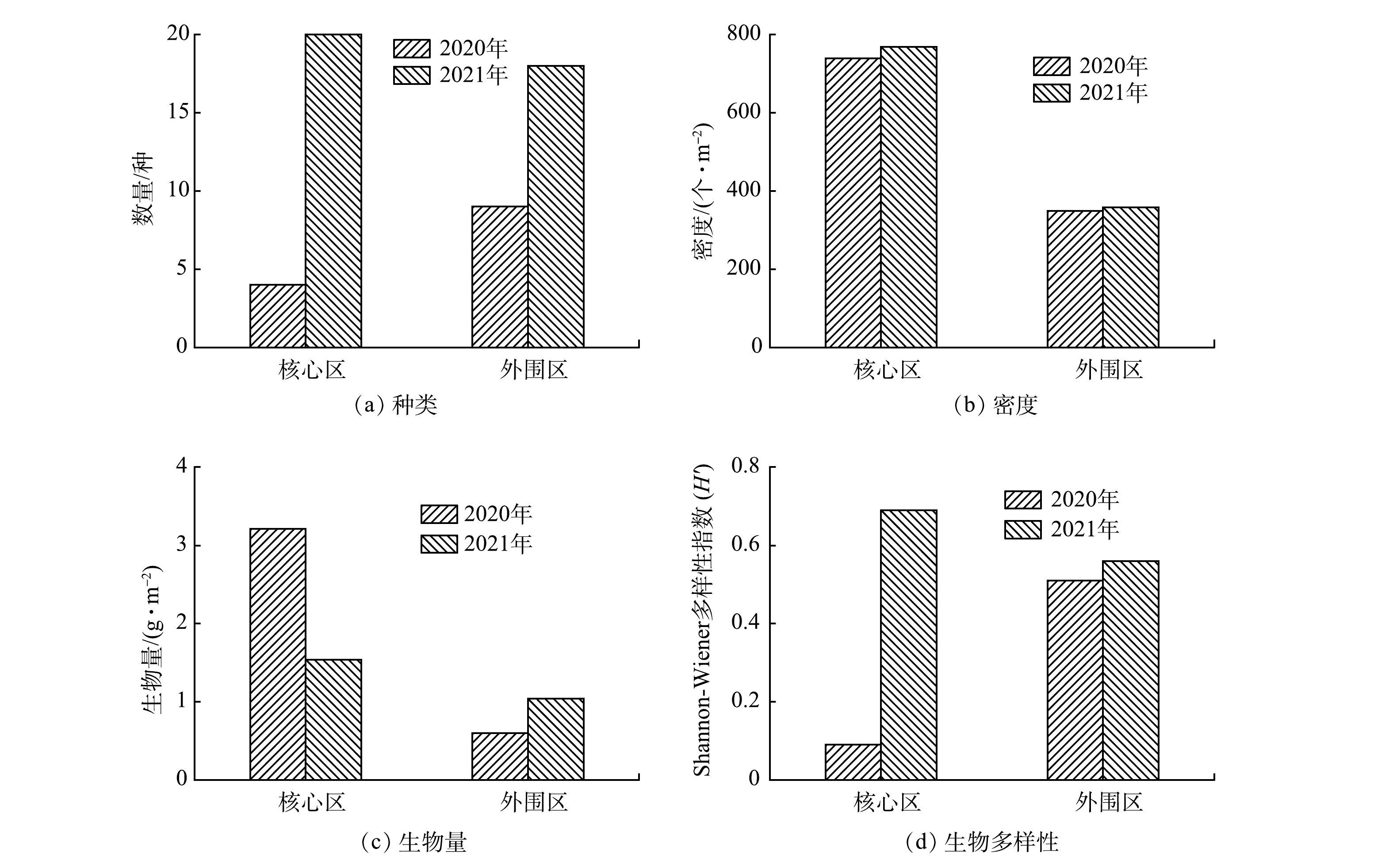
重建前后核心区内外底栖动物群落结构变化见图4。2020年,核心区和外围区分别鉴定出大型底栖动物4种和9种,平均密度分别为740个·m−2和349个·m−2,平均生物量分别为3.21 g·m−2和0.60 g·m−2,优势种类均为摇蚊幼虫。2021年共采集到底栖动物28种(核心区20种,外围区18种),主要由昆虫类(摇蚊幼虫)、寡毛类(水丝蚓、尾鳃蚓)、甲壳类(虾蟹)、腹足类(螺类)、瓣鳃类(蚬)组成。底栖动物数量和生物量主要组成仍然是摇蚊幼虫类。与重建前相比,生物密度变化幅度不大,但生物量变化显著,其中核心区生物量减少了52%,外围区生物量增加了73.3%。生态修复1年后,核心区水体中底栖动物生物多样性存在一定的好转趋势,Shannon-Wiener多样性指数较2020年增长近7倍,而外围区生物多样性变化不大。
2.4 鱼类群落
2020年,保育区刚刚通水不久,调查过程中未发现鱼类。2021年,核心区共采集到鱼类10种,除增殖放流存活品种(鲢、鳙、鲤、鲫、草鱼、团头鲂)外,还鉴定出4种野生杂鱼,其中,3种鉴定到种(翘嘴鲌、鮻、鲈),1种鉴定到属(鰕虎鱼属)。野生杂鱼的出现,可能是在湿地补水或夏汛水位涨时,湿地与外部河道的水交换所致。经统计,鲢鱼、鳙鱼质量约为300 g左右,鲤鱼、鲫鱼、团头鲂多为100~200 g,草鱼平均为700 g,较增殖放流鱼苗质量显著增加,鱼类群落恢复初见成效。虽然增殖放流点位均设置在核心区,但由于核心区和外围区存在水体交换,导致部分鱼类逃逸扩散进入了外围区。调查中发现,除团头鲂外,其他4种增殖放流种(鲢、鳙、鲤、鲫)均在外围区有检出。尽管如此,核心区与外围区鱼类群落结构不尽相同,核心区以底层分布鱼类占优势,鲫鱼的数量和质量最高,分别占渔获物总量的16.9%和21.3%;外围区中上层鱼类占优势,鳙的数量和质量最高,分别占渔获物总量的24.4%和33.0%。
3. 讨论
临港二期湿地保育区经过1年的生态重建,整体生态环境正在逐步改善,残缺的水生生态系统也处于逐步恢复过程中。鱼类处于水生态系统食物链的较高端,本研究中增殖的先锋物种有鲢、鳙、草鱼、鲫、鲤、梭鱼、泥鳅、团头鲂,项目实施1年后,除泥鳅、梭鱼种群未恢复外,其他增殖鱼类均长势良好。泥鳅是底层鱼类,喜密集扎堆在20~30 cm浅水区[10],而临港保育区泥鳅增殖放流点为深水区,并非泥鳅生长的理想环境,这可能间接造成了泥鳅苗种死亡。梭鱼未成活的原因可能是在进入淡水培育前未经过充分淡化[11]。
作为湿地主要生物类群之一,浮游动物群落结构主要由水体中的有效营养成分、物理因子及鱼类捕食作用等因素决定[12]。生态重建工程实施前后水体均来自人工湿地区净化水,其有效营养成分、物理因子相对稳定,故浮游动物的组成变化主要受制于鱼类增殖放流影响。浮游动物是幼鱼阶段和一些滤食性鱼类成鱼阶段的主要饵料[13]。在核心区鱼类群落恢复初期,水体中以鱼苗和幼稚鱼为主,鱼类摄食相对旺盛,较快的新陈代谢率可消耗大量的浮游动物[14]。因此,浮游动物在持续而强烈的滤食和捕食压力下,生物量急剧减少,并且呈现出低生物量和小个体种类占优势的特征[14-15]。与此相反,外围区未设置增殖放流点,鱼苗和幼稚鱼数量远不及核心区,对浮游动物捕食压力相对较小,浮游动物生物量总体变化不大。
鱼类、浮游动物通过直接或间接捕食及对水体扰动等对浮游植物群落结构产生影响。在核心区,一方面,鱼类对浮游动物的强烈捕食降低了浮游植物被牧食的压力,有可能使其生态位得以扩展[14];另一方面,鱼类的活动能使上下水层的营养盐分更加均匀,而且还能够通过搅动将底泥中的营养物质释放出来,增加水体中的营养物质,促进浮游植物的生长繁殖[16]。在上述因素的综合作用下,核心区浮游植物数量和生物量显著增加。然而,对于外围区,优势种类鲢鳙等鱼类的滤食性作用可能导致水体中浮游植物向小型化发展[17],加之植食性浮游动物的选择性摄食,进而引起了浮游植物生物量的降低。
作为渔业资源和迁徙水鸟的食物来源,底栖动物群落长期生活在底泥中,具有区域性强、迁移能力弱等特点,在食物网的能量流动和物质循环中起着重要作用[18]。随着物理生境的改善和先锋物种的直接投加,核心区和外围区的底栖动物生物数量、密度和物种多样性均呈显著增加趋势,恢复迹象比较明显。在类群组成上,底栖动物群落以轻质化、小型化摇蚊幼虫为主。摇蚊幼虫采用自然恢复方式,从侧面反映出核心区和外围区的物理生境的适宜性。前期投放的大量底栖动物死亡,仅少部分得以生存,恢复进程较为缓慢。另外值得关注的是,项目竣工1年后,核心区内底栖动物生物量显著下降,而外围区显著上升,这与浮游动物的变化规律相似。考虑底栖动物是鲤、鲫等底层鱼类的优良天然饵料[19],核心区以底层鱼类占优势,而外围区以中上层鱼类为主,故核心区底栖动物受到底层鱼类下行效应的影响更为显著。国内也有研究者通过无鱼围栏内外底栖动物对比发现,放养鱼类的存在会对底栖动物的现存量产生负面影响[19]。
4. 建议
生态重建是个极其复杂的过程,因此,要达到更为成熟、稳定的状态,需要更长的时间和更多的调控措施。针对临港湿地二期水生生物群落恢复过程中存在的问题,提出如下建议。
1) 在鱼类重建方面,考虑到水生生物物种之间的相互关系,鱼苗投放阶段应避免或减少底层鱼类的投放,同时充分遵循鱼苗生态习性和适宜水域状况等因素,优化投放前处理、投放位置、投放方式等环节。在鱼类恢复初期,核心区应同步进行大型溞等常见且易于繁殖的浮游动物投放工作,以保障鱼类食物需求和生物群落结构稳定性。
2) 在底栖动物恢复方面,应更多地关注投放过程和投放后的长效管理,如优化人工投放的关键物种、个体大小、投放时间、投放方式等,辅助配合沉水植物恢复、底质改良等措施,以加快大型底栖动物群落恢复速度[18,20-21]。
3) 在综合评估结果、食物网和工程经验的基础上,有必要深入研究水生生物群落变化的影响机制,积极探索生态容量调控技术,以促进整体生态系统的良性发展。
5. 结论
1) 临港湿地二期采用物理生境构造和水生生物快速重建相结合的方法,经过近1年的生态恢复,鱼类的种类由重建前的未检出增加到10种,底栖动物数量由重建前的11种提高到重建后的28种,生物多样性明显提高,残缺的水生生态系统处于逐步恢复过程中。
2) 受鱼类增殖放流影响,核心区水域浮游动物呈低生物量和小个体种类占优势的特征,生物量减少了91.7%;外围区由于未设置增殖放流点,浮游动物生物量总体变化不大。鱼类、浮游动物群落结构的波动导致了水体系统中浮游植物群落结构的快速响应和结构变化。
3) 在恢复期间,底栖动物类群组成以自然恢复的轻质化、小型化摇蚊幼虫为主,人工投放的大型底栖动物恢复进程相对缓慢。受底层鱼类下行效应的影响,核心区底栖动物生物量减少了52%。
4) 针对临港湿地二期仍然面临着浮游生物群落结构稳定性差、大型底栖动物物种恢复缓慢、鱼类群落结构不完善等问题,针对性地提出了鱼类和底栖动物重建优化调控建议,以促进北方滨海人工湿地的重建并加强对水鸟的保护。
-
表 1 临港湿地二期生态重建工程
Table 1. Ecological reconstruction projects of Lingang constructed wetland (phase II)
类别 重建项目 重建具体措施 物理生境构造 微地形改造 营建4个面积共计22×104 m2的浅滩,水位控制在15 cm以下;在浅滩内部构建10个集中分布的不同形态的小型岛屿;浅滩外围深挖沟渠,形成深水区,提高保育区内部连通性和整合度 水系连通 在湿地保育区核心区外围建设环流渠(外围区),引入人工湿地区净化水,形成环流,对湿地保育区核心区进行生态补水 水生生物重建 底栖动物重建 摇蚊幼虫类以自然恢复为主,虾蟹类、寡毛类和单壳类以人工投放为主,在核心区设置放流点位6处,每处投放总量的1/6,累计投放量280×104个 鱼类重建 鱼类群落重建先锋种包括鲢、鳙、草鱼、团头鲂、鲫、泥鳅、梭鱼、鲤鱼,在核心区设置鱼类放流点3处,每处投放总量的1/3,累计投放34 000尾 -
[1] 刘红磊, 李艳英, 周滨, 等. 北方滨海人工湿地水生生物群落快速重建目标及适宜物种清单确定: 以天津临港二期湿地为例[J]. 生态学报, 2021, 41(15): 6091-6102. [2] 魏帆, 韩广轩, 张金萍, 等. 1985-2015年围填海活动影响下的环渤海滨海湿地演变特征[J]. 生态学杂志, 2018, 37(5): 1527-1537. [3] 胡吉. 滨海湿地生态景观修复规划设计初探: 以江苏盐城国家级珍禽自然保护区湿地恢复与重建工程为例[J]. 中国市政工程, 2015(2): 61-63. doi: 10.3969/j.issn.1004-4655.2015.02.021 [4] 车铭哲, 于劲翔. “以鸟为本”理念下的滨海湿地生态修复规划: 以北戴河七里海潟湖湿地生态修复项目为例[J]. 规划师, 2019, 35(7): 55-59. doi: 10.3969/j.issn.1006-0022.2019.07.008 [5] 李艳英, 刘红磊, 付英明, 等. 天津临港人工湿地二期工程中鸻鹬类水鸟栖息地构建及生境恢复[J]. 环境工程学报, 2021, 15(3): 1112-1120. doi: 10.12030/j.cjee.202008062 [6] 王凤琴, 陈晨, 刘威, 等. 天津冬季水鸟多样性和优先保护区域分析[J]. 生态与农村环境学报, 2021, 37(4): 509-517. [7] 吴丹丹, 蔡运龙. 中国生态恢复效果评价研究综述[J]. 地理科学进展, 2009, 28(4): 622-628. doi: 10.11820/dlkxjz.2009.04.020 [8] 陈亚瞿, 施利燕, 全为民. 长江口生态修复工程底栖动物群落的增殖放流及效果评估[J]. 渔业现代化, 2007, 34(2): 35-39. doi: 10.3969/j.issn.1007-9580.2007.02.013 [9] 孙晓萌, 彭本荣. 中国生态修复成效评估方法研究[J]. 环境科学与管理, 2014, 39(7): 153-157. doi: 10.3969/j.issn.1673-1212.2014.07.041 [10] 刘学谦. 泥鳅的生理生态特性[J]. 水产科技情报, 1981(2): 26-27. [11] 韩士群, 严少华, 周庆. 海生梭鱼苗种淡化培育及高效益, 低排污的生态养殖方法: CN201810103277.5[P]. 2018-06-12. [12] BAI Q S. Zooplankton composition in neusiedlersee with regard to fish predation[J]. Supplement to the Acta Scientiarum Naturalium Universitatis Sunyatseni, 1990, 9(2): 123-133. [13] MEHNER T, THIEL R. A review of predation impact by 0+ fish on zooplankton in fresh and brackish waters of the temperate northern hemisphere[J]. Environmental Biology of Fishers, 1999, 56(1): 169-181. [14] 江孝军, 韩博平, 林秋奇. 水库鱼类放养密度对浮游动物群落结构的影响[J]. 水生态学杂志, 2013, 34(1): 30-36. [15] DENSON W L T. Feeding behavior of major 0+ fish species in a shallow, eutrophic lake (Tjeukemeer, The Netherlands)[J]. Journal of Applied Ichthyology, 1985, 1(2): 49-70. doi: 10.1111/j.1439-0426.1985.tb00412.x [16] 孙育平. 营养盐加富、滤食性鱼类和浮游动物对水库浮游植物群落结构的影响[D]. 广州: 暨南大学, 2010. [17] 张艳艳, 魏金豹, 黄民生, 等. 环境因子对滴水湖浮游植物生长的影响分析[J]. 华东师范大学学报(自然科学版), 2015(2): 48-57. [18] 戴雅奇, 熊昀青, 由文辉. 苏州河底栖动物群落恢复过程动态研究[J]. 农村生态环境, 2005, 21(3): 21-24. [19] 傅相明, 王宇庭, 曲晓. 黄河三角洲平原型水库摇蚊幼虫对磷的积累效应[J]. 农业环境科学学报, 2005, 24(S1): 134-136. [20] 陈泽豪, 王颖, 王乔, 等. 基于习性和食物网的白洋淀大型底栖动物群落恢复研究[J]. 生态毒理学报, 2021, 16(5): 136-147. [21] 薛庆举, 汤祥明, 龚志军, 等. 典型城市湖泊五里湖底栖动物群落演变特征及其生态修复应用建议[J]. 湖泊科学, 2020, 32(3): 762-771. doi: 10.18307/2020.0316 -






 DownLoad:
DownLoad: