-
城市河道在人居生活和景观调节中发挥着重要作用。近年来,随着我国水环境治理相关政策体系的不断完善,特别是自《水污染防治行动计划》(“水十条”)发布和“污染防治攻坚战”开展以来,我国的水环境质量得到较大改善。2020年底全国地级以上城市2 914个黑臭水体消除比例达到98.2%[1],2021年底3641个国家地表水考核断面中水质劣V类仅占2.1%。然而,环保专项督查发现各地均有出现黑臭污染反弹现象;督查报告指出,水体底泥的内源污染未有效解决是黑臭污染反弹的主要原因之一[2]。
底泥是河流生态系统的重要组成部分,但长期污染已使其成为营养盐、难降解有机物、重金属等污染物的蓄积库[3]。即使外源污染得到有效控制,底泥中的污染物释放仍可能对水体产生“二次污染”[4]。目前,污染底泥治理思路分为异位处置和原位治理两类。异位处置主要指底泥清淤及后续处置,在水环境治理工程中被广泛采用,但实践中存在工程成本高、施工难度大、二次污染控制难度大等弊端[5]。原位治理的思路则是通过向底泥定向投加微生物、化学剂等,在泥水界面乃至底泥中对底泥污染物进行氧化和分解,以达到重建底泥生境,恢复底泥生态功能的目的。相较异位处置,原位治理技术所需费用一般较低,并可避免清淤处置过程的二次污染等问题,符合生态文明建设目标,已得到广泛研究及应用[6-8]。
硝酸盐介导的底泥修复技术是一种底泥原位治理技术。在硝酸盐刺激下,反硝化细菌的活性被激活,其中异养反硝化菌利用硝酸盐为电子受体降解底泥中的有机物(NO3− + OM
→ N2 + CO2)[9-10],自养反硝化菌以硝酸盐为电子受体氧化底泥中的硫化物(NO3− + S2−→ N2 + SO42−)[11-12],达到消除底泥黑臭(H2S、FeS等)和有机污染物的效果。硝酸盐底泥修复法可解决传统曝气充氧难以突破泥水界面的难题,利用硝酸盐的强水溶性和对反硝化菌的强化特性深度氧化黑臭底泥[13-15],是极具潜力的底泥原位治理方法;但由于硝酸盐的添加可能对水体引入营养污染风险[16-17],而限制了其应用推广。本研究通过室内泥柱、原位泥柱和现场中试实验,探索硝酸钙修复黑臭底泥过程中河道水相水质的影响和响应,客观评价硝酸钙底泥修复法的效果与风险,为底泥原位治理技术的应用提供参考。
-
供试底泥修复的硝酸钙缓释颗粒为广东省科学院微生物研究所专利产品(专利号:201610316764.0)。该颗粒以底泥为辅料,富集了反硝化菌休眠体,并含有211.7 mg·g−1缓释硝酸钙,被命名为SedCaN颗粒。
-
为验证硝酸钙缓释颗粒对黑臭底泥的修复效果,模拟真实底泥环境设立了室内泥柱修复实验。采集佛山某黑臭河道0~15 cm的浮泥层底泥和15~30 cm的淤泥层底泥,并将2种底泥各1.57 kg按原分层次序装入5 L量筒,静置平衡1 d。经测定,底泥的密度为1.25 kg·L−1,其还原氧化电位(oxidation-reduction potential,ORP)为-450 mV,含水率为68.5%,有机质含量为14.6%,总磷、总氮和酸挥发性硫(acid volatile sulfide,AVS)含量分别为8 760、3 450和440 mg·kg−1。
设置4个处理组,分别为“SedCaN+原水”、“SedCaN+稀释水”、“CK+原水”、“CK+稀释水”。其中,SedCaN为添加SedCaN颗粒处理组,CK为未添加SedCaN颗粒的对照组,每个处理组2个重复。参考HE等[18]计算硝酸钙剂量的方法,SedCaN颗粒的添加量设定为5 kg·m−2,投放在两层底泥之间。
向泥柱缓慢注入4 L上覆水,水质指标见表1。上覆水同样取自该河道,代表典型黑臭水体,同时取部分河水用去离子水稀释8倍,模拟清水补给措施下的情形。为排除藻类和微生物活动的干扰,通过氮吹排出水中氧气,保持水质溶解氧(DO)在0.5 mg·L−1以下。处理后的河水水质指标见下表,可见河道水经8倍稀释后达《地表水环境质量标准(GB3838-2002)》的V类水标准。
泥柱静置培养4 h后开始采样,共采样24次。每次取上覆水200 mL,取样后补充200 mL相应上覆水。其中,第1~7次采样间隔4 h,第8~13次采样间隔8 h,第14~20次采样间隔12 h,第21~24次采样间隔24 h。水样中的溶解氧、pH、溶解氧和ORP采用YSI ProPlus多参数便携式水质检测仪测定;铵态氮(NH4+-N)、硝态氮(NO3−-N)、总磷(TP)和化学需氧量(COD)分别采用国家环境保护标准HJ 535-2009、HJ 346-2007 HJ 671-2013、HJ 828-2017测定。
-
为验证真实河道环境下硝酸钙颗粒对底泥和上覆水的影响,在实验河道北段、中段、南段随机选取3个间距15 m的位点,每个位点设置对照组(CK)和硝酸钙处理组(SedCaN)2个处理,每个处理2次重复。同时,为避免投放颗粒过程引起底泥扰动,先抽干该段的河水,然后使用插播式播种器将SedCaN颗粒加入浮泥层以下(约15 cm),随后再恢复水流。将白色PVC管(DN200)插入泥下50 cm,管身露出河面20 cm,PVC管内上覆水抽干,SedCaN组以10 kg·m−2剂量将硝酸钙缓释颗粒均匀埋入底泥中,之后沿管壁小心注回原河水15 L,管口加帽遮光,静置1 d后开始采样测试。测定样品的溶解氧、pH、铵态氮、COD和总磷等指标。
-
河道现场中试实验选取河道北段、中段、南段3个示范点,长度为50~85 m。为便于精准投加和采样,提前将示范点区域水抽干,在河道底部铺设浮台和格栅。格栅大小为1.5 m×1.0 m,孔径0.1 m×0.1 m。使用插播式播种器在每个格栅内埋入SedCaN颗粒于浮泥层下(约15 cm),随后对河道进行补水。SedCaN颗粒使用量为10 kg·m−2,
定期使用柱状采样器采集示范区底泥进行AVS、亚铁、总铁、硝态氮、硫酸盐含量等指标的测试。测定详见参考文献[19-20]。同时,监测底泥修复对上覆水影响,分析上覆水溶解氧、pH、铵态氮、硝态氮、COD和总磷变化。实验延续28 d期间,采集对照区和示范区浮泥层下(约15 cm)底泥样品(各3个平行样),使用PowerSoilTM DNA提取试剂盒提取样品总DNA,在Illumina Miseq平台测定16S rRNA基因V4区序列;通过质量控制的序列数据在RDP数据库比对获得327~447个OTUs;使用ANOVA分析对照区与示范区优势菌属差异(差异大于1%的菌属),具体方法参考相关文献[9-10]。
-
SedCaN颗粒施放后,底泥黑臭消除效果明显。如图1所示,试验10 d后颗粒铺设位置向上约10 cm处的底泥已由原来的黑色转为黄色,形成明显的氧化层,并随时间逐渐扩展至泥水界面。此结果与前人利用硝酸钙修复黑臭底泥的小体系模拟实验结果相似[9, 11, 20-23]。本研究的室内模拟实验主要讨论上覆水差异,以筛选清水补水措施,促进硝酸钙促进黑臭底泥的修复。无论上覆水为原水(劣V类)还是模拟清水(V类),底泥黑臭消除的效果均相近。硝酸钙治理黑臭底泥过程实际上是自养反硝化菌和异养反硝化菌在硝酸盐的刺激下将硫化物和有机质氧化降解的过程[11]。反硝化-硫氧化过程属于厌氧反应,而底泥持续处于厌氧状态且离子扩散效率低,反硝化微生物所需的电子供体(有机质和硫化物)和电子受体(硝酸盐)在底泥中相对稳定[10]。这表明在底泥中缓释硝酸钙驱动黑臭物质厌氧氧化的过程基本不受上覆水水质的影响。
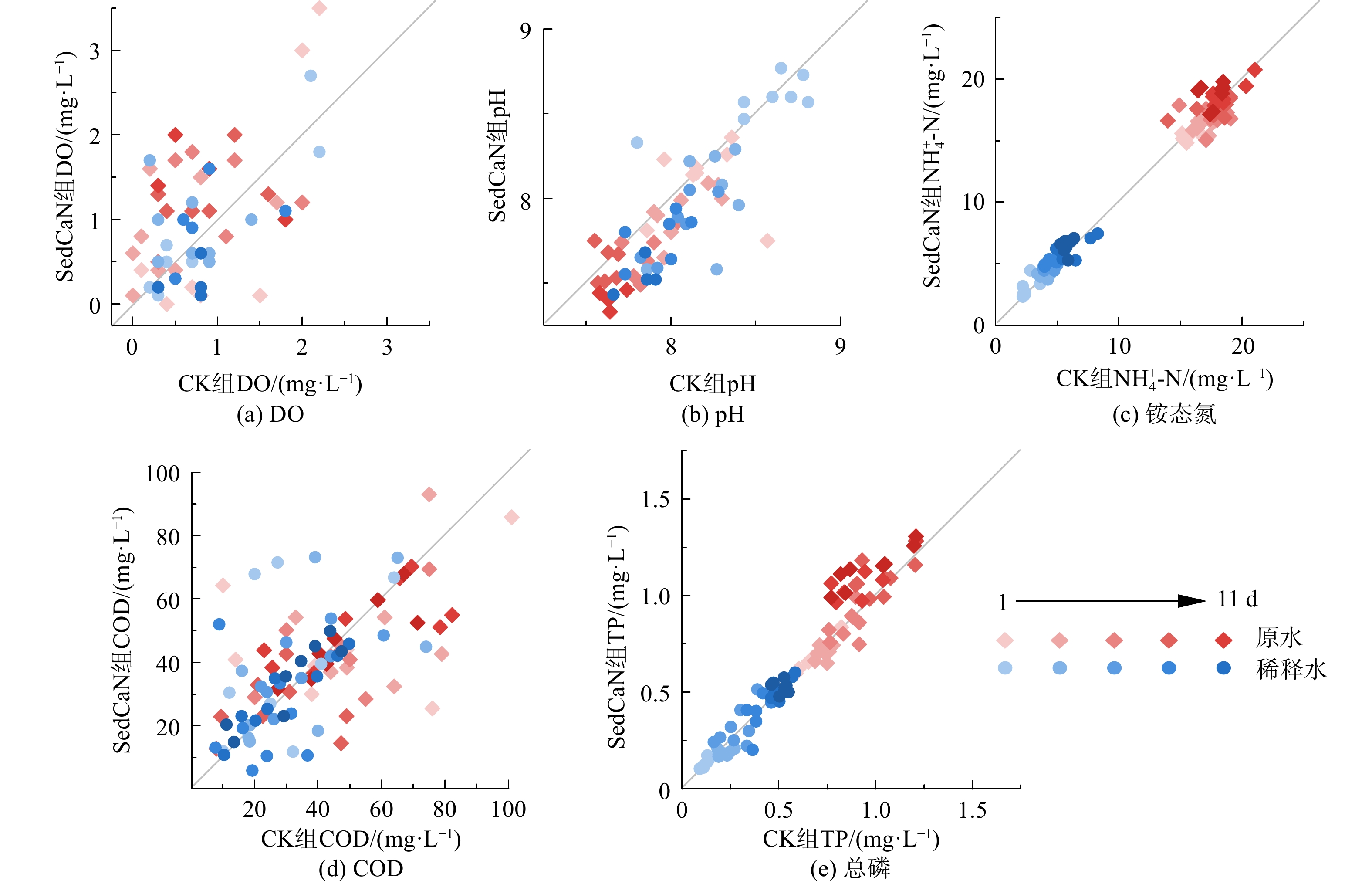
图2为上覆水理化指标的变化及对照组(CK组)和硝酸钙修复组(SedCaN组)的比较。其中,横坐标表示CK组的水质指标,纵坐标表示SedCaN组的水质指标。溶解氧、pH、铵态氮、COD和总磷5个指标值分布呈“左下-右上”。通过对CK组与SedCaN组所有指标进行相关性分析(表2),发现无论是原水还是稀释水,对照与处理均呈显著相关性(r=0.460~0.944,Pr<0.01)。这说明其他环境因子,如温度、气压等在实验期较窄的变化范围内对处理没有产生差异性影响,即其他环境因子与硝酸钙的刺激没有产生交互作用。
进一步对同时间的CK组和SedCaN组样品进行了成对样品T检验,以分析2组处理在实验过程中的差异(表2)。结果显示,溶解氧在原水中SedCaN组显著高于CK组(Pt<0.05)。这说明硝酸钙的处理有利于黑臭水体上覆水恢复溶解氧,主要由于硝酸钙修复过程为耗氧物质消除的过程,提高了水体复氧能力。然而,这个过程在耗氧物质本来就较少的稀释水中体现不明显(Pt>0.05)。对于pH这一指标,无论是原水还是稀释水,SedCaN组均略低于CK组(约0.1个pH单位),可能是由于加入的钙离子水解消耗了氢氧根离子(Ca2+ + 2OH−
→ Ca(OH)2)所致。对于COD这一指标,无论在原水还是稀释水,两组间均无显著性差异。这说明硝酸钙修复底泥过程中,被激活的反硝化菌主要利用沉积物里的有机质[9],而对上覆水的COD影响甚微。氮磷是地表水的关键指标,其中铵态氮以溶解态的分子或离子形式存在于水相,总磷则吸附在颗粒或沉积物为主[24]。因此,水相的铵态氮取决于实验柱体系中泥水交换的方向与强度[16],而水相总磷则首先受水相颗粒物含量的控制[25]。经过硝酸钙处理的底泥因反硝化产气而形成更多孔隙(可明显观察到气道),因此泥水界面的总面积得以增加,物质的泥水交换强度也增强。以上结果(图2和表1)表明,在水相铵态氮较低的稀释水实验柱中,因泥相铵态氮趋向于朝水相转移,硝酸钙处理的水相铵态氮显著高于对照(两者之差达Pt<0.001);而在水相铵态氮本来就较高的原水实验柱中,泥水交换平衡未因泥水界面的增加而打破,硝酸钙处理的水相铵态氮与对照相比没有显著差异(Pt=0.988)。此外,SedCaN处理组的硝态氮也因孔隙增加而释放到上覆水,但48 h后便快速消耗,从(2.72±0.08)mg·L−1降至(0.59±0.03)mg·L−1,与ZHAN等[21]观察到的硝态氮释放及消耗趋势相近。由于硝态氮在封闭水柱中被表层底泥快速消耗,从而影响其实际风险的评估,故本研究将在现场中试中着重讨论硝态氮的释放规律。对于总磷,因实验柱处于静置状态,大部分颗粒物已沉积;硝酸钙的处理仅在原水实验柱中体现了促进总磷释放的效果(TPSedCaN(0.921±0.206)v.s. TPCK(0.863±0.166)mg·L−1),但两者差异不大(0.058 mg·L−1)。ZHOU等发现,加入硝酸钙后底泥中总磷略有增加[26]。YAMADA等[27]也在实验室泥柱实验中发现,投加硝酸钙后释放出的钙离子会快速结合游离在上覆水中的磷,而水相中总磷含量下降,沉积物中则形成较为稳定的钙结合态磷。
-
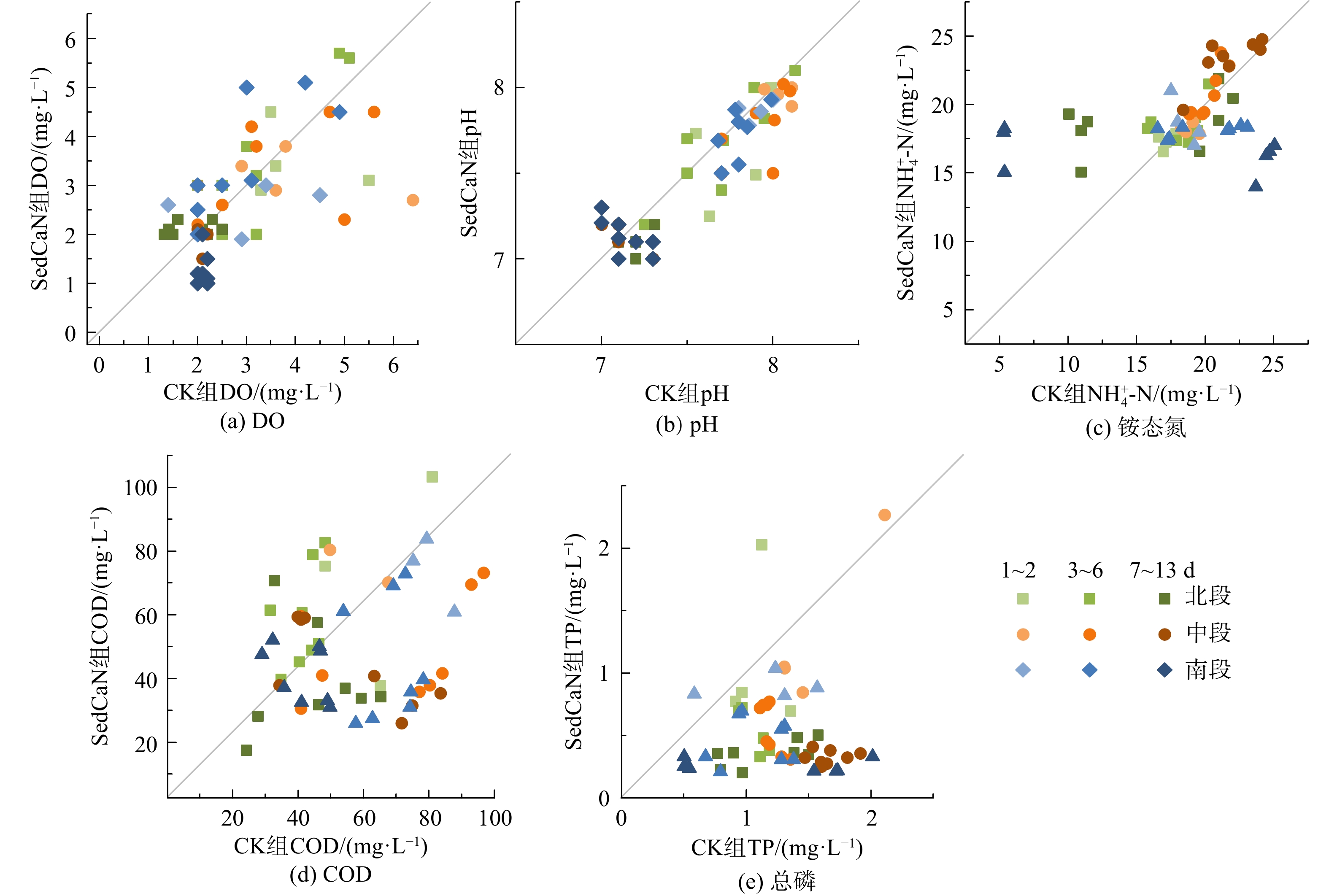
现场模拟实验与室内模拟实验最大的区别在于底泥的结构。现场底泥是自然沉积结果,而室内实验柱的底泥结构已因采样而被破坏。前者为自然分层结构,后者则是相对均匀的泥相。由图3可见,现场模拟实验结果因受更多外界因素影响,数据点相对离散。但除总磷外,SedCaN和CK组的水相指标具有显著相关性。这说明外界因素对溶解氧、pH、COD和铵态氮的影响对于SedCaN和CK组是相同的。总磷因其主要归趋于颗粒物和底泥,可能会与固相反应发生交互作用[21]。
差异性分析结果显示(表3),硝酸钙处理对水相COD和铵态氮没有显著影响,且略微降低pH(相差0.1个pH),这与室内泥柱实验结果相近。由于现场气体交换活跃,溶解氧在2组处理的差异性不显著。如上所述,总磷在处理与对照间表现出显著差异。由于钙离子的加入,溶解态的磷将趋向于形成相对稳定的钙磷形态被固定于沉积物中。因此,经过硝酸钙处理组,水相总磷被大幅降低(TPSedCaN 0.552 mg·L−1 < TPCK 1.224 mg·L−1),表现出显著锁磷效果。
-
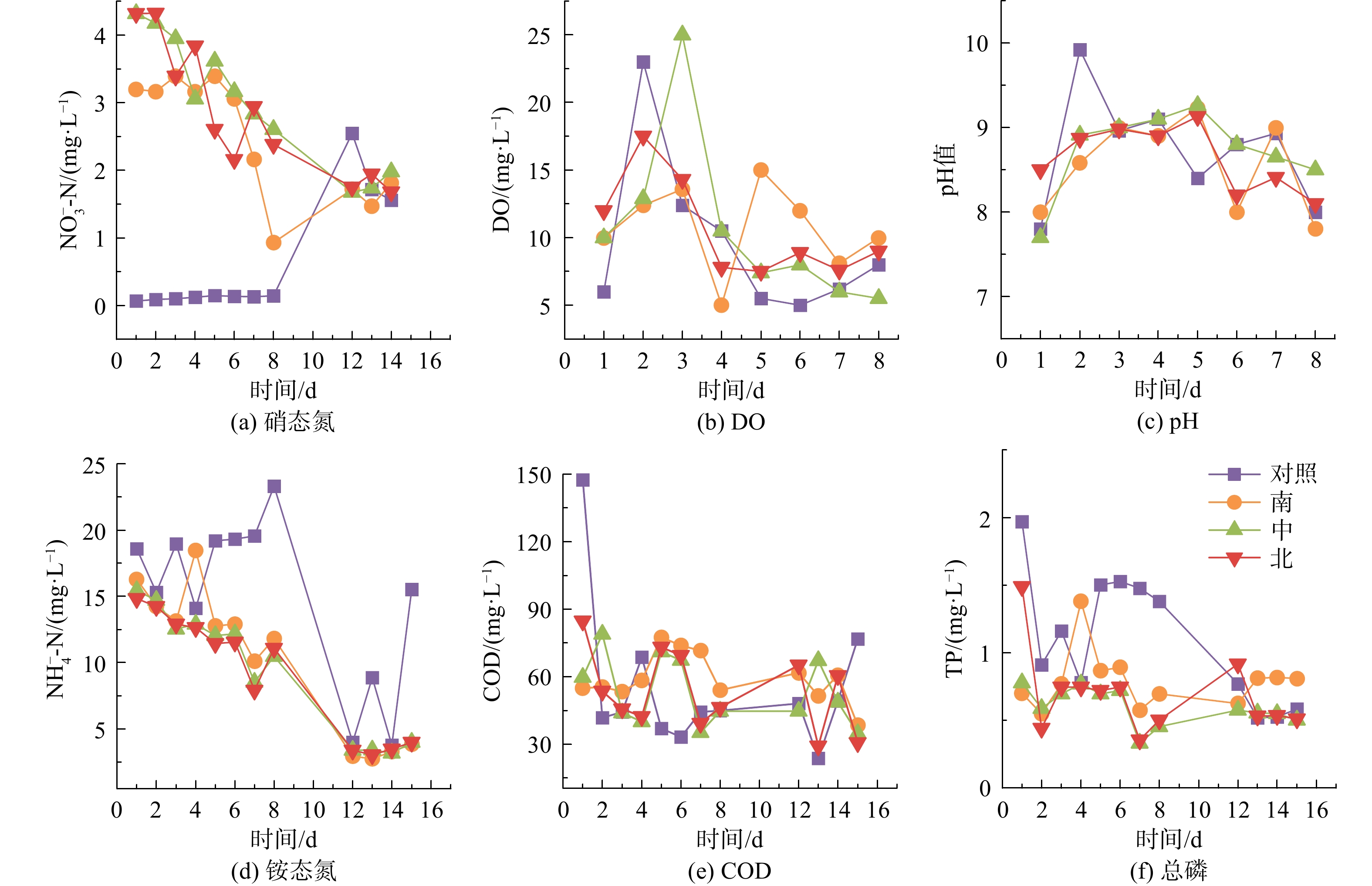
现场中试与现场泥柱实验的区别在于水相是与河道连通的,而中试研究结果反映实际河水的状况。由于实验期间有10 d发生暴雨极端天气,大雨将治理区和对照区的围隔冲断,水相被连通,致使10 d后治理区和对照区的水相指标数据趋于一致(图4)。因此,本研究主要关注底泥本身性质变化,或隔断区内的水质指标变化情况。
首先,实验期内治理区和对照区的溶解氧较高是由于河道藻密度较高,日照下光合作用产氧导致,同时在高含氧条件下,pH相应升高[28]。总体而言,治理区和对照区的水相溶解氧、pH和COD随时间发生相似波动,再次说明修复措施对水相溶解氧、pH和COD的影响不明显。然而,氮磷营养盐在2个区域间有明显区别。1)治理区的水相铵态氮在修复后的4~8 d开始下降,可能是由于硝酸根作为电子受体,促进了底泥耗氧物质(硫化物和有机污染物)氧化去除[10],使水体复氧能力整体上升,出现氨氧化速率提高的现象。此外,MAI等[23]发现,反硝化产生的亚硝酸盐可促进厌氧氨氧化,也可能是铵态氮消耗的原因。2)相比于对照区出现总磷释放的现象,治理区水相的总磷在修复过程中一直保持较低的、平稳的水平,说明钙离子作为锁磷因子,能有效将磷固定在底泥中。值得注意的是,虽然用于修复底泥的硝酸钙颗粒基于缓释工艺处理,但治理区的硝酸盐浓度仍明显高于对照区,即硝态氮的释放不可避免。然而,需要说明的是,相比于高浓度的铵态氮污染,释放的硝态氮相对较低,且随修复时间逐渐降低。本研究结果表明,铵态氮的降低量大于硝态氮释放量,因此,对氮污染总体是削减的,且对于重污染的河道修复,此SedCaN颗粒具有一定优势。
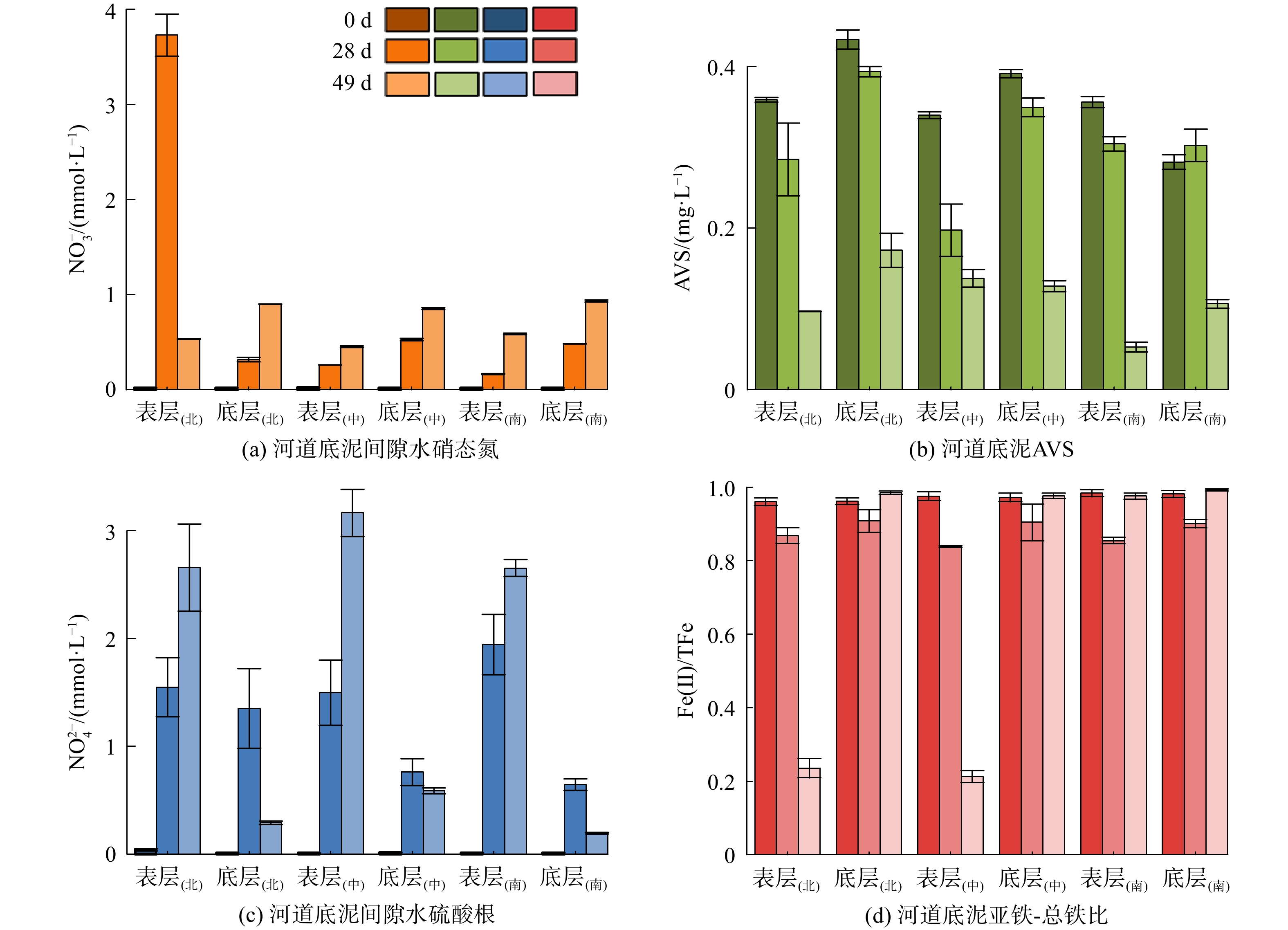
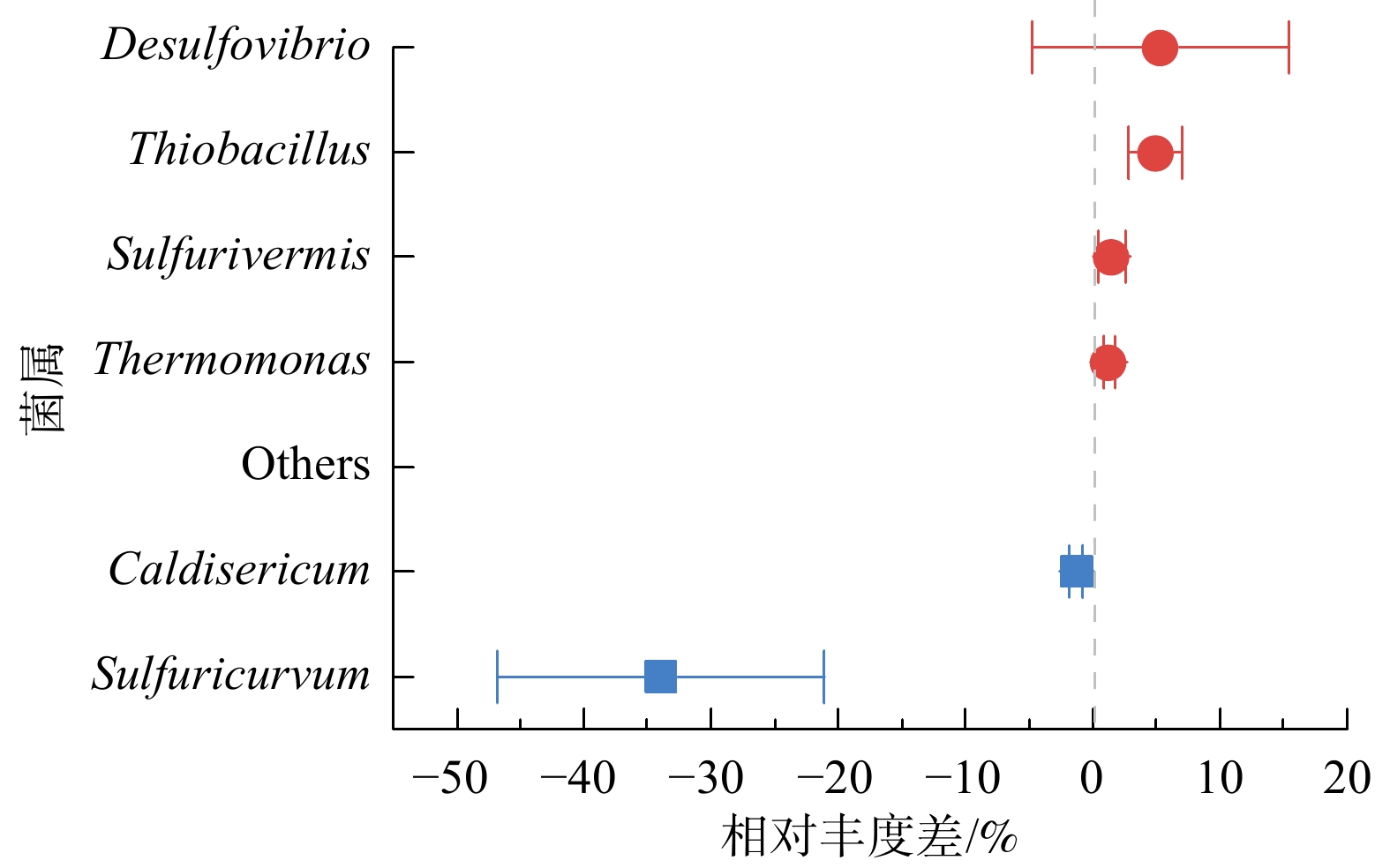
进一步分析底泥指标(图5),除北段表层受水力因素影响颗粒埋藏部位遭到破坏而引起硝酸盐的快速释放外,其他区域中(无论表层还是底层)底泥间隙水的硝态氮呈缓慢增加趋势。这说明SedCaN颗粒可持续为底泥微生物提供有效的硝酸盐。实验28 d治理区底泥的Thiobacillus、Sulfurivermis和Thermomonas菌属的相对丰度显著高于对照区5.3%、5.0%、1.5%和1.3%(图6)。Thiobacillus、Sulfurivermis和Thermomonas都是典型的硝酸盐还原-硫氧化菌,前期硝酸钙修复底泥的机理研究中均有报道[10-11, 13]。本研究印证了前期的结果,在足够的硝酸盐电子受体刺激下,自养反硝化菌利用硫化物作为电子供体,发生氧化还原反应,最终生成氮气和硫酸盐[11]。随着硝酸盐刺激作用的发生,硫化物(AVS)下降,其中表层下降(72.5%±1.3%),底层下降(63.2%±0.4%),最高出现于南段表层达85.2%;随后硫氧化产物间隙水硫酸盐也相应上升,硫酸盐还原菌Desulfovibrio相对丰度平均提高5.3%(图6)。虽然底泥硫化物的氧化率低于实验室模拟实验,如YIN等[22]以合肥南淝河的底泥为对象的硫氧化率达95%、ZHAN等[21]以上海浦东某河到底泥为对象的硫氧化率为75.9%~98.7%,但对于实际河道的修复已可达到消除黑臭的目标。如图5所示,间接表征氧化还原电位的亚铁/总铁比也随时间降低,表面底泥由还原态向氧化态转变,亦符合理论预期,验证了硝酸钙修复法(SedCaN颗粒)在实际黑臭底泥中的修复效果。此外,研究组在实验过程中采集了底泥柱状样品,对照区域底泥一直维持黑色,治理区底泥则逐渐由黑色转为灰黄色,直观实证了黑臭修复效果。CHEN等[29]也验证了硝酸钙修复法的有效性,通过在深圳河污染严重区域注射硝酸钙进行原位修复,修复14 d后大部分硝酸盐被消耗,AVS下降约86.5%,氧化还原电位显著上升。
值得注意的是,所有修复手段单独使用时都难免存在缺陷。硝酸钙刺激底泥反硝化反应过程中会产生氮气,导致底泥出现气孔,增加了泥水界面表面积和污染物扩散通量。在修复初期,存在底泥污染物和硝酸盐向其浓度较低水相扩散的风险。然而,由于底泥污染物加快释放实际上有利于底泥治理,故这一过程未必是缺陷。在实际工程中,施工段常被隔断,其风险可控,且水相污染物相对容易解决,如结合覆盖法可阻断底泥污染物的扩散[30-31],又如结合水相曝气可加速释放的还原态污染物氧化去除。因此,在运用硝酸钙修复法时应同时评估其效果和潜在风险,在控制风险的前提下达到最优底泥修复效果。
-
1)硝酸钙颗粒对实际河道黑臭底泥有显著的修复作用,体现在氧化底泥硫化物(氧化率最高达85.2%)和提高底泥还原氧化电位,使底泥由黑转黄,达到修复目标。硝酸钙修复底泥的过程不受上覆水水质的影响,且底泥在修复过程中因消耗了大量耗氧物质(硫化物和易降解有机质),使水体整体复氧能力提高,间接使水体中铵态氮的氧化速率提高。
2)钙离子的加入使磷素以较为稳定的钙磷形态转化,能改变水相总磷的归趋,以达到对水相中铵态氮和总磷的控制效果。然而,硝酸钙刺激法在修复底泥过程中,因反硝化产氮气而在底泥形成大量孔隙,引起硝态氮和其他水溶性污染物向上覆水释放,产生一定的环境风险。因此,在应用硝酸钙修复法时需结合其他治理手段,控制风险的扩散。
硝酸钙缓释颗粒原位修复黑臭底泥的作用机制及其应用
Mechanism and application of in situ remediation of black and smelly sediment by calcium nitrate sustained-release particles
-
摘要: 为解决水体中沉积底泥的内源污染释放问题,亟需高效底泥修复技术。硝酸盐为底泥微生物的电子受体,可通过反硝化作用氧化底泥的黑臭物质,是极具潜力的底泥修复剂。为探明硝酸盐在实际工程中的修复效果和潜在问题,结合实验室模拟和实际修复工程,分析了投加硝酸钙颗粒对黑臭底泥原位修复的环境过程。结果表明,投加硝酸钙缓释颗粒产品能显著提高底泥氧化还原势能(以Fe(II)/Fe(III)表征),促进黑臭物质转化,实际硫化物氧化率达85.2%,使得底泥由黑转黄,最终实现修复目标。同时,硝酸钙修复底泥的过程不受上覆水水质影响,且因修复过程消耗了大量底泥耗氧物质(硫化物和易降解有机质),使水体整体复氧能力提高。另一方面,钙离子的加入使磷素以较为稳定的钙磷形态转化,能改变水相总磷的归趋(TPSedCaN < TPCK,p < 0.01)。然而,由于反硝化产气增加了底泥孔隙,增加了泥水界面表面积和污染物扩散通量,故在修复初期存在底泥污染物和硝酸盐向其浓度较低的水相扩散,产生了一定风险,而实际上这也有利于泥相污染物的加速释放。因此,建议在可控工程段,联合覆盖法阻断污染物扩散或联合曝气加速水相污染物氧化,以确保在控制风险的前提下达到最优的底泥修复效果。Abstract: In order to solve the problem of endogenous pollution release of sediment in water body, the efficient sediment remediation technology is urgently needed. Nitrate is the electron acceptor of sediment microorganisms, which can oxidize the black-odor substance through denitrification process, therefore it is a potential agent for sediment remediation. In order to explore the remediation effects and potential problems of nitrate in practical engineering, this study conducted laboratory and field experiments to explored the environmental processes in in-situ sediment remediating by adding calcium nitrate pellets (SedCaN pellets). The results showed that the addition of calcium nitrate could significantly increase the redox potential in sediment (characterized by Fe(II)/Fe(III)) and promote the transformation of black-odor substances, meanwhile the color of sediment turned from black to yellow, which indicated that the remediation target was achieved. The actual sulfide oxidation rate was up to 85.2%. At the same time, the remediation was not affected by the quality of overlying water. A large number of oxygen-consuming substances (sulfide and easily degradable organic matter) were consumed in the process of repairing sediment, which improved the overall reoxygenation capacity of water body. The addition of calcium ions could stabilize the phosphorus as the form of Ca-P, which decreased the release of phosphorus from sediment to water phase (TPCaN < TPCK, p < 0.01). However, the gaseous nitrogen produced by denitrification increased the sediment porosity, which increased the diffusion flux of pollutants from sediment-water interface surface. At the initial stage of remediation, there was a certain risk due to the diffusion of sediment pollutants and nitrates, but in fact, it was also conducive to the accelerate the pollution release out of the sediment. Therefore, it was suggested to block the diffusion of pollutants by combining covering method or to accelerate the oxidation of water phase pollutants by combining aeration approaches in the controllable engineering section, so as to achieve the best sediment remediation effect on the premise of controlling the risk.
-
Key words:
- black-odor sediment /
- calcium nitrate /
- in-situ remediation /
- pilot test applicaition /
- bioremediation.
-
表 1 室内泥柱实验上覆水指标
Table 1. Overlying water index in indoor mud colum experiment
上覆水 DO/(mg·L−1) pH ORP/mV COD/(mg·L−1) 铵态氮/(mg·L−1) 硝态氮/(mg·L−1) 总磷/(mg·L−1) 黑臭原水 0.5 7.68 −219 64.00 13.39 N.D. 0.74 稀释水 0.4 7.89 −114 10.21 1.67 N.D. 0.09 注:N.D.表示浓度低于检测限。 表 2 室内泥柱实验上覆水指标的相关性与成对T检验差异
Table 2. The correlation and difference (paired T-test) of overlying water index from indoor mud column experiment
水样名称 水质指标 相关性r 相关的显著性Pr T检验的显著性Pt DO 原水 0.490 <0.01 0.042 DO 稀释水 0.684 <0.001 0.970 pH 原水 0.760 <0.001 0.001 pH 稀释水 0.844 <0.001 0.001 NH4+-N 原水 0.680 <0.001 0.988 NH4+-N 稀释水 0.770 <0.001 0.001 COD 原水 0.460 <0.01 0.281 COD 稀释水 0.570 <0.001 0.152 TP 原水 0.869 <0.001 <0.001 TP 稀释水 0.944 <0.001 0.233 表 3 现场泥柱实验上覆水指标的相关性与成对T检验差异
Table 3. The correlation and difference (paired T-test ) of overlying water index from field sediment column experiment
水质指标 相关性r 相关的显著性Pr T检验的显著性Pt DO 0.632 <0.001 0.355 pH 0.754 <0.001 <0.01 COD 0.344 <0.01 0.207 NH4+-N 0.343 <0.01 0.425 TP 0.114 0.388 <0.001 -
[1] 国家发展和改革委员会, 自然环境部, 住房和城乡建设部, 等. 2020年中国生态环境状况公报 [EB/OL]. 中华人民共和国生态环境部, 2021. [2] 董祎波, 吴慧芳, 张国庆, 等. 河湖底泥污染物及其原位修复技术的研究进展[J]. 广东水利水电, 2020, 12: 13-18. doi: 10.11905/j.issn.1008-0112.2020.03.003 [3] MORENO B, CANIZARES R, MACCI C, et al. Molecular tools to understand the bioremediation effect of plants and earthworms on contaminated marine sediments[J]. Journal of Hazardous Materials, 2015, 300: 398-405. doi: 10.1016/j.jhazmat.2015.07.019 [4] 雷沛, 张洪, 王超, 等. 沉积物水界面污染物迁移扩散的研究进展[J]. 湖泊科学, 2018, 30(6): 1489-1508. doi: 10.18307/2018.0602 [5] 孙健, 曾磊, 贺珊珊, 等. 国内城市黑臭水体内源污染治理技术研究进展[J]. 净水技术, 2020, 39(2): 77-80,97. doi: 10.15890/j.cnki.jsjs.2020.02.013 [6] 徐垚, 李大鹏, 韩菲尔, 等. CaO2不同投加方式对黑臭河道底泥内源磷释放抑制作用[J]. 环境科学, 2017, 38(7): 2836-2842. [7] 孙远军, 李小平, 黄廷林, 等. 受污染沉积物原位修复技术研究进展[J]. 水处理技术, 2008, 189(1): 14-18. doi: 10.16796/j.cnki.1000-3770.2008.01.004 [8] 顾鹏飞. 城市黑臭河流的原位化学修复研究[D]. 青岛: 山东大学, 2018. [9] YANG X, CHEN Z, WU Q, et al. Enhanced phenanthrene degradation in river sediments using a combination of biochar and nitrate[J]. Science of the Total Environment, 2018, 619: 600-605. [10] YANG X, LI E, LIU F, et al. Interactions of PAH-degradation and nitrate-/sulfate-reducing assemblages in anaerobic sediment microbial community[J]. Journal of Hazardous Materials, 2020, 388: 122068. doi: 10.1016/j.jhazmat.2020.122068 [11] YANG X, HUANG S, WU Q, et al. Nitrate reduction coupled with microbial oxidation of sulfide in river sediment[J]. Journal of Soils & Sediments, 2012, 12(9): 1435-1444. [12] XU M, ZHANG Q, XIA C, et al. Elevated nitrate enriches microbial functional genes for potential bioremediation of complexly contaminated sediments[J]. ISME Journal, 2015, 9(2): 532-532. [13] 王霖, 种云霄, 余光伟, 等. 黑臭底泥硝酸钙原位氧化的温度影响及微生物群落结构全过程分析[J]. 农业环境科学学报, 2015, 34(6): 1187-1195. doi: 10.11654/jaes.2015.06.024 [14] 刘近, 邓代永, 孙国萍, 等. 硝酸盐对沉积物中有机物氧化减量及微生物群落结构的影响[J]. 环境科学, 2013, 34(7): 2847-2854. doi: 10.13227/j.hjkx.2013.07.054 [15] LI W, ZHANG S, ZHANG L, et al. In-situ remediation of sediment by calcium nitrate combined with composite microorganisms under low-Do regulation[J]. Science of the Total Environment, 2019, 697: 134109. doi: 10.1016/j.scitotenv.2019.134109 [16] 张慧妍. 原位注射硝酸钙修复污染底泥过程中无机氮的迁移与转化[D]. 哈尔滨: 哈尔滨工业大学, 2015. [17] LIU T, YUAN J, DONG W, et al. Effects on inorganic nitrogen compounds release of contaminated sediment treatment with in situ calcium nitrate injection[J]. Environmental Science and Pollution Research, 2014, 22(2): 1250-1260. [18] HE Z, HUANG R, Liang Y, et al. Index for nitrate dosage calculation on sediment odor control using nitrate dependent ferrous and sulfide oxidation interactions[J]. Journal of Environmental Management, 2018, 226: 289-297. doi: 10.1016/j.jenvman.2018.08.037 [19] YANG X, HUANG S, WU Q, et al. Diversity and vertical distributions of sediment bacteria in an urban river contaminated by nutrients and heavy metals[J]. Frontiers of Environmental Science & Engineering, 2013, 7(6): 851-859. [20] LIU X, TAO Y, ZHOU K, et al. Effect of water quality improvement on the remediation of river sediment due to the addition of calcium nitrate[J]. Science of the Total Environment, 2016, 575: 887-894. [21] ZHAN Y, WU X, LIN J, et al. Combined use of calcium nitrate addition and anion exchange resin capping to control sedimentary phosphorus release and its nitrate-nitrogen releasing risk[J]. Science of the Total Environment, 2019, 689: 203-214. doi: 10.1016/j.scitotenv.2019.06.406 [22] YIN H, YANG P, KONG M. Effects of nitrate dosing on the migration of reduced sulfur in black odorous river sediment and the influencing factors[J]. Chemical Engineering Journal, 2019, 371: 516-523. doi: 10.1016/j.cej.2019.04.095 [23] MAI Y, LIANG Y, CHENG M, et al. Coupling oxidation of acid volatile sulfide, ferrous iron, and ammonia nitrogen from black-odorous sediment via autotrophic denitrification-anammox by nitrate addition[J]. Science of the Total Environment, 2021, 790: 147972. doi: 10.1016/j.scitotenv.2021.147972 [24] WU Y, WEN Y, ZHOU J, et al. Phosphorus release from lake sediments: Effects of pH, temperature and dissolved oxygen[J]. KSCE Journal of Civil Engineering, 2014, 18(1): 323-329. doi: 10.1007/s12205-014-0192-0 [25] 朱广伟, 秦伯强, 高光, 等. 长江中下游浅水湖泊沉积物中磷的形态及其与水相磷的关系[J]. 环境科学学报, 2004, 24(3): 381-388. doi: 10.3321/j.issn:0253-2468.2004.03.003 [26] ZHOU J, ZHANG M, JI M, et al. Evaluation of heavy metals stability and phosphate mobility in the remediation of sediment by calcium nitrate[J]. Water Environment Research, 2020, 92(7): 1017-1026. doi: 10.1002/wer.1297 [27] YAMADA TM, SUEITT A, BERALDO D, et al. Calcium nitrate addition to control the internal load of phosphorus from sediments of a tropical eutrophic reservoir: Microcosm experiments[J]. Water Research, 2012, 46(19): 6463-6475. doi: 10.1016/j.watres.2012.09.018 [28] 罗桂林, 田林锋. 基于WQI法的宁夏湖泊藻类爆发过程水环境质量变化及溯源探究[J]. 环境化学, 2021, 40(7): 2073-2082. doi: 10.7524/j.issn.0254-6108.2020100301 [29] CHEN L, WANG L, LIU S, et al. Profiling of microbial community during in situ remediation of volatile sulfide compounds in river sediment with nitrate by high throughput sequencing[J]. International Biodeterioration & Biodegradation, 2013, 85: 429-437. [30] ZHAN Y, WU X, LIN J. Combined use of calcium nitrate, zeolite, and anion exchange resin for controlling phosphorus and nitrogen release from sediment and for overcoming disadvantage of calcium nitrate addition technology[J]. Environmental Science and Pollution Research, 2020, 689(1): 203-214. [31] 麦顺之, 黄家明, 吴群河, 等. 活性材料覆盖法原位修复HOCs污染沉积物的研究进展[J]. 环境科学与技术, 2019, 42(6): 224-230. -





 下载:
下载: