-
颗粒物是环境污染与控制相关研究的重要对象[1]。尽管给水处理工艺通常能够保证出厂水的水质达标,但出厂水经过管网到达用户端的输配过程中难以避免发生水质变化[2]。其中,管网疏松沉积物再悬浮引发自来水变色(如“黄水”)是全世界自来水投诉中最常见的问题[3]。然而,管网疏松沉积物的结构特征及其潜在健康危害目前尚不明确。
管网疏松沉积物来源复杂,包括出厂水中的残余物质和管道的腐蚀产物等。由于给水管网中广泛使用铁质管材和管件,管网铁腐蚀产物释放是导致用户龙头“黄水”的主要原因[4-7]。ZHUANG等[8]利用合成的铁颗粒物实验首次提出,铁颗粒物导致的“黄水”不仅是感官性状问题,且铁颗粒物可通过2种机制产生潜在毒性:1)铁颗粒物(主要是针铁矿)与微量有机污染物通过特定的共价键结合方式强化电子转移,产生活性氧物种(reactive oxygen species,ROS)而增强细胞损伤[8-9];2)微量有机污染物能够显著提升铁颗粒物的比表面积,从而增强其对水中污染物的富集能力[10]。实际管网条件下生成的疏松沉积物组成往往非常复杂,以往对于“黄水”带来的风险都是基于管网的水质和水力条件进行评价和预测[11],然而“黄水”可能引发的毒性风险至今尚无评价标准[12-13]。水质的评价不能仅以饮用水标准限值为判据, 更为重要的是以水质安全风险的综合控制为依据[14]。因此,“黄水”中沉积物颗粒的风险亟需受到重视。
本研究在北方某城市频繁发生“黄水”的区域采集了管网疏松沉积物,对样品的表面形貌、元素组成、表面电位和粒径等结构特征进行了表征,利用人体健康肝脏细胞对样品的细胞毒性进行了测试,并开展了疏松沉积物的细胞毒性与其结构特征之间的相关性分析,初步明确了给水管网疏松沉积物的风险因素。
-
对中国北方某城市频繁发生“黄水”的小区进行了实地调研,截取了7个小区的入楼管管道,管材为镀锌钢管,管径均为DN40,管龄约为(15±5) a。利用软毛刷刷取管道表层疏松沉积物,将获得的疏松沉积物冷冻干燥,再通过90目(160 μm)筛网进行筛分,样品编号1#~7#。
-
管网疏松沉积物样品的表面形貌和元素组成利用场发射扫描电子显微镜(SEM,H-7500)获得,微观结构照片利用显微镜(Leica MGD41)拍摄;表面电位和粒径使用zeta电位分析仪(Malvern,Zetasizer2000)测定;样品晶体结构利用X射线衍射光谱仪(XRD, Rigaku,D/Max-2200)测试;样品粗糙度(Ra)利用原子力显微镜(AFM,Nanosurf C3000, Switzerland)测定。以DMPO作为捕获剂添加浓度为10 mmol·L−1的H2O2,利用电子顺磁共振谱仪(ESR,Bruker A300-10/12)在无光照条件下对样品产生自由基的能力进行测定。
-
以体外细胞毒性实验(MTT法)进行了疏松沉积物样品的毒性检测。实验所用的LO2人体健康肝脏细胞购买自赛柏慷生物有限公司。主要步骤为:在5% CO2、37 ℃条件下,加入疏松沉积物分散液(100 mg·L−1)和细胞共培养24 h;然后吸走原有培养基,加入PBS轻微地清洗2次,再加入200 μL含0.5 mg·mL−1 MTT的培养基,继续培养4 h后,吸走原有培养基,最后加入150 μL DMSO,振荡5 min,利用全波长酶标仪(EPOCH2, Biotek)在570 nm进行检测。实验结果以细胞存活率表示(见式(1))。
-
管网疏松沉积物样品1#~7#的SEM照片如图1所示。样品微观形貌中大多存在锋利的针刺状结构,这种结构可能来自于亚单元纳米颗粒取向聚集生长[15]。在所有样品SEM照片中,样品6#的表面针刺最密集且最为锋利,其在显微镜照片(图1内嵌图)中的结构也更加分散和细密,这可能是由于细密锋利的微观结构有助于抑制颗粒之间的团聚作用[16],而具有松散结构的沉积物更易于再悬浮到水中,导致“黄水”的风险更高。
在所有样品的元素组成中(见表1),占比最大的均为铁元素,质量占比为55%~80%,这与以往研究中镀锌钢管管垢中含量最高为铁元素一致[17]。除铁元素以外,样品中还检测到一定量的锰、铜、铝、铅、砷等金属元素。对样品6#进行进一步的元素面扫(见图2)发现,铁元素和氧元素分布均匀,故可推测,样品的主要成分为铁氧化物。此外,样品中的针刺状结构可能源于铁氧化物的取向聚集生长。
-
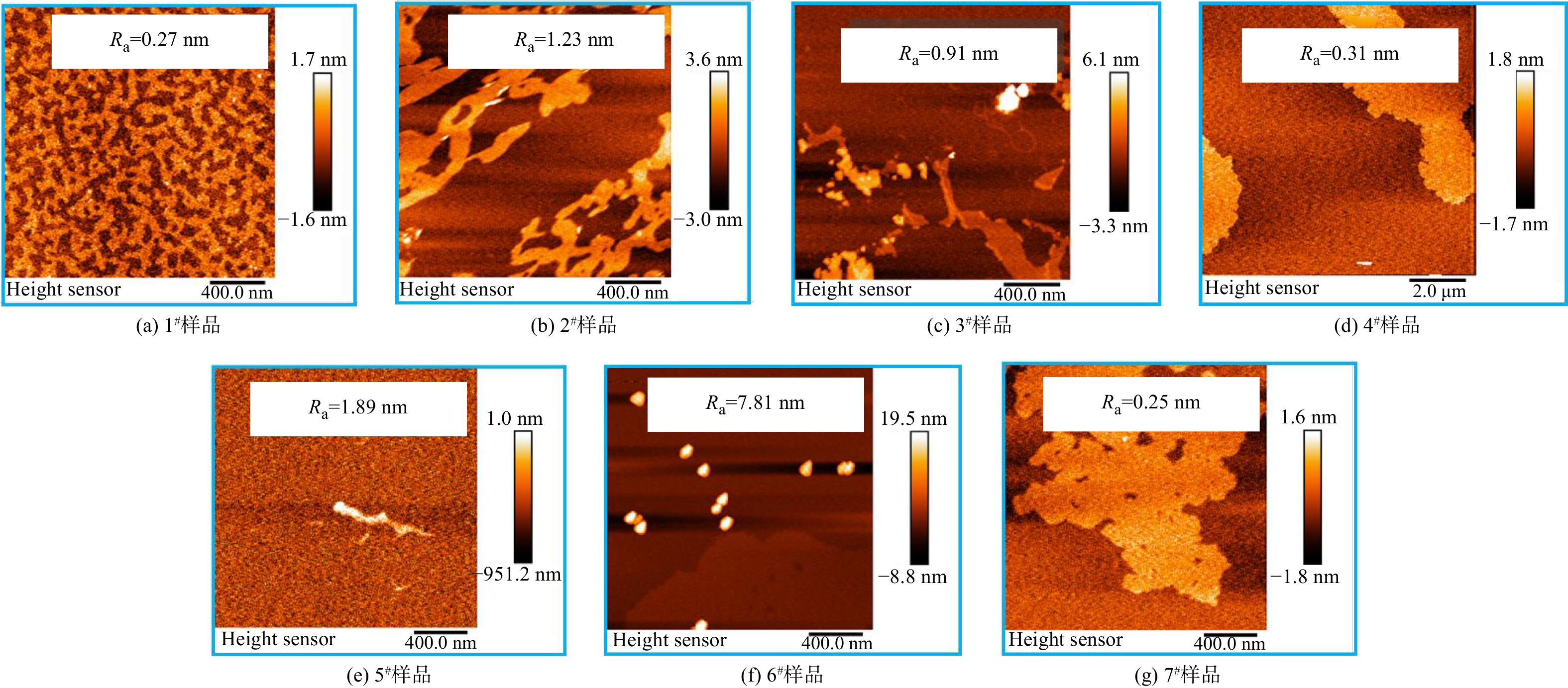
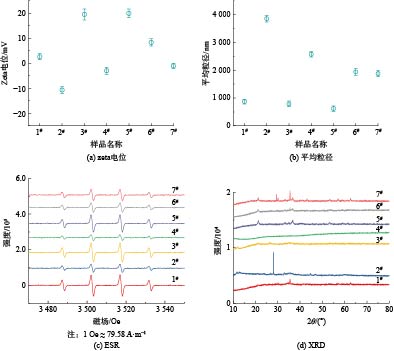
AFM测试结果(见图3)表明,样品粗糙度(Ra)为0.25~7.81 nm,具有最为细密锋利微观形貌的样品6#粗糙度最大,其表面粗糙度明显高于其他样品可能是由于细密锋利的针刺结构导致。样品的zeta电位分布在−15~20 mV,可见,管网疏松沉积物的表面电位既有可能呈正电性也有可能呈负电性。样品平均粒径范围为500~4 000 nm,表明其中包含具有较高毒性风险的纳米尺寸细颗粒。有研究表明,水中颗粒物粒径越大时水体色度变化越明显[18],可见,2#样品的致色风险最高。由于氧化应激是纳米颗粒损伤细胞的重要机制[19],故对样品产生羟基自由基的能力进行了测试(见图4),发现所有样品均能够与双氧水反应产生羟基自由基,其反应位点可能是沉积物中丰富的铁基组分[20]。通过XRD对管网疏松沉积物的晶体成分进行分析,结果如图4和表2所示,表明样品中主要晶体成分是多种铁氧化物,包括Fe2O3(α-Fe2O3、γ-Fe2O3)、FeOOH(α-FeOOH、β-FeOOH、γ-FeOOH、δ-FeOOH)、Fe3O4等,也含有少量SiO2和CaCO3晶体。大多样品中的铁氧化物晶体以γ-Fe2O3为主,但样品6#中晶体占比最高的是γ-FeOOH,故推测样品6#细密锋利的针刺状结构可能与γ-FeOOH晶体生长有关。
-
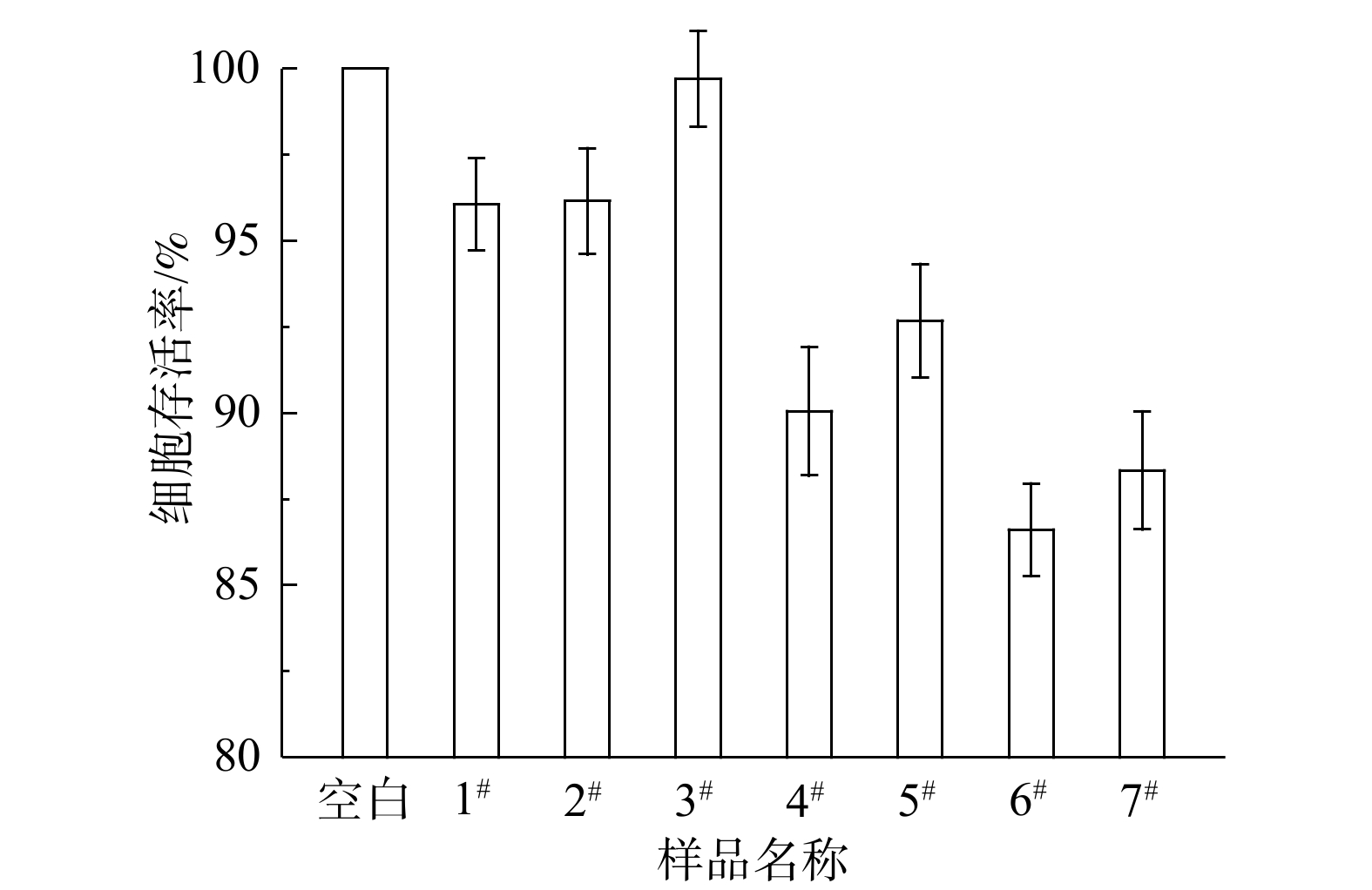
现有对饮用水毒性风险的研究大多聚焦于饮用水中的消毒副产物[21-22]和持久性有机污染物(POPs)[23-24]等有机污染物,以及重金属[25]等无机污染物。饮用水中颗粒物的毒性风险尚未引起重视。通常情况下,当滞留水放出后“黄水”会逐渐消失[26],但由于管网疏松沉积物含有细颗粒,即使是在龙头水放水放至无色时,疏松沉积物颗粒仍会不可避免地存在于水中,用户在使用龙头水时很有可能发生颗粒物的暴露。利用人体健康肝脏细胞测试了管网疏松沉积物样品分散液的MTT细胞毒性。利用样品配置分散液时,在100 mg·L−1下肉眼可见明显颜色,故在此浓度下研究了样品的细胞毒性。当样品分散液的质量浓度为100 mg·L−1时,人体健康肝脏细胞的存活率为86.61%~99.71%(如图5所示),可见疏松沉积物的毒性风险不可忽视。具有最为细密锋利结构的样品6#的细胞存活率最低,故推测疏松沉积物样品的形貌对于毒性具有重要影响。
-
主成分分析法旨在保证原始数据信息丢失最小的情况下对原始的高维变量进行降维处理,以少数的综合变量代替原有的多维变量,简化评价工作[27]。虽然粒径是影响颗粒物毒性的最常见因素[28],但在管网疏松沉积物样品的铁含量、zeta电位、粗糙度和平均粒径中(见表3),与毒性相关性最显著的是粗糙度,样品的粗糙度与细胞存活率呈现负相关,Pearson相关系数为−0.507。即粗糙度越大的疏松沉积物,毒性越高,表明形貌对样品毒性的影响比粒径更大。这是由于样品中普遍存在着针刺状结构,所以粗糙度越高的样品具有更丰富更锋利的表面,导致其对细胞的划伤能力更强;此外,样品的平均粒径与zeta电位具有负相关性(Pearson相关系数为−0.851),即粒径越大的样品zeta电位较低,可见表面电荷相同时,带负电的沉积物颗粒比带正电的更难以悬浮进入水中,健康风险较低。
如表4所示,在管网疏松沉积物的晶体组成与毒性的相关性中,与样品毒性相关性最显著的是γ-FeOOH,与细胞存活率具有负相关性(Pearson相关系数为=−0.762),即γ-FeOOH含量越高的管网疏松沉积物,毒性越大。结合粗糙度与毒性具有相关性的结果推测,γ-FeOOH可能是通过增加颗粒表面锋利程度进而增大样品毒性。李玉仙等[29]发现给水管网余氯较低时不稳定成分γ-FeOOH含量明显增加;牛璋彬等[30]发现给水管网余氯较低时铁释放现象严重。因此,在余氯不足时,“黄水”具有更高的毒性风险,一方面是由于γ-FeOOH晶体成分增多导致疏松沉积物形成毒性更高的颗粒物结构,另一方面是因为铁释放加剧形成更多的疏松沉积物导致颗粒物浓度增大。
-
1) “黄水”小区的管网疏松沉积物中含量最高的金属元素是铁元素,主要晶体成分是铁氧化物。样品微观形貌中大多存在锋利的针刺状结构;疏松沉积物的zeta电位为−15~20 mV、平均粒径为500~4 000 nm,粗糙度为0.25~7.81 nm。
2) 管网疏松沉积物在100 mg·L−1下对应人体健康肝脏细胞的细胞存活率为86.61%~99.71%。粗糙度与疏松沉积物毒性的相关性最显著,表明形貌对疏松沉积物毒性具有显著影响;γ-FeOOH是与管网疏松沉积物毒性相关性最显著的晶体组分,其对毒性的贡献是通过增加样品形貌锋利程度造成的。余氯不足时可能会因铁释放加剧和γ-FeOOH含量增大,造成更高的毒性风险。
给水管网疏松沉积物的结构特征及其风险识别
Structure characteristics and health risk of loose deposits in drinking water distribution system
-
摘要: 自来水变色问题通常被视为感官问题,而导致自来水变色的管网疏松沉积物的结构特征及其潜在危害尚不明确。采集了我国北方某城市频繁发生自来水“黄水”的7个小区管网中的疏松沉积物,并进行了分析。结果表明:所有疏松沉积物样品中含量最高的金属元素都是铁元素、主要晶体成分是铁氧化物,样品颗粒微观形貌大多具有锋利的针刺状结构;样品zeta电位范围为−15~20 mV、平均粒径范围为500~4 000 nm、粗糙度范围为0.25~7.81 nm。体外细胞毒性实验结果显示,沉积物可产生一定的细胞毒性(样品浓度100 mg·L−1时人体健康肝脏细胞存活率为86.61%~99.71%)。通过主成分分析发现,疏松沉积物毒性与粗糙度的相关性比与粒度的高,表明形貌对样品毒性的影响比粒径更大;γ-FeOOH是与疏松沉积物毒性相关性最显著的晶体组分,其对毒性的贡献可能是通过增加颗粒表面锋利程度造成的,余氯不足时可能会因铁释放加剧和γ-FeOOH含量增大造成更高的毒性风险。本研究结果可为全面认识给水管网疏松沉积物的风险提供参考。Abstract: Discoloration of tap water caused by loose deposits is usually regarded as a sensory problem, but structural characteristics and health risk of the loose deposits are not clear. In this study, we collected loose deposits from the residential areas from the section where frequently occurs “yellow water” in a northern city in China. Characterization results showed that in loose deposit samples, the highest metal element was iron and the main crystal component was iron oxide. The morphology of the samples contained sharp fiber-like structures. The zeta potentials of the samples were −15~20 mV, the average sizes were 500~4 000 nm, and the roughness values were 0.25~7.81 nm. The samples had certain toxicity to health human liver cells (the cell viability was 86.61%~99.71% under loose deposits 100 mg·L−1). Principal component analysis showed that roughness had the highest correlation with toxicity, which indicated that morphology had greater influence on sample toxicity than size. Among crystal components, γ-FeOOH had the highest correlation with toxicity, and its contribution to toxicity may due to sharpness increase. When the residual chlorine is insufficient, it will lead to higher toxicity risk due to the increase of iron release and γ-FeOOH content. Therefore, iron particles have great effects on the toxicity of loose deposits. This study provides an important basis for the comprehensive understanding on the risk of loose deposits in drinking water distribution system.
-
Key words:
- drinking water distribution system /
- loose deposits /
- yellow water /
- toxicity
-
氯代多环芳烃(Cl-PAHs)是饮用水氯消毒[1]、电子垃圾的处理[2-3]、金属冶炼[4]、垃圾焚烧[5-6]以及烹饪[7]等人类活动过程中产生的副产物,它具有与多氯联苯和二噁英相似的平面结构和类似的环境行为[8],其毒性与多环芳烃母体相当甚至高于母体。目前已在大气[9-10]、沉积物[11]、汽车尾气[12]、冶炼厂废气[4]、垃圾焚烧厂的飞灰和烟道气[6]及烧烤食品[7]中检测到氯代多环芳烃。氯代多环芳烃作为一类新型的高风险有机污染物广泛存在于环境中,对人类健康具有一定的潜在威胁。
氯代多环芳烃(Cl-PAHs)和多环芳烃(PAHs)主要通过工业废水排放和大气沉降进入地表,造成土壤污染。低水溶性和相对较高的辛醇-水分配系数(lgKow)可导致其在土壤中的积累。目前土壤中多环芳烃的测定方法有索氏抽提-高效液相色谱法[13]、微波萃取-高效液相色谱法[14]、加速溶剂萃取气相色谱-质谱法[15-16] 、加速溶剂萃取高效液相色谱法[17] 等。土壤中氯代多环芳烃的测定方法主要有加速溶剂萃取气相色谱-质谱法[18-19]、超声萃取高效液相色谱法[3]、索氏抽提萃取气相色谱-质谱法[20] 等。加速溶剂萃取设备昂贵;索氏抽提虽然设备简单但要消耗大量的有机溶剂。此外这些方法均需要进一步的浓缩、净化,操作过程繁琐,费时费力。因此发展一种简便、快速、成本低廉、环境友好的样品前处理方法对于土壤中氯代多环芳烃(Cl-PAHs)和多环芳烃的测定很有意义。
超分子溶剂(supramolecular solvent, SUPRAS)是指含亲水基和疏水基的两亲性分子在水溶性有机溶剂作用下分散在水相中,通过疏水相互作用按照一定的顺序形成的一种具有纳米结构的胶束聚集体。超分子溶剂微萃取(supramolecular solvent-based microextraction, SSBME)是由西班牙学者Rubio 等[21]提出的一种以超分子溶剂为萃取剂的新型萃取技术。超分子溶剂的一个显著特点是其具有高浓度的亲和位点,使其在较小的溶剂体积下能取得高的萃取效率,因此特别适用于微萃取;此外超分子溶剂具有纳米孔腔结构,它可以使小分目标化合物进入其中,但对腐殖酸、蛋白质、糖类等大分子具有限制进入作用,从而在萃取的同时可以达到净化的目的;超分子溶剂还有一个优点,它具有非挥发性和不易燃性,使用安全。超分子溶剂微萃取具有简便、快速、环境友好、成本低廉等优点,已经在环境、食品等领域得到了广泛应用。目前已用于鱼和贝类中噁喹酸和氟甲喹[22]、水中磺胺类[23]、生小麦中的赭曲霉毒素A[24]、人尿液中羟基多环芳烃[25]等化合物的分析。
本文尝试采用SSBME结合高效液相色谱法建立一种同时测定土壤中氯代多环芳烃(Cl-PAHs)和多环芳烃(PAHs) 的简便快速方法。
1. 实验部分(Experimental section)
1.1 仪器与试剂
Agilent 1200 型高效液相色谱仪( 美国安捷伦公司),配二极管阵列紫外和荧光检测器;Vortex Genie 2涡旋振荡器 (美国 Scientific Industries);KMS-181E 磁力搅拌器(精凿科技上海有限公司);飞鸽牌TDL-4013离心机(上海安亭科学仪器厂);乙腈(LC- grade,美国 Honeywell 公司);实验用水为经Milli-Q净化系统制备的去离子水。1-己醇、1-庚醇、1-辛醇、四氢呋喃购于阿拉丁试剂(中国)有限公司,纯度 ≧98.0%;1-葵醇购于梯希爱(上海)化成工业发展有限公司,纯度 98.0%。
16种多环芳烃混标(200 µg·mL−1,其中苊烯无荧光,不在测定之列)及2-氯蒽、9-氯菲、9-氯蒽、9,10-二氯蒽、1-氯芘(纯度大于95%)均购于百灵威化学试剂有限公司。
1.2 色谱条件
色谱条件:色谱柱为多环芳烃专用分析柱(SUPELCOSILTMLC-PAH,150 mm×4.6 mm, 5 μm);流动相为乙腈-水,采用梯度洗脱,乙腈变化为:0—18 min,40%—64%;18—25 min,64%;25—35 min,64%—100%;35—44 min,100%。流速为2 mL·min−1; 进样量10 μL。
20种目标化合物的荧光激发和发射波长见表1,高效液相色谱图见图1。
表 1 荧光激发和发射波长Table 1. Fluorescent Excitation wavelength and Emission wavelength时间/min Time 激发波长/nm Ex 发射波长/nm Em 0.00 275 330 13.90 255 375 17.90 245 450 19.80 245 370 23.50 265 390 32.40 273 440 36.50 290 410 38.50 240 480 40.00 265 420 1.3 供试土壤样品的制备
40 g 风干的山参种植土用100 mL 丙酮-二氯甲烷(1:1)超声提取3次后,加入100 mL含2400 ng 氯代多环芳烃和多环芳烃的丙酮-二氯甲烷(1:1)溶液,搅拌混匀后于通风橱中氮气吹至近干,继续放置干透后储存于磨口玻璃瓶。此土壤样品含目标化合物60 ng·g−1,用于超分子溶剂的制备及萃取的优化。
1.4 超分子溶剂的制备
移取3 mL1-辛醇于50 mL聚四氟乙烯离心管中,加入8 mL四氢呋喃、29 mL去离子水,然后以900 r·min−1磁力搅拌5 min,静置2 min后3000 r·min−1 离心5 min,用玻璃滴管将上层形成的超分子溶剂转移到具塞玻璃瓶中,放于冰箱4 ℃储存备用。
1.5 超分子溶剂微萃取过程
于5 mL 聚丙烯离心管中加入200 mg 土壤,3粒玻璃珠(3 mm直径),加入400 μL 超分子溶剂,3200 r·min−1蜗旋振荡2 min,然后5000 r·min−1 离心5 min,用1 mL注射器移出上清液,过0.22 μm 滤膜后高效液相色谱测定。
1.6 标准工作曲线用标准样品制备
将16种多环芳烃混标和5种氯代多环芳烃用乙腈配制成10000 µg·L−1的混标储备溶液,并逐级稀释成1000、100、10 ng·mL−1使用液。将此混标使用溶液添加到用丙酮-二氯甲烷(1:1)超声提取过的空白山参种植土中,使添加浓度分别为2.5 、10 、50 、 250、500、1000 ng·g−1, 4 ℃冰箱放置过夜,然后按1.5节方法萃取,用于标准工作曲线的测定。
2. 结果与讨论(Results and discussion)
2.1 萃取条件的优化
以添加60 ng·g−1,目标化合物的200 mg供试土壤样品为萃取对象,以目标化合物的峰面积为指标,考察了超分子溶剂的组成(脂肪醇种类、脂肪醇的量、四氢呋喃量)、萃取溶剂体积、涡旋振荡时间等因素对萃取效率的影响。
2.1.1 不同链长脂肪醇制备的超分子溶剂对萃取效率的影响
超分子溶剂通常由两亲分子在分散剂存在下在水相体系中通过自组装生成。本研究采用烷基醇与四氢呋喃制备超分子溶剂。为此恒定总体积为40 mL,考察了1.5 mL1-己醇、1-庚醇、1-辛醇、1-葵醇在水中分别与8 mL四氢呋喃制备的超分子溶剂对萃取效率的影响。结果表明随着脂肪醇碳链的增加,制备的超分子溶剂萃取效率逐渐增大。超分子溶剂中有两类亲和位点,一种是极性端羟基产生的氢键作用力,另一种是醇碳链部分的疏水作用力(范德华力、色散力)。对于萃取多环芳烃及氯代多环芳烃这类非极性和弱极性化合物而言,醇碳链部分的疏水作用力起主要作用,而碳链越长,这种作用力越强,因而萃取效率越大。但实验发现1-葵醇制备的超分子溶剂导致部分目标化合物色谱峰展宽且重叠,无法准确定量。故以下实验选1-辛醇制备超分子溶剂。
2.1.2 1-辛醇用量对超分子溶剂体积和萃取效率的影响
四氢呋喃的量保持8 mL,制备体系总体积为40 mL,考察了1-辛醇用量为0.5、1、1.5、2、2.5、3 mL时对萃取效率的影响。结果表明,改变1-辛醇用量,对制备的超分子溶剂的萃取效率无明显影响;但是随着1-辛醇用量的增加,生成的超分子溶剂体积增大,见图2。有文献[26]报道SUPRAs的体积Y(mL) 与烷基醇的用量X(mg) 和四氢呋喃在溶液中的体积百分比Z之间呈如下关系:Y = X(0.17 + e0.0389Z),即超分子溶剂的体积与醇的用量呈线性关系,本实验结果与文献报道一致。为了一次能制备更多的超分子溶剂,选定1-辛醇用量为3 mL。
2.1.3 四氢呋喃用量对萃取效率的影响
作为超分子溶剂的组成部分,四氢呋喃的用量不仅与制备的超分子溶剂体积有关,而且对超分子溶剂的萃取效率亦有一定影响。为此固定1-辛醇用量为3 mL,制备体系总体积为40 mL,考察了不同四氢呋喃的量对萃取效率的影响,如图3所示。结果表明,四氢呋喃用量的增加对低分子量的目标化合物的萃取效率影响不大;但对于高分子量的目标化合物,随着四氢呋喃用量的增加,萃取效率增大;当四氢呋喃大于8 mL后趋于稳定。因此本实验制备超分子溶剂时选定四氢呋喃的量为8 mL。
2.1.4 超分子溶剂体积对萃取效率的影响
为取得理想的萃取结果,考查超分子溶剂体积分别为300、350、400、500、600、700、800 μL时对萃取效率的影响。结果表明,随着萃取溶剂体积的增大,目标化合物的峰面积明显下降,即检测灵敏度下降;但同时回收率逐渐增大,当超分子溶剂体积大于400 μL时回收率趋于平稳。虽然增加萃取溶剂的体积可以萃取出更多的目标化合物,提高萃取回收率,但同时也会使目标化合物在萃取相中浓度的下降,而二者相比后者影响更大,进而导致检测灵敏度下降。综合以上结果,选定萃取溶剂的体积为400 μL。
2.1.5 涡旋振荡时间的影响
涡旋振荡可以促进萃取溶剂与样品的充分接触,提高萃取效率。为此,考查了涡旋振荡时间分别为1、2、3、4、5、6、7、8 min时对萃取效率的影响,结果表明涡旋振荡时间大于2 min后,目标化合物的峰面积变化很小。
基于以上实验结果,优化后的实验条件为,以3 mL 1-辛醇、8 mL四氢呋喃和29 mL水混合制备超分子溶剂;萃取溶剂的体积为400 μL,涡旋振荡2 min。
2.2 方法的线性范围、检出限及定量限
在优化的萃取条件下,对添加 5 种氯代多环芳烃和15种多环芳烃系列浓度的空白土壤样品进行超分子溶剂微萃取,然后HPLC荧光测定,以质量浓度 C(ng·g−1)对峰面积 A 绘制校正曲线,得到20种目标化合物的线性回归方程、线性范围及相关系数;并以目标化合物的S/N=3时的浓度定义为方法的检出限,S/N=10时的浓度定义为方法的定量限,见表2。结果表明,范围内,目标化合物在2.5—1000 µg·kg−1(9-氯菲、1-氯芘在10—1000 µg·kg−1)范围内线性关系良好,线性相关系数均大于 0.999;方法的检出限为0.07—2.3 µg·kg−1,定量限为 0.2—7.0 µg·kg−1。
表 2 目标化合物的线性范围、线性方程、相关系数、检出限及定量限Table 2. Linear ranges ,regression equation, correlation coefficients(r), limits of detection (LOD, S/N=3) and limits of quantitation (LOQ, S/N=10) of target compoundsNo. 化合物Compound 线性范围/(µg·kg−1)Linear range 标准曲线方程Regression equation 相关系数R2 检出限/(µg·kg−1)LOD 定量限/(µg·kg−1)LOQ 1 萘(Na) 2.5—1000 A=0.3182C+6.4532* 0.999 0.3 0.9 2 苊(Ace) 2.5—1000 A=0.7244C+2.6573 0.999 0.6 1.8 3 芴(Fl) 2.5—1000 A=1.5523C+0.7832 0.999 0.3 1.0 4 菲(Phe) 2.5—1000 A= 1.1875C+14.6108 0.999 0.2 0.6 5 蒽(Ant) 2.5—1000 A=2.0918C+0.2058 0.999 0.2 0.8 6 荧蒽(Fu) 2.5—1000 A=0.4013C+3.0251 0.999 0.5 1.9 7 芘(Py) 2.5—1000 A=1.0748C+6.6492 0.999 0.2 0.7 8 9-氯菲(9-ClPhe) 10—1000 A=0.0600C+1.0583 0.999 2.3 7.0 9 9-氯蒽(9-ClAnt) 2.5—1000 A=0.4078C+0.8628 0.999 0.7 2.2 10 2-氯蒽(2-ClAnt) 2.5—1000 A=0.8810C+0.2803 0.999 0.5 1.5 11 苯并[a]蒽(BaA) 2.5—1000 A=1.3297C-0.4912 0.999 0.4 1.3 12 䓛(Chr) 2.5—1000 A=1.7998C+5.9356 0.999 0.2 0.6 13 1-氯芘(1-ClPy) 10—1000 A=0.2456C-0.7780 0.999 2.1 5.4 14 苯并[b]荧蒽(BbF) 2.5—1000 A=0.8110C+1.7058 0.999 0.1 0.4 15 9,10-二氯蒽(9,10-DClAnt) 2.5—1000 A=1.6689C+0.0170 0.999 0.1 0.3 16 苯并[k]荧蒽(BkF) 2.5—1000 A= 1.8488C+1.3040 0.999 0.07 0.2 17 苯并[a]芘(BaP) 2.5—1000 A=1.3673C-0.2231 0.999 0.09 0.3 18 二苯并[a,h]蒽(DahA) 2.5—1000 A=1.1604C+2.9443 0.999 0.1 0.4 19 苯并[ghi]苝(BghiP) 2.5—1000 A=0.6349C+0.3495 0.999 0.2 0.6 20 茚并[1,2,3-cd]芘(Ipy) 2.5—1000 A= 0.3413C-0.2224 0.999 0.3 1.0 * A: peak area ;C:concentration(µg·kg−1). 2.3 实际样品的测定及方法的加标回收率和精密度
用建立的超分子溶剂微萃取高效液相色谱分析方法对山参土(2018年5月采于吉林浑春某地)和大连某地环境污染土壤样品(采于2019年10月)进行了测定。并在山参土样品中添加低、中、高的3个浓度水平的混标溶液,每个浓度水平平行测定3次,结果如表3所示。结果显示,大连某环境污染样品所有目标化合物均检出,且污染严重;山参图样品中检出萘、菲、荧蒽和芘等化合物,其余目标化合物未检出;目标化合物的加标回收率为:76.5%—105.3%,相对标准偏差(RSD)0.2%—8.5%。
表 3 实际样品测定结果、方法的回收率及精密度(n=3)Table 3. Determination results in real soil samples and recoveries and precisions of methods (n=3)化合物Compound 污染土中含量/(µg·kg−1)Content of contamined soil 山参土中含量/(µg·kg−1)Content of mountain soil 加标水平/(µg·kg−1)Spiked level 加标回收率/%Recovery RSD/% 萘(Na) 63.2 8.0 10、100、1000 90.1、97.3、88.3 7.7、3.9、1.6 苊(Ace) 563.1 nd 10、100、1000 83.0、77.9、84.8 8.3、5.4、0.7 芴(Fl) 1442.5 nd 10、100、1000 102.1、86.2、85.1 5.7,3.0,0.5 菲(Phe) 11122.8 8.0 10、100、1000 80.2、91.8、87.0 3.3、1.6、0.6 蒽(Ant) 3756.6 nd 10、100、1000 88.9、77.6、78.2 5.2、0.3、0.6 荧蒽(Fu) 19443.7 3.3 10、100、1000 94.3、79.2、85.7 3.7、4.2、0.2 芘(Py) 21200 7.6 10、100、1000 78.5、100.8、95.6 7.6、2.3、0.5 9-氯菲(9-ClPhe) 2241.6 nd 10、100、1000 78.0、84.9、84.0 7.8、3.4、0.2 9-氯蒽(9-ClAnt) 4901.8 nd 10、100、1000 81.2、90.4、78.6 8.5、3.7、0.6 2-氯蒽(2-ClAnt) 7202 nd 10、100、1000 85.6、86.6、79.1 6.8、5.3、0.4 苯并[a]蒽(BaA) 8787.4 nd 10、100、1000 95.2、88.0、87.3 4.5、1.8、0.3 䓛(Chr) 7392.2 nd 10、100、1000 96.2、89.4、87.6 3.6、2.5、0.3 1-氯芘(1-ClPy) 3022.7 nd 10、100、1000 82.3、87.1、90.7 7.9、4.0、0.5 苯并[b]荧蒽(BbF) 9073.9 nd 10、100、1000 86.5、88.1、88.6 4.2、3.9、0.2 9,10-二氯蒽(9,10-DClAnt) 392.7 nd 10、100、1000 81.2、85.2、83.0 3.6、1.8、0.6 苯并[k]荧蒽(BkF) 4041.7 nd 10、100、1000 90.2、87.9、87.5 3.2、2.4、0.3 苯并[a]芘(BaP) 9703.7 nd 10、100、1000 85.0、89.3、87.6 4.2、3.1、0.4 二苯并[a,h]蒽(DahA) 2581.7 nd 10、100、1000 79.1、89.7、88.4 4.5、2.4、0.2 苯并[ghi]苝(BghiP) 8263 nd 10、100、1000 89.2、105.3、94.8 4.2、1.6、0.6 茚并[1,2,3-cd]芘(Ipy) 7178 nd 10、100、1000 78.3、79.5、76.5 6.8、7.6、2.5 * nd: not detected. 3. 结论(Conclusion)
本文建立了超分子溶剂微萃取结合高效液相色谱荧光检测技术快速测定土壤中5种氯代多环芳烃和15种多环芳烃的分析方法。方法的基质加标回收率为 76.5%—105.3%,相对标准偏差为 0.2%—8.5%。本方法简便、快速、成本低廉且环境友好,样品处理过程不超过15 min,而且一次可同时处理多个样品。本方法可用于土壤中5种氯代多环芳烃和15种多环芳烃的快速分析检测。
-
表 1 管网疏松沉积物样品的元素组成
Table 1. Elemental compositionof the loose deposits in pipe network
% 序号 C N O As Al Si S Pb Mn Fe Cu 1# 2.40 0.29 30.90 0.46 0.55 0.55 0.55 0.33 1.66 61.65 0.32 2# 4.47 0.36 31.96 0.10 1.20 1.71 0.13 0.54 0.59 57.99 0.95 3# 2.59 0.23 18.37 0.33 1.12 1.23 0.13 0.70 0.99 73.23 1.08 4# 15.17 0.30 2.50 0.03 0.28 0.10 0.00 0.21 0.66 78.82 1.94 5# 8.53 0.38 30.70 0.27 0.41 0.60 0.32 1.02 0.43 56.20 1.14 6# 5.54 0.32 33.62 0.37 0.57 0.87 0.22 0.74 0.32 56.39 1.02 7# 3.30 0.34 32.53 0.61 1.04 1.02 0.12 0.58 0.31 59.21 0.93 表 2 管网疏松沉积物样品的晶体组成
Table 2. Crystal composition of the loose deposits in pipe network
% 样品编号 Fe3O4 CaCO3 α-Fe2O3 γ-Fe2O3 δ-FeOOH α-FeOOH Fe γ-FeOOH β-FeOOH FeCO3 SiO2 1# 15 0 37 28 0 13 0 0 7 0 0 2# 3 14 3 57 0 2 1 9 3 4 3 3# 0 5 7 19 17 16 1 4 5 4 25 4# 6 34 11 13 4 5 0 11 1 1 14 5# 13 0 5 0 0 8 0 14 35 0 26 6# 9 0 9 11 0 14 0 27 8 0 21 7# 8 5 6 7 0 7 0 10 9 0 48 表 3 管网疏松沉积物性质与细胞存活率的Pearson相关系数
Table 3. Pearson correlation coefficient of structure property and cell viability
zeta电位 粗糙度 平均粒径 PV zeta电位 1 0.225 −0.851* 0.203 粗糙度 1 0.032 −0.507 平均粒径 1 −0.191 PV 1 注:*代表显著性水平为0.05。 表 4 管网疏松沉积物晶体组成与细胞存活率相关系数
Table 4. Correlation coefficient of crystal composition and cell viability
Fe3O4 CaCO3 α-Fe2O3 γ-Fe2O3 δ-FeOOH α-FeOOH Fe γ-FeOOH β-FeOOH FeCO3 SiO2 PV Fe3O4 1 −0.411 0.600 −0.364 −0.686 0.095 −0.804* 0.072 0.533 −0.859* −0.103 −0.335 CaCO3 1 −0.190 0.179 0.100 −0.589 0.067 −0.081 −0.488 0.252 −0.210 −0.097 α-Fe2O3 1 0.091 −0.159 0.381 −0.359 −0.477 −0.177 −0.372 −0.512 0.197 γ-Fe2O3 1 −0.042 −0.349 0.679 −0.359 −0.527 0.671 −0.682 0.519 δ-FeOOH 1 0.494 0.592 −0.347 −0.262 0.625 0.114 0.588 α-FeOOH 1 −0.038 0.002 0.016 −0.112 0.084 0.184 Fe 1 −0.336 −0.339 0.981** −0.235 0.738 γ-FeOOH 1 0.212 −0.344 0.270 −0.762* β-FeOOH 1 −0.417 0.293 −0.089 FeCO3 1 −0.273 0.711 SiO2 1 −0.441 RV 1 注:*代表显著性水平为0.05。 -
[1] 汤鸿霄. 环境科学中的化学问题环境水质学中的几个化学前沿问题[J]. 化学进展, 2000, 12(4): 415-422. doi: 10.3321/j.issn:1005-281X.2000.04.008 [2] 刘书明. 饮用水管网输配过程中颗粒物与微量污染物的复合污染效应及其水质风险[J]. 环境工程学报, 2021, 15(1): 1-2. doi: 10.12030/j.cjee.202008046 [3] VREEBURG J H G, BOXALL J B. Discolouration in potable water distribution systems: A review[J]. Water Research, 2007, 41(3): 519-529. doi: 10.1016/j.watres.2006.09.028 [4] 张晓健, 牛璋彬. 给水管网中铁稳定性问题及其研究进展[J]. 中国给水排水, 2006, 22(2): 13-16. doi: 10.3321/j.issn:1000-4602.2006.02.004 [5] 顾军农. 多水源供水模式下管网腐蚀产物释放与应对措施初探[J]. 城镇供水, 2010(1): 66-70. [6] SARIN P, SNOEYINK V L, BEBEE J, et al. Physico-chemical characteristics of corrosion scales in old iron pipes[J]. Water Research, 2001, 35(12): 2961-2969. doi: 10.1016/S0043-1354(00)00591-1 [7] 邱微, 王立友, 樊庆锌, 等. 给水球墨铸铁管腐蚀特性及腐蚀对水质的影响[J]. 哈尔滨工业大学学报, 2016, 48(8): 61-66. doi: 10.11918/j.issn.0367-6234.2016.08.010 [8] ZHUANG Y, HAN B, CHEN R, et al. Structural transformation and potential toxicity of iron-based deposits in drinking water distribution systems[J]. Water Research, 2019, 165: 114999. doi: 10.1016/j.watres.2019.114999 [9] ZHUANG Y, SHEN C, GU Y, et al. Effect of trichloroacetic acid on iron oxidation: Implications on the control of DBPs and deposits in drinking water[J]. Water Research, 2021, 189: 116632. doi: 10.1016/j.watres.2020.116632 [10] ZHUANG Y, HAN B, CHEN R, et al. Mechanism study on organic pollutant accumulation by iron-based particles in drinking water conditions[J]. Chemical Engineering Journal, 2020, 396: 125157. doi: 10.1016/j.cej.2020.125157 [11] 周全, 陈汝硕, 高红涛, 等. 基于模糊综合评价法的城市供水管网黄水风险区域预测及应对措施[J]. 给水排水, 2015, 51(8): 101-104. doi: 10.3969/j.issn.1002-8471.2015.08.030 [12] LIU G, ZHANG Y, KNIBBE W J, et al. Potential impacts of changing supply-water quality on drinking water distribution: A review[J]. Water Research, 2017, 116: 135-148. doi: 10.1016/j.watres.2017.03.031 [13] 李欣, 马建薇, 袁一星. 城市给水管网水质研究与进展[J]. 哈尔滨工业大学学报, 2004, 36(10): 1392-1396. doi: 10.3321/j.issn:0367-6234.2004.10.033 [14] 刘锐平, 曲久辉. 饮用水质健康风险的末端控制[J]. 科学通报, 2009, 54(3): 273-277. [15] CHAN C S, STASIO C D, WELCH S A, et al. Microbial polysaccharides template assembly of nanocrystal fibers[J]. Science, 2004, 303(5664): 1656-1658. doi: 10.1126/science.1092098 [16] ZHUANG Y, KONG Y, LIU Q, et al. Alcohol-assisted self-assembled 3D hierarchical iron (hydr)oxide nanostructures for water treatment[J]. Crystengcomm, 2017, 19(39): 5926-5933. doi: 10.1039/C7CE01320E [17] 牛璋彬, 王洋, 张晓健, 等. 给水管网中管内壁腐蚀管垢特征分析[J]. 环境科学, 2006, 27(6): 1150-1154. doi: 10.3321/j.issn:0250-3301.2006.06.022 [18] 刘东坡, 张金松, 靳军涛. 城市供水管网通水初期水质变化规律研究[J]. 中国给水排水. 2019, 35(17): 43-49. [19] OBERDÖRSTER G. Pulmonary effects of inhaled ultrafine particles[J]. International Archives of Occupational and Environmental Health, 2000, 74(1): 1-8. [20] ZHUANG Y, LIU Q, KONG Y, et al. Enhanced antibiotic removal through a dual-reaction-center Fenton-like process in 3D graphene based hydrogels[J]. Environmental Science: Nano, 2019, 6(2): 388-398. [21] 庞维海, 杨帆, 楚文海, 等. 饮用水中氯代乙酰胺的细胞毒性和遗传毒性[J]. 同济大学学报(自然科学版), 2014, 42(12): 1873-1878. doi: 10.11908/j.issn.0253-374x.2014.12.014 [22] 楚文海, 沈杰, 栾鑫淼, 等. 疫情防控期间污水处理厂强化消毒下的水环境次生风险实证研究[J]. 给水排水, 2020, 56(6): 1-5. [23] 徐明, 阚海东, 桑楠, 等. 持久性有毒污染物环境健康研究的现状与思考[J]. 中国科学院院刊, 2020, 35(11): 1337-1343. [24] HARRAD S, WEMKEN N, DRAGE D S, et al. Perfluoroalkyl substances in drinking water, indoor air and dust from Ireland: Implications for human exposure[J]. Environmental Science & Technology, 2019, 53(22): 13449-13457. [25] PRAT O, VERCOUTER T, ANSOBORLO E, et al. Uranium speciation in drinking water from drilled wells in southern finland and its potential links to health effects[J]. Environmental Science & Technology, 2009, 43(10): 3941-3946. [26] 石宝友, 李涛, 顾军农, 等. 北方某市水源更换过程中管网黄水产生机制的探讨[J]. 供水技术, 2010, 4(4): 12-15. doi: 10.3969/j.issn.1673-9353.2010.04.004 [27] 冯利华. 环境质量的主成分分析[J]. 数学的实践与认识, 2003(8): 32-35. [28] PARK J, LIM D H, LIM H J, et al. Size dependent macrophage responses and toxicological effects of Ag nanoparticles[J]. Chemical Communication, 2011, 47(15): 4382-4384. doi: 10.1039/c1cc10357a [29] 李玉仙, 王敏, 李礼, 等. 水源切换条件下管网管垢稳定性和水质腐蚀性判定指标探讨[J]. 给水排水, 2015, 51(2): 110-114. doi: 10.3969/j.issn.1002-8471.2015.02.027 [30] 牛璋彬, 王洋, 张晓健, 等. 给水管网中管内壁腐蚀管垢特征分析[J]. 环境科学, 2006, 27(2): 310-314. doi: 10.3321/j.issn:1001-0742.2006.02.019 -






 DownLoad:
DownLoad: