-
柠檬酸是有机酸中的第一大酸,其在医药和化工等工业领域应用广泛,主要生产原料为木薯和玉米。行业统计数据表明,每生产1 t柠檬酸可产生7.5 t废水[1]。柠檬酸废水中的主要污染物为淀粉、蛋白质、各种有机酸等有机物和N、P、S等无机物[2],且其有机物含量较高,直接排放容易带来水体富营养化风险目前。国内柠檬酸行业普遍采用生物法[3-5]对废水进行处理,然而生化后的出水仍然具有色度深(90~100倍)、COD高(100~120 mg·L−1)和出水生化性(BOD5/COD)低等特点。近年来,国家加大了对污染行业的整治力度,工业废水排放标准也逐渐提高,故研究新型高效的污水深度处理技术已经迫在眉睫。
高级氧化技术是一种新型的污水处理技术,其原理是在电、超声、光照、外加催化剂或高温高压等反应条件下生成具有强氧化性的羟基自由基(·OH),利用·OH将难降解的大分子有机物分解成小分子物质甚至完全矿化[6]。根据自由基生成途径和反应条件的不同,可将其分为臭氧催化氧化[7]、光催化氧化[8]、高铁酸盐(Fe(Ⅵ))氧化[9]等。与其他高级氧化技术相比,臭氧催化氧化法具有独特的优势[10-11]。其操作步骤简单易行、占地面积小、无二次污染、无额外药剂的投入,因而在工业废水处理领域具有广阔的应用前景。
然而,单独采用臭氧催化氧化法降解柠檬酸生化尾水需要投加大量臭氧和催化剂,会增加处理成本,从而大大限制了其实际应用。有研究[12-14]表明,可将臭氧催化氧化技术作为预处理手段,在臭氧催化适度改善废水生化性的基础上耦合生物处理,能够显著降低废水处理的综合成本并提升处理效率[15-18]。作为一种新型高效的污水生物处理法,移动床生物膜反应器(MBBR)工艺兼具传统流化床和生物接触氧化法两者的优点[19]。相较于生物曝气滤池(BAF)等传统的生物处理工艺[20],MBBR工艺负荷高、不需要填料支架和反冲洗设备、操作简便,明显降低了污水的运行成本且可以达到深度处理的效果[21]。将臭氧催化氧化技术与MBBR系统组合,可以形成一种低能耗、低成本、高效率的联合处理工艺,以充分发挥2种工艺的独特优势,提高其在柠檬酸生化尾水处理中的应用价值。
本研究采用臭氧催化氧化-MBBR组合工艺,以某柠檬酸厂生化尾水作为原水进行中试研究,考察了臭氧催化氧化系统对柠檬酸生化尾水的生化性改善情况;在此基础上,进一步研究了臭氧催化氧化-MBBR组合工艺深度降解柠檬酸生化尾水的可行性、运行参数及运行效率,旨在为厂区污水处理系统的升级提供参考。
全文HTML
-
中试研究所用水来自某柠檬酸废水处理厂二级生化处理后的出水,该废水可生化性差,出水颜色呈深黄色,出水成分复杂。具体水质情况为:COD为100~120 mg·L−1,BOD为8~10 mg·L−1(B/C=0.08~0.09),pH为7.4~7.8。
-
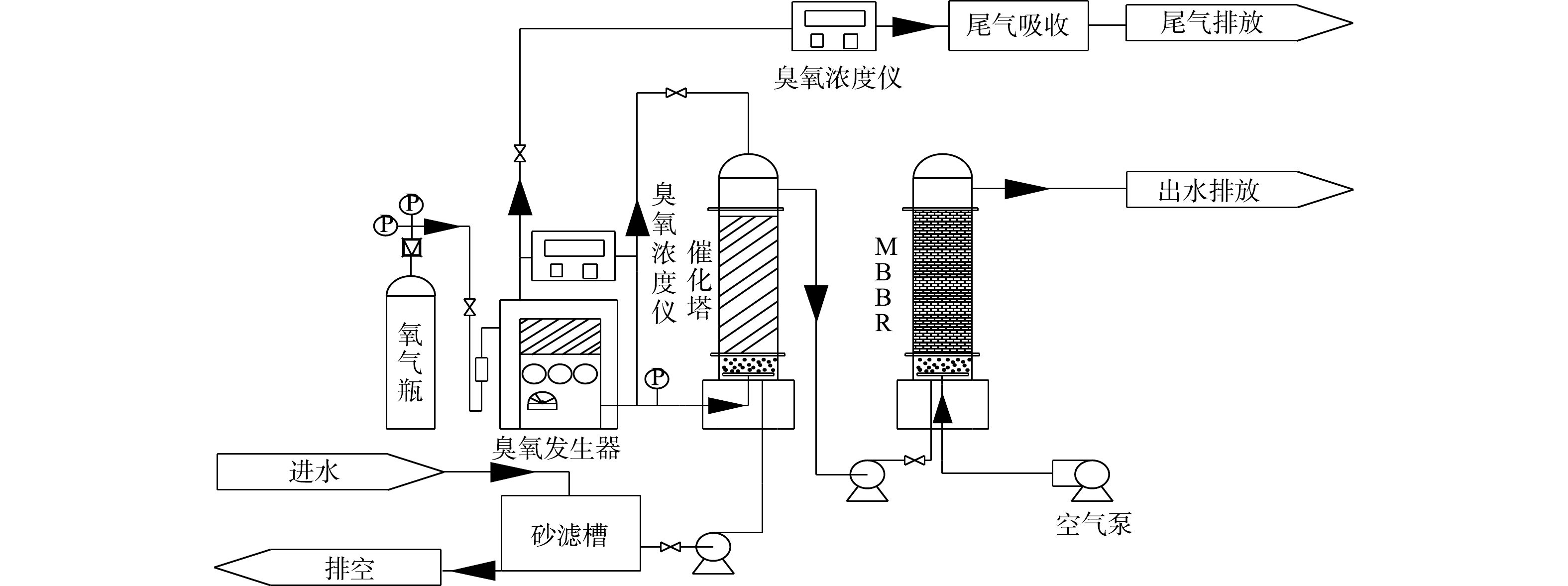
臭氧催化氧化-MBBR中试系统流程图如图1所示。主要包括臭氧催化塔和MBBR生物处理单元2个部分。所用臭氧催化塔由不锈钢加工而成,管径为75 cm,高度为4.5 m,内部填充催化剂,填充率为50%。废水通过立式泵从底部进入催化塔,臭氧发生器以氧气为气源,通过调节阀门使臭氧以1 m3·h−1的流速进入催化塔。生物处理单元的主要反应装置为MBBR,其反应器由有机玻璃加工而成,管径为50 cm,高度为3 m,内部填充有填料,填充比约为40%。反应器在设计流量为0.08 m3·h−1的条件下经立式泵完成连续进水。MBBR运行时所需的空气来自空气泵,接种污泥为柠檬酸厂活性污泥,质量浓度约为4 000 mg·L−1。
-
在臭氧催化体系中,所填充的催化剂为实验室自制的MnOx-CeOx复合双金属氧化物[22]。该催化剂经高温煅烧制得,具有机械强度高、吸附性能强和催化性能好等优点。在MBBR系统中,所用填料为圆柱体聚乙烯塑料,直径约为10 mm,高为8~9 mm。圆柱体中有十字支撑,具有较高的比表面积(160~500 m2·m−3),密度略小于水(0.92~0.97 g·cm−3)。该填料的特有性质有利于微生物在填料上富集和生长,形成比较稳定的生物膜,并且在反应器中易呈现流化状态。
-
1)臭氧催化氧化段。在进水平均COD、色度和BOD5/COD分别为110 mg·L−1、90倍和0.08的条件下,首先对臭氧投加量进行优化。在臭氧反应时间为60 min,进气流量为1 m3·h−1的条件下,连续运行,分别调整臭氧投加量为10、20、30、40、50、60、70 mg·L−1,比较在不同臭氧投加量下COD、色度的去除率以及出水BOD5/COD的变化特征,选取最佳的臭氧投加量。在获得最佳臭氧投加量的基础上,固定最佳臭氧投加量,进气流量为1 m3·h−1,连续运行,分别调整水力停留时间(HRTo)为30、40、50、60、70、80 min,比较在不同的HRTo下COD、色度的去除率以及出水BOD5/COD的变化特征,获得最佳的HRTo。
2) MBBR段。将0.4 m3左右的泥水混合物倒入反应器中,静置2 h,使污泥能够充分地与填料接触,然后加入臭氧催化氧化处理后的废水闷曝48 h。在48 h后,采用连续进水的方式,启动挂膜阶段控制气水比为4∶1,分别调整水力停留时间(HRTm)为10、8、6、4 h,每个条件运行10 d,比较不同HRTm下COD的去除率,选取最佳的HRTm;在获得最佳HRTm的基础上,分别调整气水比为7∶1、4∶1、2∶1,比较在不同气水比的条件下COD的去除率,获得最佳气水比。
-
采用标准方法[23]测定COD和SS;采用稀释倍数法测定色度;采用五日生化法测定BOD5;采用YSI DO200型溶解氧温度仪测量DO;采用同林科技ZX-01测定臭氧浓度;采用气相色谱质谱仪(GC/MS,7890B+5977A)测定污水中有机物的种类。
1.1. 实验水质
1.2. 中试设备与流程
1.3. 催化剂与填料
1.4. 实验方法
1.5. 分析方法
-
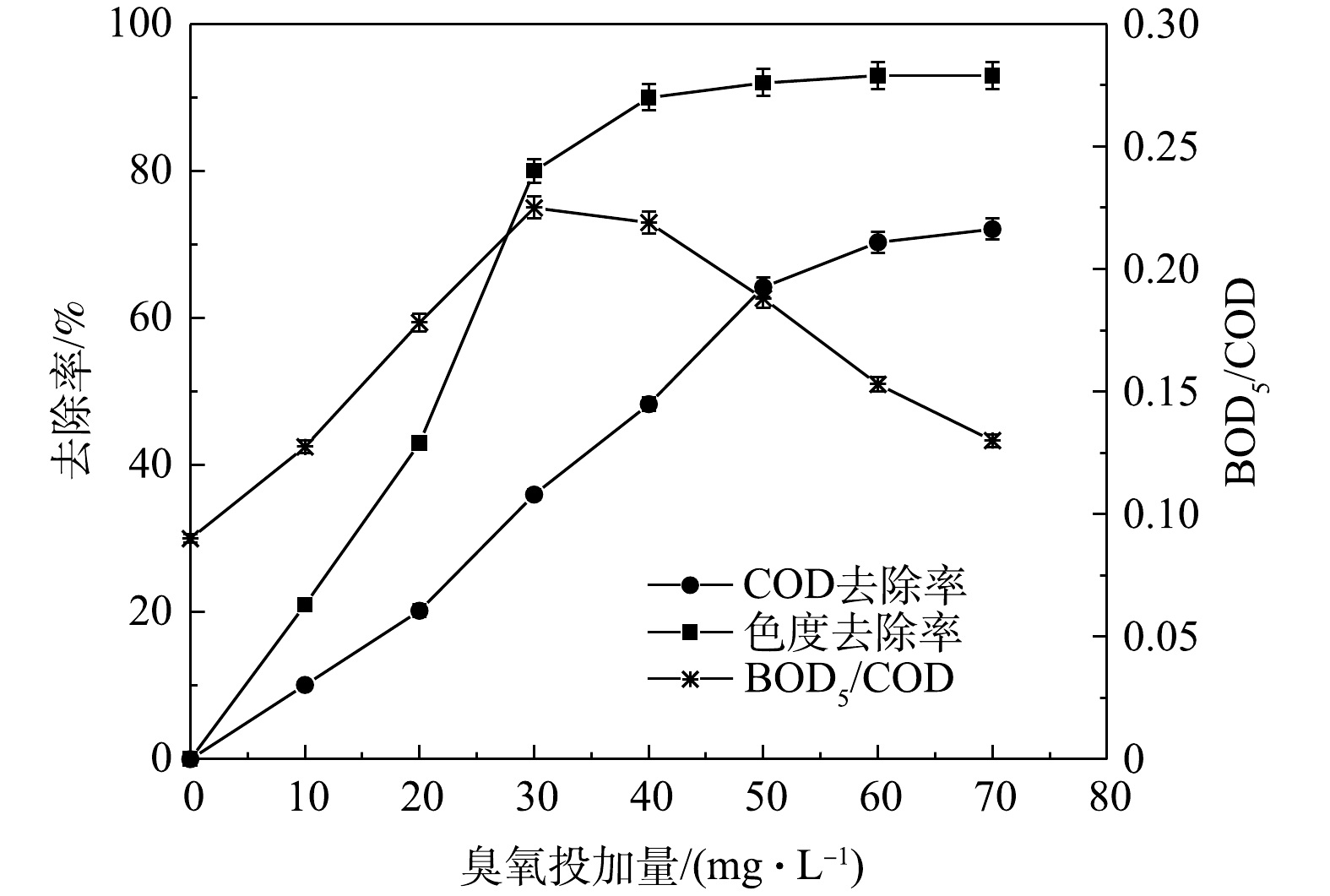
1)臭氧投加量对臭氧催化氧化的影响。由图2可知,随着臭氧投加量的增加,出水COD、色度去除率和出水BOD5/COD均不断提高,当臭氧投加量为30 mg·L−1时,COD和色度去除率分别为36.0%和80.0%,出水BOD5/COD值则达到最大值0.23。这表明此时废水中的有机成分在臭氧及羟基自由基作用下发生分解,生成大量中间产物和小分子有机物,导致生化性明显改善;继续增加臭氧投加量,COD去除率继续提高,色度的去除率趋于平稳,出水BOD5/COD开始下降。显然,这是因为·OH进一步矿化废水中的部分中间产物所导致的。因此,为保证MBBR段的进水生化性和处理效率,确定最佳臭氧投加量为30 mg·L−1。
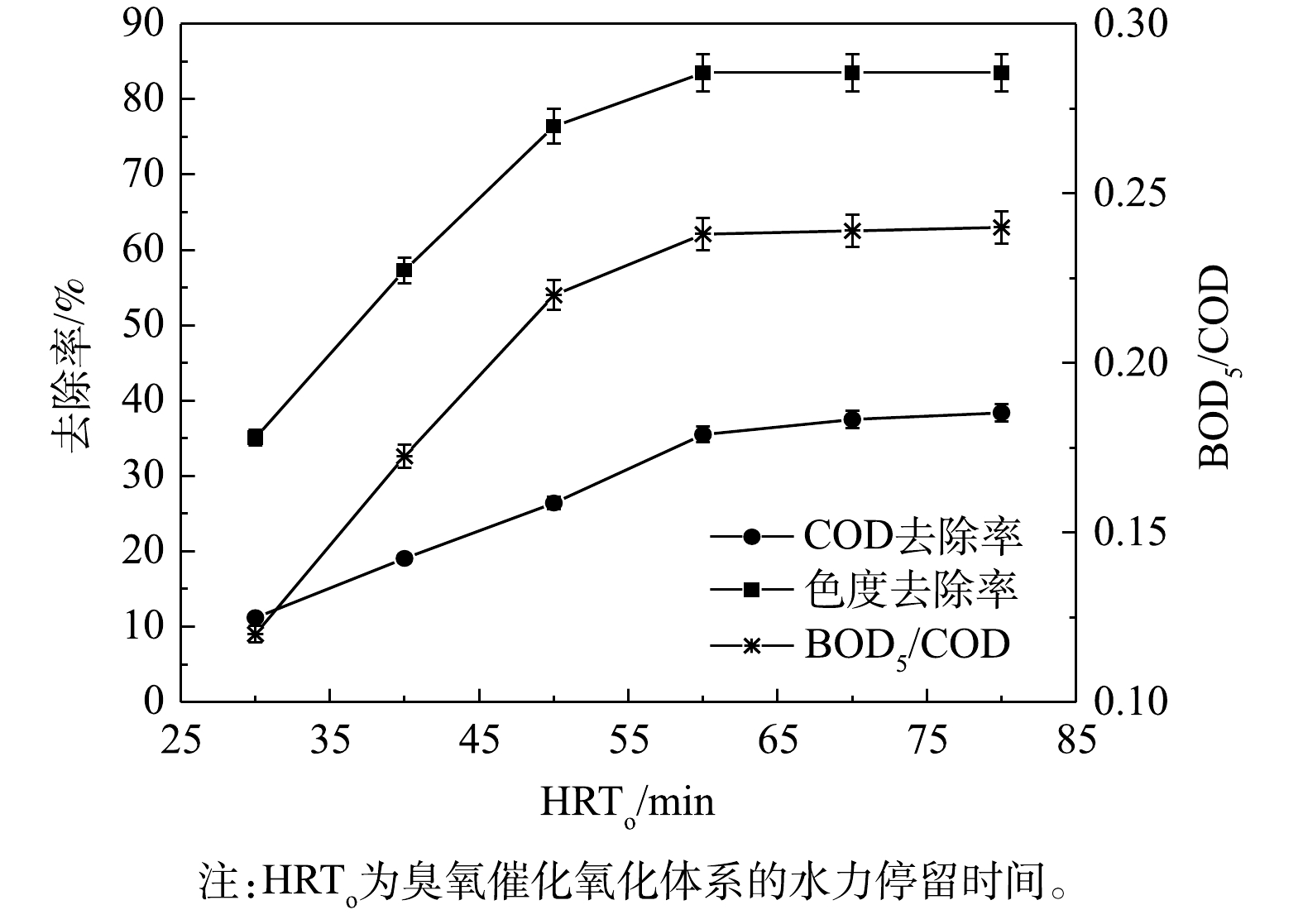
2) HRTo对臭氧催化氧化的影响。图3反映了COD、色度去除率和出水BOD5/COD随HRTo的变化情况。当HRTo为30 min时,COD、色度去除率和出水BOD5/COD分别11.2%、35.1%和0.12;当HRTo为60 min时,COD、色度去除率分别为35.4%和83.3%,出水生化性BOD5/COD由0.12提升至0.24;继续延长HRTo,COD、色度去除率和出水的BOD5/COD都趋于平缓,且反应时间越长,臭氧投加量增加,会导致运行成本升高。上述结果表明,在本实验条件下,将HRTo控制在60 min可确保臭氧催化氧化的效果,有效地改善柠檬酸生化尾水的可生化性,从而有利于后续MBBR单元的生物降解。综合考虑能耗和成本,确定最佳HRTo为60 min。
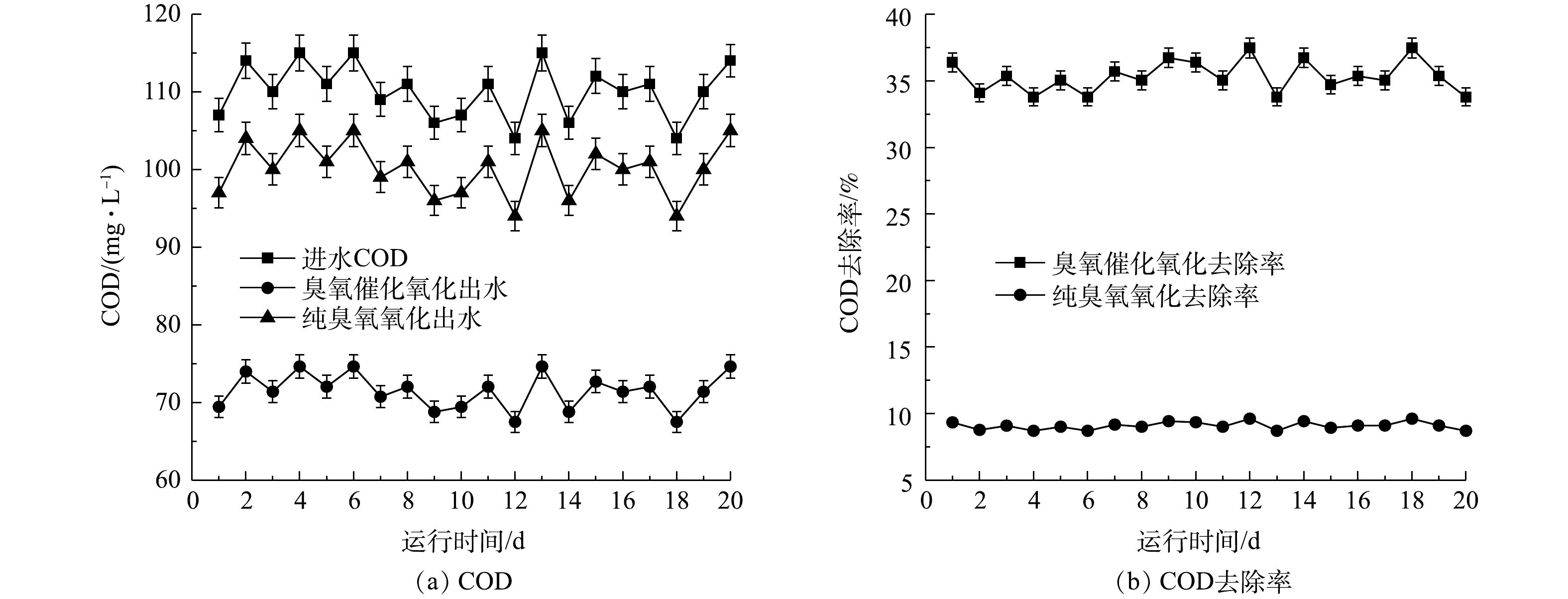
3)不同反应体系对COD去除的影响。在臭氧投加量为30 mg·L−1,水力停留时间为60 min,进气量1 m3·h−1的条件下,考察纯臭氧氧化体系和臭氧催化氧化体系对COD的去除效果,结果如图4所示。由图4可知,在臭氧催化氧化体系中,平均COD去除率为35.5%,相较于纯臭氧氧化体系中,平均COD去除率提高了24%。这是因为在纯臭氧氧化体系中,主要以臭氧直接参与反应为主,臭氧的选择性氧化和气液传质较差导致去除率较低;而在臭氧催化氧化体系中,催化剂的存在使得系统中产生了大量·OH,增强传质,进而可提高废水COD去除率。
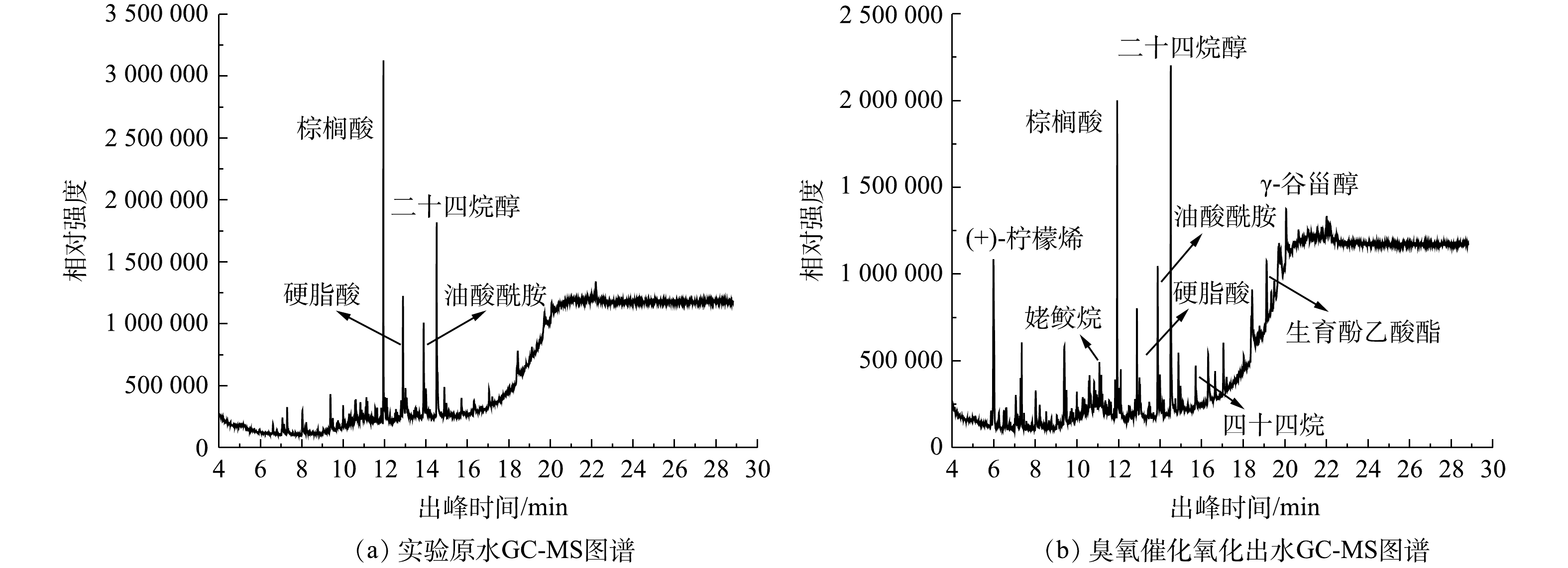
4)水质成分分析。为了进一步验证臭氧催化氧化技术能够改善柠檬酸生化尾水的生化性,在臭氧投加量为30 mg·L−1,水力停留时间为60 min,进气量1 m3·h−1的条件下,对实验原水和臭氧催化氧化出水进行GC-MS分析,分析结果如图5所示。结果表明,实验原水中的主要污染物为11种,其中脂肪酸、酰胺类等物质为主要污染物,在其他类有机物中,部分有机物含有乙烯基、羰基、苯环等发色基团,故导致柠檬酸废水呈现颜色。经臭氧催化预处理后的出水中主要污染物可达到20种,其主要为烷烃类、酯类和醇类。由此可见,在臭氧催化氧化处理后,废水中的脂肪酸类和其他类有机物被分解成简单的酯类和部分链状烷烃类,使柠檬酸生化尾水的生化性得到了显著改善,色度明显降低。
-
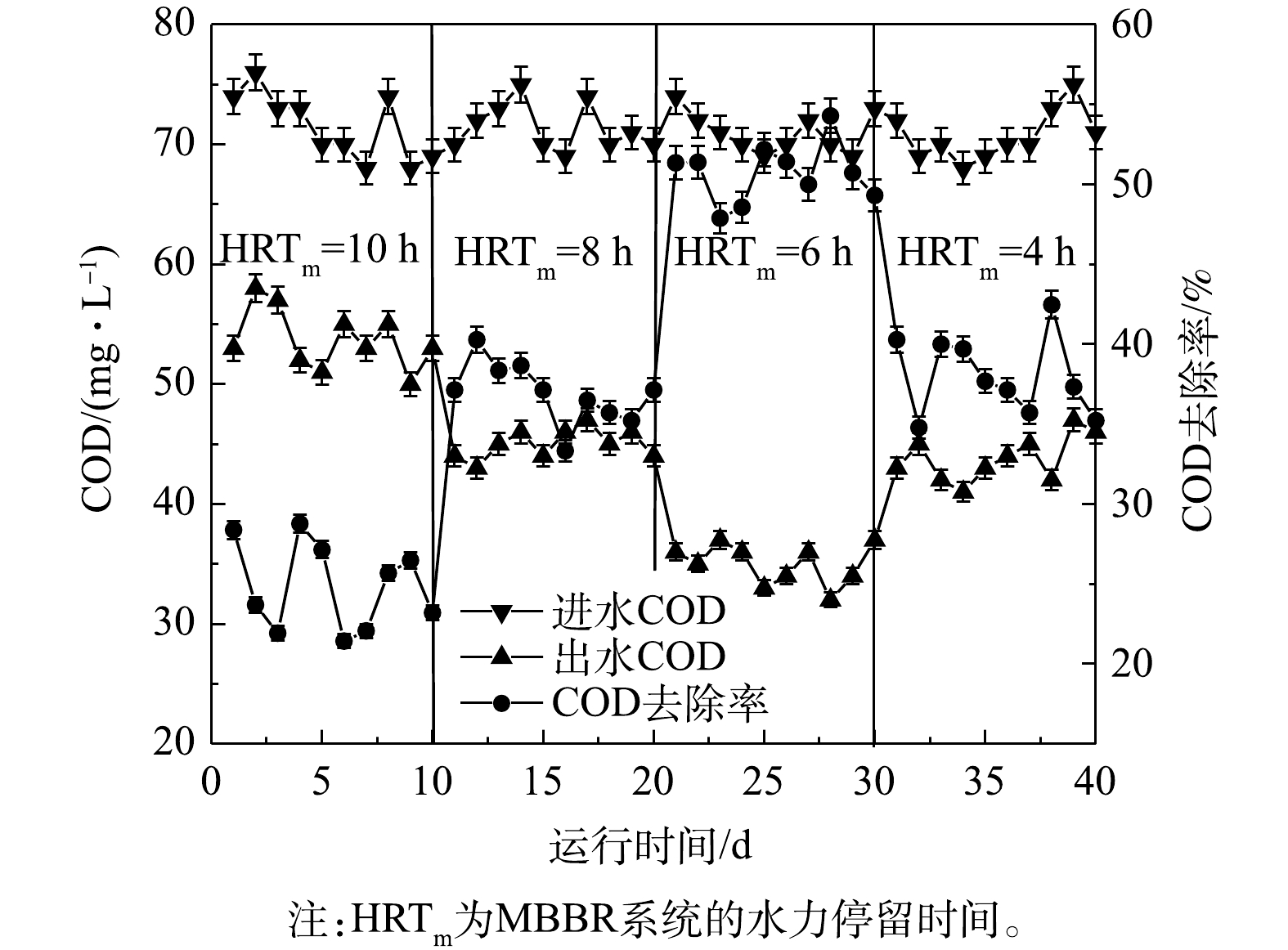
1) HRTm对MBBR系统处理效果的影响。以优化后的臭氧催化氧化工艺段的出水作为MBBR系统的进水,设定气水比为4∶1,探究HRTm对MBBR系统运行的影响。由于进水色度较低,改变运行条件对色度去除不明显,因此,主要以COD去除率为指标优化运行参数。由图6可知,当HRTm由10 h降至6 h,COD平均去除率由24.9%升高至50.7%;继续缩短HRTm,COD去除率反而开始下降。当HRTm为10 h时,系统中有机负荷较低,系统处于驯化启动阶段,COD去除效果相对较差;随着HRTm的缩短,MBBR系统的有机负荷提高,微生物大量繁殖,污染物得到充分降解,从而使得COD去除效果得到改善;继续缩短HRTm,MBBR系统中的微生物没有充分吸收和降解废水中的有机物,导致COD去除效果变差。根据上述结果,本研究确定MBBR系统的最佳HRTm为6 h。
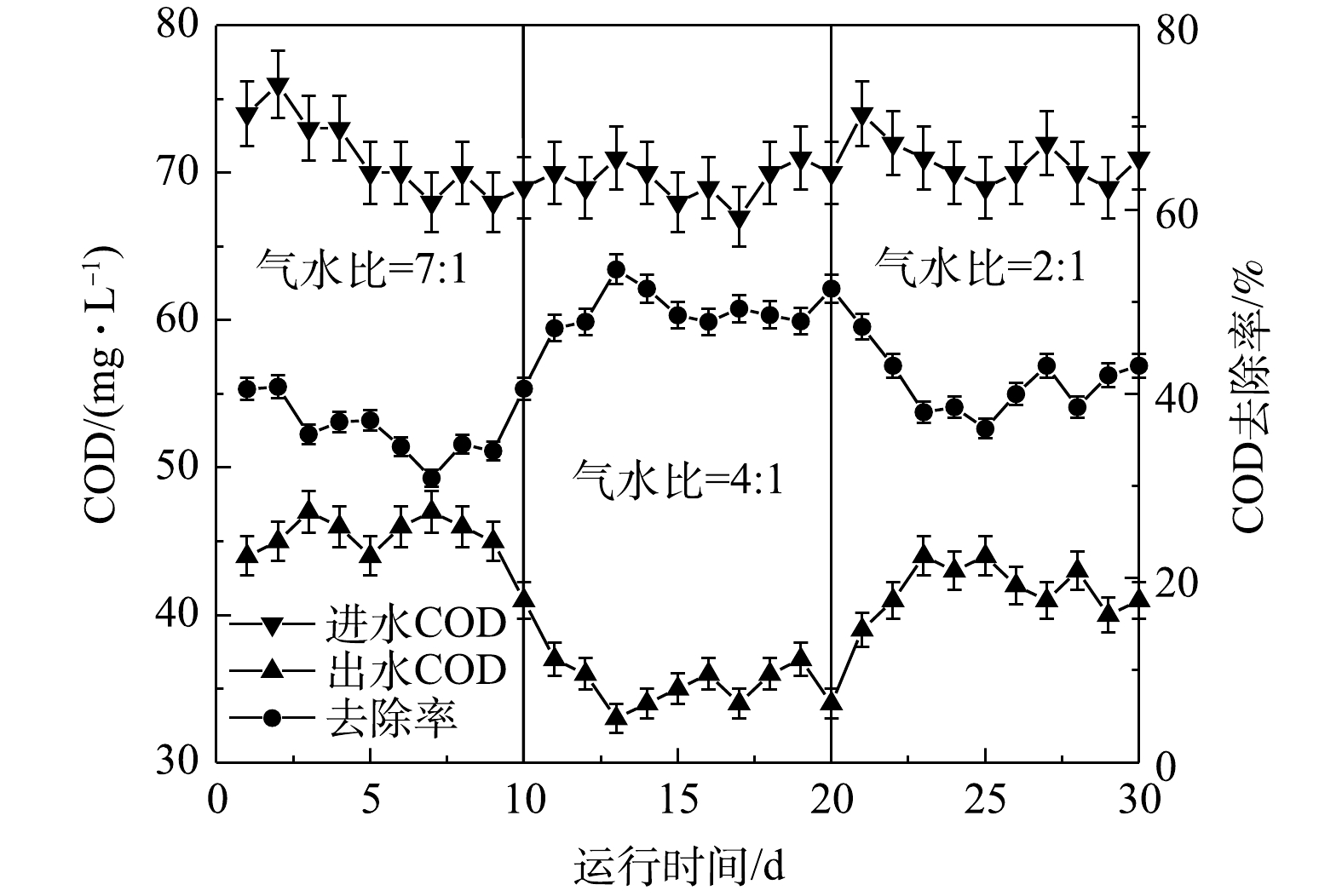
2)气水比对MBBR系统处理效果的影响。设定HRTm为6 h,探究气水比对MBBR系统处理效果的影响。由图7可知,将气水比由7∶1减小到4∶1后,COD平均去除率由36.5%增加到49.3%。继续减小气水比,COD平均去除率开始下降。这是因为初始系统中气水比过高,导致生物膜受到冲刷而脱落[24],不利于污染物的截留和微生物的生长繁殖,导致COD去除效果较差。随着气水比的降低,填料在水中逐渐呈现流化态,此时系统中气、水、填料三者充分接触,加速了生物膜的生长,从而改善了COD的去除效果。当气水比过低时,填料在水中的流化状态受到影响,同时废水中的溶解氧不足导致好氧微生物活性受到抑制,不利于废水中有机污染物的去除。根据上述实验结果,确定最佳气水比为4∶1。
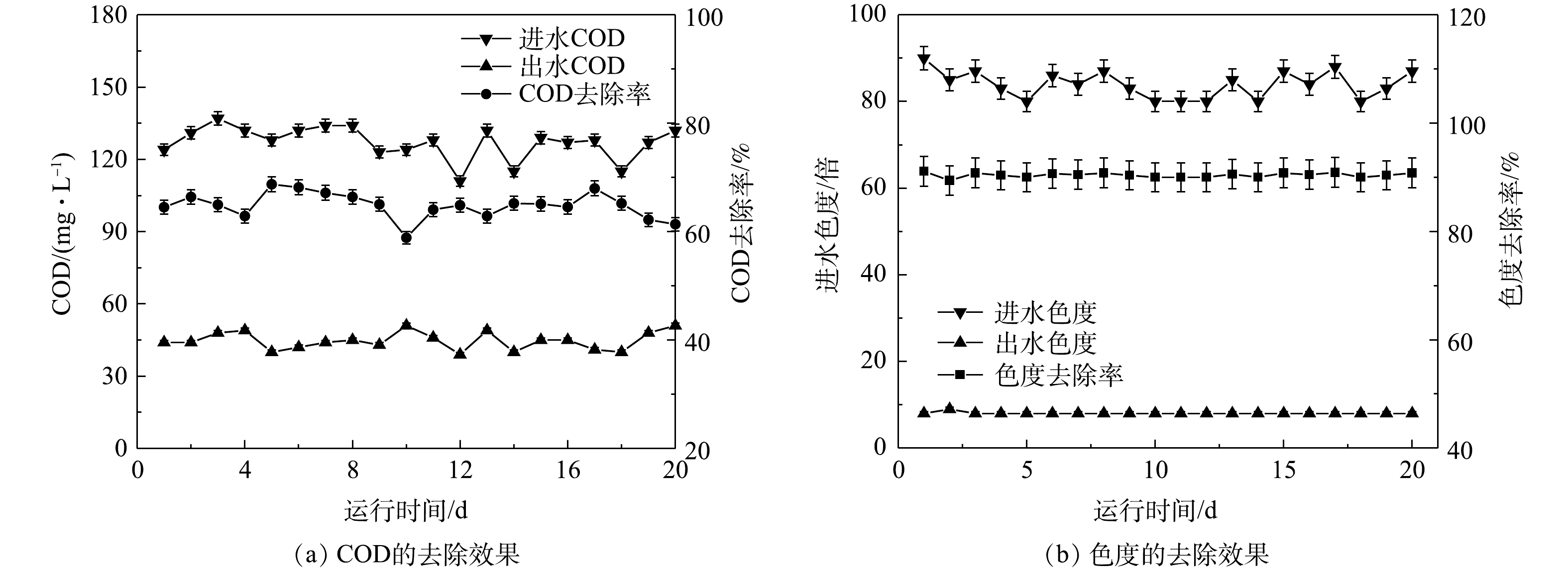
3)最优条件下连续运行效果。在确定最优的条件下将2种工艺组合运行20 d,每天定时采样测试以探究工艺连续运行的效果,结果如图8所示。在连续运行20 d期间,臭氧催化氧化-MBBR组合工艺处理效果良好,系统出水COD由100~120 mg·L−1降至32~40 mg·L−1,COD去除率维持在66.2%~74.7%,出水色度由90~100倍降至10倍左右,色度去除率维持在90.0%~94.0%。此外,该组合工艺的出水不会返色且表观清澈透明,填料上的生物膜生长良好(图9),反应器中始终维持着较高的生物量。以上结果表明,臭氧催化氧化-MBBR组合工艺对柠檬酸生化尾水深度降解有显著效果。
-
采用臭氧催化氧化-MBBR组合工艺处理柠檬酸生化尾水的运行成本主要来自臭氧催化单元中臭氧和生化处理单元的能耗2个方面。其中,当臭氧投加量为30 mg·L−1,进气量为1 m3·h−1时,每克臭氧耗电量为20 W,处理每吨水的耗电量为0.6 kW。电费按0.70 元·(kW·h)−1计,则臭氧单元的电费为0.42 元·t−1。MBBR单元处理[25]能耗按0.07 元·t−1计,该组合工艺的运行成本约为0.49 元·t−1。工业级液氧价格大约800 元·t−1,产生30 g臭氧所需要的费用约为0.24 元。催化剂折旧费用约为0.06 元·t−1,该组合工艺总费用约为0.79 元·t−1。单独使用臭氧催化氧化技术,要达到相同的处理效果需要臭氧投加量为50 mg·L−1,则需要总费用约为1.16 元·t−1。综合上述结果可知,臭氧催化氧化-MBBR组合工艺处理柠檬酸生化尾水经济效益更高。
2.1. 臭氧催化氧化系统的运行
2.2. MBBR生化系统运行情况
2.3. 运行成本初步分析
-
1)本研究以MnOx-CeOx复合双金属氧化物为催化剂,采用臭氧催化氧化法对柠檬酸生化尾水进行预处理。在臭氧投加量为30 mg·L−1、HRTo为60 min、进气量为1 m3·h−1的条件下,臭氧催化预处理生化尾水的COD和色度去除率分别35.4%和83.3%,出水生化性由0.08提升至0.23,显著提高了废水的生化性。
2)采用MBBR对臭氧催化氧化单元的出水进行处理,在HRTm为6 h、气水比为4∶1的条件下,出水COD为32~40 mg·L−1,色度能够稳定在10倍左右。
3)臭氧催化氧化-MBBR组合工艺的运行成本约为0.79 元·t−1,较单独使用臭氧催化氧化技术(1.16 元·t−1)节约运行成本。采用臭氧催化氧化-MBBR组合工艺减少了臭氧的投加量,在降低废水处理成本的同时提高了对柠檬酸生化尾水的处理效率。



 下载:
下载: