-
土壤中的污染情况往往以复合污染的形式出现[1]。其中,重金属-有机复合污染尤为常见[2]。目前,针对土壤重金属污染经常使用固化稳定化药剂,使土壤中的重金属改变赋存形态,从而使其迁移性、溶解性减弱,最终达到毒性降低的目的[3]。而针对有机污染物的热解吸技术则通过加热土壤至100~300 ℃,并保持20 min以上,使土壤中有机污染物以气体形式逸出[4]。在处理重金属-有机复合污染时,可以根据场地情况联合使用2种技术。
目前,在处理重金属-有机复合污染时,通常采用先去除有机污染物,再修复重金属污染的联用方式[5];即先加热土壤进行热解吸后再添加固化稳定化药剂。但是,以这种顺序联用2种技术,一方面存在工艺流程设计不灵活、处理等待时间较长的问题;另一方面会遇到重金属污染土壤通过高温加热对重金属形态和浸出浓度产生影响的情况。例如,杨洁等[6]发现,经固化稳定化的砷污染土壤,在80 ℃条件下老化4和10 h 后,砷的不稳定形态发生了明显的提升,分别增加了71.47%和73.33%。尚小娟等[7]和BABA等[8]研究发现,在中性及酸性条件下,环境温度由10 ℃增加至30 ℃会导致重金属浸出增加,且在酸性条件下更易将重金属浸出。在采用与热解吸技术工况相似的温度时,马晓军[9]的研究指出,在高压碱性条件下反应12 h,重金属的形态出现改变,且浸出量下降;而在相似的低压状态,在500 ℃以上反应25 min的条件下,重金属的浸出率随温度升高而降低,重金属形态由酸溶态和可还原态向可氧化态和残渣态迁移[10-12]。
然而,对于在200~300 ℃微负压的热解吸技术工况下,土壤中重金属赋存形态的变化情况缺少研究。热解吸工艺在整个工艺流程中的放置顺序是否会影响重金属稳定化的效果目前并不明晰,这为复合工艺在实际工程中的联用顺序设计带来了较大的不确定性。鉴于此,本研究将通过实验确定热解吸工艺放置顺序对重金属稳定化效果的影响,以期为工程项目实施时的工艺设计提供参考。
全文HTML
-
本实验供试土壤分别采自湖南湘潭、陕西商洛和北京通州。其中,陕西商洛和北京通州所采样品为农田土壤。重金属稳定化药剂为Fixall,其主要成分为硫酸钙、氢氧化铁和氧化锰;其中,硫酸钙及其水合物占比约为70%、氢氧化铁约为20%、氧化锰约为5%、pH为7.5~8.5。
-
本实验加热土壤的设备为多段精确控温管式炉(BTF-1200C-Ⅲ,贝意克设备技术有限公司),使用硅钼棒元件加热石英管,温度在0~1 200 ℃间可调,控制精度为±1 ℃。
1.1. 供试材料
1.2. 实验装置
-
本实验共设置16种处理工况,每种处理工况设置3次重复,以代码代指经不同工况处理后的土样(见表1)。16种处理工况每个重复样品中污染土壤重量均为150 g。热解吸加热方式为间接热交换,加热时间为30 min,从达到目标温度后开始计算。其中,需要进行稳定化处理的样品以土壤重量分数10%加药;稳定化期间,土壤含水量保持在17%,养护时间为14 d。
-
土壤pH的测定方法采用国家农业行业标准《土壤pH的测定》(NY/T 1377-2007)[13];土壤有机质质量分数测定方法采用国家农业行业标准《土壤检测 第6部分:土壤有机质的测定》(NY/T 1121.6-2006)[14]。
重金属有效态质量分数测定方法采用国家环境保护标准《土壤 8种有效态元素的测定二乙烯三胺五乙酸浸提-电感耦合等离子体发射光谱法》(HJ 804-2016)[15]。重金属有效态指可被生物吸收利用的重金属形态,其主要包括可交换态、碳酸盐结合态及部分铁锰氧化物结合态与有机结合态[16]。
重金属酸浸出浓度测定方法采用国家环境保护行业标准《固体废物 浸出毒性浸出方法硫酸硝酸法》(HJ/T 299-2007)[17]。
重金属形态分级采用Tessier五步法[18]测定,将重金属形态分为可交换态(F1)、碳酸盐结合态(F2)、铁锰氧化物结合态(F3)、有机结合态(F4)和残渣态(F5),并依次分步测定。
2.1. 样品处理
2.2. 测试指标与检测方法
-
热解吸工艺对土壤pH的影响如表2所示。对3个地区获得的土壤样品进行加热均会导致其pH升高,上升幅度随温度的上升而增加。这与KHARE等[19]和MARCOS等[20]研究高温加热森林土壤后获得的结果类似。由于本实验中有机质含量变化不大,有机物氧化导致的阳离子释放可能不是唯一的原因,该结果可能也与高温导致黏土中羟基基团的流失有关[21]。然而,因为加热对不同性质土壤的pH有不同的影响,该结论不能推广到其他研究中;而且,由于加热导致的特定物质的氧化作用、表面增加暴露、胶体脱水等因素,对其他地区的土壤进行加热也许会导致pH降低[22-23]。添加稳定化药剂会影响土壤pH。例如,陕西商洛和北京通州的弱碱性土壤,添加Fixall药剂会降低其pH;而对于湖南湘潭的酸性土壤,添加Fixall药剂会升高其pH。Fixall药剂可以改变土壤pH主要是因为其中含有铁锰双金属材料,其有相当的致碱作用,可以大幅提升土壤的酸缓冲能力,同时也具有一定程度的碱缓冲能力[24]。
-
热解吸工艺对土壤有机质质量分数的影响如表3所示。对于陕西商洛的土壤,加热造成的有机质质量分数差异未达到显著性水平;对湖南湘潭场地的土壤,加热会降低土壤有机质质量分数,这与大量的实验结果保持了一致[20-22, 25]。添加稳定化药剂后加热与未添加药剂直接加热对有机质质量分数的影响类似,这说明调整热解吸工艺位置不会对土壤中有机质质量分数的变化产生影响。北京通州的土壤在经过热解吸后出现有机质质量分数增加的现象并不符合以往的实验结果;与自然条件下山火对土壤性质的影响不同,由于在本实验中并没有引入新的碳源,其土壤有机质质量分数的增加不可能是有机质在土壤中的重新分布导致的[26]。因此,该结果更有可能是取样的异质性和实验误差所导致的,此类问题也出现在了前人的研究中[25]。此外,有研究认为,测定土壤有机质质量分数使用的重铬酸钾容量法受锰离子、亚铁离子、氯离子的干扰较大[27]。而在本研究中,由于Fixall药剂中含有锰、铁等元素,故实验结果也可能与测定时受到干扰有关。
-
实验得出的热解吸工艺对土壤重金属有效态质量分数的影响如表4所示。由表中可知,对于大多数未添加稳定化药剂的土壤样品,加热会导致土壤重金属有效态质量分数增加。将未添加药剂并以300 ℃加热的样品与空白样品相比较,As的有效态质量分数在3种土壤样品中最多增加了0.04 mg·kg−1;Cd的有效态质量分数增加了0.18~3.18 mg·kg−1;Cu的有效态含量增加了0.09~1.16 mg·kg−1;Pb的有效态质量分数增加了0.07~0.16 mg·kg−1。总体上看,加热使土壤样品中重金属有效态的质量分数增加,但增加的幅度较低,在数量级上没有差异。相较于早先的重金属有效性研究关注全量有效性,重金属有效态主要描述的是土壤中能被有机体吸收利用甚至产生中毒作用的化学形态[28]。与土壤环境质量农用地土壤污染风险管控标准(试行)(GB 15618-2018)[29]中规定的农用地土壤污染风险管制值相比,本实验中,若原样品中有效态质量分数小于管制值,有效态质量分数的增加也不会使其超过管制值。这说明,加热过程虽然理论上可能导致原本不超标的土壤有效态质量分数超标,但其可能性较低,仅在样品空白值接近管控值时存在可能。添加药剂后的土壤样本重金属有效态质量分数均有明显下降;将添加药剂未加热的样品与空白样品相比较,As的有效态含量在3种土壤样品中下降的幅度最大,达到63%~90%;Cd的有效态含量最高下降了76%;Cu的有效态含量下降了13%~54%;Pb的有效态含量下降了44%~70%。从此可以看出,药剂对降低重金属有效态质量分数有较好的作用。在添加了稳定化药剂后,土壤样品在加热前后有效态质量分数差异不显著。同时,温度高低对稳定化处理后的土壤影响也较小;对于北京通州和陕西商洛的土壤来说,在200和300 ℃下,土壤中重金属有效态含量几乎不变。这说明热解吸工艺对土壤的加热过程并不会影响土壤重金属稳定化的效果。
-
实验得出的热解吸工艺对土壤重金属酸浸出质量浓度的影响如表5所示。由表中可知,对于3个地区中的绝大多数土壤样品,在不添加稳定化药剂的情况下,加热过程提高了其重金属浸出质量浓度,将未添加药剂并以300 ℃加热的样品与空白样品相比较,As的酸浸出质量质量浓度升高了0.01~0.15 mg·L−1;Cd的酸浸出质量浓度升高了0.006~0.830 mg·L−1;Cu的酸浸出质量浓度升高了0.005~0.960 mg·L−1;Pb的酸浸出质量浓度最高升高了0.18 mg·L−1。与有效态质量分数的变化类似,和空白样品相比,加热使土壤样品中重金属酸浸出质量浓度升高,但增加的幅度较低,在数量级上没有差异。与危险废物鉴别标准 浸出毒性鉴别 (GB 50853-2007)[30]相比,若原样品的浸出质量浓度符合标准,加热增加的酸浸出量也不会使样品的浸出质量浓度超标。这说明,加热过程虽然理论上可能导致原本不超标的土壤酸浸出质量浓度超标,但其可能性较低,仅在样品空白值接近限值时存在可能。添加药剂同样会使绝大多数样品的酸浸出质量浓度下降,以添加药剂的土壤样品与空白样品比较,As的酸浸出质量浓度最高下降了93%;Cd的酸浸出质量浓度最高下降了50%;Cu的酸浸出质量浓度最高下降了20%;Pb的酸浸出质量浓度最高下降了79%。可以看出,Fixall对重金属酸浸出质量浓度降低也有较好的作用。在添加了药剂以后,经加热的土壤样品与未经加热的土壤样品在酸浸出质量浓度上无显著差异。同时,温度的高低对稳定化处理后的土壤影响也较小。对于北京通州和陕西商洛的土壤来说,200和300 ℃下,土壤中重金属酸浸出质量浓度几乎不变。这说明,热解吸工艺对土壤的加热过程并不会影响土壤重金属稳定化的效果。
在添加了Fixall药剂后,对土壤的加热过程并不会使重金属有效态质量分数与酸浸出质量浓度增加,这与未添加稳定化药剂前不同。这可能是由于药剂中的有效成分含有铁锰双金属材料,而铁锰双金属材料对重金属的稳定化过程依靠专性吸附和沉淀反应。对于As而言,主要通过专性吸附形成内表面螯合物[31],沉淀反应较弱。而对于Cu、Pb、Cd等重金属来说,既发生专性吸附,也出现沉淀反应,形成羟基金属离子,并能促进碳酸盐和氢氧化物沉淀的形成[32]。此外,重金属离子也可以和反应中新形成的次级氧化物发生表面共沉淀反应,该沉淀具有更低的溶解性[33]。对于专性吸附而言,其稳定性较强,高温不会减弱土壤中的专性吸附作用[34]。例如,ZHAO等[35]的研究证实,由于吸附过程中关键的水合鞘破坏过程是吸热反应,MnO2对Pb的吸附作用可以被高温增强,去除率在20~60 ℃范围内,随温度升高而升高。对于共沉淀反应,高温也可能促进反应发生。有研究指出,利用共沉淀铁氧体净化重金属时,铁氧体的颗粒大小可随反应温度升高而增大,使无定型沉淀转变为晶型沉淀从而更加稳定[36]。
-
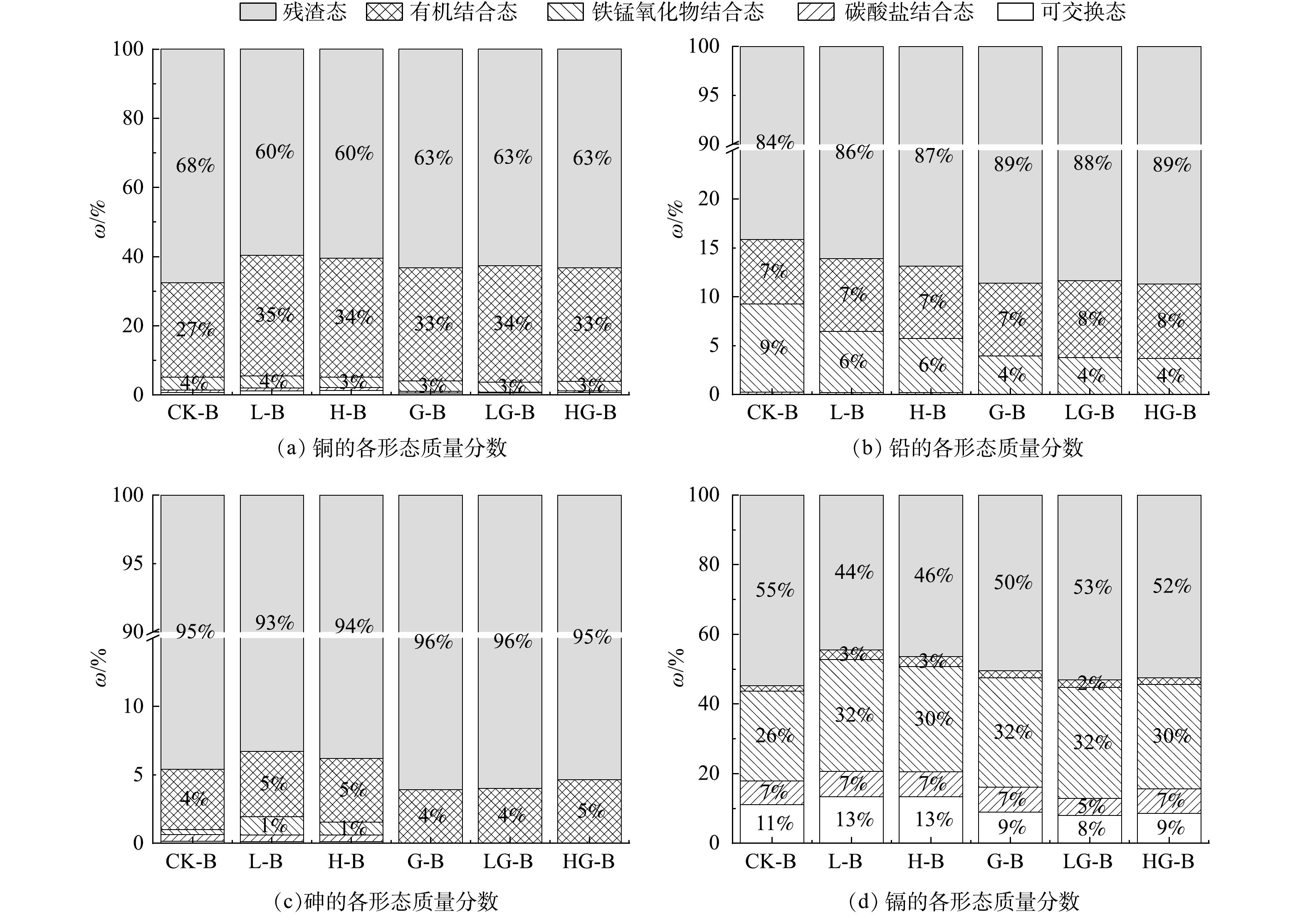
北京通州的不同种类土壤样品重金属形态如图1所示。可以看出,对于北京通州的土样,在未添加稳定化药剂前,加热使As的残渣态质量分数降低,铁锰氧化物结合态质量分数升高;Cu的残渣态质量分数降低,有机结合态质量分数升高;Cd的残渣态质量分数降低,可交换态与铁锰氧化物结合态质量分数升高。加热会增加部分重金属的不稳定性。
在添加稳定化药剂后,As、Cu向残渣态转化;Pb向有机结合态和残渣态转化;Cd向铁锰氧化物结合态和残渣态转化;各重金属稳定性均上升。在添加稳定化药剂后,加热对重金属的形态转化没有影响,不会影响药剂的稳定化效果。
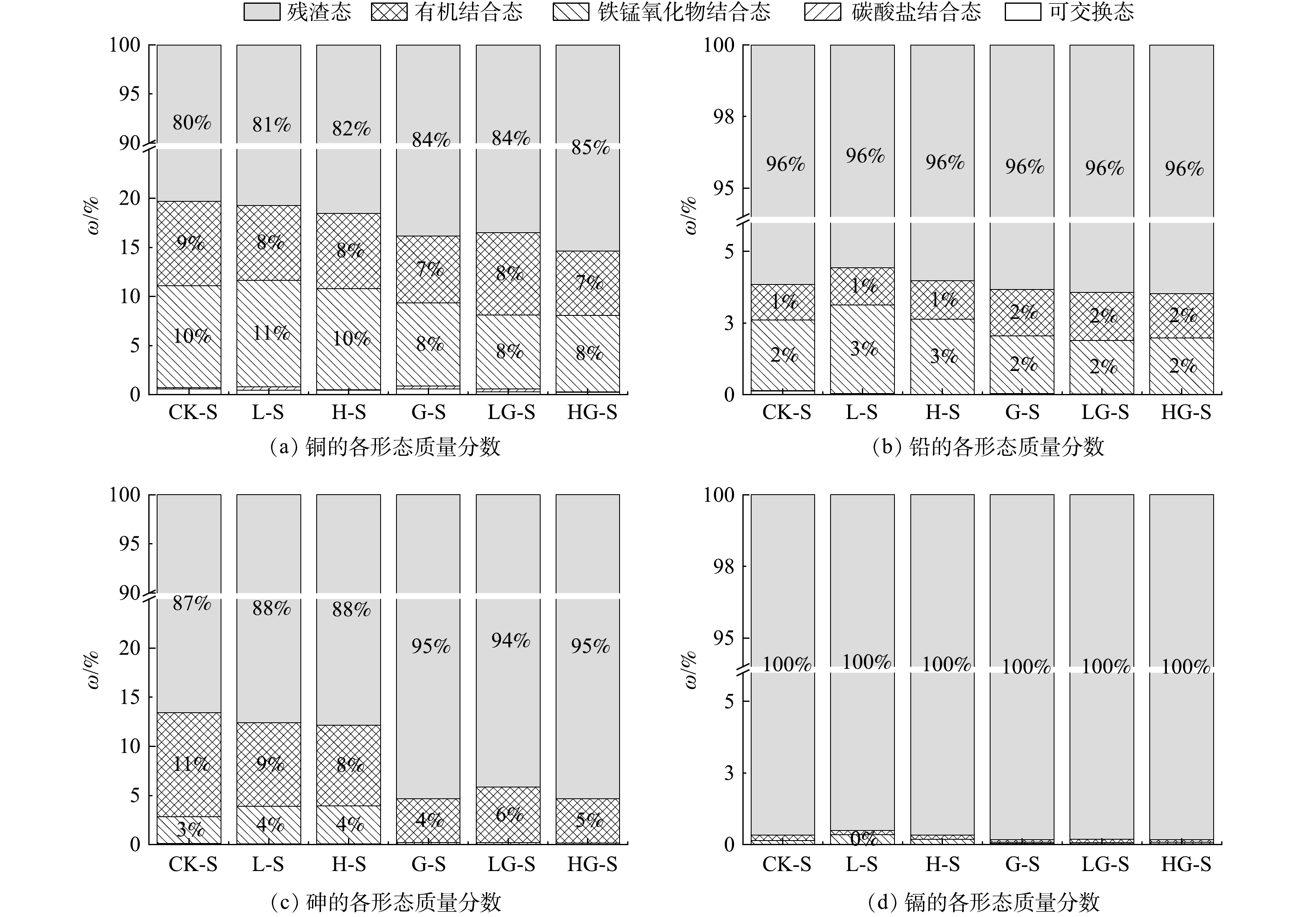
陕西商洛的不同种类土壤样品重金属形态如图2所示。对于陕西商洛的土样,在未添加稳定化药剂前,加热使As、Cu的有机结合态降低,铁锰氧化物结合态质量分数升高,Pb的铁锰氧化物结合态质量分数升高。加热会增加部分重金属的不稳定性。
添加稳定化药剂后,As由铁锰氧化物结合态和有机结合态向残渣态转化;Cu向残渣态转化;Pb向有机结合态转化;各重金属稳定性均上升。同样的,在添加稳定化药剂后,加热对重金属的形态转化没有影响,不会影响药剂的稳定化效果。
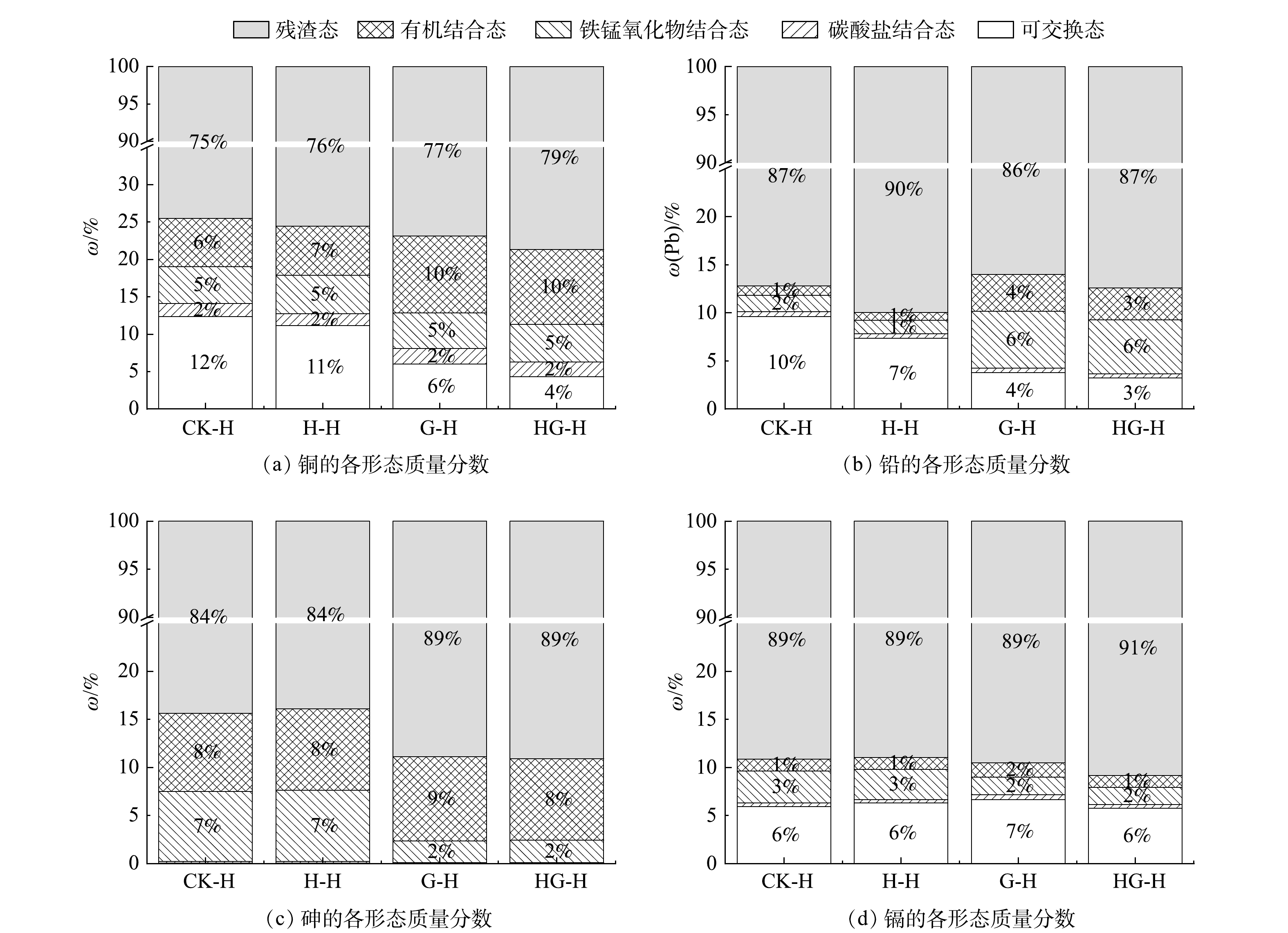
湖南湘潭的不同种类土壤样品重金属形态如图3所示。湖南湘潭的酸性土壤与陕西和北京的碱性土壤不同,在未添加稳定化药剂时进行加热,Pb与Cu重金属可交换态均有轻微降低并向残渣态转化,而As与Cd的重金属形态没有改变。
添加稳定化药剂后,As由铁锰氧化物结合态向残渣态转化;Cu由可交换态向残渣态转化;Pb由可交换态向铁锰氧化物结合态和有机结合态转化。各重金属稳定性均上升。加热后,Cd、Pb和Cu的可交换态均有轻微降低并向残渣态转化。因此,在添加稳定化药剂后,加热对酸性土壤中重金属的形态转化有正面影响,在300 ℃下加热可以加强药剂的稳定化效果。
在加入稳定化药剂前后,碱性土壤与酸性土壤在加热条件下呈现了不同的重金属赋存形态变化。总体上,碱性土壤中的重金属在加热后倾向于转化为更活跃的形态,而酸性土壤中的重金属在加热后倾向于转化为更稳定的形态。这可能是因为,加热轻微提高了酸性土壤的pH,使得土壤颗粒表面的负电荷增加,提升了土壤对重金属的吸附能力,固体表面结合力增强[37]。温度升高不会增加酸性土壤中重金属的不稳定性。判断热解吸工艺顺序是否影响其他药剂的重金属稳定化效果,也应从其重金属去除机理是否受高温影响的角度分析。一方面,若稳定化药剂主要依靠范德华力、静电相互作用等物理吸附方式稳定土壤中的重金属,那么很可能易受高温影响;例如,活性炭与生物碳材料。另一方面,若稳定化药剂主要依靠化学专性吸附、沉淀作用、络合反应和共沉淀作用稳定土壤中的重金属,那么可能不易受高温影响;例如,Fe、Mn、Al氧化物、磷酸盐、中性化物质如石灰等。此外,非物理吸附原理但高温下易于氧化变性的稳定化药剂也可能会受到影响;例如,纳米铁和有机聚合物等。
3.1. 热解吸工艺对土壤pH的影响
3.2. 热解吸工艺对土壤有机质质量分数的影响
3.3. 热解吸工艺对土壤重金属有效态质量分数的影响
3.4. 热解吸工艺对土壤重金属酸浸出质量浓度的影响
3.5. 热解吸工艺对土壤重金属形态转化的影响
-
1)在添加重金属稳定化药剂前,热解吸工艺会提高土壤的pH,并使土壤中重金属有效态质量分数、重金属浸出质量浓度增加,与土壤酸碱性无关。热解吸工艺不影响酸性土壤中的重金属稳定性,但会增加碱性土壤中重金属的不稳定性。然而,加热过程使土壤污染物质量分数超标的可能性较低,热解吸工艺的影响较小。
2)在添加重金属稳定化药剂后,热解吸工艺对重金属有效态、重金属酸浸出质量浓度无影响。热解吸工艺对碱性土壤中药剂的稳定化效果无影响,并会加强酸性土壤中药剂的稳定化效果。
3)热解吸工艺的放置顺序对土壤重金属稳定化效果影响较小,在工程项目实施中可以对2种工艺的联用顺序进行灵活设计。





 DownLoad:
DownLoad: