-
近年来,抗生素的广泛使用导致其以不同的方式大量流入环境[1-2],其中包括盐酸土霉素。盐酸土霉素属于一种广谱抗菌素,在养殖业和农业中作为杀虫剂普遍使用,但是其很难被生物体完全吸收,盐酸土霉素的部分代谢产物及大量的残留会进入环境中,危害环境并给人类带来危害风险[3]。目前,针对抗生素的废水处理方法有水解、生物降解、高级氧化法等,其中,水解和生物降解均有耗时长、耗资大等缺点。高级氧化法是目前研究最为广泛一种废水处理方法,包括有芬顿氧化法[4-5]、光催化氧化法[6]和电化学氧化法[7-8]等。
高级氧化法主要利用具有强氧化性功能的羟基自由基(·OH)或硫酸根自由基(
SO⋅−4 )与废水中的目标污染物发生反应,氧化降解污染物并使其矿化。近年来,运用SO⋅−4 [9]的高级氧化技术逐渐成为热门,跟·OH[10-11]比较发现,SO⋅−4 具有较低的氧化还原电势(2.60 V),而且SO⋅−4 的使用寿命比·OH要更长久,能在降解污染物的同时保持节能和高效[12-14]。常规的高级氧化催化剂的催化活性较低,其中,一种新颖的金属-有机骨架材料(metal-organic frameworks, MOFs)引起人们广泛的关注。MOFs因其具有高比表面积、高稳定性和高孔隙率的特点被频繁运用。如PENG等[15]和ZHANG等[16]研究基于MOFs的新型材料MIL-53(Al)和H-UiO-66s对各类废水有机污染物的捕获时发现,MIL-53(Al)和H-UiO-66s均对有机污染物产生高效的吸附和去除,这表明MOFs具备去除污染物的性能。另外,MON等[17]和胡龙兴等[18]研究MOFs对水体污染的修复效果的结果表明,MOFs能有效的降解有机污染物。本研究采用水热法制备Co-MOF催化剂,并对其物化性质进行了表征。同时,考察了Co-MOF活化PS降解盐酸土霉素的性能及重复利用效果,并进一步对该降解反应的机理进行分析,以期为新型高效降解体系的开发及其在水环境污染控制领域的应用提供参考。
全文HTML
-
实验试剂:均苯三甲酸(GR,上海化学)、三乙胺(GR,国药控股)、六水合硝酸钴(AR,国药控股)、叔丁醇(CP,国药)、抗坏血酸(AR,国药)、盐酸土霉素(国药);其他试剂均为国药分析纯试剂,实验用水为去离子水。
实验仪器:KH-100型Teflon-lined反应釜(北京瑞昌伟业)、pHS-3C型pH计(上海仪电科学)、UV1900型紫外可见分光光度计(上海佑科)、SHA-C型水浴恒温振荡箱(常州澳华)、ZA3300型火焰原子吸收分光光度计(北京日立)。
-
1) Co-MOF的制备。量取25 mL去离子水于烧杯中,加入1.45 g Co(NO3)2•6H2O、1.05 g均苯三甲酸和2 mL三乙胺,再将烧杯放置在磁力搅拌器上搅拌15 min,然后将溶液转移到Teflon-lined反应釜中,密封放置在190 ℃的电热鼓风干燥箱中24 h。将反应后所得离心(6 000 r·min−1) 2 min获取沉淀物,用乙醇和去离子水各反复冲洗3次,再60 ℃真空烘干备用。
2) Co-MOF降解盐酸土霉素的实验。量取20 mg·L的盐酸土霉素于反应器中,加入一定量的Co-MOF和PS,在恒温震荡箱中反应5 min,特定时间取样,并用紫外分光光度计在353 nm波长处测定吸光度,根据标准曲线计算盐酸土霉素反应后的浓度。实验结束后收集定量的上清液,加入适量硝酸酸化至pH≤2,然后用火焰原子吸收分光光度计测定其中的钴含量。盐酸土霉素的降解率按照式(1)进行计算。
式中:
η 为盐酸土霉素的降解率;C0和Ce分别为盐酸土霉素溶液初始浓度和平衡时的浓度,mg·L−1。
1.1. 试剂和仪器
1.2. 实验方法
-
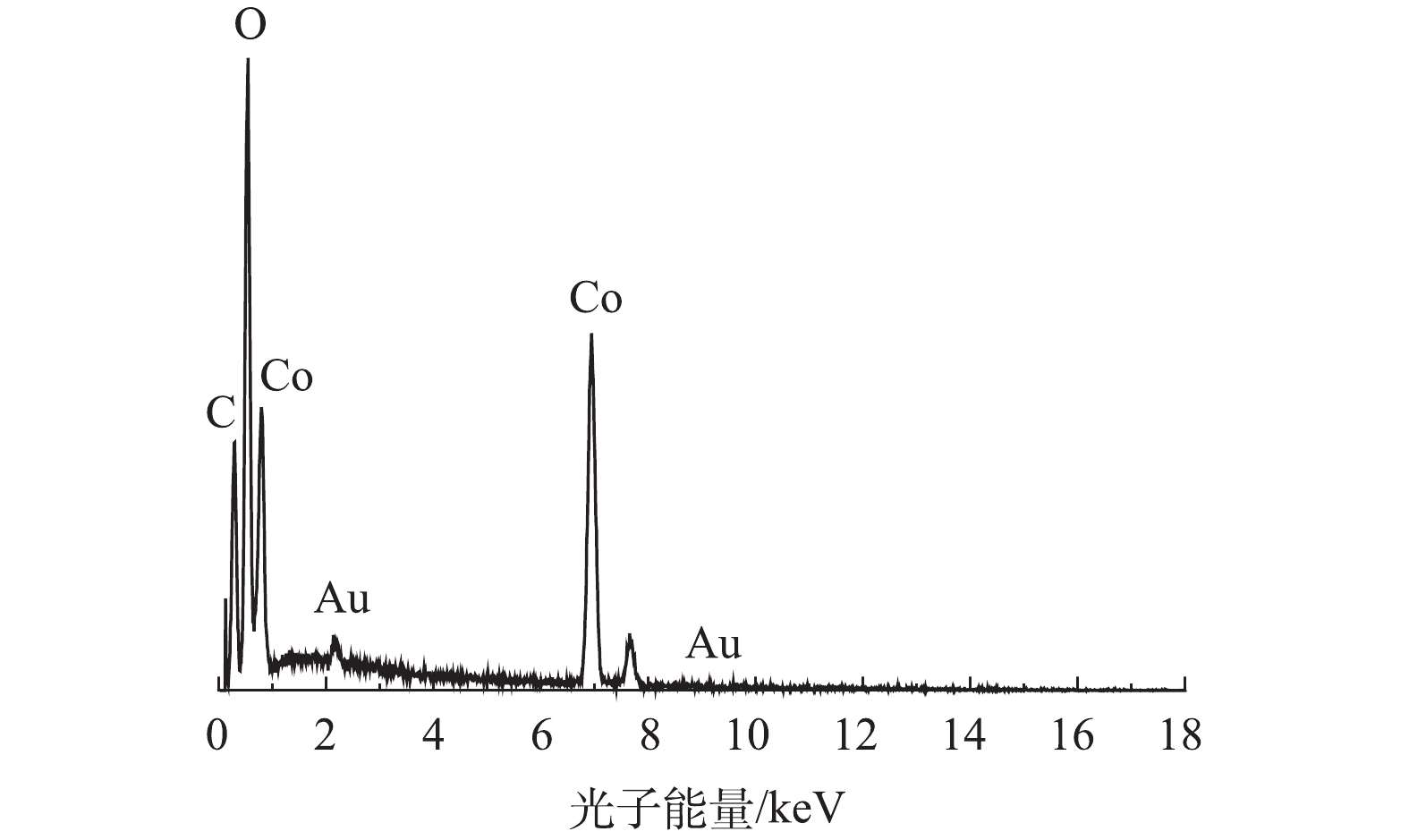
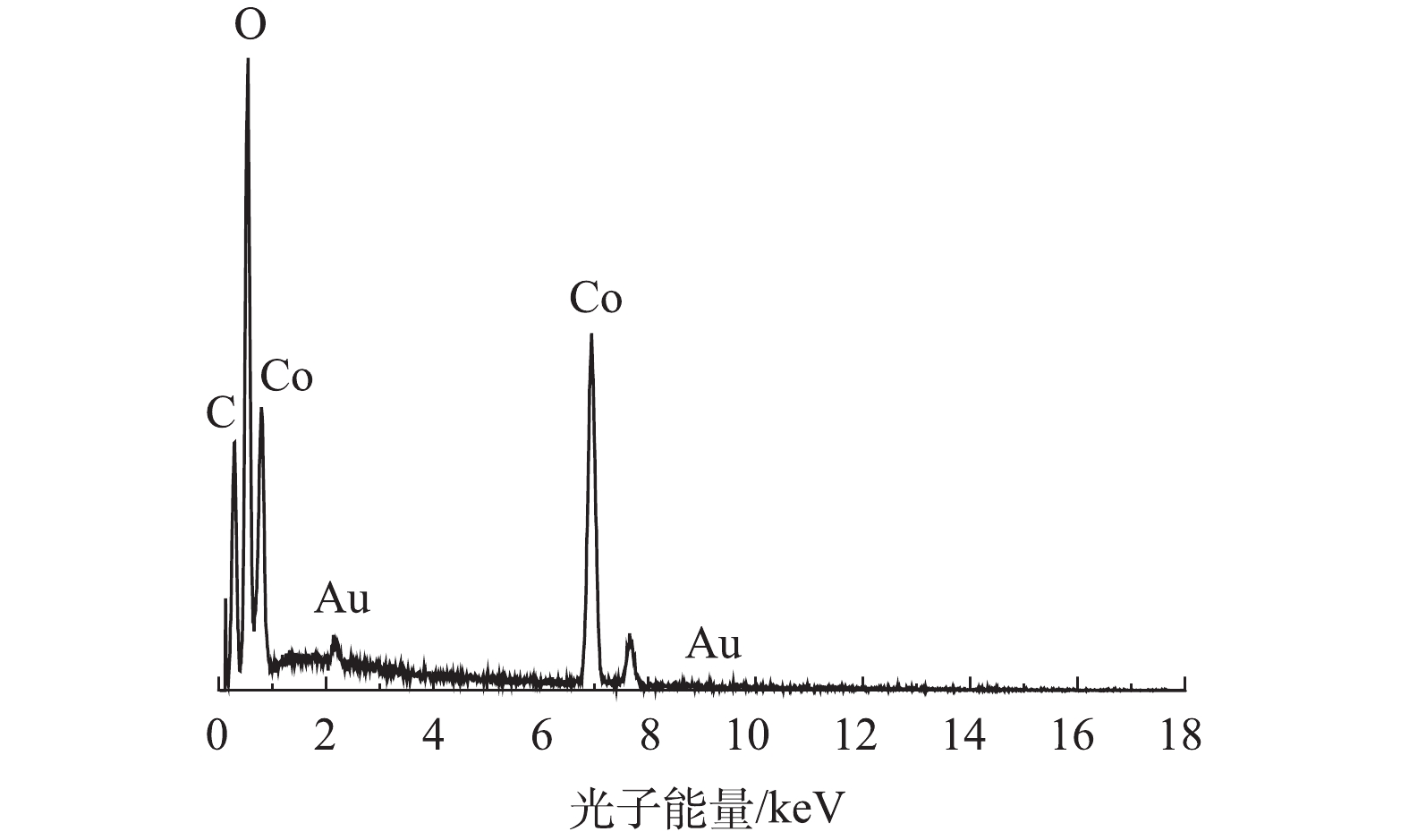
1)扫描电镜(SEM)和透射电镜(TEM)。通过SEM、TEM和EDS对制备的Co-MOF的形貌特征、粒径以及组成成分进行分析,结果见图1。如图1(a)和图1(b)的SEM表征所示,Co-MOF是由棒状晶体组成,每个棒状晶体的长度大约几百微米,宽约为30~100 μm,这与YAGHI等[19]的报道结果相似。如图2所示,Co-MOF含有C、O和Co元素,其中,Co元素的相对峰面积占比较大,这表明Co在Co-MOF结构中的重要性。如图1(c)和图1(d)的TEM表征所示,可见Co-MOF是由棒状晶体组成,并且每个棒状晶体表面平滑、多孔隙,这与PATTERSON等[20]的研究结果类似。
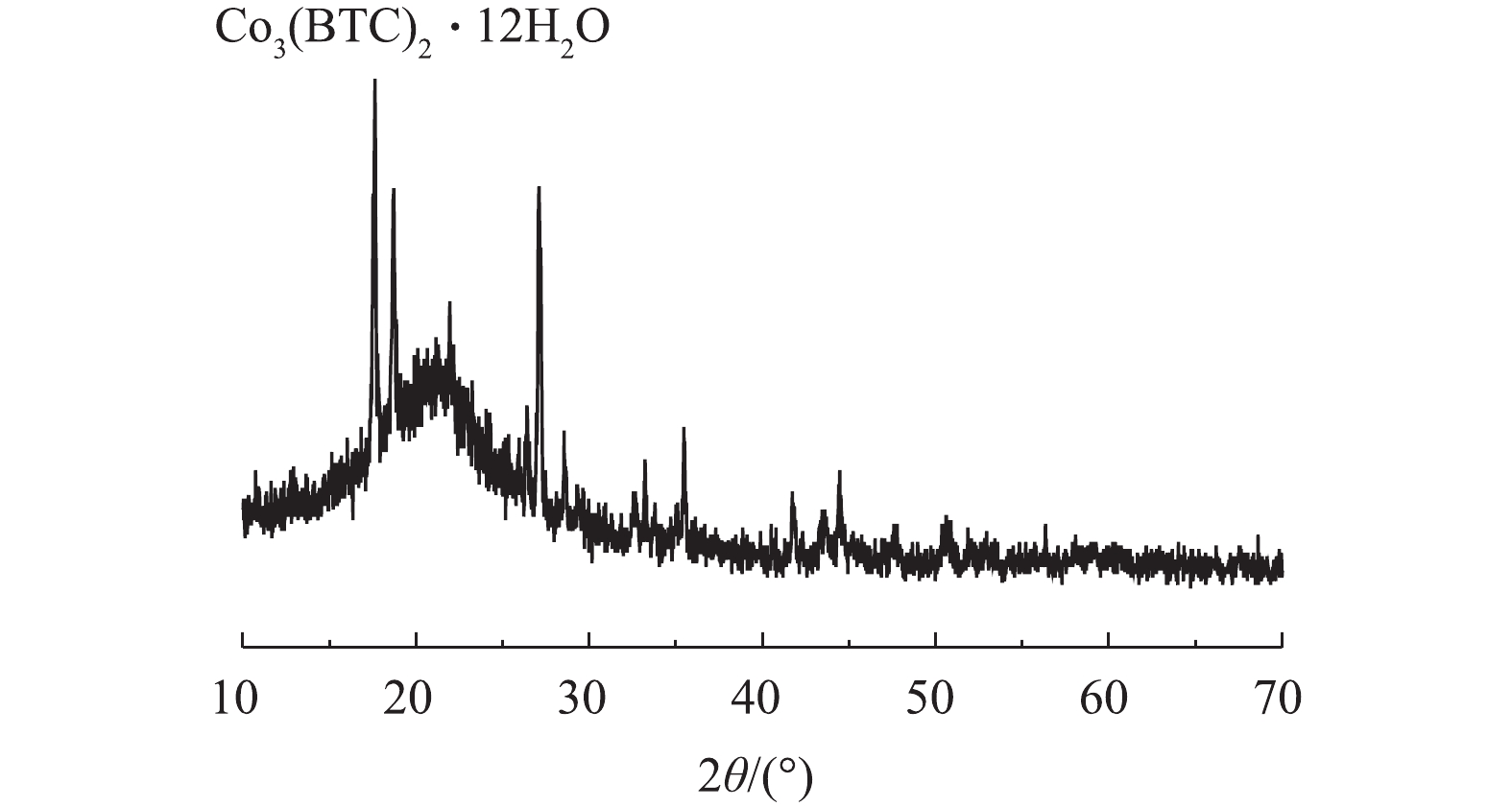
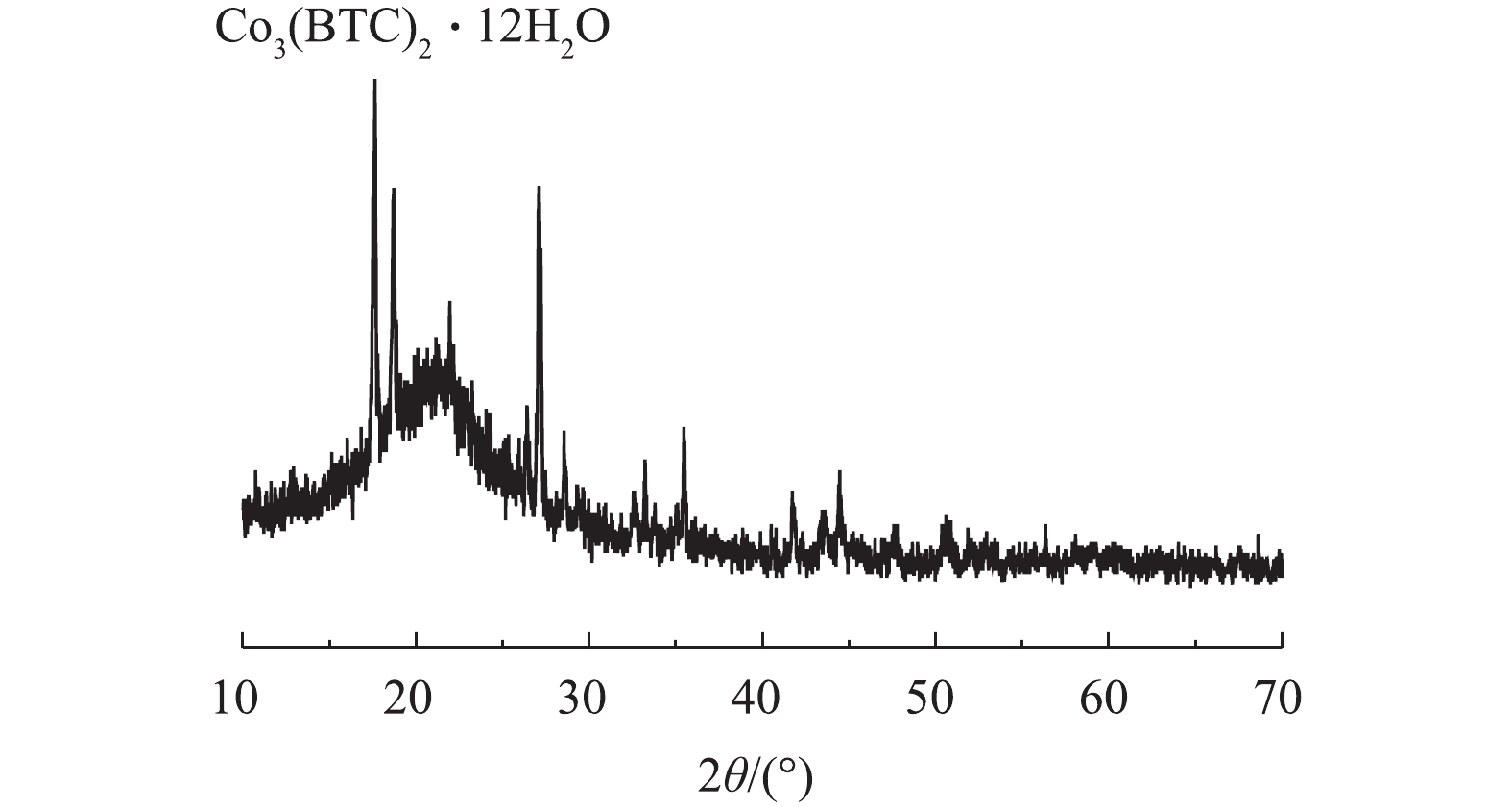
2)X射线衍射(XRD)。通过XRD对制备的Co-MOF结构进行分析。如图3所示,在17.5°附近有明显的衍射峰,此峰对应Co3(BTC)2·12H2O的晶面(014),故这表明Co(NO3)2·6H2O和均苯三甲酸发生完美融合,这与以往报道[21-22]中的Co-MOF的XRD图谱相似。
-
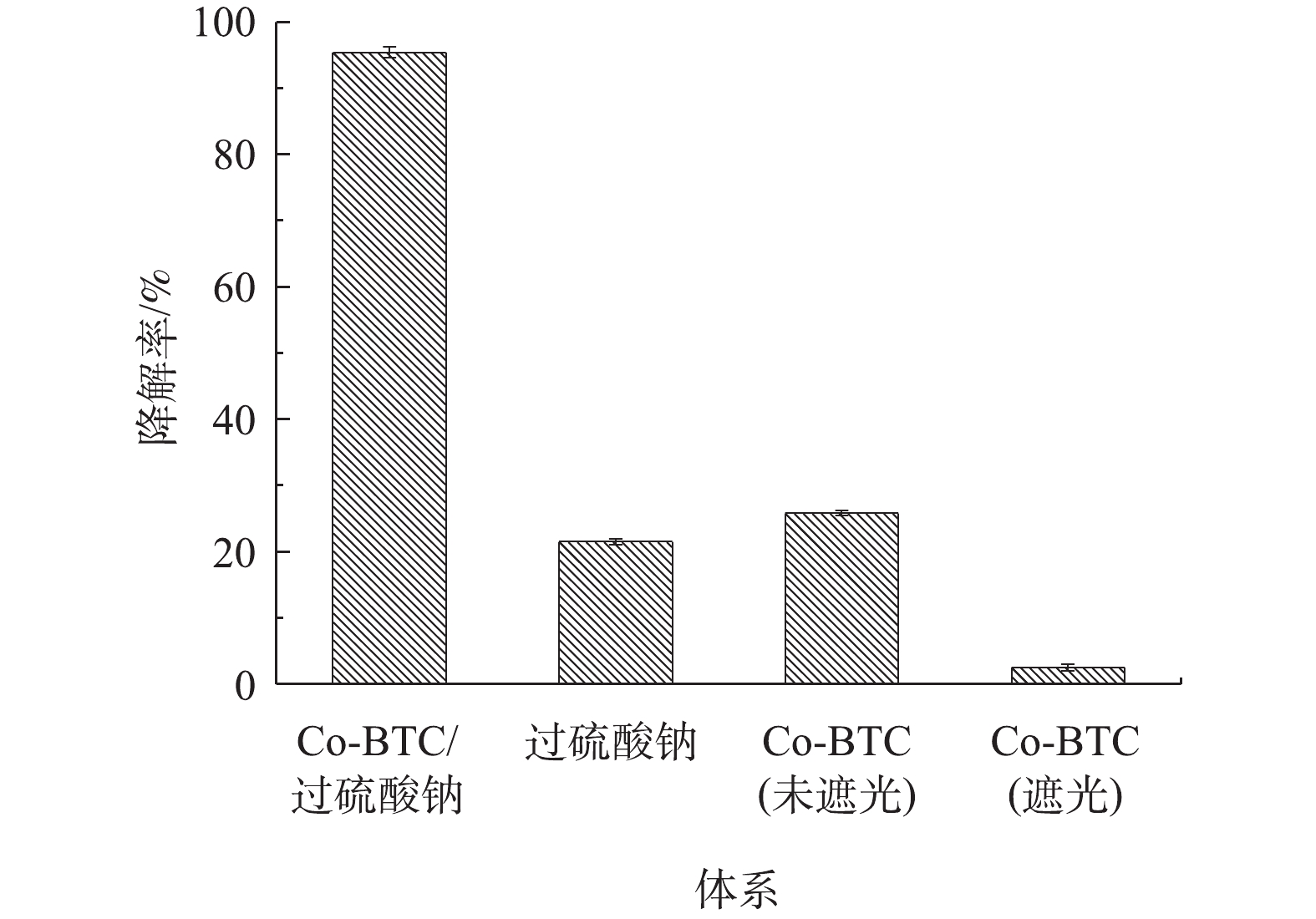
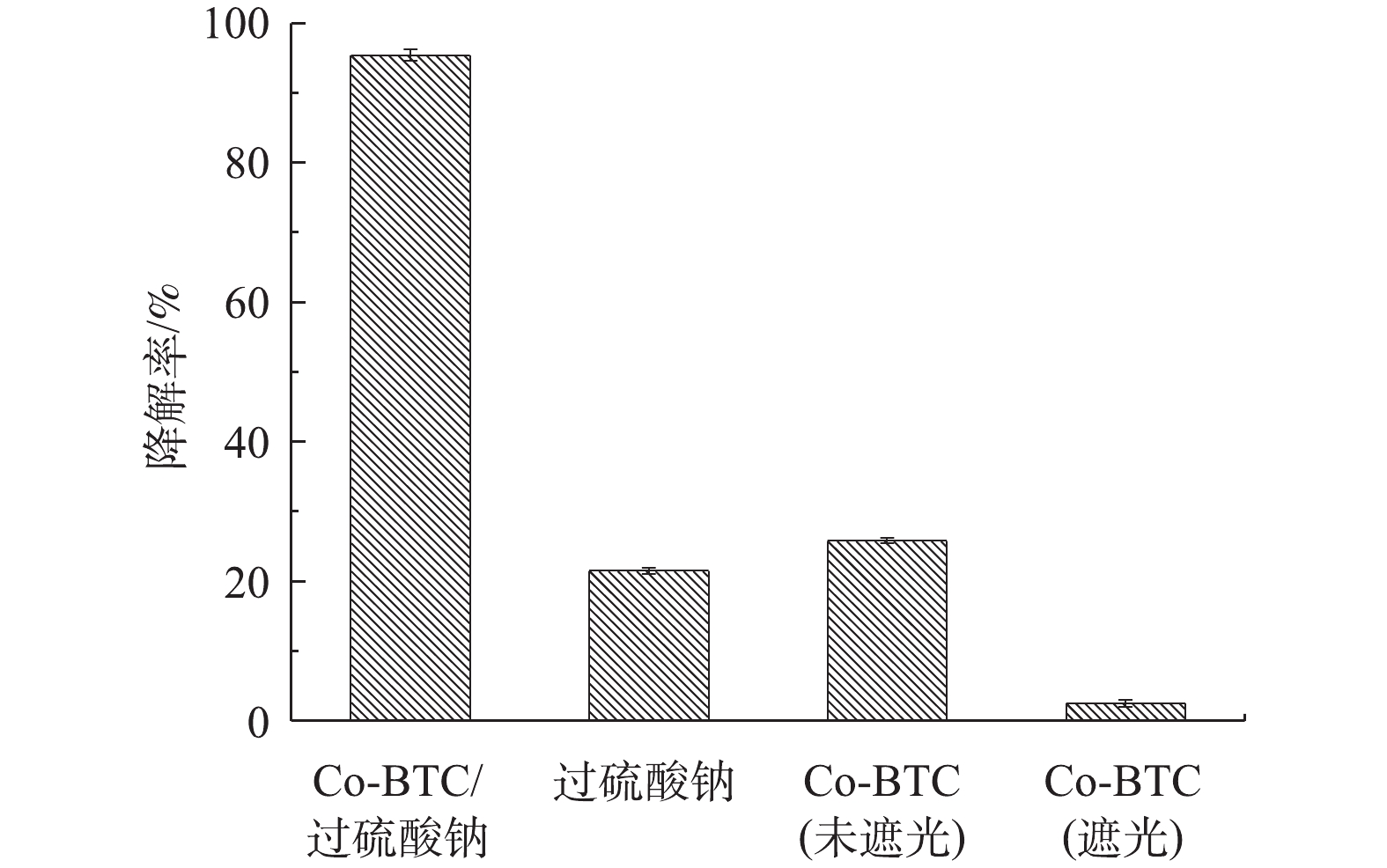
图4为不同催化剂反应体系下盐酸土霉素的降解效果对比。由图4可见,在第1组(未遮光)和第2组(遮光)中,单独的Co-MOF添加对盐酸土霉素的降解率分别为25.8%和3.9%,这是Co-MOF自身的光催化特性导致,如孙登荣等[23]研究MOFs材料的光催化性能时发现,MOFs具有光催化性能。在第3组实验中,单独的PS添加对盐酸土霉素的降解率为21.5%,这是由于PS的热活化反应导致。杨世迎等[24]开展的活化过硫酸盐高级氧化技术的研究结果表明,在热、光、过渡金属等外在条件的催化下,过硫酸盐均能通过吸收能量来使内部构造发生变化。在第4组实验中,Co-MOF/PS对盐酸土霉素的降解率为95.4%。这样的结果与预期一样,表明Co-MOF具有高效活化PS的性能。
-
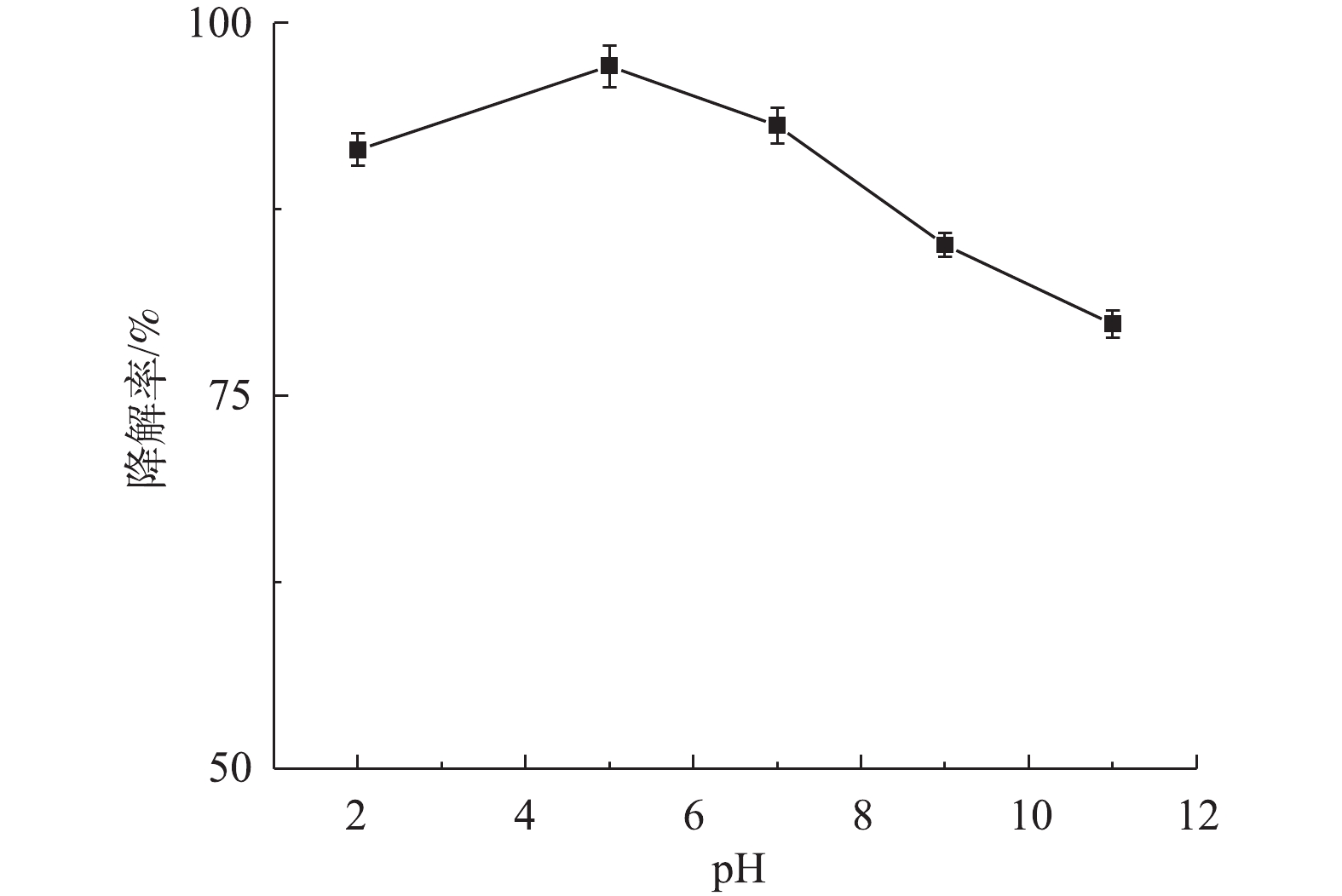
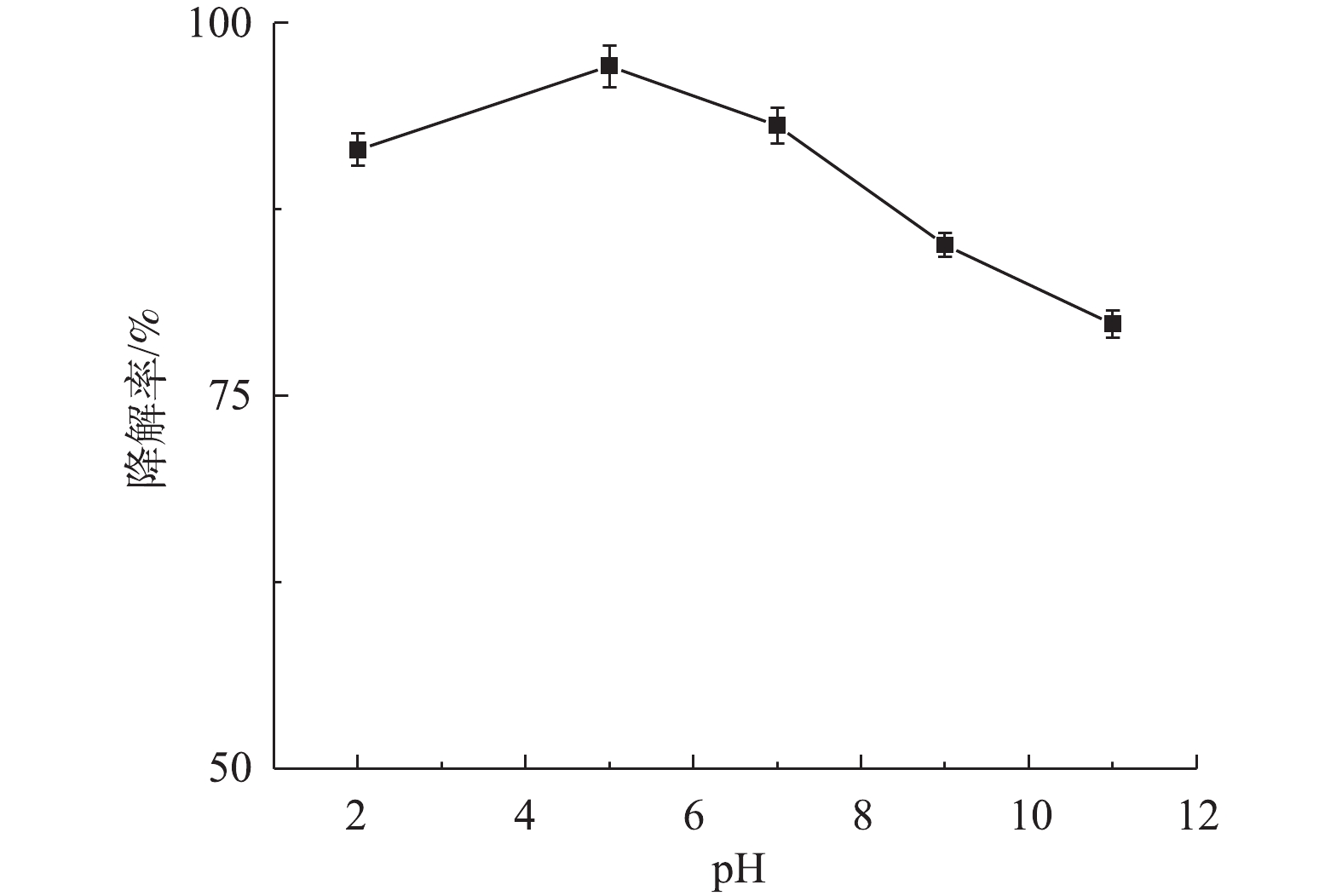
1) pH对盐酸土霉素降解的影响。图5为不同pH对盐酸土霉素降解的影响。如图5所示,盐酸土霉素在pH=2.0~11.0时均有不同程度的降解,其中,当pH=5.0时,对盐酸土霉素的降解率最高为97.1%。当pH=2.0、3.0、9.0和11.0时,对盐酸土霉素的降解率分别为91.5%、93.1%、85.3%和79.8%,这与预估一致,一方面是由于
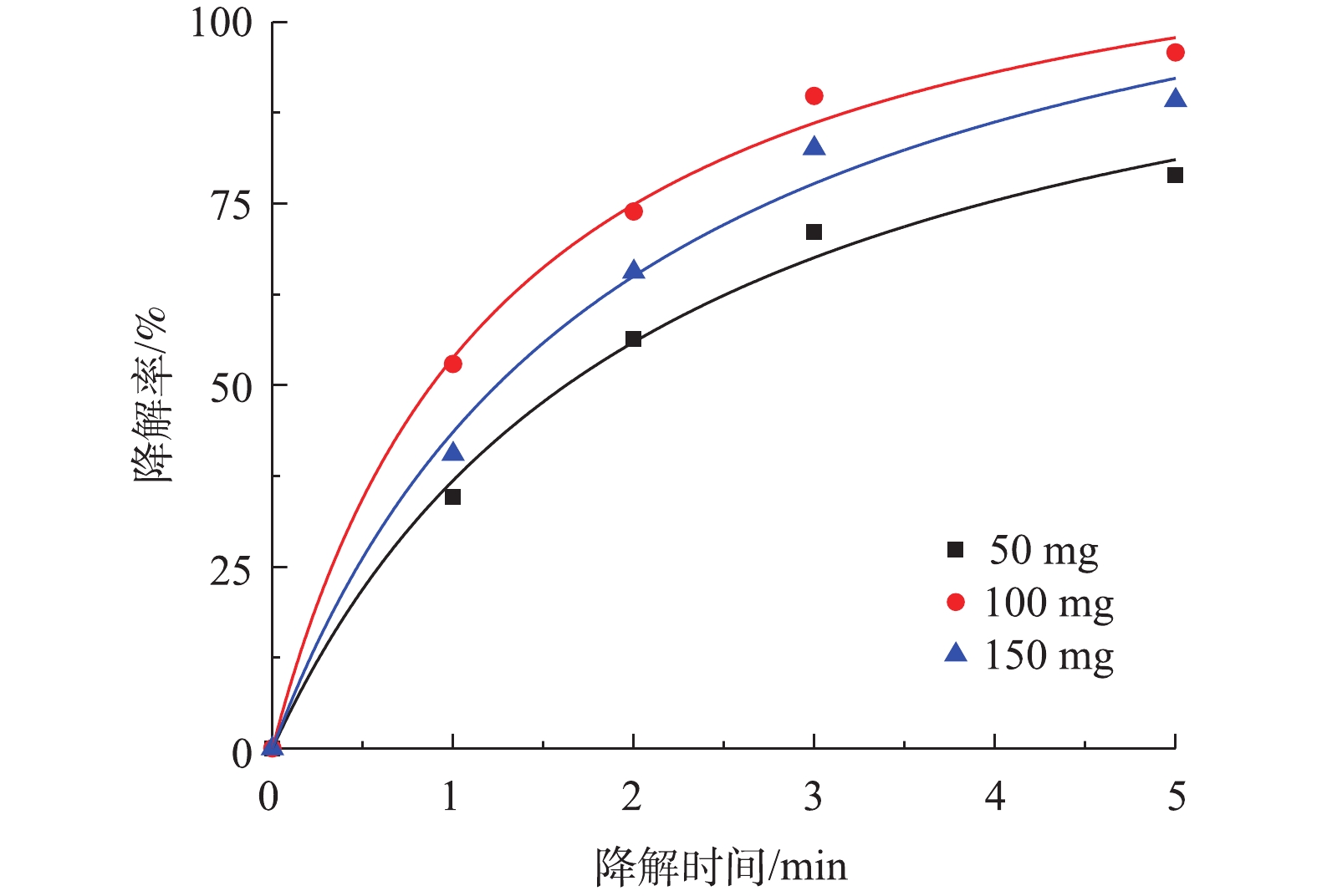
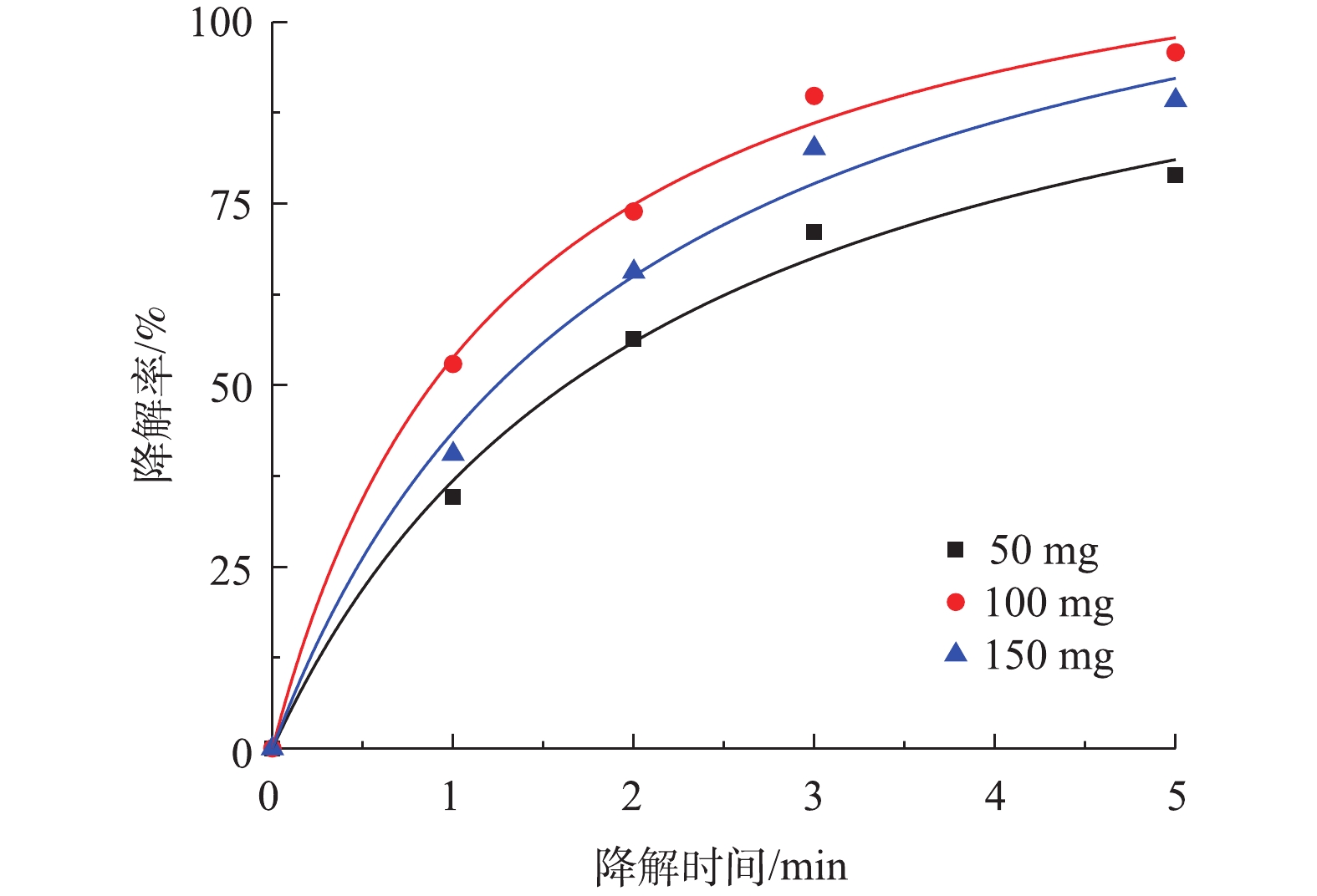
SO⋅−4 和·OH在pH≤3时与H+发生反应引起的(式(2)和式(3)),导致SO⋅−4 和·OH被清除;另一方面是由于SO⋅−4 与OH−和水发生反应引起的(式(4)和式(5)),导致SO⋅−4 被转化为·OH。2) PS投加量对盐酸土霉素降解的影响。由图6可知,当PS添加量为从50 mg增加到100 mg时,对盐酸土霉素的降解率从78.9%上升到95.8%,这表明盐酸土霉素的降解率随着PS投加量的增加而变大。而PS投加量达到150 mg时,对盐酸土霉素的降解率下降,原因是由于过多的PS会使
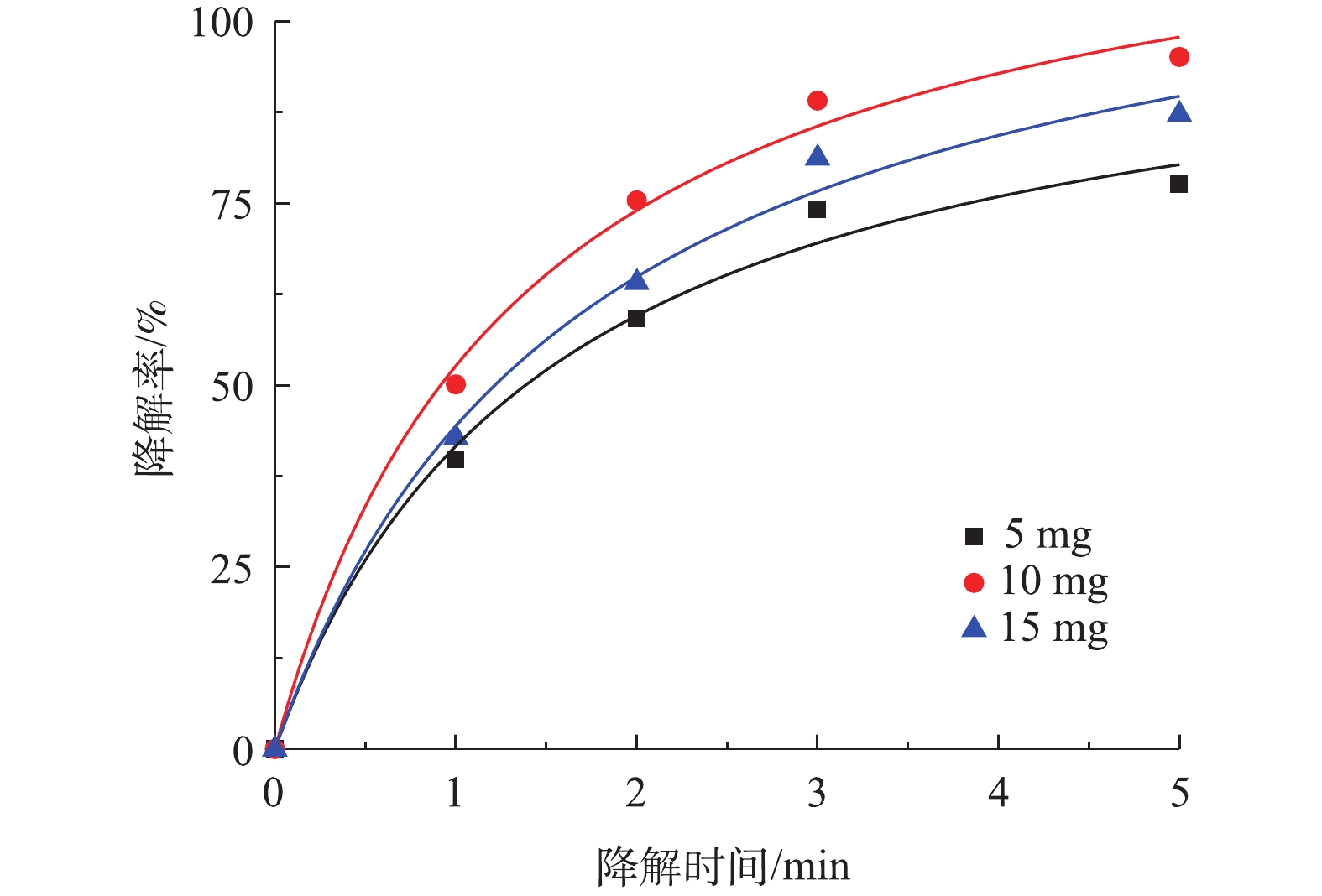
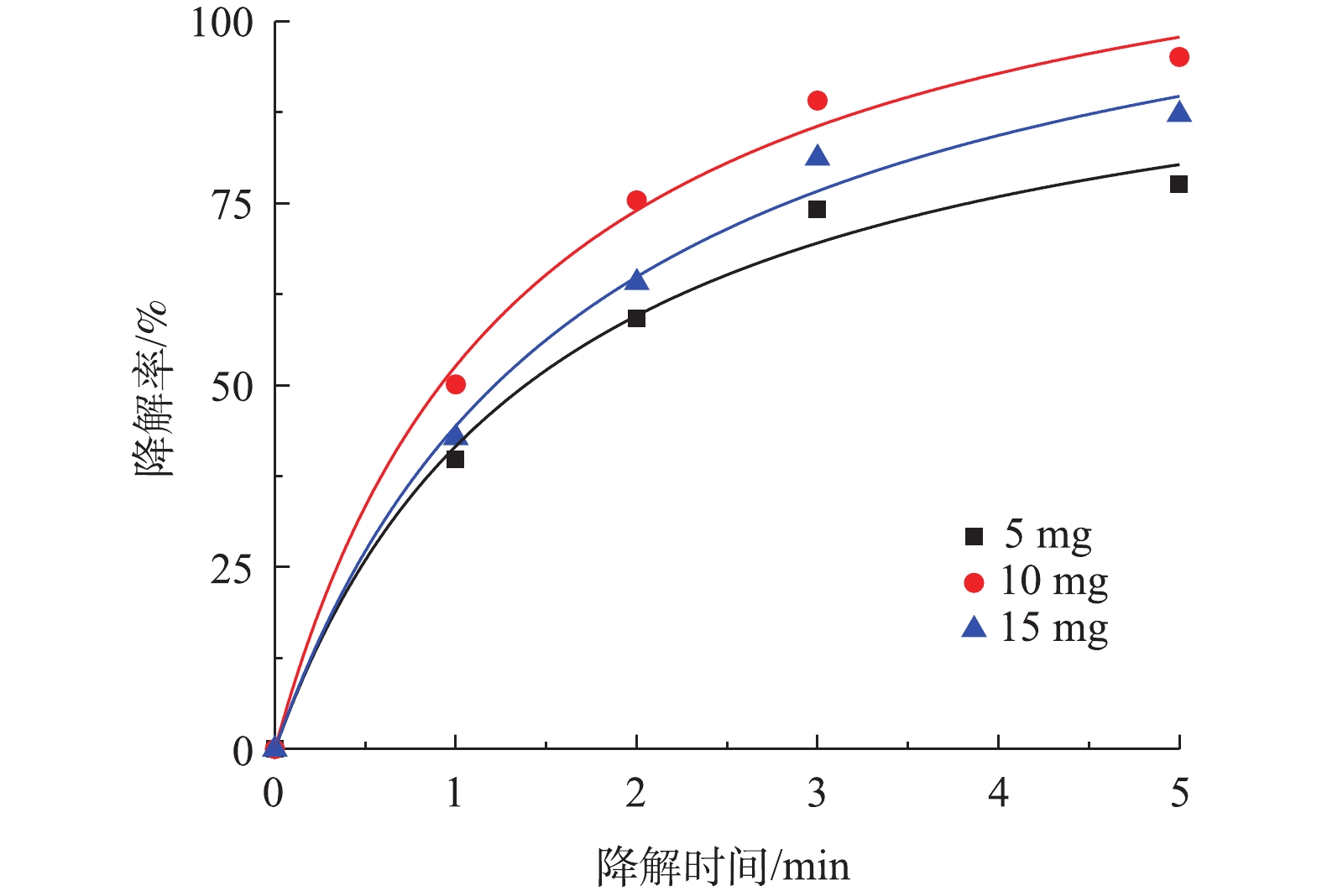
SO⋅−4 量超过临界值,使SO⋅−4 被PS捕获清除[25]。根据图6中拟合曲线结果,Co-MOF活化PS降解盐酸土霉素的动力学曲线符合准二级动力学模型,50 mg和100 mg PS添加量对应的的拟合曲线中R2分别为0.992 6和0.995 6,而150 mg PS添加量的拟合曲线中的R2最低为0.989 3,由于100 mg PS添加量的拟合曲线中R2高于50 mg添加量,所以确认本研究中最佳PS投加量为100 mg。3) Co-MOF投加量对盐酸土霉素降解的影响。由图7可知,5 mg Co-MOF添加量对盐酸土霉素的降解率为77.6%,10 mg Co-MOF添加量对盐酸土霉素的降解率为95.1%,而15 mg Co-MOF添加量对盐酸土霉素的降解率为87.2%,这表明随着Co-MOF投加量的增加,盐酸土霉素去除率呈现先增后减的趋势。造成这种情况的原因是:一方面是由于过多的
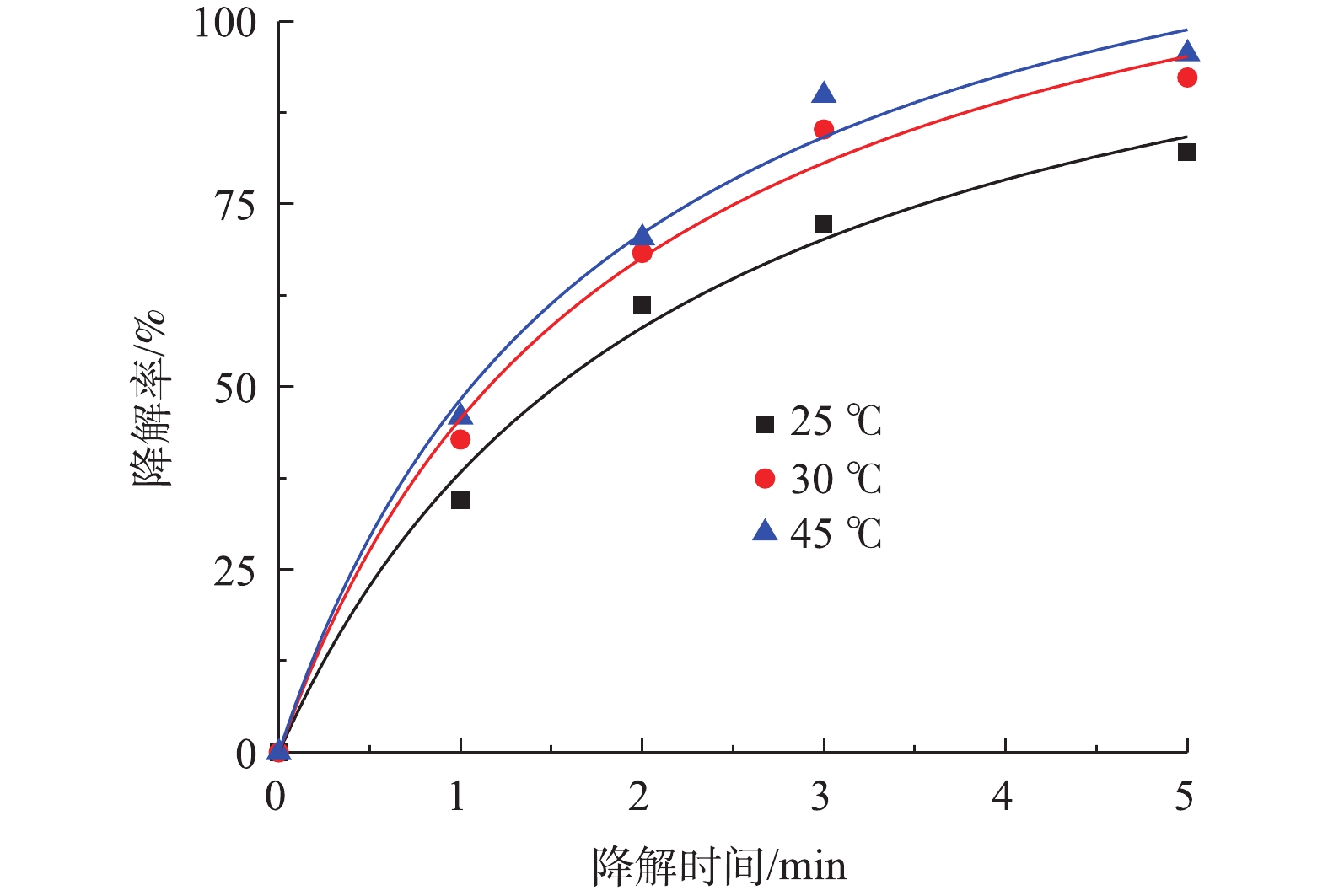
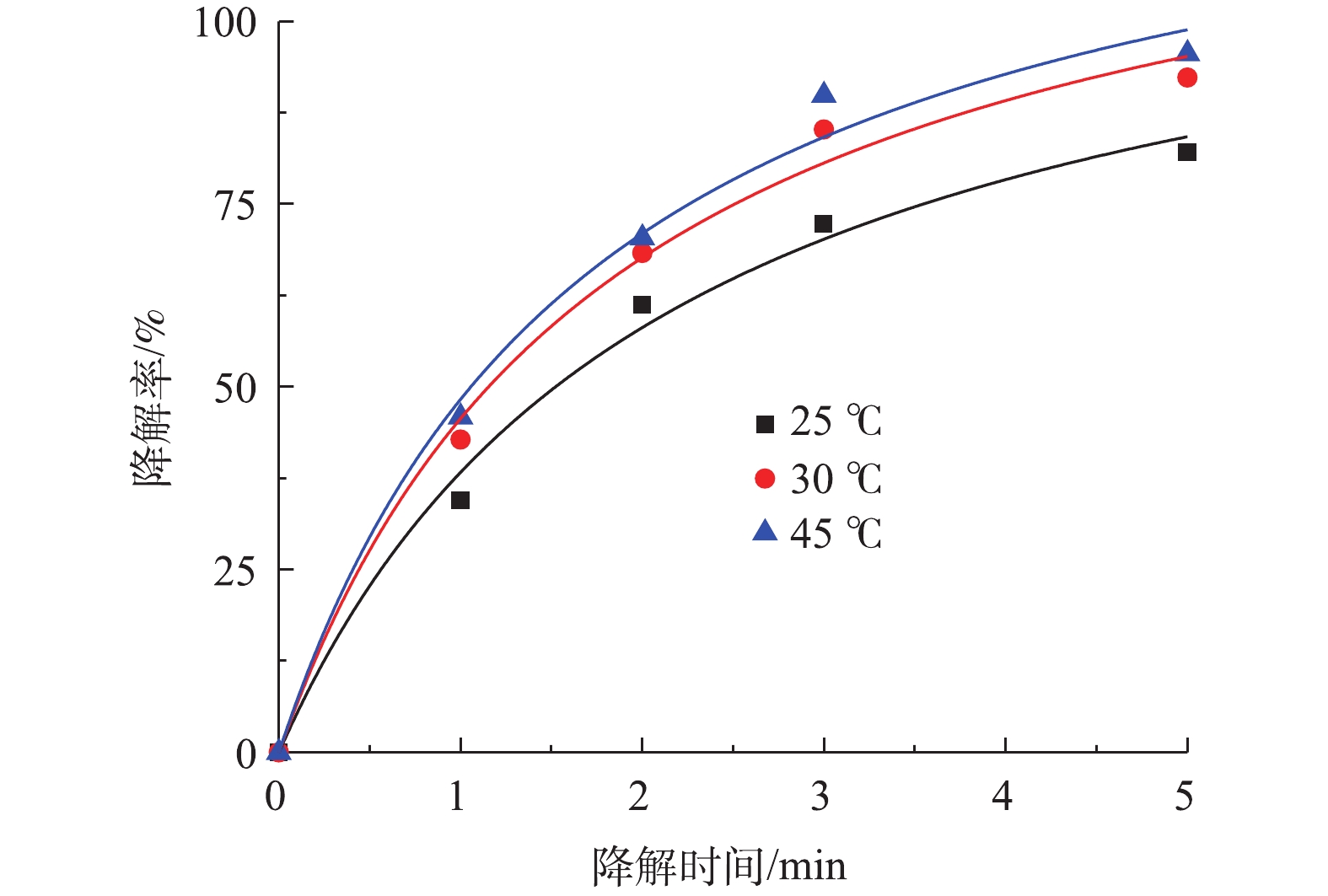
SO⋅−4 会产生自我清除反应;另一方面由于过多的Co-MOF会增加溶液内的浊度。根据图7中拟合曲线结果,Co-MOF活化PS降解盐酸土霉素的动力学曲线符合准二级动力学模型,其中5 mg Co-MOF添加量的曲线拟合度R2最小为0.989 6,而10 mg和15 mg Co-MOF添加量的曲线拟合度R2分别为0.993 7和0.992 0,由于10 mg Co-MOF添加量的拟合曲线中的R2最高,所以确定本研究中最佳Co-MOF投加量为10 mg。4)温度对盐酸土霉素降解的影响。图8为不同反应温度对盐酸土霉素降解的影响。如图8所示,在25 ℃时,对盐酸土霉素的降解率有82.1%;在30 ℃时,对盐酸土霉素的降解率上升到92.3%;而当45 ℃时,对盐酸土霉素的降解率高达95.6%。这表明随着反应温度的升高,对盐酸土霉素的降解率也随之增大。在Co-MOF/PS体系中,
SO⋅−4 的生成不仅被Co-MOF的活化性能影响,还被温度影响。随着温度的增加,加快体系中PS的热激活行为,加速电子转移,使PS的O—O键更易于断裂,SO⋅−4 的生成更多更快,从而提高对盐酸土霉素的降解率。以往的报道[26-27]也证实这点,如刘红梅等[28]开展的热活化过硫酸盐降解土壤和地下水中污染物的研究发现,当温度过低时并不能对过硫酸盐进行有效的活化并生成SO⋅−4 ,反而在升温过程中SO⋅−4 的生成速率会加快,进而促进盐酸土霉素的降解;但当温度过高时也会受到抑制影响,原因是由于自由基被高温清除。龙安华等[29]关于活化过硫酸盐降解水污染的研究结果也表明,在热活化过硫酸盐的过程中,随着温度的变化,pH、离子强度及有机质耗氧等也会产生相应的改变,所以温度会影响到污染物的降解率。根据图8的结果可见,Co-MOF活化PS降解盐酸土霉素的动力学曲线符合准二级动力学模型,其中30 ℃的曲线拟合度R2最高为0.991 0,故确定30 ℃为本次研究的最佳反应温度。 -
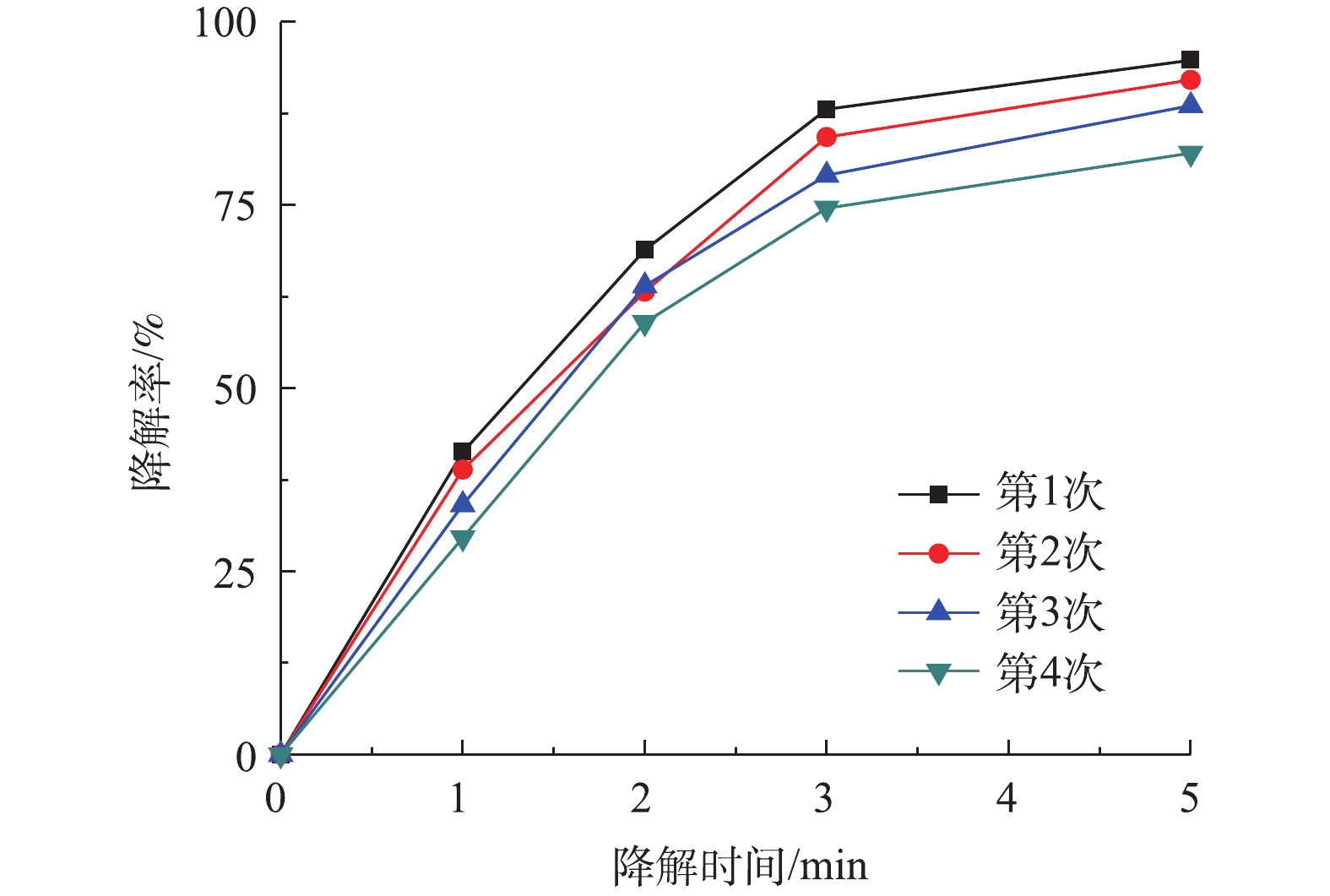
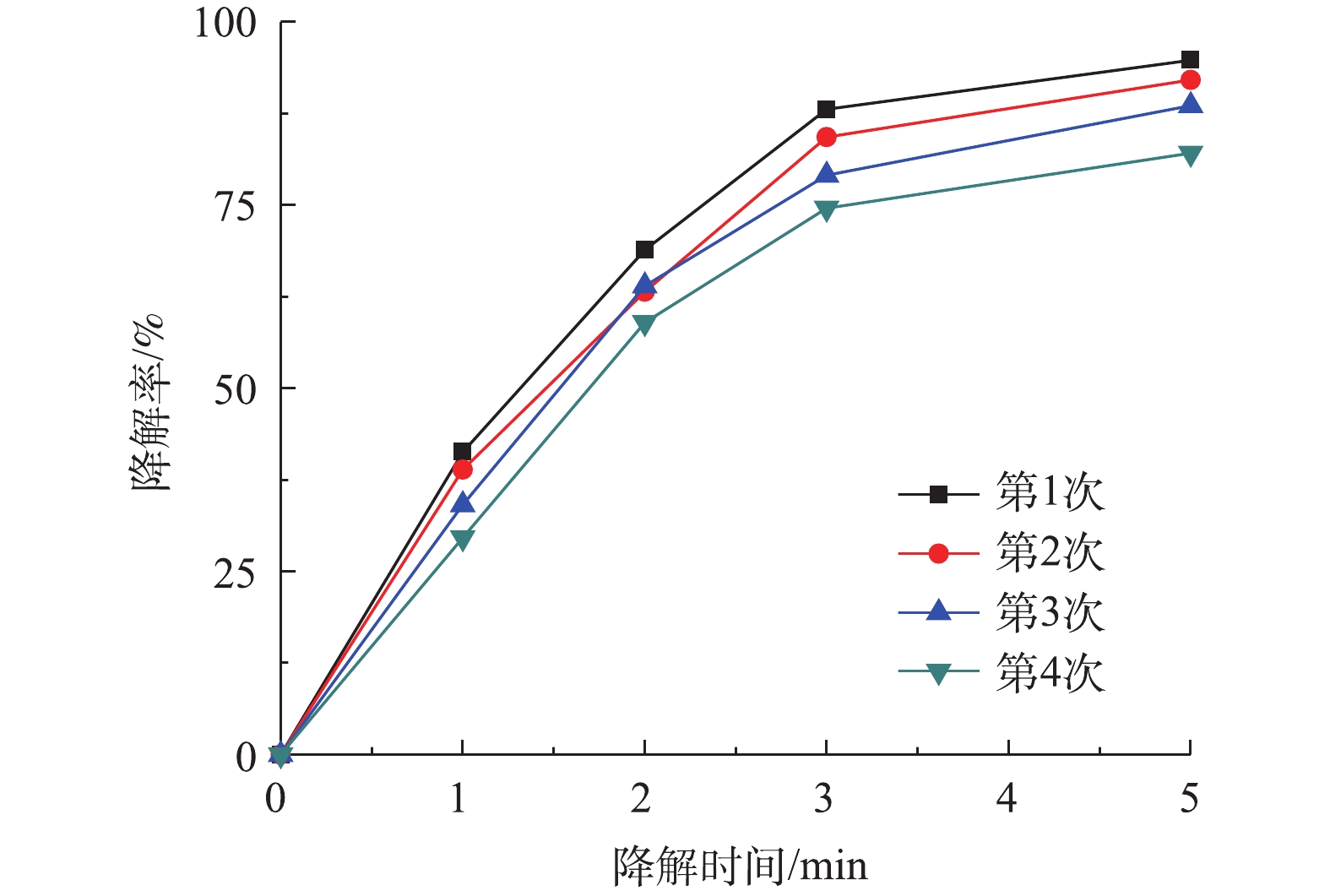
催化剂的稳定性是检验催化剂性能的重要指标,图9为Co-MOF重复利用对降解盐酸土霉素的影响。如图9所示,Co-MOF第4次运行后,对盐酸土霉素的降解率下降为82.1%,这表明Co-MOF具备较高的稳定性。其中,导致盐酸土霉素降解率降低的原因是:一方面由于Co-MOF活化PS降解盐酸土霉素时,长时间浸泡导致Co(Ⅱ)的活性位点损失;另一方面是由于Co2+随着多次循环出现微量损失(式(6))。第4次运行结束后收集定量的上清液,经检测显示钴含量为1×10−4 mg·L−1,而国标(GB 25467-2010)中的钴排放标准为总钴含量≤1 mg·L−1,故本次研究中Co-MOF的使用不会对环境造成二次污染。
-
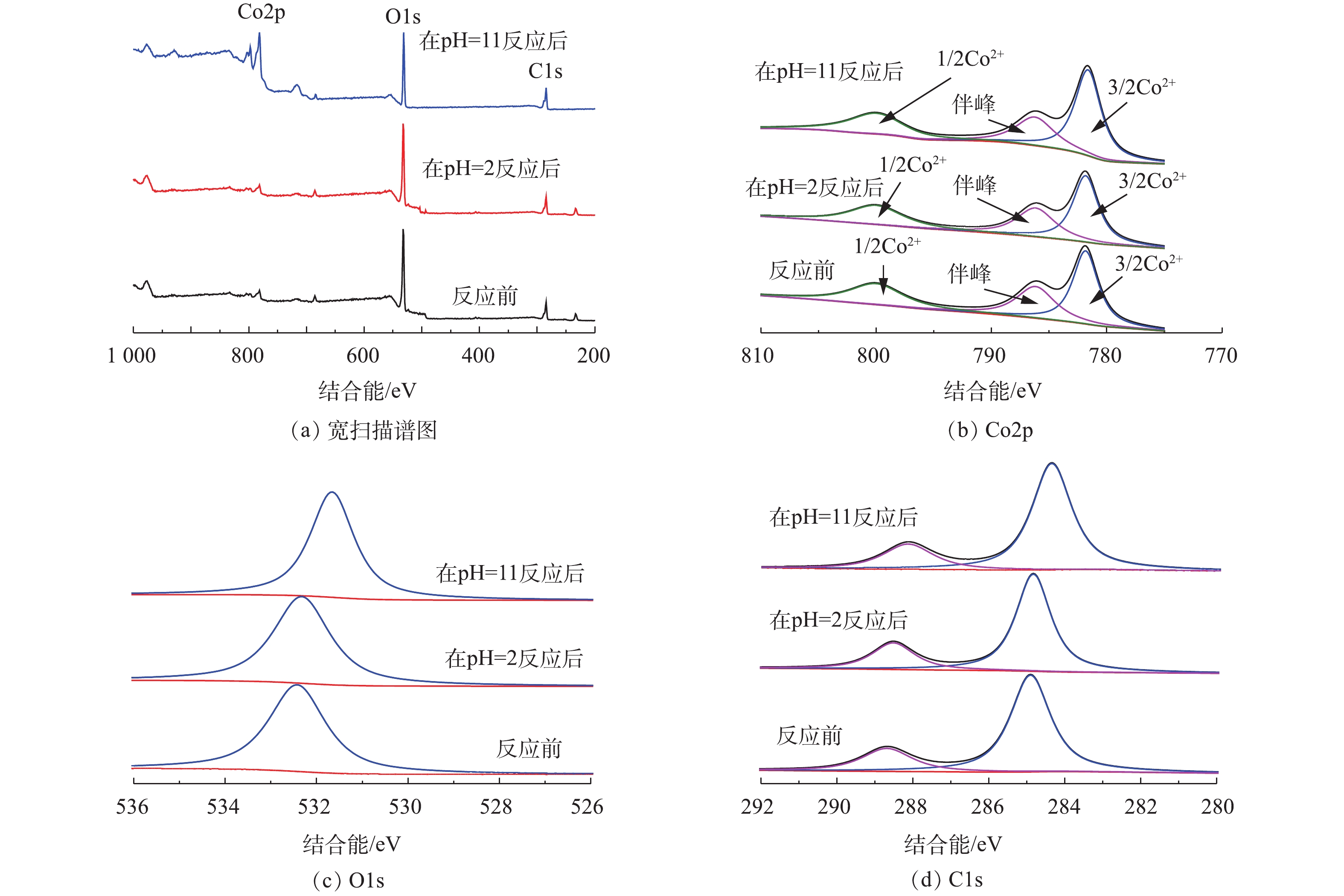
1) Co-MOF降解盐酸土霉素反应前后的XPS表征。通过XPS对Co-MOF降解盐酸土霉素反应前后的组分变化进行分析。图10为Co-MOF反应前后的XPS图谱。如图10(a)所示,Co-MOF材料的宽扫描光电子能谱呈现Co2p、O1s和C1s 3个光谱图。在Co2p核心级XPS光谱中(图10(b)),反应前的Co2p1/2和Co2p3/2的结合能对应781.4 eV和800.4 eV;在786.2 eV的峰值是由辅峰造成的,由Co的sp3杂化所形成。有研究[30]表明,在低结合能一侧的781.4 eV若是归属于Co(Ⅱ),就表明Co在材料中的主要存在状态是Co(Ⅱ)氧化态,其在pH=2时没明显变化,而在pH=11时Co2p1/2对应的强度明显增强,这表明Co-MOF在酸性条件下更稳定。由图10(a)可知,在pH=11时反应后的Co2p的峰值有所升高,这是由于碱性条件下Co3+被还原为Co2+所致(式(7))。图10(c)显示的是O1s的光谱,反应前和当体系的pH=2反应后的结合能峰均为532.4 eV,表明CO-MOF中的羧基没有受到损坏,结合C1s的XPS光谱中(图10(d))的数据,其结合能没有发生明显的变化。综上所述,Co-MOF具有良好的稳定性。
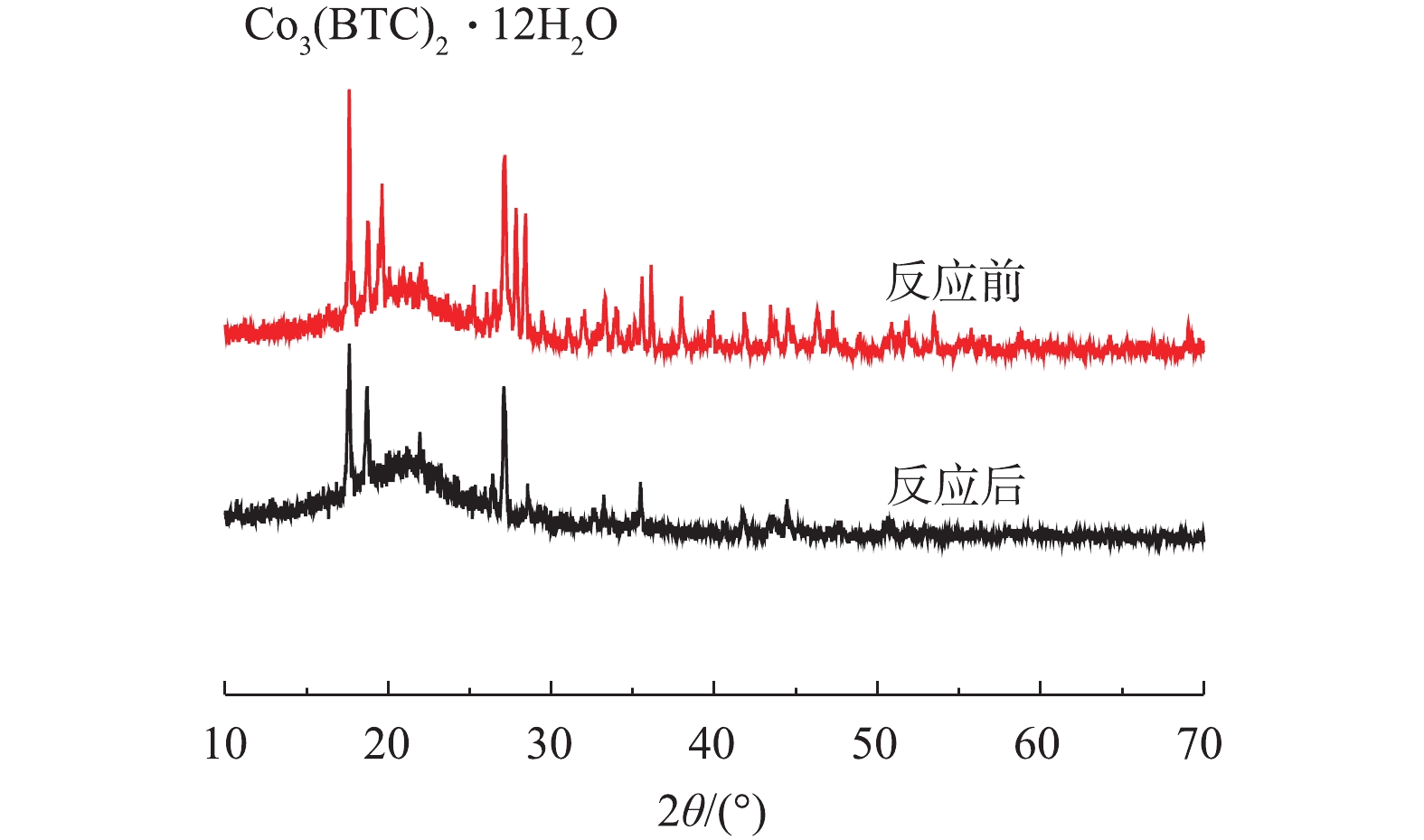
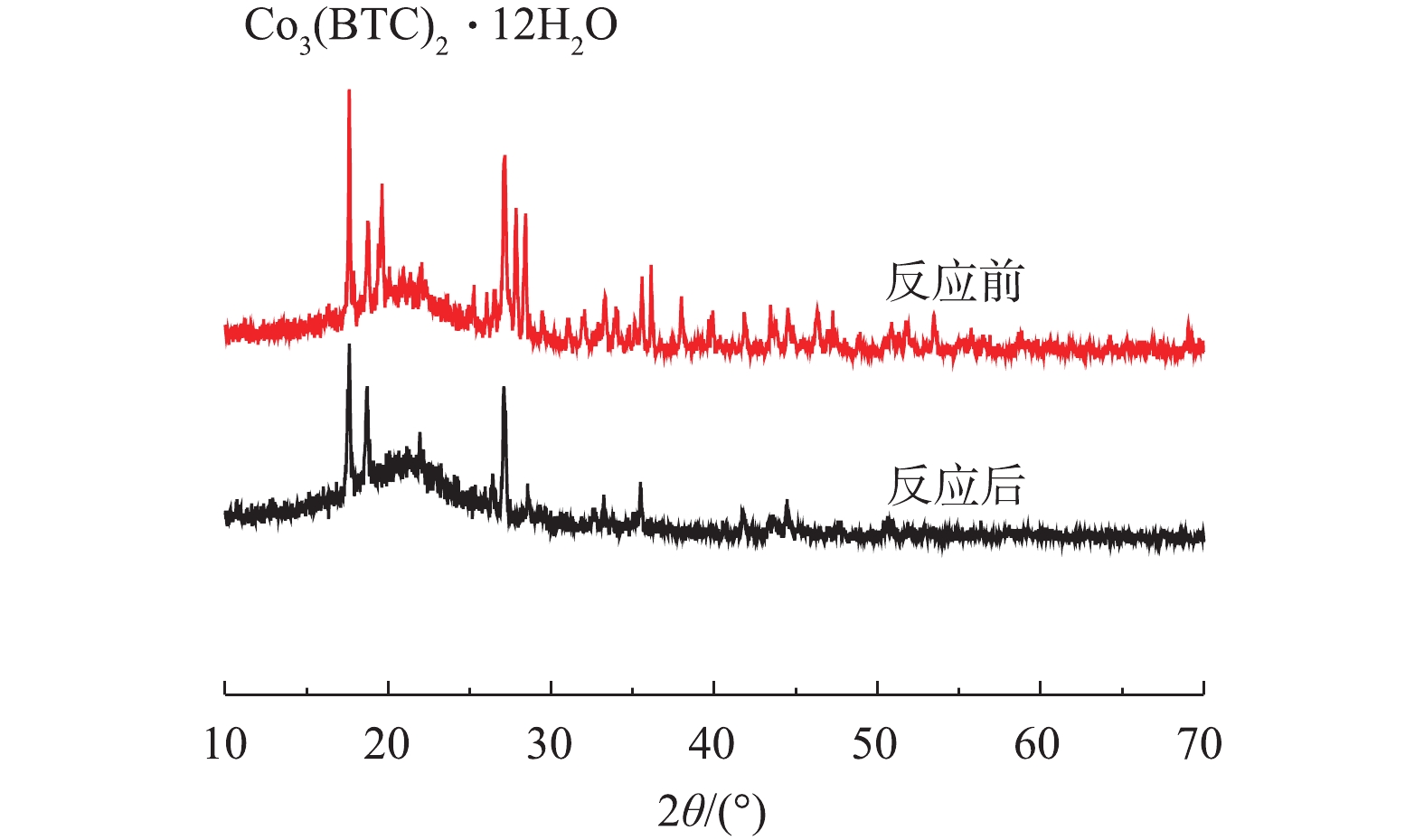
2) Co-MOF降解盐酸土霉素反应前后的XRD表征。如图11所示,在Co-MOF降解盐酸土霉素反应完成后,XRD图谱中Co3(BTC)2·12H2O对应的峰强度降低,这表明Co-MOF材料在降解盐酸土霉素的过程中有损失。
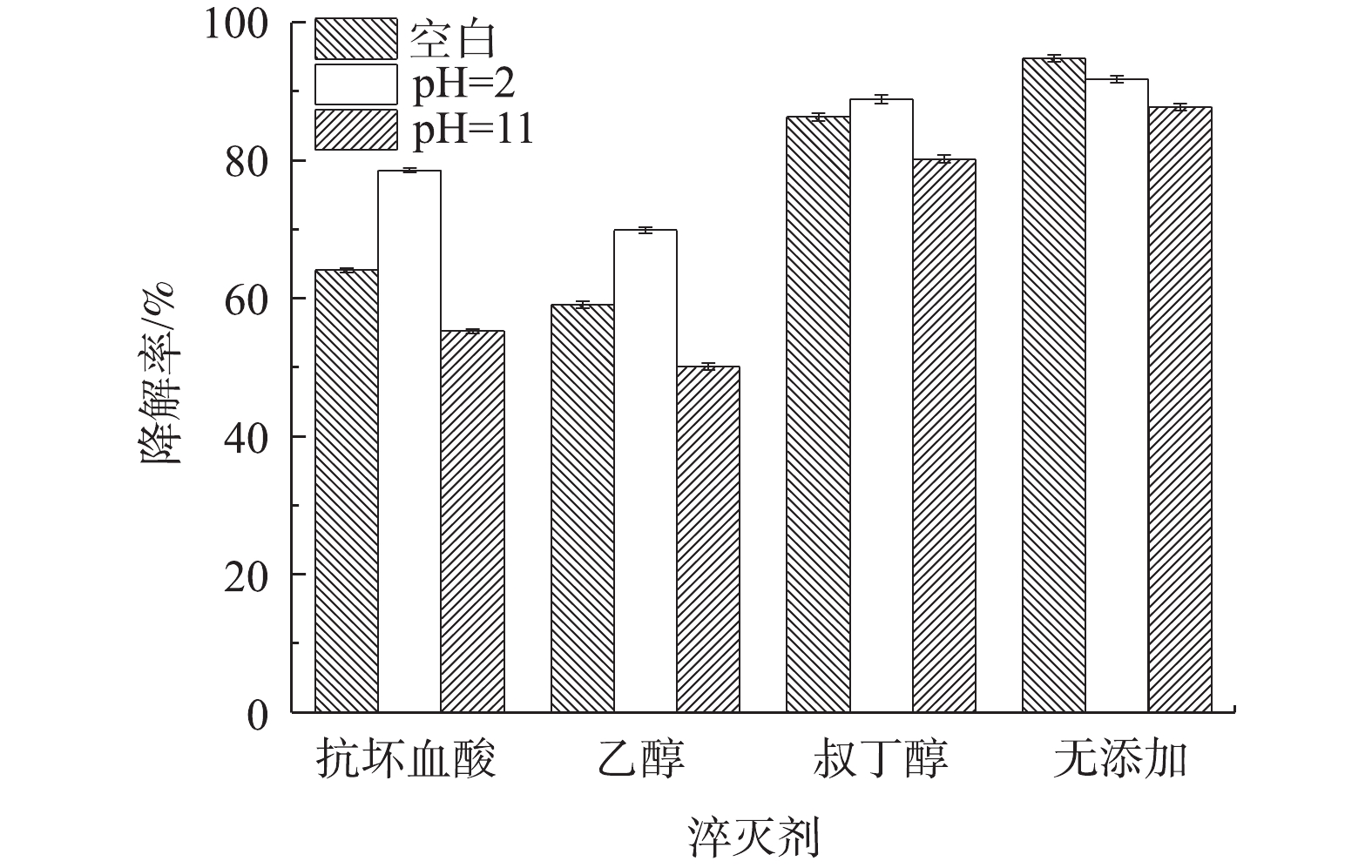
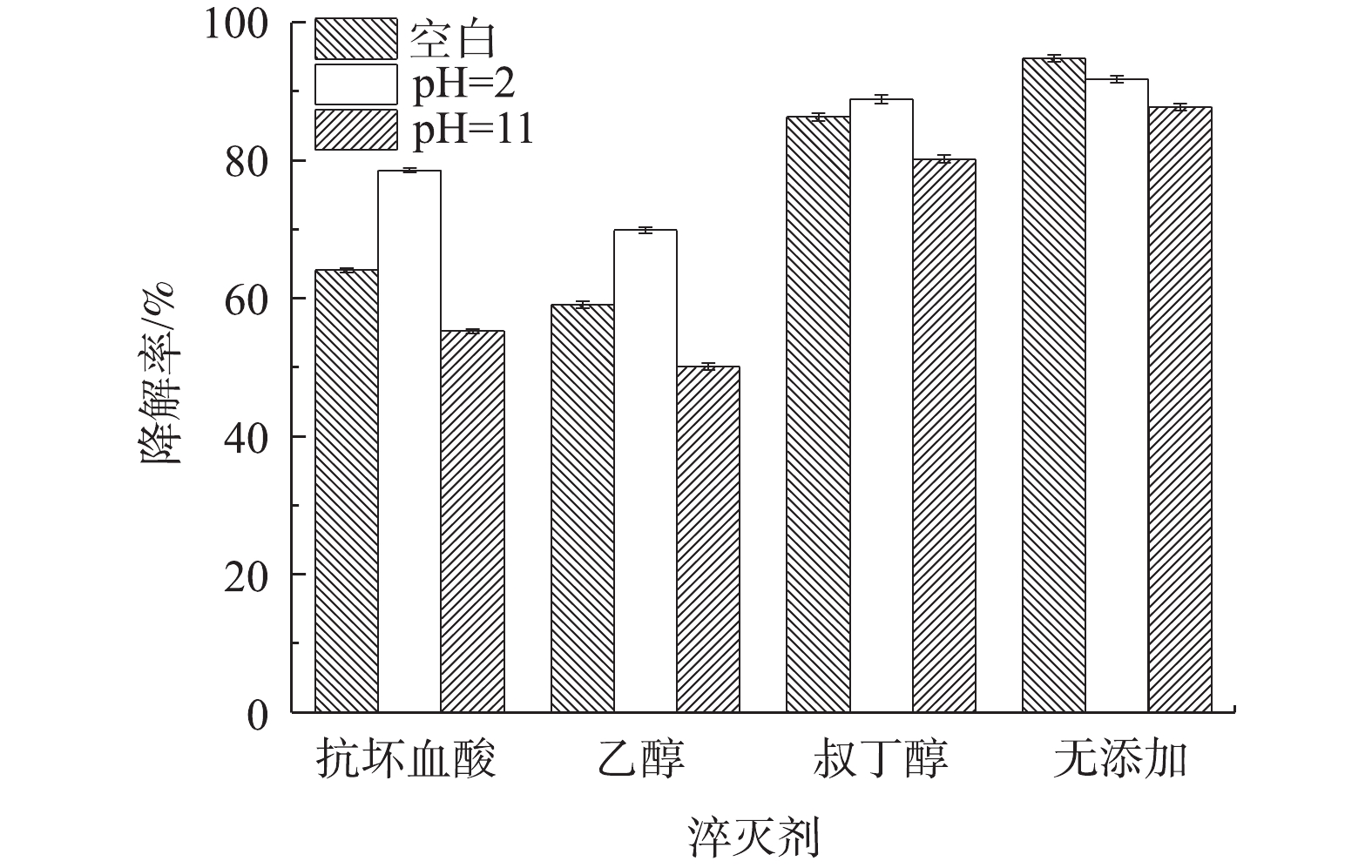
3)自由基淬灭剂对Co-MOF降解盐酸土霉素的影响。为了确定Co-MOF活化PS所产生的自由基种类,采用自由基捕获实验以验证活化体系中可能存在的自由基。众所周知,抗坏血酸和乙醇均为·OH和
SO⋅−4 的淬灭剂,而叔丁醇仅为·OH的淬灭剂。如图12所示,加入叔丁醇的实验组中,盐酸土霉素的降解率与无添加组相比有微弱下降,而加入抗坏血酸和乙醇的实验组中,盐酸土霉素的降解率无添加组相比大幅度下降,这表明在对盐酸土霉素降解的实验过程中同时涉及到SO⋅−4 和·OH,且SO⋅−4 是起主导作用的。在pH=2的条件下,加入抗坏血酸、乙醇和叔丁醇后,相比较空白条件,盐酸土霉素的降解率反而得到提升,加入叔丁醇的实验组对盐酸土霉素的降解率的提升效果微弱,这表明·OH在酸性条件下更易于生成,如陈震等[31]研究溶液pH对·OH的影响时发现,酸性环境更易于·OH的生成。当pH=11时,在加入淬灭剂后,发现对于盐酸土霉素降解效果的抑制明显高于空白条件下,原因是由于碱性环境有利于·OH的去除。
2.1. Co-MOF表征
2.2. 不同体系对盐酸土霉素的降解效果
2.3. 影响Co-MOF降解盐酸土霉素的因素
2.4. 重复利用Co-MOF对盐酸土霉素降解率的影响
2.5. 反应机理
-
1) SEM、TEM和XRD的表征结果表明,采用水热法成功制备出Co-MOF。该催化剂具有较好的降解性能,在Co-MOF浓度为200 mg·L−1、PS浓度为2 000 mg·L−1时,5 min后Co-MOF/PS对盐酸土霉素的降解率达到95.4%。
2) Co-MOF投加量、PS投加量和温度对Co-MOF降解盐酸土霉素有较大的影响,pH对降解盐酸土霉素的影响不大。其中,当pH=5、温度30 ℃、Co-MOF浓度为200 mg·L−1、PS浓度为2 000 mg·L−1时,Co-MOF/PS对盐酸土霉素的降解率可达到最高。
3)重复利用Co-MOF降解盐酸土霉素结果表明,Co-MOF具有可重复利用性能。Co-MOF反应前后的XRD和XPS数据表明,Co-MOF具有良好的稳定性。自由基捕获结果表明,在该降解反应过程中,
SO⋅−4 和·OH对盐酸土霉素的降解均有贡献,其中,SO⋅−4 的贡献最大。




 下载:
下载: