-
随着国民生活水平的日益提高,与人民生活密切相关的《生活饮用水卫生标准》也更加严苛。目前,生活饮用水面临的主要问题是输水管网带来的饮用水中生物安全隐患[1]。可同化生物有机碳(AOC)被普遍认为是饮用水生物稳定性的一个重要参数[2]。已有研究[3]发现,磷是控制管网中饮用水微生物生长的重要因素,当饮用水中磷酸盐浓度低于0.01 mg·L−1时,显示出明显的细菌生长抑制作用[4]。因此,控制饮用水中磷含量是有效的控制细菌生长的重要手段之一。
与其他的除磷技术相比,吸附法具有占地面积小、稳定性强等特点,故引起越来越广泛的关注[5]。在已有的研究中,以天然高分子材料[6]、碳基材料[7]、无机金属氧化物材料[8]、纤维材料[9]等作为改性材料来吸附水中的磷均具有良好的效果。与其他材料相比,镧基改性材料[10]对磷酸盐的吸附容量高,吸附选择性强,且具有较好的生物安全性,在水体除磷领域备受关注[11]。
本研究以熔融纺丝法制备纳米氧化镧负载的聚丙烯纤维复合材料,再经聚乙烯亚胺改性制备成PEI/La2O3/PP纤维吸附材料,研究了其对饮用水中微量磷的去除效果及对饮用水中细菌生长的抑制作用;考察了pH、共存离子等因素对磷吸附效果的影响;采用吸附等温模型、吸附动力模型对吸附机理进行了探讨;通过微生物实验,探究了饮用水中细菌生长与磷含量的关系。本研究可为控制饮用水中微生物的二次生长潜能提供参考。
-
试剂:氢氧化钠(AR,天津市风船化学试剂有限公司)、盐酸(AR,天津市风船化学试剂有限公司)、磷酸二氢钾(AR,上海麦克林生化科技有限公司)、抗坏血酸(AR,天津市天新精细化工开发中心)、钼酸铵(AR,天津市光复科技发展有限公司)、过硫酸钾(AR,天津市风船化学试剂有限公司)、H2SO4(AR,天津市风船化学试剂有限公司)、纳米氧化镧(50 nm,罗恩试剂)、聚丙烯(工业级,中国石化上海石油化工股份有限公司)、聚乙烯亚胺(M.W.600,上海麦瑞尔化学技术有限公司)、戊二醛(上海麦瑞尔化学技术有限公司)、异丙醇(AR,天津市津东天正精细化学试剂厂)、牛肉膏蛋白胨培养基(BR,北京奥博星生物技术有限公司)。
仪器:小型单丝纺丝试验机(无锡市兰华纺织机械有限公司)、真空干燥箱(恒幸仪器设备厂)、精密电子天平(奥豪斯国际上海贸易有限公司)、PH-3210PH计(德国WTW公司)、磁力加热搅拌器(C-MAG HS7)、蠕动泵BT100-2J(Longer Pump)、立式压力蒸汽灭菌器(上海博讯实业有限公司医疗设备厂)、紫外可见分光光度计TU-1810(北京朴析通用仪器有限责任公司)、超净工作台(苏州金大净化工程有限公司)、光照培养箱SPX-300B-G型(上海博讯实业有限公司)。
-
氧化镧/聚丙烯(La2O3/PP)复合纤维材料的制备:将25、50、100、300 g纳米La2O3颗粒分别与10 kg聚丙烯颗粒手动混合约2 min,然后将混合物加入到熔融纺丝机的进样料斗中,将进样料斗调到振荡模式,保证混合均匀,随后进入高温熔融室(熔融温度约为210 ℃),经过高温熔融纺丝制得负载La2O3的聚丙烯纤维材料,La2O3的负载质量分数分别为0.25%、0.5%、1%、3%。
La2O3/PP复合纤维材料的亲水性改性:使用去离子水∶异丙醇=1∶1配制质量分数为0.25%、0.5%、1%、3%聚乙烯亚胺(PEI)溶液。将筛选出的最佳La2O3负载量的La2O3/PP复合材料分别溶于不同浓度的聚乙烯亚胺溶液中,浸渍24 h。然后将其浸渍于质量分数为0.1%的戊二醛溶液中,交联反应12 h,用大量蒸馏水洗涤,烘干。最终制得吸附材料,简称为PEI/La2O3/PP。采用X射线衍射分析仪(XRD)进行晶型结构分析。
-
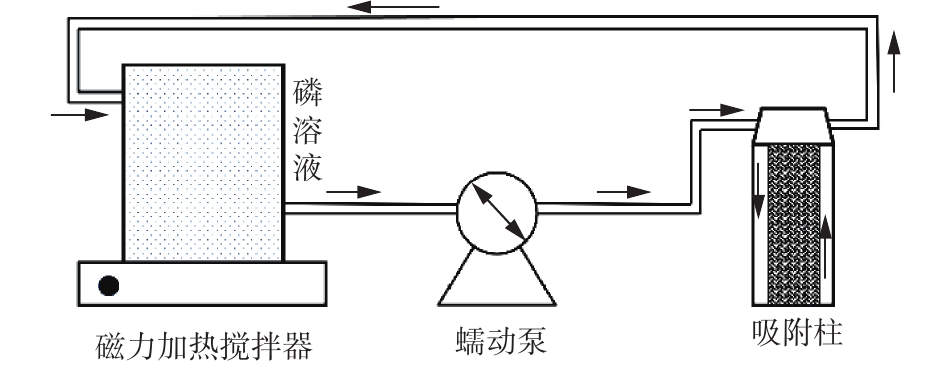
实验均取3 L不同浓度磷溶液,置于实验装置中,加入复合纤维材料,反应一定时间,测定溶液的磷含量。循环吸附实验装置如图1所示。
配置0.1 mg·L−1的磷溶液,加入氧化镧负载量分别为0.25%、0.5%、1%、3%的吸附材料,在实验装置中进行吸附反应,测定反应后磷溶液的浓度。使用磷钼蓝分光光度法(GB 11893-1989),此方法磷的检出限为0.01 mg·L−1。使用电感耦合等离子体原子发射光谱(ICP-OES)测定镧元素的溶出率,此方法的镧检出限为1 μg·L−1。
配置0.1 mg·L−1的磷溶液,加入PEI浓度分别为0.25%、0.5%、1%、3%的吸附剂,其余步骤同上述实验。
配置0.1 mg·L−1的磷溶液,用NaOH/HCl调节pH为3、4、5、6、7、8、9、10、11,其余步骤同上述实验。
配置
CO2−3 、SO2−4 、Cl−、NO−3 离子浓度均为1 mmol·L−1,磷浓度为0.1 mg·L−1的溶液,其余步骤同上述实验。配置初始浓度为1~80 mg·L−1的磷溶液,置于实验装置中,控制温度在25、35、45 ℃,反应6 h后取样,测定溶液中磷含量。
Langmuir等温吸附理论的观点是:吸附剂表面吸附位点分布均匀,吸附质在固体表面上存在着吸附和解析2种过程,这2种过程通过相互作用最后达到吸附平衡[12]。其吸附等温线模型如式(1)所示。
式中:qe为平衡吸附量,mg·g−1;qm为饱和吸附量,mg·g−1;Ce为平衡吸附浓度,mg·L−1;KL为平衡吸附常数。
Freundlich吸附机理对表面不均匀、比表面积大的固体具有很好的适应性[12],其表达式如式(2)所示。
式中:qe为平衡吸附量,mg·g−1;Ce为平衡吸附浓度,mg·L−1;KF为吸附相关系数;n为吸附相关系数。
根据Freundlich吸附理论,KF表征吸附剂的吸附能力,n值反映了吸附剂的不均匀吸附反应,当n<0.5时,吸附不易进行。
配置初始浓度为0.1 mg·L−1的磷溶液,置于吸附实验装置中,控制温度在25、35、45 ℃,在一定时间间隔中取样,测定溶液中磷含量。
准一级动力学方程认为,吸附速率与吸附剂上未被占据的吸附位点成正比,方程如式(3)所示。
式中:k1为准一级吸附速率常数,min−1;qe为平衡吸附量,mg·g−1;qt为t时刻吸附量,mg·g−1;t为吸附时间,h。
准二级动力学方程认为,吸附速率与吸附剂上未被占据的吸附位点的平方成正比,方程如式(4)所示。
式中:k2为准二级吸附速率常数,min−1;qe为平衡吸附量,mg·g−1;qt为t时刻吸附量,mg·g−1;t为吸附时间,h。
-
测定细菌浓度具体方法按照《生活饮用水标准检测方法》(GB/T 5750-2006)进行检测。取一定量超纯水,经过高温灭菌制成无菌水,用无菌水配置细菌浓度为1 000 CFU·mL−1的大肠杆菌溶液,取3 L大肠杆菌溶液于实验装置中,分别加入PEI/La2O3/PP纤维材料和PEI /PP纤维材料,在一定时间内取样,测定自来水中细菌浓度。饮用水在无菌的条件下放置3 d,以达到去除余氯的目的。取3 L自来水于实验装置中,加入复合纤维材料,在一定时间间隔内取样,测定自来水中细菌浓度。
-
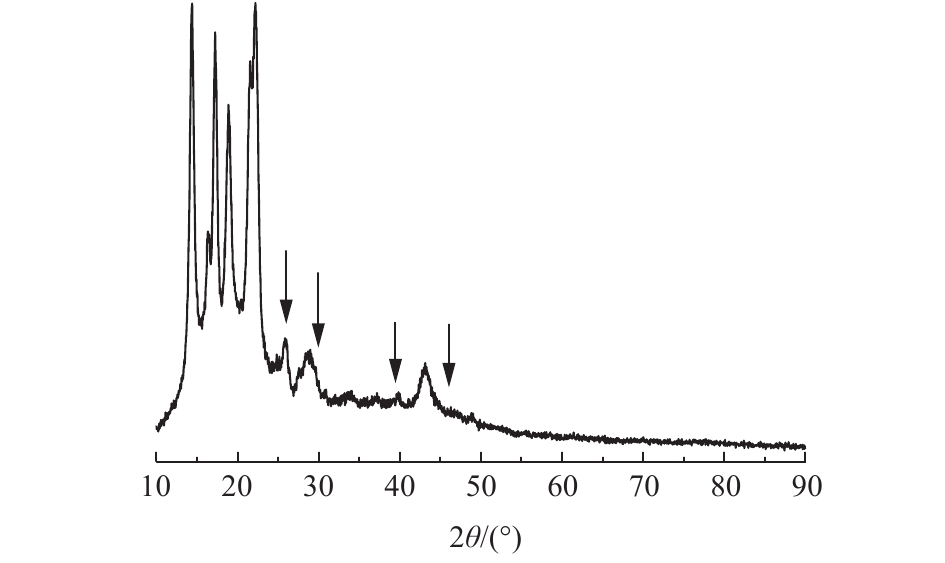
由图2可以看出,氧化镧负载聚丙烯纤维后衍射谱图中出现了较多新的峰,与PDF标准卡片进行比对,发现新出现的峰与氧化镧标准物的衍射峰相对应,说明氧化镧成功负载在聚丙烯纤维上。图2中衍射角26.106°、29.950°、39.474°、46.058°分别对应氧化镧的(100)、(012)、(012)、(110)晶面。
-
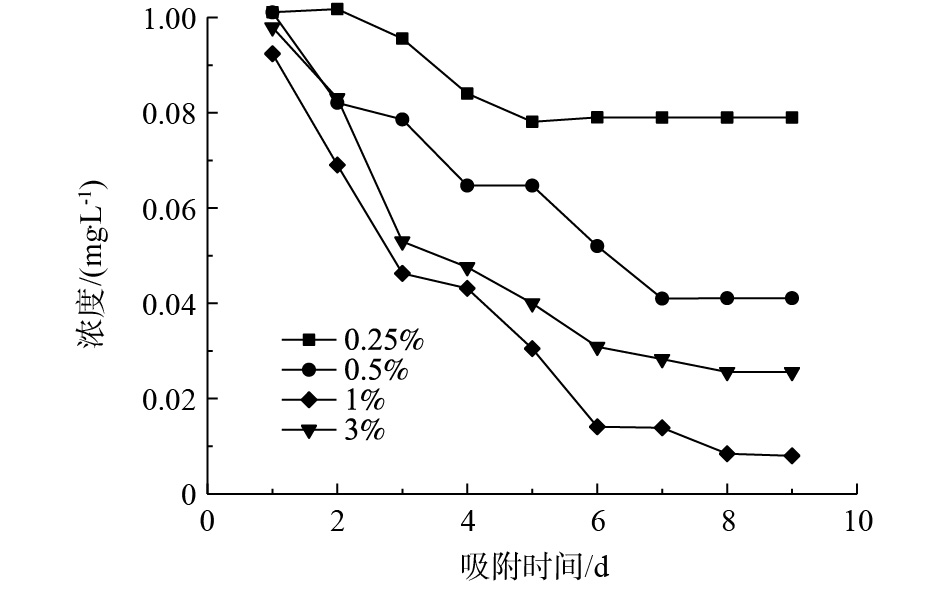
吸附剂对低浓度含磷溶液的吸附效果如图3所示。吸附8 d后,氧化镧负载量为1%的吸附剂将磷浓度吸附至0.01 mg·L−1以下。当氧化镧负载量为3%时,磷的吸附效果反而下降,这是因为较高负载量条件下,纳米氧化镧颗粒容易发生团聚现象,在聚丙烯纤维中的分散性较差,使有效的吸附位点减少,造成了吸附效果降低。而过低的氧化镧负载量会导致有效吸附位点的不足,因此,在制备La2O3/PP复合吸附材料过程中,氧化镧的最佳负载量为1%。
将最佳负载量的La2O3/PP复合材料氧化镧的溶出率进行检测,实验结果表明,吸附时间为9 d后,溶液中的镧浓度均小于10 μg·L−1,证明该复合材料具有很好的稳定性。
-
由于聚丙烯纤维表面的非极性特征,其本身亲水性能很差,并且容易带静电[13],降低了La2O3/PP材料与磷溶液的反应速率。本实验通过聚乙烯亚胺与戊二醛交联反应,在聚丙烯纤维表面交联氨基[14],使其具有良好的亲水性。改性前后La2O3/PP接触角的变化如图4所示。改性前La2O3/PP的接触角为98°,而经过PEI处理后的PEI/La2O3/PP的接触角发生明显变化,减小到50°,表现出较好的亲水性。这是由于PEI改性使纤维表面增加了一定数量的氨基亲水性基团,从而明显提高了聚丙烯材料的亲水性。材料表面亲水性的增强能够明显增加磷酸盐的吸附速率。
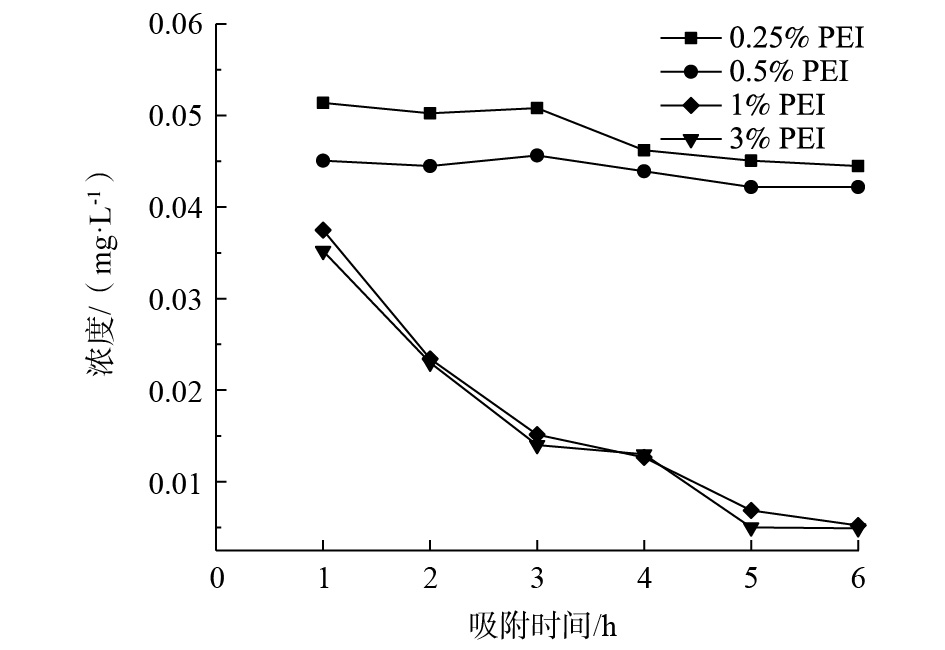
此外,氨基的质子化作用还可以与磷酸根发生静电引力作用,从而促进磷酸盐的吸附。不同PEI浓度对磷吸附效果的影响如图5所示。La2O3/PP复合材料经亲水改性后,对磷的吸附反应速率大大提高。当PEI浓度为1%和3%时,吸附速率的变化明显,吸附反应6 h后,磷浓度降至0.01 mg·L−1以下;当PEI浓度为3%时,吸附速率没有明显提高,这是由于较高浓度的PEI会导致溶液黏度增大,不利于PEI分子的扩散。因此,本实验选取PEI的最佳浓度为1%。
-
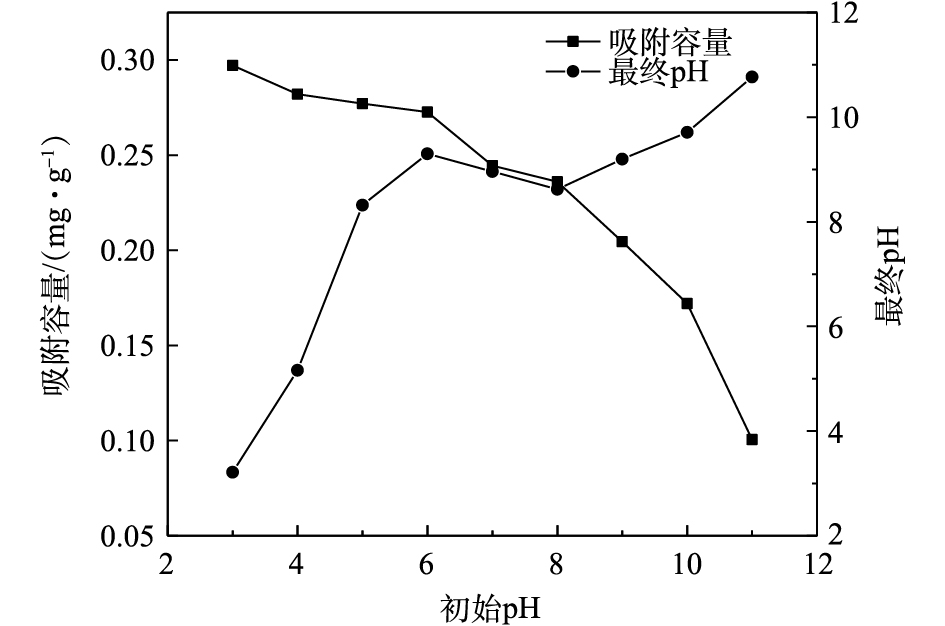
不同初始pH对磷吸附效果的影响如图6所示。随着溶液初始pH的升高,吸附容量呈现出下降趋势,吸附材料的吸附能力降低。当pH=3时,磷的最大吸附容量为0.30 mg·g−1;当pH在3~8时,磷的吸附容量保持在0.24 mg·g−1以上,这说明吸附剂具有较宽的pH适用范围。当溶液初始pH不断增大时,吸附容量快速下降,说明碱性条件不利于吸附剂对磷的吸附。吸附后溶液的pH都有所升高,这是氧化镧对磷的吸附是一个化学反应过程,且反应过程中有OH−的释放。
通过测量PEI/La2O3/PP表面的Zeta电位,测出PEI/La2O3/PP的等电点为8.2。这说明当溶液pH小于8.2时,吸附材料表面呈现正电性,可以与溶液中的带负电荷的磷酸根离子产生静电吸引作用。同时,大量质子化的磷酸根与材料表面氧化镧羟基化产生的氢氧根离子发生离子交换作用,这也进一步证实了吸附磷后溶液pH升高的现象。
-
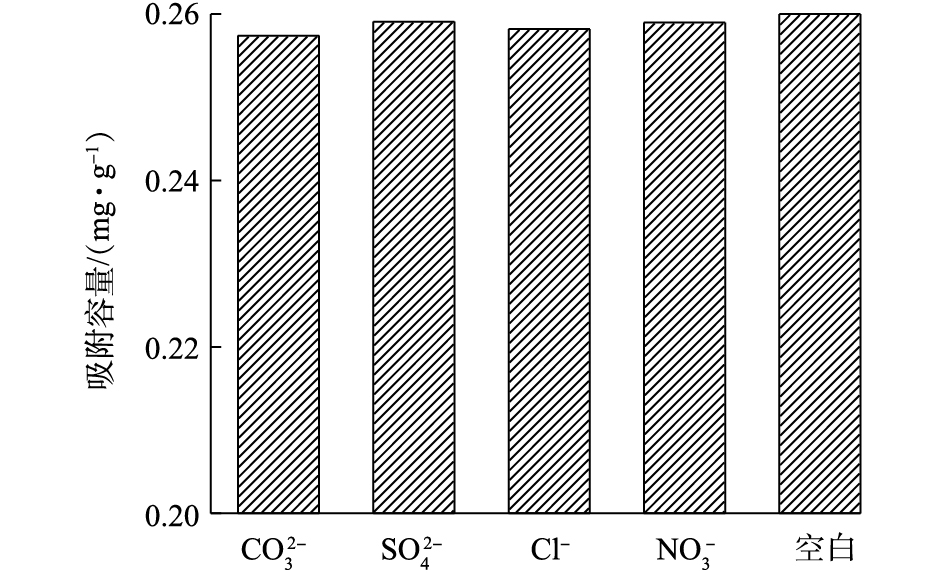
水体中与磷酸根共存的常见阴离子有
CO2−3 、SO2−4 、Cl−、NO−3 [15],这4种阴离子对PEI/La2O3/PP复合材料除磷的影响如图7所示。实验结果表明,这4种阴离子对PEI/La2O3/PP复合材料的磷吸附能力没有明显的影响,说明PEI/La2O3/PP对磷酸盐具有很强的吸附选择性。 -
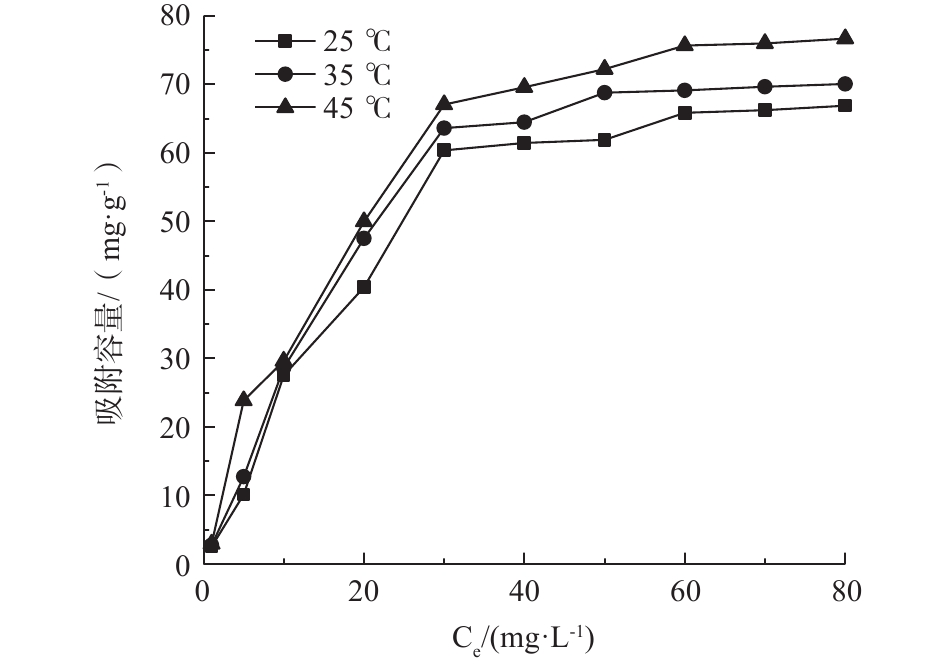
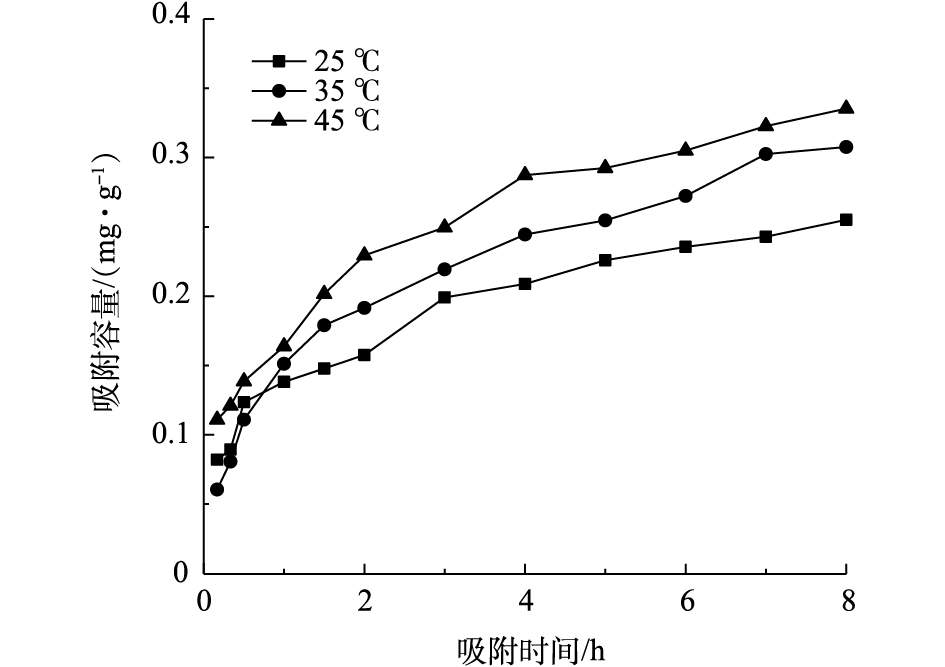
吸附等温线可以确定吸附平衡浓度与吸附容量的关系,通过模型拟合可以估算吸附剂的最大吸附容量。如图8所示,吸附剂的吸附容量随着磷初始浓度的升高而不断升高,当达到一定浓度时吸附容量趋于平稳。在不同温度条件下,磷吸附容量随着温度的升高而升高。当温度为45 ℃时,最大吸附容量达到76.67 mg·g−1。
采用Langmuir模型和Freundlich模型对吸附等温线进行拟合,拟合结果如表1所示。Langmuir模型和Freundlich模型均能较好地拟合PEI/La2O3/PP对磷酸盐的吸附,但Langmuir模型的拟合程度更好。KL是表示吸附剂对磷的吸附亲和力强弱的重要参数,随着温度从25 ℃逐渐提高到45 ℃,平衡吸附常数KL从0.032提高到0.045,表明PEI/La2O3/PP吸附磷的过程为吸热反应,在一定范围内,提高温度有利于反应的进行。Freundlich模型中的n值也能反映吸附剂对吸附质吸附能力的强弱,如表1所示,不同温度下的n值均大于0.5,表示吸附反应较容易进行。
-
吸附动力学曲线主要用于描述吸附速率变化的特征,通过拟合动力学反应模型可以进一步分析吸附原理。不同温度条件下PEI/La2O3/PP吸附磷酸盐的动力学曲线如图9所示。当温度从25 ℃上升到45 ℃时,吸附反应速率明显加快,这进一步说明升温有利于吸附反应的进行。准一级和准二级动力学模型拟合结果如表2所示,可见,准二级动力学模型能更好地拟合PEI/La2O3/PP吸附磷的反应过程,模型的R2为0.93~0.98。
-
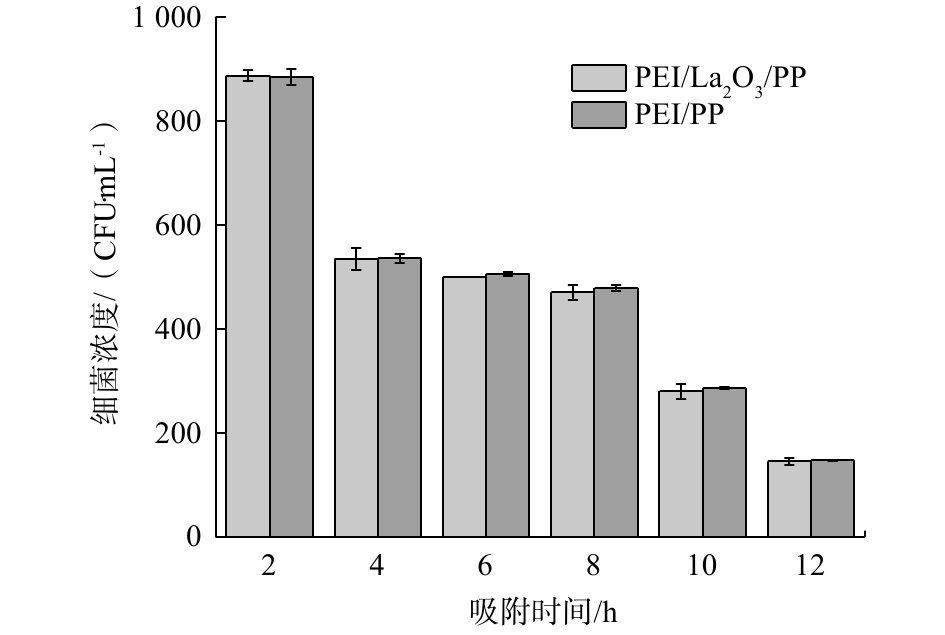
为了研究PEI/La2O3/PP纤维自身的杀菌能力,本实验对比了负载氧化镧颗粒的PP纤维与未负载氧化镧颗粒的PP纤维对大肠杆菌生长的作用。由图10可以看出,2种材料在不同的反应时间条件下大肠杆菌的数量基本相同,说明PEI/La2O3/PP纤维所负载的氧化镧颗粒自身对大肠杆菌生长没有明显的抑制作用,这可能是由于氧化镧颗粒的负载量较小的缘故。但是,在磷源极度缺乏的状态下,大肠杆菌浓度会迅速下降,证明控制磷营养源才是抑制细菌生长繁殖的关键因素。
-
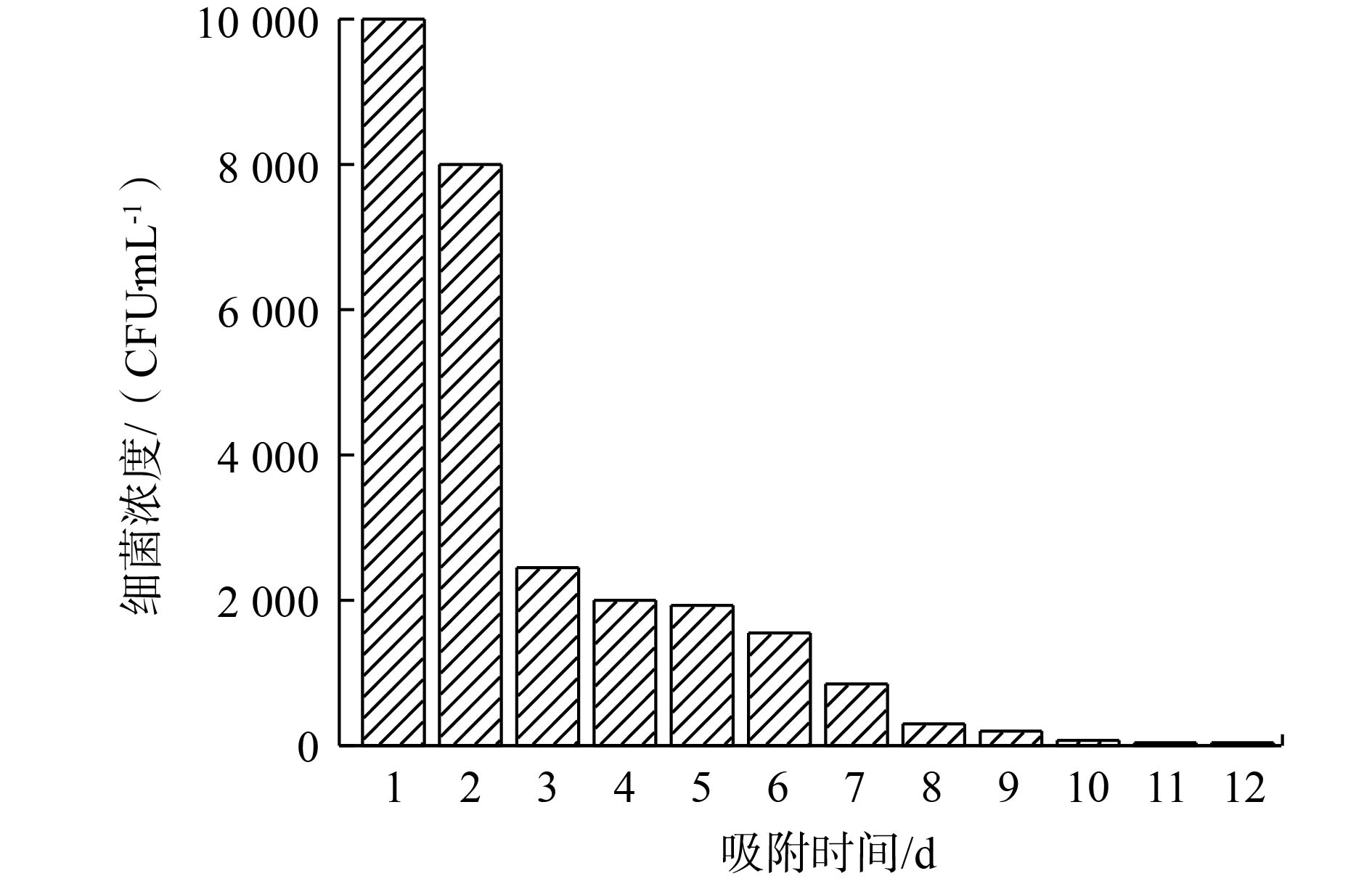
为了进一步研究本实验中制备的吸附材料对实际饮用水是否具有除磷控菌的效果,本研究以饮用水为研究对象,考察了磷浓度与细菌生长之间的关系,实验结果如图11所示。取饮用水并自然晾晒3 d,以去除余氯,之后使用平板计数法检测水中细菌浓度为10 000 CFU·mL−1,饮用水磷浓度的本底值为0.02 mg·L−1。通过PEI/La2O3/PP吸附2 h后,磷浓度降至0.01 mg·L−1以下。在磷源极度缺乏的条件下,细菌含量明显下降,除磷后的1~3 d细菌含量迅速下降,自来水中磷酸盐被去除,细菌由于失去了存活必备的磷源而迅速减少,随后是细菌缓慢凋亡的过程。到第10天,细菌含量降至100 CFU·mL−1以下;到第11天,细菌含量进一步降至10 CFU·mL−1左右。除磷控菌的微生物学实验表明,饮用水中细菌生长与磷浓度存在明显的正相关性,当水中磷浓度降低到0.01 mg·L−1以下时,细菌生长受到强烈抑制。因此,除磷控菌方法为控制饮用水中微生物的二次生长潜能提供了一种具有前瞻性的水质稳定技术。
-
1) PEI/La2O3/PP复合纤维材料的最佳制备条件:氧化镧的最佳负载量为1%,PEI的最佳浓度为1%。中性和偏酸性条件有利于磷的吸附,水中常见共存阴离子对磷的吸附效果影响不大。
2) PEI/La2O3/PP复合纤维材料对水中磷酸盐具有很好的吸附效果,最大吸附容量可达76.67 mg·g−1。在温度为25~45 ℃时,随着温度的升高,磷吸附容量和吸附速率均有明显提高。吸附模型拟合结果表明,PEI/La2O3/PP对磷的吸附过程主要以单分子层化学吸附为主。
3) PEI/La2O3/PP复合纤维材料对饮用水中的磷具有很好的吸附效果,可以将饮用水中磷浓度降至0.01 mg·L−1以下。饮用水中磷源的缺乏可以起到明显的控菌效果,吸附反应11 d后,细菌浓度从10 000 CFU·mL−1降至10 CFU·mL−1左右。
改性La2O3/聚丙烯纤维对饮用水中磷的吸附及控菌效果
Effect of phosphate adsorption and antibacteria in drinking water by modified La2O3/polypropylene fibers
-
摘要: 为了研究吸附剂在饮用水中除磷控菌效果,在聚丙烯(PP)纤维上负载氧化镧(La2O3)纳米颗粒,并用聚乙烯亚胺(PEI)对吸附剂表面进行亲水改性,制备出PEI/La2O3/PP纤维吸附材料,使用X射线衍射分析(XRD)对其进行了表征。实验结果表明:偏酸性条件有利于磷的吸附,溶液中共存离子对吸附效果的影响不大;当温度为45 ℃时,PEI/La2O3/PP对磷的饱和吸附容量达到76.67 mg·g−1,吸附过程能够较好地拟合Langmuir模型;吸附动力学过程能够较好地拟合准二级反应动力学方程。该吸附材料对饮用水中的微量磷具有良好的吸附去除效果,磷深度去除后能达到明显的抑菌效果。Abstract: In order to study the effect of adsorbent on phosphate removal and antibacteria in drinking water. Lanthanum oxide (La2O3) nanoparticles were loaded on polypropylene (PP) fibers and polyethyleneimine (PEI) was used to perform hydrophilic modification of the adsorbent surface, then PEI/La2O3/PP adsorbent was prepared. The materials were characterized by X-ray diffraction (XRD). The experimental results showed that the weak acidic conditions could facilitate its phosphate adsorption, and the coexistence ions had slight effect on the adsorption effect. When the temperature was 45 ℃, the saturated adsorption capacity of PEI/La2O3/PP towards phosphate reached 76.67 mg·g−1. The adsorption isotherm followed Langmuir model. The kinetic equation followed pseudo-second-order kinetics. The adsorbent had a good adsorption effect on trace phosphate in drinking water. Moreover, an excellent bacteriostatic effect could occur after phosphate removal.
-
Key words:
- La2O3 /
- polypropylene fibers /
- adsorption /
- phosphate /
- antibacteria
-
精神活性药品对人体中枢神经系统具有强烈抑制或兴奋作用,部分具有强烈成瘾性,主要包括抗焦虑药物、镇静安眠药物以及非法毒品等[1-2],包括苯二氮卓药物在内的精神活性药品使用量呈现逐年上升的趋势[3]. 与其他药物类似,许多精神活性药品并不能完全被人体吸收代谢,而是随排泄物进入城市污水处理系统,不能被城市污水处理厂消除完全的部分最终随污水厂出水排入受纳水环境[4-5]. 持续排放的精神活性药品对各级水生生物都具有不同程度的生态毒性效应. 研究表明,氯胺酮(948 μg·L−1)能够导致青鳉幼鱼(Oryzias latipes)行为改变,诱导其氧化应激反应,并扰乱乙酰胆碱酯酶的表达[6]. 低暴露浓度下,吗啡(0.07 ng·g−1)能够降低淡水贻贝(Elliptio complanata)组织中血清素水平和乙酰胆碱酯酶活性[7],而地西泮(100 μg·L−1)能够抑制大型蚤(Daphnia magna)的趋光行为并诱导其繁殖增强[8].
有学者采用固相萃取方法,结合液相色谱-质谱,广泛调查了环境水样中多种精神活性药品的污染水平. 结果显示,甲基苯丙胺、氯胺酮、可卡因、阿普唑仑、劳拉西泮、地西泮和咖啡因等精神活性药品作为新型污染物在污水处理厂进水、出水以及地表水中普遍检出[9-12]. 其中,甲基苯丙胺、地西泮和咖啡因在污水处理厂进水检出浓度可达2000、1180、120000 ng·L−1 [10, 13];氯胺酮在医院废水的检出浓度高达10000 ng·L-1[11]. 目前,有关精神活性药品在沉积物和污泥中的提取方法研究较少,采用超声萃取[14-15]或加速溶剂萃取[16-17]法结合固相萃取净化,提取分析甲基苯丙胺、氯胺酮、可卡因、地西泮等少数几种精神活性药品在沉积物和污泥中的含量. 事实上,沉积物和污泥作为物质的储存库是环境水体的重要组成部分[18]. 甲基苯丙胺、吗啡、可卡因等精神活性药品通过现行的污水处理工艺并不能完全降解,而是被污泥吸附并持续缓慢地向环境中释放,成为环境水体中精神活性药品的重要污染源[19-20]. 此外,由于制贩毒活动往往存在一定的隐蔽性,通过检测河流不同深度沉积物中甲基苯丙胺、吗啡等非法毒品的含量,可以溯源追踪较早排放的非法毒品,为锁定制贩毒窝点,举证制贩毒活动提供线索.
由于已报道的提取方法往往只关注少数几种精神活性药品,并且提取过程繁琐,耗时长,需要借助大型提取设备,具有一定的局限性. 因此,本研究开发了一种同时快速灵敏检测沉积物和污泥中多种精神活性药品的QuEChERS(quick, easy, cheap, effective, rugged, and safe)提取方法. 比较了开发的QuEChERS提取方法和已报道的超声萃取、加速溶剂萃取方法的效果,并通过考察加标回收率、相对标准偏差和方法定量限对方法的准确度、精密度和灵敏度进行了验证. 本研究开发的提取分析方法能够用于环境沉积物和污泥样品的检测,为环境水体中精神活性药品的来源、含量、分配和降解研究提供方法支持.
1. 实验部分(Experimental section)
1.1 仪器、试剂与材料
超高效液相色谱-三重四极杆串联质谱联用仪(UPLC-MS/MS,1290-6470,美国Agilent Technologies公司);万分之一天平(BSA224S,德国Sartorius公司);冻干机(DGJ-25C,中国博登生物科技有限公司);VORTEX涡旋混合仪(XK80-A,江苏新康医疗器械有限公司);离心机(L550,湖南湘仪实验室仪器开发有限公司);超声水浴萃取仪(PS-50T,深圳市洁康机电设备有限公司);加速溶剂萃取仪(E-916,瑞士Buchi公司);固相萃取装置(SBEQ-CG1824,上海安谱科学仪器有限公司);24孔平行氮吹仪(EFAA-DC24-RT,上海安谱科学仪器有限公司).
标准品甲基苯丙胺、氯胺酮、吗啡、可待因、可卡因、咪达唑仑、硝西泮、劳拉西泮、阿普唑仑、氯硝西泮、三唑仑、地西泮、氯氮卓、美沙酮和咖啡因均从中国食品药品检定研究院购买;浓度为100 mg·L−1 的同位素标记标准品甲基苯丙胺-D5、氯胺酮-D4、阿普唑仑-D5、硝西泮-D5、美沙酮-D9均从Cerilliant公司(美国)购买;吗啡-D3和可待因-D3从CNW公司(德国)购买. 所有标准品纯度均高于95%,15种目标精神活性药品的基本物理化学性质如表1所示.
表 1 目标精神活性药品基本物理化学性质Table 1. Basic information and physicochemical properties of target psychoactive drugs化合物Compound CAS 分子式Molecular formula lg Kow lg Koc pKa 甲基苯丙胺 537-46-2 C10H15N 2.07 3.21 9.87 氯胺酮 6740−88-1 C13H16ClNO 2.18 3.22 7.5 吗啡 57-27-2 C17H19NO3 0.89 3.47 9.12 可待因 76-57-3 C18H21NO3 1.19 3.12 9.19 可卡因 50-36-2 C17H21NO4 2.30 3.28 8.85 咪达唑仑 1622−61-3 C18H13ClFN3 4.33 5.59 5.5 硝西泮 146-22-5 C15H11N3O3 2.25 3.79 2.61;11.9 劳拉西泮 846-49-1 C15H10Cl2N2O2 3.98 3.30 13.0 阿普唑仑 28981−97-7 C17H13ClN4 3.87 6.33 5.08;18.3 氯硝西泮 1622−61-3 C15H10ClN3O3 2.53 4.02 1.86;11.89 三唑仑 28911−01-5 C17H12Cl2N4 2.42 6.55 4.32;10.08 地西泮 439-14-5 C16H13ClN2O 2.82 4.05 3.4 氯氮卓 58-25-3 C16H14ClN3O −1.57 5.79 4.8 美沙酮 76-99-3 C21H27NO 3.93 4.86 8.94 咖啡因 58-08-2 C8H10N4O2 −0.07 1.00 −0.92 注:Kow:正辛醇-水分配系数;Koc:有机碳吸附系数;pKa:酸离解常数. Note: Kow: N-octanol-water partition coefficient; Koc: organic carbon adsorption coefficient; pKa: logarithm value of acid dissociation constant. 色谱纯甲醇、乙腈、二氯甲烷、乙酸乙酯、丙酮从Merk公司(德国)购买;实验用超纯水为屈臣氏蒸馏水;色谱纯甲酸、乙酸和乙酸铵从CNW公司购买(德国);QuEChERS盐析试剂(含6 g无水硫酸镁和1.5 g无水乙酸钠)和分散固相萃取试剂(含900 mg无水硫酸镁、150 mg PSA和150 mg封端C18)从Agilent公司购买(美国).
1.2 溶液配制
标准储备溶液:分别准确称取10.0 mg标准品,加入色谱纯甲醇溶解,在100 mL容量瓶中用甲醇定容,获得100 mg·L−1 的标准储备溶液,置于-20 ℃冰箱中避光保存.
标准工作溶液:分别取100 μL浓度为100 mg·L−1的标准储备溶液至10 mL容量瓶,用甲醇定容,混合均匀,获得15种目标精神活性药品浓度均为1 mg·L−1 的混合标准工作溶液. 分别取100 μL浓度为100 mg·L−1的同位素标记标准品至10 mL容量瓶,用甲醇定容,混合均匀,获得浓度均为1 mg·L−1的混合同位素内标标准工作溶液,置于-20 ℃冰箱中避光保存.
标准系列工作溶液:分别移取浓度为1 mg·L−1 的混合标准工作溶液5、10、20、50、100、200 μL于进样小瓶中,均加入100 μL浓度为1mg·L−1的混合同位素内标标准工作溶液,用甲醇定容至1 mL,获得标准物质浓度分别为5、10、20、50、100、200 μg·L−1 ,同位素内标标准物质浓度均为100 μg·L−1 的标准系列工作溶液.
1.3 样品前处理
沉积物样品和污泥样品分别从广州市海珠湖和南沙污水处理厂获得,样品采集后,冻干,磨碎,过200目筛,置于4 ℃冷藏保存. 分别准确称取2 g冻干后的沉积物或0.5 g冻干后的污泥样品,加入100 ng混合同位素内标(100 μL,mg·L−1 ),加入5 mL超纯水,涡旋1 min混合均匀,加入10 mL乙腈(含1%乙酸),加入QuEChERS盐析试剂(6 g无水硫酸镁/1.5 g无水乙酸钠),然后立即用手剧烈振荡1 min进行提取,将提取液置于3040 g离心10 min,随后取7 mL上清液于15 mL聚丙烯离心管,加入分散固相萃取试剂(900 mg无水硫酸镁/150 mg PSA/150 mg封端C18),手摇振荡30 s,在3040 g条件下离心10 min,取5 mL上清液用氮气轻轻吹至近干,然后采用500 μL甲醇重新溶解,提取液过0.22 μm有机相滤膜,置于−20 ℃冰箱中避光保存. 样品分析前,将甲醇置换成V/V = 3:7的乙腈/水(含5 mmol·L−1乙酸铵和0.2%甲酸)溶液.
1.4 色谱条件
色谱柱:Agilent ZORBAX Eclipse Plus C18柱(50 mm × 2.1 mm,1.8 μm),色谱柱前端接孔径为0.22 μm的在线过滤器,用于滤过样品和流动相溶液中的微小颗粒物;柱温为40 ℃;进样体积为5 μL;流动相为缓冲水溶液A(含5 mmol·L−1乙酸铵和0.2%甲酸)和B乙腈,流动相流速为0.3 mL·min−1,总运行时间6 min,流动相采用如下程序梯度洗脱目标精神活性药品:0 min,30% B;1.5 min,30% B;3 min,55% B;4 min,70% B;4.5 min,70% B;5 min,90% B;6 min,90% B,每针样品分析结束后,设置4 min后运行时间平衡液相色谱柱.
1.5 离子源和质谱条件
色谱柱分离后,样品在电喷雾离子源(ESI)正离子模式下,进入质谱检测器,离子源干燥气流速5 L·min−1;干燥气温度300 ℃;雾化器压力35 psi;鞘气温度300 ℃;鞘气流速12 L·min−1;喷嘴电压500 V;毛细管电压3500 V. 样品经ESI雾化进入质谱后,通过多重反应模式(MRM)进行分析,15种目标精神活性药品的母离子、子离子、碎裂电压、碰撞能等质谱分析参数如表2所示.
表 2 目标精神活性药品质谱参数和保留时间Table 2. UPLC-MS/MS mass transitions and retention times of the target psychoactive drugs化合物Compound 母离子Parent ion(m/z) 子离子Daughter ion (m/z) 碰撞能/eVCE 碎裂电压/VFragmentor 保留时间/minRT 内标Interior label 甲基苯丙胺Methamphetamine 150.1 91.1* 29 95 2.005 甲基苯丙胺-d5Methamphetamine-d5 119.1 10 氯胺酮Ketamine 238.1 125.0* 39 110 2.226 氯胺酮-d4Ketamine 207.1 15 吗啡Morphine 286.1 152.1* 76 175 1.028 吗啡-d3Morphine-d3 165.1 50 可待因Codeine 300.2 165.1 58 170 1.760 可待因-d3Codeine-d3 215.1* 30 可卡因Cocaine 304.2 82.1 35 140 2.606 可待因-d3Codeine-d3 182.1* 23 咪达唑仑Midazolam 326.1 291.2* 33 195 3.057 阿普唑仑-d5Alprazolam-d5 249.2 46 硝西泮Nitrazepam 282.0 236.1* 28 155 3.567 硝西泮-d5Nitrazepam 180.1 48 劳拉西泮Lorazepam 321.0 275.1* 28 145 3.618 阿普唑仑-d5Alprazolam-d5 229.1 38 阿普唑仑Alprazolam 309.1 205.1 48 200 3.635 阿普唑仑-d5Alprazolam-d5 281.2* 29 氯硝西泮Clonazepam 316.0 241.1 43 155 3.672 吗啡-d3Morphine-d3 270.1* 30 三唑仑Triazolam 343.1 308.1* 30 205 3.688 阿普唑仑-d5Alprazolam-d5 315.1 35 地西泮Diazepam 285.1 154.1 32 175 4.252 吗啡-d3Morphine-d3 193.1* 38 氯氮卓Chlordiazepoxide 300.1 282.1* 29 165 2.811 氯胺酮-d4Ketamine 227.1 29 美沙酮Methadone 310.2 105.0 35 125 3.549 美沙酮-d9Methadone-d9 265.3* 15 咖啡因Caffeine 195.0 138.1 23 120 1.924 氯胺酮-d4Ketamine 110.1 28 甲基苯丙胺-d5Methamphetamine-d5 155.1 121.1 10 95 2.000 — 92.1* 23 氯胺酮-d4Ketamine-d4 242.1 129.0* 35 110 2.220 — 211.1 14 吗啡-d3Morphine-d3 289.2 152.0* 77 175 1.022 — 165.1 49 可待因-d3Codeine-d3 303.2 215.1* 28 170 1.754 — 165.1 55 硝西泮-d5Diazepam-d5 287.1 241.2* 29 175 3.545 — 185.1 41 阿普唑仑-d5Alprazolam-d5 314.1 210.1 46 170 3.624 — 286.2* 29 美沙酮-d9Methadone-d9 319.3 268.2* 15 135 3.543 — 105.0 30 注:标*的离子为定量离子. Note: The * refers to the quatification ion. 1.6 数据分析
1.6.1 加标回收率
提取前,分别称取冻干后的2 g沉积物和0.5 g污泥样品,向沉积物和污泥样品中分别加入10、40、100 μL目标精神活性药品浓度均为1 mg·L−1 的混合标准工作溶液,使15种目标精神活性药品在沉积物中的加标浓度分别为5 、20 、50 ng·g−1 ;在污泥中的加标浓度分别为20、80、200 ng·g−1 ;同时,每个样品中均加入100 μL浓度为1 mg·L−1 的混合同位素内标标准工作溶液,每个加标样品做3个平行样. 加标样品的绝对回收率Rabs和相对回收率Rrel根据公式(1)和(2)进行计算[21]:
Rabs(%)=(Ass−Ab)/As×100% (1) Rrel(%)=(Css−Cb)/Cs×100% (2) 其中,Ass和Ab分别为目标精神活性药品在加标样品(沉积物或污泥)和未加标的空白样品(沉积物或污泥)中的峰响应值,As为目标精神活性药品在对应浓度的标准工作溶液中的峰响应值;Css和Cb分别为目标精神活性药品在加标样品(沉积物或污泥)和未加标的空白样品(沉积物或污泥)中测得的浓度,Cs为目标精神活性药品在对应浓度的标准工作溶液中测得的浓度.
1.6.2 基质效应
分别称取冻干后的2 g沉积物和0.5 g污泥样品进行提取,向提取液基质中分别加入1 mg·L−1 的混合标准工作溶液5、10、20、50、100、200 μL,同时均加入1 mg·L−1的混合同位素内标标准工作溶液100 μL,获得样品基质匹配曲线溶液. 基质效应ME根据公式(3)进行计算:
ME(%)=(Smatrix−Ssolvent)/Ssolvent×100% (3) 其中,Smatrix和Ssolvent分别为目标精神活性药品在样品基质(沉积物或污泥)匹配曲线溶液和溶剂标准工作溶液中的斜率;ME > 0表示基质增强效应,ME = 0表示不存在基质效应,ME < 0表示基质抑制效应,ME的绝对值越低,表示基质效应越弱.
2. 结果与讨论(Results and discussion)
2.1 提取方法优化
本研究考察了提取溶剂乙腈中乙酸含量、盐析试剂组成及分散固相萃取试剂组成对沉积物中15种目标精神活性药品的提取效率(图1). 不同乙酸含量条件下15种目标精神活性药品的回收率结果如图1a所示,在乙腈中分别加入0%乙酸溶液、1%乙酸溶液和5%乙酸溶液时,除了可待因和地西泮,大部分目标精神活性药品的回收率逐渐下降;整体上,乙酸溶液的体积分数为0%和1%时,大部分目标精神活性药品的回收率比较接近,当乙酸溶液的体积分数为5%时,15种精神活性药品的回收率较低;考虑到环境基质来源较复杂,加入适量乙酸可以提高酸碱性精神活性药品的稳定性,为了提高提取方法对不同来源沉积物的适用性,选择提取溶剂为1%甲酸-乙腈溶液.
两种不同缓冲盐体系下15种目标精神活性药品的回收率结果如图1b所示,甲基苯丙胺、氯胺酮、阿普唑仑、氯硝西泮和三唑仑在乙酸钠缓冲盐体系下的回收率较高;可待因和劳拉西泮在柠檬酸钠缓冲盐体系下的回收率较高,其余目标精神活性药品在柠檬酸钠缓冲盐和乙酸钠缓冲盐体系下的回收率比较接近,考虑到柠檬酸钠缓冲盐价格较高,试验选择的盐析试剂为乙酸钠盐.
不同净化试剂条件下,15种目标精神活性药品的回收率结果如图1c所示,采用硫酸镁/PSA作为净化试剂时,吗啡、可待因和劳拉西泮的回收率较低;采用硫酸镁/C18作为净化试剂时,阿普唑仑和三唑仑的回收率较低;相比采用单一的硫酸镁净化试剂,采用硫酸镁/PSA/C18作为净化试剂时,阿普唑仑、三唑仑和地西泮的回收率明显提高;无水硫酸镁/PSA/C18混合分散固相萃取(d-SPE)试剂进行净化,15种精神活性药品的回收率整体比较好. 通过QuEChERS提取方法优化结果得出,试验样品采用含1%乙酸的乙腈溶液提取,加入无水硫酸镁和乙酸钠促进提取和溶液分层,提取液通过无水硫酸镁/PSA/C18混合分散固相萃取(d-SPE)试剂进行净化前处理样品.
考虑到15 种精神活性物质均采用正离子模式进行测定,在流动相中加入一定量的甲酸可以使流动相pH处于一个稳定的状态,减少因为离子形态与分子形态共存而造成的峰变形和分裂,增加目标物的离子化效率,从而增加灵敏度. 沉积物和污泥样品基质复杂,QuEChERS 法常用的吸附剂有 C18、 PSA 等. 其中无水硫酸镁作为除水剂来除去样品基质中的水分, C18 主要是去除脂肪和酯类等非极性干扰物,PSA 可去PSA是吸附基质中的碳水化合物、脂肪酸、有机酸、酚类和少量的色素,硫酸镁、PSA、C18; 采用硫酸镁/PSA/C18进行净化均获得比较理想的净化效果,且对回收率的影响较小.
2.2 方法验证
2.2.1 加标回收率
不同加标浓度条件下,QuEChERS提取方法对沉积物和污泥中15种目标精神活性药品均表现出良好的提取效果,其相对回收率Rrel结果如表3所示. 加标浓度为5、20、50 ng·g−1时,15种目标精神活性药品在沉积物中的加标回收率范围分别为56%—121%、57%—116%和58%—115%,RSD < 15%;加标浓度为20、80、200 ng·g−1 时,15种目标精神活性药品在污泥中的加标回收率范围分别为55%—117%、64%—132%和74%—135%,RSD < 12%,说明该方法具有良好的准确度和精密度. 15种目标精神活性药品在加标量均为100 ng(100 μL、1 mg·L−1 )的溶剂标准工作溶液、沉积物加标样品和污泥加标样品中的多重反应监测离子如图2所示,QuEChERS提取液中15种精神活性药品的目标离子峰清晰可辨,能高效地进行定性定量分析.
表 3 目标精神活性药品在沉积物中的回收率、方法检出限、方法定量限Table 3. Recoveries (n=3, %±relative standard deviation), method detection limits (MDLs) and method quantitation limits (MQLs) of the target psychoactive drugs from sediment沉积物Sediment 污泥Sludge 化合物Compound 加标回收率/%Recovery MDLs/(ng·g−1) MQLs/(ng.g−1) 加标回收率/%Recovery MDLs/(ng·g−1) MQLs/(ng·g−1) 5 ng·g−1 20 ng·g−1 50 ng·g−1 20 ng·g−1 80 ng·g−1 200 ng·g−1 甲基苯丙胺 107±3 95±2 97±2 0.02 0.07 101±1 120±1 115±1 0.06 0.22 氯胺酮 116±2 101±4 103±2 0.03 0.08 107±1 124±1 121±3 0.14 0.48 吗啡 121±5 116±3 115±1 0.24 0.80 113±9 132±2 135±4 0.83 2.78 可待因 118±5 105±1 107±1 0.06 0.21 105±2 129±1 128±3 0.28 0.94 可卡因 68±14 57±7 60±9 0.01 0.04 55±9 64±6 60±6 0.45 1.51 咪达唑仑 77±9 65±3 68±3 0.02 0.08 65±6 79±10 89±5 0.10 0.35 硝西泮 97±6 88±2 96±1 0.12 0.40 96±2 108±2 114±2 0.51 1.70 劳拉西泮 83±9 83±6 85±3 0.11 0.36 109±3 131±2 129±4 0.64 2.12 阿普唑仑 109±1 104±6 110±1 0.07 0.22 117±1 127±1 129±2 0.16 0.52 氯硝西泮 75±14 83±3 99±7 0.12 0.39 105±12 113±7 120±4 0.32 1.07 三唑仑 97±2 90±3 90±1 0.01 0.04 115±5 131±2 130±4 0.07 0.25 地西泮 66±15 61±9 71±7 0.07 0.24 99±6 113±7 132±6 0.21 0.71 氯氮卓 56±10 61±5 58±6 0.06 0.20 58±9 70±1 74±1 0.15 0.50 美沙酮 109±1 95±4 96±2 0.03 0.09 102±2 118±2 111±1 0.23 0.76 咖啡因 87±4 66±3 60±3 0.14 0.46 92±5 86±3 76±1 0.13 0.44 注:粗体表示化合物回收率超过70%—130%范围. Note: Bold type refers the recovery value out of the range of 70%—130%. 2.2.2 方法检出限和定量限
目标精神活性药品的方法检出限(MDLs)和方法定量限(MQLs)通过最低浓度的环境加标样品进行计算,MDLs和MQLs分别为3倍信噪比(S/N)和10倍S/N,表示方法能够从环境基质中检测到的目标精神活性药品最低量. S/N值通过仪器自带的Masshunter软件计算获得. 如表3所示,15种目标精神活性药品在沉积物中的MDLs和MQLs范围分别为0.01—0.24 ng·g−1和0.04—0.8 ng·g−1 ;在污泥中的MDLs和MQLs范围分别为0.06 —0.83 ng·g−1 和0.22—2.78 ng·g−1 . 采用本文的QuEChERS方法进行提取,甲基苯丙胺、氯胺酮和可卡因在沉积物和污泥中的MQLs低于已报道的超声萃取/固相萃取和加速溶剂萃取/固相萃取方法[14-16]. 相比沉积物,污泥中目标精神活性药品的MDLs和MDLs较高. 15种目标精神活性药品在沉积物和污泥中的方法检出限均低于1 ng·g−1 ,方法定量限均低于3 ng·g−1 ,说明QuEChERS方法能够用于环境沉积物和污泥中精神活性药品的高灵敏分析.
2.2.3 基质效应
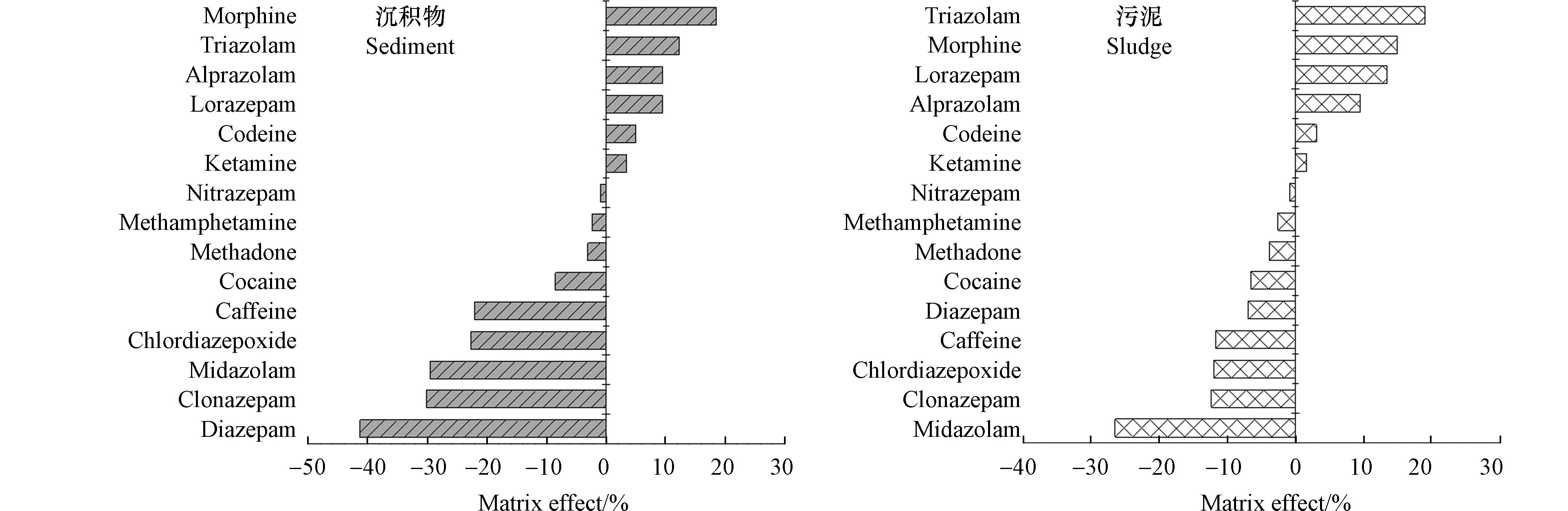
样品提取液中往往存在能够伴随目标物质一起洗脱的基质共存物,造成样品UPLC-MS/MS信号的增强或抑制,导致基质效应[22]. 如图2所示,所有目标精神活性药品在沉积物和污泥中都存在一定程度的基质效应. 其基质效应范围分别为–41.24%—18.54%和–26.45%—19.05%. 除咪达唑仑、氯硝西泮和地西泮,大部分目标精神活性药品的基质效应在±20%范围之内. 15种目标精神活性药品在沉积物和污泥中表现出相同趋势的基质效应:吗啡、可待因、劳拉西泮、阿普唑仑、三唑仑和氯胺酮在沉积物和污泥中主要受到基质增强效应的影响;甲基苯丙胺、可卡因、咪达唑仑、硝西泮、氯硝西泮、地西泮、氯氮卓、美沙酮和咖啡因在沉积物和污泥中主要受到基质抑制效应的影响. 相比污泥,大部分目标精神活性药品在沉积物中受到的基质效应更强.
2.2.4 方法应用
将开发的QuEChERS方法应用于环境样品分析,在采集于广州海珠湖底的沉积物中检出8种目标精神活性药品:甲基苯丙胺、氯胺酮、咪达唑仑、氯硝西泮、三唑仑、地西泮、美沙酮和咖啡因,其浓度范围为0.051—1.395 ng.g−1 干重;在采集于南沙污水处理厂的脱水污泥中检出4种目标精神活性药品:甲基苯丙胺、咪达唑仑、硝西泮和咖啡因,其浓度范围为<MQLs—45.119 ng.g−1 干重.
3. 结论(Conclusion)
(1)本方法快速、准确,对沉积物和污泥中15种目标精神活性药品的加标回收率为55%—135%,相对标准偏差小于15%,可同时检测环境样品中多种精神活性药品.
(2)本方法对沉积物和污泥中15种目标精神活性药品的方法检出限均低于1 ng·g−1,可用于环境样品中痕量精神活性药品的高灵敏检测.
(3)采用本方法在环境沉积物和污泥样品中分别检出8种和4种目标精神活性药品,为精神活性药品的管制、溯源追踪和环境生态风险评价提供方法支持.
-
表 1 吸附等温线模型拟合参数
Table 1. Adsorption isotherm parameters for phosphate adsorption
温度/℃ Langmuir Freundlich qm/(mg·g−1) KL/(L·g−1) R2 n KF/(L·g−1) R2 25 99.305 0.031 67 0.934 08 1.317 1 3.297 0 0.947 57 35 99.701 0.037 29 0.951 96 1.348 0 3.789 2 0.943 01 45 102.56 0.044 52 0.964 86 1.428 9 3.609 2 0.915 82 表 2 吸附动力学模型拟合参数
Table 2. Kinetic parameters for phosphate adsorption
温度/℃ 准一级动力学 准二级动力学 k1/min−1 qe/(mg·g−1) R2 k2/(g·(mg·min)−1) qe/(mg·g−1) R2 25 0.505 16 0.263 70 0.873 42 1.649 71 0.326 50 0.930 91 35 0.570 99 0.289 43 0.893 24 1.802 26 0.352 28 0.953 54 45 0.631 57 0.318 02 0.949 80 1.891 19 0.382 24 0.986 28 -
[1] 姜登岭, 张晓健. 饮用水中磷与细菌再生长的关系[J]. 环境科学, 2004, 25(5): 57-60. doi: 10.3321/j.issn:0250-3301.2004.05.012 [2] KOOIJ D V D, VISSER A, HIJNEN W A M. Determining the concentration of easily assimilable organic carbon in drinking water[J]. Journal American Works Association, 1982, 74(10): 540-545. doi: 10.1002/j.1551-8833.1982.tb05000.x [3] MIETTINEN I T, VARTIAINEN T, MARTIKAINEN P J. Contamination of drinking water[J]. Proceedings of the Academy of Natural Sciences of Philadelphia, 1996, 29(6584): 19-20. [4] MIETTINEN I T, VARTIAINEN T, MARTIKAINEN P J. Phosphorus and bacterial growth in drinking water[J]. Applied & Environmental Microbiology, 1997, 63(8): 3242-3245. [5] 孟顺龙, 胡庚东, 宋超, 等. 镧改性吸附剂废水除磷技术研究进展[J]. 环境科学与技术, 2012, 35(S2): 194-199. [6] 杨金梅, 吕建波, 李莞璐, 等. 壳聚糖载纳米羟基氧化铁对水中磷的吸附[J]. 环境工程学报, 2018, 12(5): 14-22. [7] LIU T, CHEN X, WANG X, et al. Highly effective wastewater phosphorus removal by phosphorus accumulating organism combined with magnetic sorbent MFC@La(OH)3[J]. Chemical Engineering Journal, 2018, 335: 443-449. doi: 10.1016/j.cej.2017.10.117 [8] 雷行, 杨雪, 刘婷, 等. 锆改性铝氧化物对水中磷的吸附特性[J]. 环境工程学报, 2018, 12(5): 117-124. [9] HE J J, WANG W, SHI W X, et al. La2O3 nanoparticles polyacrylonitrile nanofibers for bacterial inactivation based on phosphate control[J]. RSC Advances, 2016, 6: 99353-99360. doi: 10.1039/C6RA22374E [10] HAGHSERESHT F, WANG S B, DO D D. A novel lanthanum-modified bentonite, phoslock, for phosphate removal from wastewaters[J]. Applied Clay Science, 2009, 46(4): 369-375. doi: 10.1016/j.clay.2009.09.009 [11] COPETTI D, FINSTERLE K, MARZIALI L, et al. Eutrophication management in surface waters using lanthanum modified bentonite: A review[J]. Water Research, 2016, 97: 162-174. doi: 10.1016/j.watres.2015.11.056 [12] 于岩. 新型水相吸附材料[M]. 北京: 科学出版社, 2016. [13] ZHU H T, QIU S S, JIANG W, et al. Evaluation of electrospun polyvinyl chloride/polystyrene fibers as sorbent materials for oil spill cleanup[J]. Environmental Science & Technology, 2011, 45(10): 4527-4531. [14] LIU C, WU L L, ZHANG C C, et al. Surface hydrophilic modification of PVDF membranes by trace amounts of tannin and polyethyleneimine[J]. Applied Surface Science, 2018, 457: 695-704. doi: 10.1016/j.apsusc.2018.06.131 [15] 杜涛, 王莹, 高超, 等. 离子色谱法测定饮用水中无机阴离子[J]. 沈阳师范大学学报 (自然科学版), 2011, 29(2): 260-263. -




 DownLoad:
DownLoad: