-
化工行业的蓬勃发展为我国创造巨大经济效益的同时,其化工产品制造过程中产生的废料与废水若不能及时得当的处理亦会对环境与人类健康产生严重的危害。如化工产品制造过程中的设备洗涤废水,由于含有大量表面活性物质(LAS)及设备生产时未充分利用的原材料使得其组成成分复杂、毒性强、水质与水量波动幅度较大。该废水若不经处理而直接排入污水管网,则会对城市污水处理厂造成严重影响,甚至使污水处理厂工艺系统瘫痪。目前,该类废水的综合治理已成为环境领域亟待解决的重要难题[1-3]。
彭雨等[4]采用“混凝气浮+接触氧化+沉淀+消毒”工艺处理医用织物洗涤废水,该类废水进水COD≤500 mg·L−1,同时LAS、TP粪大肠菌群均为其主要污染物,其排放限值为COD≤120 mg·L−1,经调试运行后,该工艺出水水质已达标排放。章正勇等[5]以“微电解+芬顿氧化”作为洗涤化工废水的预处理单元,并选择间歇式的处理模式,后续处理单元采用“水解酸化+好氧”的生物处理系统,洗涤废水进水COD≤ 2 000 mg·L−1,经该工艺处理后出水COD约为138 mg·L−1。这些技术通常用于处理COD不高的洗涤废水,对于高浓度洗涤废水的处理技术目前研究较少。
本研究以青岛某化工厂的高浓度洗涤废水为对象,以实验室小试为基础,并结合洗涤废水水质分析,研究并设计出以“SMAD-BBR”为主体适用于处理该类洗涤废水的工艺。自混式厌氧反应器(SMAD)是结合多阶段生物高速厌氧消化技术的升流式反应器,内部无任何机械部件,通过混合器对产生的甲烷收集后,以脉冲的形式释放使反应器内部均匀混合。SMAD具有较高的抗负荷冲击能力,且对挥发性固体(VS)破坏效率高等优点[6]。导流式活性污泥反应器(BBR)采用一项小流量的一体化污水处理与回用技术,LIU等[7]曾于2009年在美国密苏里州罗拉市的某污水处理厂建立了一个体积为8.1 m3,处理规模为37.9 m3·d−1的BBR设备,并对其出水水质进行了1年的监测。结果表明,BBR可以长期有效地对COD、NH3-N、TP、SS等保持较高去除率,且可以维持较高的MLSS,使得系统内抗负荷冲击能力更强。SMAD-BBR工艺建设完成后,经过4个月的调试运行(2018-07-05—2018-10-31),出水水质能稳定达到《污水排入城镇下水道标准》(GB/T 31962-2015)中的B级标准。
全文HTML
-
青岛市某化工厂主要从事精细化学品的研究开发,研究领域包括有机合成及其相关产品、聚合物及其相关产品、工程塑料及其功能性复合材料。经水质分析,该化工厂生产过程中产生的高浓度洗涤废水主要成分为十二烷基葡糖糖苷(C18H36O6,95%)、邻苯二甲酸酯(C24H38O4)和大量表面活性物质,洗涤废水COD约20 000~30 000 mg·L−1。
-
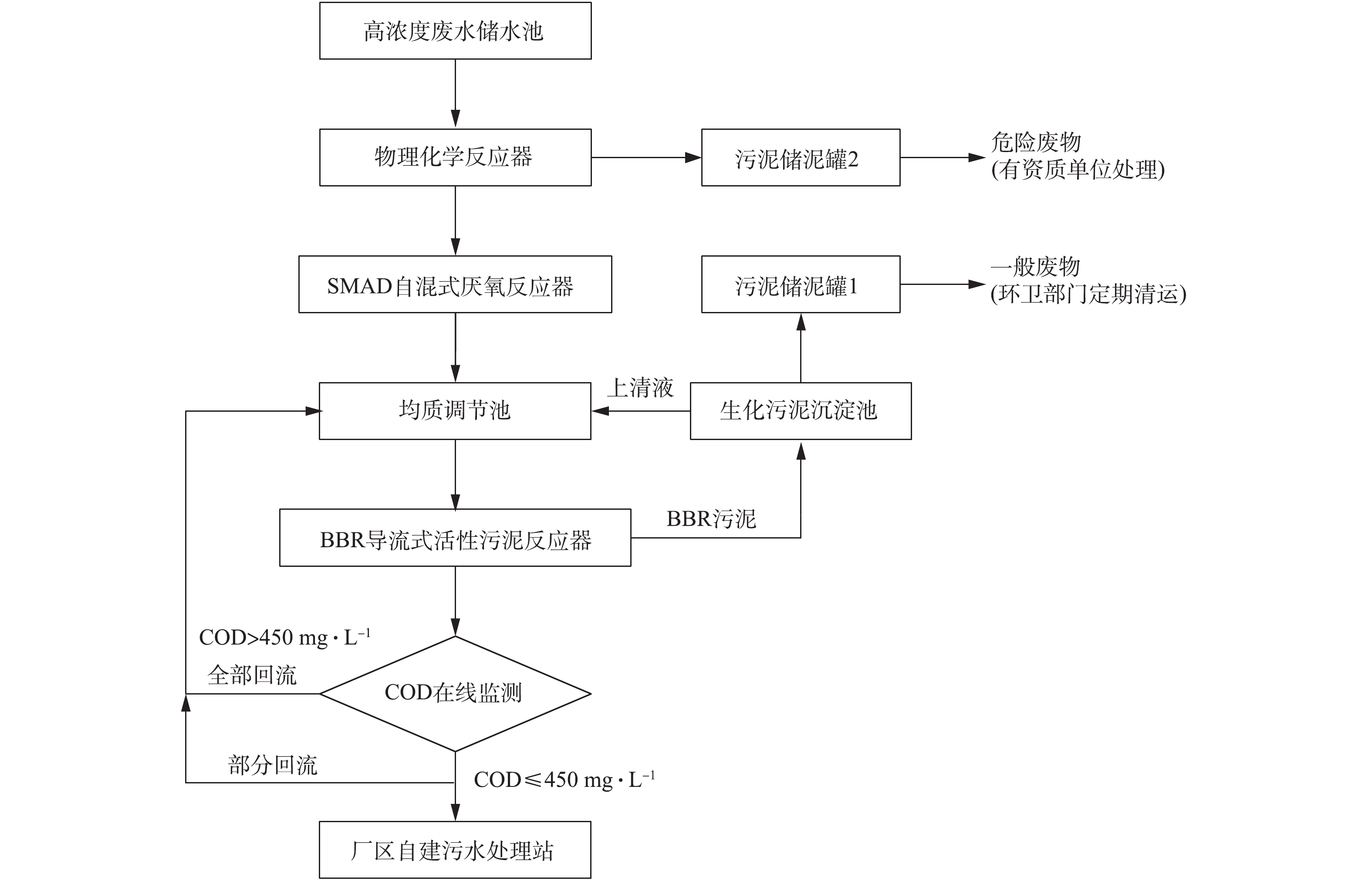
SMAD-BBR组合工艺处理高浓度洗涤废水工艺流程如图1所示。高浓度洗涤废水经厂区内管道汇流后集中排入高浓度废水储水池,后经潜污泵提升至物理化学反应器。由于厌氧微生物活性对温度要求较为严苛,为保证SMAD内温度使微生物保持最佳活性,同时考虑到设备内部辅助加热存在一定难度,发生故障不易检修,故最终选择SMAD进水预加热。在物理化学反应器顶部吊装3根加热管,加热部分没入常水位液面,由温控器控制。考虑到热量在空气和管道中的散失,温控器设定温度为40 ℃。
物理化学反应器出水从SMAD底部进入,呈上升流经过厌氧污泥停留区,进行厌氧水解、发酵、产酸和产甲烷反应,在厌氧菌和兼性厌氧菌的共同作用下,将水中大分子难降解有机物最终转化为甲烷、CO2及新的细胞物质[8-10]。
SMAD出水重力流流入均质调节池,均质调节池的作用主要是稀释厌氧出水和调节下一单元的进水流量。均质调节池中废水由潜污泵提升至BBR中,BBR中的工艺单元主要包括进水端的缺氧区、中间段的曝气区、末段的污泥截流区和终沉池。废水首先通过混合器在前端缺氧区内混合搅拌,反硝化细菌在缺氧条件下将废水中的硝酸盐还原为无害的N2释放;均匀混合后的废水进入曝气区,在鼓风曝气的作用下,微生物将水中有机物充分降解去除;处理后的泥水混合液进入污泥截留区,污泥在此单元充分沉降,由空气驱动的污泥泵回流至曝气区维持MLSS,少部分未能沉降的污泥随水流入终沉池,在终沉池沉降后,由底部排泥泵进入生化污泥沉淀池。污泥在生化污泥沉淀池中沉淀后的上清液随溢流管回流至均质调节池,用以稀释SMAD出水水质。终沉池出水管道上设有常开出水阀门,通过橡胶软管连接COD在线监测仪,实时监测BBR出水水质,若出水COD>450 mg·L−1,则由COD在线监测仪发送电流信号开启电磁阀,出水全部回流至均质调节池。在日常监测达标情况下,回流管道上的电磁阀常闭。
该工艺中设计的物理化学反应器为改良的芬顿氧化塔,原设计处理洗涤废水的COD为150 000 mg·L−1,通过Fenton高级氧化反应生成具有强氧化性的羟基自由基( · OH)。羟基自由基在水溶液中与难降解有机物进行反应,使其氧化分解,从而提高废水可生化性,为后续生化处理减轻压力[11-14]。由于目前工程进水COD约为20 000~30 000 mg·L−1,且B/C>0.4,洗涤废水具有一定可生化性,同时考虑到投加Fenton试剂会增加洗涤废水的处理成本,并产生危废“铁泥”。因此,目前物理化学反应器仅作为调节池,用于调节SMAD进水的pH、温度,同时还可对水中悬浮物进行混凝沉淀。
-
该工艺设计处理流量约2.0 m3·d−1,原设计处理洗涤废水COD约150 000 mg·L−1,目前洗涤废水COD约为20 000~30 000 mg·L−1、NH3-N≤100 mg·L−1、TP≤20 mg·L−1、pH≈4.5。各构筑物设计参数如下。
1)高浓度废水储水池。1座,地下式钢筋混凝土防腐结构。长×宽×高为10 m×5.8 m×7 m(超高0.5 m),有效容积377 m3,配置1台潜污泵(B-333,Q=24 m3·h−1,N=2.2 kW,H=17 m,U=380 V),1台流量计,储水池内设有液位传感器。
2)物理化学反应器。1座,地上式防腐塑料设备。长×宽×高为3.0 m×1.8 m×3.4 m(超高0.5 m),有效容积6.0 m3,HRT=3 d。配置1台搅拌机(BLD10-17-1.5 kW,U=380 V),3根干烧型加热管(U=220 V,N=1 kW),1台计量泵,1台pH检测仪。
3)SMAD。1座,半地下式玻璃钢防腐设备。设计参数:容积负荷(以COD计)为12 kg·(m3·d)−1,Q=2.0 m3·d−1。直径×高为φ2.0 m×7.7 m(超高0.7 m),有效容积20.0 m2,HRT=10 d。主要功能:为厌氧反应提供条件,降解水中大分子有机物,提高废水可生化性。配置温度传感器1台,沼气回流泵1台,罐体保温系统1套及沼气分压系统1套。
4)均质调节池。1座,地下式钢筋混凝土防腐结构。长×宽×高为4.0 m×3.6 m×6.0 m(超高0.5 m),有效容积75 m3。配置潜污泵1台(B-333,Q=24 m3·h−1,N=2.2 kW,H=17 m,U=380 V),1台液位传感器。
5)BBR。1座,地上式碳钢防腐设备。设计参数:容积负荷(以COD计)为0.75 kg·(m3·d)−1,Q=2.0 m3·d−1。长×宽×高为6.0 m×2.2 m×2.6 m(超高0.5 m),有效容积20.0 m3,HRT=10 d。配置污泥回流泵2台、排泥泵1台、缺氧区混合系统1套,COD在线监测系统1套,主风机1台(N=2.2 kW,U=220 V),备用外置风机1台(HG-4000S,N=4 kW,U=380 V)。
-
研究采用密封消解法测定水样中COD;纳氏试剂分光光度法(HJ 535-2009)测定水样中氨氮浓度;过硫酸钾消解钼锑抗分光光度法(GB 11893-1989)测定水样中总磷浓度;重量法测定曝气区活性污泥浓度;玻璃电极法测定水样的pH。
1.1. 工程概况
1.2. 工艺流程
1.3. 设计参数
1.4. 分析方法
-
该工艺于2018年7月初建设完成,后调试运行约4个月,调试期间运行状况良好,出水水质保持稳定,目前已稳定达到《污水排入城镇下水道标准》(GB/T 31962-2015)中的B级标准。其中COD去除率为99.1%,氨氮去除率为95.6%,总磷去除率为82.5%。处理后的污水由企业厂区内管道汇流后,排入企业自建污水处理站,与厂区内生活污水共同处理后,排放至下水道。工艺进出水质及排放标准见表1。
-
厌氧反应通常分为4个阶段反应:水解阶段、发酵阶段、产酸阶段、产甲烷阶段[15]。其中,产甲烷菌对pH条件要求苛刻,其最佳生活pH条件为6.8~7.2。考虑到厌氧反应副产物甲烷增加了附加处理费用,且污水处理站临近厂区锅炉房以免发生安全事故,因此,从设备运行调试起,保持SMAD进水pH约为4.5。由于进水pH呈酸性,使得SMAD内中的产甲烷菌活动受到抑制,无法成为优势菌属,反应器内只进行水解、发酵、产酸反应。同时,较长的水力停留时间可以使洗涤废水中的大分子难降解有机物充分转化成小分子易降解有机物,提高废水可生化性,为后续好氧处理提供有利条件。
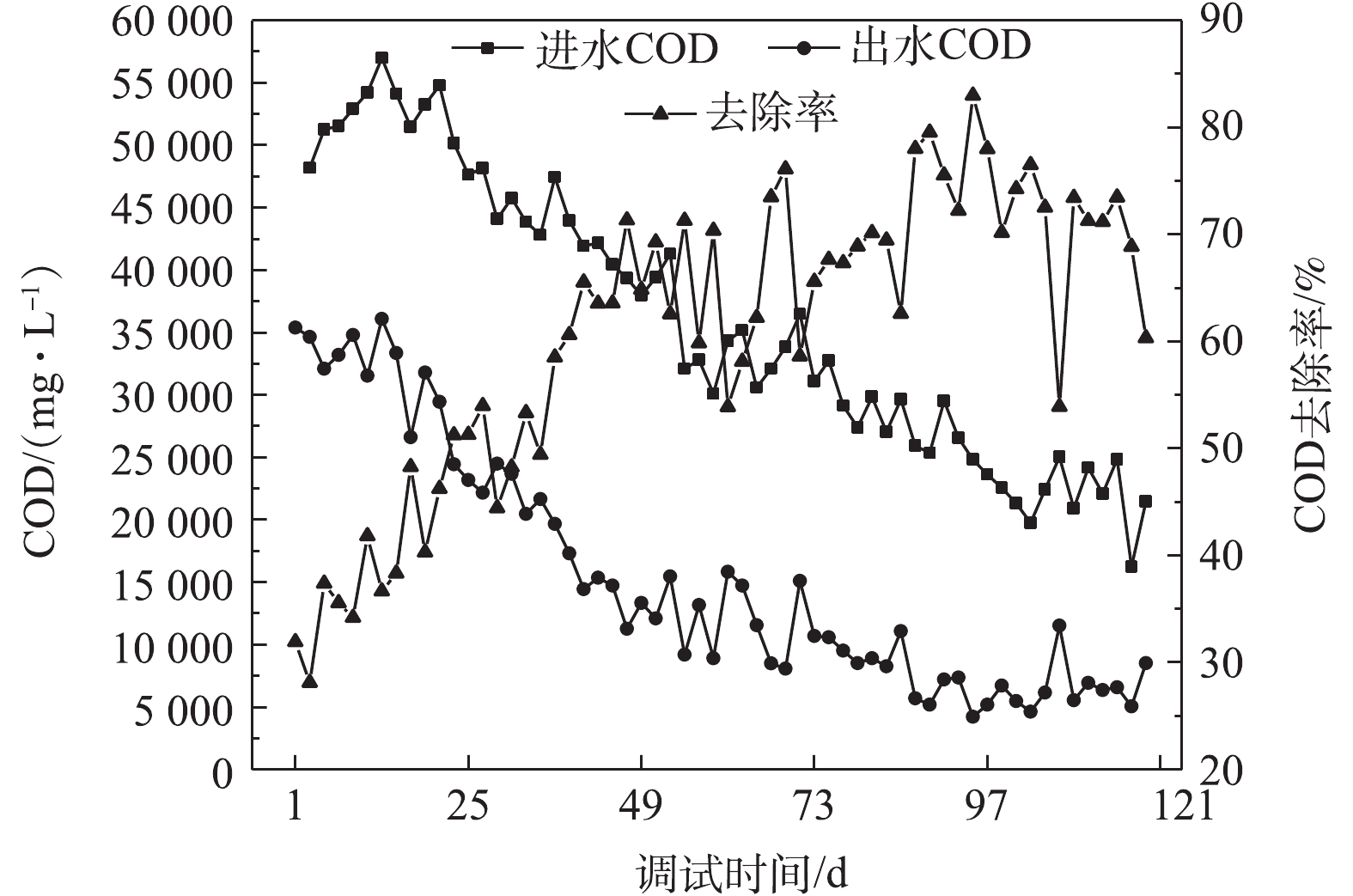
在SMAD设备安装完成后,向设备中投加10 t含水率为99%的厌氧消化污泥,进行污泥驯化。调试阶段,每隔1 d取水样回实验室进行检测。由图2可知,在设备安装完成后进入调试阶段,SMAD进水COD已降低至53 000 mg·L−1。自调试开始,SMAD进水COD仍在不断降低,于75 d后稳定在20 000~30 000 mg·L−1。进水COD大幅降低的原因是该化工厂用以清洗设备的洗涤剂浓度有所降低,且厂区管道改造使得锅炉冷凝水与洗涤废水在管道中汇流,从而降低了进水的COD。调试初期,SMAD每隔4 d提高10%的进水量,于40 d达到负荷进水,约为2.0 m3·d−1。4个月运行调试结束后,COD去除率稳定在65%~75%,SMAD出水COD约为6 000~8 000 mg·L−1。
-
好氧调试的进水方式可以分为渐进式进水和全水量式进水2种[16]:1)渐进式进水是接种污泥后向好氧反应器或生化池中灌满清水,待污泥经过闷曝恢复活性后,按照设计水量10%的进水量进水,同时监测出水水质及配合实验室镜检。若出水水质稳定或镜检结果较好(微生物活性较好、污泥结构较为紧密、曝气池混合液中污泥呈良好的絮体状),则适当增加进水水量,直至达到设计设计水量。2)全水量式进水是调试起初在接种污泥并且进行闷曝恢复活性后,向好氧反应器或生化池中加满待处理废水,随后每天按照设计水量进水。前期可能无法达到设计出水水质,随着时间的推移,出水会逐渐满足设计水质。
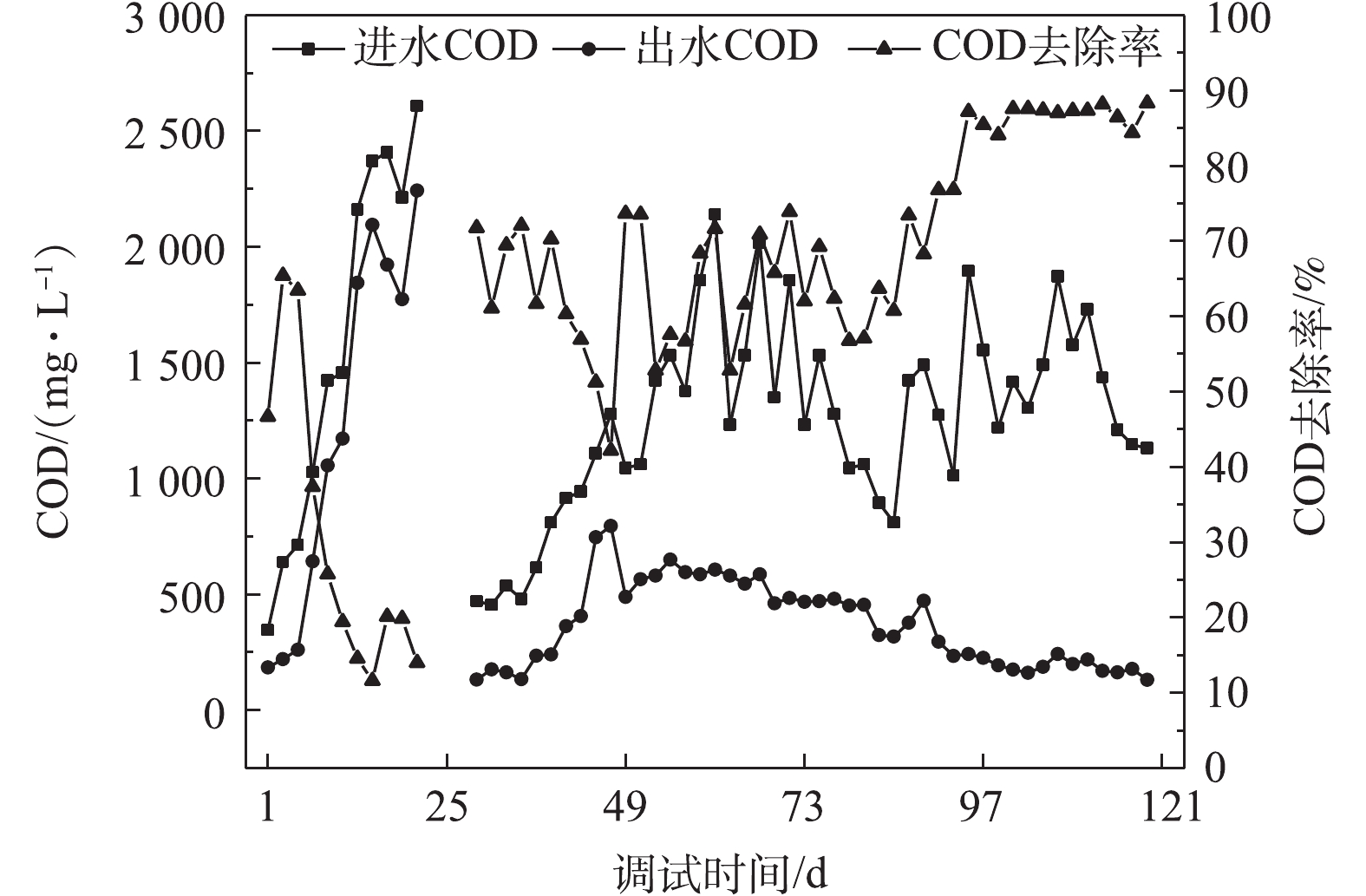
针对本工艺的实际情况,BBR调试采用渐进式进水的方式。调试初期,向BBR中投加5 t青岛市海泊河污水处理厂的预缺氧池回流污泥用于污泥驯化,该污水处理厂采用的处理工艺为MSBR一体化工艺。由图3可知,设备运行初期,由于SMAD与BBR调试过程为同步进行,SMAD前期出水浓度过高,而均质调节池内未存有足够的清水来稀释SMAD出水,故导致BBR进水负荷在前期增长过快,废水中含有大量SMAD未降解的有机大分子污染物和有毒有害物质,使得BBR中的污泥中毒(图4(a))。活性污泥中毒后,微生物活性和细胞合成受到抑制而导致污泥解体,从而使得SV30升高,污泥难以沉降,致使出水水质变差。此时,曝气区的处理能力严重下降,废水中含有的表面活性物质在鼓风曝气的作用下产生大量的白色泡沫并漂浮在曝气区上方(图4(b)),从而降低了氧传递效率,曝气区中的污泥附着在洗涤剂泡沫中从BBR顶部的隔板中溢出,使得BBR曝气区污泥浓度由起初5 600 mg·L−1降至2 320 mg·L−1。为重新恢复BBR去除效果,只能将BBR排空后,重新投加污泥二次启动。BBR二次启动采用的污泥为青岛啤酒厂自建污水处理站含水率70%的脱水污泥(图4(c))。
BBR二次启动调试前,向均质调节池中注满清水,用以混合稀释SMAD出水浓度,并配合渐进式进水方式,以达到驯化BBR中污泥及逐步提高BBR进水负荷的目的。启动时向曝气区中投加约0.6 t脱水污泥,控制BBR曝气区中的MLSS为8 000 mg·L−1左右。较高MLSS使BBR能提高BBR系统抗负荷冲击能力,同时亦有助于改善废水中的表面活性物质在曝气时产生大量泡沫的情况。BBR二次启动后,前期每2 d提高10%的进水量,后期每2 d提高20%的进水量,于43 d达到满负荷进水。
由图3可知,二次启动后29~61 d,BBR进水COD呈逐渐升高的趋势,由最初471 mg·L−1升高至2 140 mg·L−1。这是因为SMAD出水流入均值的调节池中,使得COD不断增高。随着BBR加大排泥时间,回流至均质调节池稀释SMAD出水的污泥上清液水量增大,61 d后水质尽管波动较大,但平均COD约为1 380 mg·L−1。BBR出水COD在29~39 d期间较为稳定,平均COD为168 mg·L−1。在41~47 d,水质变差,出水COD由363 mg·L−1升高至796 mg·L−1,其原因主要有2个方面。1)前期排泥时间不够,二沉池底部未排出的污泥在缺氧的条件下发生反硝化反应上浮,使得出水水质变差。2)考虑到第1次启动时由于BBR进水水量未控制好,负荷增长太快污泥中毒的情况,故第2次启动时严格控制进水水量及进水负荷,但由于BBR中的MLSS高,闷曝过后污泥恢复活性,而进水有机物浓度太低,微生物的营养物质不够,曝气池中的氧气利用率低,只有部分溶解氧被微生物用作自身内源呼吸,活性污泥容易老化,部分死亡解体,出水浑浊。
经过分析后,提高了BBR进水COD与进水水量,调整溶解氧量,使其稳定在2.5~3.5 mg·L−1,同时延长了排泥时间。最终BBR出水在第69天后达到排放标准,达标后平均出水COD为299 mg·L−1。
-
该工艺设备投入运行后,无投加药剂费用。考虑到季节因素对水温的影响,干烧型加热管在不同季节中工作时间不同,在夏季工作6 h,冬季工作24 h。水泵及风机用电量不随季节变化的情况下,按电费0.8元·(kWh)−1计算,处理废水消耗电费分别为49.5元·t−1(夏季)、63.9元·t−1(冬季)。该化工厂洗涤废水原处理方式是将废水外送处理,废水需花费2 000元·t−1,通过该工艺处理后,若不考虑设备折旧费用,每年可节约140×104元。
2.1. 整体工艺运行情况
2.2. SMAD调试运行情况
2.3. BBR调试运行情况
2.4. 工程经济分析
-
1)水质分析结果表明,SMAD-BBR组合工艺对该类废水的处理是可行的,能稳定达到排放标准。同时,该组合工艺对废水中的污染物有较高的去除率,其中COD去除率为99.1%、NH3-N去除率为95.6%、TP去除率为82.5%;稳定运行期间水质波动较大的情况下,SMAD-BBR组合工艺出水仍保持稳定,表明该工艺具有抗负荷冲击能力强的特点。下一步将探究经济与处理效果的最优匹配,在保证处理稳定达标的基础上对本工艺的投资效益与运行参数进行改进优化。
2)在进水水质生化性允许的情况下,物理化学反应器不进行Fenton反应,仅作为调节池使用,无化学药剂投加及危废的产生,在节省成本的同时还减少了对环境的二次污染。工程运行经济分析结果表明,该工艺每年可节约140×104元。




 DownLoad:
DownLoad: