-
剩余污泥是采用活性污泥法的污水处理厂主要的副产物[1]。目前,针对剩余污泥有多种处理处置方法,主要包括填埋、焚烧、厌氧消化、好氧堆肥等。其中,厌氧消化作为一种成本较低、稳定有机物、减少污泥体积、产出甲烷能源的技术,吸引了越来越多的关注[2]。然而,由于污泥在厌氧消化过程中具有缓慢的水解速率和较弱的产甲烷潜力,使该技术的应用受到了较大的限制[3-4]。为改善污泥的厌氧消化性能,常采用热水解[5]、超声波[6]、碱解法[4]等预处理技术对污泥中的细胞和胞外聚合物进行破解,从而释放有机物进入液相,达到改善污泥的水解速率和产甲烷潜力的目的。在众多预处理技术中,超声波破解效率快、破解程度高且无化学添加,使超声波破解污泥技术成为了热门的研究方向之一[6-8]。然而,目前大部分超声波破解污泥的研究仅限于实验室阶段,距离工业化应用仍有较大差距。
超声波反应器分探头式和槽式超声波反应器2种[9]。近年来,一些研究人员对2种类型的超声波技术进行了工业化应用的尝试。NICKEL等[10]在研究中报道了一种管道式超声波反应器,最大功率为3.6 kW,体积为1.3 L,利用该反应器破解污泥后,厌氧消化一级反应动力学速率常数由0.26 d−1提高至0.52 d−1。此外,NICKEL等[10]还开发了一种工业化规模探头式超声波反应器,体积为29 L,共计5个频率20 kHz、功率2 kW的超声波换能器,停留时间为30 s,在连续塞流式超声波处理污泥情况下,70 Wh·L−1能量输入条件下可获得50%的COD溶出率。GOGATE等[11-12]先后研发了双频率、三频率多探头超声波槽式反应器,但只是应用于废水处理,并未在污泥处理中取得应用。
上述研究对2种类型的超声波反应器均进行了优化并进行了工业化应用尝试。有研究[11-14]表明,同等功率下低功率多换能器槽式超声波反应器相比传统大功率单换能器探头式超声波反应器的声场强度更大,声场分布更均匀,能量利用效率更高。然而,目前对于工业化规模低功率多探头槽式超声波反应器破解污泥的研究还未见报道。本研究利用1台250 L的低功率多探头槽式超声波反应器,建立工业化规模超声波破解污泥实验,并探究了工业化规模超声波对不同浓度固体(TS)污泥物理化学特性及后续厌氧消化性能的改善效果。
-
实验所用污泥为天津某污水处理厂的剩余污泥,该厂采用A2/O活性污泥处理工艺,处理能力为300 000 m3·d−1。污泥取自于污泥脱水车间的脱水污泥,固体浓度为20%。
-
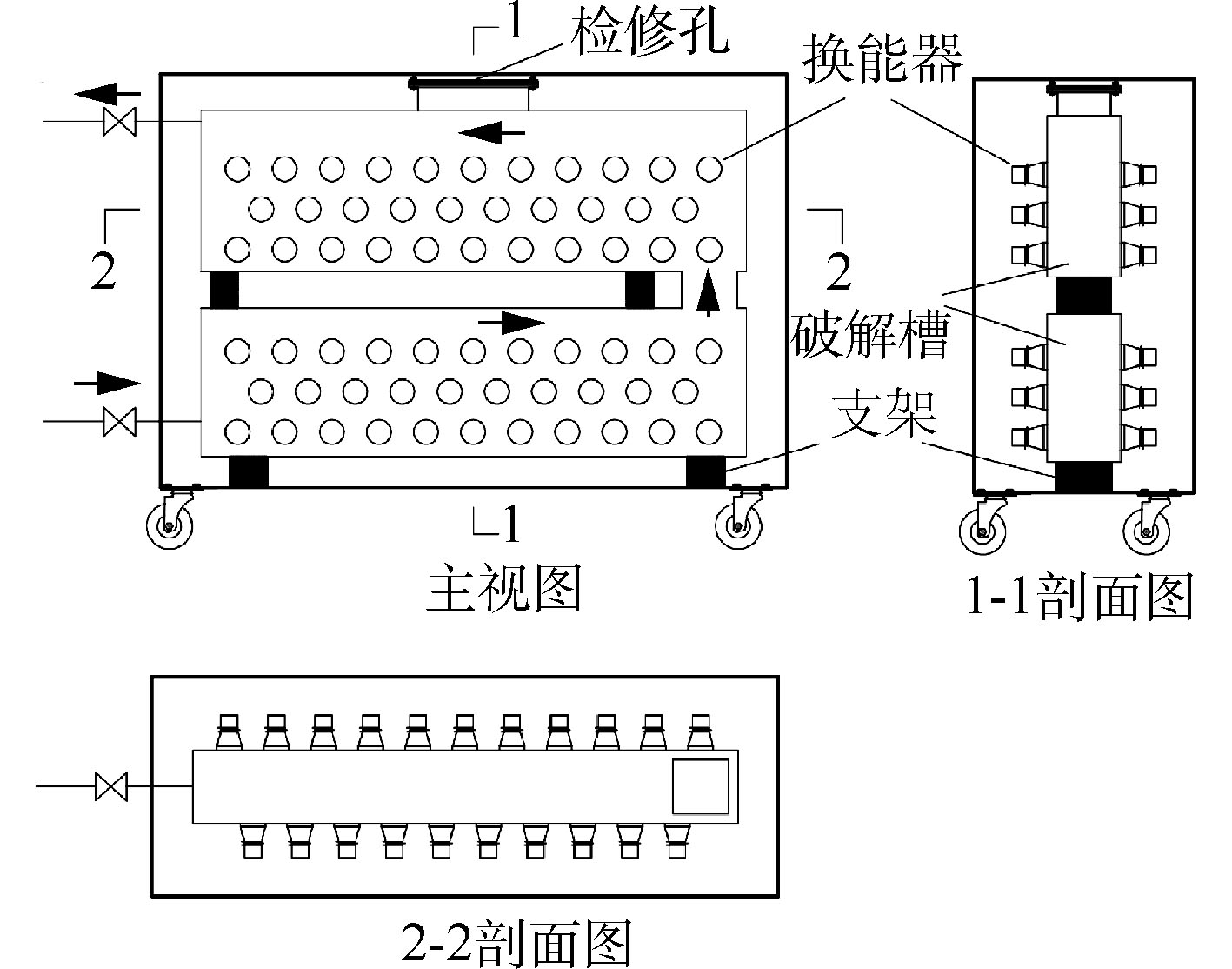
多探头槽式超声波反应器如图1所示。该超声波预处理设备主要由超声波换能器探头、超声波破解槽、超声波反应器箱体、超声波发生器、超声波发生器机柜和电缆线路系统组成。超声波破解槽体容积为250 L,总功率为10 kW。超声波换能器探头参数为20 kHz,100 W,按需求均匀错位布置于破解槽体两侧壁,反应器箱体设隔音棉环绕破解槽四周,破解槽和反应器箱体材料为304不锈钢,超声波发生器电源2台,分别使用电缆连接、控制左右两侧壁的探头,进行开闭,发生器电源功率数字显示实时超声波功率。
-
污泥在搅拌池内稀释搅拌TS至2%、4%、6%、8%、10%,之后泵入超声反应器内,工作时调整总输入功率为10 kW,设计4个污泥破解时间分别为15、30、45和60 min。破解方式为序批式,污泥加满反应器后,关闭进泥泵及反应器进出阀门,开启超声反应器,在运行15、30、45和60 min时取样监测。
-
厌氧消化实验采用全自动甲烷潜力测试系统(AMPTSⅡ,碧普(瑞典)有限公司),反应瓶体积650 mL,有效容积400 mL,混合投加泥按照基质和接种泥VS 2∶1的比例进行配比。投加污泥后,对瓶内通入氮气5 min以排出氧气。发酵温度稳定设置在37.5 ℃。沼气中CO2被100 mL瓶内80 mL 3 mol·L−1的NaOH所吸收,剩余的气体进入自动气体计量装置,每天的产气量数据会自动储存在自动化系统中,随时可以调出。
-
TS、VS、SCOD采用美国公共卫生协会推荐的标准方法[15]进行测定;溶解性多糖和总多糖采用蒽酮比色法[16-17]测定;溶解性蛋白质和总蛋白质采用Lowry法[17-18]测定;利用马尔文激光粒度仪(MasterSizer 2000,英国马尔文仪器有限公司)测定污泥粒径分布及平均粒径。
-
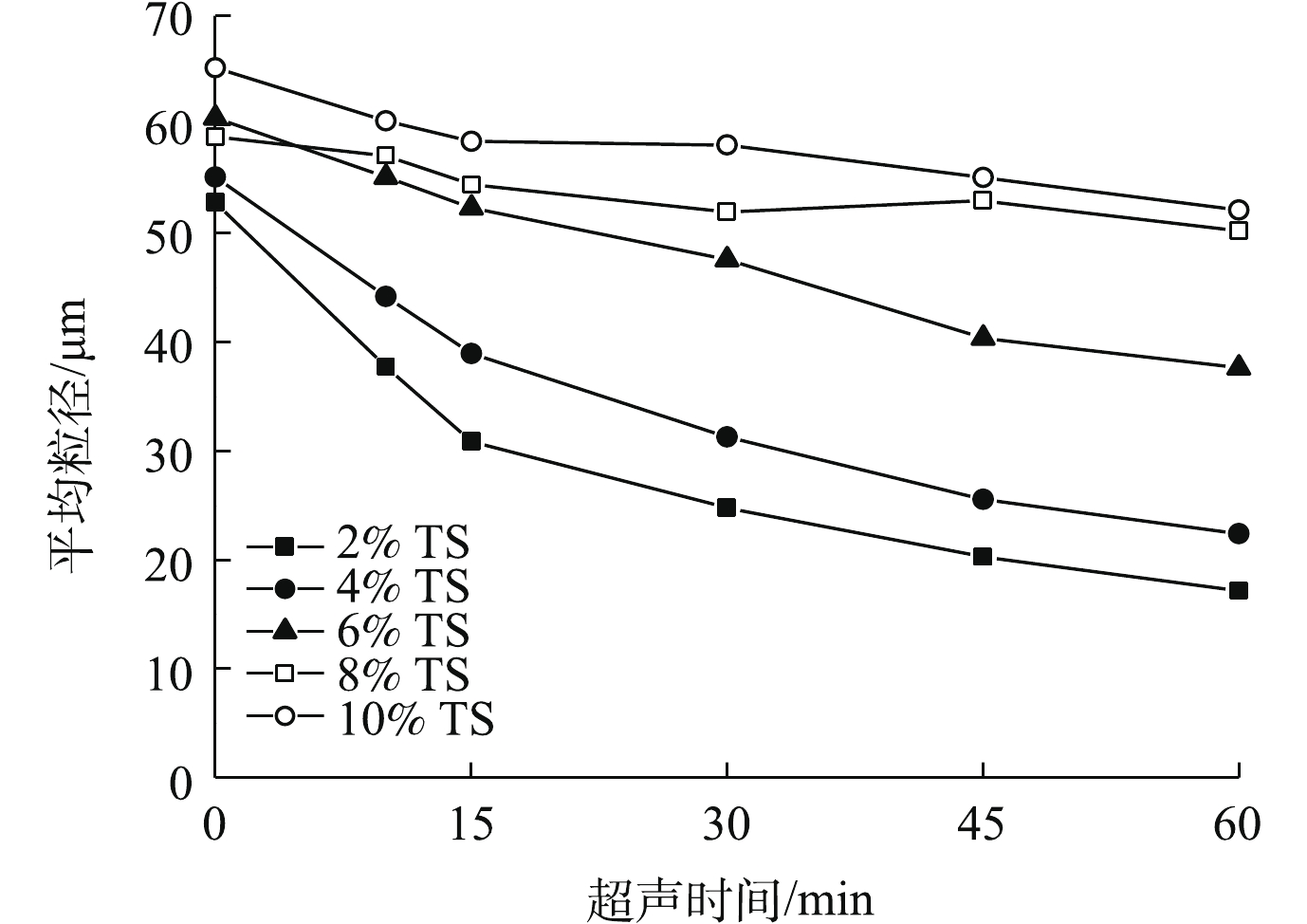
当超声破解污泥时,可以通过观测污泥中固体颗粒平均粒径的变化来分析其对污泥的破解效果。图2为不同TS污泥平均粒径随超声时间的变化情况。由图2可知,相比对照组污泥,60 min超声波破解时间条件下,2% TS和4% TS污泥的平均粒径分别由52.82 μm和55.17 μm降低至17.16 μm和22.39 μm,而6%、8%和10% TS的污泥降低幅度较小,分别由60.62、58.86和65.22 μm降低至37.66、50.22和52.14 μm。污泥粒径变小证实了超声波对污泥中的固体微粒进行了破解。在本研究中,低固体浓度和高固体浓度的污泥的粒径都有一定降低,不同的粒径变化反映了污泥不同的破解程度。对于TS在6%以上的污泥,超声波的大部分声能被固体物质所吸收,不能对污泥进行有效的破解;对于2% TS和4% TS的污泥,超声波可以对其污泥进行有效的破解,污泥中的絮体、微生物、固体颗粒和菌胶团被打散,有机物溶出,固体污泥粒径变小。
-
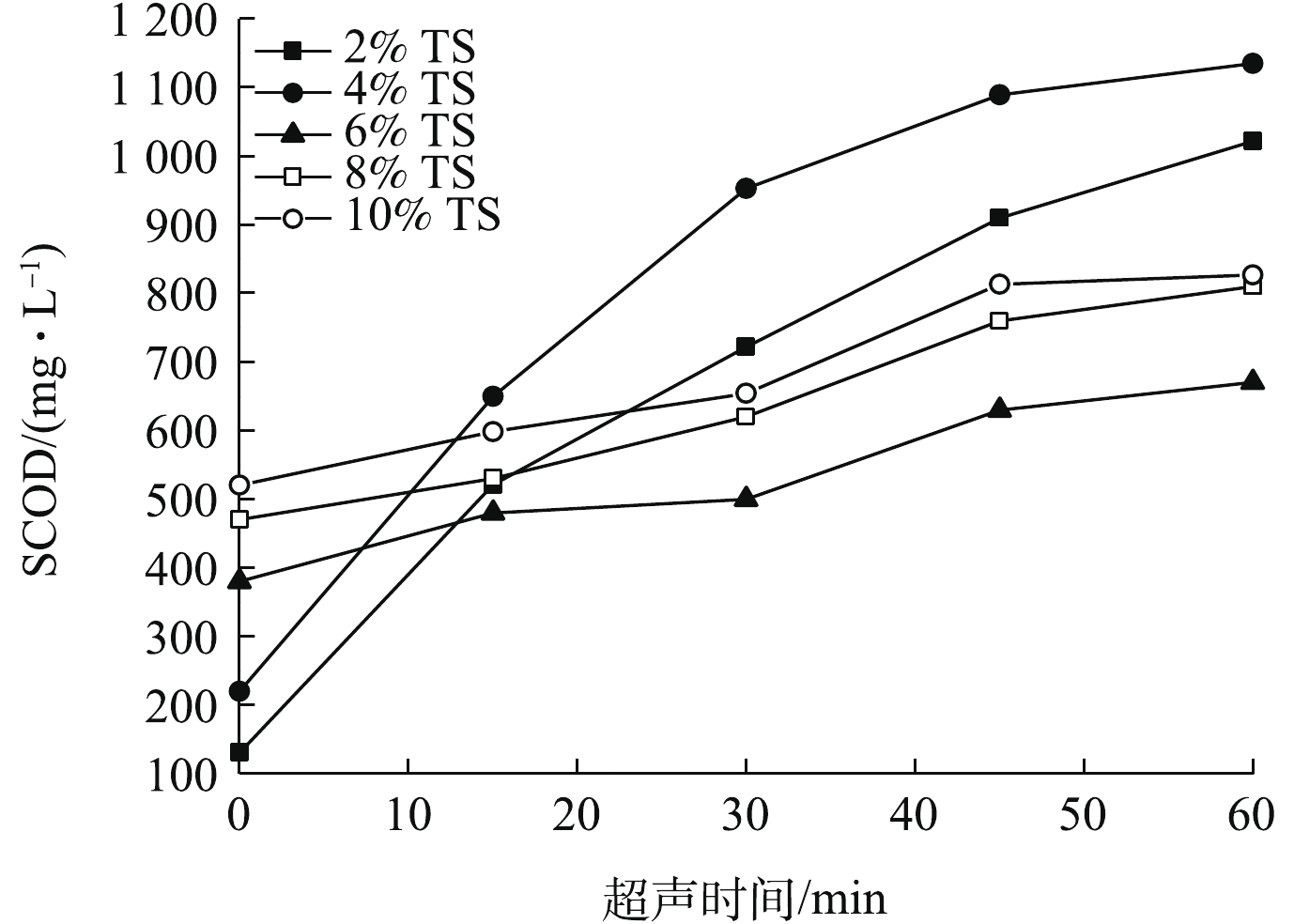
为进一步研究超声对污泥的破解程度,需要对污泥中耗氧类有机化合物(以COD计)、蛋白质、多糖的溶出情况进行测定分析。不同TS污泥超声波破解后,污泥SCOD随时间的变化如图3所示。由图3可知,随着污泥破解时间的延长,各不同比例TS下污泥SCOD均逐渐增加。当TS为2%和4%时,超声破解时间为30 min时,SCOD分别从130 mg·L−1和220 mg·L−1增加到722 mg·L−1和953 mg·L−1;超声破解时间增加至60 min,SCOD分别增长到1 022 mg·L−1和1 135 mg·L−1。当TS为6%、8%和10%时,SCOD随超声时间的增加而增加,超声破解时间增加到60 min,SCOD浓度从380、470和520 mg·L−1分别增长到670、810和827 mg·L−1。上述结果说明,超声对TS浓度2%和4%的污泥进行了有效的破解,前30 min内,破解效率较高,30 min后,SCOD增长速度明显变缓;超声波对4% TS的破解效果优于对2% TS污泥的破解效果;超声波对TS为6%、8%和10%的污泥破解效果较差,SCOD随超声时间的增加保持微弱的增加趋势。超声波对低固体浓度污泥破解效率高,但对高固体浓度的污泥破解效率较低。其主要原因是:对于较高浓度的污泥,超声波中的能量大部分被固体物质所吸收,故空化作用被衰减,达不到有效破解污泥的目的[19]。因此,利用超声波破解污泥时,宜选用TS浓度不高于4%的污泥。
-
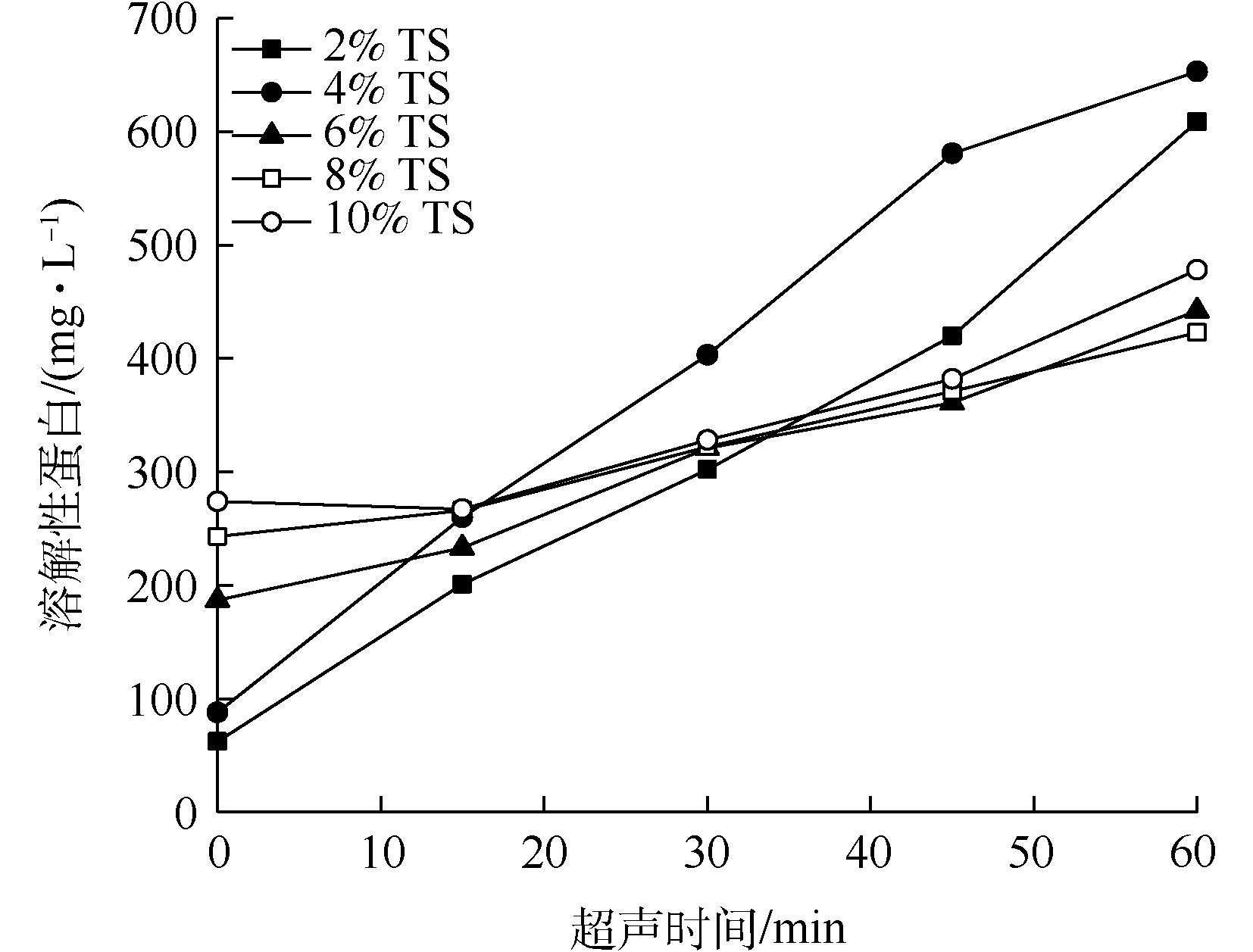
剩余污泥中的有机成分主要包括蛋白质、多糖和脂类,大部分的有机成分都被污泥中微生物细胞及胞外聚合物包裹,污泥被超声预处理以后,SCOD增加,这主要归因于蛋白质和多糖的溶出[7]。不同浓度的TS污泥被超声波破解后,溶解性蛋白质的浓度随超声时间的变化如图4所示。由图4可知,和SCOD溶出情况类似。当TS高于6%时,蛋白质溶出效果并不明显;当污泥TS为2%时,超声时间30 min和60 min条件下蛋白质浓度分别为302 mg·L−1和609 mg·L−1;当污泥TS为4%时,超声时间为30 min和60 min条件下蛋白质浓度分别为403 mg·L−1和653 mg·L−1。上述结果表明,超声波对6% TS或更高固体浓度污泥的蛋白质溶出效果不明显,当污泥TS在4%时,超声波对蛋白质破解效果优于TS为2%的污泥。
蛋白质是污泥有机物中的重要组成部分,在本研究中,对于TS浓度为2%和4%的污泥进行超声破解后,蛋白质溶出较明显。按照蛋白质的COD当量系数1.50 g·g−1[20]计算,60 min超声破解后,TS浓度为2%和4%的污泥溶出的蛋白质COD当量分别占溶出COD总量的89.3%和86.3%,以上结果证实了溶出物质的主要成分是蛋白质。
-
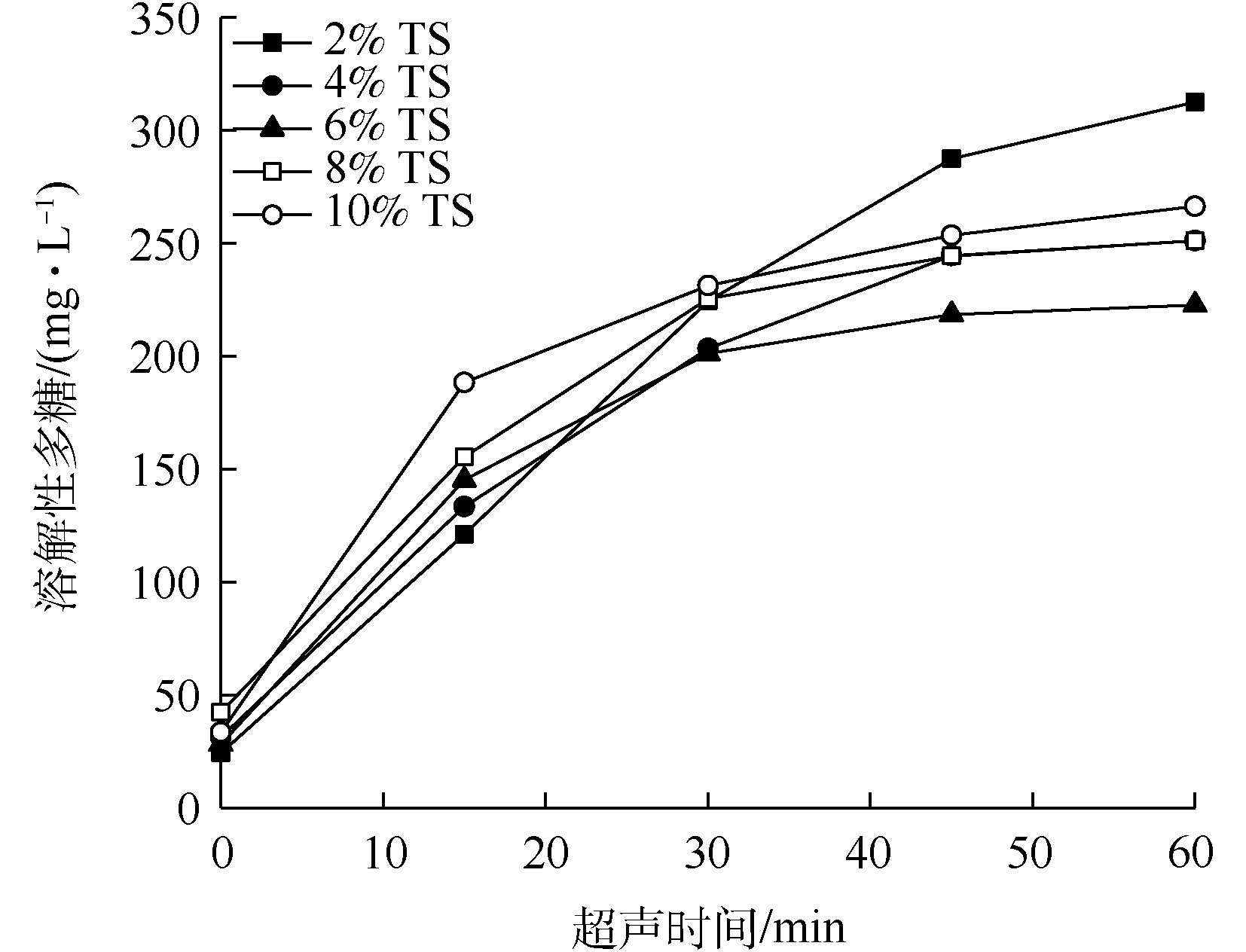
超声波破解不同浓度TS的污泥后,溶解性多糖浓度随超声时间的变化如图5所示。由图5可知,与COD及蛋白质的溶出情况不同,在30 min破解时间内,各浓度TS下的污泥溶解性多糖的溶出趋势较为相似,并无明显差别。在破解时间60 min后,2%、4%、6%、8%和10% TS污泥中溶解性多糖的浓度分别为312.4、251.1、222.7、251.2和266.3 mg·L−1。此结果表明,在本研究中,当超声波破解污泥时,超声波对污泥中多糖溶出效果有限。多糖溶出效果较差的原因可能是在本研究中所用的脱水污泥特性所致。
多糖同样是污泥有机物中的重要组成部分,在本研究中,按照多糖的COD当量系数1.07 g·g−1[20]计算,在60 min超声破解后,TS浓度2%、4%、6%、8%和10%污泥中溶解性多糖的COD当量分别占溶出COD总量的32.7%、23.7%、35.6%、33.2%和34.5%。因此,多糖也是污泥有机溶出物的主要成分,但在COD总量占比中,相比蛋白质较少。
-
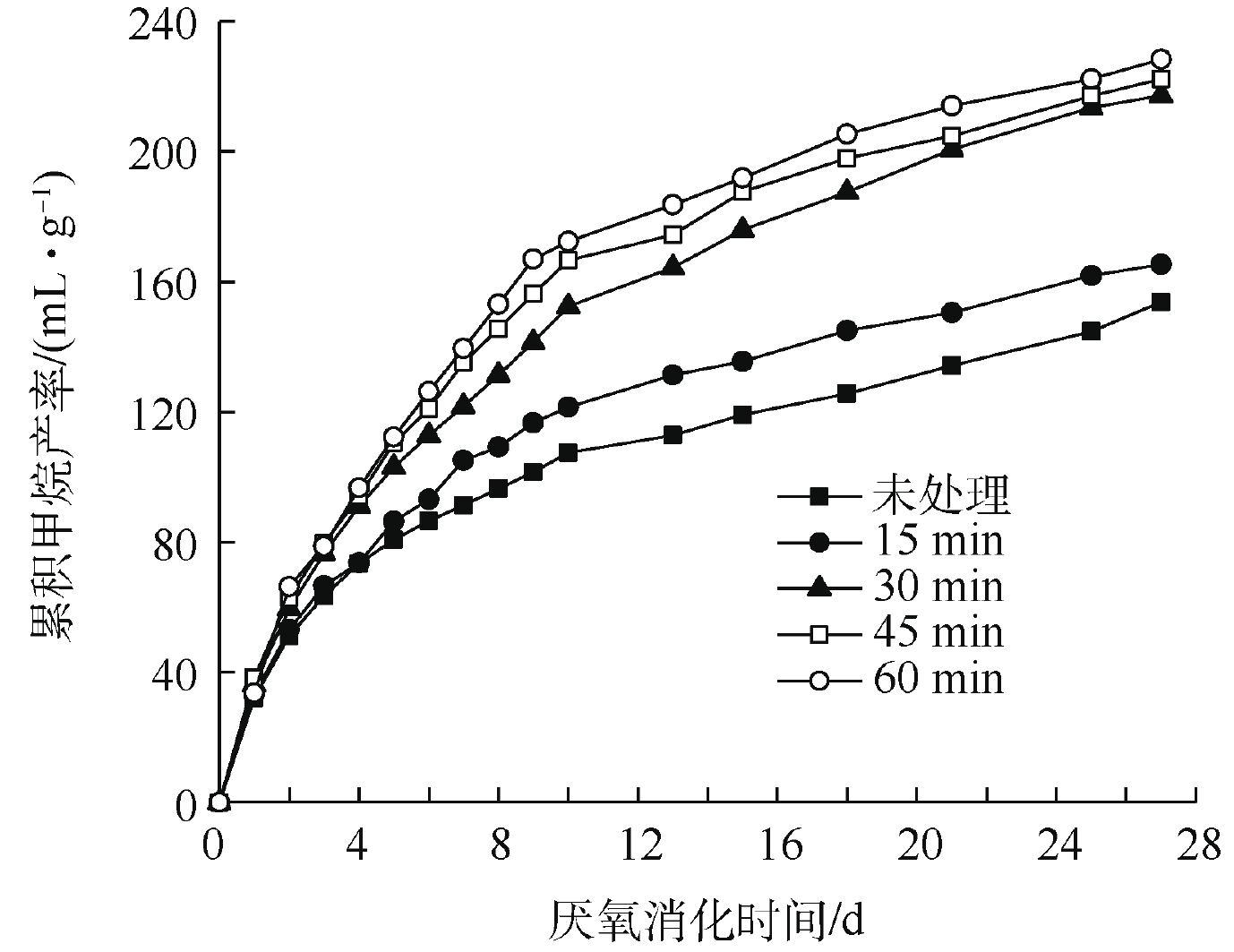
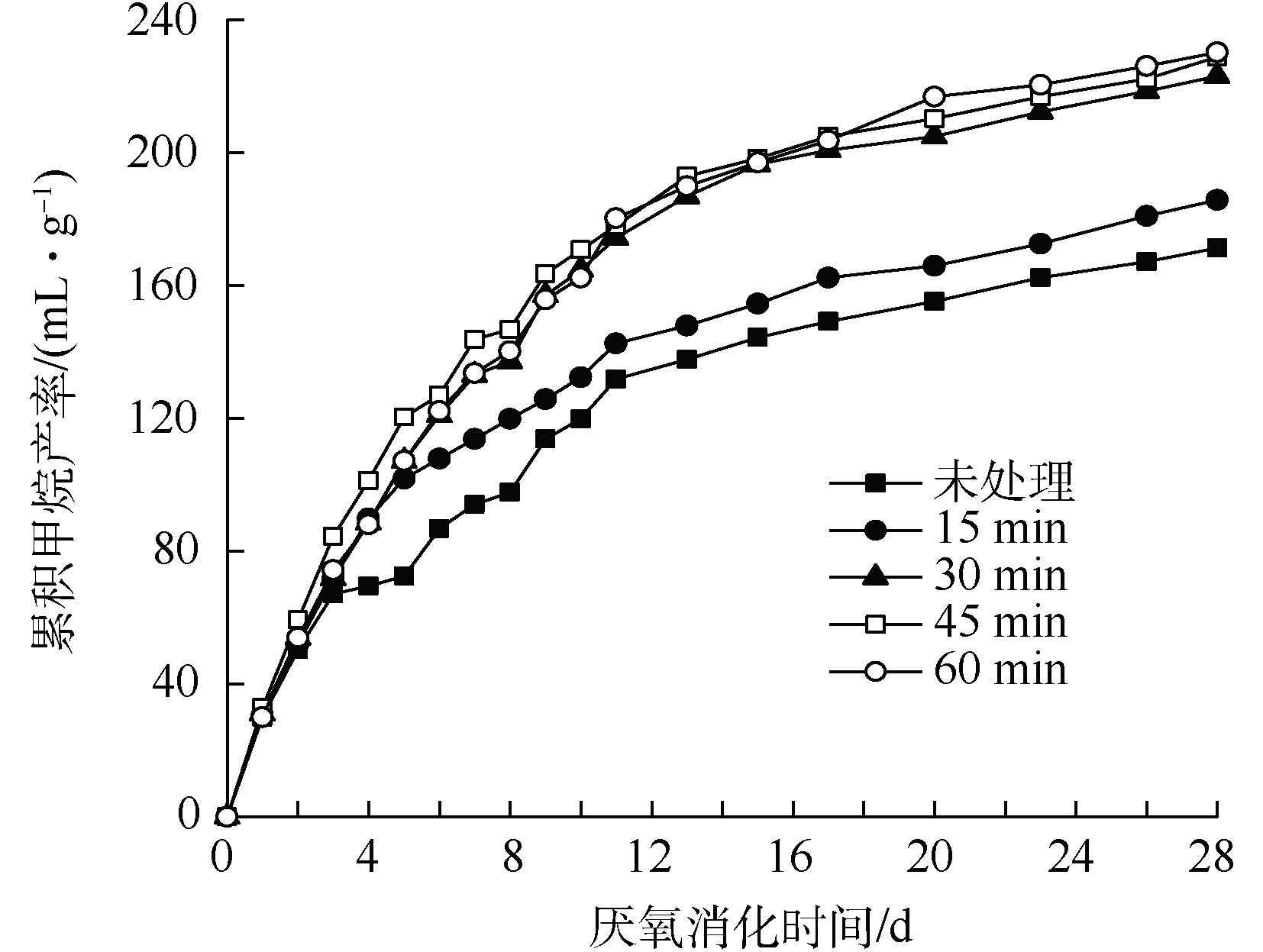
不同超声波破解时间下TS浓度2%污泥厌氧消化累积甲烷产率的变化如图6所示。由图6可知,在27 d厌氧消化过程中,厌氧消化累积甲烷产率随超声时间的增加逐渐升高。相比对照组污泥,15、30、45和60 min超声波预处理后,污泥预处理的累积甲烷产率分别增加了7.5%、41.2%、44.6%和48.5%;15 min超声波的破解时间对污泥甲烷产率增加量较小(增加了7.5%),30 min超声波破解时间下甲烷产率明显提升了41.2%,而破解时间的进一步增加对甲烷产率增加则有限。
结合前面对污泥有机物的溶出效果的研究结果,TS浓度为2%的污泥COD在60 min内几乎始终保持线性增加的趋势。然而,在评价累积甲烷产率时,30 min是有效提升甲烷产率的超声破解时间,30 min之后仅对甲烷产率有微弱提升。上述结果说明,COD的增加和甲烷产率的增加并不是绝对相关的,这和KIM等[21]的研究结果是一致的。超声波破解污泥时,较长的时间虽然会使有机物溶出浓度有一定增加,但是溶出的有机物中并不全是易生物降解的有机物,因此,超声时间对厌氧消化性能的改善也需要进行综合评估。
不同超声时间下TS浓度为4%的污泥厌氧消化过程中的累积甲烷产率如图7所示。由图7可知,随超声时间的增加,厌氧消化累积甲烷产率逐渐增加。相比对照组污泥,15、30、45和60 min超声波预处理后,污泥预处理的累积甲烷产率分别增加了8.4%、30.2%、33.6%和34.4%;相比未处理污泥,15 min超声波的破解时间对污泥甲烷产率仅增加了8.4%,30 min超声波对甲烷产率显著增加了30.2%,破解时间的继续增加对甲烷产率作用不明显。
当超声对TS浓度为4%的污泥进行破解时,前30 min超声破解时间下溶解性有机污染物的溶出量占60 min超声破解时间下溶解性有机污染物溶出量的90%,这说明30 min内对污泥破解已经达到了较高的程度,而30~60 min的超声破解对污泥COD溶出较少。上述结果说明,在低功率密度超声破解污泥时,延长时间并不意味COD溶出率和甲烷产率的增加,仍存在有效的破解时间范围,在该范围内进行超声波破解可以促进COD溶出率和甲烷产率增加,当超过该时间范围后对污泥厌氧消化改善不明显。因此,在实际应用中,需要对破解时间进行优化,根据需要选择最合适的破解时间,以获得更高的能量利用效率。
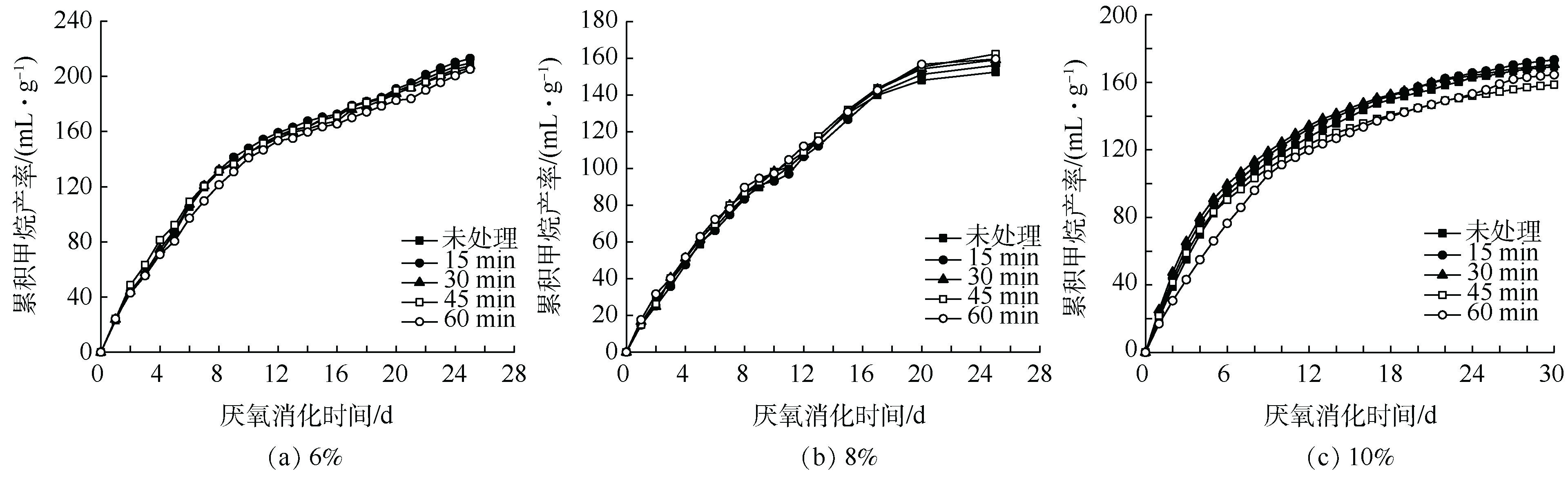
不同超声时间下,6% TS(图8(a))、8% TS(图8(b)和10% TS(图8(c)污泥厌氧消化过程中的累积甲烷产率如图8所示。相比对照组,随超声时间的增加,各浓度的TS下甲烷产率未见明显升高。因此,当TS为6%时,不但对COD、蛋白质和多糖破解溶出有限,对厌氧消化累积甲烷产量也没有明显改善。
由上述结果可知,在利用超声波预处理污泥时,要对污泥浓度、破解时间进行优化,选取最优的污泥浓度和超声波破解时间,以获得更好的破解效果和更高的能量利用效率。该多探头槽式超声波反应器破解污泥的最佳固体浓度条件是不高于4%,超声波破解时间是不超过30 min。
-
不同浓度的TS下,污泥厌氧消化后VS去除率随超声时间变化情况如表1所示。由表1可知,随固体浓度的增加,VS去除率呈现降低的趋势;而随超声时间的增加,VS去除率呈现升高的趋势。固体浓度越高,污泥厌氧消化后有机物去除率越低,该结果与FERNÁNDEZ等[22]的研究结果是一致的;超声波破解污泥后,2% TS和4% TS污泥的VS去除率相比对照组有明显提升,而6%和更高浓度TS的污泥VS去除率相比对照组提升并不明显,这与甲烷产率的结果是对应的;2% TS和4% TS污泥的VS去除率在超声破解时间为15 min时分别提升了1.84%和1.5%,在超声破解30 min时VS去除率分别提升了6.34%和8.92%,30 min之后VS去除率未见明显升高。上述结果说明,30 min内对污泥的破解更有效,继续延长时间对VS去除率提升并不明显。
在厌氧消化过程中,有机物被微生物代谢降解,转化为甲烷,因此,甲烷产率和VS去除率基本是一致的,与甲烷产量的改善情况一样,30 min破解时间对污泥厌氧消化VS去除率最有效。
-
1)随污泥固体浓度的增加,多探头槽式超声波反应器破解污泥的程度逐渐降低,污泥粒径降低幅度逐渐减缓,污泥中有机物溶出效果逐渐减弱。该多探头槽式超声波反应器破解污泥的最佳固体浓度条件为不高于4%。
2)对于TS浓度为2%和4%的污泥,随超声破解时间的延长,多探头槽式超声波反应器破解污泥的程度逐渐增加,污泥中溶解性有机物浓度逐渐增加,在30 min破解时间条件下,污泥甲烷产率分别提升了41.2%和30.2%,30 min后延长超声破解时间对厌氧消化性能改善影响较小。
3)对于TS浓度为2%和4%的污泥,多探头槽式超声波超声破解30 min时,VS去除率相比对照组分别提升了6.34%和8.92%。本研究为超声波破解污泥技术的工业化应用提供了理论依据。
工业化规模超声波预处理对不同固体浓度污泥厌氧消化性能的影响
Effect of full-scale ultrasonic pretreatment on anaerobic digestion performance of sludge with different solid concentrations
-
摘要: 针对活性污泥厌氧消化水解速率慢的问题,通过工业化规模超声波反应器对不同固体浓度污泥开展了破解研究。采用粒径分析及溶解性COD、蛋白质和多糖浓度监测的方法研究了超声波破解前后污泥物理化学特性的变化;评估了超声波破解对污泥厌氧消化产甲烷潜力及有机物降解规律的影响。结果表明:工业化规模超声波破解不同固体浓度污泥后,污泥粒径均有所降低,而溶解性COD、蛋白质和多糖的浓度均有增加;超声波对污泥的破解程度与破解时间和固体浓度有关,其随破解时间增加而增加,随污泥固体浓度增加而减弱;超声波破解固体浓度2%和4%的污泥30 min后,累积甲烷产率分别提升41.2%和30.2%,当破解时间和固体浓度进一步增加时,污泥甲烷产率无明显变化。本研究结果可为超声波破解污泥技术的工业化应用提供参考。Abstract: To resolve the problem of low hydrolysis rate of activated sludge during anaerobic digestion process, an industrial scale ultrasonic reactor was used to disintegrate excess sludge under different solid concentrations. The physical and chemical characters of sludge before and after ultrasonic disintegration were evaluated in terms of particle size, and soluble COD, protein, carbohydrate. Effects of ultrasonic disintegration on cumulative methane yield and organism decomposition during anaerobic digestion process were studied. The results indicated that with the pretreatment of ultrasonic operation, the particle size of sludge was reduced, while an obvious increase of the concentrations of SCOD, soluble protein and carbohydrate occurred. The disintegration degree increased with sonication time extension, and decreased with the increase of solid concentrations. After 30 min ultrasonic pretreatment of 2% and 4% TS sludge, their methane yield increased up to 41.2% and 30.2%, respectively. However, there was no obvious increase of methane yield as ultrasonic time and sludge TS further increased. Through above research, the results provide technological support for ultrasonic pretreatment at industrial scale.
-
Key words:
- full-scale /
- ultrasonic pretreatment /
- sludge pretreatment /
- activated sludge /
- anaerobic digestion
-
电芬顿法是芬顿法的分支,基于O2在阴极的二电子还原产生H2O2,并与溶液中添加的Fe2+发生芬顿反应产生强氧化性的羟基自由基·OH,从而氧化降解有机污染物。由于可方便地控制H2O2的连续生成,同时芬顿反应的产物Fe3+在阴极被还原为Fe2+,使Fe2+得以再生利用。相对于普通的芬顿法和其他的电化学方法,该方法所需Fe2+浓度小,高效、低能耗,且易于实现自动化控制[1-2]。
电芬顿法的技术瓶颈在于对氧的二电子还原需要具有高催化活性的阴极材料。碳材料因其化学稳定性高、价格低廉、易于表面修饰等优点而受到青睐。与传统的三维碳材料石墨等相比,由石墨剥离得到的二维材料石墨烯具有超高电导率、超大的比表面积、优异的导热和导电性等优点[3-4],是理想的电极基体材料。另一类纳米碳分支——碳量子点(CQDs),是一种主要由sp2/sp3杂化碳构成的零维碳纳米材料[5],直径通常小于10 nm,在其表面有丰富的官能团和边缘缺陷[6-7]。已有文献将CQDs结合于碳基电极表面用于电化学分析目的,显著提升了电极的电化学响应,显示CQDs具有明显的电化学催化活性[8-10]。另外,CQDs和掺氮碳量子点N-CQDs修饰的rGO复合电极也被用于电池、超级电容器等电能存储与转换材料以及光催化中[11-13]。CQDs零维的小尺寸、丰富的表面以及边缘缺陷等结构特性可能是其催化性能的来源[14]。但目前为止,尚未见到将CQDs修饰电极用于电化学催化降解污染物的报道。
基于零维CQDs和二维石墨烯材料的特性,本研究将合成的零维CQDs与制备的二维材料rGO结合,并载于石墨片(graphite flake,GF)表面制备了CQDs-rGO/GF复合电极,将该复合电极用在电芬顿法中做阴极材料,考察了由溶解氧二电子还原生成过氧化氢的情况。对硝基苯酚(PNP)是有毒性和生物蓄积性的苯酚衍生物[15],是制造药物、染料和农药等的原料,也是常用的皮革防腐剂,其结构稳定,不易生物降解。以PNP为目标污染物,考察了所制备的复合电极电芬顿体系对PNP的降解性能。
1. 材料与方法
1.1 试剂与仪器
分别以325目石墨粉(CP,河南义祥新材料有限公司)和葡萄糖(AR,天津科密欧化学试剂有限公司)为原料制备氧化石墨烯以及碳量子点,以石墨片(10 cm×2 cm,青岛宝丰石墨制品有限公司)为基体电极,以对硝基苯酚(AR,上海山浦化工有限公司)为目标污染物,以Nafion PFSA Polymer(质量分数为5.0%,美国杜邦公司)为制备电极的粘合剂,降解过程通入氧气(99.99%,腾龙化工有限公司,西安)。其余所用试剂均为分析纯。使用紫外可见分光光度计(Nicolet Evolution 300,美国尼高力仪器公司,美国)测量体系中过氧化氢和PNP的吸光度;使用荧光分光光度计(F97PRO,上海凌光技术有限公司)测定生成羟基自由基的相对含量,并对合成的电极材料进行表征;通过傅里叶红外光谱仪(IR-21,日本岛津公司)表征电极材料的官能团结构,TEM(JEM-F200,日本电子株式会社)表征材料的形貌结构;双显恒电位仪(DJS-292,上海雷兹新泾仪器有限公司)为电芬顿体系提供电源。
1.2 复合阴极的制备
氧化石墨烯由改进的Hummer’s法[16]制备。将325目石墨粉分散于浓硫酸中,于冰水浴中缓慢加入高锰酸钾并不断搅拌。加入超纯水和30% H2O2溶液终止反应。过滤洗涤后取沉淀于去离子水中超声,将所得悬浮液离心,收集棕黄色上清液并烘干,得到GO。将GO于去离子水超声至分散均匀后,加入85% N2H4·H2O,水浴24 h,用45 μm滤膜过滤洗涤,将滤渣烘干得黑色部分还原石墨烯rGO。
以葡萄糖为原料用水热法制备碳量子点[17],将葡萄糖水溶液装入反应釜,180 ℃下保温24 h。取出后冷却得浅黄色溶液,用45 μm滤膜过滤后,旋转蒸发得到凝胶状固体CQDs。取一定量CQDs凝胶状固体进行红外光谱和TEM检测。将一定量CQDs溶于水后测定紫外-可见吸收光谱和荧光光谱。
称取一定量的rGO和不同量的CQDs于烧杯中,加入N, N-二甲基甲酰胺(DMF)和5% Nafion试剂,搅拌并超声至均匀,制成一系列不同CQDs/rGO比例的均匀液体。将均匀液体涂抹在石墨片表面上(涂敷面积5.5 cm×2 cm,双面),于电热恒温干燥箱中160 ℃烘干30 min,即得到rGO/GF或CQDs-rGO/GF电极。
1.3 电芬顿体系的建立和降解实验
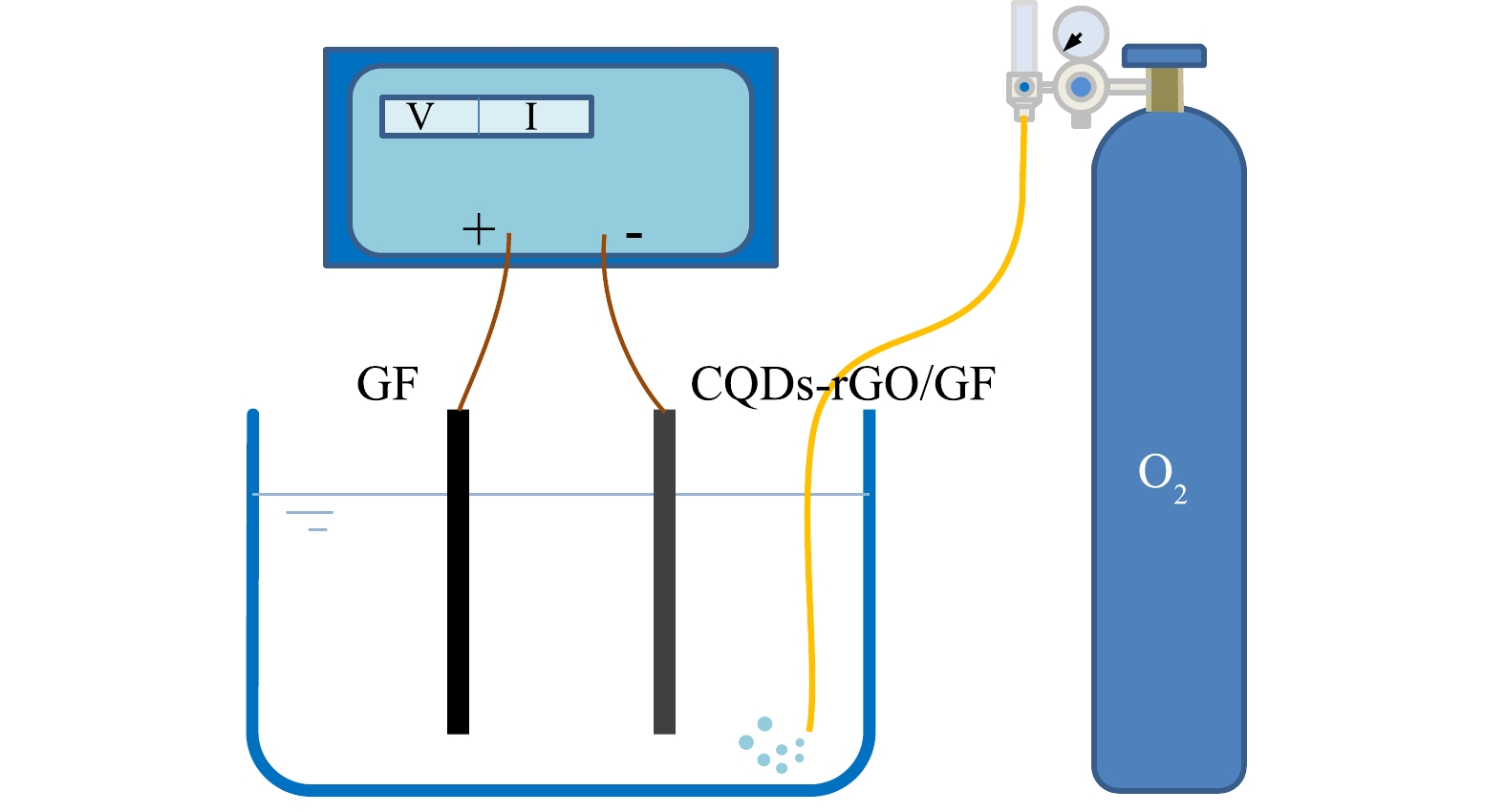
实验装置如图1所示,以双显恒电位仪为控制电源,以制备的电极为阴极,石墨片(100 mm×20 mm×2 mm)为阳极,在200 mL 0.050 mol·L−1的Na2SO4电解质溶液中,用稀H2SO4或NaOH调节pH,持续通入氧气,以恒电流电解方式使溶解氧还原生成过氧化氢。电解过程中每间隔15 min取样,用碘试剂法[18]测定生成的过氧化氢。
在电芬顿体系中加入初始溶度为240 mg·L−1的PNP,通氧条件下进行恒电流电解,每间隔15 min取样,以紫外-可见分光光度法检测PNP的浓度,以重铬酸钾法测定COD,计算其去除率,以邻二氮菲分光光度法测定溶液中Fe2+的浓度。所取样品中用盐酸羟胺还原Fe3+为Fe2+后测定二者的总浓度,并取二者差值为Fe3+浓度。
2. 结果与讨论
2.1 CQDs和rGO的表征
用TEM对CQDs固体的形貌和结构进行了表征。由图2可见,CQDs为直径不大于6 nm的零维点。HRTEM的表征结果表明,CQDs的晶面间距0.21 nm,对应于石墨相的(100)晶面[19-20]。
CQDs水溶液的紫外吸收光谱和荧光光谱如图3所示。其中,紫外吸收光谱显示CQDs在225 nm和280 nm处有强的吸收。由于葡萄糖分子本身没有紫外光吸收,该处吸收应该是石墨相CQDs的共轭C=C跃迁产生的。当激发波长为360 nm时,CQDs在480 nm发射较强的荧光,这是CQDs的显著特征,与文献报道的结果[21-22]一致。
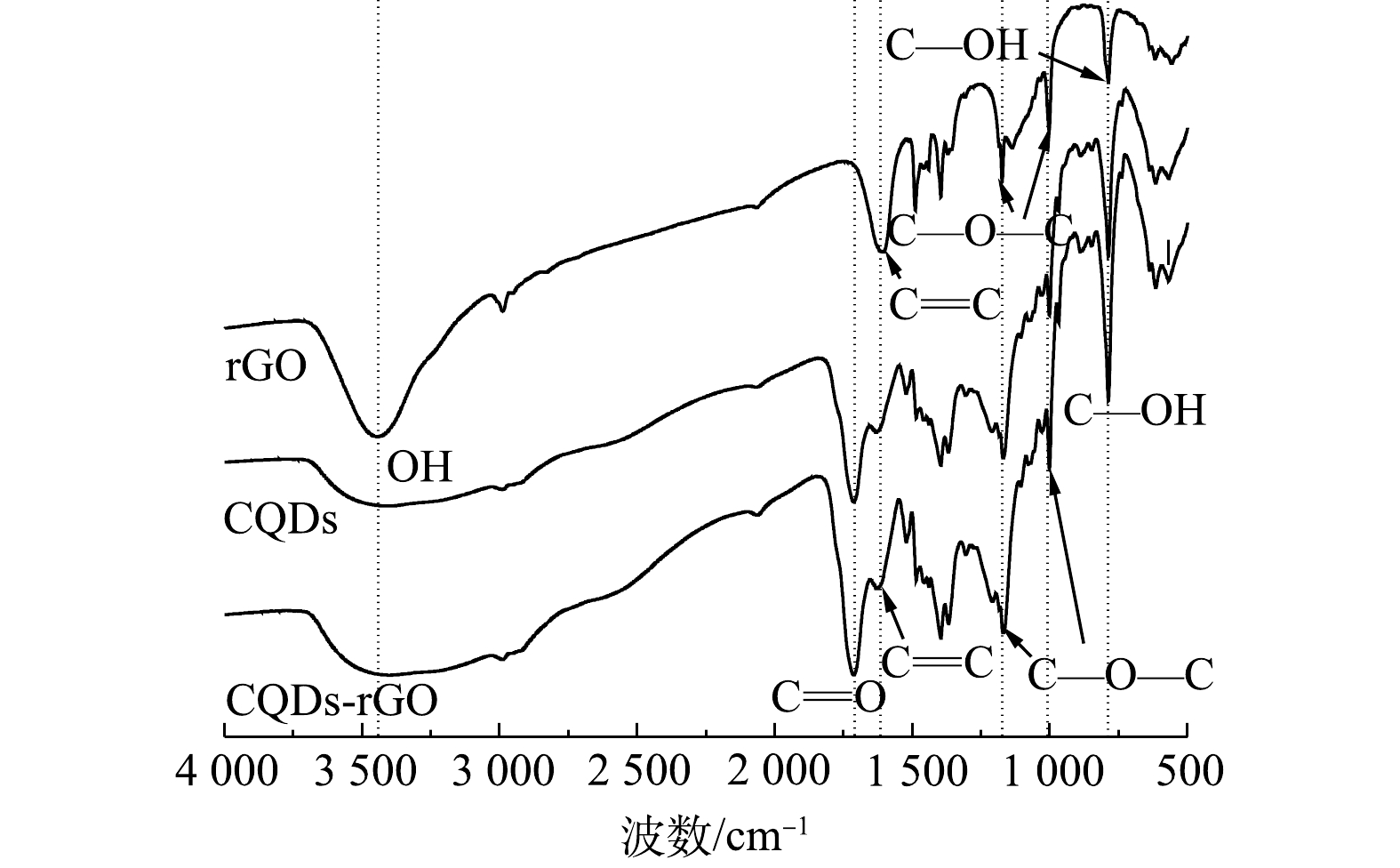
制备的CQDs的红外光谱如图4所示。CQDs在3 454、1 110、1 045 cm−1处的吸收峰分别对应于含氧基团O—H和C—OH的伸缩振动峰[23-24],在1 710 cm−1处有明显的C=O的伸缩振动峰[25],在1 653 cm−1处为C=C的伸缩振动吸收峰[26],在2 900 cm−1处的饱和C—H伸缩振动峰[27],这表明碳量子点结构中含有不饱和C=C、C=O和饱和CH等基团。这与已有研究结果一致,即在水热反应过程中,葡萄糖分子经过脱水、聚合、碳化和钝化过程,最终生成以石墨相C=C为内核,并有亲水的羟基和羰基等基团分布的零维量子点结构[28-29]。由图4还可知,rGO与CQDs有基本一致的红外光谱吸收谱图,只是在rGO中无C=O吸收峰,其他含氧官能团的强度也相对较弱。这表明制备的rGO以剥离的石墨为主要结构,但所制备的为微还原氧化石墨烯,仍然有一定量的含氧官能团[30],这部分含氧官能团有可能为结合CQDs提供位点,有利于CQDs在其表面的结合。复合材料rGO-CQDs的红外光谱显示,其C=O和C—OH吸收峰强度比CQDs明显有所降低,而C=C和C—O—C峰强度则变化不大,表明复合材料中CQDs与rGO可能以羧基和羟基等含氧官能团相结合。
由图5可见,由石墨剥离得到的GO和rGO均呈现卷曲的片状结构,但rGO的卷曲状态有所减弱,这可能是由于rGO的表面含氧官能团减少,其层间作用力减弱的缘故。当存在CQDs时,rGO的片状结构没有受到影响。
2.2 CQDs-rGO/GF阴极电生过氧化氢的性能
将制备的CQDs-rGO/GF电极用于电芬顿体系中做阴极,考察体系中电生过氧化氢的性能。分别考察了CQDs和rGO使用量、电解电流和溶液pH对过氧化氢生成量的影响,结果如图6所示。由图6(a)可见,相比于石墨片GF阴极,rGO/GF阴极体系中H2O2的生成量增大,当GF电极上rGO负载量达到3 mg 以上时,其对H2O2生成量的影响已不明显。因此,后续实验均取每片石墨片电极上5 mg rGO的负载量。随着CQDs的加入,CQDs-rGO/GF阴极体系中过氧化氢的生成量相比rGO/GF阴极显著增大。当CQDs的负载量由0 mg增大至50 mg时,过氧化氢的生成量由26.0 mg·L−1升高至48.2 mg·L−1;但当CQDs的负载量进一步增大至70 mg时,过氧化氢的生成量反而降低。这可能是由于过高的负载量会导致CQDs的聚集[11],影响电极的导电性,阻碍电极表面电子传递的结果。因此,CQDs-rGO/GF复合电极的最佳负载条件是50 mg CQDs和5 mg rGO。可见CQDs的存在显著改善了rGO/GF电极的性能,对氧的二电子还原生成过氧化氢的反应有明显的催化效果。
电解电流对过氧化氢生成量的影响结果如图6(b)所示。当控制电流密度分别由0.45 mA·cm−2升至0.91 mA·cm−2的过程中,H2O2生成量先增大后减小,在0.82 mA·cm−2时达到最大。适当提高电解电流会使更多的溶解氧在阴极还原生成过氧化氢,但过高的电解电流会使生成的过氧化氢在电极表面进一步还原,消耗生成的过氧化氢。溶液pH也是影响过氧化氢生成量的重要因素,不同pH下CQDs/rGO/GF阴极体系中过氧化氢的生成量的结果如图6(c)所示。当溶液pH为3.0时,体系中H2O2的产生量最大。随着pH由3.0升高至9.0,体系中H2O2的产生量则由48.2 mg·L−1降低至 31.53 mg·L−1。这是因为O2电化学还原生成H2O2的过程中有氢离子的参与,酸性条件对氧的电化学还原有利。综上所述,生成过氧化氢的最佳条件是:CQDs和rGO的负载量分别为50 mg和5 mg,电流密度为0.82 mA·cm−2,溶液pH为3.0。
2.3 CQDs/rGO/GF阴极电芬顿体系对PNP的降解
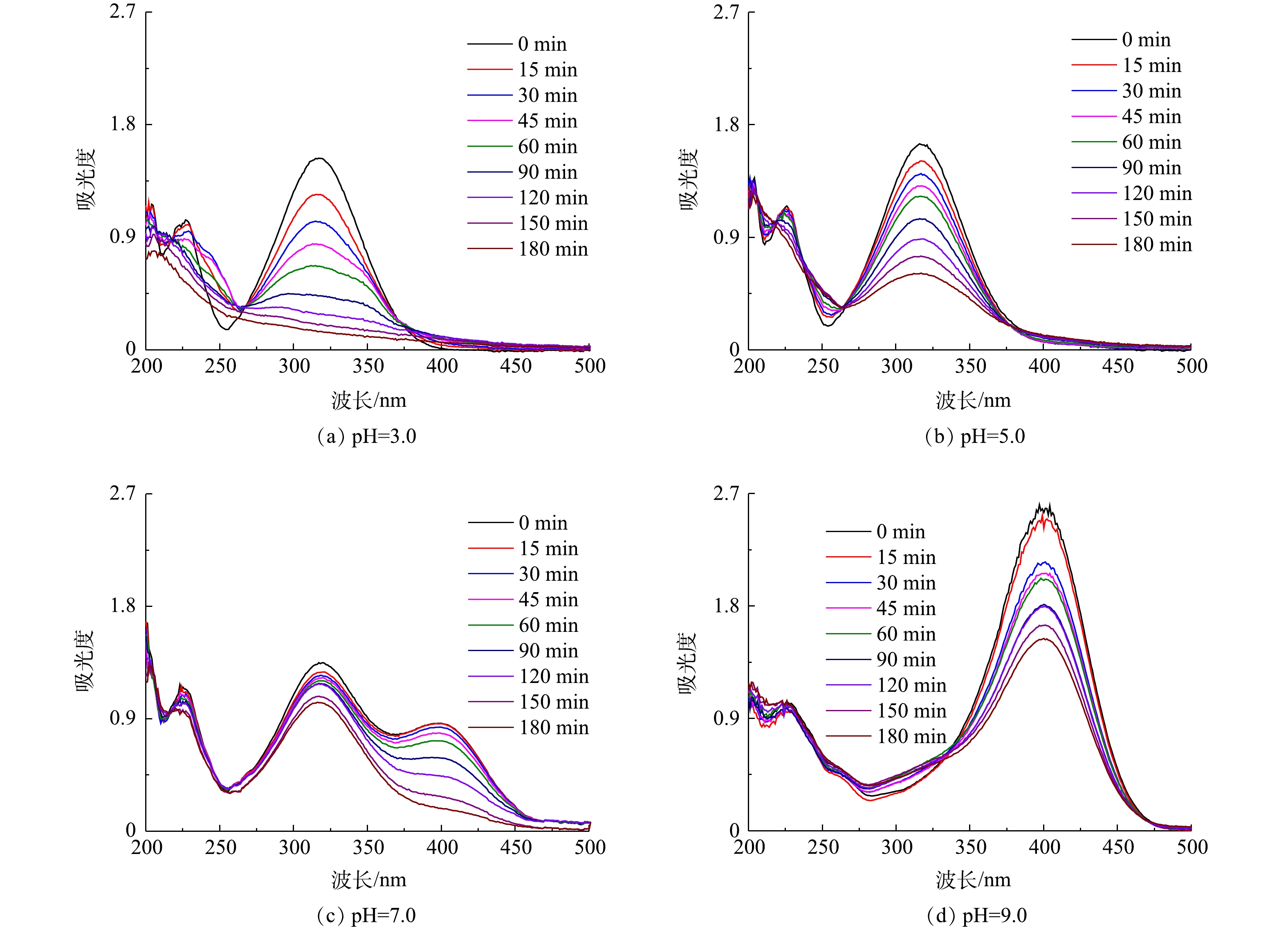
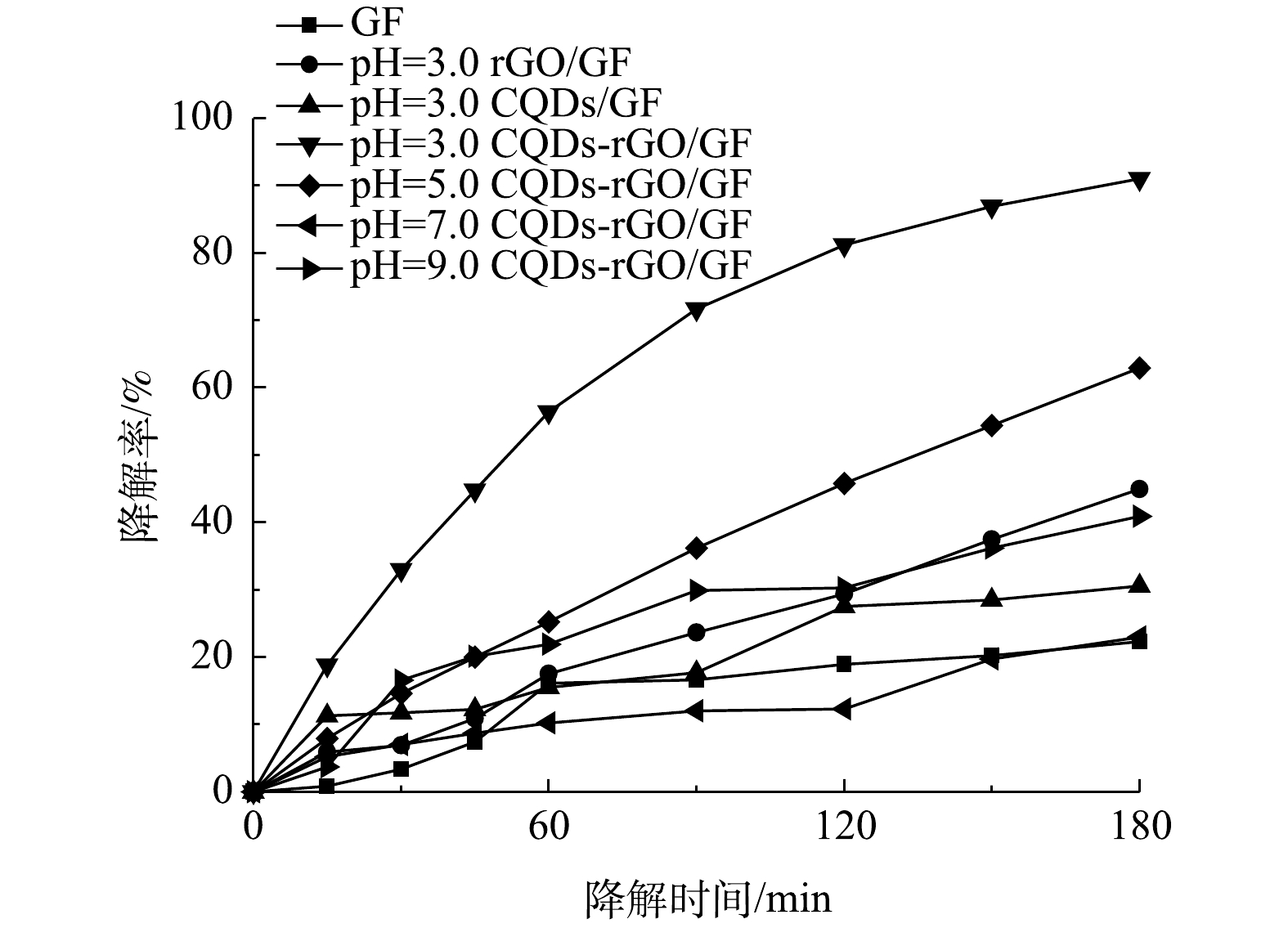
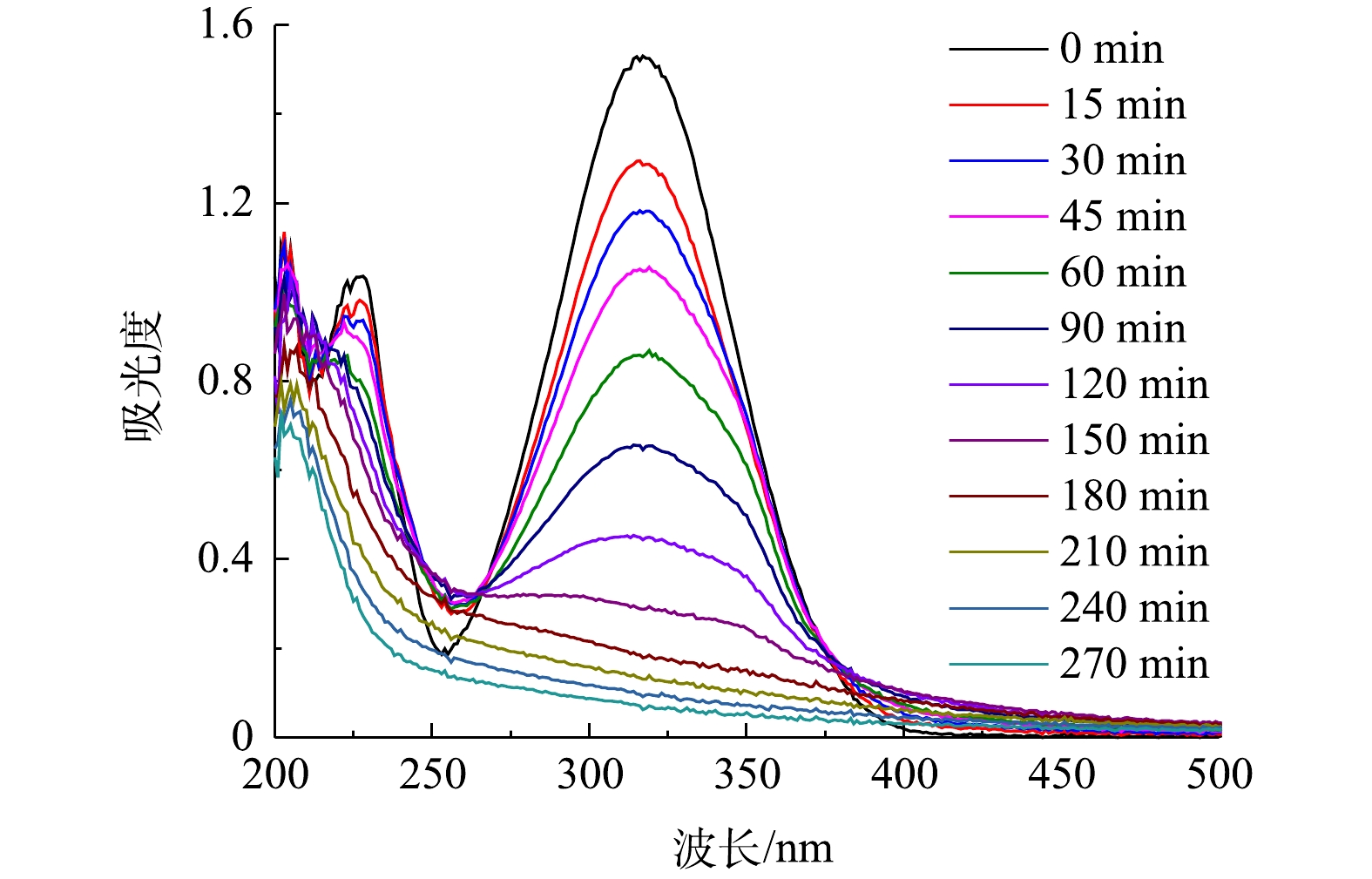
在电解液中加入Fe2+,与生成的H2O2构成芬顿体系,用以降解污染物PNP。首先考察了pH对PNP降解效果的影响。PNP为有机弱酸,pKa为7.14。在pH为7.0附近,其酸式体和碱式体将发生转化,这一结构变化清楚地体现在其紫外可见吸收光谱中。如图7(a)~(d)所示:在pH为3.0~5.0时,PNP以酸式的形式存在,其在226 nm和318 nm处的2个紫外吸收峰,分别对应于其结构中苯环的π-π*跃迁和苯环与助色团(—OH和—NO2)的n→π*跃迁[31-32];当pH增大至9.0时,其酚羟基质子解离,PNP以碱式体形式存在,氧负离子增大了硝基苯的电子密度,使吸收峰红移至401 nm处;在pH为7.0~9.0时,PNP以酸式体和碱式体共存。在降解过程中,通过PNP的紫外可见吸收光谱变化可清楚地看出PNP的降解过程。当pH为3.0时,随着电解时间的延长,PNP在226 nm和318 nm处的特征峰强度均明显降低;在pH为7.0和pH为9.0时,其226 nm处的吸收峰强度降低不明显,仅318 nm和401 nm处的吸收峰强度有所降低。为便于比较,在pH分别为3.0、5.0、7.0时以318 nm处的吸收峰强度为基准,计算电解180 min时PNP的降解率(图8),分别为91.0%、62.9%、23.1%。当pH为9.0时,以401 nm处的吸收峰为基准,计算PNP的降解率为40.9%。此外,比较了没有CQDs负载的rGO/GF电极和没有rGO的CQDs/GF电极在pH为3.0时对PNP的降解率。结果表明,rGO/GF和CQDs/GF电极对PNP的降解率均低于CQDs-rGO/GF电极,分别为45%和31%,表明CQDs的负载促进了PNP在rGO/GF电极上的降解,但CQDs对GF电极本身的作用不明显,CQDs与rGO可能存在协同作用。
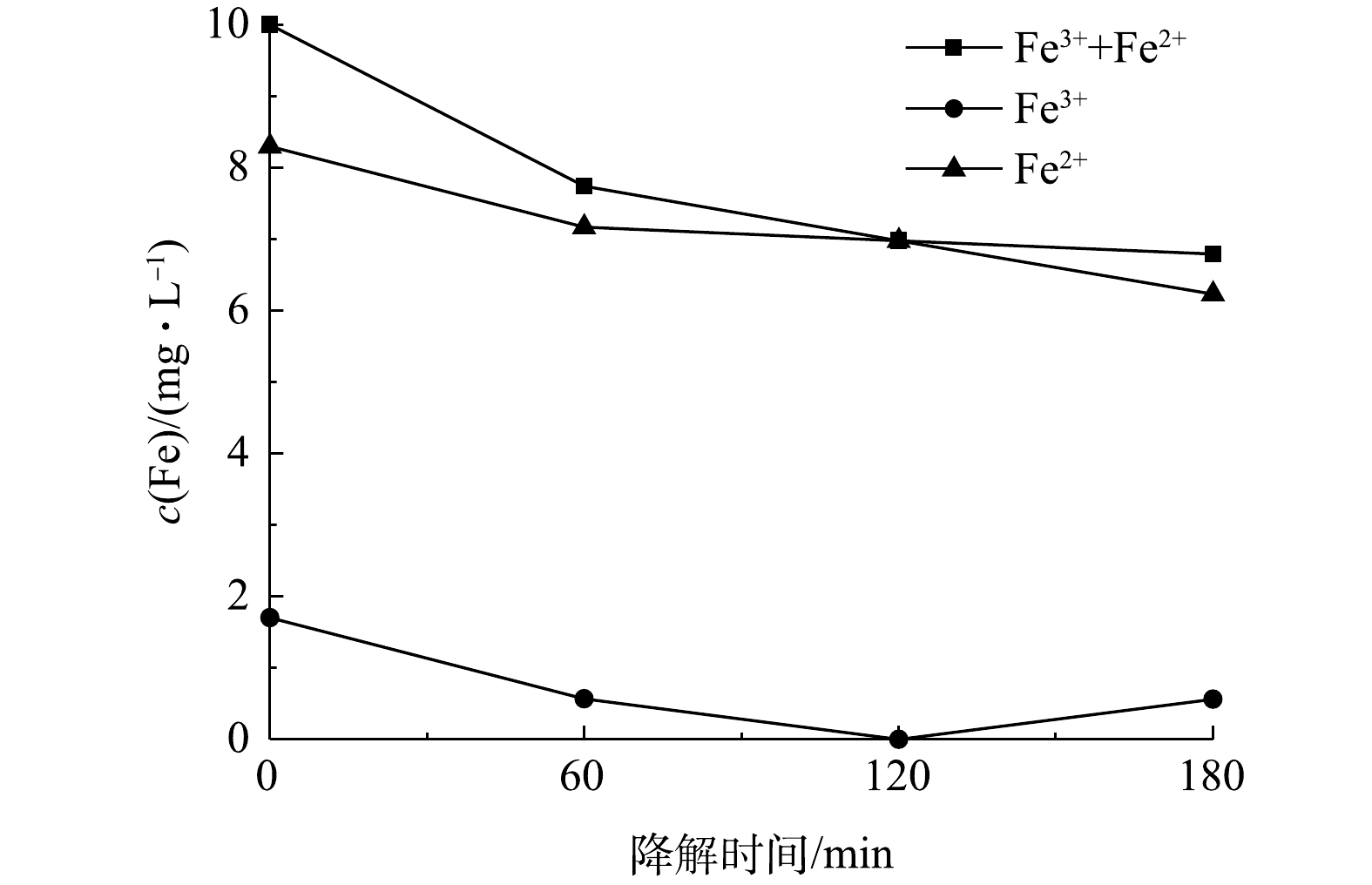
考察了Fe2+浓度对PNP降解效果的影响,结果如图9(a)所示。随着Fe2+浓度从2.5 mg·L−1增大至10 mg·L−1,PNP的降解率由64.2%升高至81.9%;继续增大Fe2+浓度至12.5 mg·L−1时,PNP的降解率反而减小。这是由于过高的Fe2+会与消耗芬顿反应产生的·OH的缘故。因此,后续实验采用的Fe2+浓度均为10 mg·L−1。此外,考察了电解电流对PNP降解率的影响,结果如图9(b)所示。随着电流密度由0.82 mA·cm−2增大至1.36 mA·cm−2,PNP的降解率逐渐提高至91.0%;继续提高电流,降解率反而降低。与生成H2O2的最佳电流密度0.82 mA·cm−2相比,电芬顿体系中PNP降解的最佳电流密度高很多。在电芬顿体系中,加入的Fe2+不断与生成的H2O2反应生成Fe3+,Fe3+会在阴极还原使Fe2+再生,形成Fe3+-Fe2+循环,保证了在较低的Fe2+浓度条件下的芬顿反应。同时,Fe3+的电化学还原也使电解回路中的电流增大,造成电芬顿体系中PNP降解的最佳电流密度高于没有Fe2+存在时过氧化氢生成的最佳电流。这一点可以从降解过程中溶液Fe2+和Fe3+浓度的变化(图10)得到证实。由图10可见,在整个降解过程中,Fe3+浓度维持在低于2 mg·L−1的水平,铁盐主要以Fe2+的形式存在,表明芬顿反应消耗的Fe2+可通过Fe3+在阴极的还原得到及时补充。由图10还可看到,随着电解时间的延长,溶液中的总铁浓度在120 min内稍有降低,之后则保持不变,这应该是少量铁盐吸附在电极表面的结果。但该浓度变化较小,对整个体系的性能影响不大。
为进一步验证该体系中·OH对降解PNP的作用,在溶液中加入·OH清除剂异丙醇,考察了异丙醇存在时PNP的降解情况。由于异丙醇与·OH的反应速率很快,二者的反应会造成以·OH为主要活性物种的电芬顿体系中污染物降解率的降低。如图9(c)所示,加入异丙醇后,PNP的降解明显受到抑制,180 min降解率由91.0% 降低至56.0%,这间接证实了·OH是该体系降解PNP的主要活性物种。
2.4 PNP可能的降解机理
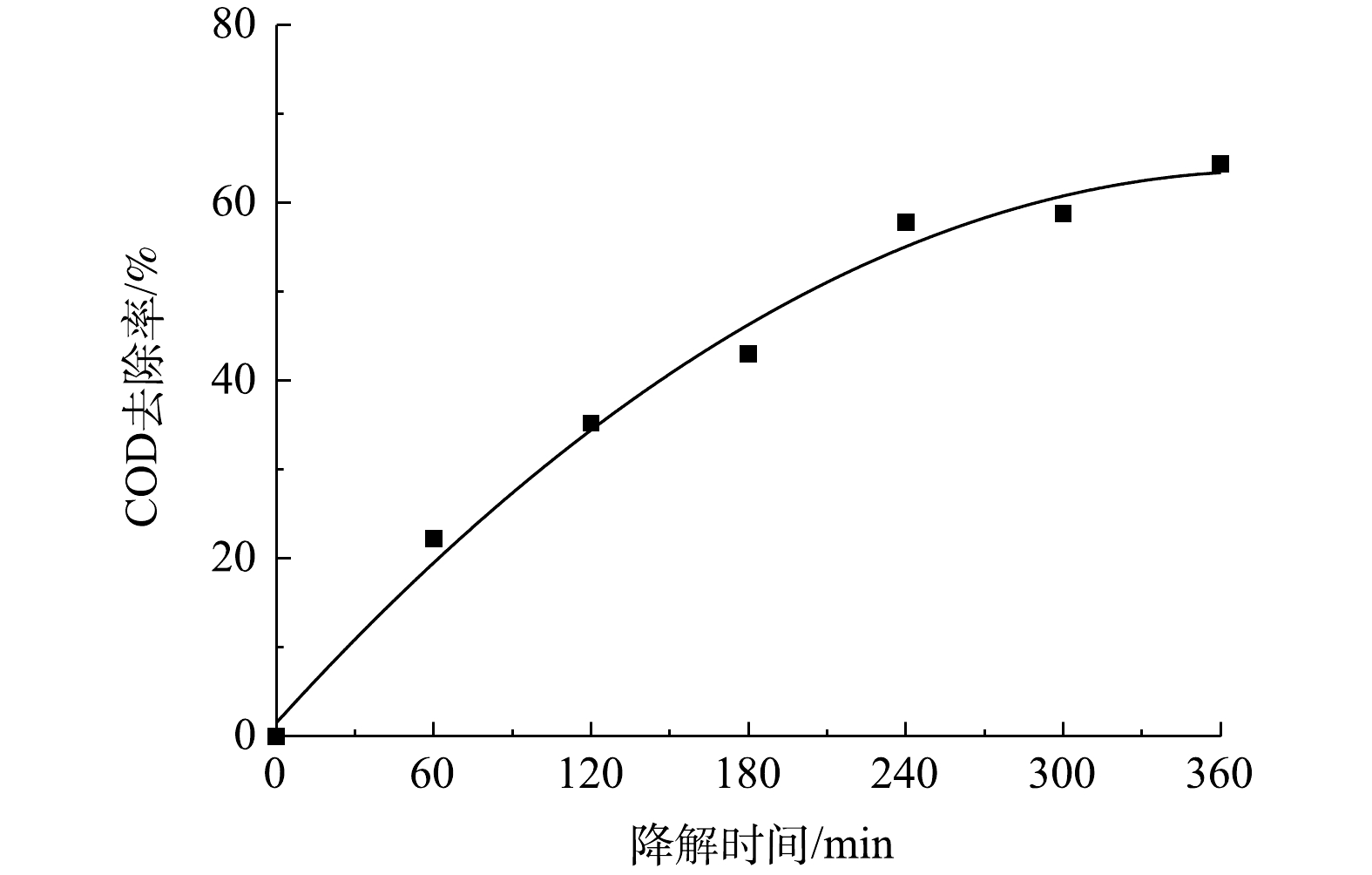
由以上实验结果和讨论可见,在CQDs-rGO/GF阴极电芬顿体系中,CQDs通过促进氧电化学还原生成过氧化氢而强化了羟基自由基的生成,该体系对PNP的降解是羟基自由基作用的结果。PNP的降解过程可由其紫外可见吸收光谱的变化清晰地体现。在最佳降解条件下,PNP的紫外可见吸收光谱变化如图11所示。降解过程中PNP的π→π*和n→π*跃迁吸收峰强度均降低直至消失,表明其共轭大π结构被破坏。但是,245~260 nm内的吸光度在电解150 min内逐渐增加,150 min至360 min时又降低至接近零。PNP本身在400~500 nm的可见光波长范围内没有吸收峰,表现为PNP溶液为无色。随着降解的进行,该范围内的吸光度值发生先增大后减小的变化,相应地观察到溶液颜色的改变。在0~150 min时,随着400~500 nm处吸光度的增大,溶液的颜色也由无色逐渐变为浅黄色,再进一步加深变为红棕色。在150~270 min时,这个波长范围内的吸光度开始减小直至为零,表现为溶液的红棕色逐渐变浅,最后转化为无色。这些现象表明,PNP在降解过程中有中间产物的生成。测定了PNP降解过程中COD的变化,如图12所示,结果显示COD去除率随降解时间的延长而逐渐增大,爱降解360 min时PNP溶液中的COD去除率达到64.3%,表明大部分的PNP被矿化分解,其余则被降解为非共轭的小分子有机物,在紫外谱图中表现为200~300 nm波长内尚有较弱的吸收。黄卫红等[33]利用GC/MS技术对PNP降解的中间产物进行了分析,认为主要中间产物有4-硝基儿茶酚、对苯二酚、对苯醌、丁二醇、丁酸和草酸。其中·OH攻击苯环上电子密度较大的碳原子,使PNP分子羟基化,生成4-硝基儿茶酚,进一步在羟基自由基的攻击下硝基脱离苯环,转化成对苯二酚,呈现棕黄色溶液。对苯二酚进而生成对苯醌的红棕色溶液。在羟基自由基作用下对苯醌开环生成丁二醇、丁酸、草酸等小分子有机酸,部分有机酸进一步降解为CO2和H2O,实现了PNP的矿化。这与PNP降解过程中其紫外可见光谱所呈现的变化结果是一致的,可见,在本文的电芬顿体系中,在电生·OH的作用下,PNP也经历了类似的降解过程,该降解过程可简单地用紫外可见吸收光谱进行表征。
3. 结论
1)将制备的粒径约5 nm的石墨相结构的CQDs,与二维材料石墨烯rGO结合得到了CQDs-rGO/GF复合电极,CQDs明显增强了电极的催化性能,该电极做阴极时O2的电化学还原产物H2O2的生成量是rGO/GF阴极的1.9倍,是空白GF阴极的2.4倍。
2)在Fe2+存在时的电芬顿体系对PNP有较好的降解效果,在pH为3.0、电流密度为1.36 mA·cm−2、Fe2+浓度为10 mg·L−1降解180 min时PNP的降解率达到91.0%,且羟基自由基是PNP降解过程中的主要活性物种。
3)在该电芬顿体系中360 min时PNP的COD去除率为64.3%。电解过程中PNP紫外可见吸收光谱的变化清晰地呈现了PNP的降解过程:PNP的共轭结构首先被破坏,生成中间产物,最终大部分中间产物被进一步降解为小分子有机物,进而实现了对大部分PNP的矿化和去除。
-
表 1 超声预处理后污泥VS去除率的变化
Table 1. Changes in VS removal of sludge after ultrasonic pretreatment
TS浓度/% VS去除率(对照组)/% VS去除率(超声处理)/% 超声15 min 超声30 min 超声45 min 超声60 min 2 34.83 36.67 41.17 40.68 42.61 4 33.52 35.02 42.44 41.70 42.94 6 32.11 33.74 32.08 34.21 31.04 8 28.54 30.01 29.62 29.55 28.42 10 28.27 27.32 29.09 30.62 28.33 -
[1] ZHANG L, DUAN H, YE L, et al. Increasing capacity of an anaerobic sludge digester through FNA pre-treatment of thickened waste activated sludge[J]. Water Research, 2019, 149: 406-413. doi: 10.1016/j.watres.2018.11.008 [2] 晏发春, 汪恂, 张雷, 等. 高温热水解预处理厌氧消化技术实例分析[J]. 中国给水排水, 2016, 32(18): 35-37. [3] ŞAHINKAYA S, SEVIMLI M F. Synergistic effects of sono-alkaline pretreatment on anaerobic biodegradability of waste activated sludge[J]. Journal of Industrial and Engineering Chemistry, 2013, 19(1): 197-206. [4] TIAN X, WANG C, TRZCINSKI A P, et al. Insights on the solubilization products after combined alkaline and ultrasonic pre-treatment of sewage sludge[J]. Journal of Environmental Sciences, 2015, 29: 97-105. doi: 10.1016/j.jes.2014.07.024 [5] 王平. 热水解厌氧消化工艺的分析和应用探讨[J]. 给水排水, 2015, 3(1): 33-38. doi: 10.3969/j.issn.1002-8471.2015.01.008 [6] PILLI S, YAN S, TYAGI R D, et al. Anaerobic digestion of ultrasonicated sludge at different solids concentrations-computation of mass-energy balance and greenhouse gas emissions[J]. Journal of Environmental Management, 2016, 166: 374-386. [7] ZHANG B, JI M, WANG F, et al. Damage of EPS and cell structures and improvement of high-solid anaerobic digestion of sewage sludge by combined (Ca(OH)2 + multiple-transducer ultrasonic) pretreatment[J]. RSC Advances, 2017, 7(37): 22706-22714. doi: 10.1039/C7RA01060E [8] GONZALEZ A, HENDRIKS A, VAN L, et al. Pre-treatments to enhance the biodegradability of waste activated sludge: Elucidating the rate limiting step[J]. Biotechnology Advances, 2018, 36(5): 1434-1469. doi: 10.1016/j.biotechadv.2018.06.001 [9] PILLI S, YAN S, LEBLANC R, et al. Ultrasonic pretreatment of sludge: A review[J]. Ultrasonics Sonochemistry, 2011, 18(1): 1-18. doi: 10.1016/j.ultsonch.2010.02.014 [10] NICKEL K, NEIS U. Ultrasonic disintegration of biosolids for improved biodegradation[J]. Ultrasonics Sonochemistry, 2007, 14(4): 450-455. doi: 10.1016/j.ultsonch.2006.10.012 [11] GOGATE P, SIVAKUMAR M, PANDIT A. Destruction of rhodamine B using novel sonochemical reactor with capacity of 7.5 L[J]. Separation and Purification Technology, 2004, 34(1/2/3): 13-24. [12] GOGATE P, MUJUMDAR S, PANDIT A. Sonochemical reactors for waste water treatment: Comparison using formic acid degradation as a model reaction[J]. Advances in Environmental Research, 2003, 7(2): 283-299. doi: 10.1016/S1093-0191(01)00133-2 [13] GOGATE P, SUTKAR V, PANDIT A. Sonochemical reactors: Important design and scale up considerations with a special emphasis on heterogeneous systems[J]. Chemical Engineering Journal, 2011, 166(3): 1066-1082. doi: 10.1016/j.cej.2010.11.069 [14] ASGHARZADEHAHMADI S, ABDULRAMAN A, PARTHASARATHY R, et al. Sonochemical reactors: Review on features, advantages and limitations[J]. Renewable and Sustainable Energy Reviews, 2016, 63: 302-314. doi: 10.1016/j.rser.2016.05.030 [15] American Public Health Association. Standard Methods for the Examination of Water and Wastewater[M]. Washington D C: American Public Health Association, 1995. [16] GAUDY A F. Colorimetric determination of protein and carbohydrate[J]. Industrial Water Wastes, 1962, 7: 17-22. [17] JIMENEZ J, VEDRENNE F, DENIS C, et al. A statistical comparison of protein and carbohydrate characterisation methodology applied on sewage sludge samples[J]. Water Research, 2013, 47(5): 1751-1762. doi: 10.1016/j.watres.2012.11.052 [18] LOWRY O H, ROSEBROUGH N J, FARR A L, et al. Protein measurement with the Folin phenol reagent[J]. Journal of Biological Chemistry, 1951, 193(1): 265-275. [19] TYAGI V, LO S, APPELS L, et al. Ultrasonic treatment of waste sludge: A review on mechanisms and applications[J]. Critical Reviews in Environmental Science and Technology, 2014, 44(11): 1220-1288. doi: 10.1080/10643389.2013.763587 [20] JIANG S, CHEN Y, ZHOU Q. Effect of sodium dodecyl sulfate on waste activated sludge hydrolysis and acidification[J]. Chemical Engineering Journal, 2007, 132(1/2/3): 311-317. [21] KIM D, CHO S, LEE M, et al. Increased solubilization of excess sludge does not always result in enhanced anaerobic digestion efficiency[J]. Bioresource Technology, 2013, 143: 660-664. doi: 10.1016/j.biortech.2013.06.058 [22] FERNÁNDEZ J, PÉREZ M, ROMERO L I. Kinetics of mesophilic anaerobic digestion of the organic fraction of municipal solid waste: Influence of initial total solid concentration[J]. Bioresource Technology, 2010, 101(16): 6322-6328. doi: 10.1016/j.biortech.2010.03.046 -




 下载:
下载: