-
污泥是污水处理中的副产品,近年来我国污泥产量持续增长[1]。污泥脱水处理是实现剩余污泥稳定化、减量化和无害化的重要措施[2-3],但脱水后产生的滤液水质成分复杂,逐渐成为污水处理厂(wastewater treatment plant, WWTP)的二次污染源[4],国内外对此类废水还未有深入研究。关于污泥脱水滤液的处理,通常采用将其直接回流到生物处理单元重新参与处理[5]。脱水滤液中富集着大量的有机污染物和无机污染物,其中,也存在大量的氮磷等元素[6]。已有研究主要关注污泥脱水滤液中的有机污染物、无机氮磷以及重金属等[7],关于滤液中有机磷(organic phosphorus, OP)的污染问题却鲜有相关研究。
污水中磷的深度去除成为近年来污水处理领域的研究重点,但现有技术对特殊含磷废水的去除效果有限。因此,通过磷组分分析强化除磷已成为有效方法,而磷组分及存在形式的研究是表征其污染特征的关键。相关研究结果表明,污水中的磷以无机磷(inorganic phosphorus, IP)和OP的形态存在,而IP分为poly-P和
PO3−4-P ,poly-P主要包括焦磷酸盐、偏磷酸盐等[8]。在市政污水处理厂中,poly-P含量一般较低,PO3−4-P 可以在生物除磷和化学除磷的协同作用下实现极限去除[9],但针对OP污染及强化去除问题的研究相对较少。LIU等[10]利用藻类生物测定法提出了OP生物利用度,其代表污水中易于微生物利用的OP比例。LI等[11]利用藻类生长曲线法研究亲疏水性OP的生物利用度,发现疏水性OP更易被藻类等微生物利用,进而促进出水中磷的去除。微生物首先通过碱性磷酸酶将污水中有机磷水解为PO3−4-P ,而后以poly-P的形式储存于胞内[12]。在先前的研究中,常使用藻类生物测定法确定微生物对有机磷等底物的生物利用度[13],但这种方法存在实验周期长、可操作性差的弊端。因此,本研究使用活性污泥作为实验对象,研究OP在生物处理过程的水相和泥相中的迁移和转化规律,从而从活性污泥的角度来阐述OP的生物利用度。针对OP的强化去除,高级氧化技术是较为可行的处理方式。O3氧化是污水处理厂常规消毒措施,宋淑静等[14]研究表明,臭氧氧化法对污水中有机磷具有较好的降解作用,OP的去除率为78.46%。因此,研究在适当的O3和O3/H2O2氧化条件下,对污泥脱水滤液中有机磷的强化去除对于污水处理厂实现总磷超低排放具有现实意义。本研究从WX-A污泥脱水滤液OP的污染特征及强化去除2个方面出发,阐述了OP的分布特性、亲水和疏水特性、生物利用度和组分构成等污染特征,分析水质特性以评价传统回流处理对污水处理厂运行的影响,并针对性地开展基于O3和O3/H2O2氧化技术的有机磷深度去除技术研究,为污水处理厂实现总磷超低排放提供参考。
-
选取位于无锡市的三座市政污水处理厂作为研究对象,编号分别为WX-A、WX-B和WX-C。WX-A和WX-B进水中工业废水水量占比均为25%,WX-C的占比达60%以上。WX-A的剩余污泥投加FeCl3和石灰协同调理后,经板框压滤完成脱水处理;WX-B和WX-C的剩余污泥投加PAM调理后,再经板框压滤完成脱水过程。实验样品均采用棕色玻璃瓶收集,经0.45 μm的无机纤维膜过滤后,避光保存在4 ℃条件下,并尽快完成相关水质指标测试。具体水质指标见表1。其中,WX-A的脱水滤液水质存在异常,OP含量明显过高,WX-B和WX-C脱水滤液OP浓度则较低,处于正常水平;OP含量存在较大的差异性,这可能与WX-A上游工业企业较多、进水波动性大以及污泥来源较为复杂有关。本研究以WX-A为对象开展脱水滤液中OP的污染特性和深度处理的研究。
-
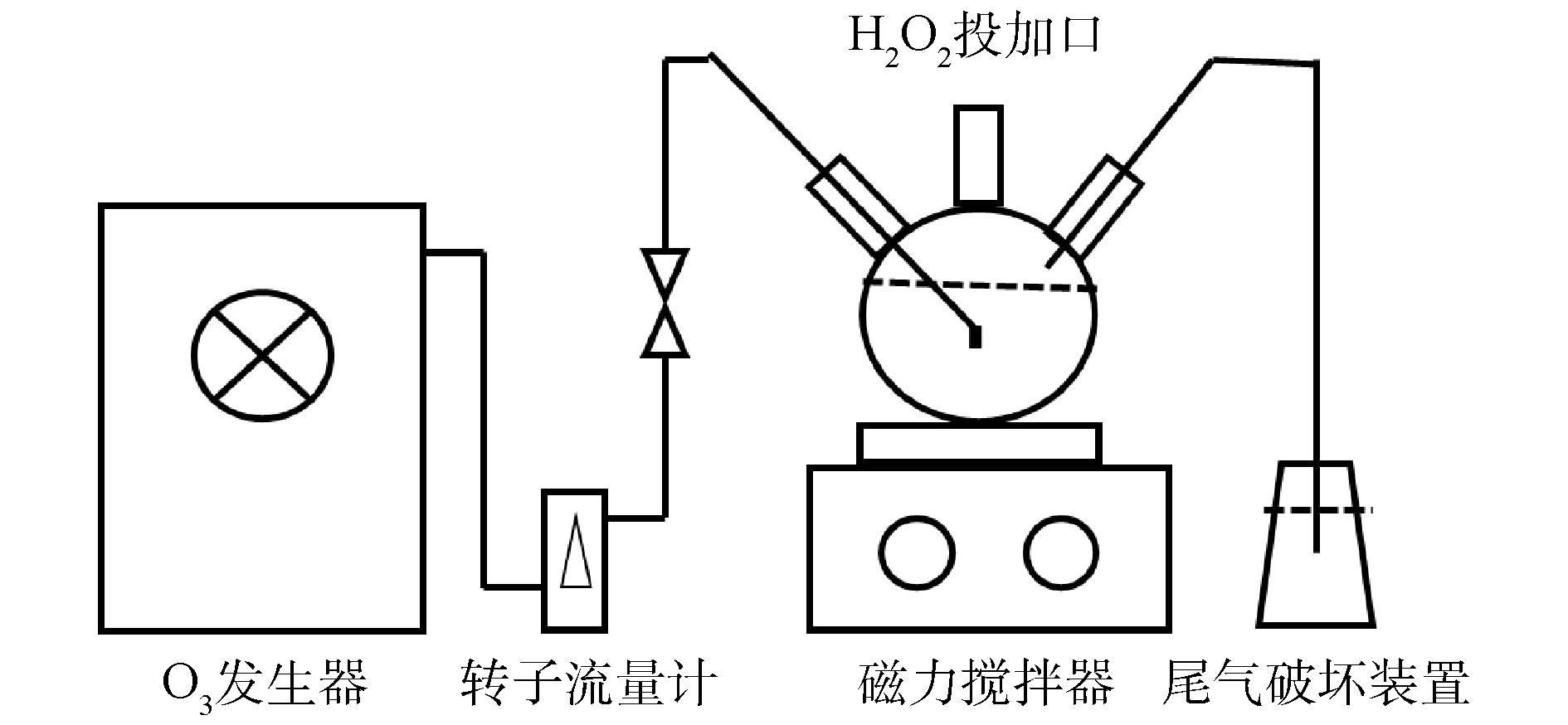
为考察OP强化去除效果,排除无机磷的干扰,水样预先以1 mL·min−1的流速通过阴离子交换树脂柱[10]。实验使用的反应装置如图1所示,装置由臭氧发生器、磁力搅拌器、转子流量计、反应器和尾气破坏装置组成。在25 ℃,初始pH为4.0、7.0和12.0的条件下,分别向反应器中通入0、5、10、15、20、25、30和50 mg·L−1的O3,接触氧化时间控制在20 min,在O3/H2O2氧化实验中,投加一定体积的H2O2(0.01 mol·L−1)来促进氧化过程。反应结束后,取20 mL样品,测定各种磷组分含量,每组进行3次平行实验,取3次实验的平均值。同时,对原水和深度处理后水样进行GC-MS和红外光谱的测定。
计算高级氧化处理前后OP的去除率,计算方法见式(1)。
式中:η为去除率;c0、c1分别为高级氧化前后OP的浓度,mg·L−1。
-
实验仪器。TOC测定仪(Shimadzu TOC, 日本岛津);真空冷冻干燥机(LABCONCO型, 美国LABCONCO公司);臭氧发生器(TOG C2B型, 英国Triogen公司),O3发生量是10 mg·min−1;磁力搅拌器(CJJ-843, 常州普天仪器制造有限公司)。
有机物特性及C/P。用6 mol ·L−1盐酸溶液将水样pH调至2,然后将水样通入离子树脂分级装置中,首先,依次通过串联的XAD-8和阴离子交换树脂柱,此时, 控制水样流速为1 mL·min−1,阴离子交换树脂的作用为吸附去除无机磷组分,其流出溶液为亲水性OP;然后,将串联的XAD-8和阴离子交换树脂柱分离开,并采用0.1 mol ·L−1的NaOH溶液对XAD-8树脂柱进行反冲,控制水样流速为0.5 mL·min−1,XAD-8树脂柱流出溶液为疏水性OP[10]。以OP和DOC计算样品回收率,均为94%~103%。水样的C/P是由DOC/OP计算而得。
生物利用度。水样经调节pH为中性后,取等体积滤液和活性污泥于1 L烧杯内,维持DO 3~5 mg·L−1;水相磷组分是定点取混合液,泥相磷组分研究方法是定点取混合液,经冷冻干燥后采用SMT方法测定污泥絮体中的OP和IP含量[15-16]。
红外光谱分析。采用红外光谱仪(VERTEX 70型, 德国布鲁克公司),扫描区间4 000~400 cm−1。
SPE-GC-MS。萃取和富集采用多通道固相萃取仪(Reeko Auto SPE-06D, 美国Reeko公司),采用气相色谱质谱仪(Trace1300-ISQ, 美国Thermo公司)完成分析。
-
水样预处理后,TP、
PO3−4-P 、TN、COD等指标均采用国标法[17]测定,poly-P的测定方法是将水样1式2份,1份测定PO3−4-P ,还有1份加等体积1 mol·L−1 HCl且保持沸水水浴10 min后测定PO3−4-P ,前后2次浓度差即为poly-P[18],OP的检测方法是差值法[19],根据式(2)计算。式中:c0为OP浓度,mg·L−1;c1为TP浓度,mg·L−1;c2为
PO3−4-P 浓度,mg·L−1;c3为poly-P浓度,mg·L−1。 -
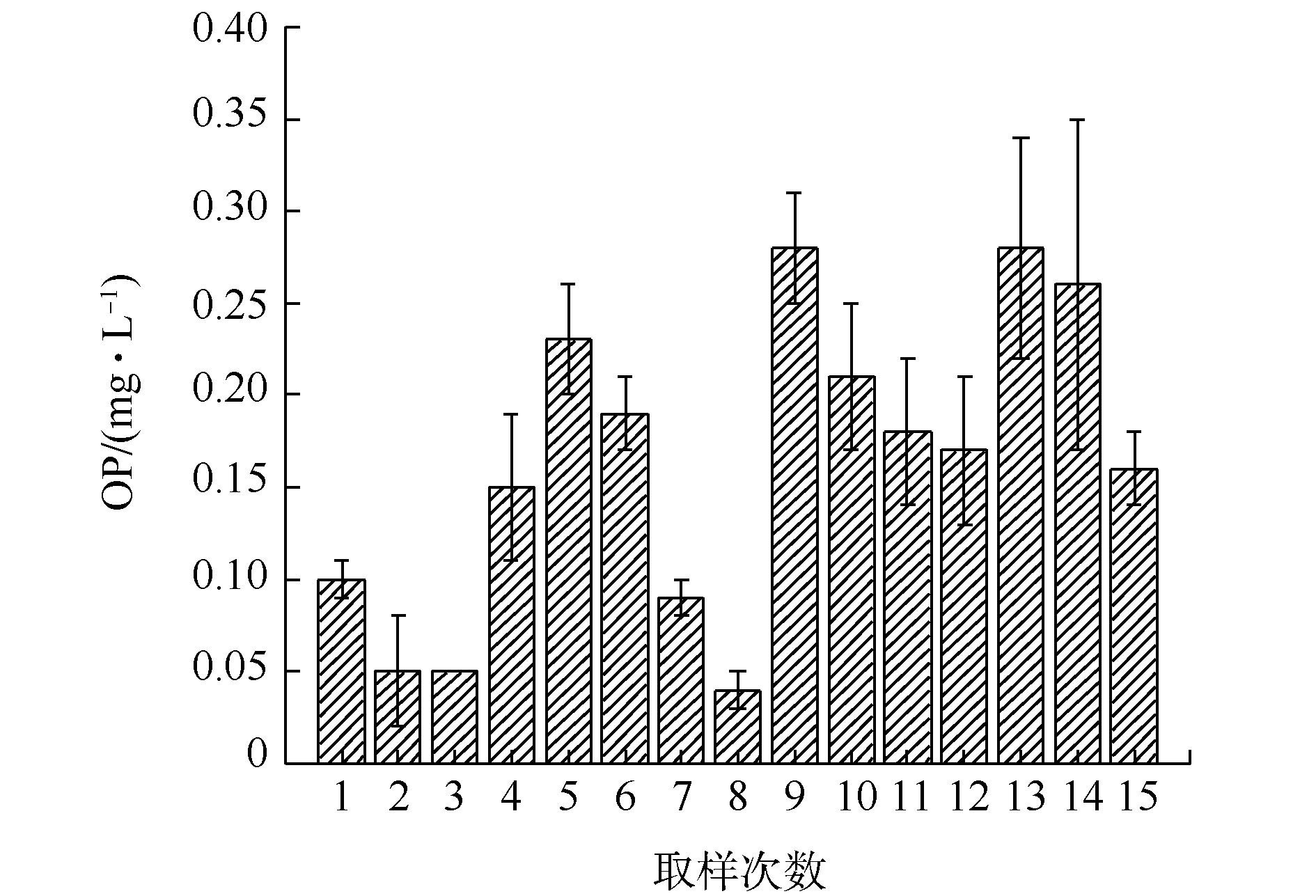
图2为采样周期内WX-A污泥脱水滤液OP组分的变化情况,含量为6.54~13.23 mg·L−1,波动性较大,且平均值高达10.1 mg·L−1。王晶等[20]经研究发现,市政污水处理厂的污泥脱水滤液成分构成较为复杂,含有大量难降解有机物、重金属和盐类以及其他有毒有害物质。但是,通常的观点是污水处理厂的污泥脱水滤液产生量与进水总量相比较小,水量占比约为1%~2%[21],而且脱水滤液的COD、TN、TP等指标并非太高,不会给生物处理单元造成冲击负荷,所以常规处理方式为回流至污水处理厂的进口,重新参与污水处理过程[22]。而本研究中,发现WX-A污泥脱水滤液OP浓度较高,先前的研究鲜有涉及到脱水滤液中OP的污染问题,常规回流处理方式对OP的处理效果或携带的OP对生物系统构成的冲击问题亦研究较少。在采样周期内,WX-A出水OP水平如图3所示,OP平均含量为0.16 mg·L−1。高洋等[23]研究表明,太湖流域污水处理厂二级出水磷组分基本都是
PO3−4-P ,WX-A出水OP高于太湖流域常规市政污水处理厂平均水平。WX-A的脱水滤液和出水OP含量水平呈大致相同的波动趋势,结合物料平衡分析可知,回流液中携带的高浓度有机磷会在进水的稀释作用下含量水平降低,而后污水中的部分有机磷会直接或间接对出水TP造成冲击。由此推测,该厂污泥脱水滤液中富含OP的水质特性对生物处理过程造成了一定冲击,进而影响了出水指标的稳定。 -
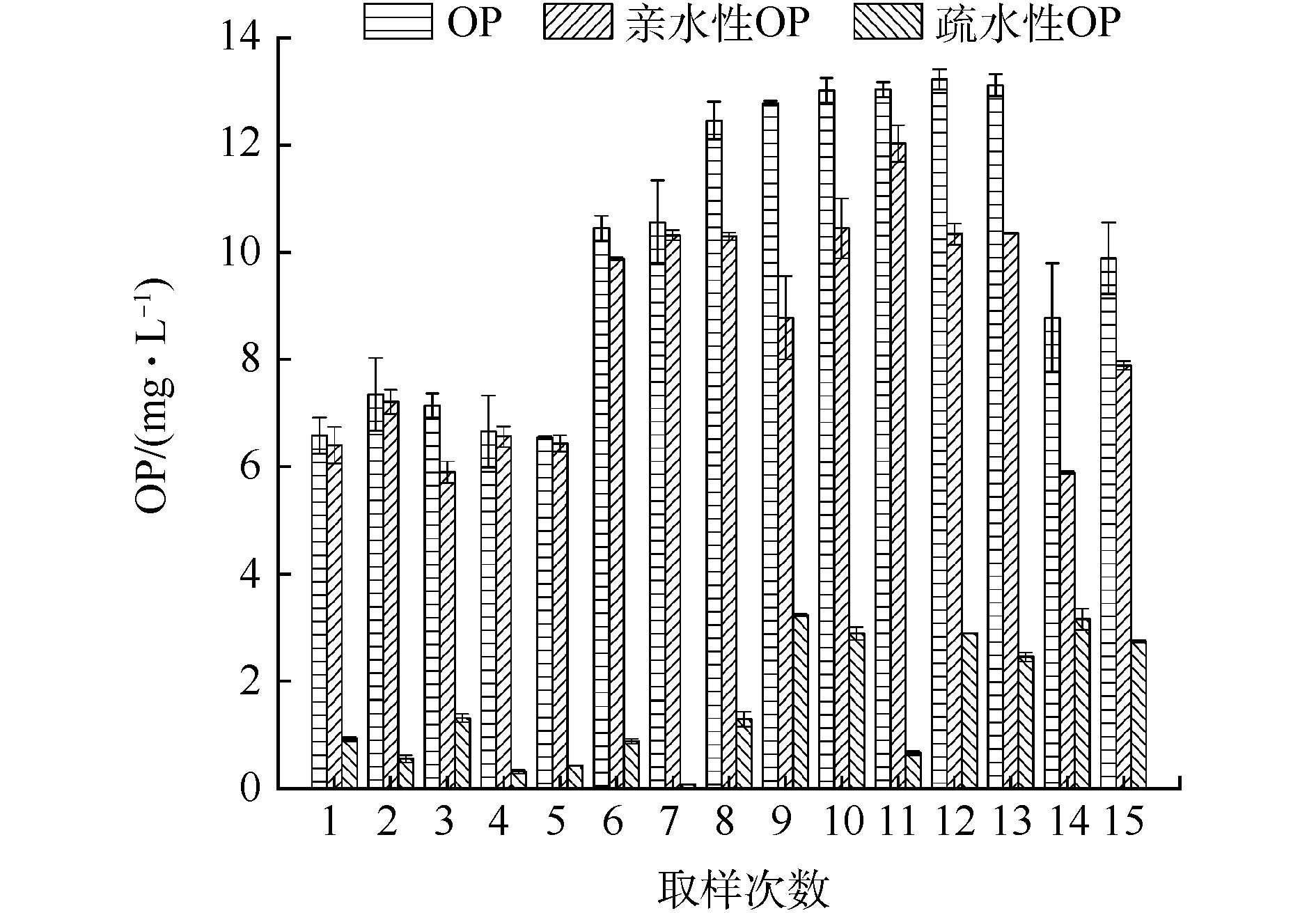
OP的亲疏水性组分及总体分布如图4所示。亲、疏水性OP的平均含量分别为8.58 mg·L−1和1.59 mg·L−1,其在OP中的占比分别为79.7%和20.3%,OP以亲水性组分为主。而先前研究表明,污水中OP以疏水性组分为主[10],该厂脱水滤液中OP的亲疏水性与污水中的性质正好相反,亲水性为主的组分特点或许增加了其处理难度。QIN等[19]和MONBETT等[24]指出,在污水处理过程中,60%~95%的有机磷酸盐会在水解酶作用下降解为低分子有机磷,因此,污水处理过程中OP主要以低分子磷酸单酯和磷酸二酯等形式存在。针对活性污泥脱水滤液中OP的生物降解性研究较少,其降解过程或机理不甚明确。
-
OP组分的C/P结果如图5所示。C/P可以在一定程度上代表污水中OP的生物利用度,从而对后续深度处理技术的选择具有指导意义。QIN等[19]发现,污水中生物利用性较高OP的C/P不宜过大,WX-A污泥脱水滤液OP的C/P处于相对较高水平,生物利用度可能较低。据此可进一步推测,出水OP以难生物降解形态为主。
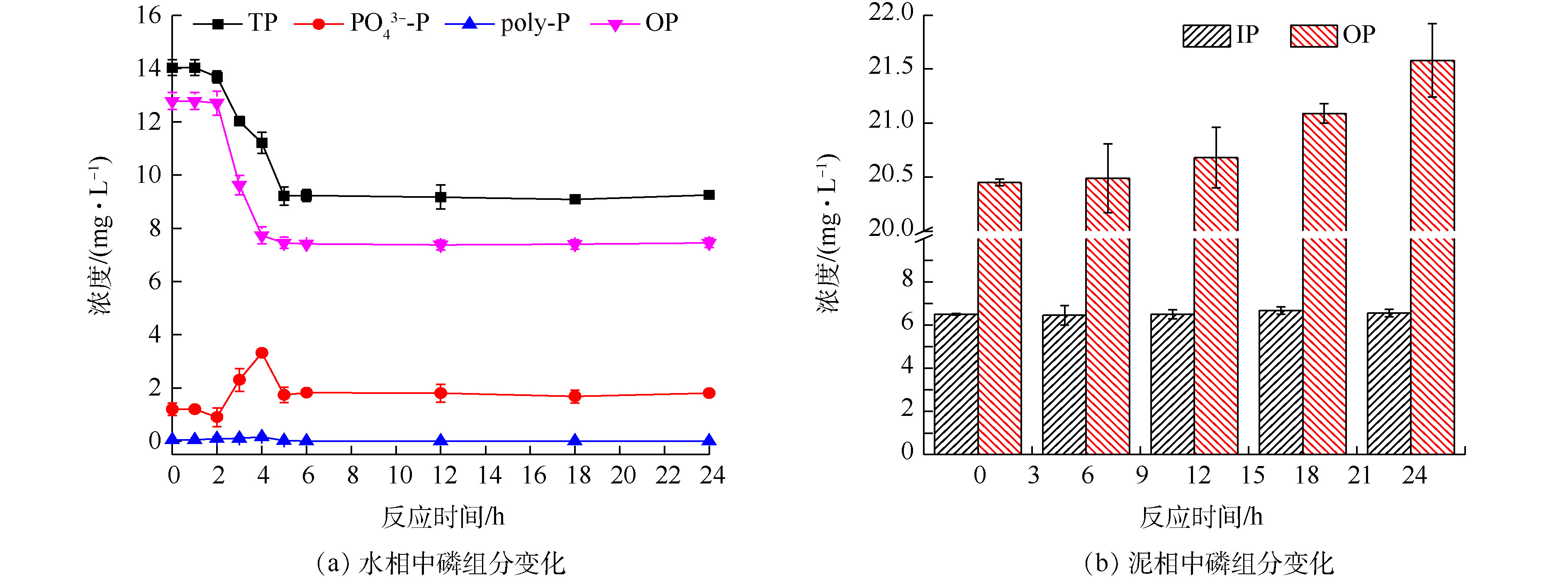
OP的生物利用度结果如图6(a)和图6(b)所示。图6(a)表示在24 h实验周期内水相中各种磷组分的变化情况,TP和OP浓度分别降低了4.78 mg·L−1和5.33 mg·L−1。反应初期(4 h),
PO3−4-P 含量出现了一定程度的上升,由初始1.2 mg·L−1增加至3.32 mg·L−1,这是由于部分易生物降解OP在碱性磷酸酶的作用下转化为PO43--P[12];6 h后,水相中的PO3−4-P 稳定在1.8 mg·L−1,推测是部分PO3−4-P 在好氧条件下被微生物所利用导致的;同时,6 h后,水相中的TP和OP含量处于稳定状态,表明此时污水中磷的赋存状态基本都是难生物降解有机磷。图6(b)表示泥相中IP和OP组分的变化情况,反应期间的悬浮固体浓度(mixed liquid suspended solids, MLSS)为2 030 mg·L−1。其中IP含量比较稳定,反应期间维持在6.5 mg·g−1;而OP含量则呈现增加趋势,由初期的20.45 mg·g−1增加至21.58 mg·g−1。物料衡算分析表明,泥相中OP含量增加了2.29 mg,推测该部分OP是被活性污泥吸附于其表面[25]。综上所述,OP在生物处理过程中的归趋可大致分为3种途径:1)仍残留在污水中,占比58.3%;2)水解为PO3−4-P 被微生物利用或者残存在污水中,占比23.8%;3)OP会被活性污泥所吸附,占比17.9%。这说明,OP的生物利用度仅为23.8%,此结果与前面所述的OP以难生物降解形态为主存在的推测一致。 -
图7所示为在不同O3投加量和pH条件下,WX-A污泥脱水滤液中有机磷组分的变化规律。在pH为4.0、7.0、12.0时,均呈现出随着O3浓度的不断增加,OP含量随之降低的趋势,说明在臭氧直接氧化和产生的·OH的间接氧化作用下[26-28],生物降解性较差的OP被逐步降解为
PO3−4-P 。pH为4.0、7.0时,未对臭氧氧化过程产生抑制或促进作用;pH为12.0时,OP含量呈现出快速降低的趋势。RODRÍGUEZ[29]指出,增加臭氧水环境中的pH或者向反应体系中投加H2O2均能极大地提高·OH的生成效率。因此,污泥脱水滤液具有的碱性水质特点有利于增强深度氧化处理的效果。考虑到实际工程应用中O3浓度不宜过大[30],故O3的最佳投加量为30 mg·L−1,pH为12.0时,OP的去除率可达51.2%。 -
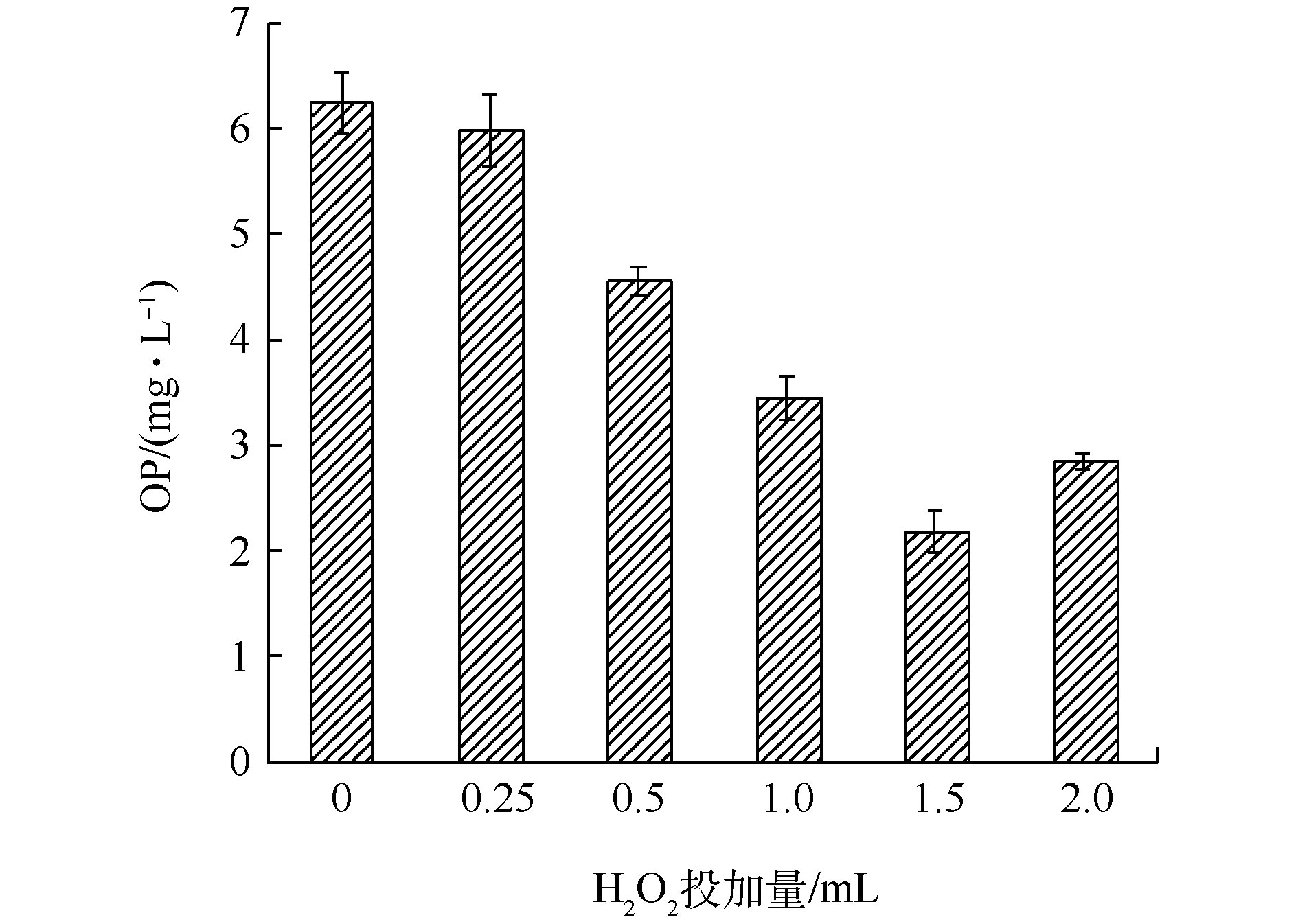
图8所示为在O3投加量为30 mg·L−1、pH为12.0和反应时间为20 min条件下,H2O2投加量对WX-A污泥脱水滤液中有机磷氧化过程中的影响。H2O2投加量为0~1.5 mL时,WX-A脱水滤液OP的去除率随H2O2投加量逐渐提高;H2O2投加量为1.5 mL时,OP的去除率达到最大,为82.9%。这说明一定剂量的H2O2对O3的氧化过程存在促进作用,复杂的含磷有机化合物在较短时间内可以降解为
PO3−4-P ,反应速率得以提高[31]。随着H2O2投加量的持续增加,OP的去除率呈现出降低趋势。这是由于过量的H2O2会和·OH反应,H2O2成为·OH的消耗剂,对氧化过程产生抑制效果[32]。因此,O3/H2O2氧化最佳条件为O3投加量为30 mg·L−1、pH为12.0和H2O2投加量为1.5 mL时,OP的去除率可达82.9%。 -
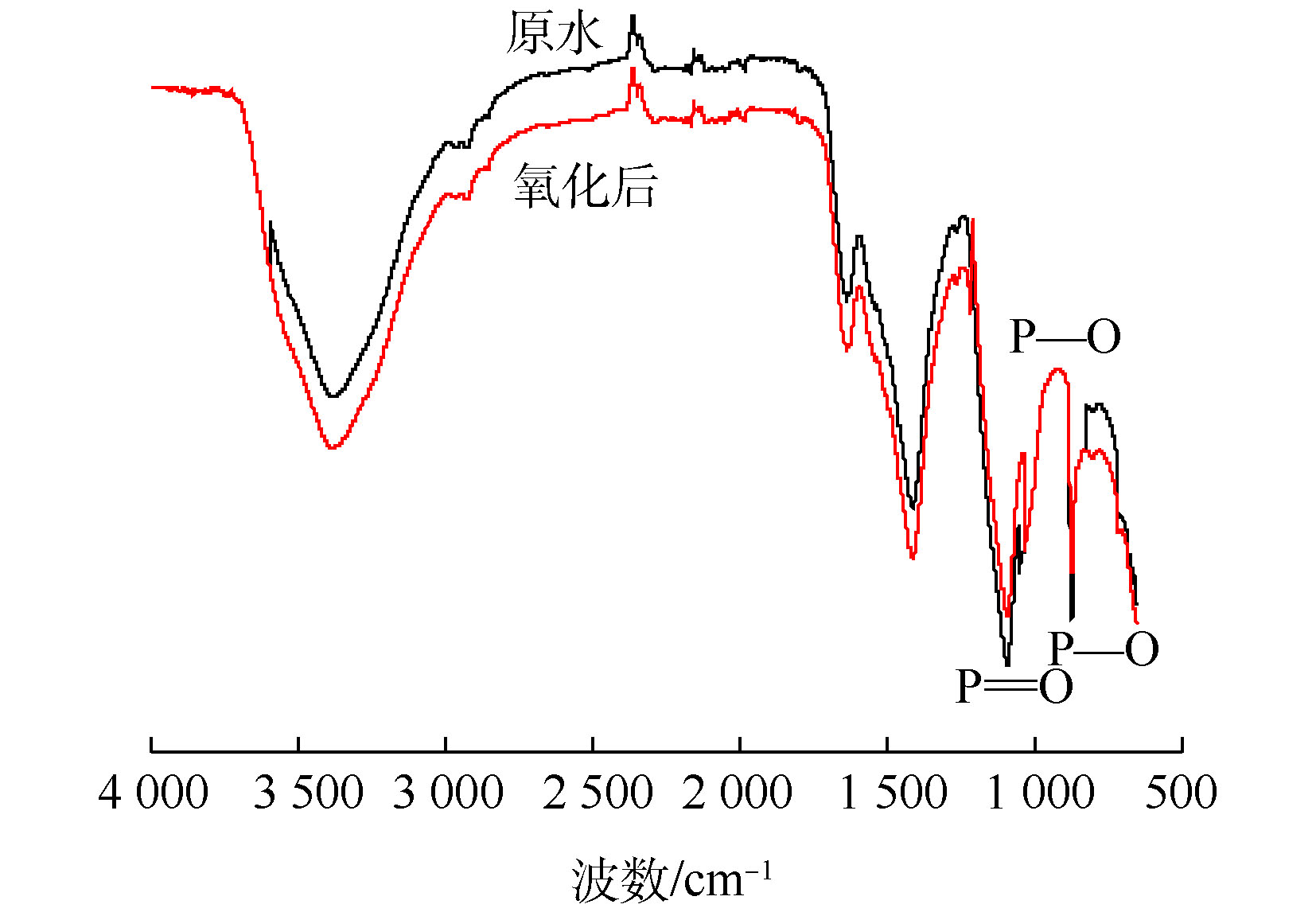
污泥脱水滤液原水和O3/H2O2氧化最佳条件下水样的FT-IR光谱如图9所示。原水经深度氧化前后的有机物特征吸收峰基本一致,而涉及到的含磷基团特征吸收峰也大致相同[33]。共有3处较为明显的含磷基团吸收峰:1)1 165~1 127 cm−1有一处较强的吸收峰,说明该吸收带存在C—O和P=O伸缩振动,其对应的是多糖和磷脂(DNA、RNA)类物质特征;2)950~900 cm−1存在明显的C=C、C—O和P—O伸缩振动,该吸收带分别高度对应烯烃、碳酸盐和芳香族P—O—C物质;3)797~779 cm−1有较窄的P—O伸缩振动谱带,对应的是脂肪族P—O—C物质。
实验结果表明,污泥脱水滤液原水和最佳氧化状态的水样中存在磷脂、芳香族P—O—C和脂肪族P—O—C类等含磷有机化合物。经过深度氧化后的各峰值均要低于原水,即氧化后各个含磷官能团的反射系数均低于原水。其主要原因是:经O3/H2O2氧化后,污泥脱水滤液中含磷有机污染物的含量明显降低,导致原水中典型的官能团结构P=O、芳香族P—O—C以及脂肪族P—O—C均减少。
-
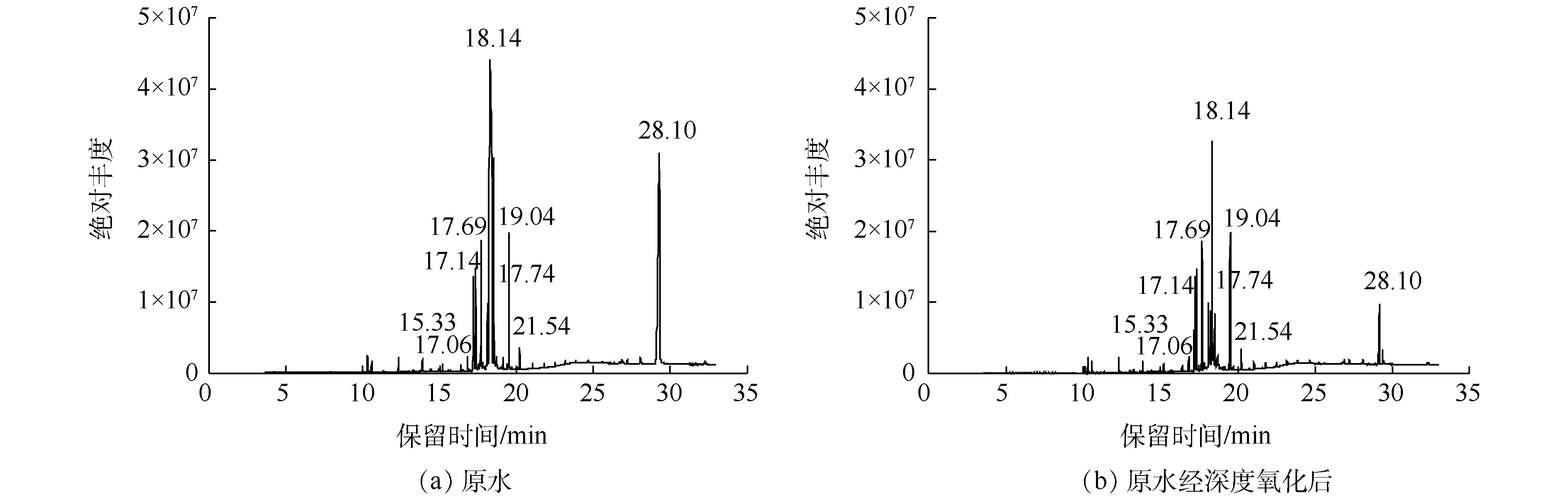
有机物丰度反映出该物质在水样总有机物中的比例。由图10可知,污泥脱水滤液原水中有机物的种类繁多,且部分有机物丰度偏大,如邻苯二甲酸二乙酯、邻苯二甲酸二甲酯、偶氮苯和丁基苄基邻苯二甲酸酯等。经过深度氧化后,有机物的种类略有减少,丰度较大的有机物峰值降低明显。进一步分析可知,氧化前后污泥脱水滤液中含磷有机物的种类基本一致,含量出现显著降低。
WX-A污泥脱水滤液原水中主要的有机磷污染物包括磷脂酰胆碱、羟基乙叉二膦酸、氨基三亚甲基磷酸、芳香族磷酸酯和脂肪族磷酸酯类物质。这些含磷有机物分子质量大,结构复杂,毒性强大,是造成脱水滤液OP难以被生物降解的主要原因[34-35]。其中,以磷脂酰胆碱为代表的磷脂类物质占有机磷组分色谱峰有效积分总面积的33.5%,芳香族磷酸酯类物质占20.5%,脂肪族磷酸酯类物质占比约为13.7%。该结果与FT-IR光谱显示出的污泥脱水滤液原水主要存在磷脂、芳香族P—O—C和脂肪族P—O—C等含磷有机化合物保持一致。同时,结合GC-MS和FTIR光谱结果,前面所述的WX-A污泥脱水滤液OP以难生物降解形态的推测也得到验证。经氧化后水样中各有机磷污染物的峰值均有降低,其中,原水中占比最大的磷脂酰胆碱类磷脂物质被有效氧化去除,芳香族磷酸酯类和脂肪族磷酸酯类物质亦得到有效氧化去除。综上可知,O3/H2O2氧化可以实现难生物降解有机磷的高效去除,适合作为脱水滤液回流的预处理技术。
-
1)WX-A污泥脱水滤液中含有大量的含磷有机污染物,OP含量为6.54~13.23 mg·L−1,均值为10.1 mg·L−1。WX-A脱水滤液和出水OP含量水平呈现出大致相同的波动趋势,推测富含OP的滤液对生物处理过程存在一定冲击。
2)OP以亲水性组分为主的特点可能增加了其生物处理的难度;脱水滤液的C/P处于较高水平,据此可推测OP的生物利用度偏低,进一步研究表明,OP的生物利用度仅为23.8%,其在生物处理过程中的归趋可大致分为3种途径;污泥脱水滤液特有的碱性环境有利于增强氧化效果。
3)原水和最佳去除下水样中存在磷脂、芳香族P—O—C和脂肪族P—O—C等有机物,O3/H2O2氧化使得典型的官能团结构P=O和P—O含量减少;原水中的有机磷包括磷脂酰胆碱、羟基乙叉二膦酸、氨基三亚甲基磷酸、芳香族磷酸酯和脂肪族磷酸酯等,其中占比最大的磷脂酰胆碱被有效去除,芳香族磷酸酯类和脂肪族磷酸酯类物质也被高效去除。
污泥脱水滤液有机磷污染特征及强化去除
Pollution characteristics and enhanced removal of organic phosphorus in sludge dewatering filtrate
-
摘要: 针对污水处理厂污泥脱水滤液有机磷污染现状,采用树脂分级、傅里叶红外光谱和气相色谱质谱等方法解析其污染特征和组分结构,进而开展强化去除研究,并初步探究OP的降解转化过程。结果表明:WX-A污泥脱水滤液OP和出水OP平均含量分别为10.1 mg·L−1和0.16 mg·L−1,脱水滤液的回流可能影响出水稳定;亲水性OP和疏水性OP平均含量分别为8.58 mg·L−1和1.59 mg·L−1,OP的生物利用度仅为23.8%,表明以难生物降解形态为主,进一步的组分解析结果验证了该推测;强化去除研究表明,最佳条件是O3投加量为30 mg·L−1、pH为12.0和H2O2投加量为1.5 mL,去除率高达82.9%。O3/H2O2氧化技术可实现脱水滤液难降解OP的高效去除,从而保证出水达标排放。Abstract: Aiming to organic phosphorus (OP) pollution of sludge dewatering filtrate in wastewater treatment plant (WWTP), resin classification, Fourier transform infrared spectroscopy (FT-IR) and gas chromatography-mass spectrometer (GC-MS) were used to analyze the pollution characteristics and composition, then the enhanced removal approaches were investigated. The degradation and transformation process of OP was further explored. The experimental results showed that average contents of OP in sludge dewatering filtrate and effluent of WX-A were 10.1 mg·L−1 and 0.16 mg·L−1, respectively. Thus, the dewatering filtrate reflux may affect the stability of the effluent. And the average contents of hydrophilic and hydrophobic OP were 8.58 mg·L−1and 1.59 mg·L−1, respectively. The OP bioavailability was only 23.8%, which implied that OP was mainly constituted of refractory forms, and they were confirmed by the component analysis results. Moreover, the optimal conditions for enhanced removal by O3/H2O2 oxidation were determined as following: O3 dosage of 30 mg·L−1, pH of 12.0 and H2O2 dosage of 1.5 mL, and the removal rate was as high as 82.9%. The O3/H2O2 oxidation technology can effectively remove the refractory organic phosphorus from dewatering filtrate, and ensure the discharge to reach the relevant standard.
-
表 1 脱水滤液水质指标
Table 1. Quality of the dehydrated filtrate
污水处理厂编号 TP/(mg·L−1) IP/(mg·L−1) OP/(mg·L−1) TN/(mg·L−1) COD/(mg·L−1) DOC/(mg·L−1) pH WX-A 10.80±3.25 0.97±0.36 9.89±3.34 46.43±0.72 394±18 452±13 11.85±0.52 WX-B 0.27±0.05 0.08±0.02 0.16±0.07 37.70±2.80 268±34 412±11 11.30±1.00 WX-C 2.46±0.11 2.33±0.10 0.13±0.02 45.70±4.80 274±128 400±20 12.10±0.70 -
[1] 陈恒宝, 许立群, 张有仓, 等. 市政污泥与餐厨废弃物协同厌氧消化工程实例[J]. 中国给水排水, 2018, 34(6): 79-84. [2] 黄绍松, 梁嘉林, 张斯玮, 等. Fenton氧化联合氧化钙调理对污泥脱水的机理研究[J]. 环境科学学报, 2018, 38(5): 1906-1919. [3] 蒋秀娅. 贵阳市循环经济型生态城市污泥减量化、稳定化、无害化、资源化技术对策研究[D]. 贵阳: 贵州大学, 2009. [4] 张杰, 王印忠, 曹相生, 等. 污泥脱水滤液水质对以鸟粪石形式回收磷的影响[J]. 北京工业大学学报, 2008, 34(10): 1084-1088. doi: 10.11936/bjutxb2008101084 [5] 朱学红, 蔡奎芳, 张国锋. 污水处理厂污泥脱水滤液循环利用的研究[J]. 环境科学与管理, 2006, 31(7): 106-108. doi: 10.3969/j.issn.1673-1212.2006.07.033 [6] 王敦球. 城市污水污泥重金属去除与污泥农用资源化试验研究[D]. 重庆: 重庆大学, 2004. [7] 崔涵. 浓缩、脱水滤液中污染物对城市污水处理效果的影响[D]. 天津: 天津大学, 2010. [8] TARAYRE C, HUU THANH N, BROGNAUX A, et al. Characterisation of phosphate accumulating organisms and techniques for polyphosphate detection: A review[J]. Sensors, 2016, 16(6): 797-810. doi: 10.3390/s16060797 [9] 周峰. 生物脱氮除磷工艺中的化学辅助除磷试验研究[D]. 济南: 山东建筑大学, 2010. [10] LIU H, JEONG J, GRAY H, et al. Algal uptake of hydrophobic and hydrophilic dissolved organic nitrogen in effluent from biological nutrient removal municipal wastewater treatment systems[J]. Environmental Science & Technology, 2012, 46(2): 713-721. [11] LI B, BRETT M T. The influence of dissolved phosphorus molecular form on recalcitrance and bioavailability[J]. Environmental Pollution, 2013, 182: 37-44. doi: 10.1016/j.envpol.2013.06.024 [12] HONG H S. The availability of dissolved organic phosphorus compounds to marine phytoplankton[J]. Chinese Journal of Oceanology & Limnology, 1995, 13(2): 169-176. [13] RAND M C, GREENBERG A E, TARAS M J, et al. Standard methods for the examination of water and wastewater[J]. American Journal of Public Health, 1976, 56(3): 387-388. [14] 宋淑静, 刘雪娟. 污水中残留有机磷的深度氧化及分析测定[Z]. 郑州, 2006. [15] 杨柳, 唐振, 郝原芳. 化学连续提取法对太湖沉积物中磷的各种形态测定[J]. 世界地质, 2013, 32(3): 634-639. doi: 10.3969/j.issn.1004-5589.2013.03.024 [16] 尹晶. 城市污泥热处理过程中磷的迁移转化特性研究[D]. 沈阳: 沈阳航空航天大学, 2014. [17] 国家环境保护总局. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002. [18] TARAYRE C, DE CLERCQ L, CHARLIER R, et al. New perspectives for the design of sustainable bioprocesses for phosphorus recovery from waste[J]. Bioresource Technology, 2016, 206: 264-274. doi: 10.1016/j.biortech.2016.01.091 [19] QIN C, LIU H, LIU L, et al. Bioavailability and characterization of dissolved organic nitrogen and dissolved organic phosphorus in wastewater effluents[J]. Science of the Total Environment, 2015, 511: 47-53. doi: 10.1016/j.scitotenv.2014.11.005 [20] 王晶, 杨昌柱, 濮文虹, 等. 市政污泥深度脱水滤液水质特性研究[J]. 环境工程, 2014, 32(S1): 107-110. [21] JANUS H M, VANDERROEST H F. Don’t reject the idea of treating reject water[J]. Water Science and Technology, 1997, 35(10): 27-34. doi: 10.2166/wst.1997.0351 [22] 翟显之. 污泥水热厌氧消化脱水滤液处理研究[D]. 北京: 清华大学, 2014. [23] 高洋, 程洁红. 太湖流域污水处理厂氮磷去除现状及效能的研究[J]. 江苏理工学院学报, 2016, 22(2): 55-60. doi: 10.3969/j.issn.1674-8522.2016.02.013 [24] MONBETT P, MCKELVIE I D, SAEFUMILLAH A, et al. A protocol to assess the enzymatic release of dissolved organic phosphorus species in waters under environmentally relevant conditions[J]. Environmental Science & Technology, 2007, 41(21): 7479-7485. [25] 王超, 冯士龙, 王沛芳, 等. 污泥中磷的形态与生物可利用磷的分布及相互关系[J]. 环境科学, 2008, 29(6): 1593-1597. doi: 10.3321/j.issn:0250-3301.2008.06.024 [26] 朱秋实, 陈进富, 姜海洋, 等. 臭氧催化氧化机理及其技术研究进展[J]. 化工进展, 2014, 33(4): 1010-1014. [27] 张志伟. 臭氧氧化深度处理煤化工废水的应用研究[D]. 哈尔滨: 哈尔滨工业大学, 2013. [28] 竹湘锋. 有机废水的催化臭氧氧化研究[D]. 杭州: 浙江大学, 2005. [29] RODRIGUEZ A, ROSAL R, PERDIGON-MELON J A, et al. Ozone-based technologies in water and wastewater treatment[J]. Handbook of Environmental Chemistry, 2008, 5: 127-175. [30] 郑志洋. 城镇污水厂二级生化出水臭氧深度处理技术研究[D]. 石家庄: 河北科技大学, 2017. [31] 刘金泉, 李天增, 王发珍, 等. O3、H2O2/O3及UV/O3在焦化废水深度处理中的应用[J]. 环境工程学报, 2009, 3(3): 501-505. [32] ZHOU C, GAO N, DENG Y, et al. Factors affecting ultraviolet irradiation/hydrogen peroxide (UV/H2O2) degradation of mixed N-nitrosamines in water[J]. Journal of Hazardous Materials, 2012, 231: 43-48. [33] YANG L, HAN D H, LEE B, et al. Characterizing treated wastewaters of different industries using clustered fluorescence EEM-PARAFAC and FT-IR spectroscopy: Implications for downstream impact and source identification[J]. Chemosphere, 2015, 127: 222-228. doi: 10.1016/j.chemosphere.2015.02.028 [34] 王晓伟, 刘景富, 阴永光. 有机磷酸酯阻燃剂污染现状与研究进展[J]. 化学进展, 2010, 22(10): 1983-1992. [35] 柏文琴, 何凤琴, 邱星辉. 有机磷农药生物降解研究进展[J]. 应用与环境生物学报, 2004, 10(5): 675-680. doi: 10.3321/j.issn:1006-687X.2004.05.031 -




 下载:
下载: