水体和沉积物中毒害污染物的生态风险评价方法体系研究进展
Ecological Risk Assessment Methodology of Toxic Pollutants in Surface Water and Sediments: A Review
-
摘要: 人类活动导致大量毒害污染物进入水体和沉积物,从而对水生生物产生诸多不利影响。开展毒害污染物的生态风险评价,筛选高风险毒害污染物,是毒害污染物风险管控和生态系统保护的基础。对美国和欧盟等发达国家和地区毒害污染物的生态风险评价方法进行了综述。水体和沉积物中毒害污染物风险评价的基本方法首先是采用预测或测定环境浓度(PEC或MEC)进行暴露评价,用生态毒性的剂量-效应关系推导出的预测无影响浓度(PNEC)进行影响评价,然后以风险商(RQ)进行风险表征。对于沉积物中缺乏毒性数据的有机毒害物则通过有机碳归一化沉积物/水分配系数将沉积物中污染物的浓度转化为孔隙水中的浓度,采用水体评价方法进行评价;对于沉积物中重金属的风险,可采用风险评价码(RAC)或采用酸性可挥发性硫化物(AVS)和同步浸提重金属(SEM)差值法进行表征。据此,提出我国开展流域水体和沉积物中毒害污染物的风险评价体系,为我国毒害污染物的风险管控提供参考。Abstract: Numerous toxic pollutants enter into water and sediments due to human activities, thus causing adverse effects on aquatic organisms. Hence, conducting ecological risk assessment of contaminants and screening high-risk contaminants are the basis of risk management of contaminants and ecosystem protection. In this paper, we reviewed the methodologies of ecological risk assessment for toxic pollutants in aquatic environment used in the United States, European Union and other developed countries. Basic methodology of risk assessment for contaminants in surface water and sediments includes the following three processes:(a) Exposure assessment, which is carried out using predicted or measured environmental concentrations (PECs or MECs); (b) Impact assessment, which is performed using predicted no effect concentrations (PNECs) derived from aquatic toxicity data through dose-effect relationship; (c) Risk characterization, which is ranked by risk quotient (RQ) from the ratio of PEC (or MEC) to PNEC. However, for the pollutants lacking toxicity data in sediments, the risk assessment of the organic pollutants can be carried out using the aquatic risk assessment method after obtaining the concentration of the pollutants in pore water, which is calculated from the concentration in sediments according to the organic carbon-normalized sediment/water partition coefficient of the organic pollutant. And for the metal pollutants in sediments, the risk assessments can be characterized by risk assessment code (RAC) or by the subtraction method of acid volatile sulfide (AVS) and simultaneously extracted metals (SEM). Based on the review, we proposed a risk assessment methodology for toxic pollutants in surface water and sediments in China, aiming to provide information for contamination risk management of China.
-
Key words:
- toxic pollutants /
- ecological risk assessment /
- water and sediment /
- PNEC
-
复方益母草胶囊是由益母草、当归和熟地3味药材经过一定的工序加工制成的复方制剂,该胶囊主要药味益母草中含有生物碱类、黄酮类、二萜类、苷类、脂肪酸类、挥发油类等成分[1]. 生物碱类盐酸水苏碱是益母草的主要药效成分[2]. 盐酸水苏碱是季胺碱,极性强,无共轭结构,紫外吸收弱,属于末端吸收. 高效液相色谱法是盐酸水苏碱目前最为普遍的检测方法,盐酸水苏碱常用的检测器有紫外检测器 (DAD等) [3]、质谱检测器(MS)[4]、示差检测器(RID)和蒸发光散射检测器 (ELSD) [5]等,目前尚未报道电雾式检测器(CAD)被用于盐酸水苏碱的定量分析. 用紫外检测器测定盐酸水苏碱,存在方法重复性差、溶剂末端吸收干扰、梯度洗脱时容易出现基线漂移检测不稳定等局限性[6];依据盐酸水苏碱的结构中有旋光性的特点,采用RID检测器测定其含量,无需特殊样品处理方法就有很好的峰形,但专属性不强、灵敏度较低,且不能使用梯度洗脱分离效果不佳,应用相对较少[7-8];ELSD检测器是目前定量分析盐酸水苏碱最常用的检测器,据报道其灵敏度也较低[9]. 电雾式检测器(CAD)是一种质量相关的通用型检测器,其检测信号不依赖于被测物质的化学结构,更适用于无紫外吸收或只有较弱紫外吸收成分的定量分析.
本研究利用Thermo-fisher AcclaimTM Mixed-Mode WAX-1色谱柱结合HPLC-CAD法分离测定复方益母草胶囊中主要成分盐酸水苏碱含量,探讨该方法对比现行《中国药典》(2020版)一部中ELSD测定盐酸水苏碱的优势,为其质量评价和标准制定提供理论依据,同时为未来推广到其它含益母草类制剂中使用提供科学参考,具有现实应用价值,且目前缺少相关报道.
1. 实验部分
1.1 仪器与试剂
试剂:甲酸分析纯(纯度99.9%)(天津市科密欧化学试剂有限公司);甲酸铵质谱级(纯度99%)(Roe Scientific Inc公司);无水乙醇分析纯(天津市富宇精细化工有限公司);甲醇HPLC级(上海星可高纯溶剂有限公司);乙腈HPLC级(上海星可高纯溶剂有限公司);屈臣氏饮用水(广州屈臣氏食品饮料有限公司);盐酸水苏碱对照品(纯度98.91%)(成都普思生物科技股份有限公司).
液相色谱(美国赛默飞公司),Vanquish Core系列双三元泵:VC-P33-A-01;自动进样器:VC-A12-A-02;柱温箱:Column compartment VC-C10-A-03;可变波长检测器:Variable Wavelength Detector VC-D40-A-01;CAD检测器:Charged Aerosol Detector H VH-D20-A;变色龙色谱管理软件 Chromeleon CDS 7.3; Waters Acquity超高效液相色谱仪ELS Detector检测器;电子天平 YP30002(上海佑科仪器仪表公司);分析天平 B931029762(北京艾斯瑞克商贸公司);超声仪 KQ-250DB(昆山市超声仪器公司)。
色谱柱:AccucoreTM-Amide-HILIC(150 mm × 4.6 mm,5 µm, Thermo-Fisher公司);AcclaimTM Mixed-Mode WAX-1(250 mm × 4.6 mm,5 µm, Thermo-Fisher公司); AcclaimTM Mixed-Mode WCX-1(250 mm × 4.6 mm,5 μm, Thermo-Fisher 公司);Ascentis Express OH5 (150 mm × 4.6 mm,2.7 µm, 美国merck公司);Polar-Phenyl (250 mm × 4.6 mm,5 µm, 济南赛畅科学仪器有限公司);ShimNex HE Amide (250 mm × 4.6 mm,5 µm ,岛津中国公司);Poroshell 120 HILIC-Z (150 mm × 4.6 mm,2.7 µm, 安捷伦公司);Venusil HILIC (250 mm × 4.6 mm,5 µm,Agelag公司);XBridge BEH Amide (150 mm × 4.6 mm,5 µm Waters公司);60-5-HILIC-D (250 mm × 4.6 mm,5 µm Kromasil公司); XBridge Amide (250 mm × 4.6 mm,5 µm Waters公司).
1.2 溶液配制
对照品溶液 取盐酸水苏碱对照品适量,精密测定,加入70%乙腈(乙醇)制成每1mL含0.5 mg的溶液,即得.
供试品溶液 按2020版《中国药典》方法制备,取装量差异项下的复方益母草胶囊内容物,混匀,研细,取约0.5 g,精密称定,置具塞锥形瓶中,精密加入70% 乙腈(乙醇)25 mL,称定重量,加热回流2 h,放冷,再称定重量,用70%乙腈(乙醇)补足减失的重量,摇匀,滤过,取续滤液,即得.
阴性对照的制备:按照复方益母草胶囊处方药物组成,不加益母草和辅料,同供试品制备方法.
2. 结果与讨论
2.1 检测器选择
精密量取盐酸水苏碱对照品储备液1 mL,分别置于5、10、20、50、100 mL容量瓶中,至刻度. 再精密量取1 mL上述50 mL容量瓶溶液置于10 mL、25 mL容量瓶中,加70%乙醇置刻度,摇匀. 按照《中国药典》(2020版)一部复方益母草胶囊方法,采用AccucoreTM-150-Amide-HILIC (150 mm × 4.6 mm, 5 µm)色谱柱,以乙腈-0.2%冰醋酸溶液(80∶20)为流动相,进样量5 μL,分别用ELSD和CAD检测器测定盐酸水苏碱的信噪比,进行灵敏度对比. 按信噪比3∶1及10∶1计算,盐酸水苏碱的检测限(LOD)和定量限(LOQ)结果显示,CAD检测限是ELSD的34倍,定量限是37倍,表明CAD有更好的灵敏度.
2.2 色谱柱选择
取盐酸水苏碱标准品适量,分别采用10种不同厂家的色谱柱进行测定,其中Poroshell 120 HILIC-Z和AcclaimTM Mixed-Mode WAX-1色谱柱对复方益母草中盐酸水苏碱分离效果最好,前者理论塔板数高达26430,后者理论塔板数18413,且前后无干扰峰,因此本研究最终选择AcclaimTM Mixed-Mode WAX-1柱子作为盐酸水苏碱的定量分析.
2.3 检测方法研究
盐酸水苏碱是最简单的吡咯生物碱,其分子结构含有季铵根和羧基,极性较强。实验室尝试了 Acclaim Mixed-Mode WAX-1 和 WCX-1 两款色谱柱的 RP+IEX 保留模式,保留均较弱。其中 Acclaim Mixed-Mode WAX-1 色谱柱键合相为带有叔胺末端的疏水烷基链键合硅胶,除去反相保留(RP)和弱阴离子交换(WAX),还可提供亲水作用(HILIC)保留机制。经试验确定采用 Acclaim Mixed-Mode WAX-1 色谱柱的 HILIC 模式进行盐酸水苏碱的分离保留效果优异,因而流动相有机相优先选择乙腈。由于 Acclaim Mixed-Mode WAX-1 色谱柱必须始终使用含有缓冲盐的流动相进行活化、分析或保存,在配合 CAD 使用时,须使用挥发性缓冲盐,流动相水相可选用甲酸铵或乙酸铵。
除了色谱柱和流动相的选择外,供试品溶液的制备也需要重点考察。取复方益母草胶囊数粒去壳,将内容物混匀研细,取0.2 g,精密称定,置具塞三角瓶中,分别精密加入30%、50%、70%的甲醇,30%、50%、70%的乙醇和30%、50%、70%的乙腈,超声提取40 min(功率250 W,频率40 kHz),冷却至室温,摇匀. 离心5 min(5000 r·min−1)。转移至25 mL容量瓶并定容至刻度,经0.45 μm微孔滤膜过滤,取续滤液,即得. 进样检测,计算各提取溶剂下盐酸水苏碱的相对含量. 3种不同浓度的乙腈对盐酸水苏碱成分提取效果最好,在 HILIC 模式下,流动相通常推荐使用非质子溶剂乙腈,并且初始流动相为较高比例的乙腈,当对照品或供试品溶液乙腈比例较低时,进样后容易形成溶剂效应,影响水苏碱的峰形和响应。试验表明,采用 70% 乙腈水提取效果较好,因此本研究最终选择70%乙腈作为提取溶剂.
最终确定以CAD为检测器,采用AcclaimTM Mixed-Mode WAX-1(250 mm×4.6 mm,5 μm)柱,以20 mmol·L-1 甲酸铵 (甲酸调节 pH至 4.0) (A)-乙腈(B)为流动相,梯度洗脱:0—8 min,10%A;8—12 min,10%—50%A;12—15 min,50%A;15—20 min,50%—10%A. 柱温30 ℃,蒸发温度35 ℃;采集频率 5 Hz,过滤常数 3.6 s;进样体积5 μL. 该色谱条件通过系统考察得到较好的分离效果.
2.4 方法学验证
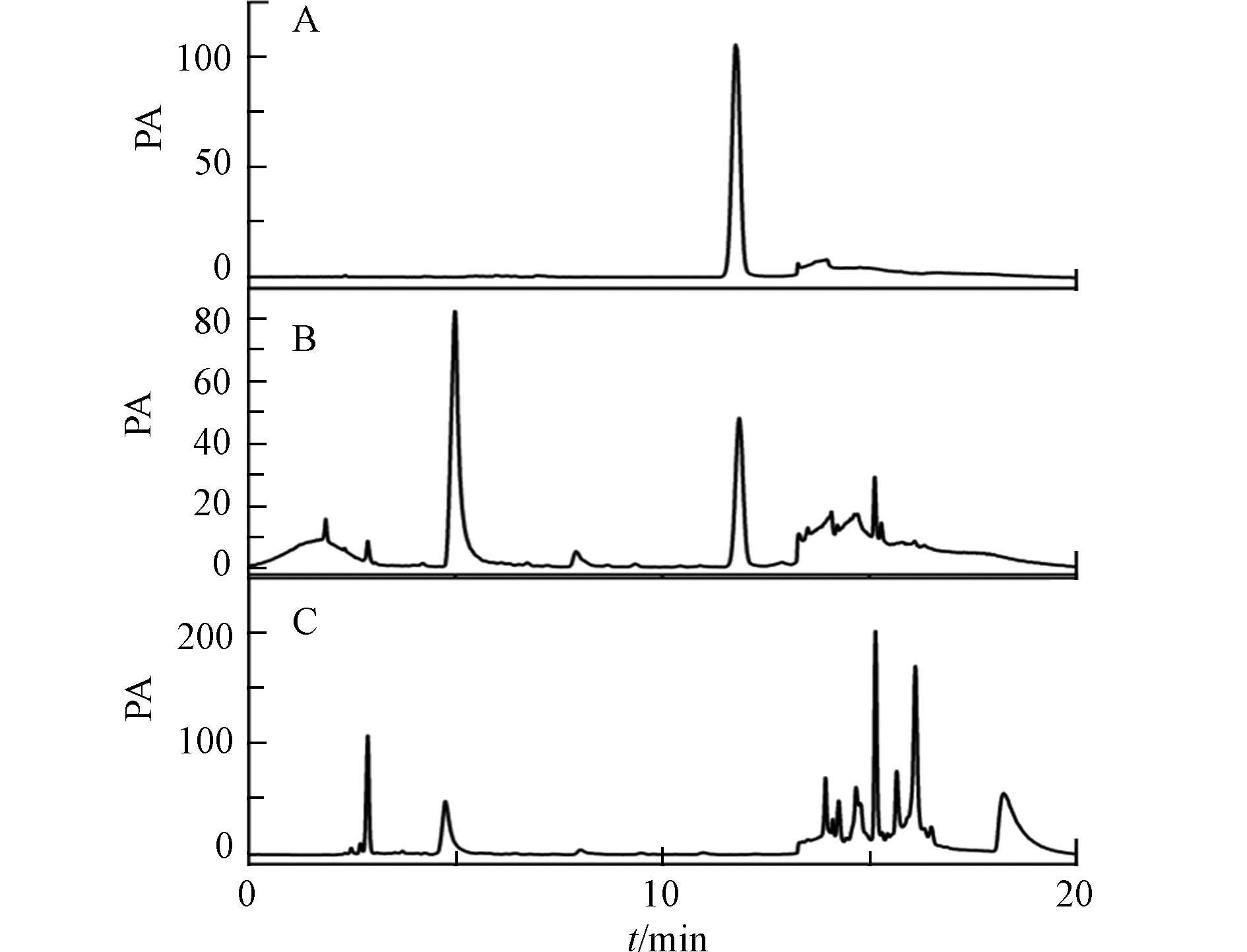
分别取盐酸水苏碱标准对照品溶液,供试品溶液,缺益母草阴性对照液适量,注入高效液相色谱仪,按2.3节色谱条件进样测定. 供试品色谱图中出现与标准对照品中保留时间相同的峰,且理论塔板数不低于18000,缺益母草阴性对照色谱图中显示阴性样品无干扰,表明该方法专属性较好(图1).
取盐酸水苏碱对照品溶液,按2.3节色谱条件连续进样6次,记录峰面积,结果峰面积RSD为1.13%. 按上述样品制备方法,制备供试品溶液,分别于0、2、6、10、24 h进样,RSD为1.93%,表明供试品在24 h内稳定性良好. 取同一批号样品(批号:20220301),按2.3节方法平行制备6份供试品溶液,在2.3节色谱条件进样分析,样品中盐酸水苏碱平均含量33.4 mg·g−1,RSD为1.38%.
采用加样回收法,精密称取0.1 g已知含量的复方益母草胶囊样品8份,分别加入适量的盐酸水苏碱标准品,按2.3节供试品制备方式制备供试品. 计算加样回收率在95.70%—99.20%,平均回收率97.37%,RSD为1.14%(表1).
表 1 盐酸水苏碱回收率(n=2)Table 1. Recovery rate of stachydrine hydrochloride(n=2)序号 取样量/g 样品含有量/mg 加标量/mg 测得量/mg 回收率/% 平均回收率/% 相对标准偏差/% 1 0.1042 3.4821 3.3420 6.7972 99.1953 97.37 1.14 2 0.1095 3.5389 3.3420 6.7904 97.2901 3 0.1079 3.6058 3.3420 6.8040 95.6998 4 0.1031 3.4454 3.3420 6.6717 96.5381 5 0.1096 3.6626 3.3420 6.9328 97.8527 6 0.1062 3.5489 3.3420 6.8387 98.4361 7 0.1040 3.4754 3.3420 6.7093 96.7638 8 0.1047 3.4988 3.3420 6.7481 97.2262 精密称量盐酸水苏碱对照品9.30 g于20 mL容量瓶中,加70%乙腈水溶液逐级稀释,制成盐酸水苏碱浓度分别为0.465、0.279、0.186、0.093、0.047、0.019 mg·mL−1,按2.3项下色谱条件下进样分析,记录相应峰面积. 以待测组分质量浓度(X)为横坐标,以峰面积(Y)为纵坐标,对一次曲线和二次曲线进行了比较,一次曲线函数为Y=52.989X+1.5521,r2为0.9862,二次曲线函数为Y=-54.114X2+78.28X+0.4612,r2为0.9995,二次曲线拟合较好,故选二次曲线进行计算.
2.5 复方益母草胶囊含量测定
依据前述盐酸水苏碱含量测定方法,分别对随机选取的同批次和不同批次(5批)复方益母草胶囊中盐酸水苏碱含量进行测定,分别计算其批内(PA)和批间(PB)盐酸水苏碱含量的差异值.结果表明,复方益母草胶囊批内差异PA值为6.3%,反映该厂家与益母草相关的生产工艺较稳定. 批间一致性差异较大,每粒含量12.00—16.14 mg不等,PB值为28.98%,推测可能是益母草原料质量差异造成.
3. 结论
通过对比10种亲水型作用色谱柱(HILIC),最终确定利用Acclaim Mixed-Mode WAX-1色谱柱键合相的叔胺官能团,在 HILIC 模式下对水苏碱的强保留能力,可有效与供试品杂质峰分离,避免基质干扰。采用乙腈-20 mmol·L−1 甲酸铵缓冲液 (pH=4.0) = 90:10作为初始流动相进行梯度洗脱,配合CAD检测器测定盐酸水苏碱含量, 结果显示CAD具有较高的灵敏度,为定量分析盐酸水苏碱提供了新方法新参考. 本研究所建立用于测定盐酸水苏碱HPLC-CAD方法,专属性强、重复性好、灵敏度高,为复方益母草胶囊及相关制剂中盐酸水苏碱的质量检测提供可行方案.
-

 点击查看大图
点击查看大图
计量
- 文章访问数: 1537
- HTML全文浏览数: 1537
- PDF下载数: 68
- 施引文献: 0



 下载:
下载:
