-
低碳氮比(C/N)进水条件造成的生化系统反硝化脱氮能力不足是我国污水处理厂运行普遍面临的主要问题之一,选择合适的外加碳源并确定碳源的最佳投加量是污水处理厂实现经济、高效、低碳运行的重要举措。外加碳源投加量会受到实际运行中多种因素的影响,包括污水处理厂进水水质水量的波动性、生化系统中微生物群落结构等,这使得传统碳源投加计算公式计算出的理论值用于指导实际工艺运行存在很大的局限性。碳源投加过量或选择碳源不当,不但会增加系统运行费用,还会使污水处理厂出水COD有超标风险。因此,以更加精准科学的方式确定碳源的种类及其投加量是城市生活污水处理厂实现减污降碳协同增效的重要途径。
-
污水处理厂生化池脱氮原理见图1,生物脱氮除磷主要是由异养微生物进行的,其功能菌反硝化菌和聚磷菌大多为异养菌[1],在有机物特别是可溶性有机物缺乏的情况下,会导致生物脱氮除磷效果变差。现有城市污水厂进水C/N往往较低,可溶性有机物不足是造成出水氮磷超标的主要原因,为了满足污水处理厂出水水质达标的要求,需向生物处理系统中投加额外的有机碳源来提高氮磷去除效果。
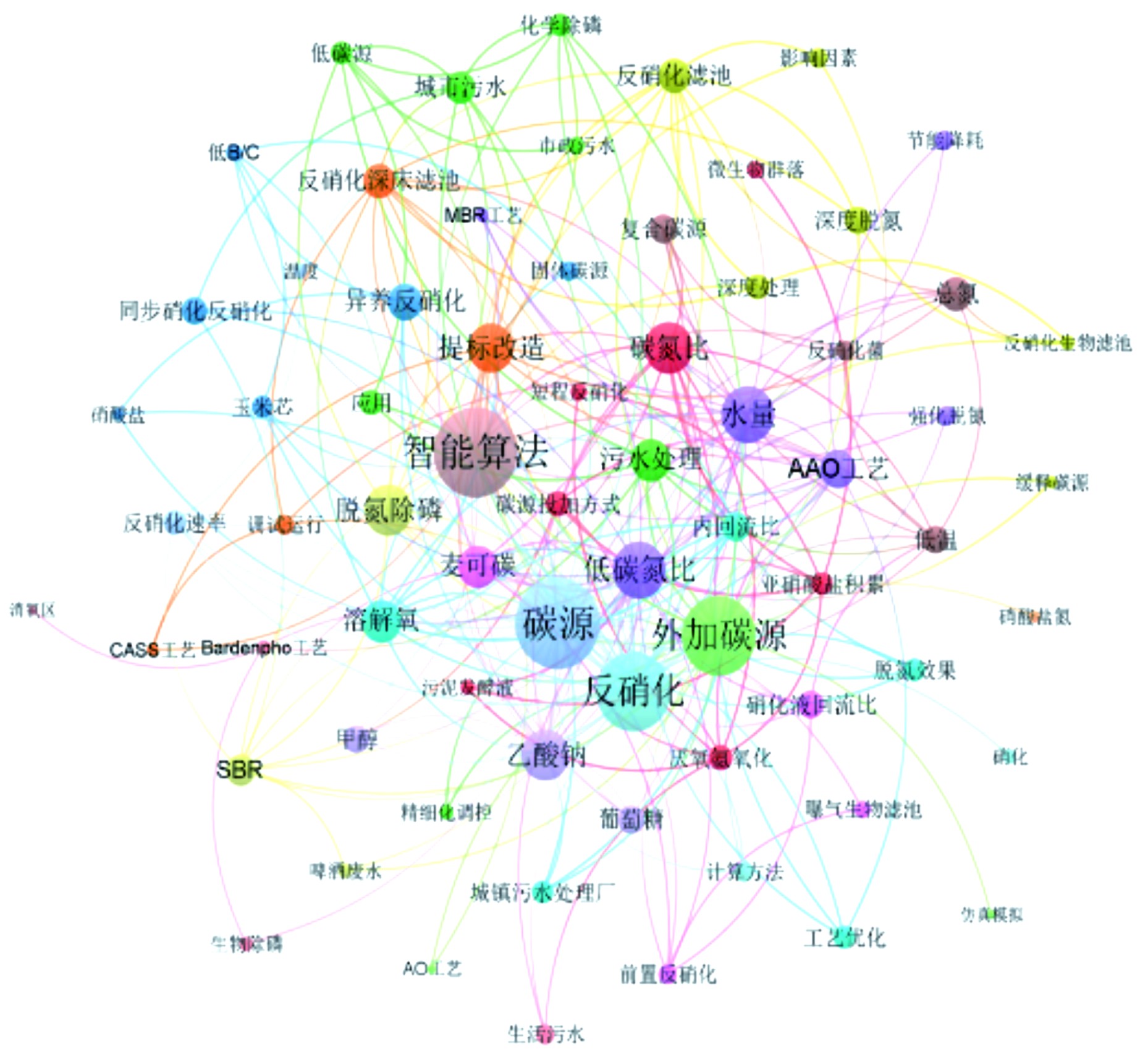
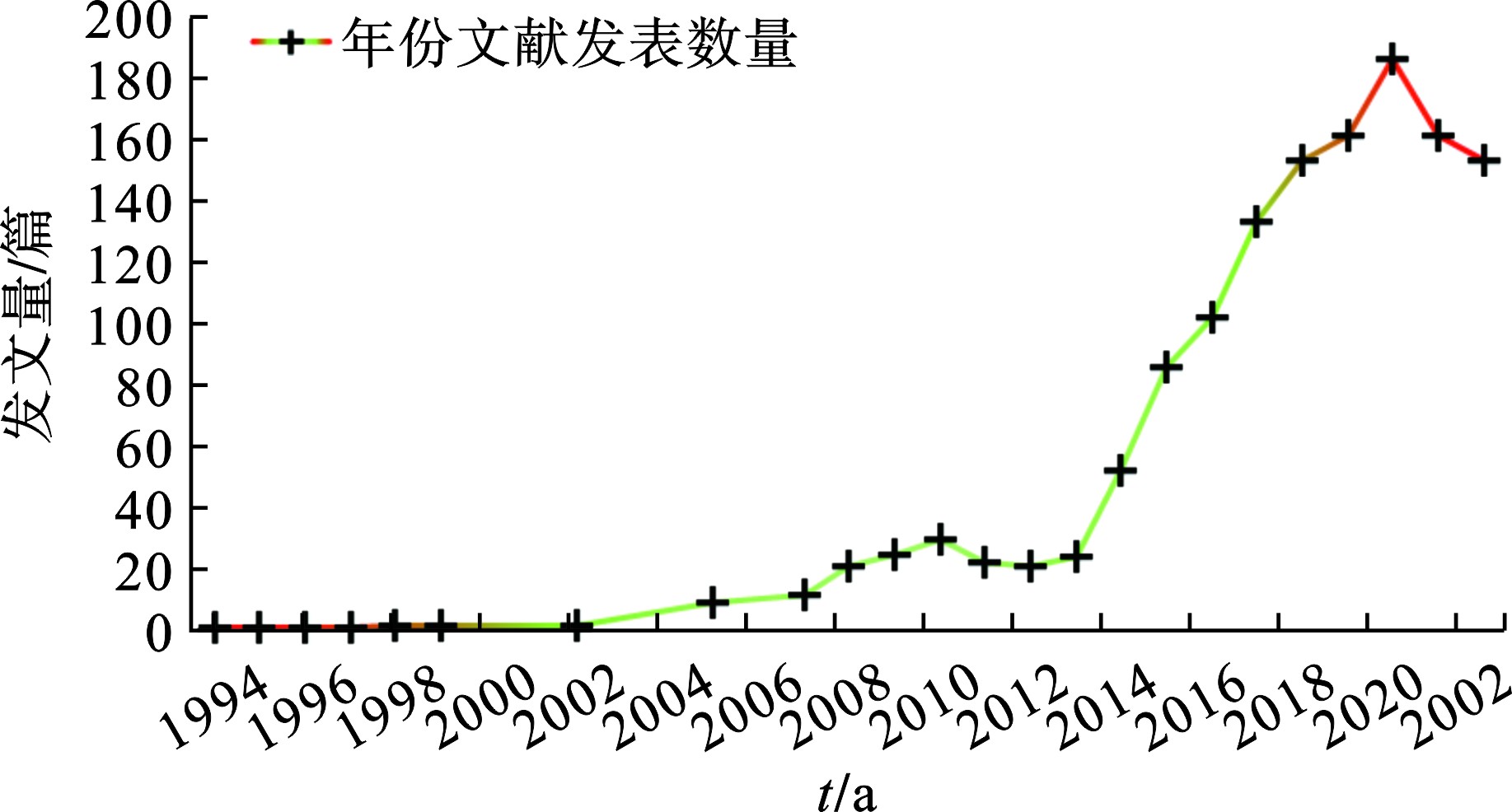
污水处理厂运行过程中的碳源投加吸引了水务行业人员和越来越多学者的关注,1994—2022年期间有关碳源投加的中文文献热点分析和数量统计见图2和图3。相关文献处于逐年上升的趋势,近20年尤为明显。为强化低C/N进水系统的脱氮能力,众研究者从功能微生物角度研究了温度、进水水质、水量、微生物种类、碳源种类、碳源投加量等影响因素对反硝化脱氮功能菌的影响。此外,为实现碳减排、碳达峰的目标,除传统碳源甲醇、乙酸钠和葡萄糖等碳源[2]、其他新兴碳源如食品工业的废物产品[3]、富含甘油副产品的生物柴油[4]、通过分解剩余污泥获取有机化合物[5]等都被用来强化废水中生物去除氮磷营养物质的效果。在实际应用中,为达到减污降碳协同增效的目的,研究者们采用多种方式对污水处理实际运行过程中碳源投加量的优化进行探讨,包括理论计算方法的指导[6]、工艺参数的优化[7-8]、建立仿真模型[9]、依据水厂实际制定智能算法[10-11]等。
为从根本上减少碳源投加,一些新兴的技术被应用于处理低C/N实际污水。吕利平等[12]在进水C/N常年为2.5~5.0实际工程中发现,在确保出水达标的情况下,采取短程硝化反硝化技术可以降低83.3%的外碳源投量。王端浩等[13]总结了国内外学者对硫自养反硝化技术的研究进展,认为低氧曝气可以通过增强系统中自养反硝化菌的活性来降低反硝化脱氮过程对碳源的依赖。虽然在实际污水处理中,这些新兴技术及其组合工艺如混养反硝化、短程硝化反硝化耦合厌氧氨氧化、自养反硝化与厌氧氨氧化组合等工艺逐步受到研究人员关注,但其在实际工程中的推广应用还有待考究。
-
在实际工程中,污水中存在促进和抑制反硝化活性的物质,生物处理系统受水温、水质波动、微生物种类与活性等运行条件的影响,很难处于理想的反应条件,具体情况要比理想条件复杂得多。因此,单靠理论计算值指导碳源投加不够精准科学,为实现污水处理减污降碳、提质增效的目标,需根据实际情况对碳源投加量进行分析。在众多碳源精确加药的研究中,有实际应用认为可采用硝态氮仪表监控工艺单元的硝氮浓度,通过对硝态氮浓度实时准确测量来实时调整碳源投加量[6,14-15],即实现碳源精确投加目标的正确方法是控制外部碳源投入速度,使“缺氧区”中的硝酸盐浓度保持在所需的水平。但应该指出,NO3--N和NO2--N的及时精准测量在实际工程运行中较难实现,可见,有必要根据实际情况合理选择有效仪表数据并科学设置在线仪表数量和位置。
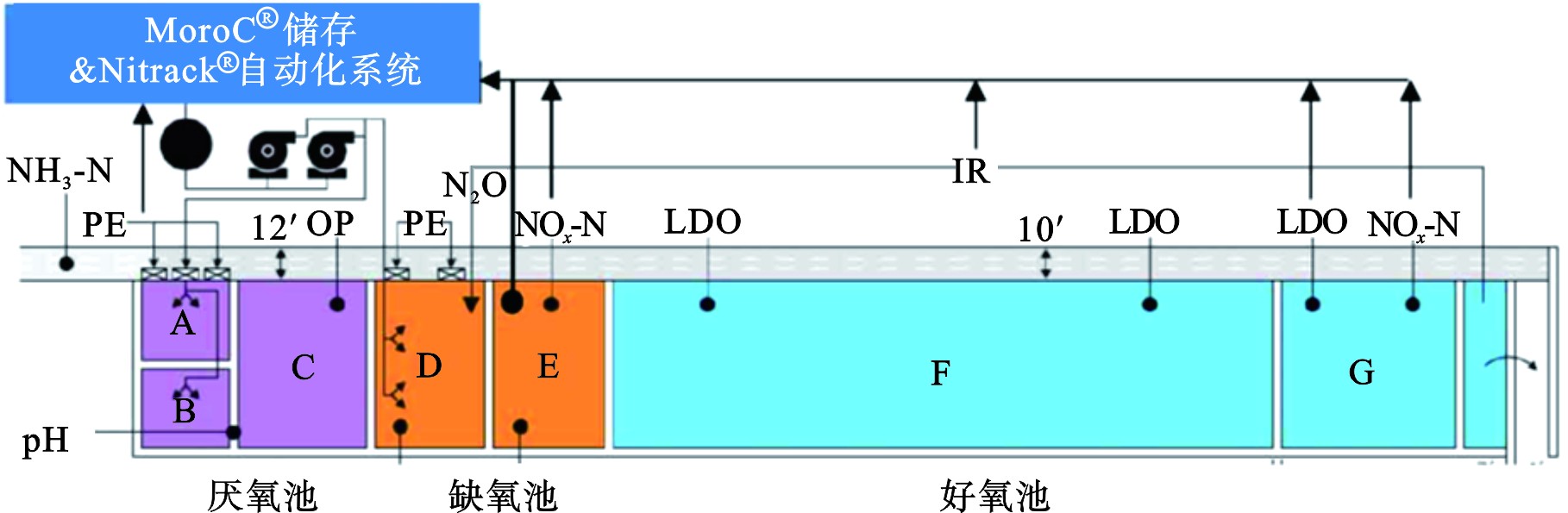
目前,国内应用较多的精准碳源投加方法主要有:(1)工艺管控措施精细化调控碳源投加量。李鹏飞等[14]通过污水处理厂实际运行经验提出从均衡进水负荷、调节运行参数、精细甲醇投加3方面的精细脱氮运行管控措施来提升反硝化生物滤池的精细调控能力,保障总氮精准达标。包遵胜等[10]制定了用于指导操作人员调控《甲醇加药量》,实施根据在线监测仪表指标,由PLC根据数学模型实时调控加药泵而自动化精确加药;(2)基于模型或智能算法的正、负反馈控制优化。ANDALIB et al[16]以硝酸盐为测量变量的前馈控制算法和以一氧化二氮为测量变量的反馈控制算法的组合,实现外部碳源投加量的自动化优化,并在目标氮极低的情况下减少N2O作为最有效的温室气体之一,见图4。吴宇行等[15]提出了基于在线硝态氮实时监测的碳源投加智能控制算法,开发的污水处理碳源智能投加控制系统,保障了青岛市某污水处理厂工艺稳定的前提下实现对碳源投加的精准控制。
-
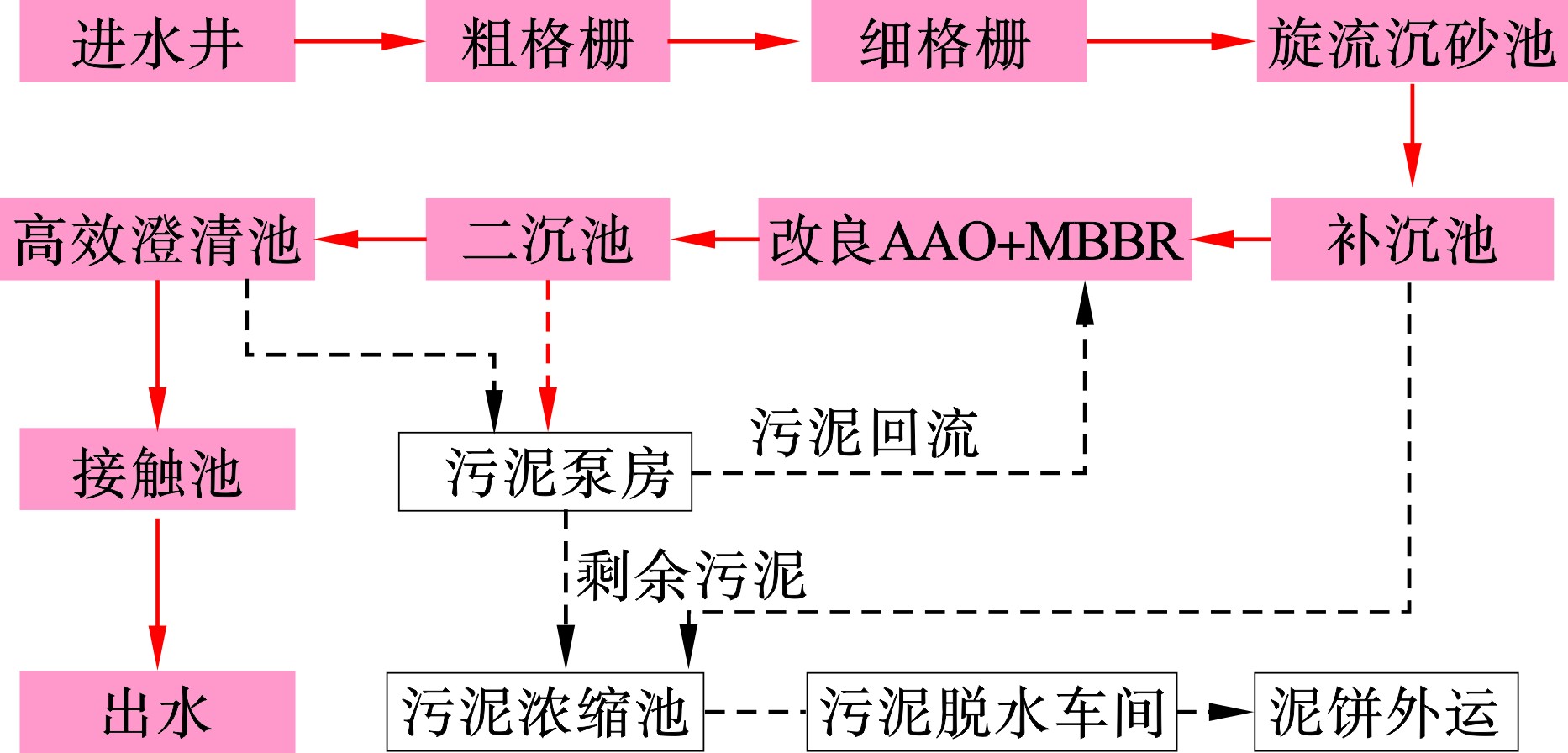
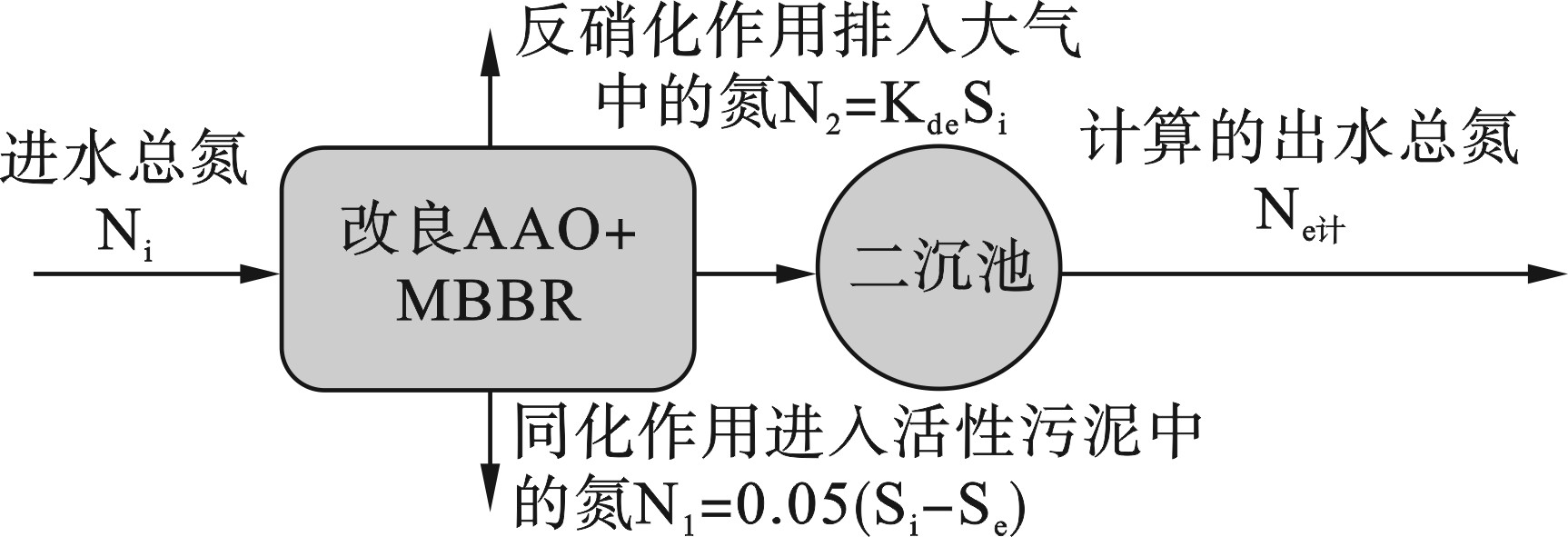
东北地区某城镇污水处理厂主体工艺采用改良A2/O+MBBR工艺,工艺流程图见图5,设计规模4.5万t/d,污水处理厂出水执行《城镇污水处理厂污染物排放标准GB 18918—2002》一级A标准。污水处理厂水质检测资料显示该厂全年进水水质波动较大,平均进水COD为210 mg/L,严重低于设计值500 mg/L,实际进水C/N比常年低于3,远低于设计标准4.5,5—8月期间此问题尤为突出,污水厂长期在低COD、高TN条件下运行,对微生物活性影响较大,水厂安全运行方面存在较大隐患。现场运行数据证实,当反硝化池污水BOD5/TKN值等于4~6时,通常表明碳源比较丰富,这一比值要求也和反硝化时间密切相关,如果反硝化时间太短,只有一部分能快速降解的BOD5,才能成为反硝化所需碳源,则所需BOD5/TKN值要更高。
为保证污水处理厂出水水质达标排放,现场进行了工艺运行调整并辅助投加碳源,具体措施如下:(1)开启旋流沉砂池至生化池的超越阀门,保证跨越初沉池进入生物处理系统的水具有更高C/N比;(2)低C/N运行期间,生物处理系统采用多点进水方式,考虑在缺氧段进水为反硝化过程提供更多碳源;(3)根据当日进水水质情况进行适量外碳源投加,投加位置在生化池缺氧段首端;(4)生化池DO值控制在2~4 mg/L,内回流开启至200%以上,及时检查外回流运行情况,保证污泥回流通畅。
-
在保证污水处理厂出水水质达标的前提下,外加碳源的选择需考虑经济性、安全性、环境友好性等因素。主要碳源类型的优缺点见表1,其中常用外加碳源有甲醇、乙酸钠和葡萄糖等,而食品工业废弃物因运输及投加因素限制目前应用较少。
理论上,甲醇是最理想的反硝化补充碳源,但因其缺点相对不适宜用于寒冷地区中小型规模的污水处理厂。该厂使用的麦可碳(MicroC 2000)没有传统碳源乙酸钠在低温下会结晶等问题,由于是液体,操作起来又比固体乙酸钠方便,经过计算相同水质条件下,麦可碳的理论投加量也远远少于乙酸钠的理论投加量,且该厂的实际应用也证明比乙酸钠有较大优势。特别的,使用甲醇的细菌比使用MicroC™的细菌对低温更敏感,在10℃时,使用MicroC™的细菌反硝化速率高于使用甲醇及乙酸钠[17],结合该地区冬季气温较低,且雨季进水水质较好,相比于甲醇、乙酸钠、葡萄糖作为碳源,高效碳源麦可碳在适用条件、经济等方面都无疑是该污水处理厂的最佳选择。
-
结合工艺运行措施的优化,当进水中COD浓度不足以满足生化系统反硝化脱氮所需碳源需求时,为达到出水总氮排放标准,补充的碳源量应恰好能去除系统依靠原水中碳源无法去除的氮量,生物处理系统需要外加碳源去除的氮量平衡计算见图6和式1。应该指出,外加碳源不同理论计算公式适用的前提是污水已充分硝化,出水氨氮已达到排放标准。
生物池氮平衡计算,见式(1):
式中:N为需要外加碳源去除的氮量,mg/L;Ns为出水总氮排放标准mg/L;Si为进水BOD;浓度,mg/L;Se为出水BOD浓度,mg/L;Kde为反硝化设计参数,kg NO3-N/kg BOD5;
-
式中:cm为必须投加的COD量,mg/L;
NO−3 -N为需要反硝化的硝态氮浓度,mg/L;NO−2 -N为需要反硝化的亚硝态氮浓度,mg/L;DO为缺氧池的溶解氧浓度,mg/L;3.7和2.3为理论计算值,每还原1 gNO−3 -N和1 gNO−2 -N为N2时,分别需要碳源3.7 g和2.3 g(以COD计)。(2)碳氮比差距弥补法,见式(3):
式中:TN为进水总氮浓度,mg/L;COD为进水中COD的量,mg/L。
(3)碳源投加简易计算公式。借鉴德国ATV-DVWK 规范[27]及标准中的ATV-A131E“单段活性污泥污水处理厂的设计”,通过大量实践的经验,得出反硝化1 kg
NO−3 -N需投加5 kg外部碳源(以COD计)更接近碳源实际用量[6],见式4。式中,5为反硝化1 kg硝态氮需外部碳源量(以COD计),kg COD/kg。
(4)麦可碳简化计算法。参照美国环保局(US EPA)建议工程实践中,典型甲醇投加剂量为1 mg/L NO3--N加入3 mg/L可以满足反硝化要求,即95%的硝态氮转化为N2后排放。结合黄良波等[28]的研究,换算成麦可碳后,由于麦克碳的BOD当量较高,以BOD当量作为换算系数更合适,将计算系数3换算为3/0.77×0.9=3.5。则公式可转化为式(5):
碳源投加化学反应方程式,见式(6):
上述4种计算中,各个公式计算原理不同。式(2)充分考虑了反硝化池中硝态氮、亚硝态氮及溶解氧消耗的碳源,相比其他公式更为复杂,适用于多段活性污泥法。式(3)是为弥补进水C/N<4,在污水处理厂日常运行中,可直接根据进水C/N确定是否需要外加碳源。计算过程较于式(2)简单,但进水COD中有机有效碳源的占比的变化会使计算值存在误差。式(4)、(5)建立了生物处理系统需要外加碳源去除的氮量平衡模型,是由大量经验得出的简化计算公式,有其各自的适用范围,只需要代入进水总氮浓度即可得出计算结果,目前应用最为广泛。
-
生化池中反硝化效率与水温密切相关,反硝化细菌的适宜生长温度为 20~40 ℃,低于15 ℃则反硝化速率明显降低。该厂所处地区2022年1—8月期间最低平均气温月为1月,平均温度-20 ℃,最高平均气温月为7月,平均温度28 ℃,进水水质水量见图7,进水水质、水量随季节波动较大。
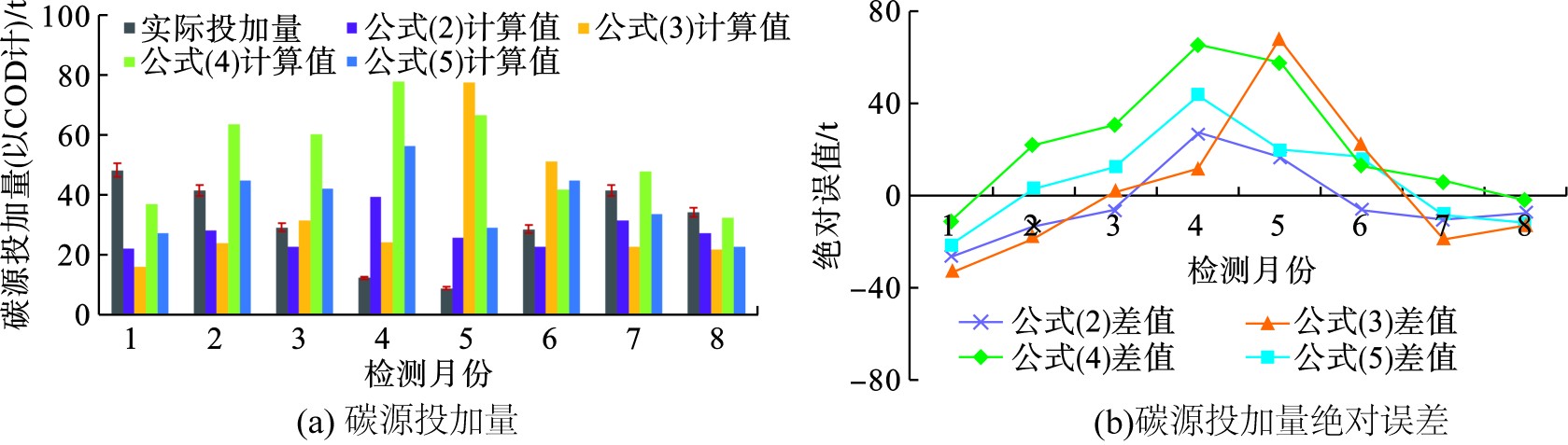
就生化技术而言,现场情况差别极大,不同技术源的投加标准均应当基于现场情况进行选择和调节。图8为该污水处理厂在2022年1—8月的碳源理论计算投加量和实际投加量的对比情况,该水厂生化池属于多段进水模式,所以式(2)理论计算值在正常情况下应与实际碳源用量更加接近。式(4)和(5)是基于考虑生物池氮平衡的碳源投加简易计算公式,相比于式(2)和(3),在碳源总量及各个月的投加量方面与实际投加值有更大的偏差,这可能与碳源的选择有关。因为目前的碳源投加公式大多是基于甲醇而确定的计算参数,而该厂的碳源为麦可碳。可以看出,基于上述4种计算的理论碳源投加量,即使式(2)计算值是最接近该厂实际碳源投加量,但二者之间仍存在不小差异。
以碳源投加计算式(2)为例,结合图7进水水质水量及当地气候条件,由于1月和2月水温低于10 ℃,反硝化反应效率低,为保证出水总氮达标,实际投加量往往大于理论计算值。进入3月份,水温逐渐升高,反硝化速率提升,实际投加量接近理论投加量。4月之后降水量逐渐增多,污水中污染物被稀释,浓度降低。导致污水污染物浓度降低,进水水质较好,如图8(a)所示,4、5月份碳源的实际投加量要比理论计算值低。而从6月份开始,理论投加值逐渐高于实际投加量,分析可能与进水水质变化有关,8月份的COD进水均值不足95 mg/L,且7、8月份水温较高,较高的活性污泥微生物活性加速了碳源的消耗,使得异养生物消耗更多的碳源。由此可见,该污水处理厂外加碳源实际投加量与理论计算值之间存在较大差异,这与黄良波等[28]的研究一致。
除温度、水量等因素的影响,污水中的水质指标中最重要的碳源指标COD又分为可溶性COD和非可溶性COD。一般而言,可溶性COD即可表征有效碳源的量,有效碳源是指能为微生物所利用的碳源。由于污水处理厂的进水水质中相同的COD中却含有不同的有效碳源,微生物所需的碳源应当是进水中的有效碳源与投加碳源的有效碳源之和,其中有效碳源在投加碳源中占比固定,使得理论计算值与实际投加量之前存在差异,现有的外加碳源理论投加公式很难指导污水厂外碳源投加。
-
(1)利用先进科技手段,在缺氧区设置氧化还原电位(ORP)、硝酸盐氮在线仪表等,根据检测数据分析系统运行工况,评估缺氧区反硝化效果,调节工艺参数,确定碳源投加方式。但这类技术方案因其较高的投资成本及复杂的操作,就目前而言并不具有推广价值。
(2)现存的碳源投加策略实施起来仍然复杂,需要较多高端的精密仪器监测及控制,从建设成本及运行成本考虑仍存在不足,理论碳源投加公式难以满足现有城镇污水处理厂多变的实际情况。实际污水处理的情况十分复杂,很难达到理想的反应条件。不仅污水中存在促进或抑制反硝化的物质,同时生化反应过程也受工程环境条件的限制,如果不考虑这种理论和工程实践的差异,将会造成较大的误差。通过现场小试实验确定最佳的投加位置,再利用相对准确的外加碳源理论值为参考进行现场小试实验,继而确定外加碳源的最佳投量,确保在出水水质达标的情况下,以这种更加精准科学的方式向生物池内补充碳源是目前更加理想的碳源投加策略。
(3)碳源投加过程中往往容易忽视N2O的排放,以小试的方式确定外加碳源类型、投加量还可以将N2O的排放量考虑在内,可以说开展现场小试实验是减少温室气体N2O的排放是实现碳减排、碳达峰不可忽视的一个重要措施。
-
结合东北地区某城镇污水处理厂实际运行经验,外加碳源的选择应在污水处理厂实际运行工况的基础上综合考虑经济、安全、环保等因素,麦可碳可作为寒冷地区污水厂长期外碳源投加的优势碳源选择。和污水处理厂达标排放实际碳源投加量相比较,四种不同碳源理论计算方法计算结果偏差较大,即理论计算值难以指导实际碳源投加需求,易造成出水水质、调试运行、成本效益核算全过程失真。考虑水温、水质水量的波动、系统中微生物群落结构与活性等因素均会造成碳源投加理论计算值与实际投加量之间的差异,有必要根据污水处理厂实际工艺运行合理设置在线仪表数量及安装位置,选择有效仪表数据实时调整碳源实际投加量,精准、科学地实现污水处理减污降碳的目标。
城镇污水处理厂碳源投加策略分析
Carbon Source Dosing Strategy of Urban domestic Sewage Treatment Plants
-
摘要: 低C/N进水条件造成的生物处理系统反硝化脱氮能力不足已成为我国污水处理厂运行面临的主要挑战。笔者应用文献计量学对目前碳源投加策略进行了总结,并以东北地区某城镇污水处理厂为考察对象,结合各碳源的实际应用情况介绍了目前常用的几种主流外加碳源的优缺点,分析了甲醇、乙酸钠、葡萄糖、麦可碳4种碳源投加公式计算理论值与实际碳源投加量之间存在差异的原因,旨在为城镇污水处理厂实现经济、高效、低碳运行碳源投加策略提供技术指导。Abstract: The lack of denitrification and nitrogen removal capacity of biological treatment systems caused by low C/N ratio in influent has become a significant challenge for the operation of sewage treatment plants. This paper summarizes the current carbon source dosing strategy using bibliometrics. Taking a municipal sewage treatment plant in Northeast China as an example, combined with the practical application of various carbon sources, the advantages and disadvantages of several mainstream external carbon sources commonly used are introduced. And the reasons for differences between the theoretical values calculated with the carbon source addition formula and the actual carbon source dosages of four carbon sources of methanol, sodium acetate, glucose, and MicroC. All these results aimed to provide technical guidance for the carbon source dosing strategy of urban domestic sewage treatment plants, which realize economical, efficient and low-carbon operation.
-
Key words:
- denitrification /
- urban sewage treatment plant /
- carbon source /
- carbon source dosing
-
甲醛的传统处理方法主要有吸附法[1]、植物净化法、等离子体技术、负离子技术和热催化氧化等,这些方法在处理室内甲醛时效果不佳。光催化氧化[2-4]和室温下催化氧化[5-6]作为新型催化氧化技术,是应用前景广阔的室内空气净化方法。尤其是光催化剂能够在室温下利用光能进行甲醛气体降解,对低浓度污染物去除效率也很高,并且能够长期起效,成为近年来的研究热点[7-9]。然而,由于室内的光线为可见光,光的强度也往往不高,单组分光催化剂在此条件下催化性能较低,因此,需要开发可见光响应型复合光催化剂,才能高效降解室内甲醛气体。
BiOBr是一种可见光催化剂[10],与其它材料复合能够有效提高其催化性能[11-13]。还原氧化石墨烯(RGO)具有优良的导电性和巨大的比表面积,BiOBr/RGO复合材料在可见光下具有很强的光催化活性,就是源于BiOBr的光生电子可以迅速迁移到RGO表面,从而有效提高了光生载流子的分离效率[14];而且,RGO对污染物有一定的吸附富集作用,这也对光催化剂的性能提高很有利[15]。应用光催化剂和多孔材料构建的复合催化剂具有很高的光催化降解性能,原因是多孔材料具有很大的比表面积、大量的孔隙、良好的分散性和很强的吸附性,可以吸附富集低浓度污染物,富集的污染物分子可以通过二者之间的界面从吸附剂向光催化剂转移[16]。硅藻土(diatomite,DT)是制备复合光催化剂的一种良好的多孔材料,它的多孔形态和表面羟基使其能够吸附富集空气或水中的污染物分子,提高光催化剂的性能[17]。基于吸附富集-光催化协同降解低浓度气态甲醛这一思路,使用BiOBr、RGO和硅藻土构建三元复合催化剂,会产生更好的协同作用效果。
本研究使用溶剂热法制备复合光催化剂BiOBr/RGO/DT,并对催化剂的形貌、组成和光吸收性能等进行详细表征。筛选出复合催化剂中硅藻土和BiOBr的最佳比例,并研究复合催化剂降解气态甲醛的机理。本研究可为室内气态甲醛和其他挥发性有机污染物的净化提供参考。
1. 材料与方法
1.1 仪器与试剂
电热鼓风干燥箱(DHG-9079A,上海一恒科学仪器有限公司),超声波清洗器(KQ-100B,昆山超声仪器有限公司),小型高速离心机(5427,德国Eppendorf),模拟日光氙灯光源(CEL-S500,北京中教金源科技有限公司),恒流泵(BT-100,上海沪西分析仪器有限公司);可见光分光光度计(L3,上海仪电分析仪器有限公司),X射线衍射仪(XRD,Bruker D8-advance),扫描电子显微镜(SEM,TESCAN MAIA3),X射线光电子能谱(XPS,ESCALAB 250Xi,Thermo Scientific),紫外-可见光谱仪(岛津 UV-2550),电子顺磁共振波谱仪(ESR,JES FA200),自动吸附仪(Micromeritics ,ASAP2010 V402A)。1-十六烷基-3-甲基溴咪唑(C20H39BrN2);乙二醇甲醚(C4H10O2);五水合硝酸铋(Bi(NO3)3·5H2O),甲醛(39~40%,CH2O),冰醋酸(C2H4O2),乙酸铵(CH3COONH4),乙酰丙酮(C5H8O2)均为分析纯;鳞片石墨粉和硅藻土为化学纯。
1.2 复合光催化剂BiOBr/RGO/DT的制备
首先,采用改进Hummers法制备了氧化石墨烯(GO),然后将GO还原为RGO[18]。复合光催化剂中RGO的添加量为相对于BiOBr的质量分数。复合光催化剂BiOBr/RGO/DT制备方法:将0.97 g Bi(NO3)3·5H2O和 1.16 g [C16mim] Br加入到 40 mL乙二醇甲醚中,磁力搅拌彻底溶解,标记为溶液A。以RGO添加量1%为例,取6.1 mL RGO溶液(1 mg·mL−1)和0.303 g硅藻土加入到40 mL乙二醇甲醚中,超声30 min后继续搅拌30 min形成悬浮液B。将溶液A和悬浮液B混合,继续搅拌30 min,然后装入100 mL水热釜中,在160 °C下反应2 h。反应完毕后,离心分离、收集沉淀物,并用去离子水和乙醇交替洗涤数次,在60 °C下真空干燥12 h,制备得到的复合光催化剂中硅藻土与BiOBr的理论质量比为0.5∶1,标记为BiOBr/RGO/DT-0.5。改变硅藻土的加入量分别为0.606、0.909、1.212和1.818,其它条件不变,按照上述步骤可以制备出光催化剂BiOBr/RGO/DT-1、BiOBr/RGO/DT-1.5、BiOBr/RGO/DT-2和BiOBr/RGO/DT-3。
1.3 甲醛降解实验和测定方法
自制的气态甲醛光催化降解实验装置总体积为约2.7 L,实验时处于密封状态。该装置的光照反应器具有石英玻璃窗口,500 W 氙灯作为光源,加装紫外线截止滤光片(UVcut 400)。将0.5 g 复合光催化剂BiOBr/RGO/DT分散在2 mL乙醇中制备成浆料,然后用油画笔均匀涂刷到固定面积的毛玻璃表面,避光干燥后放入光照反应器底部。连接好管路,盖上反应器的石英密封盖,管路可切换到干燥器管调节体系中空气的湿度。用微量注射器吸取一定量的甲醛溶液注入到缓冲瓶中。开启恒流泵,使甲醛溶液完全挥发。然后打开氙灯进行光催化降解反应。经过3 h反应完毕后,关闭氙灯和恒流泵,在进入缓冲瓶的管路前接入甲醛吸收管,然后打开恒流泵,循环吸收1 h后,再切换干燥空气继续缓慢吹0.5 h,将吸收液移入100 mL容量瓶中。反应用过的催化剂用去离子水洗涤、离心3次。洗涤液和吸吸收液合并一起定容,采用乙酰丙酮分光光度法[18]对甲醛的质量浓度进行测定。用式(1)计算甲醛的光催化降解效率。
η=C0−CtC0×100% (1) 式中:η为降解效率,%;C0为初始甲醛质量浓度,mg·L−1;Ct为降解时间为t时甲醛剩余质量浓度,mg·L−1。
2. 结果与讨论
2.1 催化剂的表征结果分析
1) XRD分析。使用XRD对硅藻土、BiOBr和复合光催化剂BiOBr/RGO/DT的晶相和成分进行了研究。如图1所示,硅藻土的谱图在2θ=21.9°、31.5°和36.1°处有3个特征峰,它们归属于SiO2的方石英石晶相(JCPDS卡号:39-1425)[19]。BiOBr的衍射峰归属于BiOBr的纯四方相(JCPDS卡号73-2061)[20]。复合光催化剂BiOBr/RGO/DT中出现的衍射峰分别归属于BiOBr和硅藻土,随着硅藻土含量的增加,硅藻土的特征峰也增强。硅藻土的存在不会影响BiOBr的晶相结构。BiOBr/RGO/DT图谱中没有发现RGO的峰,这是因为,RGO的量太低的缘故。未检测到其他杂质峰,这说明合成的催化剂纯度比较高。尖锐的衍射峰表明制备的材料具有良好的结晶度。
2) SEM分析。BiOBr、硅藻土和复合光催化剂BiOBr/RGO/DT-1.5的SEM图像如图2所示。从图2(a)可以看出,单一的BiOBr是由薄纳米片组成的纳米花球;硅藻土有很多的孔隙(图2(b)),这种高孔隙率的材料具有良好的吸附性能和较大的比表面积,适合作为纳米光催化剂的载体。制备的复合光催化剂BiOBr/RGO/DT-1.5(硅藻土含量60%)由大量BiOBr纳米片附着在硅藻土表面,分布均匀(图2(c)),从高倍SEM图可以看到,硅藻土表面附着了分散的BiOBr纳米片(图2(d))。硅藻土可以作为固体分散剂有效分散BiOBr,防止其聚集,暴露出BiOBr的活性位点。硅藻土的用量对BiOBr纳米片的分布有很大影响,随着硅藻土含量的增加,BiOBr的分布变的更加均匀,在硅藻土与BiOBr比例为1.5时,分布效果最好。由于RGO的量只有BiOBr的1%,所以在SEM图中很难看出来。在水热反应过程中,RGO与BiOBr复合,并一起结合在硅藻土表面。
3) XPS分析。用X射线光电子能谱研究了催化剂的元素组成和表面化学状态(图3)。以C1s峰(284.8 eV)校正所有的峰位置。从样品的全扫描图谱(图3(a))可以看出,纯BiOBr含有Bi、O和Br元素成分;硅藻土主要由Si和O元素组成;样品BiOBr/RGO/DT-1.5中的Bi、Br、O和Si元素的特征峰与BiOBr和硅藻土的元素特征峰相一致。采用高分辨率XPS研究了复合光催化剂BiOBr/RGO/DT-1.5的表面原子化学状态。对于纯BiOBr,Bi 4f7/2和Bi 4f5/2的峰分别位于159.64和164.95 eV处(图3(b)),Br 3d5/2和Br 3d 3/2的峰分别位于68.76和69.80 eV处(图3(c))。硅藻土的Si 2p轨道的结合能为103.37 eV(图3(d))。但是,在复合光催化剂BiOBr/RGO/DT-1.5中,Bi 4f7/2和Bi 4f5/2的峰分别位于159.30和164.61 eV处,Br 3d5/2和Br 3d3/2的峰分别位于68.36和69.40 eV。可以看出,相对于纯BiOBr,BiOBr/RGO/DT-1.5的Bi 4f结合能向低偏移0.35 eV左右,Br 3d的结合能向低偏移了约0.4 eV;而相对于纯硅藻土,Si 2p的结合能则向较高处偏移了0.22 eV。结合能的偏移表明复合光催化剂中硅藻土上的电子偏移到了BiOBr[21],这说明BiOBr和硅藻土的SiO2之间有较强的化学键作用。
4)紫外-可见漫反射光谱分析。所制备的催化剂的光学性质通过紫外-可见漫反射吸收光谱进行了研究。如图4(a)所示,BiOBr的吸收带边缘约为430 nm,与纯BiOBr相比,复合光催化剂BiOBr/RGO/DT的吸收边界基本没有变化。通过公式计算纯BiOBr的带隙[22]:αhν =A(hν-Eg)n/2。其中α,h,ν,A,n和Eg是光吸收系数,普朗克常数,光频率,常数,4(BiOBr作为间接跃迁半导体)以及带隙能量。因此,从图4(b)可看出,制备的BiOBr的带隙能(Eg)为2.71 eV。由莫特-肖特基图可以得出BiOBr的价带(VB)位置[23];图4(c)中p型光催化剂BiOBr的平带电势(Efb)约为2.60 V(vs. NHE),和它的价带电势(EVB)大约相等[24]。由公式EVB = ECB + Eg[25],可以计算出BiOBr的导带电势(ECB)的值为-0.11 V(vs. NHE)。图4(d)示意图描述了BiOBr的能带结构。
5) BET分析。图5分别为硅藻土、BiOBr和BiOBr/RGO/DT-1.5复合材料的N2吸附-脱附等温线和孔径分布。从图5(a)可以看出,硅藻土的 N2 吸附-解吸等温线显示出II 型等温线特点,这表明硅藻土中存在大孔隙[17, 26] 。BiOBr 和BiOBr/RGO/DT-1.5复合材料显示出IV 型等温线,其中 H2 和 H3 滞后线重叠,这说明材料存在墨水瓶状和狭缝状孔隙。材料的孔径分布如图5(b),BiOBr/RGO/DT-1.5的孔径主要分布为6~40 nm,硅藻土、BiOBr和BiOBr/RGO/DT-1.5复合材料平均孔径分别为10.6、16.4和18.9 nm。硅藻土的BET比表面积和孔容分别为8.09 m2·g−1和0.02 cm3·g−1;BiOBr的比表面积和孔容分别为24.06 m2·g−1和0.14 cm3·g−1;BiOBr/RGO/DT-1.5复合材料的相同分析值分别为21.75 m2·g−1和0.11 cm3·g−1。BiOBr/RGO/DT-1.5的比表面积和孔容大于硅藻土,比纯BiOBr的略小,这说明BiOBr纳米片在硅藻土表面能够很好地分散,从而增强了复合催化剂的多孔结构。
2.2 光催化降解气态甲醛的条件优化
1)复合催化剂中硅藻土和BiOBr的最佳比例。可见光照射下含有不同比例硅藻土和BiOBr的复合光催化剂降解甲醛的效果对比如图6(a)所示,降解效率随着硅藻土比例的增加而先增大后减小,在比例为1.5时具有最佳的催化性能。这是因为,复合光催化剂BiOBr/RGO/DT降解甲醛时按照吸附富集-光催化降解这一过程进行,吸附剂硅藻土和光催化剂BiOBr在一个特定的比例,才能让催化降解性能处在一个最佳平衡点。硅藻土对甲醛的吸附能力较高,当硅藻土含量较少时,BiOBr会完全覆盖硅藻土表面,削弱硅藻土吸附甲醛的作用,而且BiOBr会在硅藻土表面团聚,分散性不好,所以,复合催化剂降解甲醛的效率不高。当硅藻土和BiOBr比例为1.5时,复合催化剂BiOBr/RGO/DT-1.5中硅藻土含量为60%,此时BiOBr在硅藻土表面分散性好,活性位点暴露充分,而硅藻土表面也有足够的外露部分,导致吸附富集和光催化氧化都能够充分发挥作用,因此复合催化剂降解甲醛的效率就高。当硅藻土含量太多时,光催化剂BiOBr的量则相对太少,光催化降解甲醛的能力会显得不足。从BET分析结果可以看出,BiOBr/RGO/DT-1.5的比表面积略小于BiOBr,比纯硅藻土大很多,这说明BiOBr在硅藻土表面分散性好,提高了复合催化剂的比表面积,这有利于催化性能提升。
图6(b)为不同RGO含量(相对于BiOBr)的复合催化剂降解甲醛性能比较,其中硅藻土和BiOBr的比例固定为1.5。可以看出,随着RGO含量增加,复合催化剂降解甲醛的效率也随着提高。当RGO含量超过1%以后,催化效果的提高变得缓慢。由于RGO制备复杂成本较高,综合考虑催化剂的成本因素,本研究选择RGO的添加量为1%。
2)不同材料降解甲醛的性能对比和常见光源对甲醛降解率的影响。从图7(a)可以看出,硅藻土和硅藻土/RGO不具备光催化降解性能,而单独的BiOBr光催化降解气态甲醛的活性也不高,3 h只有55.7%的降解率,BiOBr/RGO的性能比BiOBr好,这是主要是因为RGO增加了BiOBr的光生载流子的分离效率所致。硅藻土与BiOBr按1.5∶1制备的BiOBr/DT 复合材料的性能比BiOBr/RGO好,而BiOBr/RGO/DT-1.5具有最佳的催化性能,对气态甲醛的去除率在3 h可达89.6%,是单独使用BiOBr的1.6倍。这是由于,硅藻土虽然没有光催化降解能力,但是吸附甲醛的能力比较强,可以吸附富集低质量浓度甲醛气体;当BiOBr表面上的甲醛分子被光催化氧化分解后,硅藻土上富集的甲醛分子会迅速扩散到BiOBr的活性位点上从而被分解。而单独的BiOBr吸附甲醛的能力较弱,所以光催化降解甲醛的性能比BiOBr/RGO/DT-1.5低。由BET分析可知,与纯BiOBr相比,BiOBr/RGO/DT-1.5复合材料的比表面积和孔容略小。但是由图7(a)中的小插图可以得出,BiOBr/RGO/DT-1.5对甲醛的吸附能力比BiOBr/RGO强很多,这说明硅藻土的加入提高了复合催化剂对甲醛的吸附能力,这可能是由于硅藻土表面羟基比较多,对甲醛的吸附能力较强所致[27]。此外,BiOBr纳米片在硅藻土表面的相对较高的分散性也是提高降解效果的另一个重要因素。气态甲醛的催化降解已有较多研究,如Pt-Ce/TiO2催化剂在55 min内可完全降解20 mg·m−3的甲醛[28];g-C3N4-TiO2/废沸石在LED光照下300 min对甲醛去除率为90%[16];H-TiO2@MG-D催化剂在180 min内可去除92%的甲醛[29];Bi2WO6纳米片负载Pt纳米粒催化剂在1 h内的去除率为93%[30]。和已有催化剂相比较,本催化剂性能相近,且成本低易制备。
图7(b)是常见的几种灯光照射下复合光催化剂降解甲醛的情况,氙灯效果最好,LED灯的最差。这种差异主要是灯的发光光谱范围不同造成的,由图4紫外-可见漫反射光谱分析可以看出,复合催化剂在光照波长超过430 nm以上的范围光响应很弱。
3)相对湿度对甲醛降解率的影响。实验密闭体系中空气的相对湿度对甲醛降解的影响如图8所示,使用0.5 g BiOBr/RGO/DT-1.5复合光催化剂在不同相对湿度下光催化降解甲醛,结果表明,最佳相对湿度为45 %。这是因为,空穴是通过氧化催化剂表面吸附的水分子和羟基来产生·OH的,适当的湿度有利于在催化剂表面形成·OH;而且,适当的湿度有利于甲醛的吸附和在复合材料上的转移。然而,如果空气相对湿度太高,由于H2O和污染物分子存在竞争性吸附,就会降低复合光催化剂对甲醛的吸附量,因此,甲醛的光催化降解效率也会降低;同时,湿度增加硅藻土也会吸附大量水分,甲醛易溶于水,从而难以与光催化材料作用而降解,所以也会导致光催化降解效率降低。
4)复合光催化剂的稳定性。为进一步研究复合光催化剂BiOBr/RGO/DT-1.5的稳定性,对其进行了甲醛光降解的催化剂循环使用实验。如图9所示,经过4个循环的光催化反应后,复合光催化剂BiOBr/RGO/DT-1.5的催化性能衰减很小。这表明其稳定性较好,适合长期使用。
2.3 光催化降解甲醛的机理分析
通过活性物种捕获实验检测了光催化降解甲醛过程中的主要活性物种(图10),当甲醛溶液中存在异丙醇(IPA)或三乙醇胺(TEOA)时,降解效率降低了50%以上;而当存在苯醌(BQ)时,降解效率降低约19%。该结果表明,羟基自由基(·OH)和光生空穴(h+)是主要的活性物种,超氧自由基(·O2−)在BiOBr/RGO/DT-1.5光催化降解甲醛的过程中也起着重要作用。
为了进一步证明·O2−和·OH的存在,用5,5-二甲基-1-吡咯啉N-氧化物(DMPO)作为捕获剂做了电子顺磁共振(ESR)实验。如图11(a)所示,在黑暗状态下没有峰出现,但是在可见光下发现了6个DMPO-·O2− 特征峰,并且信号强度随着光照射时间的延长而增加。这表明BiOBr/RGO/DT-1.5在可见光下产生了·O2−。在·OH实验中观察到了4个峰,峰的强度比为1∶2∶2∶1(图11(b))。这是典型的DMPO-·OH化合物的特征峰谱图,说明体系中有·OH生成[31]。ESR的这些结果表明,光催化降解过程中存在·O2−和·OH。
结合能带结构、捕获剂实验和ESR测试结果分析,可以得出BiOBr/RGO/DT-1.5光催化降解甲醛的机理(如图12所示)。复合光催化剂中的硅藻土有很强的吸附性能,可以将低浓度的气态甲醛分子吸附富集在催化剂上面,使得BiOBr能够和甲醛分子充分接触。在可见光照射下,BiOBr价带上的电子被激发到导带上。由于RGO具有良好的导电性和很大的表面积,光生电子可以迅速从BiOBr上转移到RGO表面,从而降低了BiOBr的光生电子和空穴的复合率;同时,光生电子能够与RGO上吸附的O2反应生成·O2–。当吸附在BiOBr表面上的甲醛分子被氧化分解后,硅藻土表面上富集的甲醛分子会扩散到BiOBr的活性位点上从而被进一步分解[32]。总之,BiOBr/RGO/DT-1.5能够高效降解气态甲醛得益于2个方面:1)复合催化剂中的光生电子和空穴得到有效分离;2)硅藻土能够吸附富集到甲醛分子。
3. 结论
1)制备了复合光催化剂BiOBr/RGO/DT。其具有良好的结晶度,不含其它杂质,BiOBr纳米片均匀附着在硅藻土表面,BiOBr和硅藻土的SiO2之间有很强的结合作用。
2)硅藻土与BiOBr按1.5∶1制备的复合光催化剂BiOBr/RGO/DT-1.5具有最佳的催化性能,对气态甲醛的去除率在3 h可达89.6%,是单独使用BiOBr去除率的1.6倍,催化剂使用的最佳空气相对湿度为45%。经过4个循环的光催化反应后,催化性能衰减很小,说明该催化剂稳定性较好。
3) BiOBr/RGO/DT-1.5对甲醛的光催化降解效率高,一方面是由于RGO导电性良好、表面积大,BiOBr导带上的光生电子可以快速迁移到RGO上面,从而实现光生载流子的快速分离;另一方面,硅藻土能够吸附富集低浓度气态甲醛,从而提高BiOBr对甲醛的接触氧化几率。
-
表 1 各类碳源及其优缺点
Table 1. Various carbon sources and their advantages and disadvantages
名称 优点 缺点 参考文献 常用外加碳源 甲醇 成本低、可大量获得、污泥产量低 是一种易燃易爆、神经毒性的化学物质,运输安全及成本等问题限制了其广泛应用 [1] 乙酸钠 易被利用,反硝化速率较快,适用于应急项目 运输费用高;产泥量大,污泥处理费用增加;价格较贵,基本不会大规模使用 [18] 糖类 糖类中以葡萄糖为代表作为外加碳源处理效果不错,其产品成本低、运输便捷、且容易被生物降解 易引起细菌的大量繁殖,使污泥膨胀,出水COD值升高,影响出水水质,易产生亚硝态氮积累的现象;需现场配制溶液,投加精准性差,大型污水处理厂无法使用;工业葡萄糖含杂质多而食品葡萄糖价格贵 [19] 复合碳源 反硝化速率高,成本降低 构成成分复杂 [20] 食品工业的废物产品 玉米淀粉加工废水 具有较高的有机浓度、良好的可生化性、毒副作用小、且氮、磷释放小 运输成本高、投加设备要求特殊 [3,21][22] 甜品、汽水、啤酒废水 乳品、肉类加工残渣 富含甘油的生物燃料副产物 麦可碳 MicroC不易燃,且来自可再生农产品,具有环境优势及经济优势 不经驯化污泥难以利用 [23] 粗甘油 粗甘油作为生物柴油的主要副产物来源丰富价格低廉 含有较多杂质、存在环境风险 [4,24] -
[1] PREFACE. Wastewater Engineering: Treatment and Reuse[M]. New York: McGraw Hill Education, 5th edition, 2014. [2] PAN Y, NI B J, BOND, P L, et al. Electron competition among nitrogen oxides reduction during methanol-utilizing denitrification in wastewater treatment. Water Research 2013: 47 (10), 3273–3281. [3] XIE T, ZENG Z, LI L L. Achieving partial denitrification using organic matter in brewery wastewater as carbon source[J]. Bioresource technology, 2022, 349: 126849. doi: 10.1016/j.biortech.2022.126849 [4] SCHROEDER A, SOUZA D H, FERNANDES M, et al. Application of glycerol as carbon source for continuous drinking water denitrification using microorganism from natural biomass[J]. J Environ Manage, 2020, 256: 109964. doi: 10.1016/j.jenvman.2019.109964 [5] ZUBROWSKA-SUDOL M, WALCZAK J, PIECHOTA G. Disintegration of waste sludge as an element bio-circular economy in waste water treatment plant towards carbon recovery for biological nutrient removal[J]. Bioresour Technol, 2022, 360: 127622. doi: 10.1016/j.biortech.2022.127622 [6] 周丹, 周雹. 污水脱氮工艺中外部碳源投加量简易计算方法[J]. 给水排水, 2011, 47(11): 38 − 41. doi: 10.3969/j.issn.1002-8471.2011.11.009 [7] 滕荣国, 庄新民. 城市污水厂减少外碳源投加量的研究[J]. 中国给水排水, 2013, 29(21): 65 − 68. doi: 10.19853/j.zgjsps.1000-4602.2013.21.016 [8] 支丽玲, 郑凯凯, 王燕, 等. 全流程分析AAO工艺碳源投加减量控制研究[J]. 水处理技术, 2021, 47(2): 119 − 121. doi: 10.16796/j.cnki.1000-3770.2021.02.023 [9] 孙月娣. Bardenpho工艺内回流与碳源投加耦合控制动态模拟[J]. 中国给水排水, 2017, 33(23): 66 − 70. doi: 10.19853/j.zgjsps.1000-4602.2017.23.014 [10] 包遵胜, 熊晓励, 刘纪成, 等. 某污水深度处理厂人工精细化调控碳源投加量的探究[J]. 环境工程, 2023, 41(4): 137 − 142. [11] 李晨修. 基于智能算法的污水厂碳源投加系统研究[D]. 武汉: 华中科技大学, 2021. [12] 吕利平, 李航, 庞飞, 等. 交替好氧/缺氧短程硝化反硝化工艺处理低C/N城市污水[J]. 环境工程学报, 2020, 14(6): 1529 − 1536. doi: 10.12030/j.cjee.201908121 [13] 王端浩, 李爱民, 李俊, 等. 硫自养反硝化技术研究进展与展望[J]. 环境保护科学, 2023, 49(2): 38 − 43. [14] 李鹏飞, 蒋奇海, 张达飞, 等. 北京某大型再生水厂反硝化生物滤池运行管控实践[J]. 给水排水, 2021, 57(4): 39 − 44. doi: 10.13789/j.cnki.wwe1964.2021.04.007 [15] 吴宇行, 王晓东, 陈宁, 等. 典型城镇污水处理厂碳源智能投加控制生产性试验[J]. 环境工程, 2022, 40(6): 212 − 218. [16] ANDALIB M, TAHER E, DONOHUE J, et al. Correlation between nitrous oxide (N2O) emission and carbon to nitrogen (COD/N) ratio in denitrification process: a mitigation strategy to decrease greenhouse gas emission and cost of operation[J]. Water Science & Technology, 2018, 77(1-2): 426 − 438. [17] IBRAHIM N E L S. Comparison of MicroC™ methanol and acetate as External carbon sources in removal of nitrate and Perchlorate from wastwater by denitrifying Enrichments[D]. Massachusetts: Environmental Engineering Northeastern University. 2008: 1-66. [18] 吴光学, 时运红, 魏楠, 等. 外加常规碳源污水反硝化脱氮研究进展[J]. 给水排水, 2014, 50(S1): 168 − 172. doi: 10.3969/j.issn.1002-8471.2014.z1.055 [19] 李弘义. 碳源投加量和污泥运行参数对污水脱氮效率的影响研究[J]. 海河水利, 2020(3): 45 − 48. doi: 10.3969/j.issn.1004-7328.2020.03.014 [20] 熊子康, 郑怀, 尚娟芳, 等. 污水反硝化脱氮工艺中外加碳源研究进展[J]. 土木与环境工程学报(中英文), 2021, 43(2): 168 − 181. [21] 曾祥专, 杨佘维, 卢欢亮, 等. 高值化利用废燕麦糖作为污水脱氮碳源的生产性研究[J]. 给水排水, 2018, 54(增2): 155 − 157. doi: 10.13789/j.cnki.wwe1964.2018.0341 [22] CARREY R, RODRÍGUEZ-ESCALES P, SOLER A, et al. Tracing the role of endogenous carbon in denitrification using wine industry by-product as an external electron donor: Coupling isotopic tools with mathematical modeling[J]. Journal of Environmental Management, 2018, 207: 105 − 115. [23] CHERCHI, CARLA, ONNIS-HAYDEN, et al. Investigation of MicrocTM as an alternative carbon source for denitrification[J]. Proceedings of the Water Environment Federation, 2008, 2008(13): 3149 − 3167. doi: 10.2175/193864708788733530 [24] CHONG-HAO B, MIN M, YONG N, et al. Process development for scum to biodiesel conversion[J]. Bioresource Technology, 2015, 185. [25] 给水排水设计手册[M]. 第5册. 北京: 中国建筑工业出版社, 2004. [26] 郑兴灿, 李亚新. 污水除磷脱氮技术[M]. 北京: 中国建筑工业出版社, 1998. [27] ATV-DVWK 专家委员会. 德国 ATV 标准 ATV-DVWK-A131E(单段活性污泥法污水处理厂设计)[M]. 德国: GFA 出版公司, 2000. [28] 黄良波, 奚洋, 黄世浏, 等. 低碳源污水AAO脱氮外加碳源计算方法研究[J]. 给水排水, 2021, 57(S1): 175 − 179. doi: 10.13789/j.cnki.wwe1964.2021.S1.036 -





 下载:
下载: