-
氮、磷污染是造成水体富营养化的主要原因,同时氮和磷也是一种重要资源,是生产农肥和畜禽饲料的原料。全球磷资源十分有限,且单向流动、难以再生。在现有技术、经济水平条件下,全球探明可供开采的磷矿资源不足100 a[1]。富含氮磷元素废水的排放不仅会造成氮磷的流失,还会造成地表水体富营养化。因此,高效回收废水中的氮磷资源,已成为相关领域的研究热点之一。
目前的氮磷共存水体主要是养殖废水、食品废水和市政污水。其中山东某食品公司产生的废水氨氮和总磷含量高达160 mg·L−1和100 mg·L−1,经过初沉池、UASB池、A/O池和二沉池处理后氨氮含量显著降低,但总磷含量依然高达77 mg·L−1[2]。此外,在甘肃某养牛场养殖废水中氨氮和磷酸盐质量浓度也高达1 304 mg·L−1和146 mg·L−1[3]。目前,最常用的脱氮除磷工艺为氧化沟工艺、A2O工艺和SBR工艺。但上述工艺对污水水质的稳定性要求较高,水质的大幅度变化会影响微生物脱氮除磷效果。此外,污水经二级处理后增加深度处理方能较好净化水质,但随之而来的是高昂的化学添加剂成本以及基建和电力费用。因此,寻找一种廉价的清洁材料用于同步、高效去除氮磷对于治理氮磷废水至关重要。
目前,磷酸铵镁(magnesium ammonium phosphate,MAP)结晶法往往具备同步实现对氮、磷的高效脱除和有效回收,广泛用于尿液、垃圾渗滤液、焦化废水的处理[4-6]。MAP英文俗名为struvite,中文俗称鸟粪石,化学成分为MgNH4PO4·6H2O,是一种较难溶于水的无色、白色(脱水后)、黄色、棕色或浅灰色的晶体,且含有氮、磷植物营养元素,是一种很好的缓释化肥[7-8]。其基本原理是在沼液中投加Mg2+,在碱性条件下使沼液中的PO43−、HPO42−、H2PO4−及NH4+与Mg2+反应成生MgNH4PO4·6H2O(struvite,即鸟粪石),从而回收水体的氮磷[9]。传统的MAP结晶法回收率较低,如磷结晶率达90%以上时,氨氮结晶率仅为13%左右,难以达到两者同步高效结晶[10]。鸟粪石的形成需要在较高的溶液pH条件下,需投加含Mg2+沉淀剂和碱溶液,原材料成本过高限制该方法的使用,且反应过后的材料回收困难[11]。HUANG等[12]利用镁盐改性天然沸石同步去除废水中的氮磷获得良好的去除效果。针对以上问题,选择一种自身碱性高、成本低和易回收的材料尤为重要。
常见镁来源有Mg(OH)2、MgSO4、MgCl2等。其中,MgO由于其安全稳定且自身碱性高等优点,受到广泛应用[10, 12-13]。生物炭比表面积大、离子交换能力强,可以去除水中的污染物[13-14]。并且生物炭表面呈负电荷,可以吸附水中的氨氮,但通常不能吸附磷酸盐。利用金属氧化物进行生物炭进行改性,可以有效改善其对磷的吸附性能[14]。生物质原料包括农业和森林残余物及其副产品(水稻秸秆[15]、小麦秸秆[16]、玉米芯[17]和菜叶[18]等)、动物粪便、造纸厂废料、城市固体废物和污泥[19-20]。选择市政污泥作为原料制备污泥基生物炭,具有来源稳定、成本低等优点,同时也为污泥的资源化利用提供了一种途径,具有良好社会意义。
因此,本研究开发了一种以镁离子为靶向供给、碱性调控能力强、成本低廉且易于回收的新型磁性污泥基生物炭复合材料(Mg/Fe sludge biochar, MF-SBC),用于废水中氮磷的同步回收。考察了初始pH、接触时间、共存离子、投加量对氮磷回收效果的影响,采用动力学模型等分析了回收特征,并结合XRD、XPS、SEM等多种表征手段探讨了新型磁性污泥基生物炭对水溶液中氮磷同步回收的作用机制,为其实际应用提供参考。
-
实验所用试剂包括七水合硫酸亚铁(FeSO4·7H2O)、六水合氯化镁(MgCl2·6H2O)、氢氧化钠(NaOH)、氯化铵(NH4Cl)和磷酸二氢钾(KH2PO4),以上试剂均为化学纯或分析纯。使用去离子水制备所有溶液。本实验原料取自中国江苏省武进区武南污水厂的脱水污泥,将脱水污泥在105 ℃条件下烘至恒重,研磨过200目筛,置于干燥器中备用。通过X射线荧光光谱仪检测到污泥粉末中主要的无机化学成分有SiO2、Al2O3、CaO、MgO、Fe2O3和P2O5。
-
MF-SBC的制备具体步骤如下:准确称取2.5 g干燥的污泥粉末加入到50 mL 0.2 mmol·L−1 FeSO4·7H2O溶液中浸泡并振荡6 h;将污泥/FeSO4混合溶液放入烘箱中经80 ℃烘干并研磨过200目筛,之后将其加入50 mL 1.25 mmol·L−1 MgCl2·6H2O溶液,并进行磁力搅拌30 min;随后,向上一步得到的混合溶液中缓慢加入50 mL 2.5 mmol·L−1 NaOH溶液并磁力搅拌12 h,紧接着陈化24 h;过滤以上溶液后所得沉淀物用去离子水反复清洗至中性,再经80 ℃烘干;将得到的干燥沉淀物放置管式炉中以5 ℃·min−1慢速升温至450 ℃,并在该温度下持续煅烧2 h,得到磁性MF-SBC。
-
分别使用KH2PO4和NH4Cl配置磷酸盐和氨氮储备溶液,并稀释至实验所需浓度。对于每批次实验,将一定量的MF-SBC材料加入到100 mL含有磷酸盐和氨氮的锥形瓶中,并用0.1 mmol·L−1 HCl和NaOH调节溶液至所需pH,之后将密封的锥形瓶置于恒温振荡器中振荡。反应结束后,取上层清液,用0.45 μm滤膜过滤后用UV-vis分光光度计(pharo300,merck, 德国)检测。分别考察了初始pH、氨氮和磷酸盐的质量浓度、MF-SBC投加量和反应时间对MF-SBC同步吸附氨氮和磷酸盐的影响,各批次实验的详细实验条件见表1。
-
1)生物炭表征。采用阶级开门扫描方式进行分析,扫描角2θ范围为10°~80°,工作电压和电流分别为60 kV和300 mA;分别利用扫描电子显微镜(SEM,SUPRA5,德国)和快速全自动比表面和孔径分析仪(BET,Autosorb-iQ2-MP,美国)来观察和测定微观形貌和比表面积;使用X射线光电子能谱仪(XPS,EscaLab 250Xi,美国)和能量色散X射线光谱(EDX)分析样品结构表面处的局部元素组成。在400~4 000 cm−1内通过傅里叶光谱仪(FTIR,Nicolet IS5 美国)记录红外光谱,鉴定所制备样品官能团。
2)溶液中污染物浓度的测定。采用国标钼酸铵分光光度法(GB11893-89)和纳氏试剂分光光度法(GB11893-89)测定溶液中磷和氨氮含量,每组3个平行样,到达反应平衡时,利用式(1)计算MF-SBC的去除量。
式中:Qe为吸附剂的吸附量,mg·g−1;C0为溶液的初始质量浓度,g·L−1;Ce为吸附后的溶液质量浓度,mg·L−1;V为溶液的体积,L;M为吸附剂质量,g。
-
为分析MF-SBC对磷酸盐和氨氮的吸附动力学情况,采用准一级动力学方程(式(2))、准二级动力学方程(式(3))和颗粒内扩散方程(式(4))对其进行拟合。
式中:t表示吸附时间,min;Qt表示t时吸附剂的吸附量,mg·g−1;Qe表示吸附平衡的吸附量,mg·g−1;k1为一级速率常数,min−1;k2为二级速率常数,g·(mg·min)−1;kp表示颗粒内扩散速率常数,mg·(mg·min)−1;C是常数,为颗粒内扩散方程的截距。
-
吸附实验结束后,过滤收集MF-SBC,用1 mol·L−1 NaOH溶液超声30 min并静置浸渍1 h,再用去离子水冲洗至pH为中性后烘干,干燥保存并用于下一次的循环使用。
-
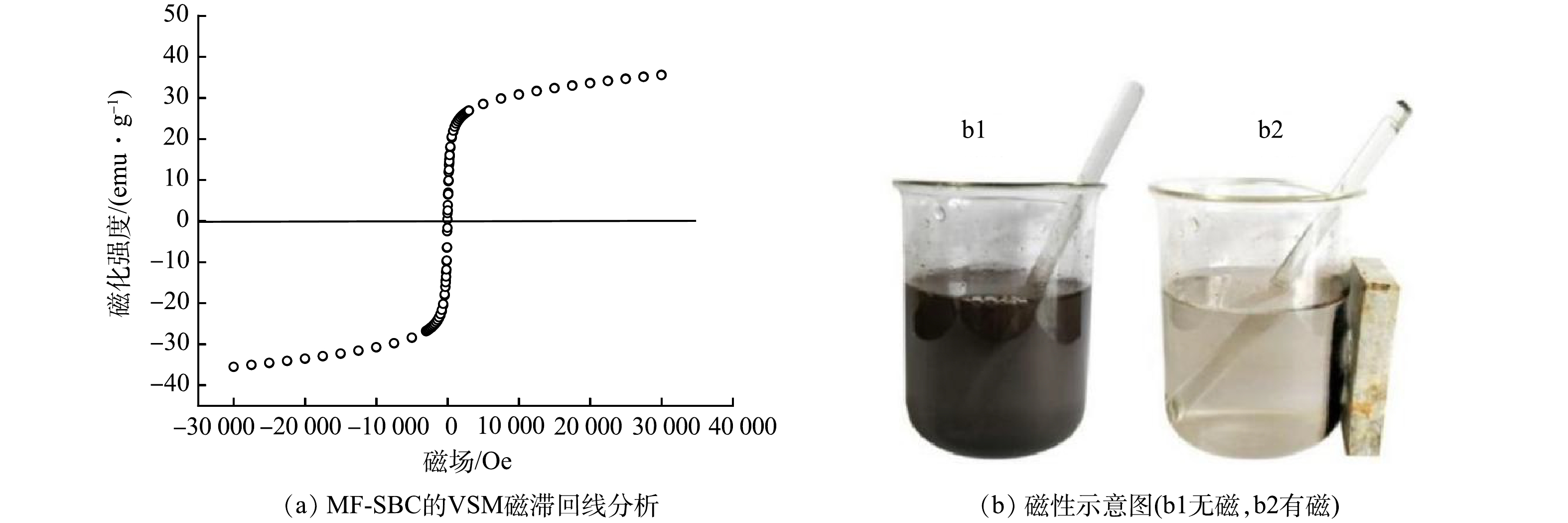
为了确定MF-SBC的磁性,在室温下通过振动样品磁强计(VSM)来测量材料的磁性,得到磁滞回线(图1(a))。由图1(a)可以看出,MF-SBC的曲线显示出正常的S形窄磁滞回线,饱和磁化强度为52.48 emu·g−1。曲线的剩磁和矫顽力几乎为零,表明MF-SBC具有超顺磁特性。MF-SBC的超顺磁行为有利于同步吸附水溶液中的磷酸盐和氨氮,并且外部磁场可以从处理溶液中将材料分离出来。如图1(b)所示,可使用磁铁能够将吸附后的MF-SBC从溶液中分离出来,这便于材料的回收。
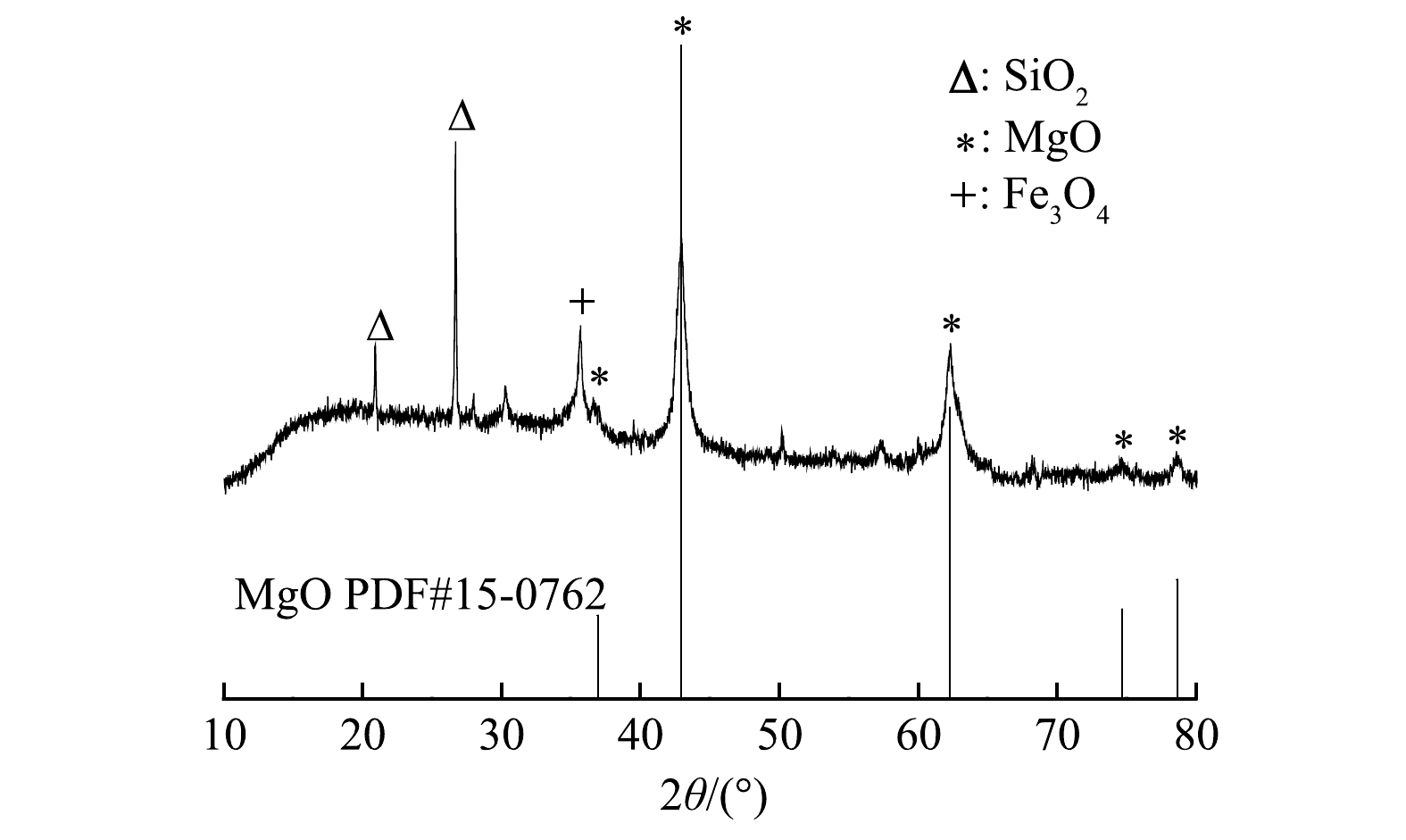
由图2可以看出,在2θ=35.66°处有一个对应于Fe3O4的衍射峰。这表明MF-SBC中含有Fe3O4,解释了MF-SBC具有磁性的原因。在2θ为20.98°和26.66°处可以观察到SiO2的衍射峰,这是污泥中自带的杂质成分。此外,在2θ为42.94°、62.30°、74.67°和78.64°处均有衍射峰,与MgO标准卡片 (PDF#45-0946) 高度吻合,可判定生物炭中含有MgO,表明MF-SBC是富含MgO颗粒的磁性污泥生物炭。
吸附剂的表面形貌和微观结构特征与材料的吸附性能有着密切联系,是材料表征的一个重要参数。图3为MF-SBC在不同放大倍数下的SEM表征结果。可见,随着放大倍数的增加,MF-SBC表面呈不规则形态,具有稠密生长的团聚颗粒。这可能是嵌入到生物炭表面的MgO颗粒,致使MF-SBC比表面积大,反应位点多,镁离子可以在溶液中不断释放,因此有利于对氨氮和磷酸盐同步回收。
MF-SBC吸附氨氮和磷酸盐前后的N2吸附脱附曲线见图4。由图4可以看出,吸附前后MF-SBC对氮气的吸附脱附属于IV型吸附等温线,在相对压力为0.4~1.0时有明显的滞回环,且吸附后的滞回环大于吸附前。这表明吸附后MF-SBC上部分介孔变成了微孔[20-21]。此外,从孔径分布图看出,吸附后MF-SBC表面孔径有所变小。
利用BET法可以计算同步吸附氨氮和磷酸盐前后MF-SBC的总孔体积、平均孔径和比表面积。可以看出,MF-SBC的总孔体积、平均孔径和比表面积分别为0.16 m3·g−1、10.99 nm和58.99 m2·g−1,平均孔径为2~50 nm,属于介孔结构。在MF-SBC同步吸附氨氮和磷酸盐后,总孔体积、平均孔径和比表面积均有所下降,分别为0.12 m3·g−1、10.24 nm和48.69 m2·g−1,与N2吸附脱附曲线的分析相一致,表明同步吸附氨氮和磷酸盐后,MF-SBC表面孔隙发生堵塞,这可能由于MF-SBC将磷酸盐和氨氮吸附到其表面并占据了部分吸附位点。
-
如图5(a)所示,当pH为3.0~11.0,MF-SBC对氨氮的吸附量大于对磷酸盐的吸附量,氨氮和磷酸盐的吸附量都是随着pH的升高而变大。在pH为9.0~11.0时,氨氮和磷酸盐的吸附量随着pH的升高而降低,在pH为9时,氨氮和磷酸盐最大吸附量分别为85.8 mg·g−1和209.95 mg·g−1。△pH为吸附后溶液的pH减去溶液初始pH。如图5(b)所示,在初始溶液pH为8.8时,△pH为0,表明MF-SBC的pHpzc在8.8左右。另外,MF-SBC的Zeta电位值变化也证实了这一点。因此,当溶液pH小于8.8时,MF-SBC表面带正电荷,且pH越低,MF-SBC所带的正电荷越强越易吸引带有负电荷的磷酸盐而排斥带有正电荷的铵根离子。反之,当溶液pH大于8.8时,MF-SBC表面则呈负电荷。在溶液pH为11时,氨氮表现出极低的吸附量,这可能是高pH溶液会使大量的NH4+水解并挥发成NH3,进而降低氨氮吸附量。
-
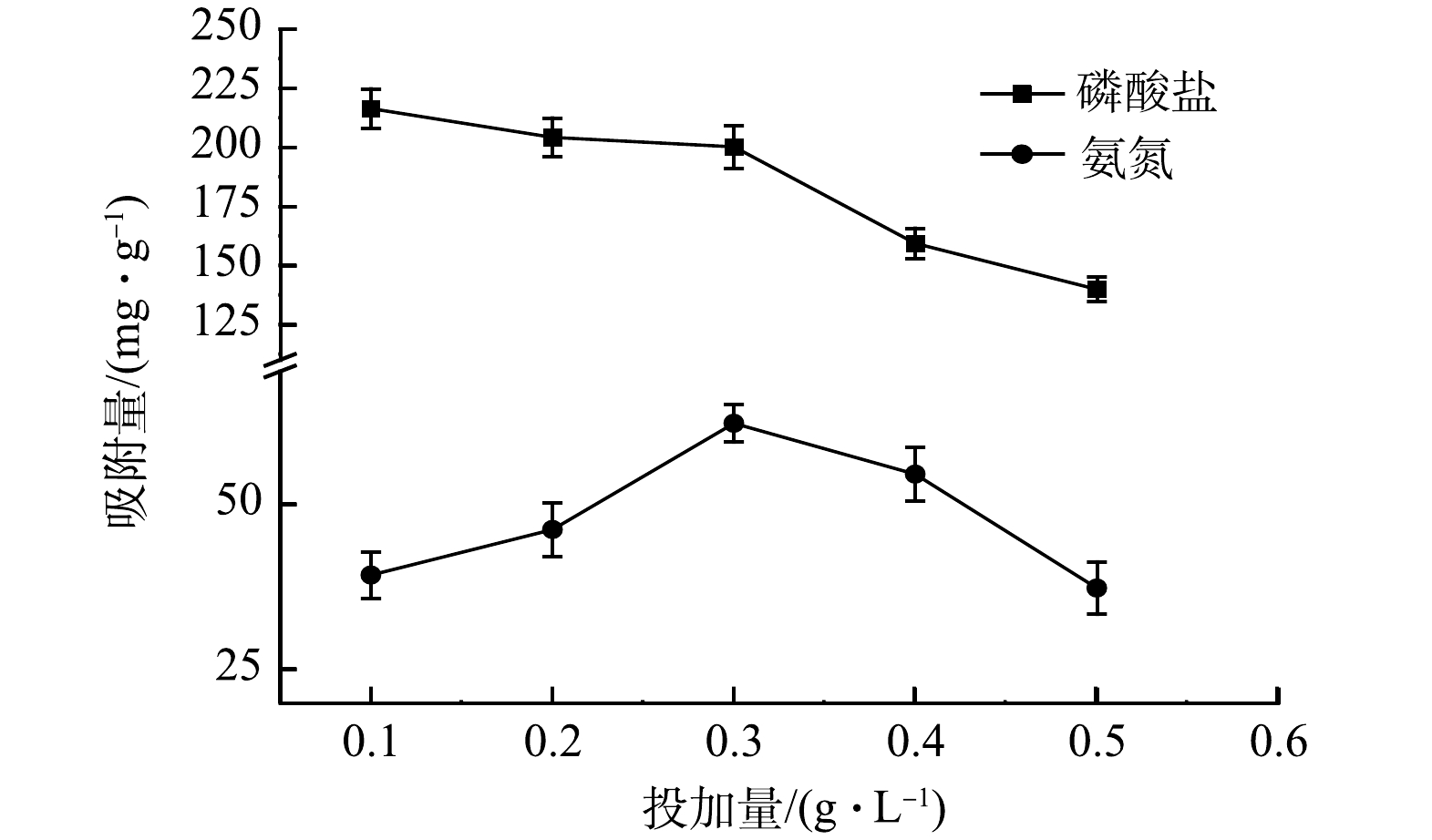
由图6可以看出,MF-SBC的投加量从0.1 g·L−1加至0.3 g·L−1时,氨氮的吸附量有明显的增加,而继续增加投加量后,氨氮的吸附量开始减小。对于磷酸盐的吸附,从0.1 g·L−1加至0.3 g·L−1时,磷酸盐的吸附量缓慢减小,几乎无变化;继续增加投加量后,磷酸盐吸附量有大幅度的减小。因此,当MF-SBC的投加量为0.3 g·L−1时,同步吸附溶液中氨氮和磷酸盐的效果最佳。造成这种现象的原因可能是,MF-SBC投加量的增大降低了磷酸盐和氨氮与单位质量MF-SBC比值,此时,吸附位点仍然保持不饱和状态[22]。
-
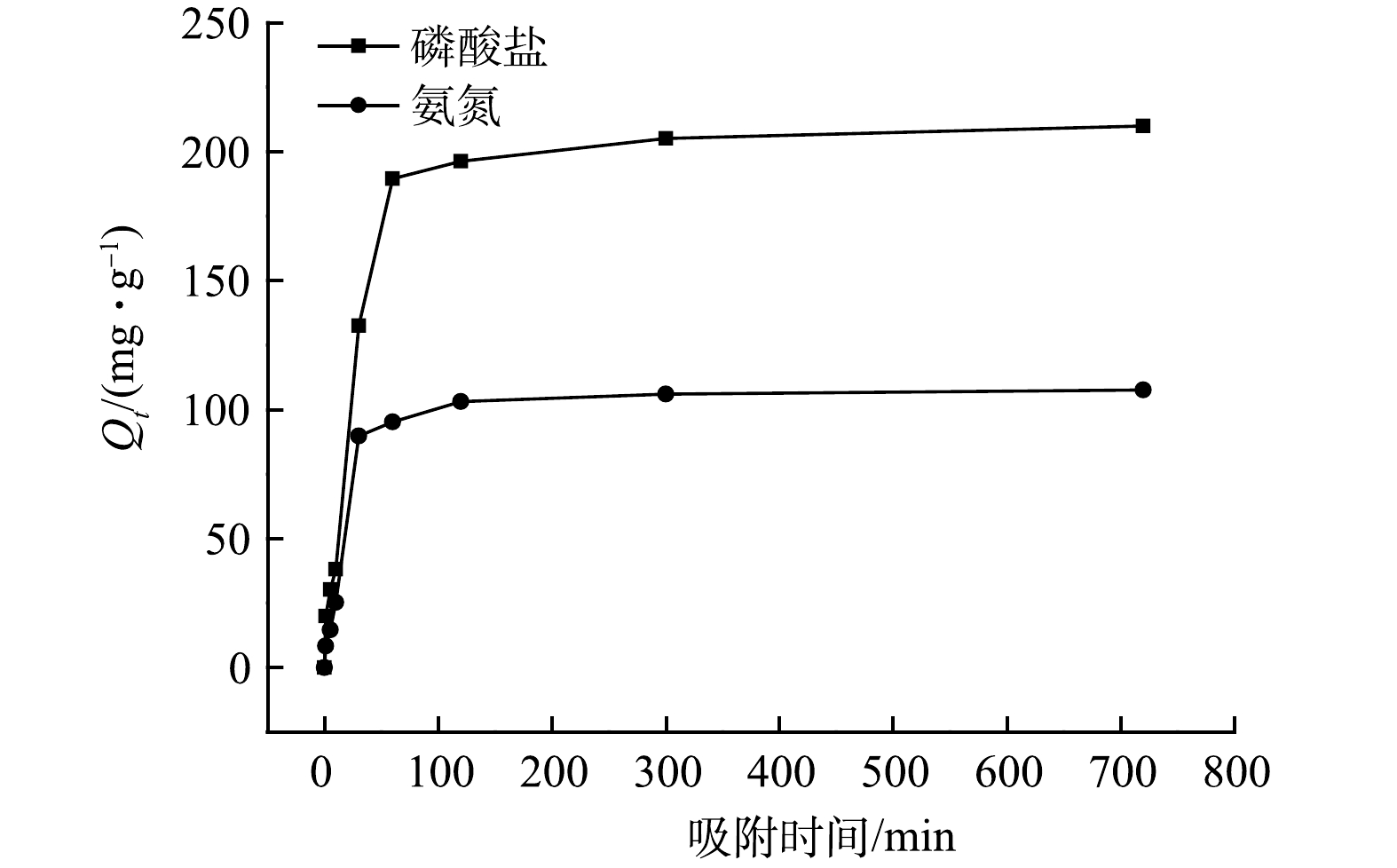
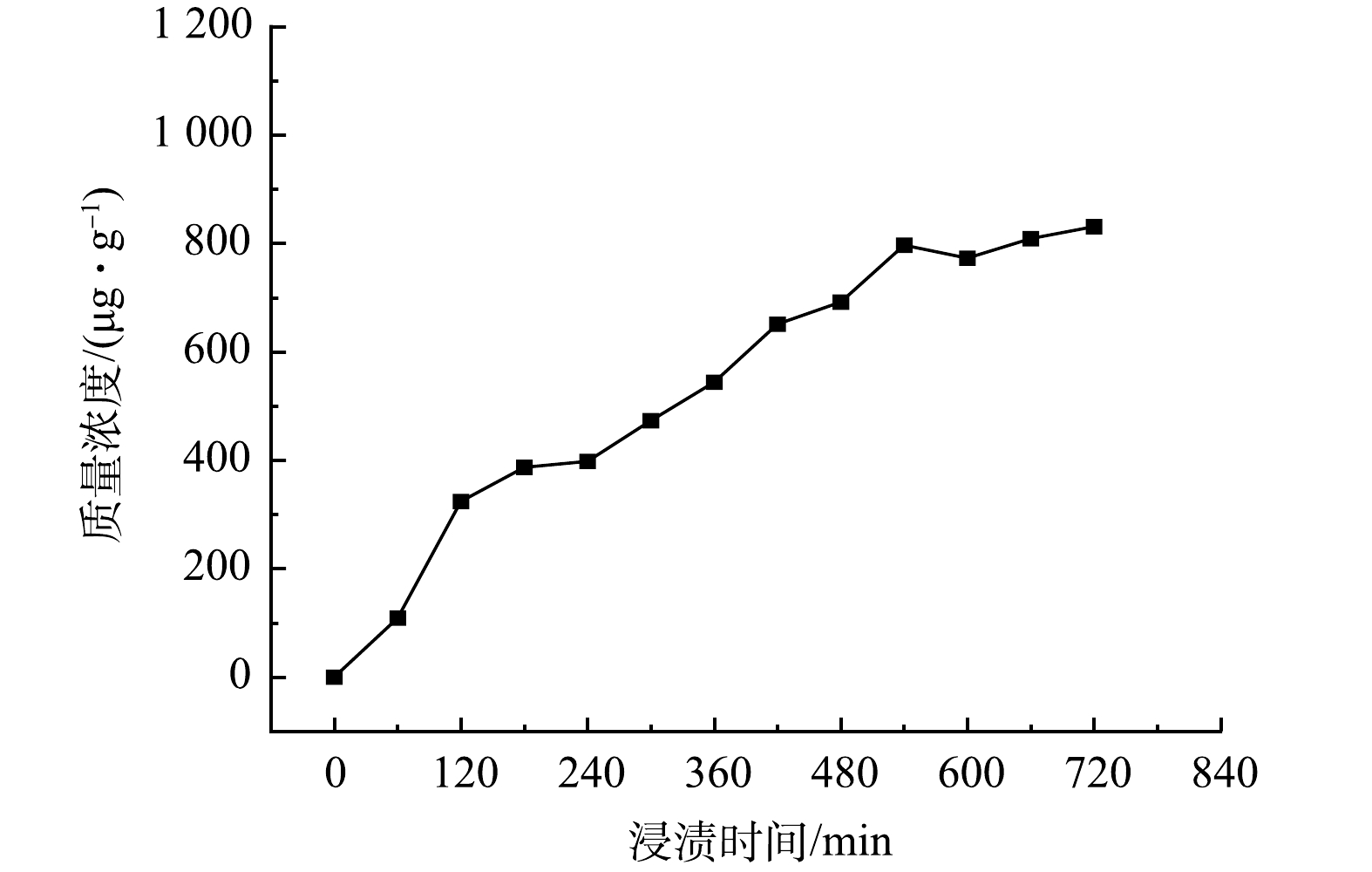
图7反映了在初始pH为9的情况下,接触时间对MF-SBC同步吸附溶液中氮磷的影响。可见,在0~60 min内,MF-SBC对氨氮和磷酸盐的吸附量急剧上升,再缓慢增加到120 min后达到吸附平衡状态,此时氨氮和磷酸盐的吸附量分别达到了103.12 mg·g−1和205.07 mg·g−1。在MF-SBC同步吸附溶液中氨氮和磷酸盐的初期,MF-SBC表面含有大量的吸附位点和镁离子,反应容易进行,但随着反应的进行,MF-SBC表面吸附位点被逐渐占据,且镁离子浓度也随之减低,不利于反应的进行。
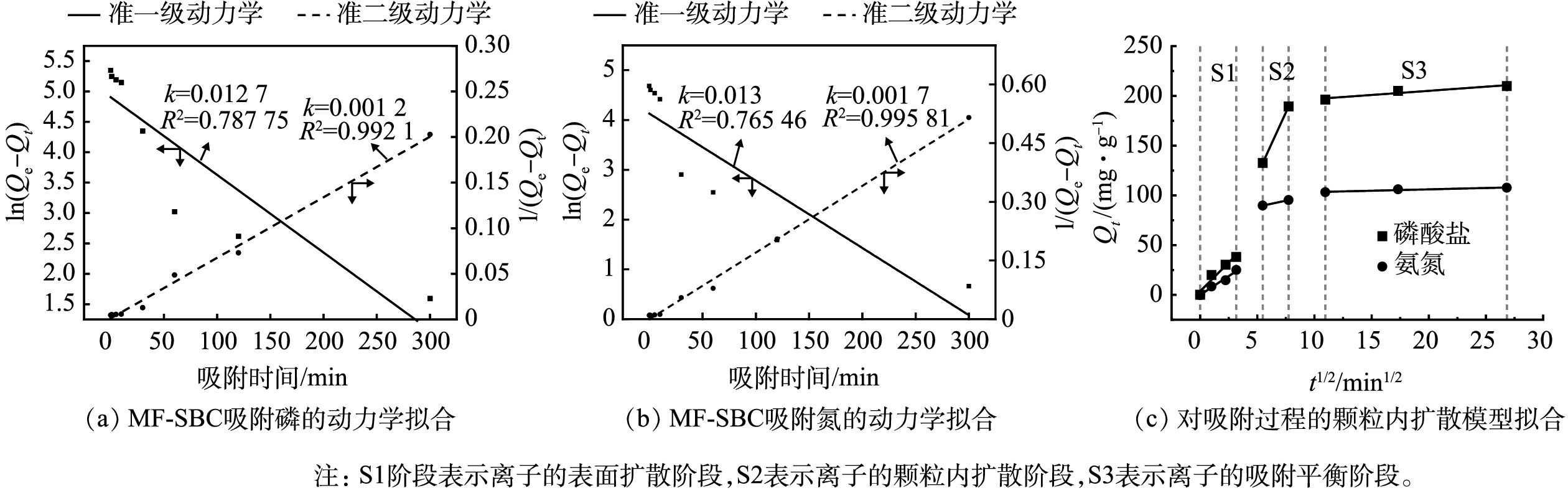
为进一步分析MF-SBC对氨氮和磷酸盐的吸附过程,采用准一级动力学和准二级动力学模型对吸附数据进行拟合,结果见图8和表2。对于氨氮和磷酸盐,准二级动力学模型的拟合系数均高于准一级动力学模型,Qe的计算值与实际值更相近,表明吸附过程更符合准二级动力学,这说明吸附过程是以化学吸附为主,其中可能包括阳离子交换、络合和沉淀[23]。另外我们还拟合了吸附数据的颗粒内扩散模型(图8(c)和表3),其中S1阶段表示离子的表面扩散阶段,S2表示离子的颗粒内扩散阶段,S3表示离子的吸附平衡阶段[24]。结果表明,S1阶段所占时间最长,因此吸附过程是以S1阶段的表面扩散为主。此外,S1阶段的拟合直线斜率不为0,这表明吸附过程不仅仅只有表面扩散阶段,还包含颗粒内扩散阶段[21,25]。
-
在实际废水中往往存在很多共存离子,由于这些离子由于本身都带有电荷,可能会与水中的氨氮和磷酸盐形成竞争吸附关系。Ca2+、Na+、SO42− 3种离子对MF-SBC同步吸附氨氮和磷酸盐的影响,结果见图9。由图9可以看出,Ca2+对MF-SBC吸附磷酸盐基本无影响,对氨氮的吸附有抑制作用,且Ca2+的浓度越高,抑制效果越明显,当Ca2+的浓度为100 mg·L−1时,MF-SBC对氨氮的吸附量仅为56.33 mg·g−1。这可能是由于Ca2+会与磷酸盐发生反应生成羟基磷灰石(Ca(PO4)6(OH)2)[25],不利于鸟粪石沉淀的生成。此外,Ca2+在溶液中易水解释放H+,降低溶液pH,从而抑制氨氮的去除。Na+、SO42−对MF-SBC吸附氨氮和磷酸盐几乎没有影响。
-
MF-SBC的回收率以及用于循环实验后对离子的去除率是影响材料后续应用成本的重要指标。MF-SBC经过Fe改性,4次循环实验后,回收率依然高达62.99%(图10)。结果表明,在循环实验中,MF-SBC对氨氮的吸附容量由103.11 mg·g−1降至75.63 mg·g−1,对磷酸盐的吸附容量由204.97 mg·g−1降至173.22 mg·g−1。这可能是由于在去除氨氮和磷酸盐的过程中Mg2+的消耗所导致的,但总的来说,MF-SBC对氨氮和磷酸盐吸附容量分别仅下降了26.65%和15.49%,仍具有较高的去除率。
-
在溶液初始pH为9时,磁性污泥生物炭MF-SBC对氨氮和磷酸盐的吸附机理主要有以下几种。表面吸附机理:MF-SBC作为负载MgO颗粒的污泥基生物炭材料自身具有较大的比表面积和孔体积,能够将氨氮和磷酸盐吸附到其表面。离子交换机理:MF-SBC材料中除Mg2+外,还包含一些来自污泥的碱金属,如Na+、Ca2+和K+等。这些金属离子附着在生物炭表面会与溶液中的NH4+发生离子交换反应,如反应式(5)和式(6)所示。此外,MF-SBC中的羟基也会与磷酸盐离子发生离子交换反应,如反应式(7)所示。为了判断离子交换去除氮磷的可能性,对MF-SBC在pH为9的条件下进行了浸渍(图11)。结果表明,只有微量Ca2+存在溶液中,有部分氨氮是通过离子交换固定在MF-SBC表面。但Ca2+数量极少,以Ca2+为主的离子交换并不是主要的去除机理。此外,由Mg1s的XPS图谱中可以看到,吸附后Mg1s的峰面积相比于吸附前降低了26.14%,这也是在吸附过程中Mg以离子交换形式去除氨氮和磷酸盐的直接证据[26-28]。
鸟粪石沉淀机理。在初始pH=9的条件下,表面吸附和离子交换对氨氮和磷酸盐的回收能力有限,并不能做到生物炭对氨氮和磷酸盐的高效同步回收,其主要回收方式是鸟粪石沉淀法。当初始溶液pH=9时,磷酸盐的主要存在形态为HPO42−和PO43−,氨氮在溶液中的存在形态是NH4+。此时,当MF-SBC中的镁离子释放到溶液中,会与磷酸盐离子和NH4+反应形成鸟粪石沉淀(式(8)和式(9))。可见,在形成鸟粪石过程中会有一定量的H+释放到溶液中,解释了反应后溶液pH变低的现象,同时H+的增加,也促进了MF-SBC表面MgO的水解,进一步促进了鸟粪石沉淀反应的发生。
通过红外和XRD分析可以鸟粪石沉淀的生成。由图12(a)可以看出,对于吸附前后的MF-SBC,在3 458 cm−1的宽吸收带和1 634 cm−1的峰归因于H—O—H水分子的伸缩峰与弯曲振动峰。吸附后的谱图在1 438 cm−1和1 079 cm−1处生成了2个明显的特征吸收峰,分别对应于NH4+和PO43−,这表明NH4+和PO43−都存在于回收的MF-SBC中。图12(b)是回收产物的XRD谱图。可以看出在2θ为14.98°、15.92°、20.87°、30.24°、31.90°、33.17°和46.36°处有明显的高强度衍射峰,与鸟粪石的标准卡片 (PDF#15-0762) 基本吻合。表明回收产物中含有大量的鸟粪石晶体,进一步证实了鸟粪石沉淀是MF-SBC同步吸附溶液中氮磷的主要作用机制。
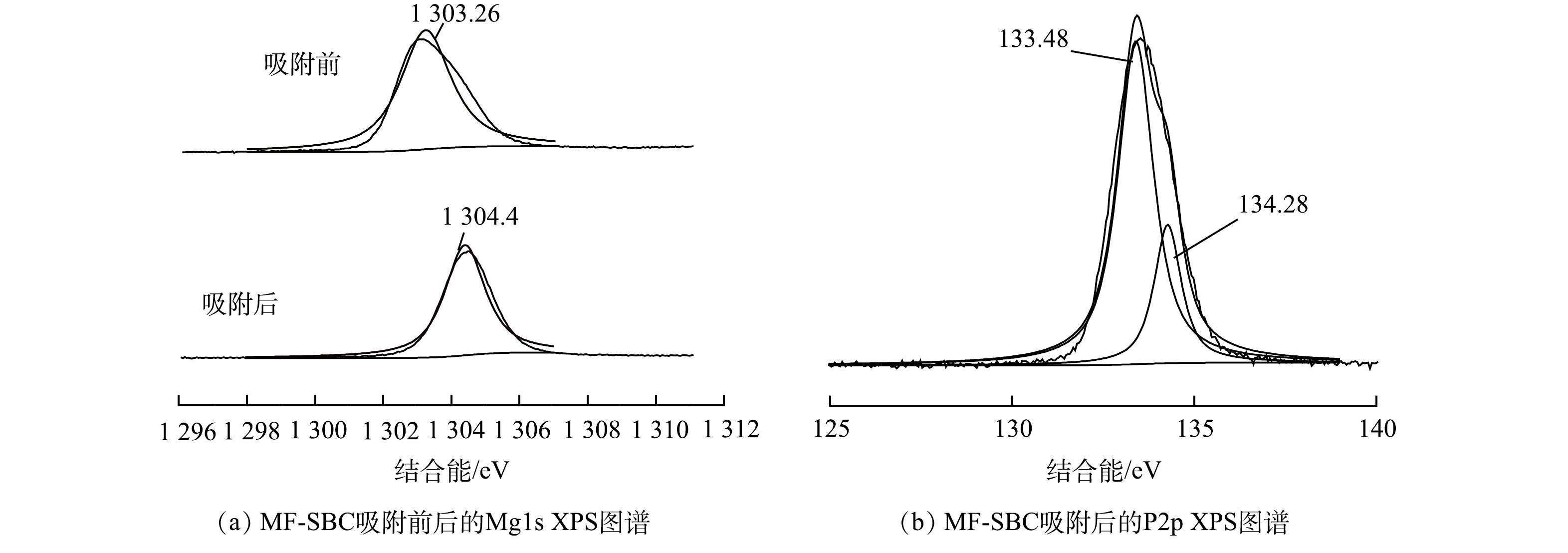
由图13(a)可以看出,吸附前后MF-SBC中Mg元素的特征峰分别在1 303.26 eV和1 304.42 eV处,归属于不同的Mg形态。吸附前位于1 303.26 eV处的特征峰表明Mg以金属氧键的方式,即氧化镁的形式存在;而反应之后在1 304.42 eV处的特征峰则归属于Mg的非金属形态,表明镁离子参与反应生成了鸟粪石沉淀。由图13(b)可见,不同形态的磷所处的结合能不同,吸附后MF-SBC的P2p峰可分为133.48 eV和134.28 eV 2个单峰,分别是鸟粪石沉淀表面的P=O和P—OH官能团。
-
1)通过煅烧法,成功合成了磁性污泥基生物炭MF-SBC,其表面含有大量的氧化镁颗粒,比表面积为58.99 m2·g−1,饱和磁化强度为52.48 emu·g−1。
2)在MF-SBC投加量为0.3 g·L−1,溶液初始pH为9时,MF-SBC同步吸附氨氮和磷酸盐的吸附量最大,分别为103.12 mg·g−1和205.07 mg·g−1,且吸附过程符合准二级动力学方程。Ca2+、Na+、SO42− 3种离子对磷酸盐的吸附无影响,而Ca2+和SO42−对氨氮的吸附有抑制作用。
3)在初始溶液pH=9的条件下,MF-SBC对水溶液中氨氮和磷酸盐同步吸附的作用机制包括表面吸附、离子交换和鸟粪石沉淀,其中鸟粪石沉淀为主要作用。
磁性污泥基生物炭的制备及其对水溶液中氮磷的同步回收
Preparation of magnetic sludge-based biochar for the simultaneous recovery of nitrogen and phosphorus from aqueous solution
-
摘要: 以城市污泥为原料与MgCl2和FeSO4复合,并热解碳化合成磁性污泥基生物炭(MF-SBC),用于水中氮磷的同步回收研究,分别考察了MF-SBC投加量、初始pH、接触时间和共存离子对氮磷回收性能的影响,同时通过SEM、XRD、BET、XPS和FTIR表征了MF-SBC的组成、形貌和官能团等,并对反应过程进行了动力学拟合。结果表明,当MF-SBC投加量为0.3 g·L−1、溶液初始pH为7、反应时间为720 min时,MF-SBC对水溶液中氨氮和磷酸盐的回收效果最佳,吸附量分别为103.12 mg·g−1和205.07 mg·g−1,并且MF-SBC对水中氨氮和磷酸盐的回收过程均符合准二级动力学模型。Ca2+、Na+、SO42对MF-SBC回收磷酸盐几乎没有影响,Ca2+和SO42-对氨氮的回收有抑制作用。MF-SBC对氮磷的回收机制包括表面吸附、离子交换和鸟粪石沉淀,其中以鸟粪石沉淀为主。Abstract: In this study, municipal sludge was taken as raw material combined with MgCl2 and FeSO4, magnetic sludge-based biochar (MF-SBC) was synthesized by pyrolysis carbonization, which was used to simultaneously recover nitrogen and phosphorus in water. Meanwhile, the effects of dosage, initial pH, contact time and coexisting ions on the recovery performance were investigated. The composition, morphology and functional groups of MF-SBC before and after adsorption were characterized by SEM, XRD, BET, XPS and FTIR, and the reaction process was fitted by kinetic models. The results showed that MF-SBC had the best recovery effect of ammonia nitrogen and phosphate in aqueous solution, and the maximum adsorption capacities were 103.12 mg·g−1 and 205.07 mg·g−1, respectively, when MF-SBC dosage was 0.3 g·L−1, the initial pH was 7, and the reaction time was 720 min, and the recovery process of ammonia nitrogen and phosphate in water by MF-SBC conformed to the pseudo-second-order kinetic model. Ca2+, Na+ and SO42- had slight effect on phosphate recovery by MF-SBC, Ca2+ and SO42− had an inhibitory effect on ammonia recovery. The recovery mechanism included surface adsorption, ion exchange and struvite precipitation, which was dominated by struvite precipitation.
-
Key words:
- sludge-based biochar /
- nitrogen and phosphorus /
- simultaneous recovery /
- struvite
-
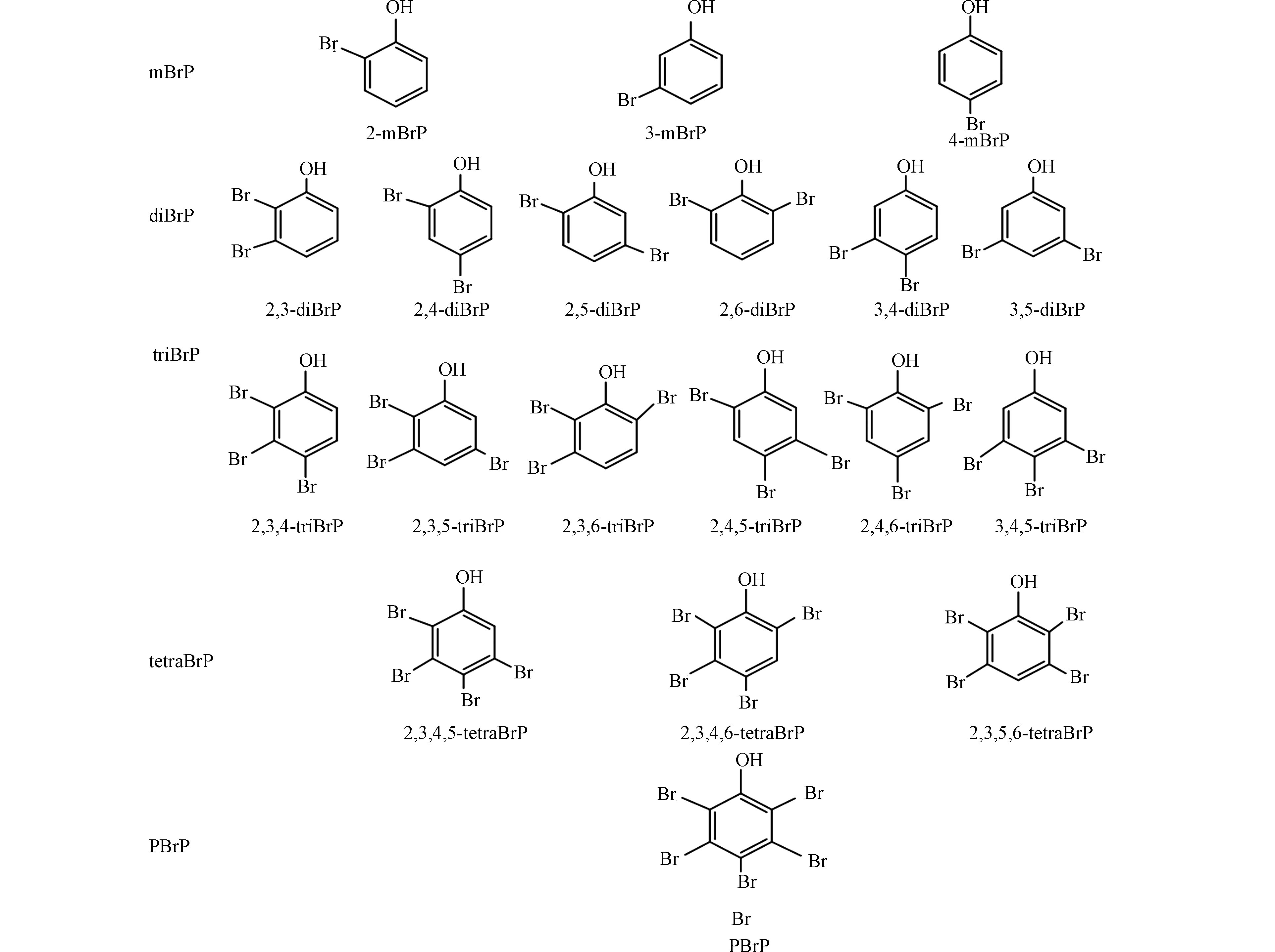
溴酚类化合物(bromophenols,BrPs)不仅具有人为来源,被用作阻燃剂、木材防腐剂等,也具有海洋藻类合成等天然来源,是重要的海洋风味物质[1-2]. 根据苯环上溴原子的取代数目和位置不同,BrPs有19种化合物(图1),在大气、水、土壤、油松树皮及海洋生物等环境样本中均有检出[3-6],甚至在血液和脐带血等人体样本中也有检出[7],电子厂工人血清中检出的BrPs浓度为360 pg·g−1 ww (湿重) [8]. 2,4,6-三溴酚 (2,4,6-bromophenol,2,4,6-triBrP)和五溴酚(pentabromophenol,pBrP)不仅能破坏生物体内甲状腺激素的平衡,也具有显著的抗雌激素效应[9-10]. 因此,BrPs逐渐引起学者们的广泛关注.
海洋中的螺类、贝类和鱼类等动物经摄食藻类可以累积BrPs,经转化等途径也可以将一些人为污染物(如多溴代二苯并二噁英及多溴代二苯并呋喃等)转化为BrPs[11]. 海产品在居民(特别是沿海居民)的膳食结构中占有重要地位,随着人们对健康生活的需求,海产品在膳食中所占的比重呈现显著增加趋势,因此关注海产品质量安全极为必要. 已有研究发现,中国香港市售不同种类海产品中BrPs的含量和分布存在差异[12],但我国其他城市市售海产品中BrPs的赋存情况,特别是海产品中常食用的部位(如贝肉、鱼肉)中BrPs的赋存尚不清晰. 因此,本研究选取9种居民喜食且消费量大的海产品,开展江苏省连云港市海产品中19种BrPs的组织分布及种间差异的研究,为BrPs的生态健康风险和食品安全提供数据支撑.
1. 材料与方法 (Material and methods)
1.1 样品采集和制备
于2021年7月在江苏省连云港市某海鲜市场采集了人们广泛食用、销售量较大的一些海产品,包括双壳类软体动物(牡蛎、紫贻贝和扇贝)、螺类(脉红螺、扁玉螺和花螺)、和鱼类(海鲈鱼、小黄花鱼和金鲳鱼)共9种捕捞的野生海产品. 每种海产品均采集个体大小相近的新鲜样品,在冷藏条件下运回实验室. 贝类和螺类用去离子水清洗后分离去壳,用解剖刀和镊子将每个双壳贝类个体的鳃、外套膜和肉(包含闭壳肌)部分分离,用吸水纸吸干组织表面水分. 由于贝类除鳃和外套膜以外的其他组织以大量贝肉和少量内脏为主,无法将内脏清晰分离,且人们食用这几种贝类通常是净化处理后将贝肉(包括闭壳肌)和内脏团一起食用,因此将内脏合并到贝肉中进行分析和讨论. 螺类样品则分离为螺肉和内脏部分. 为保证足够的样品量并避免个体差异的影响,每种贝与螺的每种组织都由20—35只个体的样品混合而成. 鱼类样品则被分离为鳃、肉和内脏(所有内脏混合在一起)部分,每种组织的样品均由3—4条鱼体的组织混合制备. 每种生物组织的混合样品均进行了准确的质量称量,精确到0.01 g. 随后将所有样品冷冻干燥后用小型粉碎机将其研磨为粉末状固体,密封在棕色玻璃瓶中,置于-20 ℃冰箱中. 海产品个体的干重、湿重等信息详见表1.
表 1 9种海产品的样本数量、组织重量以及含水率.Table 1. Numbers, weights, and the moisture content for the 9 tested seafood samples.种类Species 拉丁名Latin name 数量Quantities 部位Tissues 湿重/gWet weight 干重/gDry weight 含水率/%Moisture content 牡蛎 Crassostrea gigas n=20 鳃 17.0 3.09 81.8 外套膜 20.6 4.49 78.2 肉 91.0 21.0 76.9 扇贝 Patinopecten yessoensis n=30 鳃 23.9 5.96 75.1 外套膜 25.3 6.72 73.4 肉 157 37.7 75.9 紫贻贝 Mytilus edulis n=35 鳃 17.4 3.42 80.3 外套膜 43.8 12.0 72.6 肉 105 22.1 79.0 脉红螺 Rapana venosa n=20 内脏 46.5 14.5 68.9 肉 113 27.4 75.7 花螺 Babylonia areolata n=35 内脏 55.7 18.2 67.2 肉 113 27.4 75.7 扁玉螺 Glossaulax didyma n=35 内脏 99.5 32.4 67.4 肉 200 55.0 72.5 小黄花鱼 Larimichthys crocea n=4 鳃 18.5 6.42 65.3 内脏 67.1 29.2 56.6 鱼肉 553 210 61.9 金鲳鱼 Trachinotus ovatus n=3 鳃 17.8 6.08 65.8 内脏 57.3 35.6 37.8 鱼肉 487 210 57.0 海鲈鱼 Lateolabrax japonicus n=3 鳃 38.4 13.1 66.0 内脏 88.8 58.7 33.9 鱼肉 621 180 70.9 注:湿重、干重、含水率均基于n个个体的混合样品计量. Note:The wet weight, dry weight, and the moisture content were based on the mixed samples of individualities. 1.2 试剂材料
19种BrPs标准物质,包括2-一溴酚(2-monobromophenol, 2-mBrP)、3-一溴酚(3-bromophenol, 3-mBrP)、4-一溴酚(4-bromophenol, 4-mBrP)、2,3-二溴酚(2,3-dibromophenol, 2,3-diBrP)、2,4-二溴酚(2,4-dibromophenol, 2,4-diBrP)、2,5-二溴酚(2,5-dibromophenol, 2,5-diBrP)、2,6-二溴酚(2,6-dibromophenol, 2,6-diBrP)、3,4-二溴酚(3,4-dibromophenol, 3,4-diBrP)、3,5-二溴酚(3,5-dibromophenol, 3,5-diBrP)、2,3,4-三溴酚(2,3,4-tribromophenol, 2,3,4-triBrP)、2,3,5-三溴酚(2,3,5-tribromophenol, 2,3,5- triBrP)、2,3,6-三溴酚(2,3,6-tribromophenol, 2,3,6-triBrP)、2,4,5-三溴酚(2,4,5-tribromophenol, 2,4,5-triBrP)、2,4,6-triBrP、3,4,5-三溴酚(3,4,5-tribromophenol, 3,4,5-triBrP)、2,3,4,5-四溴酚(2,3,4,5-tetrabromophenol, 2,3,4,5-tetraBrP)、2,3,4,6-四溴酚(2,3,4,6-tetrabromophenol, 2,3,4,6-tetraBrP)、2,4,5,6-四溴酚(2,4,5,6-tetrabromophenol, 2,4,5,6-tetraBrP)、pBrP,均购自加拿大Wellington Laboratories. 同位素内标物质13C6-4-mBrP、13C6-2,4-diBrP、13C6-2,4,6-triBrP、13C6-2,3,4,6-tetraBrP 和13C6-pBrP购自美国Cambridge Isotope Laboratories. 以上标准物质纯度均大于95%. 所有标准溶液均保存于棕色毛细管瓶,并放于4℃冰箱中保存. 色谱级甲醇、乙腈、二氯甲烷等有机溶剂均购自J.T. Baker公司. Poly-Sery WAX(500 mg/6 mL, CNW Technologies GmbH) 和醋酸铵购自中国上海安谱实验科技股份有限公司,盐酸购自国药集团化学试剂有限公司.
1.3 样品前处理
前处理方法参照已有文献[13],并依据样品性质进行了微调. 准确称量2.00 g样品置于50 mL离心管中,加入20 mL乙腈:二氯甲烷溶液(1:1, 体积比)和20 μL同位素混合内标(13C6-4-mBrP、13C6-2,4-diBrP、13C6-2,4,6-triBrP,浓度分别为(500 ng·mL−1). 分别经超声(53 kHz,20 min)和振荡 (275 次·min−1,20 min)顺序萃取,以3500 r·min−1速度离心10 min取其上清液. 重复萃取3次,合并的萃取液氮吹至近干,用甲醇复溶后过0.22 μm聚四氟乙烯(PTFE)滤膜,随后用盐酸调节样品pH值至2.0±0.01. 随后用Poly-Sery WAX固相萃取柱(500 mg/6 mL)进行浓缩和净化,萃取柱先用6 mL甲醇和6 mL超纯水预处理,上样后用3 mL超纯水洗去杂质. 再用15 mL甲醇进行洗脱,收集洗脱液置于棕色小瓶中,经氮吹定容至500 μL.
1.4 色谱与质谱条件
本研究采用高效液相色谱-三重四极杆串联质谱仪(HPLC-MS/MS)(Ultimate 3000, Thermo Fisher Science, U.S.;Triple-Quad 5500, AB SCIEX, U.S.)检测19种BrPs.
液相色谱条件:色谱分离柱为 Inertsil ODS-4(150 mm×3.0 mm×2 μm, GL Science, Japan),进样量为 5 μL,柱温控制在40 ℃,流动相为含1 mmol·L−1 醋酸铵的水(A)和含0.1%乙酸的乙腈(B)的混合溶剂,流速为0.3 mL·min−1. 流动相梯度为:0 min,45%B/55%A;15 min,70%B/30%A;20—23 min,80%B/20%A;27 min,60%B/40%A;27.5—30 min,45%B/55%A. 质谱条件:在负离子多反应监测模式下对BrPs进行检测,离子源为电喷雾离子源,温度为500℃,离子化电压为-4500 V,气帘气和喷雾气的流速分别设定为38 psi和50 psi. 不同种BrPs检测的母离子、定量离子、碰撞能和去簇电压见表2.
表 2 不同BrPs的母离子、定量离子、碰撞能和去簇电压Table 2. The precursor and quantitative ion, collision energy, and declustering potential for different BrP congeners.化合物Compounds 母离子(m/z)Precursor ion 定量离子(m/z)Quantitative ion 碰撞能/eVCollision energy 去簇电压/eVDeclustering potential mBrPs 170.8 78.8 −22 −85 172.8 80.8 −22 −85 diBrPs 250.8 78.8 −30 −110 80.8 −30 −110 triBrPs 328.8 78.8 −70 −120 80.8 −70 −120 tetraBrPs 408.6 78.8 −85 −130 80.8 −85 −130 pBrP 488.6 78.8 −82 −130 80.8 −82 −130 13C6−4-mBrP 176.8 78.8 −22 −85 178.8 80.8 −22 −85 13C6−2,4-diBrP 256.8 78.8 −30 −110 80.8 −30 −110 13C6−2,4,6-triBrP 334.9 78.8 −70 −120 80.8 −70 −120 13C6−2,3,4,6-tetraBrP 414.6 78.8 −85 −130 80.8 −85 −130 13C6−PBrP 494.6 78.8 −82 −130 80.8 −82 −130 1.5 海产品个体中BrPs平均含量的计算方法
基于海产品不同组织混合样品的质量与对应组织中BrPs浓度,计算得到每个海产品中不同种类BrPs及∑4BrPs的个体平均含量,公式如下:
海产品个体平均含量=m1×C1+m2×C2+m3×C3+…m1+m2+m3… 其中,m1、m2、m3、…分别代表不同组织混合样品的质量(g),C1、C2、C3、…分别代表对应的不同组织混合样品中BrPs含量(ng·g−1 dw).
1.6 质量控制和质量保证
每10个样品分析一组9点标准曲线(0.1、 0.2、0.5、1.0、2.0、5.0、10.0、20.0、50.0 ng·mL−1,R2>0.995). 用2.00 g色谱纯硅藻土作为空白样品进行相同的全流程提取分析,在程序空白和仪器空白实验中均未检出BrPs. 每个样品均加入10.0 ng 同位素内标物质(20 μL, 500 ng·mL−1),以校正和消除样品前处理及仪器波动的影响. 除2,3,4,5-tetraBrPs回收率为58.8%外,海产品中其他18种BrPs回收率范围为77.1%—105%. BrPs的浓度值以干重计量,方法检出限(3倍噪声)范围为0.0248—32.1 ng·g−1 dw. 为了便于与文献数据进行对比,文献中BrPs含量如果以湿重或脂重计,则通过文献中给出的含水率(若文献中无含水率数据则按照贝、螺、鱼的含水率(80%)计算)或脂肪含量推算为以干重计的BrPs含量.
2. 结果与讨论(Results and discussion)
2.1 不同海产品中的BrPs
在采集的螺、贝和海鱼样品中,共检出了4种BrPs,分别为4-mBrP、2,4-diBrP、2,6-diBrP和2,4,6-triBrP,在所有海产品各部位样品中的检出率分别为87.5%、54.2%、50.0%和100%,其他15种BrPs在海产品中均未检出. 有研究表明[12, 14],4-mBrP、2,6-diBrP、2,4-diBrP和2,4,6-triBrP是藻类、鱼类、软体动物、甲壳类动物等海洋生物中广泛检出的BrPs,其中以2,4,6-triBrP占比最高,与本研究结果一致. 在多个海产品相关的研究中还检出了2-mBrP、2,3,4-triBrP、2,3,5-triBrP、2,3,6-triBrP、2,4,5-triBrP、2,4,6-triBrP、3,4,5-triBrP、2,3,4,5-tetraBrP、2,3,4,6-tetraBrP、2,3,5,6-tetraBrP、pBrP等其他多种BrPs[15-17],但这些BrPs在本研究中均未检出,这可能与不同种BrPs的来源、环境暴露浓度、累积特性以及海产品种类有关.
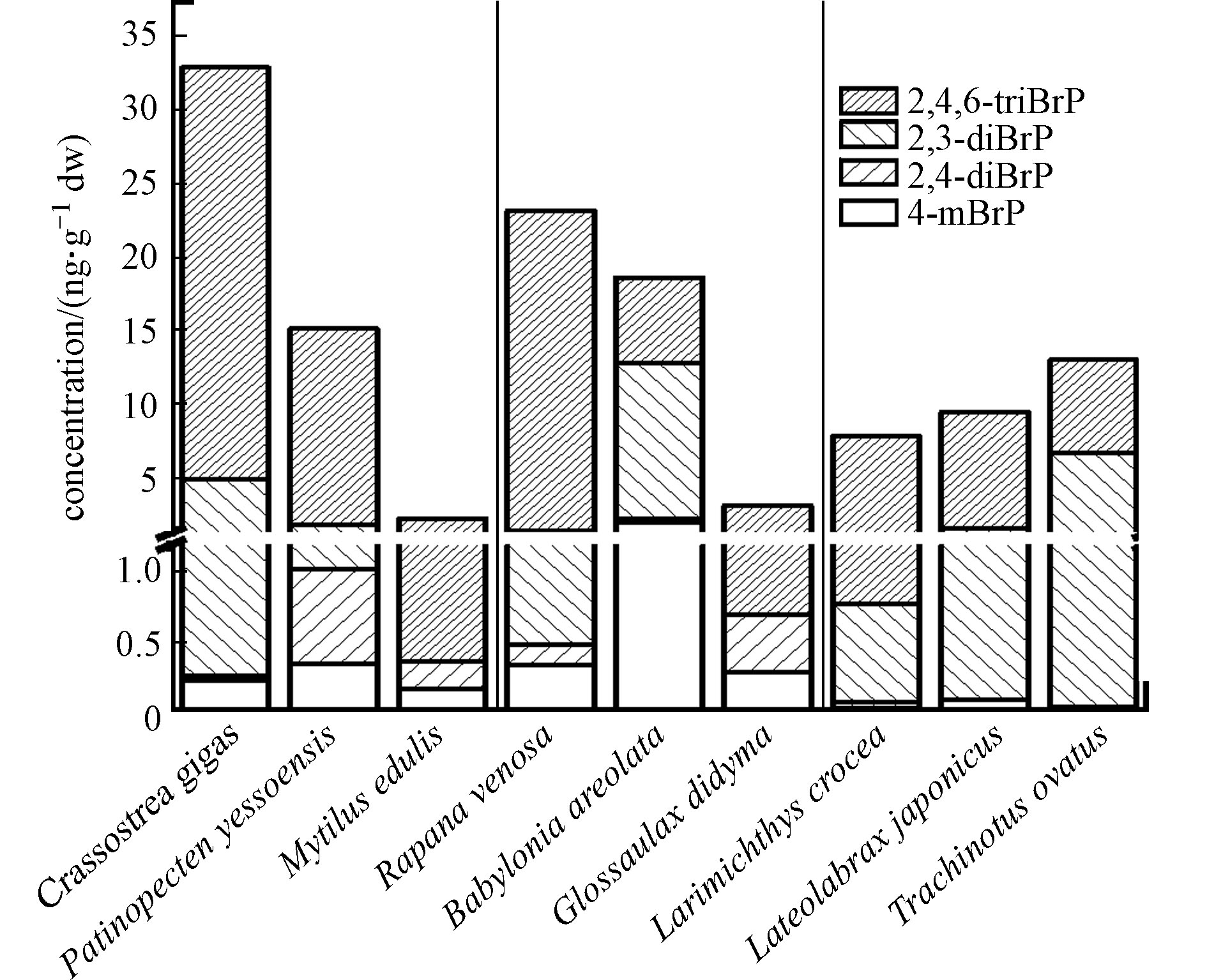
经海产品个体中BrPs含量推算,牡蛎、扇贝、紫贻贝、脉红螺、花螺、扁玉螺、小黄花鱼、海鲈鱼、金鲳鱼中∑4BrPs个体平均含量分别为33.0、15.2、2.25、23.2、18.7、3.11、7.85、9.52、13.0 ng·g−1 dw(图2). 比较不同海产品的含量发现,3种贝类中∑4BrPs、2,4-diBrP、2,4,6-triBrP个体平均含量((16.8±12.6)、(0.304±0.272)、(14.4±10.7) ng·g−1 dw)高于3种螺类((15.0±8.60)、(0.284±0.112)、(10.0±8.43) ng·g−1 dw)和鱼类((10.1±2.17)、(0.0136±0.0193)、(7.10±0.654) ng·g−1 dw),4-mBrP和2,6-diBrP则在螺类((0.863±0.785) ng·g−1 dw和(3.82±4.76) ng·g−1 dw)中高于贝类和鱼类. BrPs在物种间的差异,与生物的习性和生活环境有关,在韩国东南沿海、中国北江等区域的研究显示,BrPs在海洋沉积物中的浓度高于海水[5, 18],因此,贝类样品,特别是牡蛎和扇贝中某些BrPs单体的含量远高于螺类和鱼类,可能与其长期在沉积物中的底栖生活习性相关.
在3种贝类中,牡蛎的∑4BrPs、2,6-diBrP、2,4,6-triBrP个体平均含量最高(33.0、4.70、28.0 ng·g−1 dw),接下来是扇贝(15.2、0.774、13.4 ng·g−1 dw),二者均远高于紫贻贝(2.24、<MDL、1.88 ng·g−1 dw). 扇贝的4-mBrP和2,4-diBrP含量(0.343、0.677 ng·g−1 dw)高于牡蛎(0.221、0.0352 ng·g−1 dw)和紫贻贝(0.161、0.200 ng·g−1 dw). 本研究牡蛎中的溴酚单体4-mBrP、2,4,6-triBrP的个体平均含量高于中国香港地区牡蛎中对应BrPs的含量(<MDL、平均值(8.98±6.82) ng·g−1 dw,范围1.37–18.1 ng·g−1 dw)[12]和美国俄勒冈州州立大学海洋研究站获取的两种牡蛎样品中对应BrPs含量(<MDL、10.0、6.00 ng·g−1 dw)[19];2,6-diBrP处在中等水平,高于中国香港地区牡蛎(平均值(0.858±0.616) ng·g−1 dw,范围0.345—2.18 ng·g−1 dw)[12]低于美国俄勒冈州州立大学海洋研究站的两种牡蛎(含量5.00 ng·g−1 dw和6.00 ng·g−1 dw)[19];但溴酚单体2,4-diBrP的含量远低于中国香港牡蛎(平均值(30.6±18.5) ng·g−1 dw,范围9.8—52.9 ng·g−1 dw)[12]和在美国俄勒冈州的牡蛎(6.00 ng·g−1 dw和6.00 ng·g−1 dw)[19]. 本研究3种贝类中2,4,6-triBrP的个体含量的平均值((14.4±10.7) ng·g−1 dw)远高于在欧洲意大利、丹麦、法国、爱尔兰、西班牙等国家市场上采集的软体动物/甲壳类动物中2,4,6-triBrP的含量(范围0.316—3.73 ng·g−1 dw,数据经文献中脂肪含量换算)[20].
在3种螺类中,∑4BrPs和2,4,6-triBrP的含量按照脉红螺(23.2 ng·g−1 dw和21.8 ng·g−1 dw)、花螺(18.7 ng·g−1 dw和5.85 ng·g−1 dw)、扁玉螺(3.11 ng·g−1 dw和2.41 ng·g−1 dw)依次递减. 花螺中4-mBrP和2,6-diBrP含量(1.97 ng·g−1 dw和10.5 ng·g−1 dw)高于脉红螺(0.337 ng·g−1 dw和0.935 ng·g−1 dw)、扁玉螺(0.278 ng·g−1 dw和<MDL). 与另外3种BrPs不同,2,4-diBrP在扁玉螺中最高为0.419 ng·g−1 dw,接下来依次为花螺(0.288 ng·g−1 dw)和脉红螺(0.144 ng·g−1 dw).
对于3种鱼类,在金鲳鱼中∑4BrPs、2,6-diBrP含量(13.0、6.70 ng·g−1 dw)最高,接下来依次为海鲈鱼(9.52、1.51 ng·g−1 dw)和小黄花鱼(7.85、0.713 ng·g−1 dw). 海鲈鱼中2,4,6-triBrP和4-mBrP含量(7.91 ng·g−1 dw和0.0854 ng·g−1 dw)高于小黄花鱼(7.07 ng·g−1 dw和0.0244 ng·g−1 dw)和金鲳鱼(6.31 ng·g−1 dw和0.0332 ng·g−1 dw). 金鲳鱼和小黄花鱼均为咸水鱼,只能在海洋中生活,而海鲈鱼在海水与淡水中均能生活,因此海鲈鱼还有可能受到淡水生活环境的影响,而2,4,6-triBrP作为人为生产的溴代阻燃剂,往往对流经城市和人类生活区的淡水水体影响更大,这也可能是海鲈鱼体内2,4,6-triBrP含量高的原因.
2.2 三种贝类中BrPs的组织分布
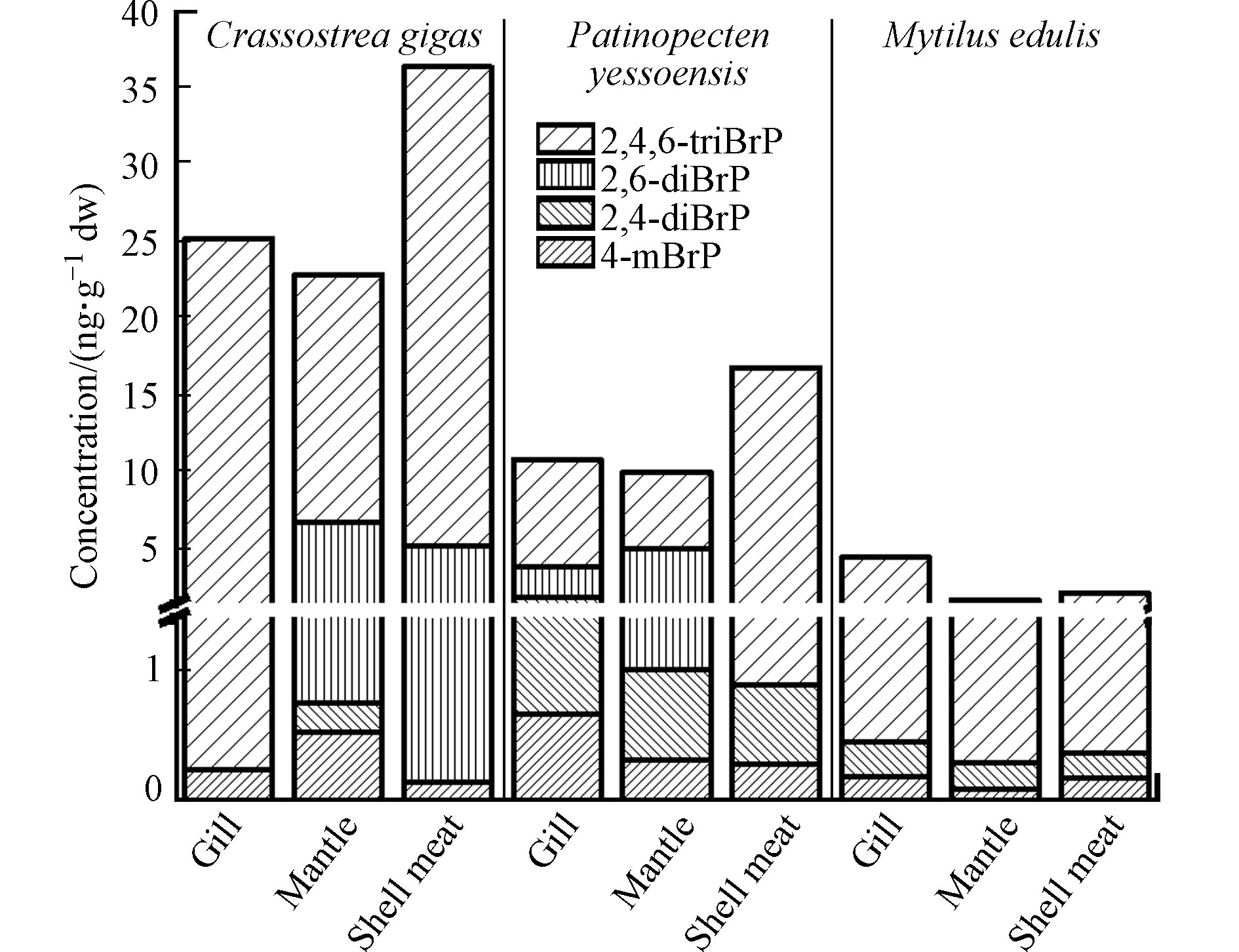
对于紫贻贝,除2,6-diBrP未检出外,检出的BrPs(4-mBrP、2,4-diBrP、2,4,6-triBrP)及∑4BrPs(0.197、0.262、4.00、4.46 ng·g−1 dw)均主要累积在鳃内(图3),高于贝肉(0.187、0.188、1.81、2.19 ng·g−1 dw)和外套膜(0.102、0.204、1.42、1.73 ng·g−1 dw)中对应BrPs的含量. 扇贝鳃中4-mBrP(0.663 ng·g−1 dw)和2,4-diBrP(1.20 ng·g−1 dw)也高于外套膜(0.326 ng·g−1 dw和0.681 ng·g−1 dw)和贝肉(0.295 ng·g−1 dw和0.594 ng·g−1 dw). 这说明鳃也是贝类BrPs暴露及分布的重要组织. 牡蛎和扇贝的贝肉中2,4,6-triBrP(31.0 ng·g−1 dw和15.9 ng·g−1 dw)、∑4BrPs的含量(36.3 ng·g−1 dw 和16.8 ng·g−1 dw)高于鳃和外套膜. 另外,牡蛎与扇贝中2,6-diBrP在外套膜中(6.04 ng·g−1 dw与4.00 ng·g−1 dw)高于鳃和贝肉中含量. 对3种贝类中BrPs的组织分布进行比较,发现紫贻贝各组织中的∑4BrPs均远低于牡蛎和扇贝,BrPs在3种贝类中的组织分布差异与3种贝类不同的生活方式和生长特性有关,牡蛎、扇贝多生活在潮间带、潮下带、低潮带底泥中,而紫贻贝多生活于浅海区附着在岩礁上,从BrPs浓度相对较低的海水中滤食,使其体内BrPs含量相较牡蛎和扇贝要低. 而紫贻贝的外套膜占个体干重的32.0%,远高于牡蛎(15.7%)和扇贝(13.3%). 紫贻贝、牡蛎、扇贝外套膜中∑4BrPs含量分别占对应贝类个体BrPs含量的24.6%、10.9%、8.79%. 由此可见,不同种贝类间相同生物组织在其体重中的占比也影响了BrPs的浓度分布. 整体上,贝类肉中∑4BrPs((18.4±14.0) ng·g−1 dw)高于鳃中((13.5±8.68) ng·g−1 dw)和外套膜((11.5±8.71) ng·g−1 dw).
2.3 三种螺类中BrPs的组织分布
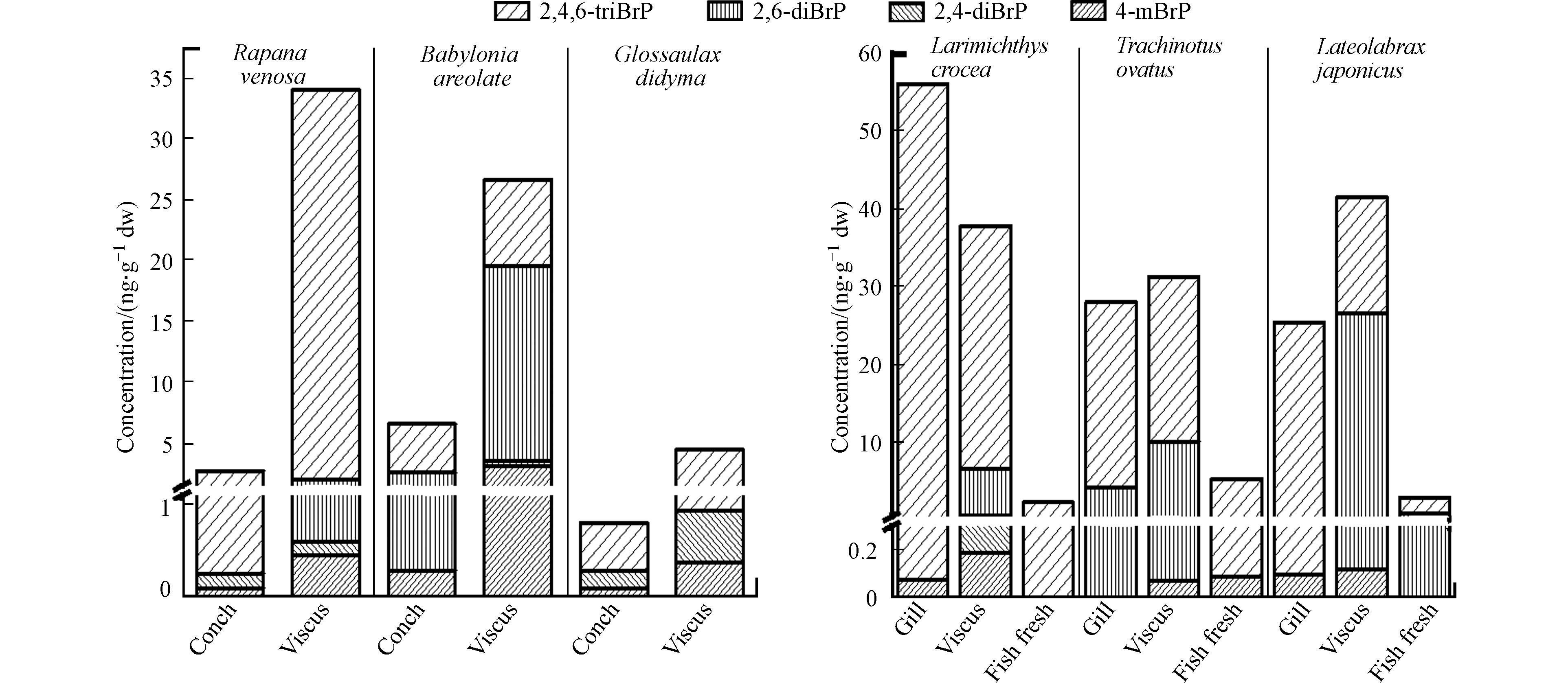
3种螺中各种BrPs及∑4BrPs在内脏中的含量均远高于螺肉中的含量(图4). 3种螺内脏中∑4BrPs平均含量((21.7±12.6) ng·g−1 dw)远高于螺肉((3.37±2.41) ng·g−1 dw). 对于螺肉样品,花螺螺肉中∑4BrPs最高(6.59 ng·g−1 dw)(图4),分别是脉红螺(2.71 ng·g−1 dw)和扁玉螺 (0.806 ng·g−1 dw)的2.43倍和8.18倍. 花螺的螺肉和内脏中4-mBrP、2,6-diBrP、2,4,6-triBrP的含量均高于脉红螺、扁玉螺的对应部位. 2,4-diBrP的最高浓度出现在扁玉螺的螺肉和内脏团中(图4). 3种螺螺肉中∑4BrPs的平均含量((3.37±2.41) ng·g−1 dw,范围0.806—6.59 ng·g−1 dw)远低于3种贝肉的平均含量((18.4±14.0) ng·g−1 dw,范围2.19—36.3 ng·g−1 dw),但花螺和脉红螺螺肉中∑4BrPs的含量则高于紫贻贝贝肉.
2.4 三种鱼体中BrPs的组织分布
如图4所示,小黄花鱼、海鲈鱼和金鲳鱼肉中的∑4BrPs含量(2.21、5.29、2.87 ng·g−1 dw)均远低于内脏(37.8、31.3、41.5 ng·g−1 dw)和鳃中的含量(56.1、28.0、25.4 ng·g−1 dw). 检出率最高的2,4,6-triBrP在鱼体中的最高浓度均出现在3种鱼的鱼鳃(56.0、28.0、25.3 ng·g−1 dw)中. 这说明鳃也是鱼类2,4,6-triBrP暴露与分布的重要组织. 4-mBrP和2,6-diBrP在内脏团中的含量均高于鱼肉和鱼鳃中(图4). 其中金鲳鱼内脏中的2,6-diBrP(26.4 ng·g−1 dw)占∑4BrPs(41.5 ng·g−1 dw)的63.6%,超过了检出率最高的2,4,6-triBrP(15.0 ng·g−1 dw,占比36.1%),这一比例也远高于小黄花鱼和海鲈鱼中2,6-diBrP所占比例(15.9%和31.9%)以及文献中报道的鱼类肠胃中2,6-diBrP所占的比例(0—16.9%)[1, 12]. 2,4-diBrP除在小黄花鱼的内脏团中检出(0.344 ng·g−1 dw)外,在小黄花鱼其他组织、海鲈鱼和金鲳鱼的所有组织中均未发现. 3种鱼中检测到的BrPs的∑4BrPs平均含量在内脏中含量最高为(36.9±4.22) ng·g−1 dw,高于鳃((36.5±13.9) ng·g−1 dw)和鱼肉((3.46±1.32) ng·g−1 dw),与其他研究中发现的内脏含量高于肉中含量的现象是一致的.
本研究的海鲈鱼鱼肉中以2,4,6-triBrP为主要BrPs单体,与文献中同种鱼的检测结果一致,但2,4,6-triBrP的含量(5.20 ng·g−1 dw)高于澳大利亚市场上采集的野生与养殖尖吻鲈鱼鱼肉中的含量(平均值(0.0857±0.0481) ng·g−1 dw,范围<MDL—0.800 ng·g−1 dw,经含水率80%计算)[21],低于在瑞典斯德哥尔摩群岛的Nämdö岛周围采集的鲈鱼鱼肉的含量(平均值(6.59±3.15) ng·g−1 dw,范围:(1.45—10.0) ng·g−1 dw,经含水率80%换算)[22];4-mBrP含量((0.0900) ng·g−1 dw)低于澳大利亚尖吻养殖鲈鱼鱼肉中的含量((0.250) ng·g−1 dw,以鱼肉含水率80%计干重)[21]. 本研究海鲈鱼鱼肉中2,4-diBrP和2,6-diBrP均未检出,但在澳大利亚尖吻野生鲈鱼中均有检出.
与其他种类的鱼相比,本研究3种鱼鱼肉中2,4,6-triBrP含量平均值((3.17±1.44) ng·g−1 dw)低于在中国香港市场上采集的不同季节的河豚与褐斑石斑鱼的鱼肉(平均值(15.6±9.91) ng·g−1 dw,范围(2.43–39.2) ng·g−1 dw)[12]和从美国阿拉斯加、密歇根湖、威斯康星州等地采集的鲑鱼、鲱鱼等鱼肉中2,4,6-triBrP的含量((18.5—166) ng·g−1 dw)[19]. 本研究3种鱼内脏中2,4,6-triBrP含量平均值((22.5±6.72) ng·g−1 dw)也均低于在中国香港的河豚与褐斑石斑鱼(平均值(49.1±50.2) ng·g−1 dw,范围(2.18—155) ng·g−1 dw)[12]和澳大利亚新南威尔士州采集的多种底栖食肉性与杂食性鱼类(平均值(203±264) ng·g−1 dw,范围<MDL—850 ng·g−1 dw,按照含水率80%计算)[23] 内脏中2,4,6-triBrP的含量. 本研究3种鱼类的鱼肉及内脏中BrPs含量低于其他研究1—2个数量级,整体上处在较低水平.
3. 结论(Conclusion)
在贝类、螺类和鱼类的鳃、外套膜、内脏、肉等不同组织中共检出4种BrPs,4-mBrP、2,4-diBrP、2,6-diBrP、2,4,6-triBrP,其中2,4,6-triBrP含量水平和检出率均相对较高,在9种海产品所有组织中的浓度范围为0.512—56.0(平均值:(14.1±13.8) ng·g−1 dw),∑4BrPs的范围为0.806—56.1(平均值:(18.2±15.5) ng·g−1 dw). 3种贝类中∑4BrPs个体平均含量高于3种螺类和鱼类. 3种贝类鳃中∑4BrPs高于外套膜和贝肉. 3种螺的内脏和鳃中∑4BrPs含量平均值远高于螺肉中的含量. 3种鱼内脏中的∑4BrPs含量平均值远高于鳃和鱼肉. 研究证实了BrPs在不同海产品内脏中的高累积,另外鳃也是海产品BrPs暴露及分布的重要组织.
-
表 1 MF-SBC同步吸附氨氮和磷酸盐的详细实验条件
Table 1. Experimental conditions for the simultaneous adsorption of nitrogen and phosphate by MF-SBC
影响因素 时间/min 氨氮质量浓度/(mg·L−1) P质量浓度/(mg·L−1) pH 共存离子 MF-SBC质量浓度/(g·L−1) pH 720 160 80 3~11 — 0.3 MF-SBC投加量 720 160 80 9 — 0.1~0.5 共存离子 720 160 80 9 Ca2+、Na+、SO42− 0.3 反应时间 1~720 160 80 9 — 0.3 表 2 MF-SBC同步吸附氮磷的动力学拟合参数
Table 2. Kinetic parameters for the simultaneous adsorption of nitrogen and phosphorus by MF-SBC
污染物 准一级动力学 准二级动力学 Qe /(mg·g−1) k1/ min−1 R2 Qe/(mg·g−1) k1/(g·(mg·min)−1) R2 磷 168.44 0.0127 0.79 203.65 0.0012 0.99 氨氮 83.86 0.013 0.77 101.34 0.0017 0.99 表 3 MF-SBC同步吸附氮磷的颗粒内扩散模型参数
Table 3. Intra particle diffusion model parameters for the simultaneous adsorption of nitrogen and phosphorus by MF-SBC
污染物 S1 S2 S3 K R2 K R2 K R2 磷 11.57 0.95 25.07 - 0.83 0.92 氨氮 7.56 0.98 2.43 - 0.28 0.92 -
[1] 赵玉芬. 磷化学与化工进展[J]. 中国科学:化学, 2010, 40(7): 801. [2] 孙理密, 翟纪学, 张德清, 等. 高氮磷有机食品废水处理工程实例分析[J]. 工业水处理, 2022, 42(1): 171-174. [3] 聂坤, 杨成建, 李志华, 等. 鸟粪石结晶-絮凝沉淀同步法回收养殖场废水的氮磷[J]. 水处理技术, 2022, 48(7): 38-42. [4] XIE F, WU F, LIU G, et al. Removal of phosphate from eutrophic lakes through adsorption by in situ formation of magnesium hydroxide from diatomite[J]. Environmental Science & Technology, 2014, 48(1): 582-590. [5] ZENG, F Z, ZHAO Q L, JIN W B, et al. Struvite precipitation from anaerobic sludge supernatant and mixed fresh/stale human urine[J]. Chemical Engineering Journal, 2018, 344: 254-261. doi: 10.1016/j.cej.2018.03.088 [6] 李亮, 王德汉, 邹璇. 曝气在沉淀法回收沼气发酵液氮磷中的作用[J]. 农业工程学报, 2010, 26(1): 313-318. [7] 张琪, 赵首萍, 叶雪珠, 等. 鸟粪石结晶法回收氮磷的影响因素研究[J]. 科技通报, 2015, 31(7): 237-244. [8] 霍守亮, 席北斗, 刘鸿亮. 磷酸铵镁沉淀法去除与回收废水中氮磷的应用研究进展[J]. 化工进展, 2017, 26(3): 371-376. [9] 杨明珍, 包震宇, 师晓春, 等. 鸟粪石沉淀法处理沼液实验研究[J]. 工业安全与环保, 2016, 37(3): 31-32. [10] BARBOSA S G, PEIXOTO L, MEULMAN B, et al. A design of experiments to assess phosphorous removal and crystal properties in struvite precipitation of source separated urine using different Mg sources[J]. Chemical Engineering Journal, 2016, 298: 146-153. doi: 10.1016/j.cej.2016.03.148 [11] 吴彦霖, 周荣敏. MAP法与沸石吸附组合工艺的脱氮除磷实验研究[J]. 中国环保产业, 2015(2): 45-48. [12] HUANG H, XIAO D, ZHANG Q, et al. Removal of ammonia from landfill leachate by struvite precipitation with the use of low-cost phosphate and magnesium sources[J]. Journal of Environmental Management, 145: 191-198. [13] 张记市, 王玉松. 鸟粪石结晶法回收垃圾渗滤液氨氮研究[J]. 环境工程学报, 2009, 3(11): 2017-2020. [14] ZHANG J S, WANG Q Q. Sustainable mechanisms of biochar derived from brewers' spent grain and sewage sludge for ammonia-nitrogen capture[J]. Journal of cleaner production, 2016, 112: 3927-3934. doi: 10.1016/j.jclepro.2015.07.096 [15] HALL K E, CALDERON M J, SPOKAS K A, et al. Phenolic acid sorption to biochars from mixtures of feedstock materials[J]. Water Air & Soil Pollution, 2014, 225(7): 2031. [16] FENG Y, XU Y, YU Y, et al. Mechanisms of biochar decreasing methane emission from Chinese paddy soils[J]. Soil Biology & Biochemistry, 2012, 46(1): 80-88. [17] 李时琛, 方海旭, 李俊青. 菜叶生物质炭的磷酸活化制备及其吸附性能研究[J]. 化工管理, 2018(1): 80-81. [18] BOESCH D F, BURRESON E, DENNISON W, et al. Factors in the decline of coastal ecosystems[J]. Science, 2001, 293(5535): 1589-1691. [19] ENDERS A, HANLEY K, WHITMAN T, et al. Characterization of biochars to evaluate recalcitrance and agronomic performance[J]. Bioresource Technology, 114: 644-653. [20] OZCAN A, OZCAN A S, TUNALI S, et al. Determination of the equilibrium, kinetic and thermodynamic parameters of adsorption of copper (II) ions onto seeds of Capsicum annuum[J]. 2005, 124: 200-208. [21] 杨奇亮, 吴平霄. 改性多孔生物炭的制备及其对水中四环素的吸附性能研究[J]. 环境科学学报, 2019, 39(12): 3973-3984. [22] LIU J W, JIANG J G, AIHEMAITI A, et al. Removal of phosphate from aqueous solution using MgO-modified magnetic biochar derived from anaerobic digestion residue[J]. Journal of Environmental Management, 2019, 250: 109438. doi: 10.1016/j.jenvman.2019.109438 [23] CUI X, HAO H, ZHANG C, et al. Capacity and mechanisms of ammonium and cadmium sorption on different wetland-plant derived biochars[J]. Science of the Total Environment, 2016, 539: 566-575. doi: 10.1016/j.scitotenv.2015.09.022 [24] LYU H H, GAO B, HE F, et al. Effects of ball milling on the physicochemical and sorptive properties of biochar: Experimental observations and governing mechanisms[J]. Environmental Pollution, 2018, 233: 54-63. doi: 10.1016/j.envpol.2017.10.037 [25] YAN H, SHIH K. Effects of calcium and ferric ions on struvite precipitation: A new assessment based on quantitative X-ray diffraction analysis[J]. Water Research, 2016, 95: 310-318. doi: 10.1016/j.watres.2016.03.032 [26] CHENG S, ZHAO S, GUO H, et al. High-efficiency removal of lead/cadmium from wastewater by MgO modified biochar derived from crofton weed[J]. Bioresource Technology, 2022, 343: 126081. doi: 10.1016/j.biortech.2021.126081 [27] LI A, XIE H, QIU Y, et al. Resource utilization of rice husk biomass: Preparation of MgO flake-modified biochar for simultaneous removal of heavy metals from aqueous solution and polluted soil[J]. Environmental Pollution, 2022, 310: 119869. doi: 10.1016/j.envpol.2022.119869 [28] WU J W, WANG T, WANG J, et al. A novel modified method for the efficient removal of Pb and Cd from wastewater by biochar: Enhanced the ion exchange and precipitation capacity[J]. Science of the Total Environment, 2021, 754: 142150. doi: 10.1016/j.scitotenv.2020.142150 -




 下载:
下载: