-
污泥作为城市污水处理厂的主要废物,因其含有大量病原微生物、寄生虫卵、重金属以及大量难降解的有机物[1],所以,污泥最终的处理处置技术广受关注。截至2017年12月,我国建成污水处理厂5 072座,年产生含水率80%的污泥超过5×107 t,如果这些污泥得不到妥善处置,将对环境和生态造成严重危害。目前,对于污泥的处置多采用填埋和堆肥,填埋处理要求污泥的含水率达到60%以下[2],而我国大多数污水处理厂不能达标,所以,须在污泥脱水之前对污泥进行调理,改变污泥的组织结构,减小污泥的黏性,实现污泥高效脱水[3]。有研究[4]发现,污泥难以脱水的主要原因是由于胞外聚合物(EPS)的存在,将EPS絮体破解,释放内部水分,才能实现污泥高效脱水。EPS是细菌分泌于体外的一些高分子聚合物,主要成分是多糖、蛋白质和核酸等高分子物质。
此外,随着我国造纸行业的发展,造纸污泥的量也在逐年增加。造纸污泥是制浆造纸过程中产生的固体废物,富含碳酸钙、高岭土等无机物和纤维素、半纤维素、木素等有机物,并且还存在部分成分复杂的污染物,如果处理不当,将对环境造成严重危害[5]。
目前,Fenton法和酸处理法用于污泥调理,但对pH的要求较为苛刻[6]。高级氧化法中的过硫酸盐经过渡金属、紫外以及热活化产生的硫酸根自由基(
SO2−4 ·),其氧化还原电位E0=2.50~3.10 eV[7],具有很强的氧化性和非选择性,可以氧化绝大部分有机物,使EPS絮体破解。宋秀兰等[8]和ZHEN等[9]采用亚铁离子活化过硫酸盐对污泥进行调理,可以有效降低污泥的含水率,提高污泥的脱水效果。基于上述研究基础,本研究采用Fe2+活化过硫酸盐联合造纸初沉污泥对市政污泥进行调理,探究不同调理方式对市政污泥的各项指标的影响,以期解决市政污泥高含水率、难以脱水的难题。
-
实验污泥取自某污水处理厂的浓缩池污泥(原泥),污泥性质如表1所示。骨架构建所用的造纸污泥取自某造纸废水处理厂初沉污泥,有机质(VSS/TSS)为44.25%。
-
实验药品:过硫酸钾(K2S2O8)、硫酸亚铁(FeSO4·7H2O)、氢氧化钠(NaOH)、氯化钠(NaCl)、苯酚(C6H5OH)、考马斯亮蓝(C47H48N3NaO7S3),抗坏血酸(C6H8O6),钼酸铵((NH4)6Mo7O24·4H2O),所用药品均为分析纯,浓硫酸(98%)。
实验仪器设备:毛细吸水时间测定装置(HDFC-10A型,北京恒奥德仪器仪表有限公司)、污泥比阻测定装置(KL-WBC-1型,武汉科林高教学设备有限公司)、黏度计(NDJ-8SN型,上海平轩科学仪器有限公司)、恒温干燥箱(WGL-125B型,天津泰斯特仪器有限公司)、紫外分光光度计(SP-UV1100型,上海奥析科学仪器有限公司)、搅拌器(JJ-4型,国华电器有限公司)、雷磁pH计(PHS-3C型,上海仪电科学仪器有限公司)、马弗炉(KSL-1200X型,上海虔钧科学仪器有限公司),手提式压力蒸汽灭菌锅(DSX-280B型,济南欧迪医疗器械有限公司),化学需氧量(COD)快速测定仪(5B-6C型,上海沛升仪器设备有限公司)等。
-
将取回的污泥放置在4 °C冰箱中保存。实验取200 mL待测污泥于500 mL烧杯中,置于机械搅拌器上搅拌5 min,加入过硫酸钾继续搅拌10 min,继续加入硫酸亚铁继续搅拌5 min,最后加入100 mL造纸初沉污泥继续搅拌10 min,量取100 mL污泥进行污泥比阻的测定,量取10 mL调理后的污泥进行毛细吸水时间测定。污泥脱水实验在各个条件下进行3次,以保证实验的可靠性。
-
1)污泥泥饼含水率:泥饼含水率是作为表征污泥调理效果好坏最为直观的参数,泥饼含水率越低,污泥调理效果越好。
2)污泥比阻SRF:SRF是表征污泥过滤特性的综合指标,SRF越大,表示污泥脱水效果越差[10],SRF按式(1)进行计算。
式中:RSRF为污泥比阻,1012 m·kg−1;P为过滤压力,Pa;A为过滤面积,m2;b为布氏抽滤实验的t/V对V作线性图的斜率,s·m−6;μ为滤液黏度,Pa·s;C为单位体积滤液产生的滤饼质量,kg。
3)毛细吸水时间CST:CST也是污泥脱水效果的表征指标,CST越大,污泥脱水效果越差[11]。
4)污泥EPS:污泥中EPS分为溶解型EPS(S-EPS)、松散结合型EPS(LB-EPS)、紧密结合型EPS(TB-EPS),参照文献中的方法[12]提取EPS,测定蛋白质和多糖含量,蛋白质采用考马斯亮蓝法[13],多糖采用苯酚硫酸法[14],探究胞外聚合物的破解程度。
5)滤饼和滤液中总氮、总磷:由于脱氮除磷工艺过程中,氮和磷被微生物吸收合成细胞,通过排泥得到去除[15],EPS破解后,氮、磷释放进入滤液中,造成滤液中总氮和总磷的含量增加。
-
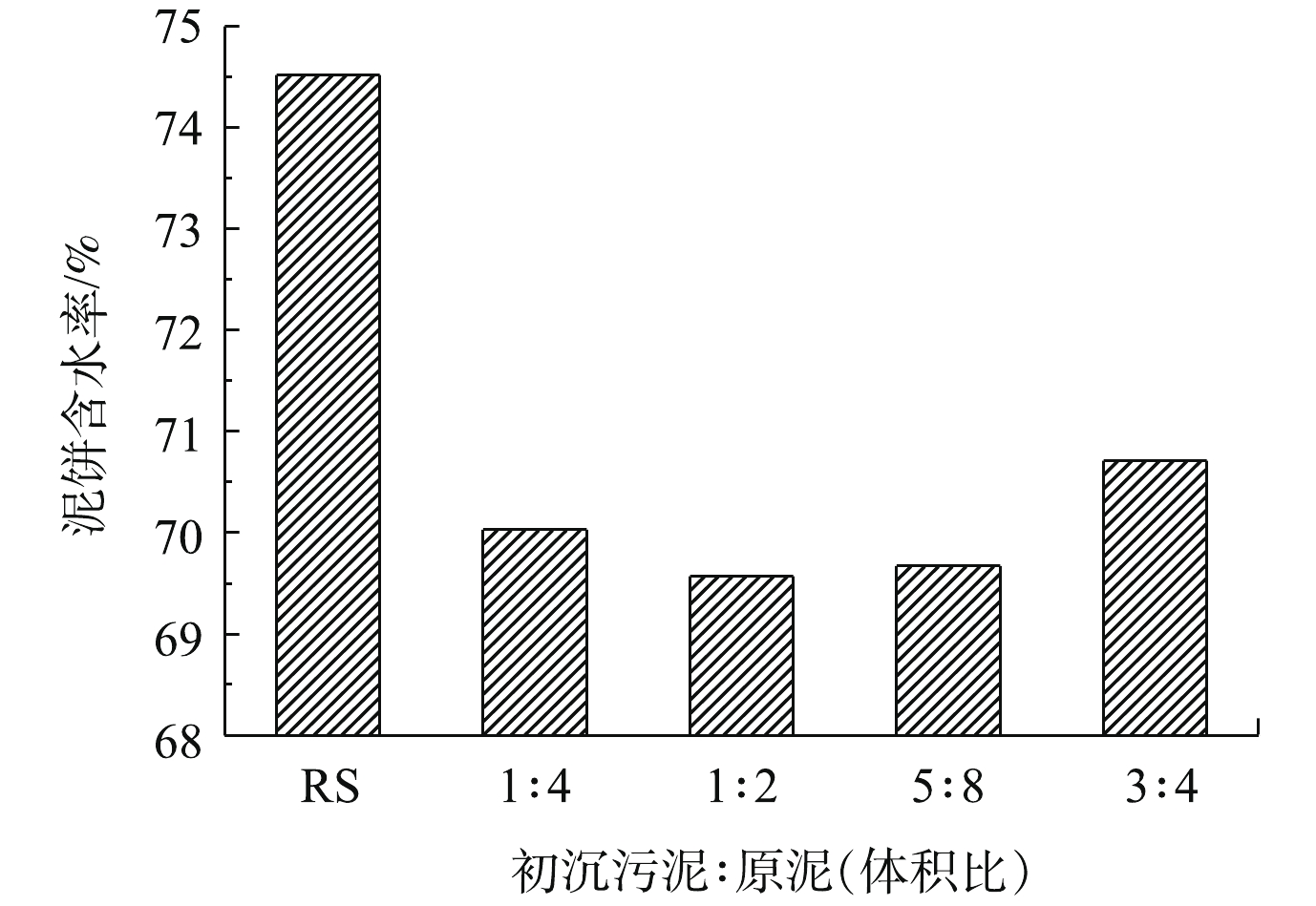
造纸污泥投加量对污泥泥饼含水率的影响如图1所示。由图1可以看出,未经调理的污泥泥饼含水率为74.52%,采用过硫酸盐联合造纸初沉污泥调理后,泥饼的含水量显著降低。随着初沉污泥与原泥混合比例的增加,泥饼的含水率先迅速降低,后又出现上升的趋势;当初沉污泥与原泥以1∶2的体积比混合时,泥饼的脱水效果达到最好,泥饼含水率降至69.57%。这是因为造纸初沉污泥中含有细小纤维、碳酸钙等物质[5],一定量的细小纤维可以在污泥中起到骨架支撑的作用,使污泥在抽滤过程中保持多孔性,形成水通道,使污泥内部的水分高效脱出[16]。随着初沉污泥投加量的增加,细小纤维的含量增加,会在污泥脱水过程中阻塞水通道,不利于水分的脱出,所以初沉污泥与原泥最优的混合比例为1∶2。
-
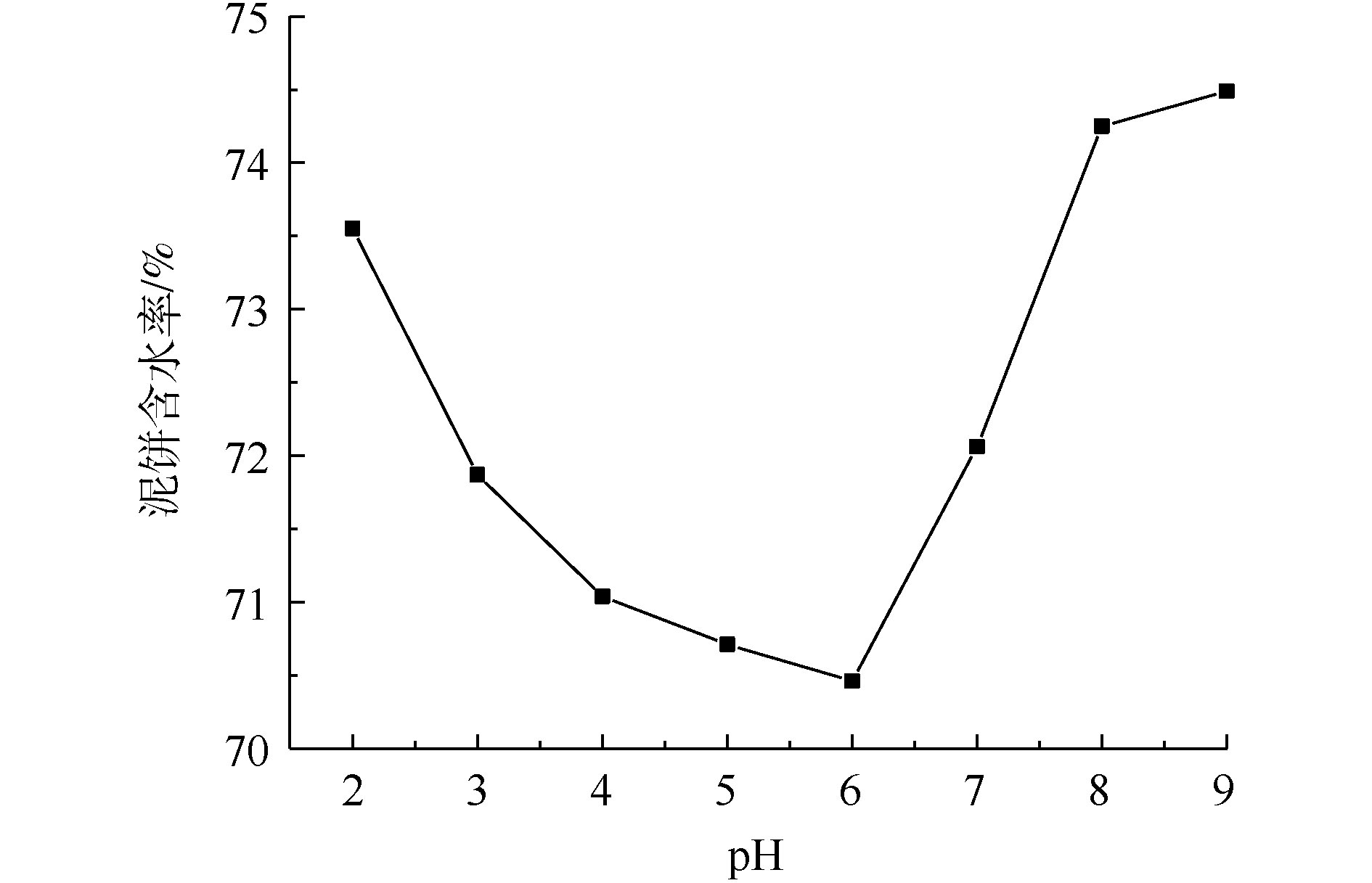
污泥初始pH对泥饼含水率的影响如图2所示。由图2可以看出,随着污泥初始pH的增加,泥饼含水率出现先降低后增加的趋势;当污泥初始pH=6时,泥饼的含水率由74.52%降至70.46%。在酸性条件下,随着pH的增大,泥饼的含水率下降。这是因为当pH<3时,硫酸根自由基的氧化性能受到抑制,使得泥饼含水率没有明显的降低。当3<pH<6时,EPS会在酸性条件下破解,形成细小的絮体,使内部的水分释放,在抽滤过程中过小的絮体可能会导致污泥系统崩溃,堵塞水通道,使内部的水分不能顺利脱出。当pH=6时,由于体系接近于中性环境,一方面由于硫酸根自由基的氧化性能,另一方面由于酸环境,污泥含水率可以显著降低。当污泥初始pH>7时,污泥系统处于碱性环境,体系中的Fe2+和Fe3+会形成低活性的氢氧化物沉淀[17],导致能活化过硫酸盐的Fe2+量减少,限制了过硫酸盐的氧化效率。
-
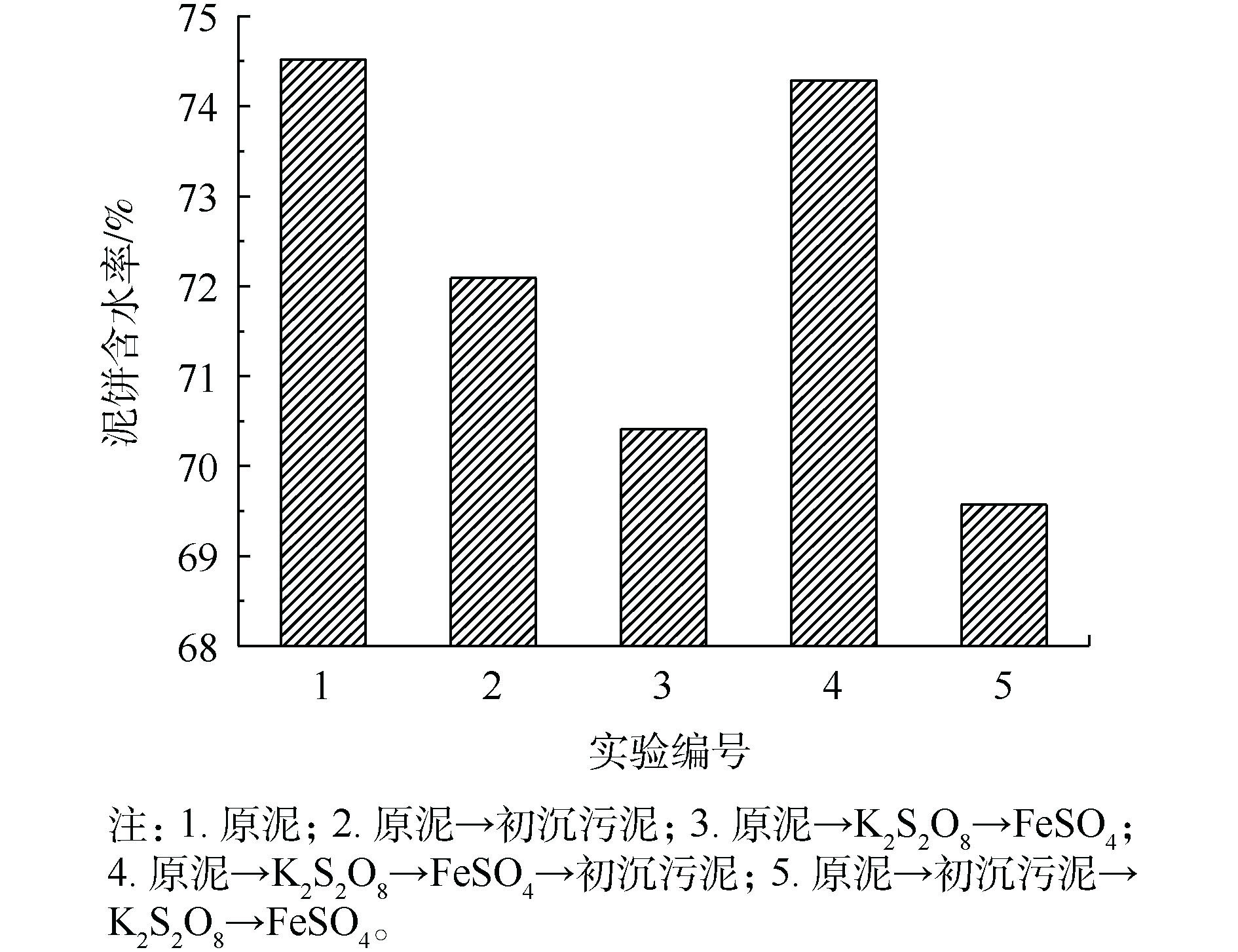
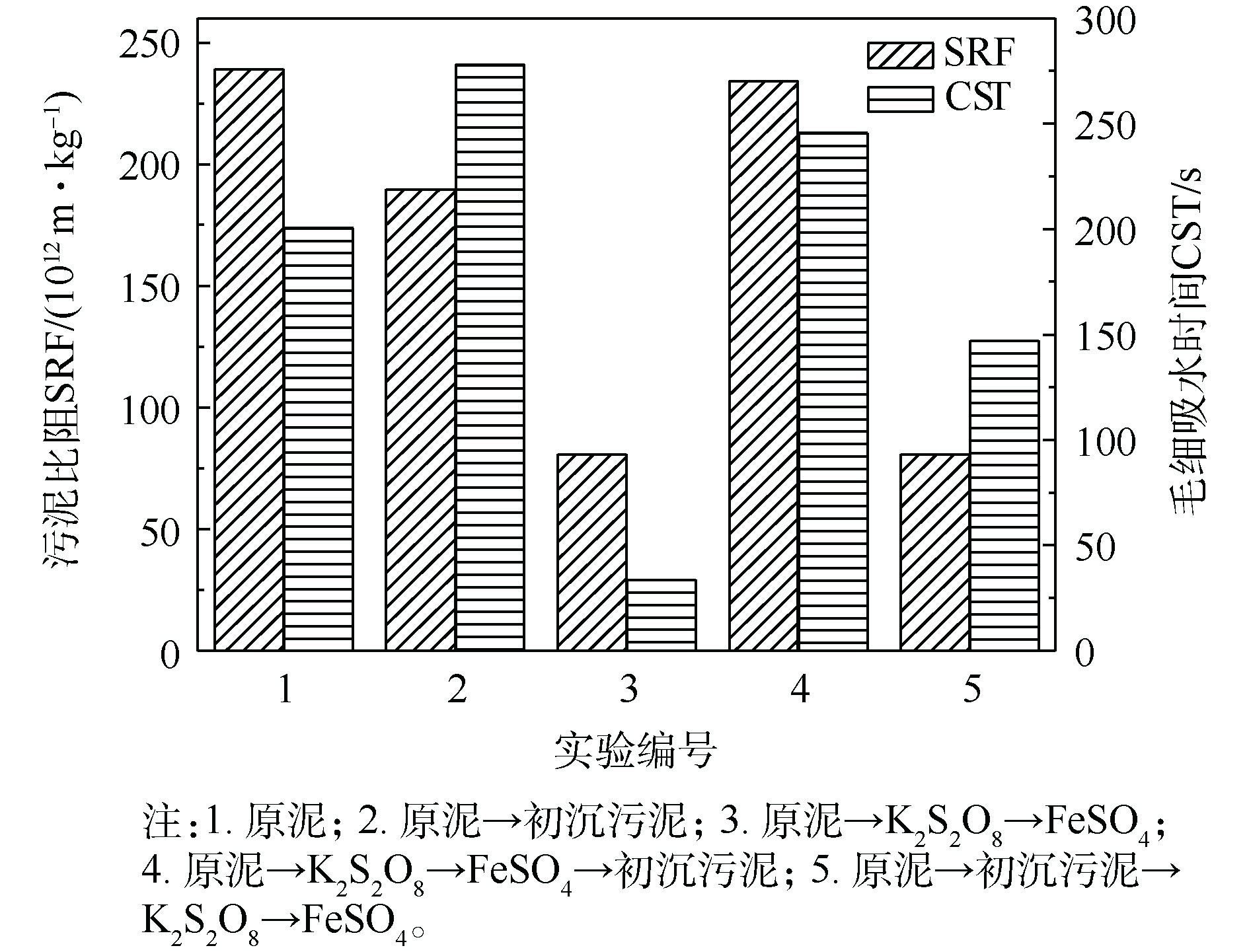
不同调理方式对污泥泥饼含水率、SRF以及CST的影响如图3和图4所示。由图3和图4可以看出,未经调理的原泥经抽滤脱水后泥饼的含水率为74.52%,SRF为238.97×1012 m·kg−1,CST为199.8 s;采用亚铁活化过硫酸盐调理后,原泥泥饼的含水率降至70.41%,SRF下降至80.75×1012 m·kg−1;单独使用初沉污泥调理后,泥饼含水率降至72.09%,SRF降至189.70×1012 m·kg−1;经初沉污泥复合调理后污泥泥饼的含水率69.57%,污泥SRF下降至80.71×1012 m·kg−1,较原泥含水率降低6.64%,污泥比阻降低了66.23%。
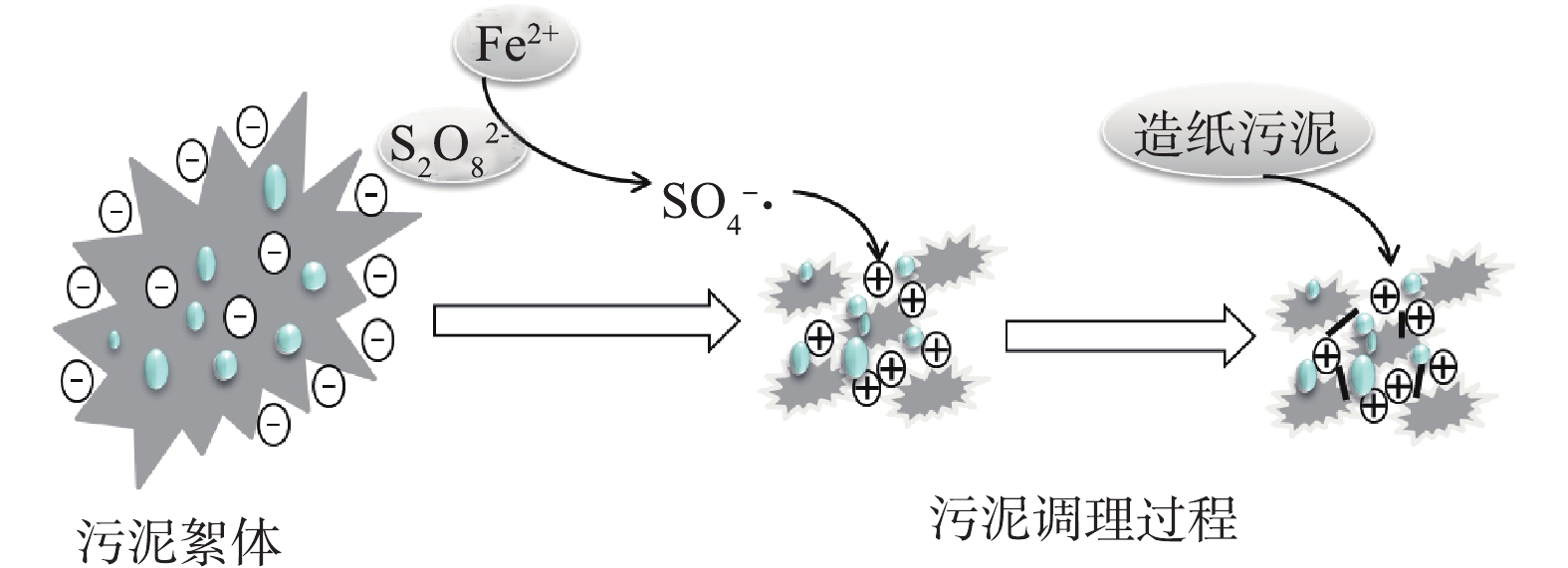
第2组较第1组的含水率、SRF和CST有所降低。这是因为初沉污泥中含有的细小纤维在污泥抽滤过程中形成了水通道,使水分有效脱出。污泥调理示意图如图5所示。第3组的含水率较第1、2组有所降低。这是因为亚铁活化过硫酸盐产生强氧化性的SO4−·将胞外聚合物氧化破解,细胞内部水分释放,降低泥饼含水率。第4组与第5组相比,泥饼的含水率以及SRF、CST指标较高。这可能是因为造纸污泥中的纤维粒径过大,不能起到骨架支撑的作用,不利于内部水分脱除。第5组将原泥与初沉污泥进行混合后再用过硫酸盐进行调理,SO4−·的强氧化性可以将纤维分解为小粒径,使其在污泥内部成功搭建骨架,胞外聚合物破解后将内部的水分释放,可以通过水通道将水分抽滤脱除,使泥饼的含水率进一步降低,这一现象与吴彦[16]的研究结果一致,当稻壳粉的粒径为109~150 μm时,泥饼的含水率降至最低。
-
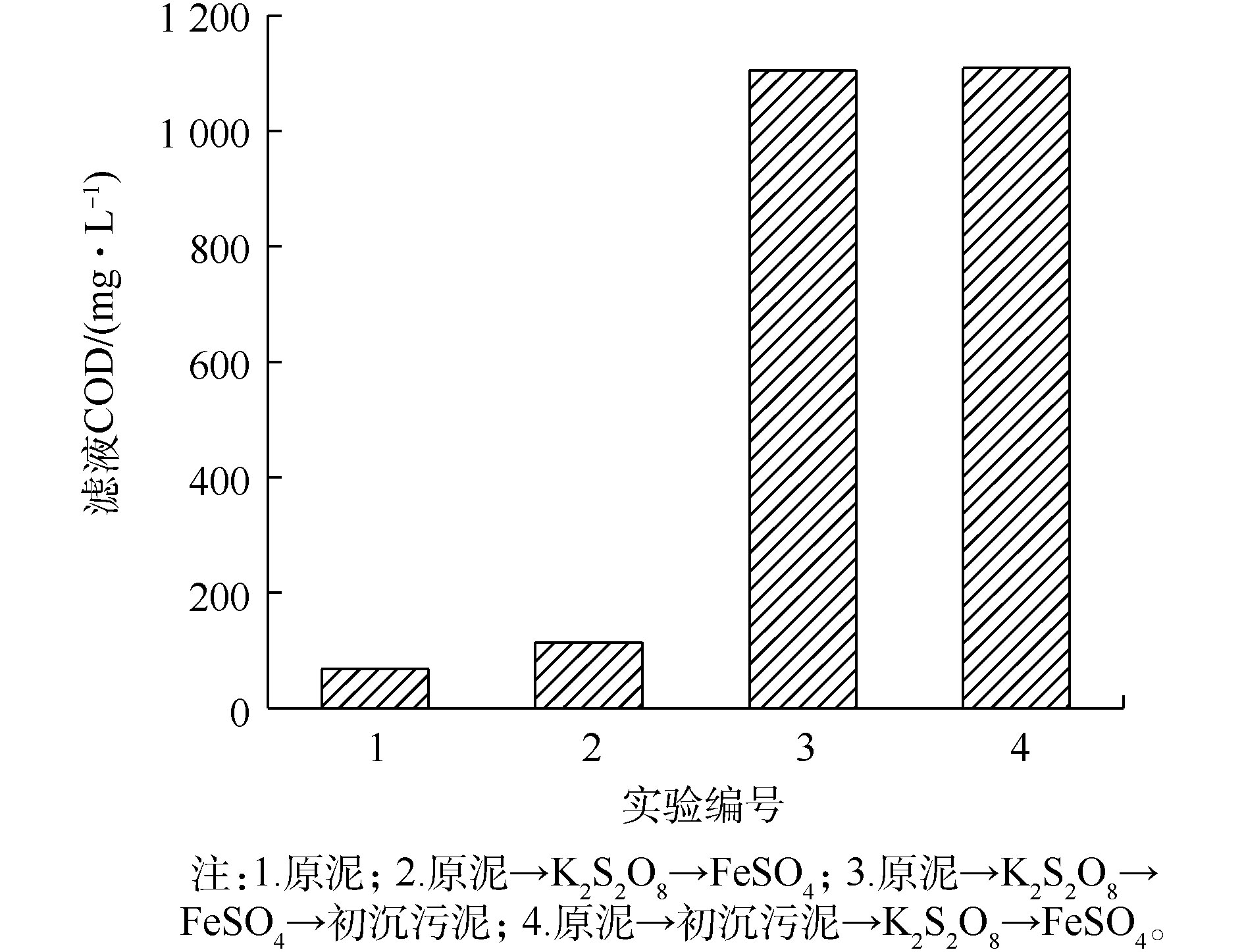
不同调理方式对污泥滤液COD的影响如图6所示。由图6可以看出,原泥滤液COD为67.22 mg·L−1,经过硫酸盐调理之后滤液COD上升至114.4 mg·L−1。这是因为
SO2−4 ·将EPS破解使细胞内部的蛋白质、多糖、核酸等有机物释放进入污泥中,经过滤后有机物进入滤液中,导致滤液COD含量升高。而经造纸污泥联合调理之后滤液COD上升至1 104.67 mg·L−1,较原泥滤液COD增加了16.5倍。这是因为初沉污泥中含有EPS和大量有机物,在构建骨架的同时,部分有机物进入滤液中,造成滤液COD值急剧增加。 -
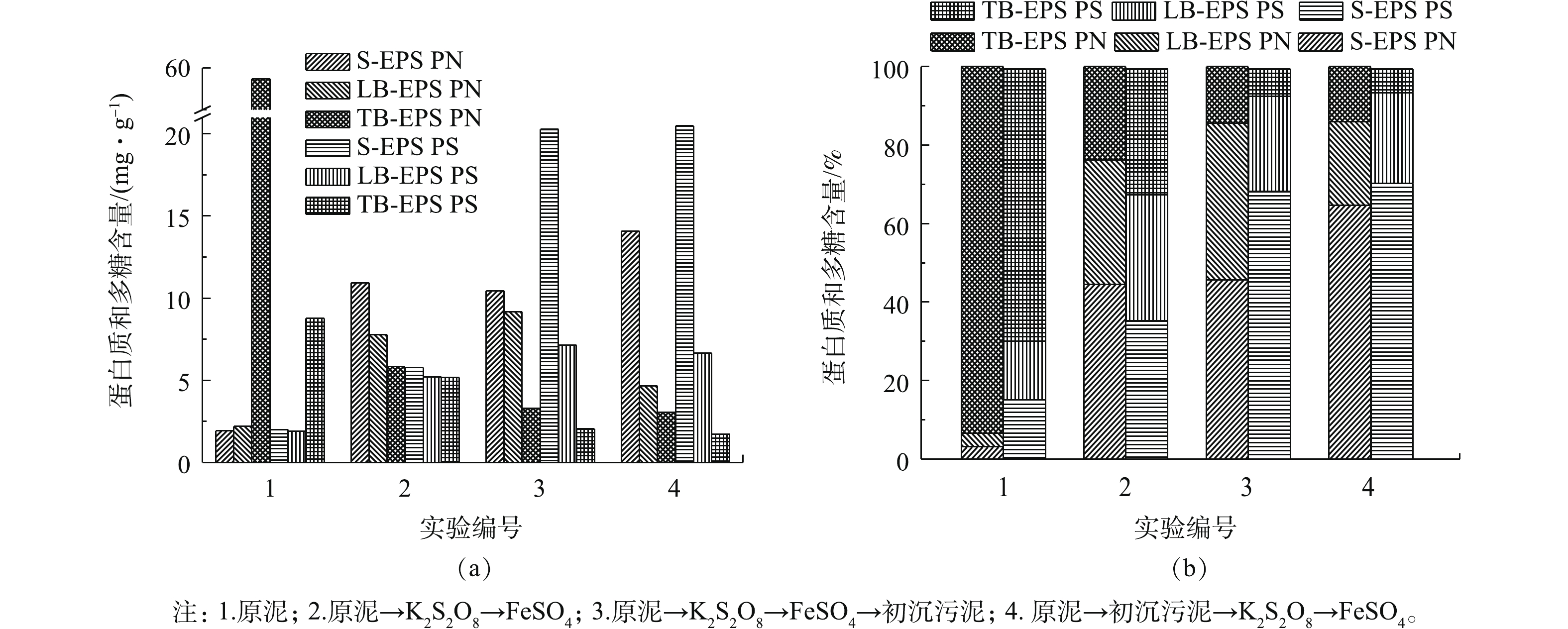
不同调理方式对污泥EPS中蛋白质(PN)和多糖(PS)的影响如图7所示。由图7可以看出,原泥中PN和PS的分布关系为TB-EPS>LB-EPS>S-EPS,经调理后PN和PS的分布关系为S-EPS>LB-EPS>TB-EPS,其中变化最为显著的是第4组。由图7(a)可以看出,S-EPS中的PN由1.92 mg·g−1上升至14.074 mg·g−1,较原泥增加61.56%;PS由1.99 mg·g−1上升至20.48 mg·g−1,较原泥增加55.25%。同时,由图7(b)可以看出,经调理后污泥的S-EPS中的PN和PS明显增多,而TB-EPS和LB-EPS中的PN和PS也显著增多,这一结果与张昊[18]的研究相一致。
因为污泥中的EPS被SO4−·氧化破解,使细胞内部的PN和PS等物质释放,转化为溶解态,使得S-EPS中PN和PS含量增大。调理后PN和PS的含量较原泥有大幅降低,因为
SO2−4 ·具有强氧化性,可以将PN和PS氧化分解为小分子的有机物。骨架复合调理较单独使用过硫酸盐调理的S-EPS中PN和PS要多,是因为造纸污泥中也存在EPS,SO2−4 ·会将其氧化释放,使得PN和PS的含量增多。 -
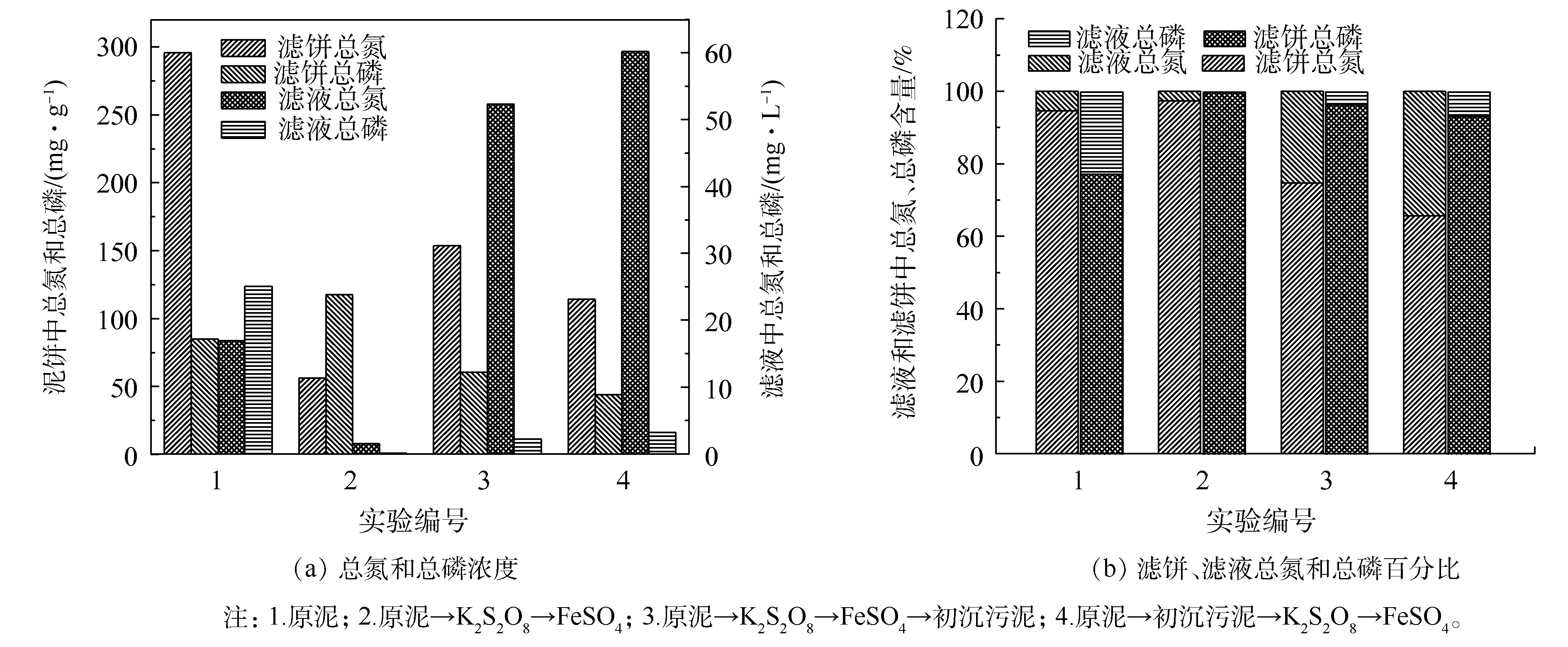
不同调理方式对滤饼和滤液中总氮、总磷的影响如图8所示。由图8(a)可以看出,原泥泥饼中总氮的含量为295.75 mg·g−1,总磷的含量为85.00 mg·g−1。这是因为经脱氮除磷工艺后,将大部分的氮和磷固定在污泥当中,最终随污泥排出污水处理系统。由图8(b)可以看出,经过硫酸盐单独调理的污泥,泥饼中总磷的含量较原泥所占比例更大。这是因为污泥中存在Fe3+和Fe2+,会吸附泥饼中的磷,产生沉淀,截留在泥饼中造成泥饼中总磷所占比例增加,这一结果与阚丹等[19]的研究中混价铁氢氧化物对无机磷的吸附/沉淀相一致。
经初沉污泥复合调理后,泥饼中总氮所占比例下降,由原泥的94.60%下降至65.62%。这是因为2种污泥中的EPS被破解,将含有N元素的物质(蛋白质、核酸等)释放到滤液中,造成滤液中总氮的增加,而总磷由于Fe3+和Fe2+的存在并无显著变化。总氮和总磷分布关系的变化验证了
SO2−4 ·的强氧化性能可破解EPS,从而提高污泥脱水性能。 -
1)经初沉污泥复合调理后污泥的脱水效果显著增强,SRF由121.18×1012 m·kg−1下降至32.67×1012 m·kg−1,降低了73.04%;泥饼含水率由75.51%下降至71.75%,降低了4.98%。
2)经过硫酸盐调理之后滤液COD由67.22 mg·L−1上升至114.4 mg·L−1,而经造纸污泥联合调理之后滤液COD上升至1,104.67 mg·L−1,较原泥滤液COD增加了16.5倍。
3)过硫酸盐可以有效破解EPS,使细胞内部水分释放,并通过初沉污泥骨架形成的水通道排出,从而有效降低泥饼的含水率,调理后泥饼中PN和PS的分布关系为S-EPS>LB-EPS>TB-EPS。
4)经调理后的污泥由于EPS的破解,使泥饼中总氮所占比例由原泥的94.60%下降至65.62%,而总磷由于Fe3+和Fe2+所产生的吸附/沉淀作用并无显著变化。
Fe2+活化过硫酸盐对市政污泥EPS性能的影响
Effect of Fe2+ activated persulfate on EPS properties of sewage sludge
-
摘要: 针对污泥难以脱水、处理难度大的问题,通过过硫酸盐高级氧化技术联合造纸污泥作为骨架对市政污泥进行调理,以泥饼含水率、污泥比阻(SRF)、毛细吸水时间(CST)、胞外聚合物(EPS)中蛋白质和多糖的分布关系,以及滤饼和滤液中总氮、总磷含量为指标,研究Fe2+活化过硫酸盐联合造纸污泥骨架构建体对EPS的影响。结果表明:将造纸污泥与市政污泥1∶2混合,再添加过硫酸盐和Fe2+,对污泥的调理效果最好,泥饼的含水率由74.52%降至69.57%,SRF降低了66.23%;蛋白质和多糖的分布关系为S-EPS>LB-EPS>TB-EPS,滤饼中总氮所占比例由94.60%下降至65.62%,EPS被有效破解,污泥脱水效果显著改善。
-
关键词:
- 市政污泥 /
- 造纸污泥 /
- 骨架 /
- 胞外聚合物(EPS)
Abstract: In response to the difficulty in sewage sludge dewatering and treatment, the combination of Fe2+-activated persulfate oxidation and skeleton builders of paper sludge was used to condition the sewage sludge. In this study, moisture content of sludge cake, specific resistance to filtration (SRF), capillary sunction time (CST), the distribution of protein and polysaccharide in the EPS, and the total nitrogen and total phosphorus content in the filter cake and filtrate were used to evaluate the effect of above combination on the EPS. The result showed that when the sewage sludge was mixed with the paper sludge with a ratio of 1:2, the addition of Fe2+ and persulfate could result in the best dewaterability effect. The moisture content of sludge cake decreased from 74.52% to 69.57%, and the SRF was reduced by 66.23%. The distribution of protein and polysaccharide was S-EPS>LB-EPS>TB-EPS, and the proportion of total nitrogen in cake decreased from 94.60% to 65.62%. The EPS was effectively disrupted, and the sludge dewaterability was significantly improved.-
Key words:
- sewage sludge /
- paper sludge /
- skeleton /
- extracellular polymeric substance (EPS)
-
近年来,随着人们生活水平的提高,我国餐厨垃圾产生量以每年10%的速度增长,截至2018年,餐厨垃圾产生量突破了1×108 t,占城市生活垃圾的57%左右。餐厨垃圾含有的大量有机物质容易腐烂变质并携带病原菌,不仅污染环境而且威胁人体健康。同时,餐厨垃圾又富含碳水化合物、蛋白质和油脂,营养价值高,是有机废物厌氧能源化的理想底物[1]。氢能被广泛认为是未来最具潜力的绿色可再生能源之一[2],与传统的电解水、化石燃料制氢相比,暗发酵生物制氢具有运行成本低、能耗低、操作简单等特点,可实现餐厨垃圾等高浓度复杂有机废物的能源化利用,成为最具前景的氢能制备策略之一,符合我国绿色可再生能源的战略需求。
暗发酵制氢是产氢微生物利用氢酶的催化作用将有机物降解产生氢气,同时生成挥发性脂肪酸(VFA)、乙醇等代谢产物的过程。当末端产物为乙酸时,葡萄糖的理论产氢量为4 mol·mol−1,但实际产氢量不足2 mol·mol−1,底物的氢能转化效率不足50%[3]。有研究[4-7]表明,暗发酵制氢与[2Fe-2S]铁氧化还原蛋白和[4Fe-4S]氢酶的活性密切相关,铁氧还原蛋白可作为氢化酶的电子载体参与氢分子的产生过程,其中,铁是其重要组成部分,能够影响微生物的产氢潜力[8]。此外,铁离子的种类和含量也会影响微生物的产氢功能基因表达,进而影响复杂底物的产氢性能[9]。因此,如何克服高浓度有机废物暗发酵制氢过程的代谢障碍,提高复杂底物的利用效率和产氢潜力是制约暗发酵生物制氢技术的瓶颈问题。
有研究[10-12]发现,投加纳米零价铁(NZVI)和零价铁(ZVI)可以提高暗发酵制氢过程中的微生物活性,进而提高暗发酵制氢潜力和底物的利用效率。ZVI以其低成本成为氢发酵中最具吸引力的添加剂,能够降低发酵系统中的氧化还原电位(ORP),可以为发酵菌提供更有利的环境[13]。ZHANG等[14]研究了ZVI对葡萄糖发酵产氢量的影响,当ZVI浓度为400 mg·L−1时,最大产氢量为1.22 mol·mol−1,比对照组高出了37.1%。ZHU等[15]发现,ZVI的浓度为16 g·L−1时,产氢量从3.8 mol·mol−1提高到8.7 mol·mol−1。NZVI具有较高的催化活性和较大的表面积,从而提高了暗发酵制氢过程的效率[16]。NATH等[17]采用NZVI强化葡萄糖间歇暗发酵产氢,发现当NZVI为100 mg·L−1时,最大产氢量可达到1.9 mol·mol−1,比未加NZVI的对照组高出1倍。ZADA等[18]发现,在加入250 mg·L−1 NZVI条件下,水葫芦的产氢量从31.7 mL·g−1增加到57 mL·g−1。可见,投加NZVI和ZVI添加剂均可提高产氢性能,且具有操作简单、能耗低的优点。目前,研究主要集中在投加NZVI与ZVI对以葡萄糖、蔗糖等单一底物暗发酵制氢性能的影响,而以餐厨垃圾等复杂有机废物为底物,深入研究暗发酵制氢过程中铁离子转化规律和产氢酶活性的影响还鲜有报道。本研究通过投加不同浓度的NZVI和ZVI,研究了其对餐厨垃圾在(55±1) ℃高温条件下的暗发酵制氢潜力、末端代谢产物变化规律的影响,通过分析发酵前后铁离子组成及浓度变化、氢化酶和脱氢酶活性表达,探究了NZVI与ZVI强化餐厨垃圾暗发酵制氢的作用机制,以期为餐厨垃圾等复杂有机废物的绿色能源化提供科学依据。
1. 材料与方法
1.1 实验原料
本实验所用的餐厨垃圾取自北京市某大学食堂,分拣出餐厨垃圾中骨头、塑料袋等杂质后破碎至5 mm,经90 ℃水热预处理30 min,离心去油(去油可提高餐厨垃圾的水解效果,利于提高产气潜力[19]),置于4 ℃冰箱备用[20]。接种污泥取自北京某生活垃圾综合处理厂的干式厌氧发酵剩余污泥。实验材料的基本理化指标如表1所示。
表 1 实验材料基本理化指标Table 1. Basic physical and chemical indexes of experimental materials分析项目 TS/% VS/% VS/TS/% 含水率/% pH COD/(mg·L−1) C/% N/% 餐厨垃圾(水热后) 22.55 20.59 91.31 77.45 6.07 107 100 53.10 3.94 接种污泥 15.13 7.59 50.15 84.87 7.20 7 600 22.13 2.27 1.2 实验设计
将11.65 g经水热去油预处理的餐厨垃圾与50 g接种污泥混合放入500 mL广口瓶中,接种比为0.63∶1(VS∶VS),分别加入不同浓度(0、100、200和300 mg·L−1)的NZVI和ZVI,实验反应器情况记为:NZVI-0、NZVI-1、NZVI-3和ZVI-0、ZVI-1、ZVI-2、ZVI-3。加去离子水定容至200 mL,有机负荷为6 g·(L·d)−1(以VS计),采用1 mol·L−1 HCl与1 mol·L−1 NaOH调节初始pH为6,通氮气10 min排除反应装置内空气。在(55±1) ℃的高温条件下进行暗发酵制氢,搅拌速度为120 r·min−1,采用排水法收集产生的气体。实验编号如表2所示。
表 2 暗发酵产氢动力学分析Table 2. Dynamic analysis of dark fermentation hydrogen production实验组 Pmax/mL Rmax/(mL·h−1) λ/h R2 NZVI-0 220.72 38.41 1.95 0.999 55 NZVI-1 259.25 49.43 3.27 0.999 35 NZVI-2 224.87 47.04 2.66 0.999 85 NZVI-3 248.70 76.48 6.02 0.996 37 ZVI-0 308.51 216.07 5.72 0.998 48 ZVI-1 425.72 66.32 4.59 0.998 44 ZVI-2 350.91 70.96 5.58 0.998 90 ZVI-3 459.24 77.67 4.72 0.989 22 注:Pmax代表最大产氢量潜力,Rmax代表最大产氢速率,λ表示反应启动时间。 1.3 分析方法
铁离子浓度采用GB/T 12496.19-2015邻菲啰啉分光光度计法测定;氢化酶、脱氢酶活性采用辛红梅等[21]方法测定。VFA和乙醇浓度测定采用9790II气相色谱仪分析测定,色谱条件为:色谱柱采用CP-Wax(FFAP)25 m×0.32 mm×0.2 μm毛细管柱,FID氢火焰离子检测器,进样量1 μL,柱温箱初始温度为80 ℃,保持5 min,以10 ℃·min−1速率升温至190 ℃;进样口和检测器温度为250 ℃;高纯氮气为载气,流速为1.5 mL·min−1。气体成分测定采用上海天美公司GC7900气相色谱仪分析发酵气相产物和含量,色谱条件为:色谱柱采用填充柱,TCD热导检测器,分析柱1为2 m hayesep Q,分析柱2为5 A分子筛3 m;柱温箱120 ℃,进样口和检测器温度为150 ℃,电流为30 mV,载气为高纯氩气,进样量为1 mL。以峰面积定量,校正归一法计算气体含量。
2. 结果与讨论
2.1 NZVI和ZVI对餐厨垃圾暗发酵制氢性能的影响
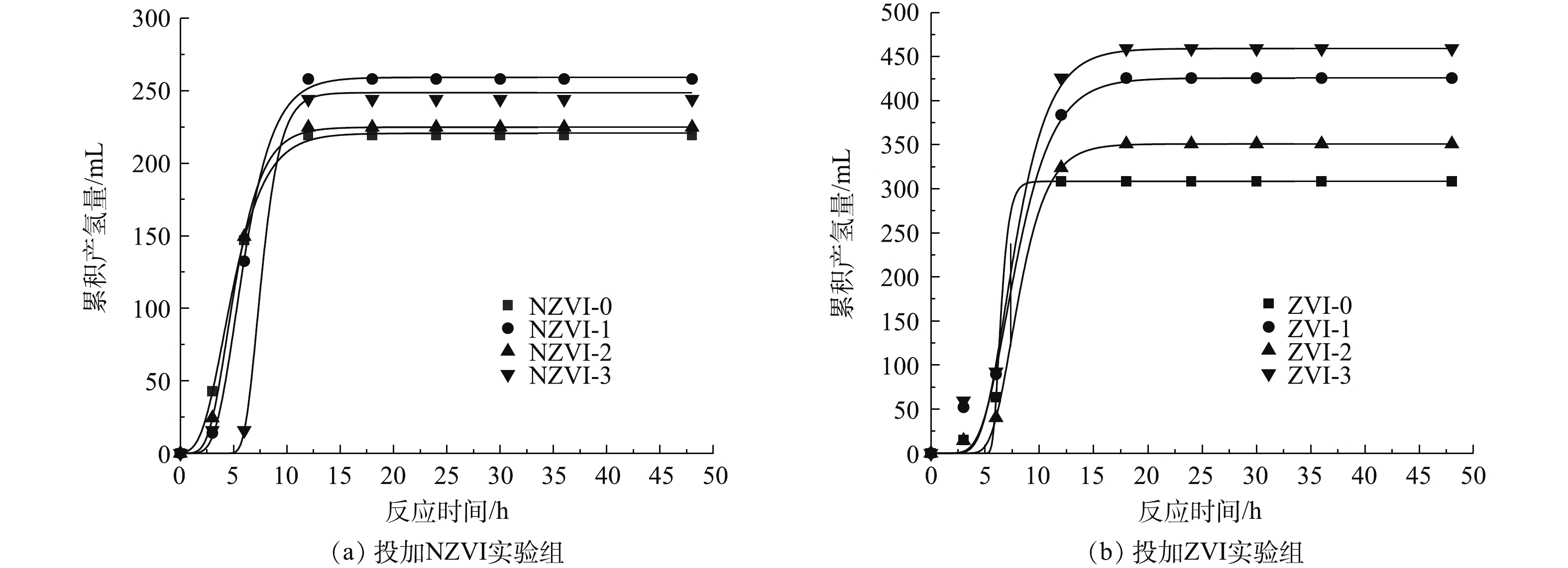
1) NZVI和ZVI对暗发酵制氢性能的影响。图1为不同浓度NZVI和ZVI对餐厨垃圾高温暗发酵累积产气量和氢气百分含量的影响结果。结果表明,所有实验组在暗发酵前18 h累积产气量显著提高,之后累积产气量增加趋势变缓直至趋于稳定。在暗发酵产氢的过程中,氢气百分含量呈现先升高后降低的趋势。在投加NZVI添加剂时,浓度为100 mg·L−1的NZVI-1组的暗发酵制氢性能最好,累积产气量和氢气百分含量在12 h和30 h达到最大值,分别为676 mL(单位VS产气量为281.68 mL)和83.76%,是未投加NZVI实验组的1.08倍和1.1倍。其次为NZVI-0实验组,累积产气量和氢气百分含量分别为625 mL(单位VS产气量为260.43 mL)和79.16%。由此可见,与未投加NZVI相比,NZVI-1组最多可提高产气量51 mL(单位VS产气量为21.25 mL),提高氢气百分含量8.53%。
在投加ZVI添加剂时,暗发酵产氢性能较好的实验组为投加浓度300 mg·L−1的ZVI-3组和浓度100 mg·L−1的ZVI-1组,获得累积产气量分别为798 mL和732 mL(单位VS产气量分别为332.51 mL和305.01 mL),最大氢气百分含量分别为72.79%和81.95%,从节省添加剂的角度考虑,暗发酵产氢性能最好的是添加ZVI浓度为100 mg·L−1的ZVI-1组。由此可见,与未投加ZVI相比,投加100 mg·L−1 ZVI最多可提高产气量90 mL(单位VS产气量为37.50 mL),提高氢气百分含量2.74%。
2)NZVI和ZVI产氢动力学分析。在累积产气量和氢气百分含量分析基础上,利用修正过的Gompertz模型对暗发酵产氢过程的累积产氢量进行动力学拟合,产氢动力学分析结果如图2和表2所示。由图2可知,除NZVI-3实验组外,投加NZVI实验组的启动时间均比投加ZVI实验组短,但ZVI组的最大产氢潜力和最大产氢速率均比NZVI组高。在投加NZVI实验组中,NZVI-0实验组启动时间最短,为1.95 h,但最大产氢潜力和最大产氢速率均为最低,分别为220.72 mL和38.41 mL·h−1。浓度为100 mg·L−1的NZVI-1组最大产氢潜力最高为259.25 mL,浓度为300 mg·L−1的NZVI-3实验组的最大产氢速率最高,为76.48 mL·h−1。虽然NZVI-3实验组的最大产氢速率值最高,但其启动时间(6.02 h)是NZVI-1实验组(3.27 h)的1.84倍。NZVI-3实验组的最大产氢潜力(248.70 mL)也小于NZVI-1实验组(259.25 mL)。由此可见,投加NZVI可以提高最大产氢速率和最大产氢潜力,且投加浓度为100 mg·L−1时达到的效果最好。
投加ZVI的实验组的产氢潜力均高于未投加ZVI的ZVI-0实验组(308.51 mL)。其中,ZVI-3实验组的最大产氢潜力最高,为459.24 mL,ZVI-1实验组次之,为425.72 mg·L−1。此外,ZVI-1实验组的启动时间最短,为4.59 h。当ZVI投加量为100 mg·L−1时,餐厨垃圾最大产氢潜力是投加NZVI实验组的1.64倍。可见投加ZVI可有效提高产氢微生物对底物的利用效率和产氢潜力。
2.2 NZVI和ZVI对餐厨垃圾暗发酵制氢发酵途径的影响
乙醇和VFAs是暗发酵制氢的重要末端代谢产物,根据其浓度和组成可将暗发酵制氢的代谢类型分为乙醇型发酵、丁酸型发酵、丙酸型发酵和混合酸发酵[22]。投加不同浓度的NZVI和ZVI后,餐厨垃圾暗发酵制氢末端乙醇和VFAs各组分占比如图3所示。结果表明,末端代谢产物中以乙醇、乙酸和丁酸为主,其中乙醇占比最高(53.71%~77.09%),发酵类型是以乙醇型发酵为主的混合型发酵。与未投加ZVI的实验组相比,投加浓度为300 mg·L−1的ZVI-3实验组中的乙醇浓度提高了7.04%。
在投加NZVI的实验组中,乙酸在NZVI-1、NZVI-2、NZVI-3组中末端代谢产物中的占比分别为18.04%、16.89%、14.22%,均高于NZVI-0对照组(9.42%)。而对于投加ZVI的实验组,ZVI-1、ZVI-2、ZVI-3实验组中乙酸在末端代谢产物中的占比分别为6.44%、7.70%、6.62%,均低于ZVI-0对照组(8.18%)。由此可见,与投加ZVI相比,投加NZVI更有利于乙酸的转化,但产氢潜力和速率有所较低。可能由于发酵过程中产生的乙酸使体系pH降低,产生过剩的NADH+H+,未能被氧化为NAD+,影响微生物酶活或酶合成,进而抑制NADH/NAD+平衡产氢[23]。
投加NZVI的实验组相比未投加NZVI的实验组(67.7%),其中乙醇的占比均有所降低。对应投加NZVI的实验组,随着NZVI投加量的增加,乙醇占比由53.71%逐渐升高至63.50%,同时累积产气量和氢气百分含量有所下降,这说明NZVI在一定程度上改变了产氢细菌的代谢产氢途径,产生了更多的乙醇副产物和更少的乙酸副产物,投加低浓度的NZVI有利于产氢,浓度过高可能对微生物活性产生了抑制作用。投加ZVI的实验组相比未投加ZVI的实验组(70.05%),其中乙醇的占比略有提高。随着ZVI投加量的增加,乙醇占比由72.65%升高至77.09%,同时在ZVI-3实验组中的累积产气量大于ZVI-1实验组。发酵过程中所产生的乙醇可以氧化过多的NADH+H+,有利于产氢潜力的提高[23]。对于投加NZVI和ZVI的实验组,暗发酵末端代谢产物中乙醇的占比均有所升高,但累积产气量的变化趋势却相反,这可能是由于2种添加剂对与产氢相关的关键酶影响有所不同。
2.3 NZVI和ZVI对餐厨垃圾暗发酵制氢ORP的影响
在发酵过程中,ORP是控制微生物代谢和增殖的重要参数之一[24-25]。其可以通过还原/氧化NAD(NADH/NAD+)来改变细胞内外的ORP,从而调控微生物代谢。一般认为,厌氧微生物所需ORP的最适范围为-180~-260 mV[26]。
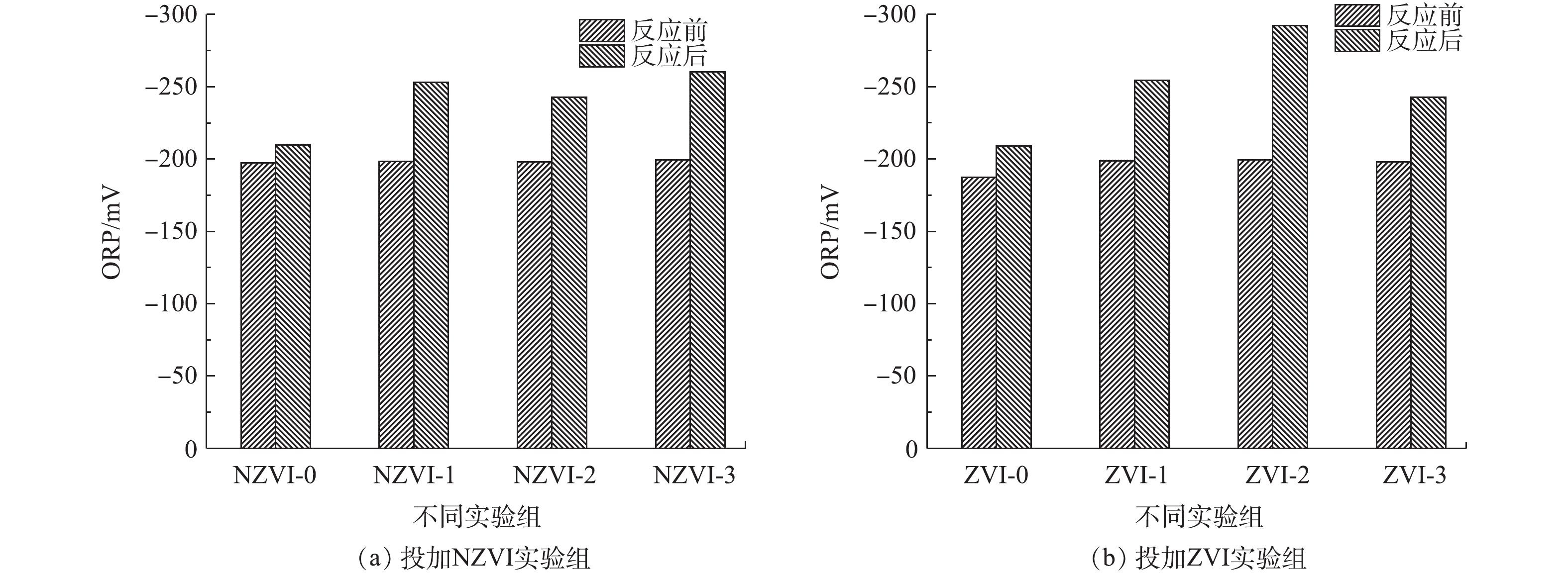
暗发酵产氢前后体系中的ORP变化结果如图4所示。结果表明,投加与未投加NZVI和ZVI的实验组在反应结束后ORP均有所下降,其中投加NZVI与ZVI的实验组中ORP下降更为显著。投加NZVI的实验组,NZVI-3实验组ORP下降最大,由反应前的−199.6 mV下降至−260.1 mV,是未投加NZVI实验组的1.24倍。其次是NZVI-1实验组,由反应前的−198.5 mV下降至−253 mV,是未投加NZVI实验组的1.20倍。对于投加ZVI的实验组,ZVI-2实验组的ORP下降最大,由反应前的−199.4 mV下降至−292.2 mV,是未投加ZVI实验组的1.39倍。其次是ZVI-1实验组,由反应前的−198.8 mV下降至−254.3 mV,是未投加ZVI实验组的1.21倍。
结合产氢潜力结果分析可知,产氢效果好的NZVI-1实验组(−253 mV)与ZVI-1实验组(−254.3 mV)ORP值相近,均在厌氧微生物最适ORP的范围内,从而有利于产氢性能的提高。分析原因可能是:反应器内的ORP迅速降低,说明分子氧等氧化剂被消耗掉,这可能由于投加的NZVI和ZVI被用作电子供体,铁可作为底物诱导因子,作用于细菌代谢途径中,既能参与细菌的生物氧化过程,又能使反应器内的ORP迅速降低,使ORP维持在产氢的最适范围内,从而提供更好的还原条件[27-29];另一方面,氢化酶活性和NAD+/NADH平衡产氢均需要较低的ORP[30]。
2.4 NZVI和ZVI对餐厨垃圾暗发酵制氢过程中铁离子浓度的影响
图5表示投加NZVI和ZVI进行暗发酵制氢前后,各实验组发酵液中Fe2+和Fe3+浓度的变化情况。由图5可知,在餐厨垃圾暗发酵制氢前,体系中Fe2+和Fe3+的浓度较低,分别为23.74 mg·L−1和28.52 mg·L−1。反应结束后,未投加NZVI与ZVI的实验组中Fe2+和Fe3+的浓度有所下降,投加NZVI与ZVI的实验组中Fe2+浓度显著上升,而Fe3+浓度略有提升,这证明了NZVI和ZVI是作为电子供体而存在的。铁在产氢细菌的代谢机制中起着至关重要的作用,是形成氢化酶和铁氧还蛋白的重要成分[31]。Fe2+可以促进了生物量的增长和功能基因的表达,从而促进氢气的产生。对于投加NZVI的实验组,NZVI-3实验组中的Fe2+浓度最高,为43.78 mg·L−1,是未投加NZVI实验组的2倍,NZVI-2的Fe2+浓度次之,为42.47 mg·L−1,是未投加NZVI实验组的1.96倍。在投加ZVI的实验组,ZVI-1实验组的Fe2+浓度最高,为38.21 mg·L−1,是未投加ZVI实验组的1.96倍,ZVI-3的Fe2+浓度次高,为36.51 mg·L−1,是未投加ZVI实验组的1.87倍。
厌氧微生物可以将Fe3+还原为生物利用性更高的Fe2+。在投加NZVI的实验组中,NZVI-2实验组的Fe3+浓度最高,为15.99 mg·L−1,是未投加NZVI实验组的1.72倍,NZVI-1的Fe3+浓度次之,为14.21 mg·L−1, 是未投加NZVI实验组的1.53倍。在投加ZVI的实验组中,ZVI-3实验组的Fe3+浓度最高,为12.12 mg·L−1,是未投加ZVI实验组的1.30倍,ZVI-1的Fe3+浓度次之,为10.34 mg·L−1,是未投加ZVI实验组的1.28倍。
综上所述,在暗发酵制氢体系中投加NZVI和ZVI,可使Fe2+浓度升高,Fe3+浓度略有升高。一方面,这是由于投加的NZVI和ZVI有部分转化为了Fe2+;另一方面是由于微生物对Fe3+的利用将Fe3+还原成Fe2+。但投加NZVI与ZVI浓度过高,铁离子会与蛋白质结合生成难以被生物降解的螯合物,故使产氢潜力下降[32]。
2.5 NZVI和ZVI对餐厨垃圾暗发酵制氢过程pH的影响
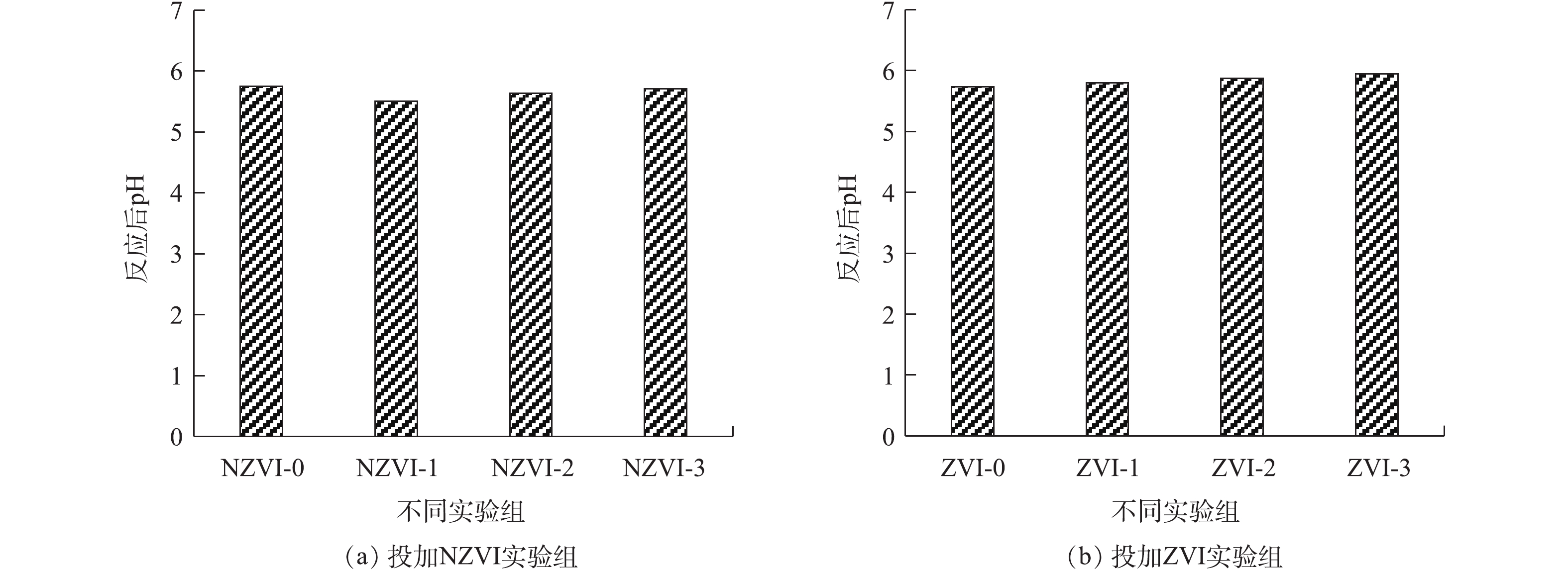
反应结束时pH的变化情况如图6所示。由图6可知,NZVI和ZVI对反应器的pH的影响作用并不明显。在暗发酵制氢反应结束时,投加NZVI和ZVI的实验组的pH均在5.5~6.0。在投加NZVI实验组中,pH最高的实验组为NZVI-3实验组(5.71),最低的为NZVI-1实验组(5.51)。投加ZVI的实验组中,pH最高的为ZVI-3实验组(5.94),最低的为ZVI-1实验组(5.8)。随着投加NZVI和ZVI浓度的增加,pH也随升高。这可能是由于投加的NZVI和ZVI作为诱导因子作用于细菌代谢途径中,参与了产氢细菌的生物氧化过程,发酵类型为以乙醇型发酵为主的混合型发酵[33]。末端代谢产物中乙醇的占比随着NZVI和ZVI投加量的增加而增大,从而导致了pH的升高。投加NZVI的实验组在反应结束时pH低于未投加NZVI的实验组(5.75),投加ZVI的实验组在反应结束时pH高于未投加ZVI实验组,这说明与投加ZVI相比,投加NZVI更有利于乙酸的转化,产生的乙酸可使体系pH降低。
2.6 NZVI和ZVI对餐厨垃圾暗发酵制氢过程中酶活性的影响
有机物的暗发酵制氢过程是在一系列酶和辅酶以及中间传递体的作用下完成的一种生物氧化过程。其中,氢化酶是一类能够高效可逆地催化产生氢气的酶,含有双核铁原子的铁氢化酶具有很高的催化活性。脱氢酶中的电子载体铁氧还蛋白是暗发酵生物氧化过程产生氢分子的重要功能蛋白。可见,铁是决定餐厨垃圾暗发酵制氢过程氢化酶和脱氢酶活性的重要物质,对产氢微生物的生长代谢有着重要的影响。
投加不同浓度的NZVI和ZVI对氢化酶和脱氢酶活性的影响结果如图7所示。结果表明,对于未投加NZVI与ZVI的实验组,氢化酶活性分别为2.49 mL·(g·min)−1和2.76 mL·(g·min)−1(以VSS计)。在投加NZVI后,氢化酶活性有所提高,其中,NZVI-3组的氢化酶活性最高,为2.56 mL·(g·min)−1,是未投加NZVI实验组的1.02倍,NZVI-1实验组氢化酶活性次高,为2.55 mL·(g·min)−1。在投加ZVI后,氢化酶活性有显著提高。ZVI-3实验组氢化酶活性(3.96 mL·(g·min)−1)最高,是ZVI-0实验组的1.43倍。ZVI-1实验组次之,为3.54 mL·(g·min)−1。有研究[5]表明,NZVI可以降低培养基中溶解氧的水平,从而提高氢化酶的活性。李永峰等[33]提出金属元素在微生物生命活动中具有重要作用,其对酶的作用主要有2方面:一是作为酶的辅助因子,在酶促反应中运输转移电子、原子或某些功能基团参与氧化还原或运载酰基团作用;二是作为激活剂来提高酶的活性。铁作为铁氧还蛋白及氢化酶重要的组成成分,投加NZVI和ZVI可以提高铁氧还蛋白和氢化酶的活性,促进电子的转移,进而提高产氢效能。
对于NZVI-0和ZVI-0实验组,脱氢酶活性分别为128.32 μg·(g·min)−1和140.53 μg·(g·min)−1(以VSS计)。然而,投加NZVI的实验组脱氢酶活性出现了显著下降,由NZVI-0实验组的128.32 μg·(g·min)−1下降到NZVI-1实验组的34.37 μg·(g·min)−1,下降了73.2%。且随着投加NZVI浓度增加,脱氢酶活性继续下降,NZVI-3实验组中脱氢酶活性下降到最低,为8.40 μg·(g·min)−1。在投加ZVI的实验组中,脱氢酶活性有显著的提高。脱氢酶活性在ZVI浓度小于300 mg·L−1时,随着投加ZVI浓度的增加,其由140.53 μg·(g·min)−1提高到150.84 μg·(g·min)−1,提高了7.3%,但当ZVI浓度为300 mg·L−1时,脱氢酶活性下降到80.96 μg·(g·min)−1。这说明过高的ZVI浓度抑制了脱氢酶的活性。结合相关文献,其原因可能是因为铁的投加量过高超出了体系中产氢微生物的所需,而过剩的铁形成了铁盐或亚铁盐,从而使系统的渗透压升高,导致脱氢酶活性的降低[21]。
有研究[34]表明,当金属元素浓度维持在较低水平时,对微生物可以起到激活作用,但当浓度过高时,便会对微生物的酶活性产生抑制作用。由此可见,投加ZVI的同时提高了氢化酶和脱氢酶的活性。结合铁离子浓度变化趋势可知,投加的NZVI和ZVI会向系统环境中释放铁离子,为微生物提供生长代谢过程中所需的铁元素并提高氢化酶活性。但投加NZVI时虽然提高了氢化酶活性,脱氢酶活性却受到了抑制,这可能缘于纳米材料中活性氧的生成和氧化应激反应引起的生物毒性损害了微生物细胞结构,导致细胞死亡,进而影响微生物产氢能力[35]。
由此可见,投加100 mg·L−1 NZVI和ZVI均可有效提高氢化酶活性,投加ZVI还可提高脱氢酶活性,有利于产氢微生物的暗发酵制氢。
3. 结论
1)投加NZVI和ZVI均可显著提高餐厨垃圾暗发酵制氢性能,投加100 mg·L−1 ZVI效果最佳,最大产氢潜力和最大产氢速率分别为425.72 mL和66.32 mL·h−1,是投加NZVI实验组的1.64倍和1.34倍。投加NZVI与ZVI后,末端代谢产物以乙醇、乙酸和丁酸为主,其中乙醇占比最高(53.71%~77.09%),发酵类型是以乙醇型发酵为主的混合型发酵。
2)投加NZVI和ZVI可使反应体系中ORP显著下降,有利于暗发酵制氢的进行。反应结束后,未投加NZVI与ZVI的实验组中Fe2+和Fe3+的浓度较反应前均有所下降,投加NZVI与ZVI的实验组Fe2+浓度有显著上升,Fe3+浓度略有提升。在投加的NZVI和ZVI浓度为300 mg·L−1时,Fe2+浓度分别是未投加NZVI和ZVI实验组的2倍和1.87倍。
3)投加NZVI和ZVI均可有效提高氢化酶活性,投加100 mg·L−1 ZVI-1实验组氢化酶活性最佳,为3.54 mL·(g·min)−1,是NZVI-1实验组的1.38倍。投加ZVI可同时提高氢化酶和脱氢酶活性,有利于产氢微生物的暗发酵制氢。
-
表 1 污泥的特性
Table 1. Characteristics of sludge
含水率/% 污泥比阻/(1012 m·kg−1) 毛细吸水时间/s pH 有机质(VSS/TSS)/% 98.68 238.97 199.8 6.71 49.85 -
[1] KRACH K R, BURNS B R, LI B, et al. Odor control for land application of lime stabilized biosolids[J]. Water, Air and Soil Pollution, 2008, 8(3/4): 369-378. [2] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. 城镇污水处理厂污泥处置混合填埋用泥质: GB/T 23485-2009[S]. 北京: 中国环境科学出版社, 2012. [3] 高廷耀, 顾国维, 周琪. 水污染控制[M]. 北京: 高等教育出版社, 2015. [4] MARIE C, ZHANG Y R, YANG J K. Extracellular polymeric substances and sludge solid/liquid separation under Moringa oleifera and chitosan conditioning: A review[J]. Environmental Technology Reviews, 2017, 6(1): 59-73. doi: 10.1080/21622515.2017.1282544 [5] 毛杰, 林珩, 郑柏存, 等. 造纸污泥表面改性的研究[J]. 中国造纸, 2017, 36(1): 31-35. [6] SUN W Q, TANG M D, SUN Y J, et al. Effective sludge dewatering technique using the combination of Fenton’s reagent and CPAM[J]. Canadian Journal of Chemical Engineering, 2018, 96(6): 1256-1263. doi: 10.1002/cjce.v96.6 [7] 邵永, 肖蕾, 吴云霞, 等. 过硫酸钠降解印染有机废水的研究进展[J]. 应用化工, 2017, 46(1): 180-183. [8] 宋秀兰, 石杰, 吴丽雅. 过硫酸盐氧化法对污泥脱水性能的影响[J]. 环境工程学报, 2015, 9(11): 5585-5590. doi: 10.12030/j.cjee.20151172 [9] ZHEN G Y, LU X Q, ZHAO Y C, et al. Enhanced dewaterability of sewage sludge in the presence of Fe(II)-activated persulfate oxidation[J]. Bioresource Technology, 2012, 116: 259-265. doi: 10.1016/j.biortech.2012.01.170 [10] MA W C, ZHAO L, LIU H L, et al. Improvement of sludge dewaterability with modified cinder via affecting EPS[J]. Frontiers of Environmental Science and Engineering, 2017, 11(6): 19-32. doi: 10.1007/s11783-017-0967-x [11] 徐文迪, 常沙, 明铁山, 等. 基于硫酸根自由基(SO4−·)的污泥预处理技术[J]. 环境工程学报, 2018, 12(5): 1528-1535. [12] LI X Y, YANG S F. Influence of loosely bound extracellular polymeric substances (EPS) on the flocculation, sedimentation and dewaterability of activated sludge[J]. Water Research, 2007, 41(5): 1022-1030. doi: 10.1016/j.watres.2006.06.037 [13] 赵璐, 何婷, 丁文欢, 等. 考马斯亮兰法(Bradford法)测定驼乳中蛋白质的含量[J]. 应用化工, 2016, 45(12): 2366-2368. [14] GHOLIKANDI G B, ZAKIZADEH N, MASIHI H. Application of peroxymonosulfate-ozone advanced oxidation process for simultaneous waste-activated sludge stabilization and dewatering purposes: A comparative study[J]. Journal of Environmental Mangement, 2018, 206: 523-531. [15] 孟维, 汪苹, 唐文涛. 反硝化聚磷菌在低碳源城市污水脱氮除磷处理中的应用[J]. 环境科学与技术, 2016, 39(7): 91-95. [16] 吴彦. 稻壳基骨架颗粒制备及调理城市污泥脱水作用和机理分析[D]. 长沙: 湖南大学, 2016. [17] LU M C, LIN C J, LIAO C H, et al. Dewatering of activated sludge by Fenton’s reagent[J]. Advances in Environmental Research, 2003, 7(3): 667-670. doi: 10.1016/S1093-0191(02)00039-4 [18] 张昊. 基于新型骨架构建体与高级氧化剂的污泥复合调理及脱水研究[D]. 武汉: 华中科技大学, 2014. [19] 阚丹, 孙静娴, 张雯, 等. 混价铁氢氧化物对无机磷的吸附/沉淀[J]. 土壤, 2012, 44(3): 520-524. -






 DownLoad:
DownLoad: