7种酚类化学物质对活性污泥的呼吸抑制作用
Respiratory Inhibition Effect of Seven Phenolic Chemicals on Activated Sludge
-
摘要: 苯酚类化学物质是废水中常见的有机污染物,其对活性污泥的毒性数据对于污水处理厂稳定运行和化学品危害性评估具有重要意义。本研究采用活性污泥呼吸抑制试验(209)测定7种酚类化学物质对活性污泥的呼吸抑制作用。结果显示,2,6-二叔丁基苯酚和对特辛基苯酚对活性污泥未产生明显的毒性效应;2,4-二氯酚、2-苯基苯酚、4-硝基酚、4-氯酚和对甲酚等5种化学物质都对活性污泥呼吸有不同程度的抑制效应,3 h-EC50值分别为49.7、77.6、102、150.1和462 mg·L-1,构效关系分析结果表明-Cl、-NO2等官能团是导致活性污泥呼吸抑制效应增强的关键因素。在化学品生物降解性测试研究中,要确保有毒化学物质的测试浓度低于EC50值的1/10。Abstract: Phenolic chemicals are ubiquitous organic contaminants in wastewater. The toxicity data of those compounds on activated sludge is of vital importance to steady operating of sewage treatment plant and performing of chemicals hazard assessment. In this study, respiratory inhibition effect of seven phenolic chemicals on activated sludge was tested by employing the activated sludge respiration inhibition test (TG 209). The experimental results indicated that there is no significant respiratory inhibition effect on activated sludge for 2,6-di-tert-butylphenol and 4-(1,1,3, 3-tetramethy (butyl)-phenol. However, significant respiratory inhibition effect on activated sludge was observed for other five tested phenolic chemicals i.e. 2,4-dichlorophenol, 2-phe-nyl-phenol, 4-nitrophenol, 4-chlorophenol and p-cresol. And their 3 h-EC50 values were 49.7, 77.6, 102, 150.1 and 462 mg·L-1, respectively. The structure-activity relationship analysis results indicated that the functional groups such as -C1, -NO2 are key factors for strong inhibiting of activated sludge respiration. In addition, the results present here also imply that the tested concentration of those toxic compounds should be lower than 1/10 EC50 in their biodegradability test.
-
Key words:
- phenolic chemicals /
- activated sludge /
- respiratory inhibition /
- toxicity
-
湖泊、水库是我国重要的饮用水源,且不少水体都存在不同程度的富营养化问题。当富营养水体发生“水华”时,造成水质恶化[1]。水源水中有害藻华(HABs)因其对水生态系统安全和人类健康产生了负面影响,引起了全世界的关注[2-3]。作为淡水中最普遍的蓝藻之一,铜绿微囊藻(Microcystis aeruginosa)具有生长繁殖的生态优势,在富营养化水体中成为优势藻种影响水质[4]。藻类种群密度在藻华季节的急剧增加严重影响了水处理过程的效率[5]。混凝作为一种常规处理方式,也常用于处理含藻水体工艺中[6]。原水水质是影响混凝效果的最主要因素之一,不同的原水水质,水中污染物含量、成分、pH、碱度等差异将直接影响混凝剂种类的选择和投加量[7-8]。藻华暴发将导致水体pH、碱度等异常升高,水体中的pH甚至可达到9~10,碱度会高于120 mg·L−1。而原水的碱度过高会对混凝过程产生不利影响,尤其是对于铝盐混凝剂,可能会产生出水余铝含量超标的问题[9-10]。
因此,本研究以氯化铝作为混凝剂,以铜绿微囊藻为研究对象,通过投加不同浓度的碳酸氢钠溶液来调节水样的碱度,考察了碱度对混凝去除藻细胞的性能影响,以期为处理富营养化水体和保证饮用水水质提供参考。
1. 实验材料和方法
1.1 实验试剂
氯化铝(AlCl3·6H2O)、碳酸氢钠(NaHCO3)、硝酸钠(NaNO3)、氢氧化钠(NaOH)、盐酸(HCl)均购自国药集团化学试剂有限公司。
1.2 藻种培养
铜绿微囊藻(PCC7820),购自中国科学院水生生物研究所,采用BG11培养基进行培养,无菌条件下接种至锥形瓶中,放在人工气候培养箱中培养,培养条件为温度(25±1) ℃、光照强度2 000 lx、光暗比(L∶D)=12 h∶12 h。定期进行细胞计数,绘制生长曲线,待藻种达到稳定期后用于实验。
1.3 水样配制
为了模拟蓝藻暴发时水体中的藻细胞浓度,控制水样藻细胞密度为1×106个·mL−1[11],并加入5. 0 mmol·L−1NaNO3提供离子强度。由于饮用水中只含有碳酸氢根碱度,故在此实验中只考虑调节碳酸氢根碱度[12-14]。配制0. 5 mol·L−1NaHCO3溶液,在500 mL稀释好的藻液中分别加入0、1.0、2.0、2.5、3.5、4.5 mL溶液,制成总碱度(以CaCO3计)分别为50、95、175、245、330、415 mg·L−1的水样,使用盐酸(0. 1 mol·L−1) 和氢氧化钠(0. 1 mol·L−1)溶液调节水样pH。
1.4 实验方法
使用MY3000-6G智能型混凝搅拌仪(武汉梅宇有限公司)进行混凝实验,在200 r·min−1下快搅60 s,加混凝剂后,在200 r·min−1下快搅90 s,再在40 r·min−1下,慢搅10 min,静置沉淀30 min。在液面以下2.0 cm处取上清液,测定藻的吸光度及浊度。
利用马尔文激光粒度分析仪(Laser Particle Analyzer,Mastersizer2000,Malvern,UK)对混凝实验中絮体的形成过程进行在线监测,以D50代表絮体的平均粒径,并对已经形成的絮体进行破碎实验(5 min,200 r·min−1),随后进行絮体恢复实验(10 min,40 r·min−1),考察絮体的强度因子、恢复因子以及分形维数。
1.5 分析方法
藻细胞密度采用UV-8500紫外/可见分光光度计(上海天美公司)测定;浊度采用浊度仪(2100N,Turbidimeter,HACH,USA)测定;将水样经0.45 μm水相滤头过滤后,采用总有机碳分析仪(Shimadzu,Japan)测定DOC;pH采用pH计(MP220,pH Meter,Mettler-Toledo,Switzerland)测定;出水余铝采用电感耦合等离子-原子发射光谱仪(ICP-OES OPTIMA-2000,PerknELMER,US)测定;于混凝快搅结束后取样,采用Zeta电位仪(zetasizer2000,Malvern,UK)测定Zeta电位;混凝静沉后的底部絮体经高速冷冻离心机(Aantij26XP,Beckman Coulter.Inc.USA)冷冻干燥后采用扫描电子显微镜(HITACHI SU8020 FE-SEM,Japan)测定。
2. 结果与讨论
2.1 混凝剂投加量对混凝性能的影响
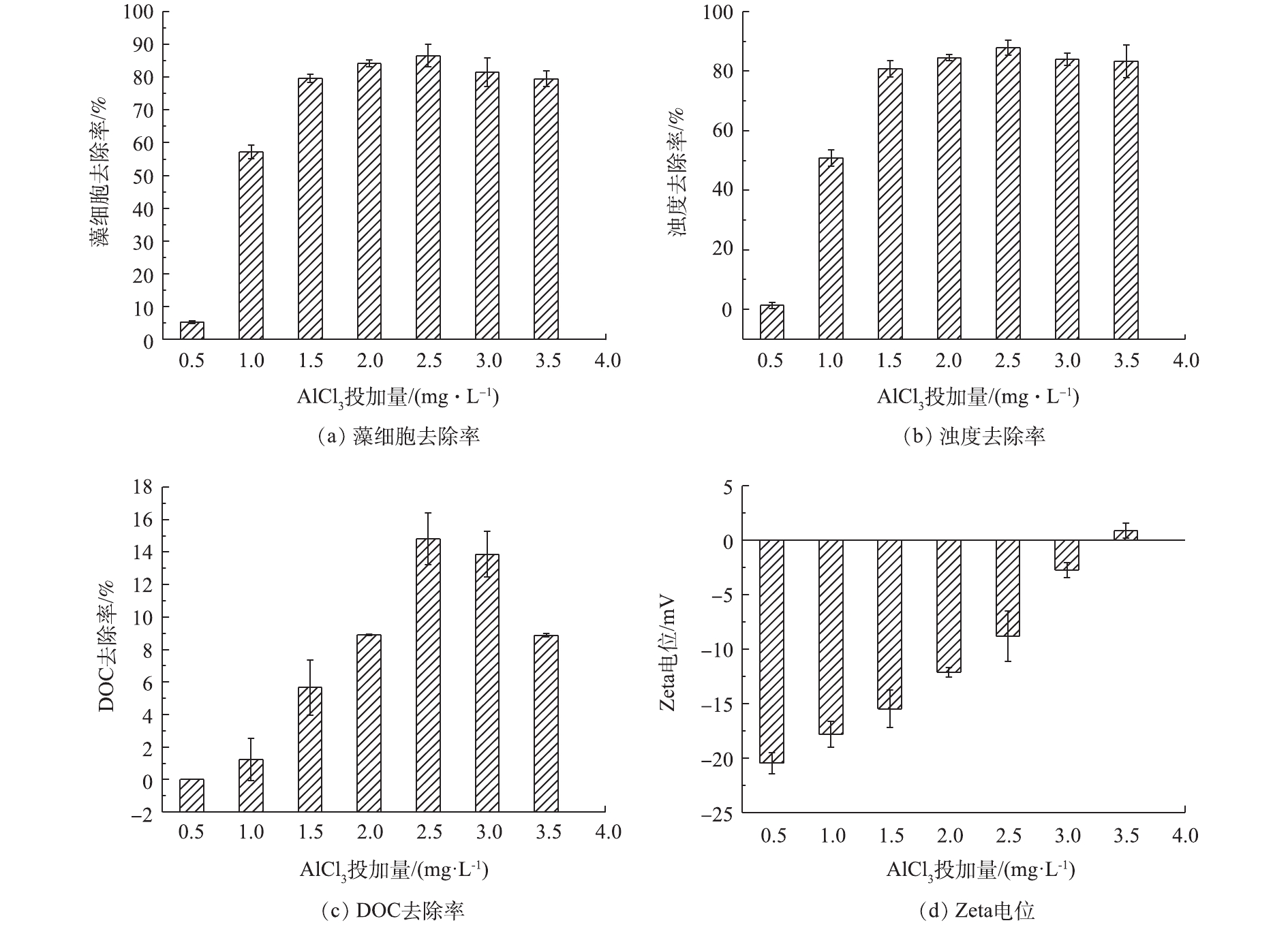
为探究混凝剂投加量对混凝效果的影响,考察了AlCl3(以Al计)投加量为0.5~3.5 mg·L−1、水样pH=7.5条件下藻细胞、浊度和DOC的去除率,结果见图1。由图1可见:当混凝剂投加量为0.5~2.0 mg·L−1时,藻细胞、浊度和DOC的去除率随着混凝剂投加量的增加而增加;当AlCl3投加量为2.5 mg·L−1时,藻细胞、浊度和DOC的去除率分别达到了86.52%、87.95%和14.80%;当投加量增大至3.5 mg·L−1时,藻细胞、浊度和DOC的去除率均有所降低。这主要是因为:当混凝剂投加量为0.5~2.0 mg·L−1时,投加量不足,导致电中和能力受到抑制,因此,藻细胞、浊度和DOC的去除率均不高;当混凝剂投加量过大时,体系中的胶体颗粒由于带有过高的正电荷而出现复稳现象,部分颗粒物难以聚集形成絮体而被去除,导致混凝效果下降。
2.2 不同碱度对混凝性能的影响
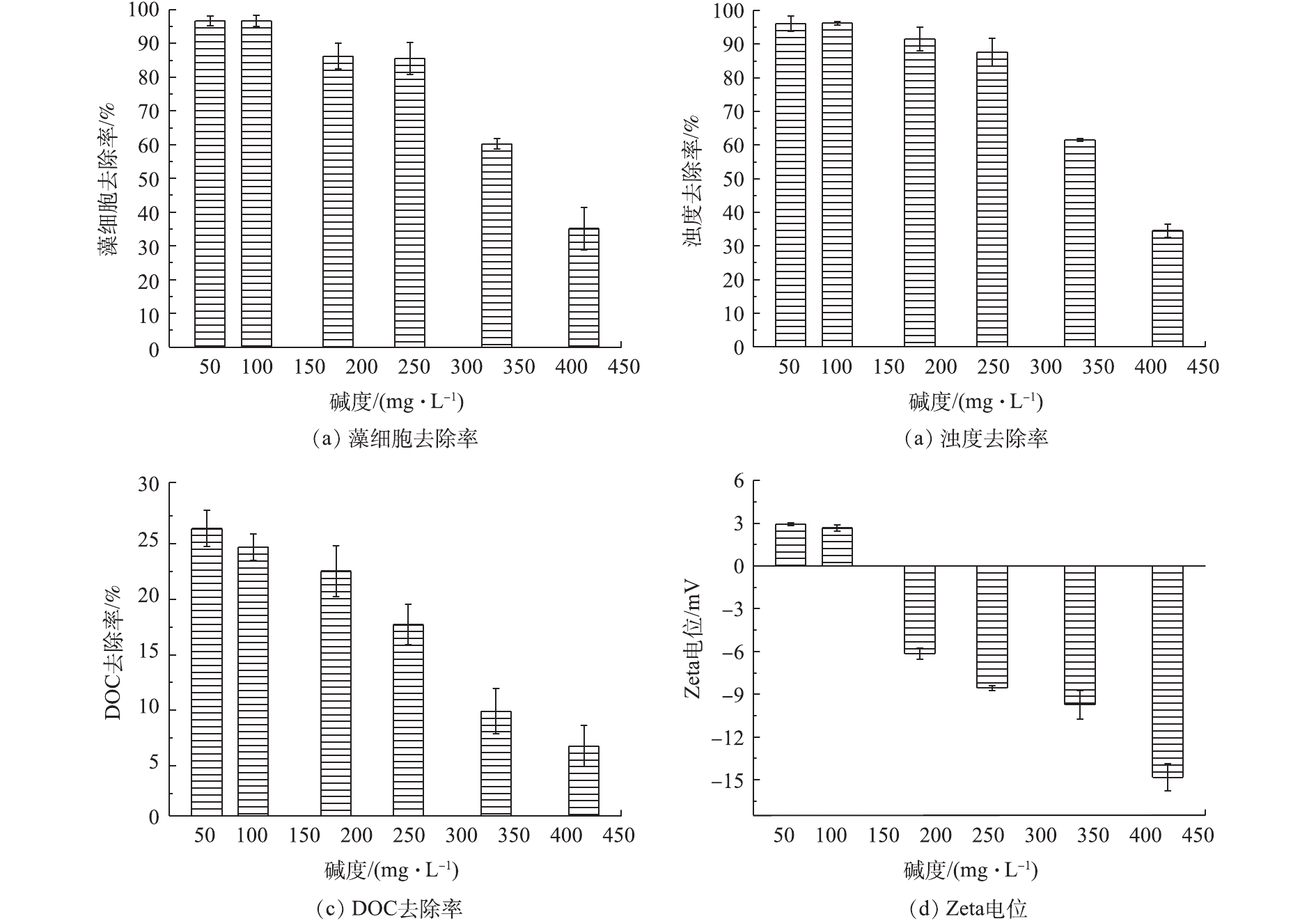
为探究碱度对混凝性能的影响,考察了各碱度含藻水样在AlCl3投加量为2.5 mg·L−1、pH=7.5条件下的藻细胞、浊度和DOC的去除率,结果见图2。由图2可知,随着碱度的增加,藻细胞、浊度、DOC的去除率以及Zeta电位值均呈下降趋势。藻细胞的去除率由96.65%降低至35.12%,浊度的去除率由96.12%降低至34.55%,有机物的去除率由24.61%降低至15.26%。同时也可以看到,随着碱度的增加,Zeta电位由2.67 mV降低至-14.83 mV。分析其原因在于,当水样pH=7.5、碱度为50~245 mg·L−1时,水样中主要存在Al(OH)3活性溶胶和一些具有较高聚合度的带正电水解产物,其可通过黏附架桥、网捕卷扫等作用达到较好的混凝效果[15],导致藻细胞、浊度和DOC的去除率较高。随着碱度的增加,负离子形态的
Al(OH)−4 占据优势,与带负电荷的铜绿微囊藻细胞之间产生了静电排斥,导致混凝效率下降[16],Zeta电位值也逐渐减小。2.3 pH对不同碱度含藻水混凝性能的影响
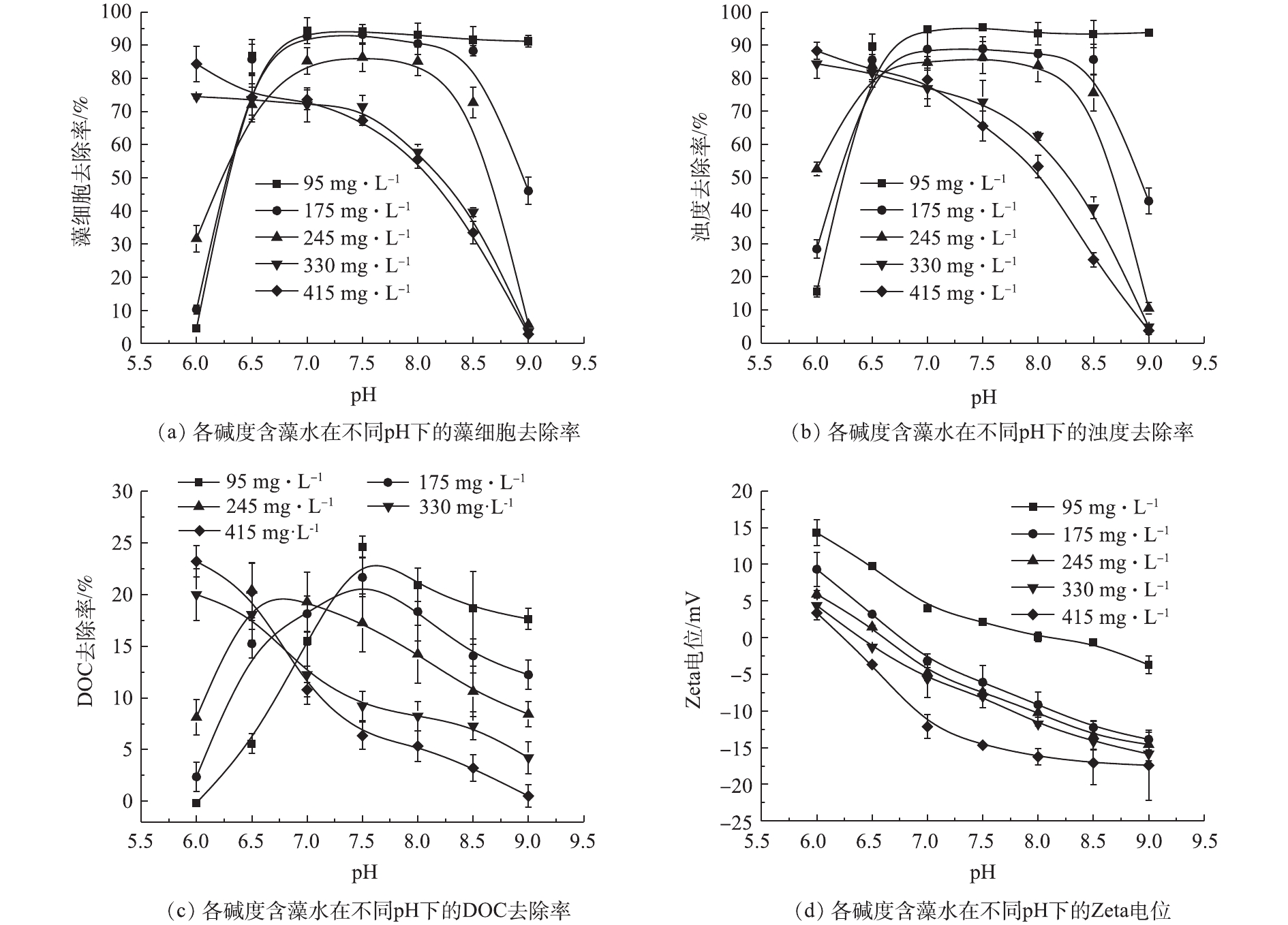
碱度和pH共同决定铝盐投加后的水解形态,进而影响混凝性能[17]。因此,可通过调整pH缓解碱度对混凝性能的影响,结果如图3所示。由图3可知:当碱度为95 mg·L−1和175 mg·L−1、pH=6.0时,藻细胞的去除率分别为4.59%和10.27%,在相同碱度条件下,当pH=6.5~8.5时,藻细胞的去除率在88.30%以上;当碱度为245 mg·L−1、pH=7.0~8.0时,藻细胞的去除率达到86.31%,当pH=6.0、9.0时,藻细胞的去除率均在31.64%以下;在碱度为330 mg·L−1和415 mg·L−1时,随着pH的增大,藻细胞的去除率呈下降的趋势,分别由74.45%和84.32%降低至3.56%和2.81%。浊度的去除率和藻细胞的去除效果一致。DOC的去除率虽然不高,在25%以下,但与藻细胞和浊度的去除率趋势一致。
分析原因在于,当水样的pH=6.0时,随着碱度的增加,Zeta电位绝对值逐渐减小,趋于等电点状态,体系的稳定性逐渐减弱,电荷排斥力逐渐下降,有助于絮体形成,有利于混凝过程进行,因此,导致藻细胞、浊度以及有机物的去除率增加。当水样的pH=6.5、碱度为95、175、245 mg·L−1时,混凝过程主要依靠吸附架桥和网捕卷扫协同作用,形成较大絮体,絮体沉降性好,去除率增加。当水样的pH=7~9、碱度为95 mg·L−1时,Zeta电位值趋近于0,体系趋于失稳状态,颗粒间的排斥力降低,藻细胞和浊度的去除率趋于稳定。而在其他各碱度下,随着pH的增大,铝盐混凝剂发生过度水解反应,生成的
Al(OH)−4 负离子增多,网捕卷扫作用减弱,且系统脱稳困难,不利于混凝过程的进行[18-20],所以藻细胞、浊度和DOC的去除率逐渐下降。在各碱度下,体系Zeta电位值均随pH的增大而降低,这是因为藻细胞本身的Zeta电位值会随着pH的增大而降低;水样pH对铝盐的水解形态分布也会影响体系的Zeta电位值;在相同pH下,碱度越高,带正电荷的铝盐水解产物越少,从而也会降低体系的Zeta电位值。综上所述,通过调节水样的pH,可以达到减缓碱度影响混凝过程的目的。当体系碱度较低时,可将pH调整至中性范围,以提高藻细胞的去除率;当体系碱度过高时,可以调节水样pH,从而使体系Zeta电位的绝对值趋近于0,打破体系稳定状态,进而有利于混凝过程的进行。
2.4 絮体特性
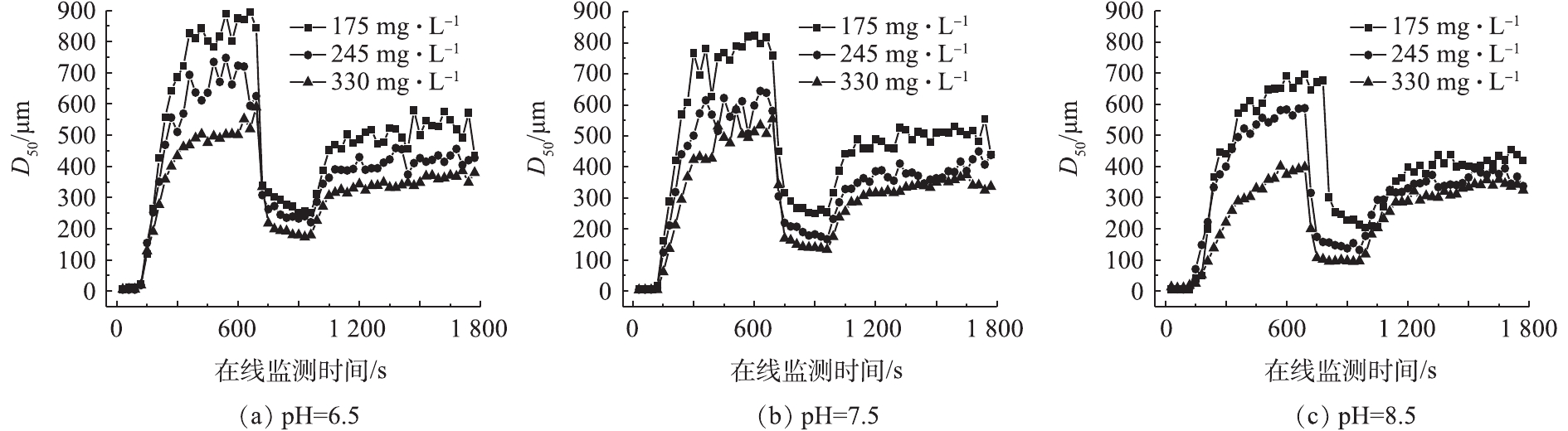
由于絮体的大小和强度对于分离过程有重要影响,因此,在大多数水处理过程中,絮体特性被当作是一个重要的操作参数[21],混凝过程絮体粒径变化情况如图4所示。
由图4可以看出,在相同pH条件下,随着碱度的增加,平衡时的絮体粒径逐渐减小。当pH=7.5、碱度为175、245和330 mg·L−1时,平衡时絮体粒径分别为811.02、633.28和540.62 μm。分析原因在于,在水样pH一定的条件下,碱度较低时,混凝过程依靠吸附架桥和网捕卷扫协同作用,形成粒径较大的絮体。随着碱度的增加,铝盐的水解产物Al(OH)3胶体更多转变为
Al(OH)−4 ,絮体间排斥能力增强,不利于颗粒聚集生成,故导致平衡时的絮体粒径减小。为了更好地了解不同条件下混凝形成絮体的特性,对强度因子(Sf)和恢复因子(Rf) (表1)以及分形维数(Df)[22](表2)进行了计算。
表 1 各碱度含藻水样在不同pH条件下形成絮体的强度因子和恢复因子Table 1. Strength factors and recovery factors of flocs formed in algae-laden water sample with different alkalinity at different pHspH 碱度为175 mg·L−1 碱度为245 mg·L−1 碱度为330 mg·L−1 强度因子/% 恢复因子/% 强度因子/% 恢复因子/% 强度因子/% 恢复因子/% 6.5 37.41 30.12 32.98 38.97 25.95 39.20 7.5 35.97 35.31 32.29 44.42 24.79 47.88 8.5 34.19 47.68 27.39 45.86 21.17 73.99 表 2 各碱度含藻水样在不同pH条件下形成絮体的分形维数Table 2. Fractal dimension of flocs formed in algae-laden water sample with different alkalinity at different pHspH 碱度为175 mg·L−1 碱度为245 mg·L−1 碱度为330 mg·L−1 平衡时 破碎后 再生长后 平衡时 破碎后 再生长后 平衡时 破碎后 再生长后 6.5 1.744 1.916 1.908 1.591 1.756 1.734 1.584 1.748 1.704 7.5 1.586 1.733 1.718 1.516 1.694 1.63 1.372 1.554 1.503 8.5 1.550 1.704 1.677 1.432 1.615 1.551 1.25 1.434 1.395 由表1可知,在相同pH条件下,随着碱度的增加,絮体的强度因子逐渐减小,恢复因子逐渐增大。当水样pH=7.5时,随着碱度的增加,絮体强度因子由35.97%降低至24.79%,恢复因子由35.31%增加至47.88%。强度因子逐渐减小的原因为:在相同pH条件下,碱度较低时,网捕卷扫在混凝机理上占主导地位,体系中有足够的Al(OH)3胶状沉淀,会促使形成比较密实的絮状结构[23],相应的强度因子就大;随着碱度的升高,铝盐水解生成的无定型Al(OH)3胶状沉淀逐渐转变为
Al(OH)−4 ,Al(OH)3胶状沉淀减少,导致网捕卷扫作用减弱,形成的絮体变得疏松,相应的强度因子就减小。恢复因子逐渐增大的原因在于,当网捕卷扫在混凝机理上占主导地位,破碎的絮体颗粒带正电荷[24],这些破碎的絮体颗粒可以继续吸附水样中的残余颗粒物。在水样pH一定的条件下,碱度较低时,藻细胞和有机物的去除率高,水样中残余颗粒物就少,在一定时间内与破碎的颗粒物碰撞概率小,因此,絮体恢复因子小;而碱度较高时,平衡时絮体粒径小,而且由于藻细胞去除率低,水样中还有大量的颗粒物,这就增大了与破碎絮体的碰撞概率,一定时间内破碎絮体吸附中和这些颗粒物使粒径再次增大,因此恢复因子也增大。由表2可以看出:在相同pH条件下,随着碱度的增加,平衡时絮体的分形维数逐渐减小;同一碱度下,随着pH的增加,平衡时絮体的分形维数也逐渐减小。当水样pH=7.5时,随着碱度的增加,平衡时絮体的分形维数由1.586减小到1.372;当碱度为245 mg·L−1时,随着pH的增加,平衡时絮体的分形维数由1.591降低至1.432。分析原因在于:当pH和碱度较低时,网捕卷扫占主导地位,形成的絮体结构更为致密,相应的分形维数就较高[25];随着碱度的增加,铝盐水解生成的Al(OH)3胶状沉淀逐渐转变为
Al(OH)−4 ,网捕卷扫作用减弱,胶体颗粒间的静电斥力增加,因此,形成的絮体结构变得疏松,相应的分形维数较低[26]。2.5 扫描电镜分析
由图5可知,水样pH和碱度的不同导致混凝过程的作用机理不同,而不同混凝机理形成的絮体结构是有差异的。当水样pH和碱度较低时,形成的絮体更为致密,而当水样pH和碱度较高时,形成的絮体相对疏松。这主要是因为,在水样pH和碱度不同的情况下,形成的絮体粒径和分形维数不同。水样pH和碱度较低时,混凝过程依靠吸附架桥和网捕卷扫协同作用,形成絮体的分形维数大,絮体结构更为密实,絮体沉降性好,所以混凝效果较好;随着水样pH和碱度的增加,
Al(OH)−4 逐渐增多,致使网捕卷扫作用减弱,絮体间排斥能力增强,因此,分形维数逐渐减小,絮体结构越来越疏松,形成的絮体表面粗糙且多孔,而且絮体粒径小,沉降性差,导致混凝效果减弱。2.6 出水余铝
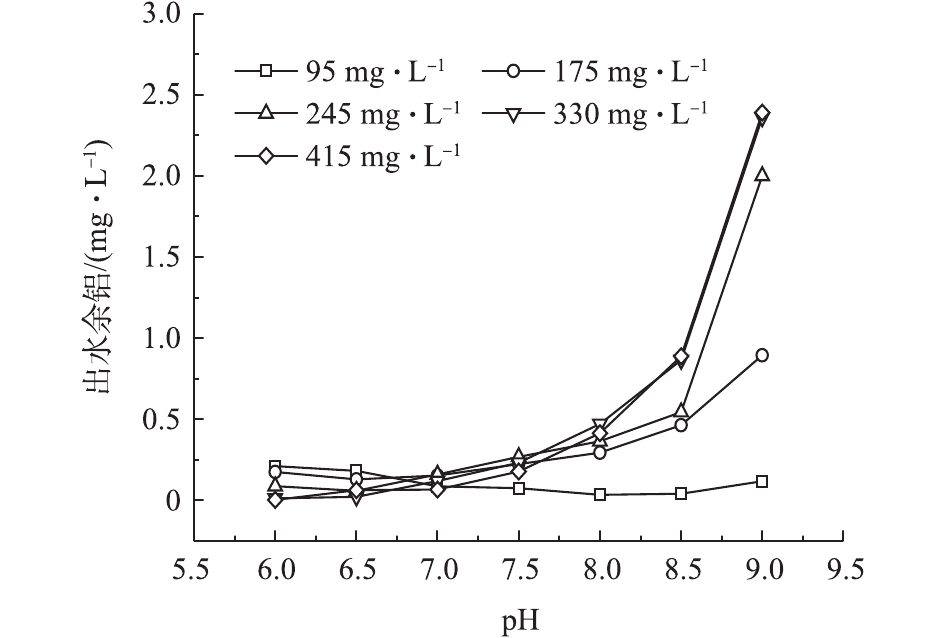
水样的碱度过高会导致使用铝盐混凝剂的残留铝含量增加,因此,实验对比了各碱度含藻水在不同pH条件下的出水余铝,结果如图6所示。可以看出:当碱度为95 mg·L−1、pH为6.0~8.0时,出水余铝从0.212 0 mg·L−1降低至0.035 3 mg·L−1。这是因为混凝效果逐渐增强,沉后出水中的溶解态铝含量降低,所以出水余铝减少。在其他碱度下,随着pH的增大,出水余铝均有所增加,且在相同pH下,随着碱度的增加,出水余铝也呈升高的趋势,当pH=9.0时,碱度为245、330和415 mg·L−1对应的出水余铝分别为2.030、2.360和2.390 mg·L−1。这是因为随着pH和碱度的升高,铝离子水解形成的 Al(OH)3胶状沉淀会溶解为负离子
Al(OH)−4 ,导致出水余铝含量升高。2.7 反应体系出水pH
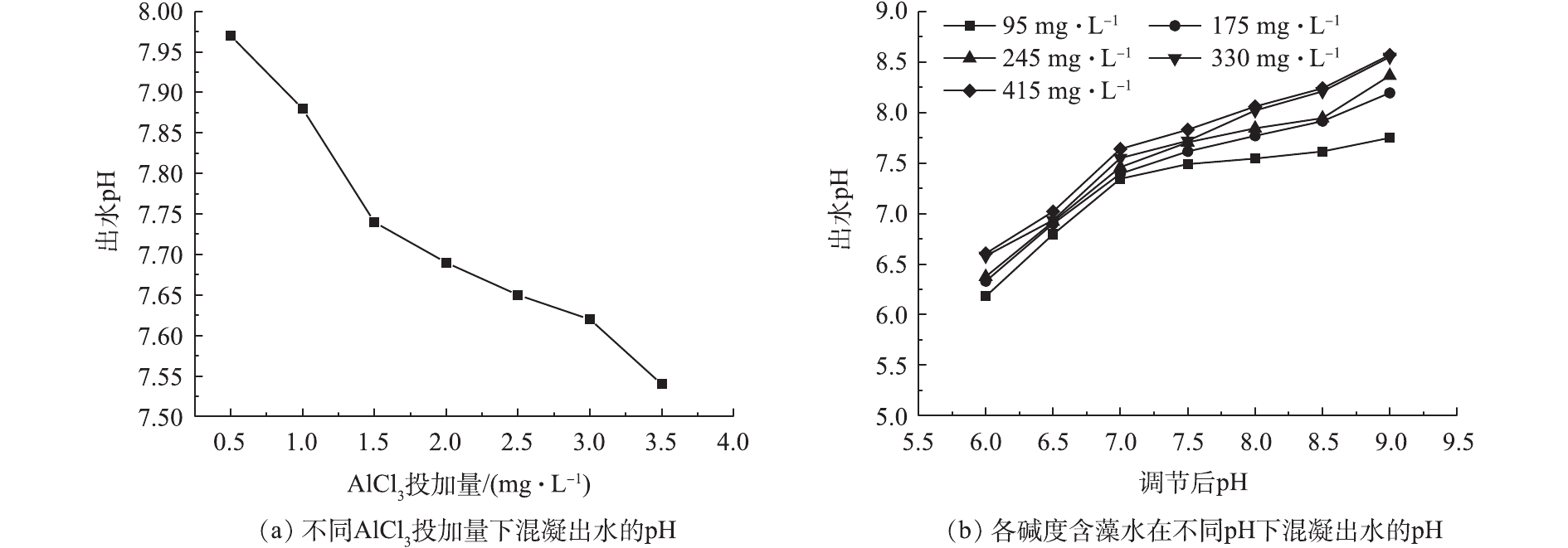
本研究对不同AlCl3投加量和各碱度含藻水在不同pH条件下混凝出水的pH进行测定,结果如图7所示。如图7(a)所示,当pH=7.5、碱度为245 mg·L−1时,随混凝剂投加量增大,出水pH由7.97降低至7.54。这是因为铝盐水解过程中会产生H+,H+的积聚会使体系的pH有所降低,虽然
HCO−3 能吸收H+,使体系pH波动减小,但是因为体系中HCO−3 的量是有限的,因此,无法中和过多的H+,所以随着混凝剂投加量的增加,体系出水pH有所降低。如图7(b)所示,在调节后的pH相同条件下,出水pH随着碱度的增大而增大,这是因为在体系中投加的铝离子的量是有限的,铝盐水解产生的H+也就有限,而HCO−3 浓度是增加的,其水解产生的OH−逐渐增多,但是没有足够的H+来中和,因此,反应后的出水pH随着碱度的增大而升高。3. 结论
1)当水样pH=7.5、氯化铝投加量为2.5 mg·L−1、碱度为50、95 mg·L−1时,对于藻细胞和浊度的去除率均在96.50%左右,随着碱度的升高,对于藻细胞,浊度以及有机物的去除率均呈下降趋势,并且水样的Zeta电位值也逐渐降低。
2)通过调整水样pH,可有效缓解碱度对混凝过程的影响。当体系碱度较低时,可将pH调整至中性范围,提高藻细胞的去除效率,出水余铝含量也会降低;当体系碱度过高时,可通过调节pH使体系Zeta电位的绝对值趋近于0,打破体系稳定状态,从而有利于混凝过程的进行,出水残留铝含量也会有相应减少。
3)当水样pH≥6.5,碱度较低时,混凝过程依靠吸附架桥和网捕卷扫协同作用,形成的絮体粒径较大,而且絮体的结构较为致密,分形维数较大;随着pH和碱度的增加,絮体间排斥能力增强,不利于颗粒物的聚集生成,导致形成的絮体粒径较小,而且絮体结构比较疏松,分形维数逐渐减小。
-

 点击查看大图
点击查看大图
计量
- 文章访问数: 873
- HTML全文浏览数: 873
- PDF下载数: 26
- 施引文献: 0



 下载:
下载: