Fe3O4/SDS磁性纳米颗粒吸附水体中的Cd2+和Zn2+
SDS coated Fe3O4 magnetic nanoparticles for adsorption of Cd2+ and Zn2+ in aqueous solution
-
摘要: 一种新型纳米固相萃取吸附剂,由阴离子表面活性剂十二烷基磺酸钠(SDS)包裹在Fe3O4磁性纳米颗粒表面形成,用于吸附水溶液中的重金属离子。研究了吸附过程的主要影响因素(如SDS浓度、溶液pH等)以及解吸过程的最佳条件,并对其机理进行了初步的探讨。研究结果表明,共沉淀法制备的Fe3O4颗粒粒径分布均匀,平均粒径约为54 nm; SDS浓度为300 mg/L时, Fe3O4/SDS磁性纳米颗粒吸附Cd2+和Zn2+的能力最强;在一定浓度范围内, Fe3O4/SDS体系对Cd2+和Zn2+的吸附平衡数据符合Langmuir吸附等温方程,饱和吸附量分别为22.42 mg/g和13.95 mg/g。最终结果表明, Fe3O4/SDS磁性纳米颗粒具有较强磁分离能力和较好的吸附效果。Abstract: A novel nanosize solidphase adsorbent, i.e. Fe3O4 magnetic nanoparticles coated by SDS, could be used to remove heavy metal from aqueous solution. The main factors affecting the adsorption process, such as SDS concentration and the solution pH, and the optimal condition for desorption, were investigated. The mean diameter of Fe3O4 nanoparticles prepared by co-precipitating method was about 54 nm. The adsorbent had the highest adsorption capacity when the concentration of SDS was 300 mg/L. The adsorption of Cd2+ and Zn2+ agreed well to Langmuir adsorption model with the maximum adsorption capacities of 22.42 mg/g and 13.95 mg/g, respectively. It had strong magnetic separability and great adsorption capacity.
-
Key words:
- Fe3O4 /
- surfactant /
- SDS /
- adsorption /
- Cd2+ /
- Zn2+
-
磷是所有生物生存所必需的营养元素,也是现代工农业生产中不可缺少的资源[1]。作为一种珍贵的不可再生资源,全球磷资源的日益短缺和枯竭令人担忧。据估计,2040年后,全球磷需求量将超过全球磷供应量[2],农业磷需求将在2050年达到峰值[3]。以目前的磷矿储量和消耗速度计算,世界磷矿资源将在100~200年内消耗殆尽[4],届时将发生无磷可用的“磷危机”现象[5]。我国磷资源短缺问题同样严重,截至2020年我国的磷矿储量不到世界储量的5%,每年的磷矿消耗量却达世界水平的40%~50%,因此磷资源回收成为我国可持续发展的战略性需求[2]。污水处理厂剩余污泥中富集了大量的磷[6],这使得污泥成为潜力巨大的“二次磷资源”。从剩余污泥中回收磷既可以解决磷资源紧缺与水体富营养化问题,又可以实现废物的资源化利用。然而金属、致病菌等有毒害污染物质的存在,使富磷污泥不能直接作为磷肥使用。目前,污泥中的磷先释放再回收成为磷回收的主要手段,其中磷的有效释放是磷回收的关键。
污泥水热碳化技术是指高含水率污泥在一定温度、反应时间和自产生压力下,经过水解、脱水、脱羧和缩聚等一系列复杂反应,最终产生富碳固体—水热炭,以及液体产品—水热液[7]。污泥水热碳化反应对磷的迁移及形态转化影响较大。随着水热温度的升高污泥胞外聚合物及细胞结构破坏,胞内聚磷酸盐、磷脂等被释放至水热液中,并进一步分解为无机磷(P2O74−和PO43−)[8],而暴露在液相中的P2O74−和PO43−会与污泥中溶出的钙、镁、铝、铁等金属离子结合生成相应的金属磷酸盐,经沉淀或吸附于固体物质表面形成吸附态磷,并经溶解和重组/重结晶形成更加稳定的磷化物,从而使磷不断富集在固相水热炭中[9]。为从污泥水热炭中回收磷,研究人员开展了大量研究。如PÉREZ等[10]采用有机酸浸取污泥水热炭中的磷,发现有机酸可以将磷的浸取率提高至75%以上,其中草酸在5 min时几乎可以将水热炭中全部的磷释放至液相。SHETTIGONDAHALLI等[11]研究了在污泥水热碳化过程中和水热碳化后加酸(H2SO4)对磷浸出的影响,结果表明在水热碳化之后加入硫酸具有更高的磷浸出效果。XUE等[7]研究了HCl对城市污泥水热碳化过程中磷转移和转化的影响,结果发现在水热碳化过程中加入0.5%~2.5%HCl,可使富集在水热炭中的磷含量由污泥总磷含量的99.5%降低至91.8%,非磷灰石无机磷由34%增长到94%,这是由于盐酸提供了低pH环境,促进了钙相关磷沉淀物溶解并释放磷至液相所至。
乙二胺四乙酸(EDTA)是一种金属络合剂,在污泥水热碳化过程中可与释放的金属离子络合形成可溶性金属络合物,从而可避免金属离子与磷酸根形成沉淀沉积在固相中,便于磷释放至液相。例如,MA等[12]采用EDTA与高压脉冲放电相结合的方法预处理污泥,在破坏污泥结构的同时防止金属磷酸盐沉淀的形成,显著提高了污泥厌氧发酵过程中磷的释放。ZOU等[13]的研究表明,在厌氧消化过程中添加EDTA可以损伤细胞膜并与金属离子络合,有效提高了磷的释放效率(达82%),并且对Fe-P中磷的释放效果优于对Al-P中磷的释放效果。陈树俊[14]、史可等[15]在污泥低温热水解过程中添加EDTA,磷的释放率分别达到65%和77.9%,远高于原污泥中磷的释放效果(分别为5%和39.7%)。此外,EDTA对EPS具有一定的溶解破坏作用,能改变微生物的细胞结构,促进胞外物质与污泥细胞的分离。刘博文等[16]采用热碱-EDTA耦合法强化破解污泥,破解后SCOD、TN、TP、多糖和蛋白质溶出量均升高,污泥残渣中VS含量小于热碱破解法。肖倩等[17]利用EDTA对消化污泥胞外紧密型EPS(TB-EPS)进行提取,发现EDTA对TB-EPS具有一定的溶解破坏作用,并造成细胞膜损伤。因此,采用EDTA与污泥水热碳化相结合对污泥溶胞释磷以及避免磷与金属离子形成沉淀,促进磷从固相向液相转移将具有非常积极的作用,但目前这方面的研究有限。
本研究采用EDTA强化污泥水热碳化释磷,研究不同条件下磷的释放特性,并通过SMT法提取水热炭中不同形态的磷,分析磷的形态分布规律,探讨磷的迁移转化行为和内在机制,这对从污泥水热碳化过程中回收磷资源具有重要意义。
1. 材料与方法
1.1 试验原料
试验所用污泥取自天津市某污水厂二沉池的剩余污泥,取回后剔除杂质经2 h自由沉淀后去除上层清液,冷藏于4 ℃冰箱待用。污泥性质如表1所示。
表 1 污泥的基本性质Table 1. Basic properties of sludgepH SS/(mg·L−1) VSS 含水率 SCOD/(mg·L−1) TP/(mg·g−1) 6.24±0.91 12 000±2 000 72.50%±2.60% 95.20%±3.60% 102.00±78.00 19.97±5.87 1.2 试验方法
将污泥样品搅拌均匀,取70 mL转移到反应釜中,投加EDTA 0~35 mmol·L−1,设置反应温度150~250 ℃,反应0~6 h。反应结束后自然冷却至室温,采用0.45 μm滤膜对样品进行抽滤,分别得到固相和液相产品,将固相产品放入电热恒温干燥箱中105 ℃干燥至恒重,经充分研磨后,得水热炭;液相进行相关指标测定。
1.3 分析方法
采用Flash EA
1112 型全自动元素分析仪(美国)测定污泥和水热炭中C、H、N、S元素,O元素含量采用差减法计算;根据《煤的工业分析》(GB/T212—2008)测定污泥的灰分,根据Dulong公式计算水热炭的高位热值;采用Optima8300 电感耦合等离子体光谱仪(美国)测定金属(Fe、Al、Mg、Ca)浓度。利用SMT法提取污泥及水热炭中五种形态的磷,分别为总磷(TP)、有机磷(OP)、无机磷(IP)、磷灰石无机磷(AP,通常为与Ca和Mg结合的各种磷)和非磷灰石无机磷(NAIP,通常为与Fe、Mn和Al氧化物及其氢氧化物结合的磷)[18-19]。磷含量采用钼锑抗分光光度法测定。
2. 结果与讨论
2.1 温度对EDTA强化污泥水热碳化释磷的影响
在EDTA投加量为5 mmol·L−1、水热碳化时间为30 min时,研究了不同反应温度对污泥释磷的影响,如图1所示。由图1(a)可知,液相中TP和PO43−的浓度随温度的升高而增加,210 ℃后趋于平缓。这是由于温度是有机大分子降解和高活性化学键断裂和重组的主要能量来源,在150~190 ℃时主要发生水解和脱水反应,此阶段主要以有机物的释放为主;210~250 ℃脱羧、缩聚和芳香化等反应加剧[20]。高温高压环境破坏污泥絮体结构,水解有机物,使得细胞内及胞外聚合物中的磷大量释放至液相,由于同时释放的金属离子与EDTA络合,使得磷以离子态形式大量存在于液相中。但在较低温度时,由于不能提供足够的能量,使得150~190 ℃时磷的释放速率小于210 ℃;在210 ℃时,高温促进了反应的剧烈进行,提高了磷的释放效率并基本达到最大值,此时水热液中TP和PO43−为178.8和154.3 mg·L−1,磷的浸出率为64.4%(图1(b))。随着反应温度的继续升高,磷从固相转移到液相的释放量不再发生明显变化。由于温度过高会增加能耗,加大成本,因此本研究选择210 ℃作为最佳水热碳化温度。
2.2 时间对EDTA强化污泥水热碳化释磷的影响
在水热碳化温度为210 ℃,EDTA投加量为5 mmol·L−1的条件下,探究了不同水热时间对TP和PO43−的影响,见图2。图2(a)显示,液相中磷的浓度随反应时间的增加呈先增加后少量降低的趋势。这是由于反应过程中发生的污泥破解释放磷和金属,以及释放的金属离子与EDTA发生络合反应置换磷等过程均需要一定的反应时间。因此,随着反应时间的增加,磷浓度呈线性增长,并在4 h时达到峰值,此时液相中TP和PO43−的浓度分别达到300.6和295.59 mg·L−1,对应磷的浸出率可达79.9%(图2(b))。此时大部分污泥细胞已经破裂,胞内物质被释放出来,同时液相中EDTA与溶出的金属离子络合,阻止了金属离子与磷再结合形成金属磷酸盐沉淀又向固相中沉积的过程。随着反应时间的延长,释放的金属离子增多,而EDTA有限,导致多余的金属与液相中的磷结合,从而使得部分磷重新形成金属磷酸盐沉淀或结晶[21],液相中磷释放量少量下降。可见在一定范围内延长反应时间对磷的释放具有促进作用,但过长时间不利于磷释放,因此本研究选择4 h作为磷释放的最佳反应时间。
2.3 EDTA投加量对污泥水热碳化释磷的影响
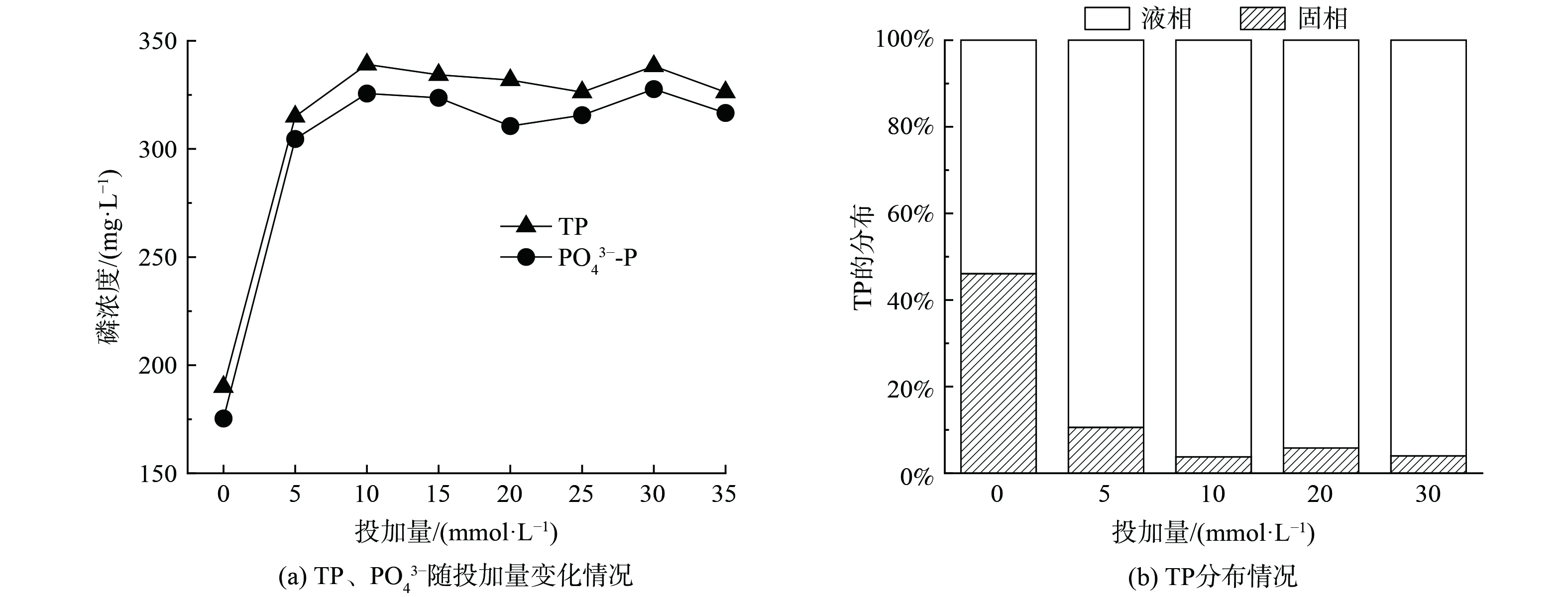
在温度210 ℃,时间4 h条件下,考察不同EDTA投加量对污泥中TP和PO43−释放的影响,情况如图3所示。由图3(a)可知,磷的浓度随EDTA投加量的增加而升高,在投加量为10 mmol·L−1时,TP和PO43−的浓度达到最大值,分别为339.1和325.6 mg·L−1,约是未投加EDTA时的2倍,此时磷的释放率达到96.2%(图3(b));此后继续增加EDTA用量,液相中的磷浓度基本趋于稳定,但仍有约4%的磷存在于固相中,并以AP的形式存在。这可能是由于过量EDTA使溶液呈酸性,导致小部分与钙、镁结合的磷无法释放出来。
图3结果说明EDTA可以有效促进磷从固相向液相大量转移,显著高污泥释磷效果。这是由于:一方面EDTA螯合大量金属离子,防止磷与金属离子沉淀;另一方面,EDTA可以分解EPS并溶解细胞膜,使细胞部分暴露在污泥中并释放胞内有机物,增强污泥中磷的释放[12]。因此,在污泥水热碳化阶段加入EDTA不仅可以掩蔽金属离子对磷释放的影响,还可以溶解EPS,增强释磷效果。
2.4 污泥浓度对EDTA强化污泥水热碳化释磷的影响
在温度为210 ℃,时间为4 h,EDTA投加量为10 mmol·L−1的条件下,考察了不同污泥浓度(3.7~33.6 g·L−1)对TP和PO43−释放的影响,结果见图4。由图4(a)可知,随着污泥浓度的降低,TP和PO43−的浓度减少,其中由33.6 mg·L−1降低到8.4 mg·L−1时,TP和PO43−的下降速率较快,8.4 mg·L−1降低到3.7 mg·L−1时,TP和PO43−的下降速率变缓。这主要是由于污泥浓度降低导致反应物中磷的总含量降低,从而使得污泥浓度减少时上清液中磷的释放量降低。而从图4(b)可以看出,污泥浓度对TP在固相和液相之间的转移影响不大,不同污泥浓度的反应液在试验条件下磷的释放率均在92%~95%范围,这是由于在EDTA辅助污泥水热碳化的作用下可以将污泥中大部分的磷释放出来。
2.5 EDTA对固相中磷形态的影响
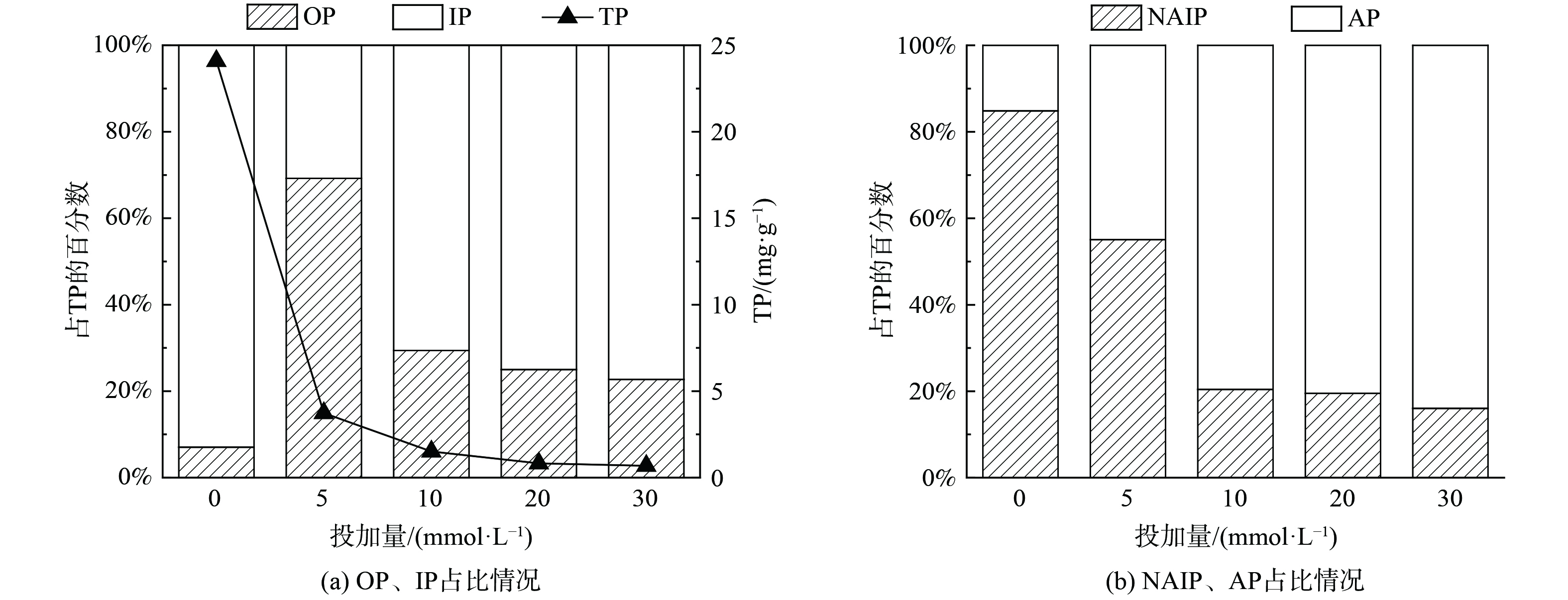
图5显示了不同EDTA投加量下水热炭中磷的形态分布。由图5(a)可知,水热炭中TP的质量分数随投加量的增加而降低,这与前文结论一致(图3)。该结果说明在水热碳化过程中投加EDTA促进了固相中的磷向液相转移。水热炭中的磷可分为有机磷(OP)和无机磷(IP),其中OP主要包括正磷酸单酯、磷酸二酯等,而IP主要包括正磷酸盐和焦磷酸盐等[22-23]。
图5(a)显示,当直接将污泥水热碳化后(EDTA=0 mmol·L−1),水热炭中IP占比较高,约为92.8%,OP占比较少为7.2%。这是由于原泥中含有大量金属成分,如Ca、Mg、Al、Fe等,其与磷结合形成无机金属磷酸盐等形态存在于污泥中,同时污泥中含有细胞物质,部分磷以卵磷脂、磷壁酸、聚磷酸等有机磷形式存在,且经水热碳化后,从细胞中释放的金属离子会与从有机磷中释放的磷结合形成金属磷酸盐,使得固相中大部分磷以IP形态存在。当EDTA投加量为5 mmol·L−1时,水热炭中的OP占比升高,IP降低,这是由于EDTA能与溶胞释放的金属结合,部分金属被EDTA络合进入液相,同时释放的磷也进入液相,从而导致水热炭中IP的占比降低。随着EDTA浓度的升高,水热炭中的IP升高,OP降低,这是由于水热碳化使污泥中的有机聚磷酸盐在高温下降解,导致短链聚磷酸盐的数量增加,并为金属络合提供了额外的P-O键,从而使IP占比增多;同时,OP和焦磷酸盐水解,转化为正磷酸盐[24],而水解形成的正磷酸盐与金属结合形成的含磷沉淀物在EDTA的作用下向液相中释放出磷,从而导致OP占比降低。由图5(b)可知,水热炭中AP占TP的比例不断升高,NAIP相反。说明EDTA促进了NAIP向AP转化。这可能是由于EDTA与金属离子形成稳定络合物的酸度范围不同,与Ca2+和Mg2+在碱性范围络合,而污泥经EDTA强化水热碳化处理后,溶液pH呈酸性,EDTA与Ca2+和Mg2+络合减少,导致AP在TP中的占比升高。
2.6 EDTA对水热碳化过程中金属浸出的影响
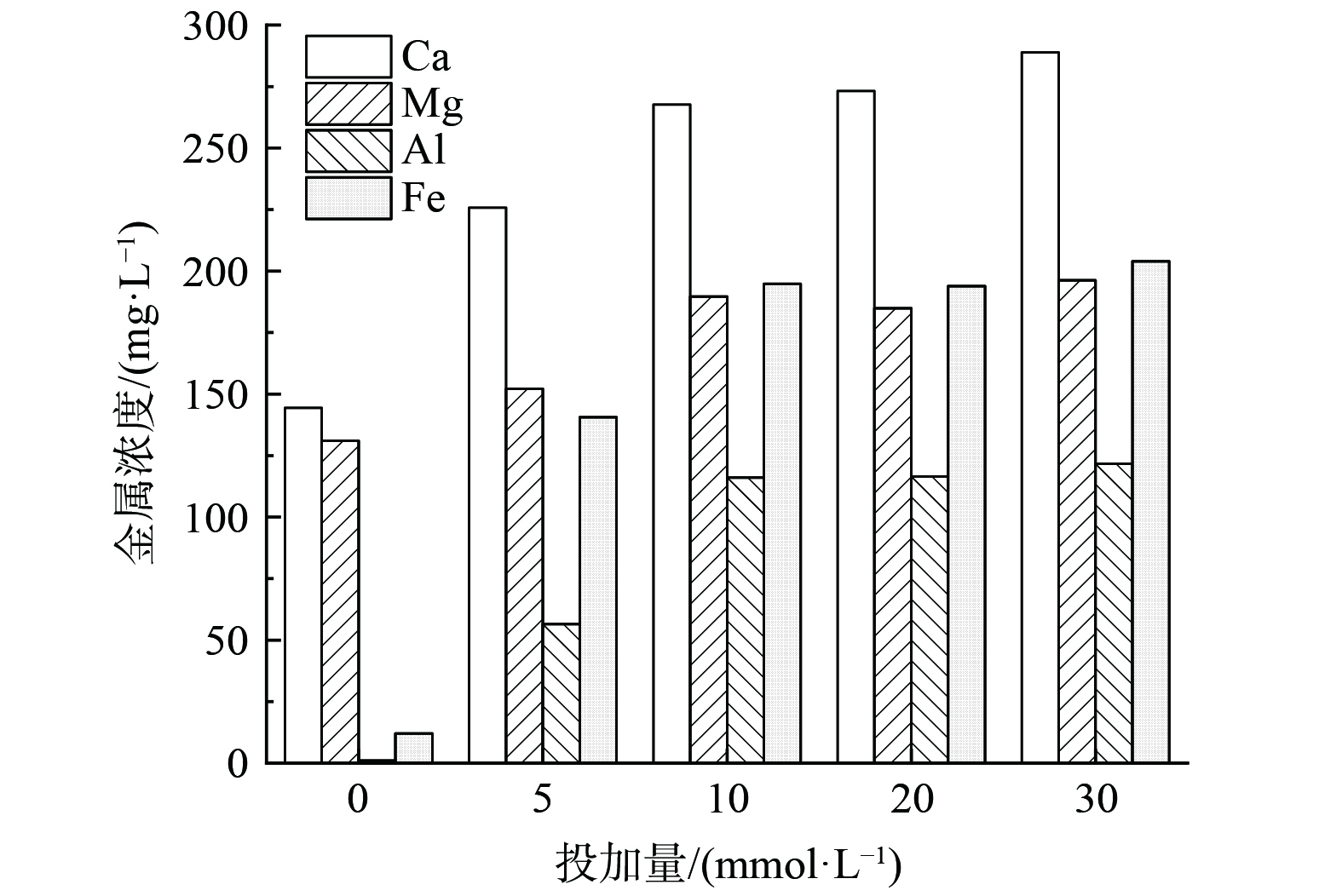
由图6可知,随着EDTA投加量的增加,Ca2+、Mg2+、Al3+和Fe3+的浓度呈现先增加后趋于平缓的趋势。当对污泥单独进行水热碳化处理时,液相中Ca2+、Mg2+、Al3+和Fe3+含量分别从原始污泥的84.5、19.5、0.9和0 mg·L−1增加至144.4、131.0、1.0和12.1 mg·L−1,说明单独水热碳化处理对Ca2+和Mg2+的释放有一定影响,而Al3+和Fe3+只有少量释出。当EDTA投加量为10 mmol·L−1时,Ca2+、Mg2+、Al3+和Fe3+分别增加至267.7、189.6、116.1和194.8 mg·L−1。该结果表明,EDTA的投加对Al3+和Fe3+的释出量影响较大,Ca2+和Mg2+的浸出量受水热碳化和EDTA的双重影响。Ca2+、Mg2+、Al3+和Fe3+在污泥中的赋存形态不同,导致其浸出量之间的差异。Mg2+主要存在于细胞内,Fe3+、Ca2+和Al3+主要储存在细胞内和EPS中[25]。由于污泥中Ca2+含量高,处于EPS外围吸附能力弱的部分,Ca2+在静置条件下被释放进入液相,导致原始污泥上清液中Ca2+含量较高。经水热碳化处理后,细胞膜破裂,EPS结构被破坏,存在于细胞内的Ca2+、Mg2+等金属离子被释放,但由于Ca2+与EPS之间的架桥作用,且部分从细胞内释放的Fe3+、Al3+被EPS捕获,因而只经过水热碳化处理后Fe3+、Ca2+和Al3+的释放量小于Mg2+。当加入EDTA后,EDTA会进一步造成细胞膜破裂和EPS裂解,并与细胞内和胞外聚合物释放的金属离子络合形成可溶性物质进入液相,由于EDTA与Fe3+、Ca2+和Al3+离子的络合能力大于Mg2+,所以与单独水热碳化处理相比,液相中Fe3+、Ca2+和Al3+的释放量大于Mg2+。随着EDTA的增加,大量的金属离子不断释出与其发生络合反应,进而释放出大量的磷酸根进入液相中,此结果也解释了EDTA的添加可以有效地促进污泥中磷的释放,为后续磷的高效回收创造了有利条件。
2.7 水热炭理化性质
对原污泥和经EDTA强化污泥水热碳化后水热炭的元素组成和热值进行了分析,探讨EDTA对水热炭性质的影响,见表2。污泥经过EDTA强化水热碳化处理后,水热炭中的C、H、O、N均有不同程度的下降,这是由于在水热碳化过程中大量有机物发生水解、脱水、脱羧、再聚合等化学反应,分解成小分子物质[26],各元素溶解进入液相,尽管污泥中大量的金属及磷溶出,但仍有部分矿物质(如SiO2)及其它无机组分富集在固相产物中,导致水热炭中各元素含量整体下降,而灰分含量增加[27]。水热炭中的H/C和(O+N)/C降低,说明水热炭的芳香性增强而极性减弱,疏水性更好,有利于提高污泥的脱水性能[28-29]。O/C的值降低,说明随着脱水、脱羧、脱羟基等反应的发生,水热炭表面含氧官能团减少。同时H/C和O/C的降低,使得水热炭有靠近褐煤特性的趋势,而O含量的降低有利于其充分燃烧,提高了其类煤性能。经水热处理之后,O、H含量降低使得水热炭的高位热值升高,也表明发生了脱水和脱羧反应。总体而言,经过EDTA强化污泥水热碳化处理后,水热炭的热值增加、燃烧性能增强。
表 2 污泥及水热炭的元素组成和热值Table 2. Elements composition and calorific value of sludge and hydrochar样品 元素分析(wt) 元素比 HHV/(MJ·kg−1) C H N S O 灰分 H/C O/C (O+N)/C 污泥 30.30% 4.47% 5.48% 0 34.81% 24.94% 0.15 1.15 1.33 10.44 水热炭 29.28% 3.92% 4.61% 0 23.43% 38.76% 0.13 0.80 0.96 11.36 2.8 水热炭表征分析
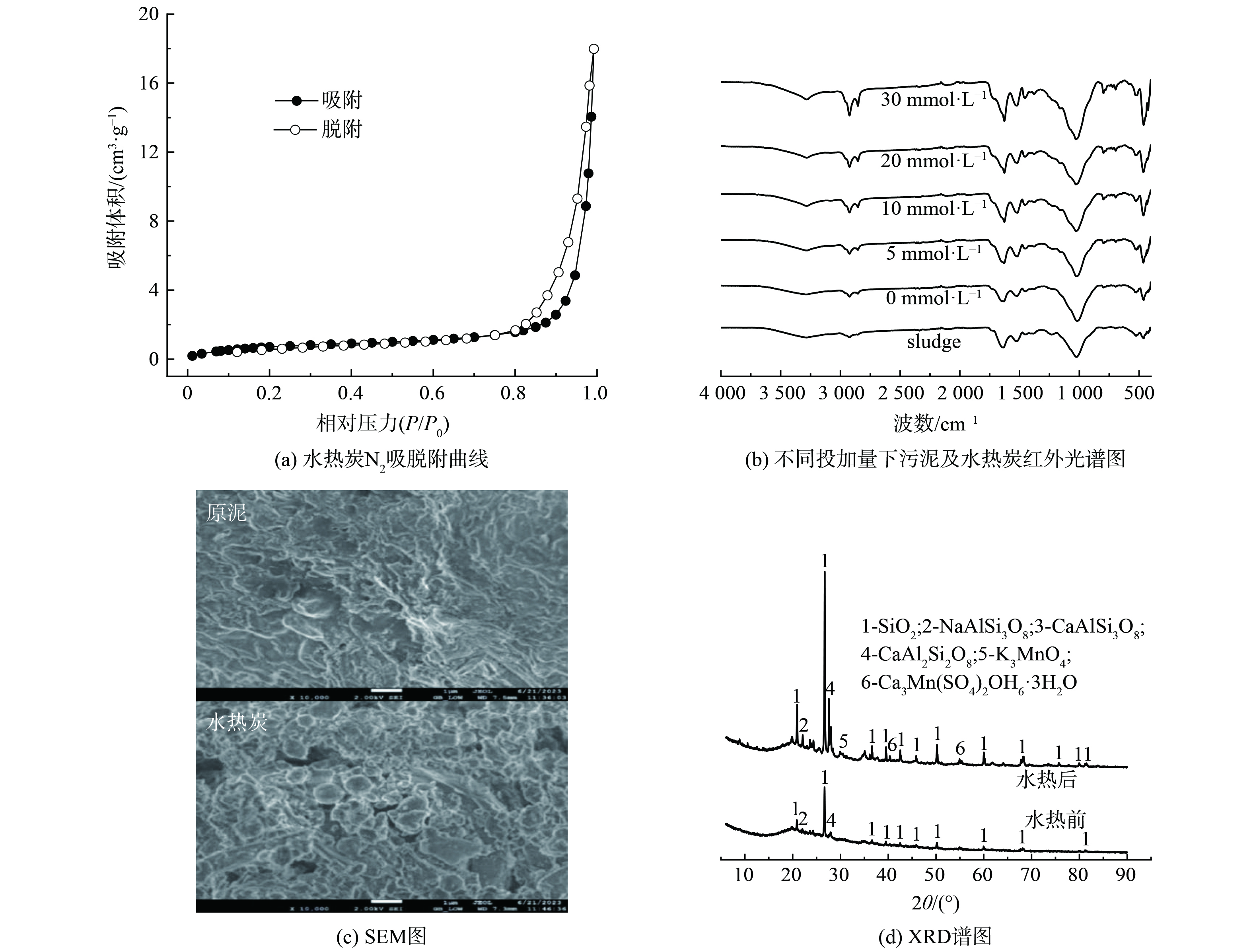
图7(a)为EDTA强化污泥水热碳化处理后得到的水热炭的氮气吸-脱附等温曲线。从图7(a)中可知,吸附曲线与脱附曲线不一致,吸脱附过程中存在滞后环,根据国际纯粹与应用化学联合会(IUPAC)的分类标准,该等温曲线符合Ⅳ型曲线特征,表明水热炭属于介孔材料,孔径在2~50 nm之间。
使用傅里叶转换红外光谱(FTIR)对水热炭主要有机官能团进行分析测定,结果如图7(b)所示。从图中可以看到,不同谱图之间的官能团种类没有明显差异,说明水热碳化过程保留了污泥原有的官能团结构,但官能团峰值强度有所变化。3 200~3 500 cm−1处的吸收峰为O—H伸缩振动峰[30],说明水热炭中存在醇类、羧酸类等物质[31]。随着EDTA投加量的增加,3 282 cm−1处的缔合O—H伸缩振动峰逐渐突出,可能是由于发生了脱水反应,羧基逐渐降解,使得O—H伸缩振动增强[30]。2 924和2 854 cm−1吸收峰分别为C—H拉伸和伸缩振动峰,吸收峰随EDTA用量增加逐渐增强,表明有脂肪物质生成[30]。1 023 cm−1处的吸收峰由SiO2引起的[31],经EDTA强化水热碳化处理后比原污泥增强。说明水热炭中SiO2的相对含量增加。
图7(c)为污泥与经EDTA强化水热碳化处理后得到的水热炭的表面形貌图(SEM)。图7(c)结果显示,处理前后固体表面微观结构发生了比较明显的变化。处理前,原污泥表面光滑平整,呈致密的片状结构;处理后,水热炭表面变得疏松、凹凸不平且有孔洞,说明污泥絮体结构和细胞结构在EDTA强化水热碳化过程中被破坏。水热碳化过程是在高温高压环境里进行的,处于次临界的水相经氧化作用进入污泥内部并大量溶解其中的有机物,在温度降低和释压后,这些水相则与污泥迅速分离,最终使得水热炭呈现出松散多孔的蜂窝状结构[32],这也更有利于磷的释出。
污泥经水热炭后,灰分含量仍占有很大比例,这些灰分主要为一些无机盐成分。使用X-射线衍射(XRD)的方法,对水热炭中存在的无机晶相进行成像分析,对比水热碳化前后污泥中主要组分的变化,见图7(d)。从图7(d)中可以看出,对于污泥和水热炭,出峰主要集中在19°~85°之间。污泥中主要成分包括石英(SiO2)、钠长石(NaAlSi3O8)、方解石(CaAlSi3O8)、钙长石(CaAl2Si2O8),由于这些物质在水热炭化过程中热稳定性强,大部分晶体结构仍然以灰分的形式被保留在水热炭中。与原污泥相比,经水热碳化反应后,增加了钾锰氧化物(K3MnO4)和钙锰钒。
3. 结论
1)经过EDTA强化污泥水热碳化处理后,污泥絮体结构被破坏,胞内有机物质被释放,大分子物质水解,大量磷从固相转移至液相,使水热液中TP和PO43−含量显著增加。在210 ℃,时间4 h,EDTA投加量10 mmol·L−1的条件下,TP和PO43−的浓度分别可达339.1和325.6 mg·L−1,释放率为96.2%。
2)在水热碳化过程中,高温促使污泥破解释放金属离子和磷至液相,EDTA的加入促进了EPS和细胞膜的溶解,并阻止了金属离子与磷再形成难溶沉淀物,促进了磷的释放;增加EDTA投加量会促使大量的OP转化为IP,NAIP转化为AP。
3)经过EDTA强化污泥水热碳化后,水热炭保留了污泥中原有的官能团,燃烧性能和热值均有所提高,芳香性增强而极性减弱,同时出现了孔结构。
-

 点击查看大图
点击查看大图
计量
- 文章访问数: 2105
- HTML全文浏览数: 975
- PDF下载数: 1324
- 施引文献: 0



 DownLoad:
DownLoad: