-
近年来,环境污染问题愈趋严峻,其中重金属对环境的污染和破坏作用尤为突出,严重危害人类的健康和生存[1 − 3]. 汞是环境中毒性最强的重金属元素之一,汞离子在生物体内能和蛋白质及各种酶发生强烈的相互作用,使生物体失去活性,进而导致机体产生病变或表现出毒性[4 − 5]. 汞离子具有不易降解性、易迁移性和高度生物蓄积性的特点,当在人体内积累达到一定程度时,即可呈现出毒性作用,从而危害人体健康[6 − 7]. 世界卫生组织(WHO)将Hg2+视为能够造成重大公共健康风险的十大化学品或物质之一[8 − 9]. 探索水环境中高选择性、高灵敏度检测Hg2+的方法已成为环境生态科学领域的研究热点[10 − 11].
荧光探针检测技术具有操作简单、高选择性、高灵敏度、响应时间迅速等优点,近年来已被广泛应用于环境污染物的检测研究[12 − 14]. 利用Hg2+与S原子的强结合能力,多种以硫代苯甲酸酯为识别基团的荧光探针被开发应用于环境和生物体内Hg2+的高选择性和高灵敏度识别检测[15 − 17]. 孙艳丽等[18]以半花菁染料为荧光基团,设计合成了一个席夫碱型荧光探针用于实际水样中Hg2+的高选择性检测. 李淑雅等[19]以7-羟基吩恶嗪酮为荧光基团,开发了一个比色荧光双通道探针,该探针对Hg2+检测的线性范围为0—10 μmol·L−1,检出限为17 nmol·L−1. Wang等[20]以苯并噻唑作为荧光基团,设计合成了一个比率型荧光探针,通过405 nm和525 nm处荧光强度的比值变化,对50—100 μmol·L−1浓度范围内的Hg2+进行准确定量检测. Jiang等[21]以香豆素为荧光基团,构建了一个近红外荧光探针,该探针通过695 nm处的强荧光发射实现Hg2+的检测,同时展现出巨大的斯托克斯位移(316 nm). 此类荧光探针大多以硫代苯甲酸酯为识别基团,本文选择以N,N-二甲氨基硫代甲酸酯为识别基团构建荧光探针,丰富了Hg2+识别基团的选择.
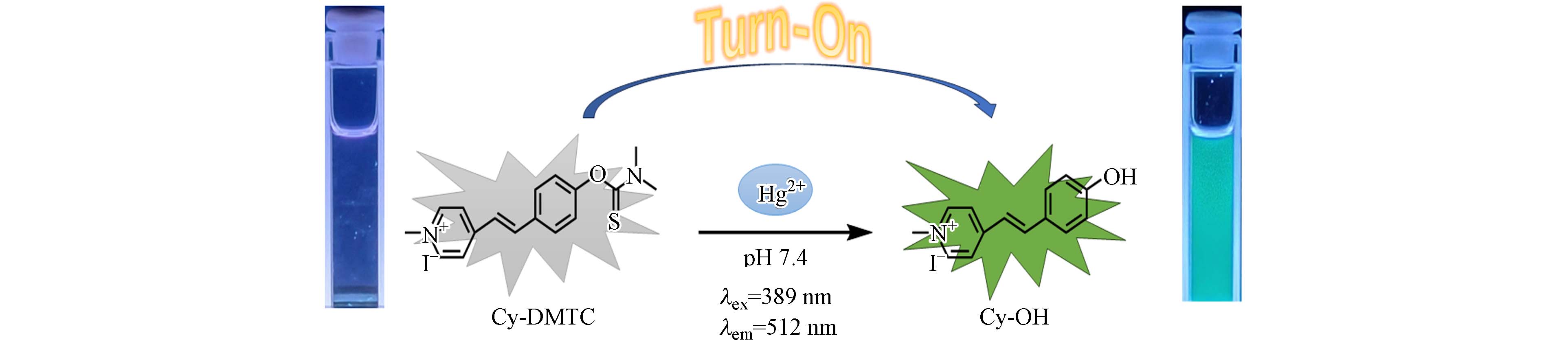
半花菁染料是由氮杂环阳离子通过π共轭桥连与电子供体连接而成的D-π-A体系,因其具有良好且稳定的光学性质、较高的结构修饰度、溶解度好、荧光量子产率高及较大的Stokes位移等优点,被广泛应用于构建荧光探针和生物传感器[22 − 25]. 本文以半花菁类染料为荧光信号基团,以N,N-二甲基硫代甲酸酯为识别基团,构建了一个高选择性高灵敏度检测Hg2+的荧光探针,并研究了该探针在环境水Hg2+检测中的应用.
-
RF-5301PC荧光分光光度计(日本岛津);IRTracer-100(日本岛津);UV-2450紫外分光光度计(日本岛津);BrukerAscend 400 MHz超导核磁共振波谱仪(德国布鲁克公司).
N,N-二甲氨基硫代甲酰氯、碘甲烷、三乙烯二胺(DABCO)、4-羟基苯甲醛、4-甲基吡啶均购于上海阿拉丁有限公司;所用试剂均为分析纯试剂;实验所用水为二次去离子水.
-
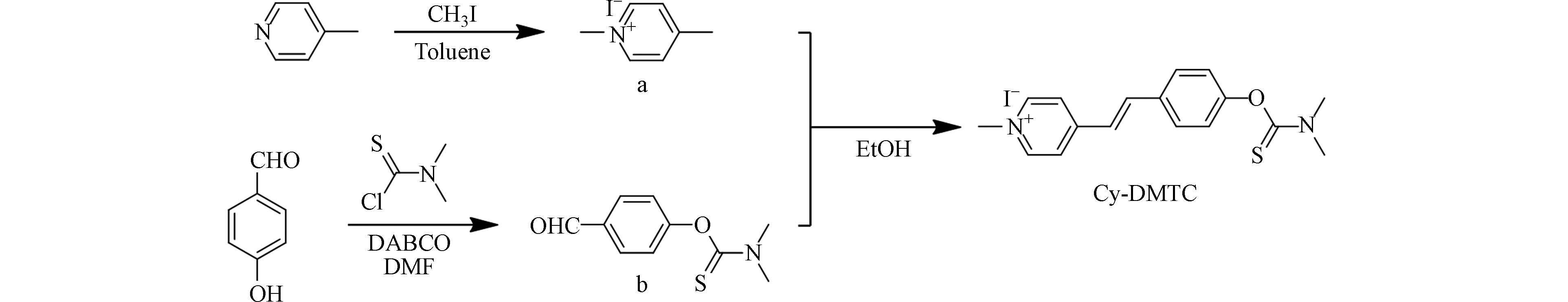
合成路线见图1.
中间体a的合成及表征:于50 mL反应瓶中加入碘甲烷(3.00 g,21.1 mmol)、4-甲基吡啶(2.00 g,21.5 mmol)、10 mL甲苯. 110 ℃加热回流24 h,冷却至室温,将甲苯溶液移出,再用乙醚多次洗涤沉淀,除掉残留的4-甲基吡啶得到白色固体,即为中间体a(4.26 g,86%). 1H NMR (400 MHz, CDCl3) δ 9.12 (d, J = 6.4 Hz, 2H, Py-H), 7.86 (d, J = 6.4 Hz, 2H, Py-H), 4.64 (s, 3H, —N+CH3), 2.69 (s, 3H, —CH3).
中间体b的合成及表征:于50 mL反应瓶中加入N,N-二甲氨基硫代甲酰氯(2.00 g,16.2 mmol)、4-羟基苯甲醛(1.00 g,8.2 mmol)、DABCO (1.80 g,16.0 mmol)、8 mL DMF. 氮气保护下室温搅拌4 h,反应完全后,将体系倒入冰水中有沉淀析出,后进行减压抽滤,多次水洗沉淀得到白色固体,即为中间体b(1.61 g,94%). 1H NMR (400 MHz, DMSO-d6) δ 10.00 (s, 1H, —CHO), 7.97—7.94 (m, 2H, Ar-H), 7.33—7.30 (m, 2H, Ar-H), 3.37 (s, 3H, —N(CH3)2), 3.33 (s, 3H, —N(CH3)2).
探针Cy-DMTC的合成与表征:于50 mL反应瓶中,加入10 mL乙醇、中间体a(1.12 g,4.78 mmol)、中间体b(0.50 g,2.39 mmol),78 ℃加热回流24 h,反应完全后,冷却至室温,过滤,乙醇洗涤沉淀,所得黄色固体为探针Cy-DMTC (0.55 g,54%). 1H NMR (400 MHz, DMSO-d6) δ 8.86 (d, J = 6.8 Hz, 2H, Py-H), 8.21 (d, J = 6.8 Hz, 2H, Py-H), 8.02 (d, J = 16.4 Hz, 1H, alkene-H), 7.77 (d, J = 8.8 Hz, 2H, Ar-H), 7.48 (d, J = 16.4 Hz, 1H, alkene-H), 7.21 (d, J = 8.4 Hz, 2H, Ar-H), 4.26 (s, 3H, —N+CH3), 3.37 (s, 3H, —N(CH3)2), 3.33 (s, 3H, —N(CH3)2). 13C NMR (100 MHz, DMSO-d6) δ 186.42, 155.64, 152.89, 145.61, 140.19, 133.15, 129.46, 124.13, 124.01, 123.74, 47.43, 43.34, 39.10.
-
称取探针Cy-DMTC(5.30 mg,0.01 mmol)溶于MeOH溶液中,配制浓度为5×10−4 mol·L−1的探针储备液25 mL,逐级稀释备用. 光谱分析时,移取探针Cy-DMTC的5×10−6 mol·L−1储备液3 mL到1 cm × 1 cm 的比色皿中,分别进行荧光光谱和紫外-可见吸收光谱的测定. 其中,荧光光谱分析的仪器参数为:激发波长为389 nm,激发及发射狭缝分别为5 nm、10 nm.
称取各类金属离子(Hg2+、Li+、Mg2+、Na+、Zn2+、K+、Ca2+、Ba2+、Co2+、Pb2+、Cr2+、Al3+、Fe3+、Ni2+、Ag+、Cu2+、Cd2+)的高氯酸盐或硝酸盐溶解于水中,配制浓度为1×10−3mol·L−1的储备液25 mL,备用.
-
分别选取矿泉水、自来水、湖水3个水样10 mL,超声处理10 min,通过0.22 μm微孔滤膜进行过滤,并以HEPES缓冲液调节水样pH至7.4;再分别加入探针Cy-DMTC和不同浓度的Hg2+(0、2、5、10 μmol·L−1). 充分摇匀并静置10 min后,通过荧光光谱仪进行荧光光谱测定.
-
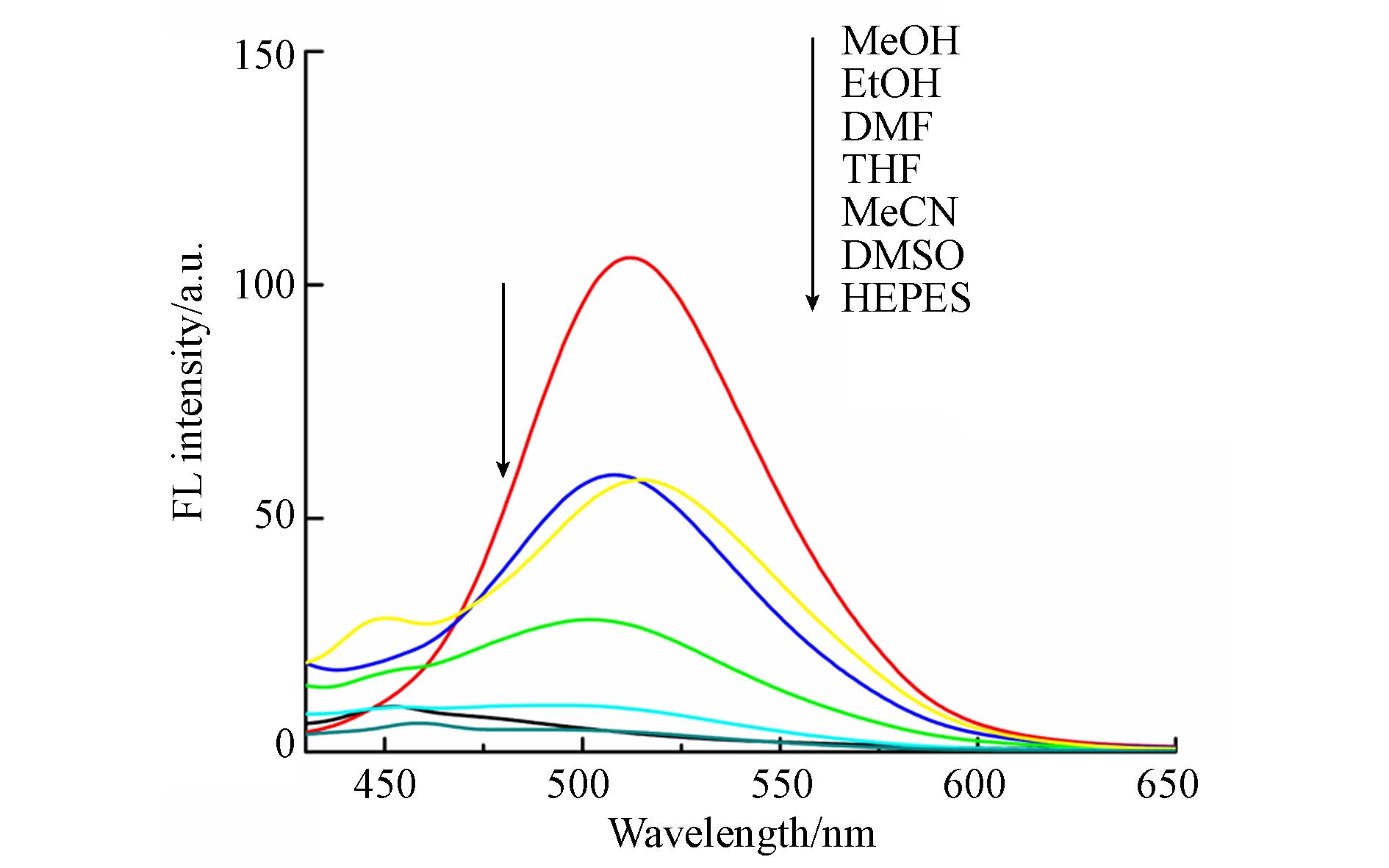
分别配制探针Cy-DMTC(5×10−6 mol·L−1)的不同溶剂供试液(MeOH、DMSO、EtOH、THF、MeCN、DMF)/HEPES缓冲液(1/1,V/V,pH = 7.4)以及100%HEPES缓冲液(pH = 7.4),再分别加入Hg2+(5×10−6 mol·L−1)以考察不同溶剂体系对荧光光谱的影响. 结果如图2所示,在MeOH、EtOH、DMF、THF混合溶剂体系中,探针Cy-DMTC识别Hg2+后荧光强度增强,其中在MeOH溶剂中荧光强度最高,灵敏度最优. 此外,该探针易溶于MeOH,并且在MeOH溶剂中十分稳定. 因此,本研究选择以MeOH作为测试溶剂.
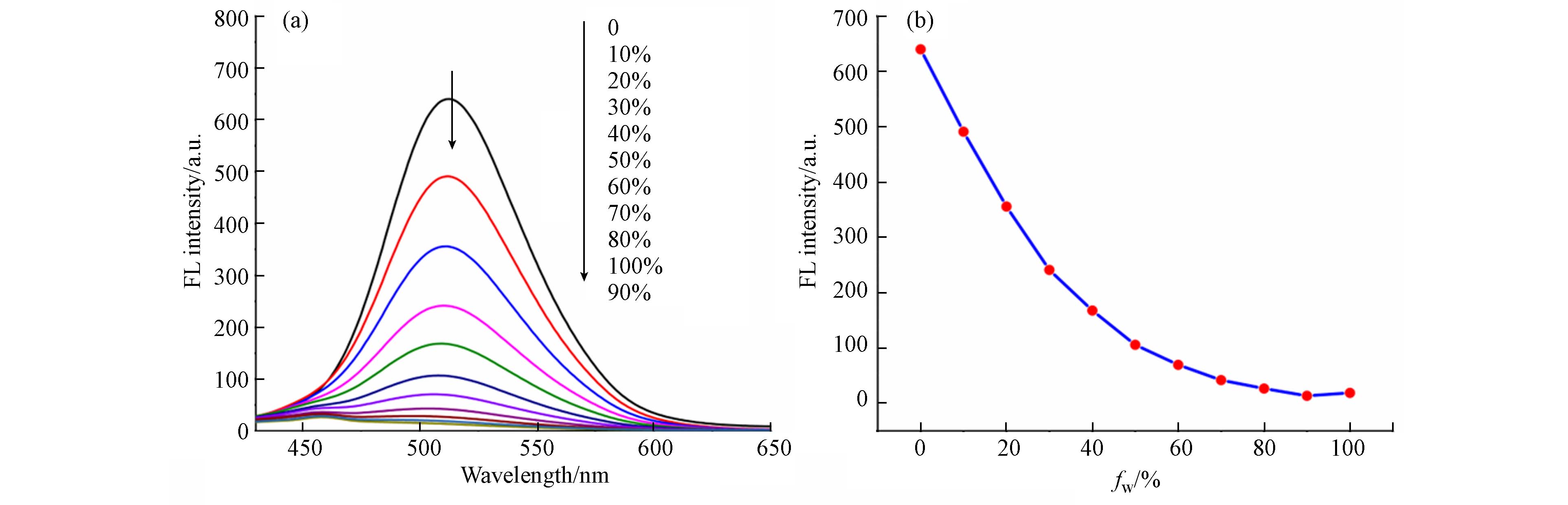
为了进一步考察含水量对探针Cy-DMTC识别检测Hg2+的影响,测试了探针Cy-DMTC+Hg2+ (5×10−6 mol·L−1)在不同含水量的MeOH溶液中的荧光光谱. 结果如图3所示,探针Cy-DMTC在识别Hg2+的过程中,在纯MeOH溶剂中荧光强度最高,随着含水量增加,其荧光强度逐渐减弱直至淬灭. 考虑到探针的实际应用场景多为含水体系,因此,选择以MeOH/HEPES (9/1,V/V,pH = 7.4)作为后续分析条件.
-
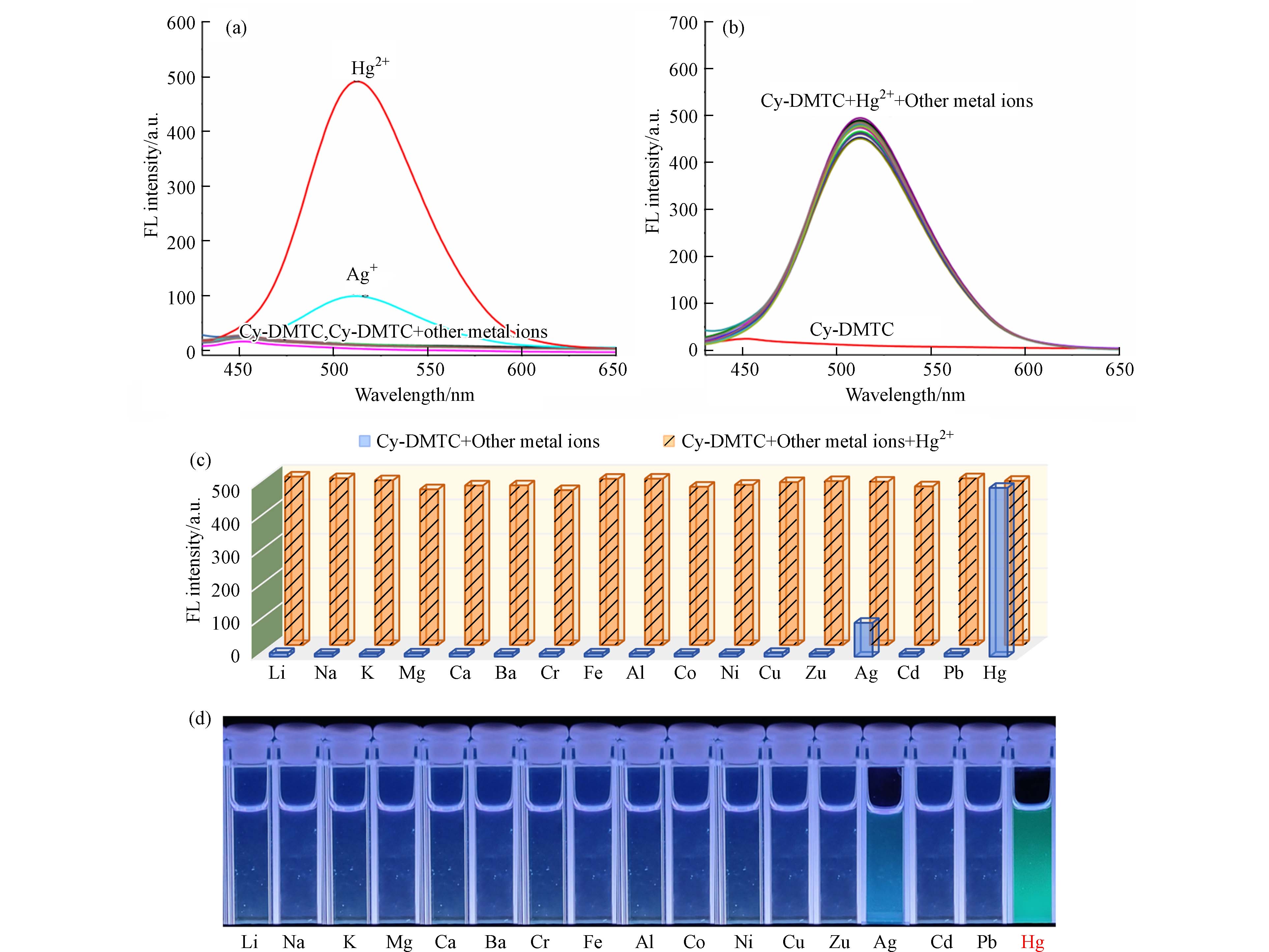
通过荧光光谱研究了探针Cy-DMTC对各种金属离子如Hg2+、Li+、Na+、K+、Mg2+、Ba2+、Ca2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Ag+、Cr3+、Al3+、Pb2+、Cd2+的选择性. 结果如图4a所示,探针Cy-DMTC本身无荧光,加入Hg2+后在512 nm处出现强荧光发射峰,并呈现出强绿色荧光(图4d);除Ag+发生少许荧光响应之外,其余金属离子的加入均未引起荧光光谱的明显变化,表明该探针对Hg2+具有高选择性识别作用. 此外,抗干扰性是荧光探针应用于实际复杂环境检测的重要前提,因此,进一步考察了该探针在干扰离子存在下对Hg2+的特异选择性识别检测能力. 在上述相同的条件下,测定了不同金属离子与Hg2+共存时对探针Cy-DMTC检测Hg2+的影响. 结果如图4b所示,在其他金属离子共存时,探针Cy-DMTC对Hg2+的检测几乎未受到影响. 表明该探针Cy-DMTC对Hg2+具有较高的选择性,且抗干扰性强,有望在复杂的实际环境中实现对Hg2+的定性定量检测.
-
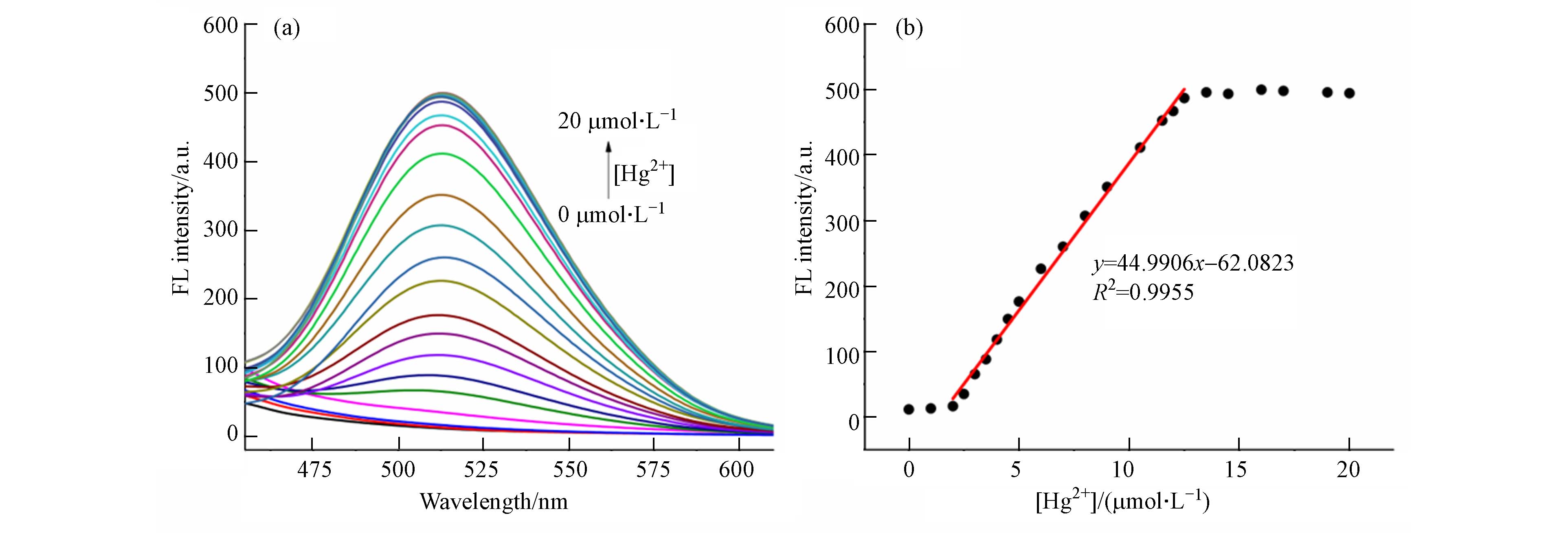
为了探究探针Cy-DMTC对Hg2+的定量分析检测能力,在探针MeOH/HEPES (9/1,V/V,pH = 7.4)溶液中加入0—2.0×10−5 mol·L−1的Hg2+测量荧光光谱. 如图5a所示,随着Hg2+浓度增加,探针Cy-DMTC在512 nm处的荧光强度逐渐增强,直至加入2.5倍Hg2+时,其荧光强度增强了42倍,达到最高值且持续稳定. 探针Cy-DMTC的荧光强度与Hg2+浓度(2.0×10−6—12.5×10−6 mol·L−1)呈现出良好的线性关系,其线性回归方程为y=-62.0823+44.9906x (R2=0.9955) (图5b),检出限LOD为8.65×10−8 mol·L−1 (3σ/k). 更为重要的是,探针Cy-DMTC在检测Hg2+的过程中产生了显著的stokes位移(156 nm),较大的stokes位移能降低背景的干扰,从而提高检测的灵敏度. 以上结果表明,该探针可实现2.0×10−6—12.5×10−6 mol·L−1范围内Hg2+的定量检测.
-
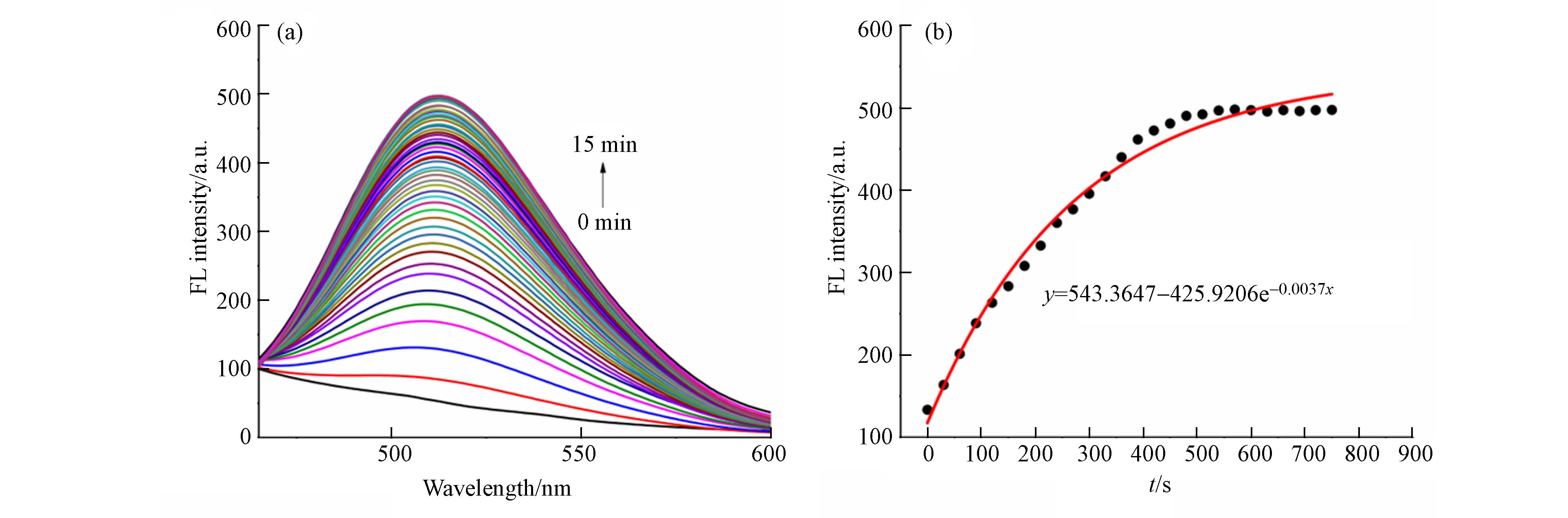
响应速度是评价荧光探针性能的重要因素,因此,进一步考察了探针Cy-DMTC识别检测Hg2+的反应速率. 于探针Cy-DMTC(5×10−6 mol·L−1)溶液中加入Hg2+后,每间隔30 s测定一次. 如图6a所示,向探针Cy-DMTC的溶液中加入Hg2+后,其在512 nm处的荧光强度随时间呈现快速增强的趋势,直至8 min后荧光强度趋于平衡. 通过非线性拟合计算出Cy-DMTC与Hg2+的反应速率为3.68×10−3 s−1(图6b),表明探针Cy-DMTC可作为快速识别Hg2+的荧光传感器.
-
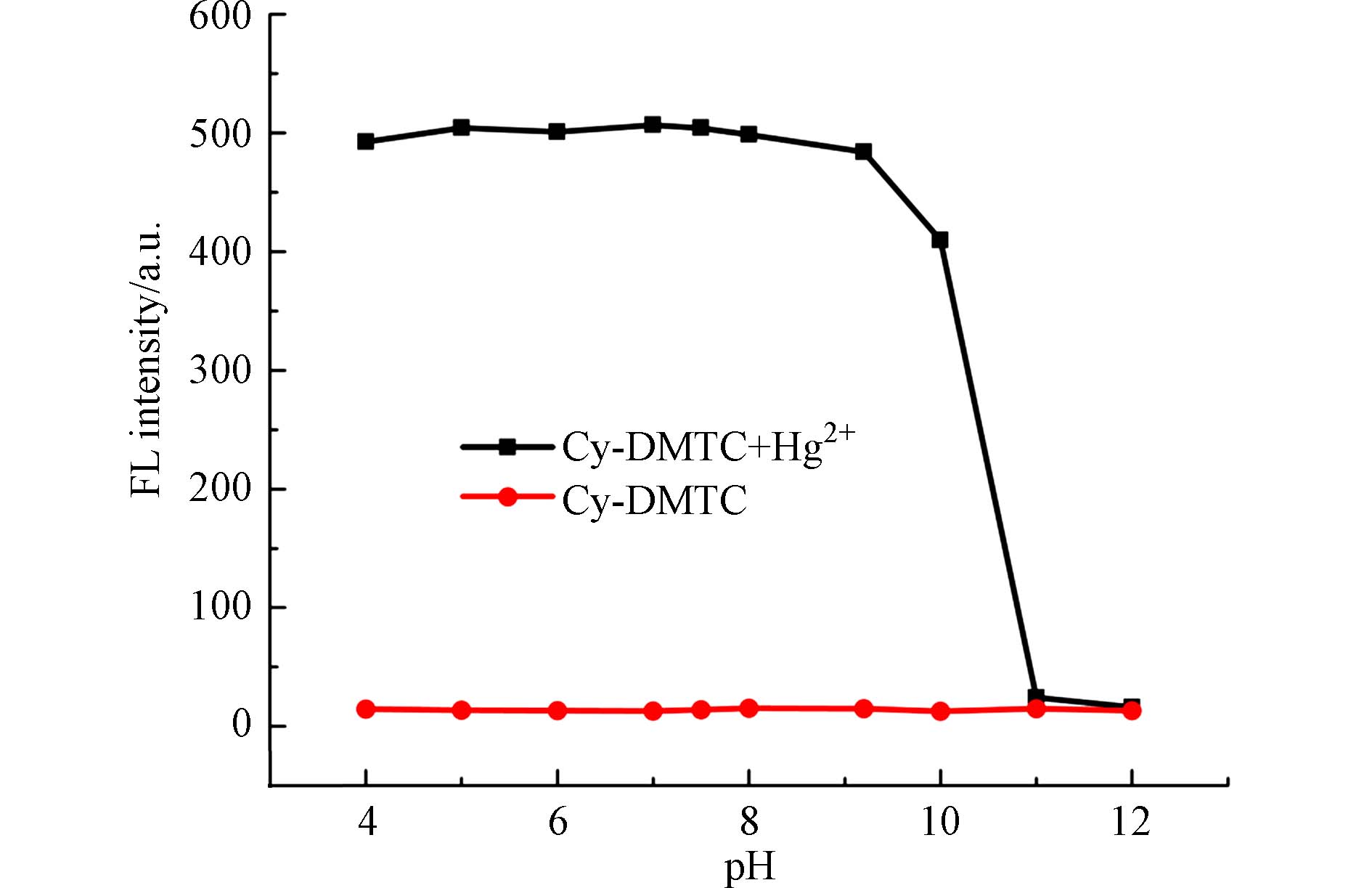
为了考察该探针在不同pH下检测Hg2+的稳定性,测定了探针Cy-DMTC及Cy-DMTC+Hg2+在不同pH下的荧光光谱. 结果如图7所示,pH在4.0—12.0范围内,探针Cy-DMTC在512 nm处的荧光强度几乎无变化,表明该探针不受pH的影响,且较为稳定. 当加入Hg2+后,pH在4.0—9.0范围内,探针在512 nm处的荧光强度显著增强,且在这一pH范围内较为稳定;当pH值大于9.0时,探针荧光强度逐渐降低,直至pH大于11后荧光淬灭. 结果表明,探针Cy-DMTC能够在较广泛的pH (4.0—10.0)范围内识别检测Hg2+.
-
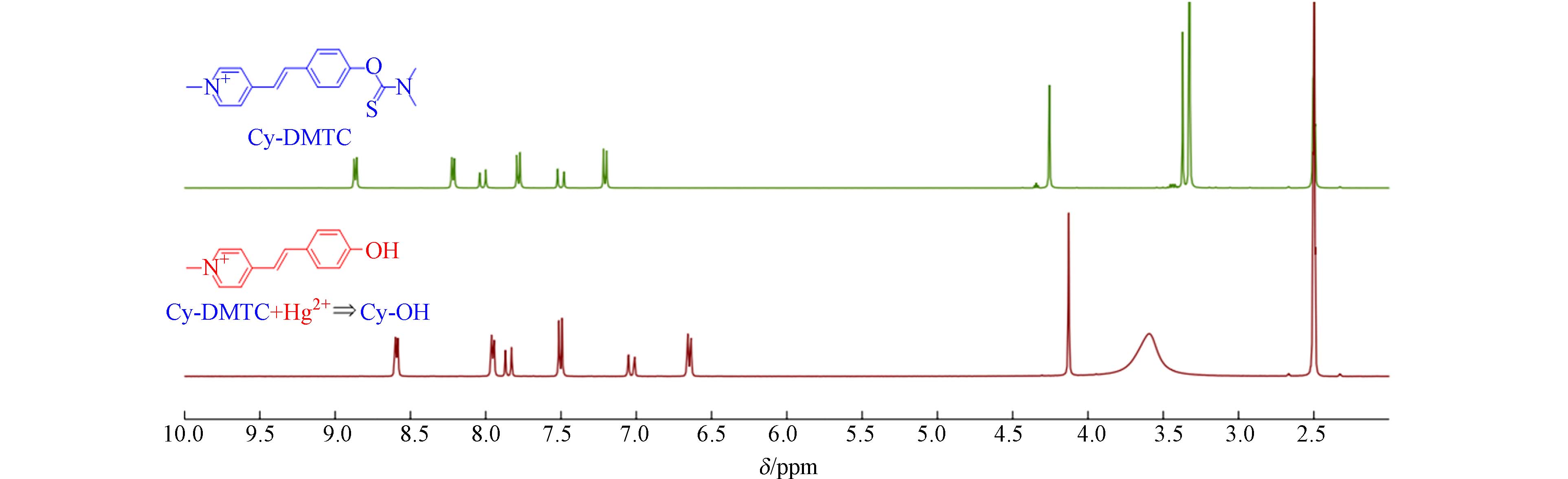
为了阐明探针Cy-DMTC识别Hg2+的作用机制,分别进行了1H-NMR、IR及HRMS的测定. 于100 mL圆底烧瓶中加入探针Cy-DMTC(100.00 mg,0.2 mmol)、高氯酸汞(96.00 mg,0.2 mmol)、10 mL甲醇. 室温搅拌,经TLC监测反应进程,反应完全后旋干溶剂,以正己烷/乙酸乙酯(5/1,V/V)作为洗脱剂,柱层析进行分离纯化后得到红色固体. 1H NMR (400 MHz, DMSO-d6) δ 8.60 (d, J = 6.8 Hz, 2H, Py-H), 7.96 (d, J = 6.8 Hz, 2H, Py-H), 7.87 (d, J = 16.0 Hz, 1H, alkene-H), 7.51 (d, J = 8.4 Hz, 2H, Ar-H), 7.05 (d, J = 16.0 Hz, 1H, alkene-H), 6.66 (d, J = 8.4 Hz, 2H, Ar-H), 4.13 (s, 3H, —CH3). 通过将探针Cy-DMTC与Hg2+反应后得到的产物进行1H-NMR测定,如图8所示,探针Cy-DMTC在化学位移δ = 3.37和δ = 3.33处的两个单峰(—CH3)消失,表明硫代甲酸酯部分发生水解生成—OH;由于—OH具有更强的推电子作用,导致芳环和吡啶环上的电子云密度增大,化学位移移向高场,因此证实水解产物为Cy-OH.
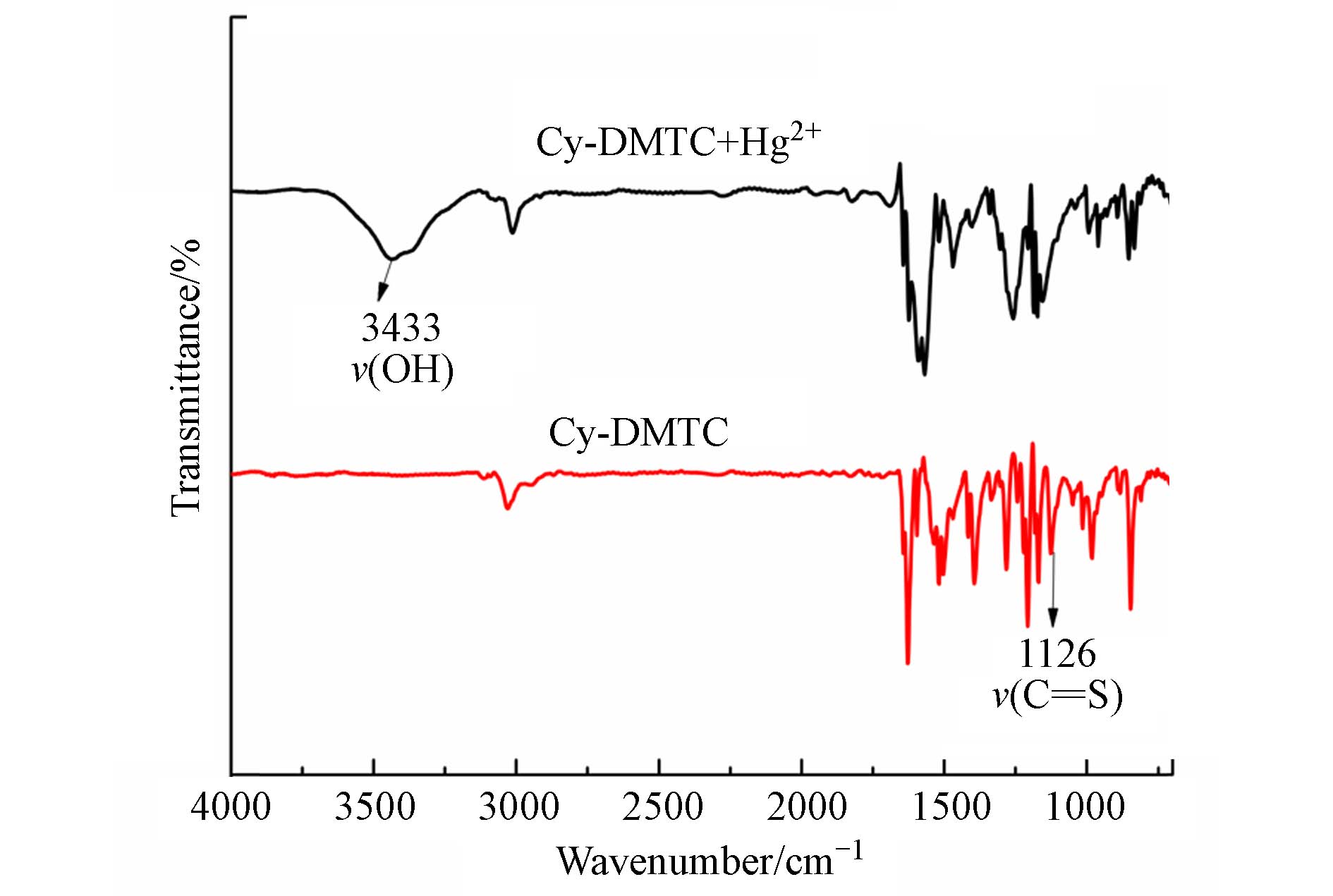
此外,通过红外光谱考察了探针Cy-DMTC识别检测Hg2+的机理. 如图9所示,当Hg2+与Cy-DMTC作用后,在3433 cm−1处明显出现了—OH伸缩振动的特征峰,同时Cy-DMTC在1126 cm−1的C=S伸缩振动峰消失. IR光谱的实验结果与上述1H-NMR的结论一致,也进一步证实Cy-DMTC识别检测Hg2+后的产物为Cy-OH.
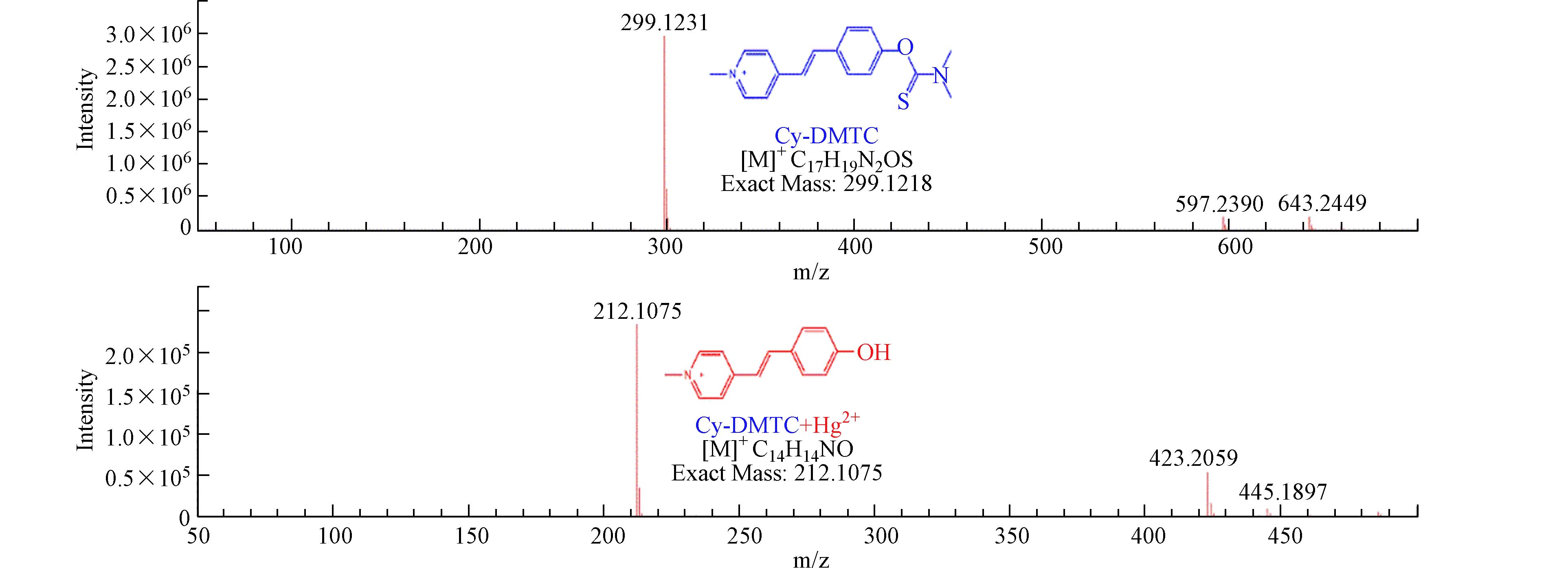
高分辨质谱(HRMS)进一步研究发现(图10),当Cy-DMTC溶液中加入Hg2+后,测得的分子量为212.1075,与Cy-DMTC水解产物Cy-OH的理论分子量212.1075相符. 通过1H-NMR、IR和HRMS的研究结果,可以证实探针的识别机理为Hg2+诱导硫代甲酸酯发生水解,生成Cy-OH,从而引起羟基到吡啶环的分子内电荷转移,导致荧光增强. 综上,识别机理如图11所示.
-
为了探究Cy-DMTC检测Hg2+的实用性,选取湖水、自来水、矿泉水3种水样,测试探针在实际水样中检测Hg2+的能力. 将水样过滤,pH值调节到7.4,用水样配制Cy-DMTC (5×10−6 mol·L−1)的MeOH/HEPES (V/V,9/1)供试液进行Hg2+的荧光检测,结果均未检出. 因此在水样中加入浓度分别为2、5、10 μmol·L−1的Hg2+进行加标回收实验,平行测试3次. 结果见表1,实际水样中Hg2+加标回收率达96%以上,且RSD%介于1.03%—1.89%之间,表明该方法具有较高的准确度和重现性,可用于环境水中Hg2+的定量分析检测.
-
本文基于Hg2+促进的N,-N-二甲基硫代甲酸酯水解反应,以半花菁染料为荧光基团,设计合成了一种可用于Hg2+识别检测的反应型荧光探针Cy-DMTC. 该探针展现出对Hg2+的高选择性和高灵敏度识别检测,且不受其他共存金属离子的干扰. 该探针适用于酸性、中性和弱碱性条件下Hg2+的荧光检测,可在较为广泛的pH范围内应用,且被成功应用于实际水样中Hg2+的分析检测,具有潜在的应用前景.
一种反应型荧光探针的构建及其在环境水汞离子检测中的应用
Construction of a reaction-based fluorescent probe and its application in the detection of mercury ions in environmental water
-
摘要: 汞因具有高毒性、迁移性等特点对环境及人体产生巨大的伤害. 因此,建立便捷、高效、快速检测Hg2+的分析方法具有重要意义. 本文以半花菁染料为荧光基团,N,N-二甲氨基硫代甲酸酯为识别基团,设计合成了一种反应型荧光探针Cy-DMTC. 荧光光谱滴定分析显示探针Cy-DMTC能够特异性识别Hg2+,且灵敏度高、抗干扰能力强. 随着Hg2+浓度增加,其512 nm处荧光强度不断增强且呈现出强绿色荧光,同时产生了显著的stokes位移(156 nm). 探针的荧光强度与Hg2+浓度在2.0×10−6—12.5×10−6 mol·L−1范围内呈现良好的线性相关(R2=0.9955),检出限为8.65×10−8 mol·L−1. 机理研究证实由于Hg2+诱导硫代甲酸酯发生水解反应,导致电荷转移荧光增强,从而实现对Hg2+的定性定量检测. 探针Cy-DMTC已被成功应用于实际水样中Hg2+的检测,可为Hg2+的检测提供了一种高效的解决方案.
-
关键词:
- 荧光探针 /
- 半花菁 /
- N,N-二甲氨基硫代甲酸酯 /
- 汞离子 /
- 反应型探针.
Abstract: Mercury is extremely harmful to ecosystems and human health due to its toxicity and mobility. Consequently, the development of a convenient, efficient, and rapid analytic method for the detection of Hg2+ is of great importance. Herein, Cy-DMTC was designed and synthesized as a reaction-based fluorescent probe by using hemicyanine dye as the fluorescent group and N,N-dimethylthiocarbamoyl as the recognition group. The results of the fluorescence titration investigation demonstrate that Cy-DMTC can specifically recognize Hg2+ with high sensitivity and strong anti-interference ability. The fluorescence intensity at 512 nm exhibits a consistent increase as the concentration of Hg2+ is raised, resulting in strong green fluorescence and a substantial Stokes shift (156 nm). The fluorescence intensity of Cy-DMTC exhibits an excellent linear correlation with Hg2+ concentration in the range of 2.0×10−6—12.5×10−6 mol·L−1 (R2=0.9955), with a detection limit of 8.65×10−8 mol·L−1. Mechanism studies revealed that Hg2+ triggers the hydrolysis of thiocarbonate, thereby enhancing charge transfer fluorescence and making Hg2+ detectable both qualitatively and quantitatively. Cy-DMTC has been successfully used to detect Hg2+ in real water samples, thus providing an effective method for Hg2+ detection.-
Key words:
- fluorescent probe /
- hemicyanine /
- N,N-dimethylthiocarbamoyl /
- mercury ion /
- reaction-based probe.
-
当前人工合成化学物被大量生产使用,给食品安全风险评估带来严峻挑战. 传统的化学物风险评估数据主要依赖于动物试验及体外试验等各类测试方法,但测试成本、试验周期、动物伦理以及“3R”原则的限制,导致了无法开展高通量、快速的风险评估. 随着毒理学测试方法的发展和风险评价策略的调整,2007年美国国家研究委员会提出“21 世纪的毒性试验:愿景与策略”(Toxicity Testing in the 21st Century: A Vision and a Strategy),强调了未来化学物毒性测试应借助计算毒理学和基于人源细胞、细胞系或细胞组分体外测试的组合方法[1],即新策略方法(New Approach Methodologies,NAMs),包括我国在内的很多国家和国际组织正在开展下一代风险评估技术研发[2 − 5],而NAMs是下一代风险评估的技术支持.
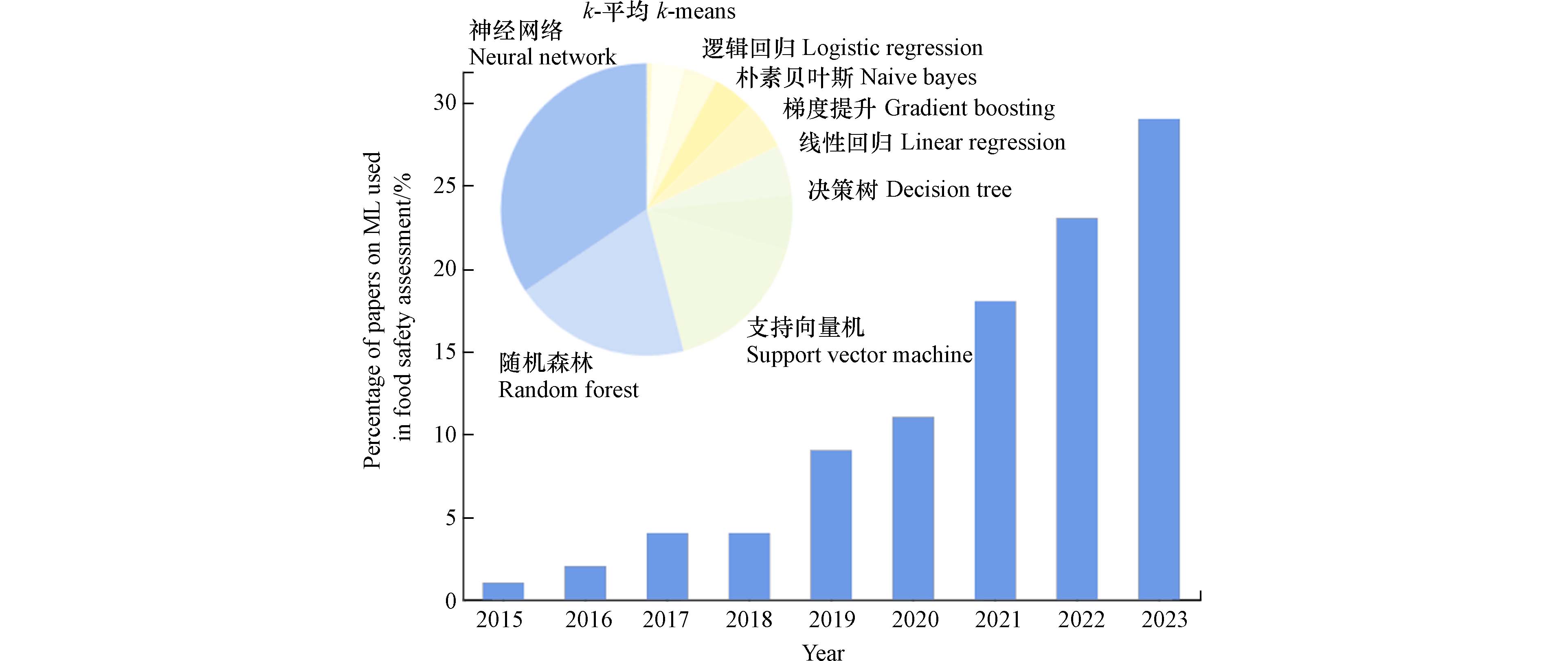
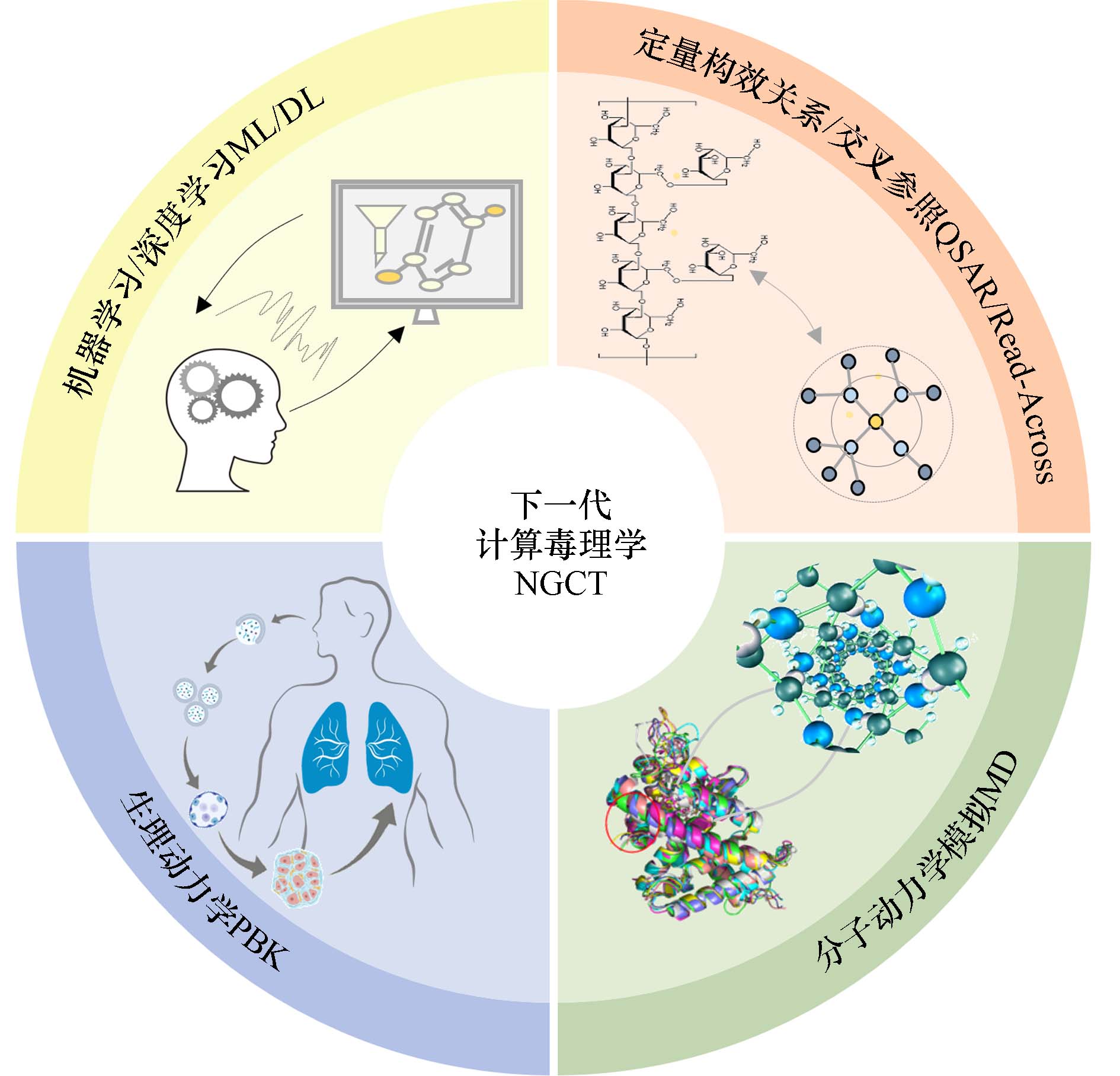
随着人工智能(Artificial Intelligence,AI)的快速发展,基于机器学习(Machine Learning,ML)和深度学习(Deep Learning,DL)的下一代计算毒理学(Next-Generation Computational Toxicology,NGCT)逐渐兴起(图1),为化学物的高通量测试提供技术支撑[6]. NGCT通过挖掘化学、毒理学、医学、多组学、系统生物学等在内的多模态大数据,对化学物的各类属性以及毒性等进行高通量预测. 目前NGCT被逐渐用于开发化学物风险评估的NAMs[7],美国食品和药品管理局关于建模和仿真的相关报告中重点强调了NAMs的应用,如基于生理的动力学模型(Physilogically Based Kinetics,PBK)建模、定量构效关系(Quantitative Structure-Activity Relationship,QSAR)分析、交叉参照分析(Read Across)用于风险评估的概率和统计建模等. 为进一步促进NGCT在化学物风险评估中的应用,本文介绍NGCT主要方法及其在食品安全风险评估中的应用,为化学物安全风险评估研究提供借鉴.
1. 基于人工智能的安全性评估(AI-based safety assessment)
ML和DL在食品安全领域具有多种用途,常被用于预测食品安全风险. 随着AI的快速发展和大型数据库的建设,基于ML和DL的预测方法整合了多种NAMs,在化学物风险评估中发挥重要作用,近年关于机器学习的食品安全风险评估研究论文数量持续增加(图2).
ML和DL模型被广泛用于食品及食品相关化学物的安全性评估[8],可用于构建针对外源性化学物暴露的毒性筛查模型,包括贝叶斯网络[9]、神经网络[10,11]、支持向量机[12]和决策树[13,14]等算法常被用于食品安全风险分析及预警. 针对食品添加剂的潜在神经毒性,基于神经网络的ML模型建立了通用的食品有害因素分类评估分数,为大规模进行食品中具有神经毒性物质的风险评估提供有效手段[15]. 基于DL开发的DeepCarc模型运用碱基分类选择策略,实现了高准确率的化合物致癌风险优先级的筛选[16]. 通过亚临床和癌症前期阶段获得的数据构建ML模型,将有助于建立与饮食和儿童患传染性单核细胞增多症的关联,确定食品加工过程中产生的具有不良作用的化合物摄入的风险阈值[17]. 针对食品及食品添加剂的危害水平预测,将基于膳食暴露评估和暴露限值建立的风险评估模型,以及熵权-层次分析法计算食品中化学成分的风险值,进一步利用反向传播神经网络建立安全风险预警模型,预测食品的生产和加工过程是否存在安全风险,从而从源头上进行管控.
AI可结合电子鼻、电子舌、气相色谱-质谱、质谱代谢组学技术等检测方法,用于食品安全质量分析,特别是食品中特定成分或污染物的追踪[18]. 基于贝叶斯框架的稳定同位素混合模型通过建立同位素指纹、化学指纹等分析食品样品中的稳定同位素比例,实现食品中痕量污染物的溯源. 基于神经网络的稳定同位素混合模型,可以预测出不同品种、产地蜂蜜的地理来源,准确率达90%以上[19]. 针对食品中痕量或微量的化学残留分析,稳定同位素混合模型结合质谱分析技术可检测食物中的残留农药和未公开的添加剂[20],并对其空间分布进一步预测[21],这为食品添加剂的监管提供了技术支撑.
2. ML赋能的 QSAR /Read-Across研究(ML-aided QSAR /Read-Across research)
QSAR是基于化学物分子结构与生物活性/毒性建立的定量关系(图3). 数据集及分子特征描述的限制导致QSAR模型的应用域及泛化能力有限[22],而基于ML/DL的QSAR模型能够完全由数据驱动,数据量越大,模型的预测能力越强. 随着高通量试验的快速发展,大量的测试数据可用于训练深度QSAR模型[23].
随着AI的快速发展,围绕受体相关的关键分子靶点,利用化学物与受体分子交互作用的数据信息,可构建基于ML的QSAR模型[24]. 目前,基于ML/DL的QSAR模型已经用于食品-药物相互作用[25]、受体的结合活性[26-27]、肝脏毒性[28]及其他多种毒性终点的预测[29-30],在食品安全风险评估中显示出巨大应用前景.
ML/DL及QSAR模型常在数据量充足时表现出良好的预测性能,当化学物数据不足时,通常采用Read-Across作为数据缺口填补方法,用于预测目标物质的相同终点[31]. 基于ML的Read-Across工具能够估计所选结构特征的相关性[32],实现小型数据集上的高准确率预测效果. 将Read-Across集成到基于ML的QSAR模型中,通过数据融合为每种化学物质构建基于相似性的大型特征向量,结合QSAR和Read-Across的优点,使用多种相似性规则进行计算和加权,提高了模型的预测效率、可靠性和可解释性[33]. 如定量跨结构活性关系模型,使用最小二乘法消除了描述符之间的关联,且采用了ML方法对超参数进行优化,实现了高准确度的化学物心脏毒性预测[34]. 基于ML的Read-Across方法有助于解决相似性假说的不确定性,提高论据的充分性和可靠性、判断证据权衡结果是否明确已被广泛应用于化学物风险评估[35].
3. 融合分子交互作用特征的ML模型(ML models with molecular interaction features)
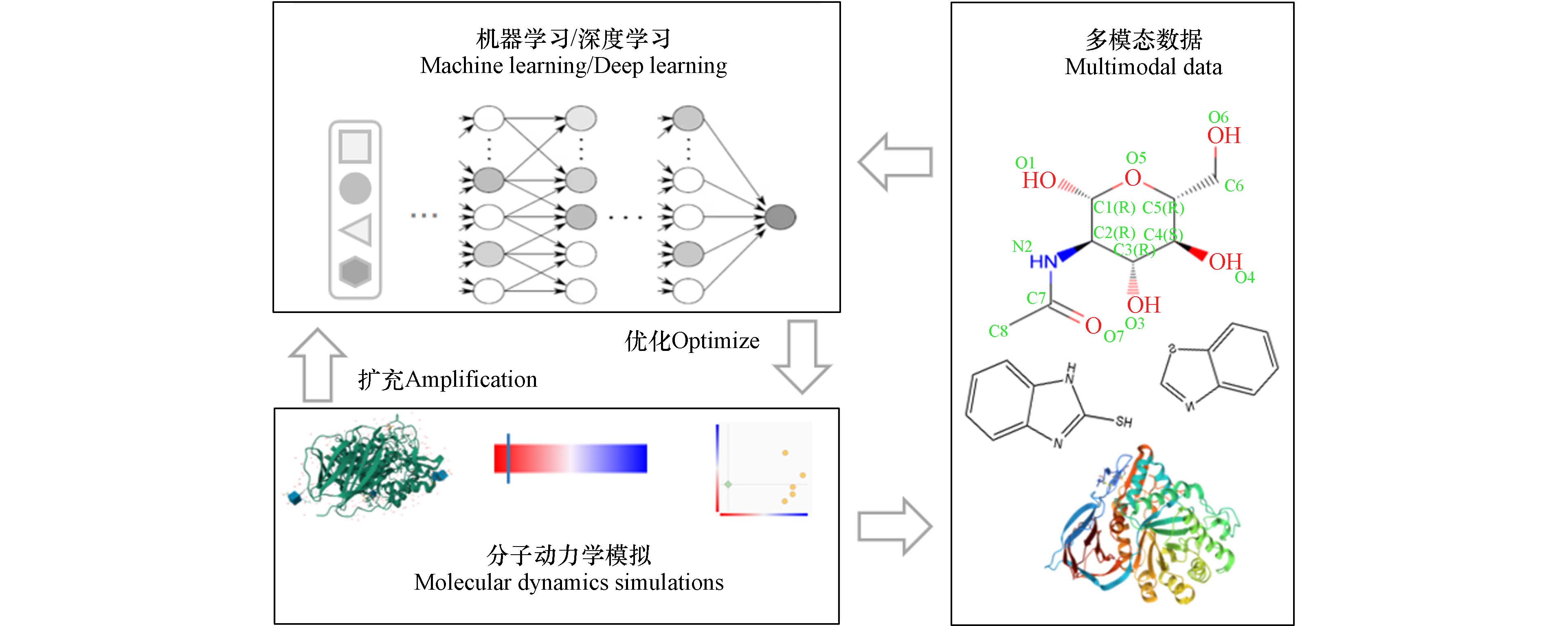
分子动力学(Molecular Dynamics,MD)模拟用于识别化学物质和生物大分子间的动态分子交互作用,为化学物风险评估提供更为全面的相互作用信息[36]. 分子模拟技术由于受到计算资源和算法的限制,精度和效率通常难以兼得,而将ML模型引入到分子动力学模拟中,能够在满足第一性原理精度的同时,计算速度媲美经验式模型,满足快速、低成本且高通量的预测要求(图4).
研究污染物与受体的交互作用有利于从蛋白质分子水平识别分子起始事件(Molecular initiation events,MIE),有利于深入了解MIE、关键事件(Key events,KE)和有害结局(Adverse outcome,AO)的关联,促进深入了解污染物毒性作用机制. 基于ML/DL的蛋白质-配体相互作用预测目前已显示出巨大的潜力[37]. 基于图学习的自适应机器能够适应多类数据集,比传统的分子动力学模拟展现出更好的预测性能[38];基于X射线结构中蛋白质-配体相互作用信息,利用六种图神经网络算法构建的模型准确预测了配体的亲和力[39]. 目前,AlphaFold 3模型在蛋白质-配体相互作用方面的预测性能皆优于其他传统分子模拟方法,能够预测包括蛋白质、核酸和小分子及多种复合物的结构,为化学物和受体相互作用研究提供更加准确全面的受体结构信息. 通过基于ML的原子间相互作用建模对食品成分及添加剂中的分子进行精确模拟,有利于预测由外源化合物暴露导致的内源性小分子的相互作用以及对人体健康的潜在影响[40].
随着大规模计算资源的持续增加,针对大量化学物开展MD模拟逐渐普及[41]. 基于分子交互作用信息,加强多模态数据扩充,构建融合MD重要特征的ML/DL预测模型,成为当前研究的新方法. 强化ML和MD领域之间的联合应用,构建集成式分子模拟及结构预测的综合性平台,将是人工智能与分子物理交叉领域荟萃方法的全新变革.
4. AI辅助的PBK模型(AI-aided PBK model)
PBK模型可根据器官或组织内化学物及其代谢物浓度的时间变化,评估其在人体内的分布,模拟肝脏等代谢转化功能,提供毒物在体内的生物转化数据(图5). 在评估食品安全时,通过化学-生物相互作用的机理获得相关剂量-反应数据,借助PBK模型来预测人体体内的暴露量,最后进行风险表征.
PBK模型广泛用于预测特定人群通过食品摄入化学物质的暴露量,可预测化学物质在动物及人体内的分布和浓度,包括在血液、组织、乳汁等中的水平[42 − 44]. 欧洲食品安全局对食品中全氟烷基化合物对人类健康的风险进行评估时使用了PBK模型[42],能准确预测人类器官浓度-时间曲线、药代动力学行为和化学物的每日摄入剂量. PBK模型还能用于经由膳食摄入的化学物质到人体内浓度的推导[43],如预测乳汁中的化学物暴露,预测目标化合物的母体血浆暴露量和婴儿日摄入量[44].
传统的PBK模型受到动物试验伦理和低通量的限制,难以推广使用. 基于AI建模的下一代PBK模型克服了传统模型的技术瓶颈问题,可广泛应用于高通量化学物风险评估. 基于微生理系统的PBK模型用于皮肤-肝脏-甲状腺模型的开发,通过研究微流体循环连接的“器官”间的相互作用,预测几种典型的化学物在特定器官中的暴露[45],通过由皮肤和肝脏中的代谢及甲状腺激素表征化学物的生物效应. 与普通PBK模型相比,基于AI的PBK模型能够进一步预测器官水平的化学物质暴露,定性及定量描述化学物在体内的生物转化数据. 目前,通过使用计算机模拟、体外和人体生物监测数据对化学物的人体PBK模型进行细化和校准[46],极大促进从机制上理解食品安全风险,并提高预测结果的准确性.
定量危害表征依赖于对体外试验读数的解释,这需基于体外基准浓度将体外浓度-效应数据外推至体内剂量-效应数据,即定量体外-体内外推(Quantitative in vitro to in vivo Extrapolation,QIVIVE),通过体外组学数据预测体内毒性,区别于传统的动物实验,更加符合下一代风险评估的要求. 基于AI的PBK模型整合了关于化学物在人体或生物体中的吸收、分布、代谢和排泄的知识,成为体外-体内外推的有效工具,能够实现跨物种、途径和各种暴露情景预测[47]. 基于深度学习的Deep-PK模型能够识别影响化合物属性的关键分子区域,其在分子层面上的识别和预测性能远超常规的生理动力学模型[48]. 基于人工神经网络并融合化学物质文本描述和结构信息的多模态模型,能够实现同时预测不同物种、组织、测量方法和血液基质的组织-血液分配系数,为化学物内暴露评估提供了有效手段[49]. 将QIVIVE用于化学物的暴露,能够帮助深入理解化学物毒性的分子机制[50].
5. 结论与展望(Conclusions and prospects)
大量人工合成化学物被生产、投入使用并不断产生相关测试新数据,亟需为其开发通用的评估模型. 包括我国在内的很多国家和国际组织正在探索下一代风险评估方法,将整合有关分子系统生物学的信息纳入未来的风险评估范畴. NGCT将海量多模态数据有机整合,可实现对于化学物多种性质的高通量预测,揭示化学物质如何在生物体内引发不良健康效应,为食品安全风险评估提供深层次的机制性理解,能够推动化学物食品安全风险评估研究新范式的建立. 目前大语言模型(Large Language Model,LLM)在提取和整合高通量数据上表现突出,能够处理来自高通量筛选、组学、生物信息学和其他来源的大量复杂数据,其中垂直大模型能够专注于特定领域的数据处理和分析,通过自然语言处理技术更深层次地理解、整合并分析多模态数据,训练数据中的模式和关系,对新化学物的行为进行高精度预测,将促进化学物风险评估的变革性发展. 未来需要进一步结合LLM在自然语言处理、预测分析和决策制定方面的先进能力,提高风险评估的准确性和透明度.
-
图 4 (a)探针Cy-DMTC (5×10−6 mol·L−1)选择性识别实验;(b)探针Cy-DMTC+Hg2+ (5×10−6 mol·L−1)与干扰离子共存实验;(c)探针Cy-DMTC (5×10−6 mol·L−1)的选择性识别及抗干扰性实验的柱状图;(d)探针Cy-DMTC(5×10−6 mol·L−1)识别各种金属离子的荧光变化
Figure 4. (a) Selectivity of probe Cy-DMTC (5×10−6 mol·L−1) towards Hg2+; (b) Fluorescence spectra of Cy-DMTC+Hg2+ (5×10−6 mol·L−1) coexists with interfering metal ions; (c) Histogram of selective recognition and anti-interference experiments with the probe Cy-DMTC (5×10−6 mol·L−1); (d) Fluorescence change for probe Cy-DMTC (5×10−6 mol·L−1) in the presence of various metal ions
图 5 (a)探针Cy-DMTC(5×10−6 mol·L−1)与不同浓度Hg2+ (0—2.0×10−5 mol·L−1)反应后的荧光光谱图;(b)探针Cy-DMTC在512 nm处的荧光强度与Hg2+浓度的变化趋势图
Figure 5. (a) Fluorescence spectra of Cy-DMTC (5×10−6 mol·L−1) with increasing concentrations of Hg2+ (0—2.0×10−5 mol·L−1); (b) Plot of Hg2+ concentration with fluorescence intensity of Cy-DMTC at 512 nm
图 6 (a)探针Cy-DMTC+Hg2+ (5×10−6 mol·L−1)随时间变化的荧光光谱图;(b)探针Cy-DMTC+Hg2+ (5×10−6 mol·L−1)在512 nm处的荧光强度与时间(s)拟合曲线图
Figure 6. (a) Fluorescence spectral changes of probe Cy-DMTC+Hg2+ (5×10−6 mol·L−1) in the presence of Hg2+ over time; (b) Time dependent increase of fluorescence intensities of Cy-DMTC at 512 nm after addition of Hg2+
表 1 探针Cy-DMTC对实际水样中Hg2+的检测
Table 1. Detection of Hg2+ in actual water samples by probe Cy-DMTC
样品Sample 加标量/(μmol·L−1)Hg2+ Add 回收量/(μmol·L−1)Hg2+ Recovery RSD/%(n=3) 回收率/%Recovery 矿泉水Mineral water 0.00 — — — 2.00 1.98 1.21 98.95 5.00 4.97 1.05 99.45 10.00 9.67 1.25 96.75 自来水Tap water 0.00 — — — 2.00 1.99 1.16 99.85 5.00 4.90 1.03 97.93 10.00 10.11 1.12 101.13 湖水Lake water 0.00 — — — 2.00 1.98 1.89 98.93 5.00 5.10 1.73 102.05 10.00 9.61 1.81 96.10 -
[1] WANG Z, LUO P P, ZHA X B, et al. Overview assessment of risk evaluation and treatment technologies for heavy metal pollution of water and soil[J]. Journal of Cleaner Production, 2022, 379: 134043. doi: 10.1016/j.jclepro.2022.134043 [2] PENG J Y, ZHANG S, HAN Y Y, et al. Soil heavy metal pollution of industrial legacies in China and health risk assessment[J]. Science of the Total Environment, 2022, 816: 151632. doi: 10.1016/j.scitotenv.2021.151632 [3] LI Y, ZHOU S L, JIA Z Y, et al. Temporal and spatial distributions and sources of heavy metals in atmospheric deposition in western Taihu Lake, China[J]. Environmental Pollution, 2021, 284: 117465. doi: 10.1016/j.envpol.2021.117465 [4] KAEWNOK N, SIRIRAK J, JUNGSUTTIWONG S, et al. Detection of hazardous mercury ion using [5]helicene-based fluorescence probe with “TurnON” sensing response for practical applications[J]. Journal of Hazardous Materials, 2021, 418: 126242. doi: 10.1016/j.jhazmat.2021.126242 [5] NAFI A W, TASEIDIFAR M. Removal of hazardous ions from aqueous solutions: Current methods, with a focus on green ion flotation[J]. Journal of Environmental Management, 2022, 319: 115666. doi: 10.1016/j.jenvman.2022.115666 [6] WANG Y, ZHANG L, HAN X Y, et al. Fluorescent probe for mercury ion imaging analysis: Strategies and applications[J]. Chemical Engineering Journal, 2021, 406: 127166. doi: 10.1016/j.cej.2020.127166 [7] YUAN Z H, YANG Y S, LV P C, et al. Recent progress in small-molecule fluorescent probes for detecting mercury ions[J]. Critical Reviews in Analytical Chemistry, 2022, 52(2): 250-274. doi: 10.1080/10408347.2020.1797466 [8] TUNSU C, WICKMAN B. Effective removal of mercury from aqueous streams via electrochemical alloy formation on platinum[J]. Nature Communications, 2018, 9: 4876. doi: 10.1038/s41467-018-07300-z [9] HASAN A, NANAKALI N M Q, SALIHI A, et al. Nanozyme-based sensing platforms for detection of toxic mercury ions: An alternative approach to conventional methods[J]. Talanta, 2020, 215: 120939. doi: 10.1016/j.talanta.2020.120939 [10] SU M J, LIU C Y, ZHANG Y, et al. Rational design of a water-soluble TICT-AIEE-active fluorescent probe for mercury ion detection[J]. Analytica Chimica Acta, 2022, 1230: 340337. doi: 10.1016/j.aca.2022.340337 [11] 管怡晗, 黎广进, 刘盛华, 等. 汞离子比色型荧光探针的合成与性质[J]. 环境化学, 2021, 40(8): 2544-2550. doi: 10.7524/j.issn.0254-6108.2020041201 GUAN Y H, LI G J, LIU S H, et al. Synthesis and properties of colorimetric fluorescent probe for mercury ions[J]. Environmental Chemistry, 2021, 40(8): 2544-2550 (in Chinese). doi: 10.7524/j.issn.0254-6108.2020041201
[12] CHEN H J, LI X W, GAO P, et al. A BODIPY-based turn-off fluorescent probe for mercury ion detection in solution and on test strips[J]. Journal of Molecular Structure, 2022, 1262: 133015. doi: 10.1016/j.molstruc.2022.133015 [13] WANG P, XUE S R, CHEN B, et al. A novel peptide-based fluorescent probe for highly selective detection of mercury (II) ions in real water samples and living cells based on aggregation-induced emission effect[J]. Analytical and Bioanalytical Chemistry, 2022, 414(16): 4717-4726. doi: 10.1007/s00216-022-04094-4 [14] MENG A L, ZHANG Y, WANG X H, et al. Fluorescence probe based on boron-doped carbon quantum dots for high selectivity “on-off-on” mercury ion sensing and cell imaging[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2022, 648: 129150. doi: 10.1016/j.colsurfa.2022.129150 [15] LI X Q, CHU D D, WANG J, et al. A dicyanoisophorone-based ICT fluorescent probe for the detection of Hg2+ in water/food sample analysis and live cell imaging[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2023, 295: 122628. doi: 10.1016/j.saa.2023.122628 [16] CUI W L, ZHANG Z H, WANG L, et al. A novel and stable fluorescent probe for tracking Hg2+ with large Stokes shift and its application in cell imaging[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2022, 267: 120516. doi: 10.1016/j.saa.2021.120516 [17] WU Y M, WANG Z L, YANG Y Q. A novel flavonol-based fluorescent probe for rapid detection of Hg2+ and its multi-functional applications[J]. Dyes and Pigments, 2023, 216: 111353. doi: 10.1016/j.dyepig.2023.111353 [18] 孙艳丽, 王芹, 郝亮, 等. 荧光恢复型半花菁荧光探针的构建及其在水样中汞离子检测中的应用[J]. 环境化学, 2022, 41(11): 3756-3765. doi: 10.7524/j.issn.0254-6108.2022042004 SUN Y L, WANG Q, HAO L, et al. Construction of a merocyanine-based turn-on fluorescent probe and its application in the detection of mercury ion in water sample[J]. Environmental Chemistry, 2022, 41(11): 3756-3765 (in Chinese). doi: 10.7524/j.issn.0254-6108.2022042004
[19] 李淑雅, 魏超, 赵晗, 等. 检测汞离子的比色-荧光双通道探针的设计合成及应用[J]. 分析化学, 2023, 51(2): 204-214. doi: 10.19756/j.issn.0253-3820.221199 LI S Y, WEI C, ZHAO H, et al. Synthesis and application of colorimetric and fluorescent dual mode probe for detection of mercury ion[J]. Chinese Journal of Analytical Chemistry, 2023, 51(2): 204-214 (in Chinese). doi: 10.19756/j.issn.0253-3820.221199
[20] WANG L H, CHEN H, ZHANG N N, et al. Reaction-based two novel fluorescent probes for Hg2+ detection using benzothiazole derivatives via ESIPT mechanism in aqueous solution and serum[J]. Tetrahedron Letters, 2021, 64: 152735. doi: 10.1016/j.tetlet.2020.152735 [21] JIANG L, ZHENG T, XU Z X, et al. New NIR spectroscopic probe with a large Stokes shift for Hg2+ and Ag+ detection and living cells imaging[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2022, 271: 120916. doi: 10.1016/j.saa.2022.120916 [22] WONG R C H, LO P C, NG D K P. Stimuli responsive phthalocyanine-based fluorescent probes and photosensitizers[J]. Coordination Chemistry Reviews, 2019, 379: 30-46. doi: 10.1016/j.ccr.2017.10.006 [23] LIU H, YIN J J, XING E Y, et al. Halogenated cyanine dyes for synergistic photodynamic and photothermal therapy[J]. Dyes and Pigments, 2021, 190: 109327. doi: 10.1016/j.dyepig.2021.109327 [24] CHEN H W, XIA H C, HAKEIM O A, et al. Phenothiazine and semi-cyanine based colorimetric and fluorescent probes for detection of sulfites in solutions and in living cells[J]. RSC Advances, 2021, 11(55): 34643-34651. doi: 10.1039/D1RA06868G [25] ZHOU Z, XIA X F, LI Z, et al. An activatable near-infrared fluorescent probe for tracking nitroxyl in vitro and in vivo[J]. Dyes and Pigments, 2023, 209: 110945. doi: 10.1016/j.dyepig.2022.110945 -




 下载:
下载: