-
自上世纪80年代以来,水中的砷(As)污染已被视为最严重的环境健康危害因素之一. 在天然水体中,砷的主要存在形式为无机砷酸盐与亚砷酸盐,也有少量的砷以甲基砷化物等有机砷形式存在[1]. 砷的毒性与其存在形态有关,其中无机亚砷酸盐的毒性最大. 无机亚砷酸盐主要存在于地下水等还原性环境中. 当As污染的地下水被用作饮用水、农业灌溉用水或渔业用水后,人群通过食物链长期接触会导致多种癌症及心血管、免疫、神经、内分泌问题的发生率增加[2]. 据估计,全球有
9400 万至2.2亿人可能受高浓度As污染地下水影响,其中绝大多数(94%)在亚洲[1]. 在中国,有近2000万人存在As污染饮用水暴露风险[3]. As的慢性毒性没有阈值,应尽可能地减少其摄入,在使用As地下水之前进行处理,是降低其健康风险的最可行和最佳策略[4].吸附是成本效益高且操作方便的除砷技术. 铁基材料,包括磁铁矿氧化物[5]、赤铁矿氧化物[6]、零价铁[7 − 8]、施氏矿物[9]、铁与其他金属的复合氧化物[10 − 12]及各种载体材料负载的铁氧化物[13 − 15]等,常被用作水体As吸附剂. 其中,纳米级吸附剂尤其受青睐,因为其较大的比表面积和表面活性,对As具有较大的吸附容量和吸附速率[16]. 近年来,磁性纳米氧化铁吸附剂引起了研究人员的广泛关注[17 − 18]. 磁性吸附剂在使用后,可以在外加磁场的作用下,非常便利地从水中分离. 典型的磁性氧化铁包括Fe3O4和γ-Fe2O3等. 研究人员发展了多种磁性纳米氧化铁的制备方法,如NaBH4还原[19]、金属有机物热分解[20]和羰基铁蒸气氢火焰燃烧[21]等,这些方法需要用到特殊原料,或者制备条件苛刻,需要用到特殊设备等. 简单和低成本的磁性纳米铁基吸附剂制备方法是研究开发的方向之一.
本研究的目的是开发简单的乙酸盐热分解法制备磁性纳米氧化铁,探究制备条件对材料结构的影响,并揭示材料对地下水中常见的亚砷酸盐形态砷(As(III))的吸附性能.
-
乙酸铁(含铁量18%—22%)购自武汉市伟琪博星生物科技有限公司,亚砷酸钠购自成都艾科达化学试剂有限公司,其余试剂产自国药化学试剂公司.
-
将10 g乙酸铁分别在空气和氮气中于250 ℃焙烧2 h,得到的样品分别命名为FeAc-A和FeAc-N. 其中焙烧时的升温速率为10 ℃·min−1,在空气中焙烧是在马弗炉中进行,在氮气中焙烧是在管式炉中进行且氮气气体流量为30 mL·min−1.
-
X射线衍射(XRD)在X射线衍射仪(荷兰PANALYTICAL)上测定,使用铜靶光源,其中XRD的扫描范围为10°—80°,扫描速率为10°·min−1. 透射电镜(TEM)图在JEM-2100F型透射电子显微镜(日本JEOL)上获得. BET比表面积用V-sorb 2800P型比表面积与孔径分析仪(北京金埃谱)测定,样品测定前在300 ℃真空中脱气2 h. 磁化曲线用
7404 型振动样品磁强计(美国LakeShore)测定. -
用稀HCl或稀NaOH溶液将一定浓度的亚砷酸钠溶液调至一定的pH值,取10 mL该溶液加入到25 mL的螺口样品瓶中,加入4 mg吸附剂,盖紧瓶盖后,在摇床上振荡10 h(25 ℃,250 r·min−1)确保达到吸附平衡,离心后,测上清液中As的浓度.
-
不同初始As浓度(1—50 mg∙L−1)吸附实验,以吸附剂的平衡吸附量对溶液中As的平衡浓度作图,得到As的吸附等温线. 分别用Langmuir模型和Freundlich模型进行吸附等温线数据拟合.
Langmuir模型描述了匀质表面的单层吸附行为,其线性表达式如式(1)所示[22 − 23]:
式中,Ce(mg∙L−1)和Qe(mg∙g−1)分别指溶液中As的平衡浓度和吸附剂对As的平衡吸附量,Qm(mg∙g−1)是最大吸附容量,b(L∙mg−1)是吸附常数,与吸附能有关.
Freundlich模型描述了非匀质表面的多层吸附行为,其线性表达式如式(2)所示[22 − 23]:
式中,Ce(mg∙L−1)和Qe(mg∙g−1)分别指溶液中As的平衡浓度和吸附剂对As的平衡吸附量,Kf(mg·g−1)与吸附容量有关,常数n与吸附强度有关并反映了浓度对吸附的影响.
根据Langmuir模型中的吸附平衡常数b(L∙mol−1),可以依据式(3)计算吸附过程的吉布斯自由能变化量:
式中,ΔG°(kJ∙mol−1)是吸附过程的吉布斯自由能变化量,R是通用气体常数(8.31 J∙mol−1∙K−1),T是吸附发生时的温度(K). 如果ΔG°小于0,说明吸附是自发的.
-
在一系列25 mL的样品瓶中各加入6 mg吸附剂,然后各加入10 mL浓度为10 mg∙L−1的亚砷酸钠溶液,将溶液pH调为7,放在摇床上(25 ℃,250 r·min−1),在不同设定时间取出一个样品瓶,测定溶液中As的浓度,即可计算得到反应不同时间后的吸附量,分别用准一级动力学模型和准二级动力学模型进行数据拟合.
准一级动力学模型与准二级动力学模型的公式分别如式(4)与式(5)所示[19 − 20]:
式中,Qe(mg∙g−1)和Qt(mg∙g−1)分别为达到吸附平衡时和吸附时间为t时吸附剂对砷的吸附量,k1(min−1)代表准一级动力学吸附速率常数,k2(g∙mg−1∙min−1)为准二级动力学吸附速率常数.
为明确扩散过程对吸附的影响,用颗粒内扩散模型(Webber-Morris模型)对吸附动力学数据进行拟合,表达式如式(6)所示[22 − 23]:
式中,Qt(mg∙g−1)为吸附时间为t(min)时吸附剂对As的吸附量,kp(mg∙g−1∙min−0.5)为内扩散速率常数,c(mg∙g−1)反映了边界层对吸附速率的影响. 如果Qt对t0.5作图所得曲线是通过原点的直线,则内扩散是决速步;如果不过原点,内扩散不是唯一的决速步. 常数c的值越大,则边界层的扩散速率对吸附速率的影响也越大.
-
采用氢化物发生-原子荧光法(HJ 694—2014)在AFS-
8220 型原子荧光光度计(北京吉天仪器)上测定上清液中残留As的浓度,根据式(7)计算吸附剂对As的平衡吸附量,根据式(8)计算吸附剂对As的去除率. -
图1是吸附剂的TEM图. FeAc-N由较小的纳米颗粒组成,且粒径分布范围窄,多数颗粒的粒径为10—12 nm. 相比之下,FeAc-A的粒径较大,且分布范围宽,多数为20—50 nm. FeAC-A的颗粒表现出更显著的棱角分明的晶体特征. 在空气中焙烧时,有机配体氧化释放出大量热,不可避免造成样品局部温度过高,发生烧结团聚,生长成较大的晶体粒子,因此,FeAc-A的粒径较大.
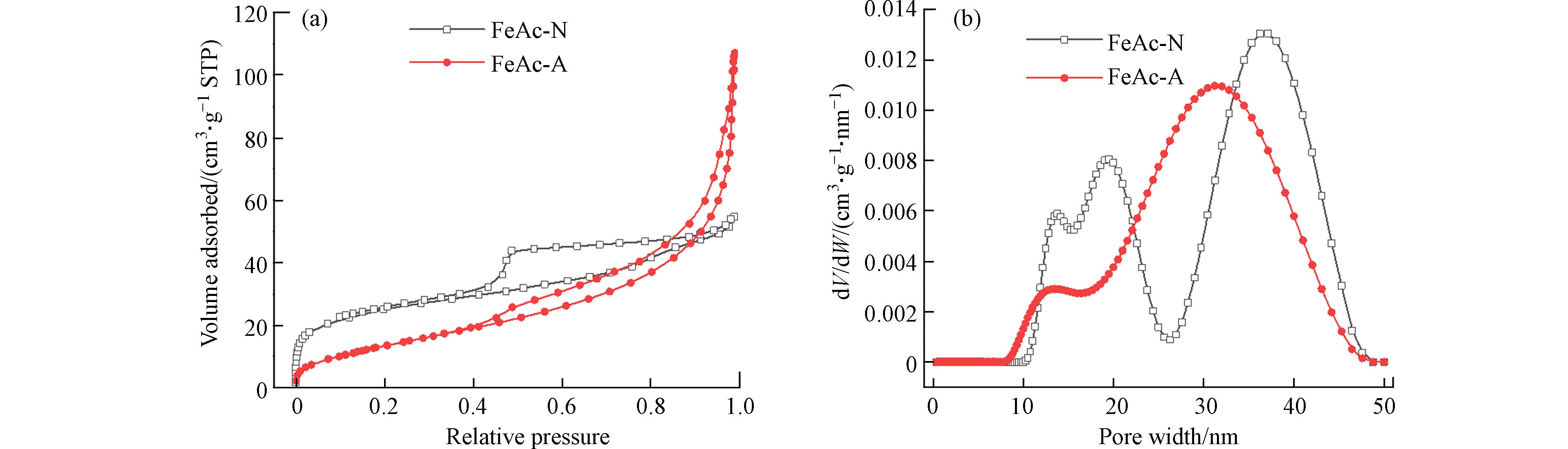
N2吸附-脱附等温线和NLDFT孔径分布曲线如图2所示. 两个材料的等温线都有显著的迟滞环,表明具有介孔结构. 而且,N2的吸附量随着相对压力的提高一直增加,在最高相对压力处也没有出现饱和平台,表明了材料的颗粒堆积孔特征[24]. 孔径分布曲线表明,主要孔径分布位于10—50 nm介孔范围内,微孔很少. 较大的孔径可归因于颗粒堆积的间隙较大,这是纳米颗粒组成的材料的特征. 测得的FeAc-N和FeAc-A的BET比表面积分别为90 m2∙g−1和53 m2∙g−1,这与TEM观察的结果一致,FeAc-N的粒径较小,因此暴露出更多的表面积.
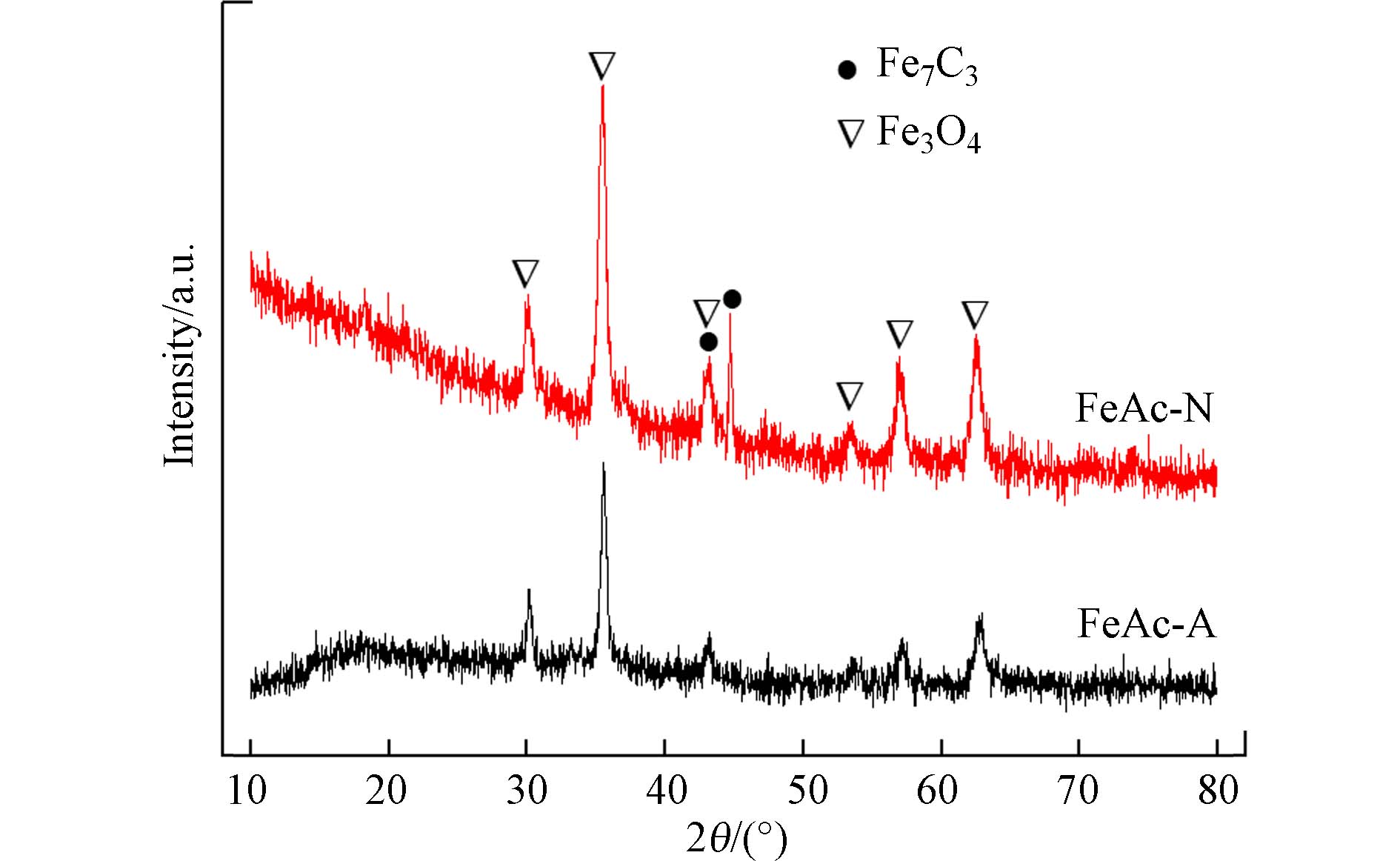
图3为吸附剂的XRD图谱. FeAc-A的衍射峰与磁铁矿相Fe3O4(JCPDS No.19-0629)的特征峰一致,且没有其他物相的显著衍射;而FeAc-N中除了含有Fe3O4外,在42.6°和44.9°处的微弱衍射峰归属于六方相Fe7C3(JCPDS No.17-0333),表明FeAc-N还含有Fe7C3. 在N2氛围下热分解乙酸铁,乙酸根配体作为碳源,生成了部分碳化物.
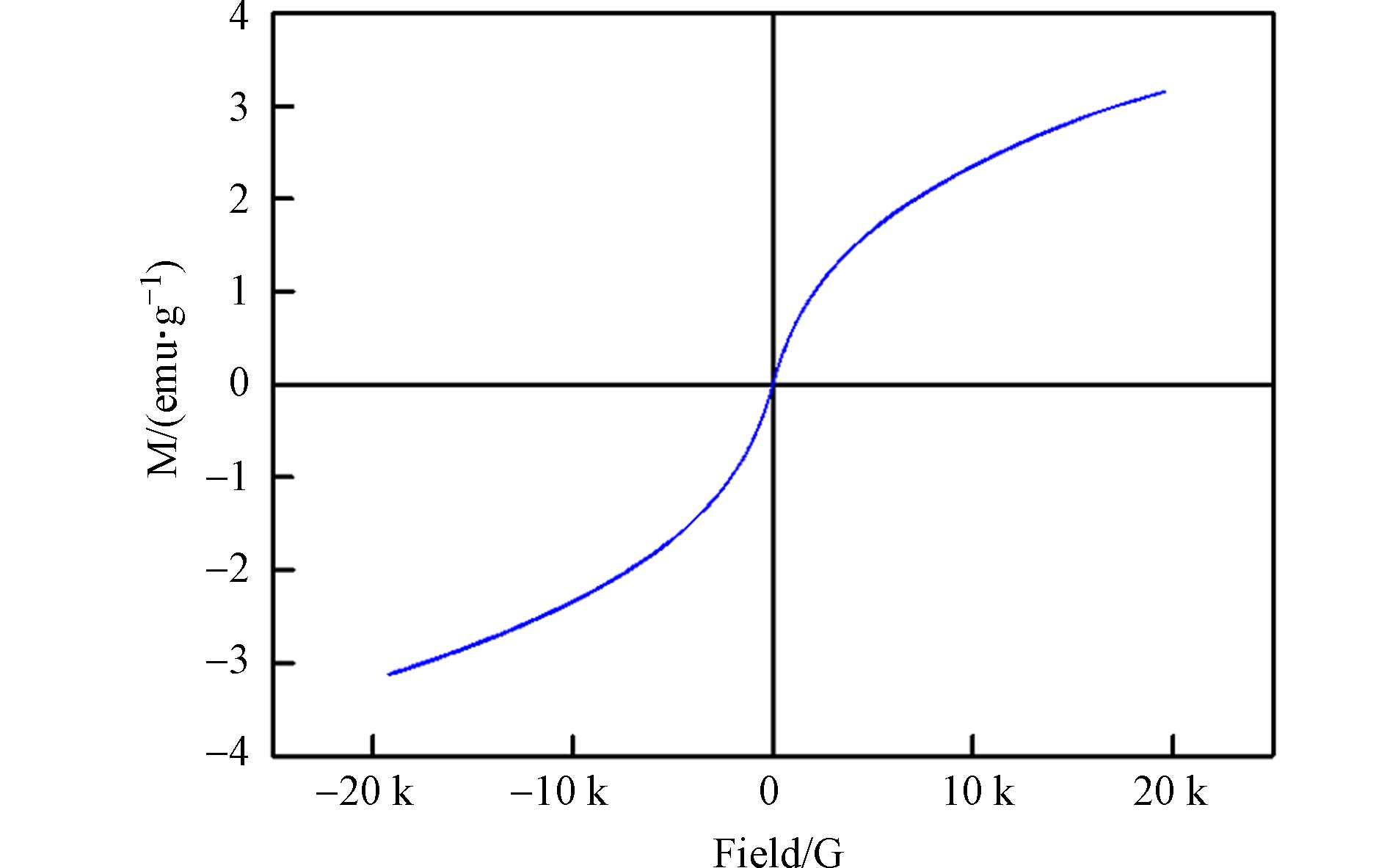
图4为FeAc-N的磁化曲线及退磁曲线. 退磁曲线和磁化曲线几乎重合,没有出现磁滞环,矫顽力和剩磁为零,说明样品具有超顺磁性,这是纳米磁性颗粒的特征[17,25]. 磁铁矿相Fe3O4的存在,使得材料可以对外部磁场做出响应,在水中作为吸附剂使用后,可以用外加磁场进行分离[22].
-
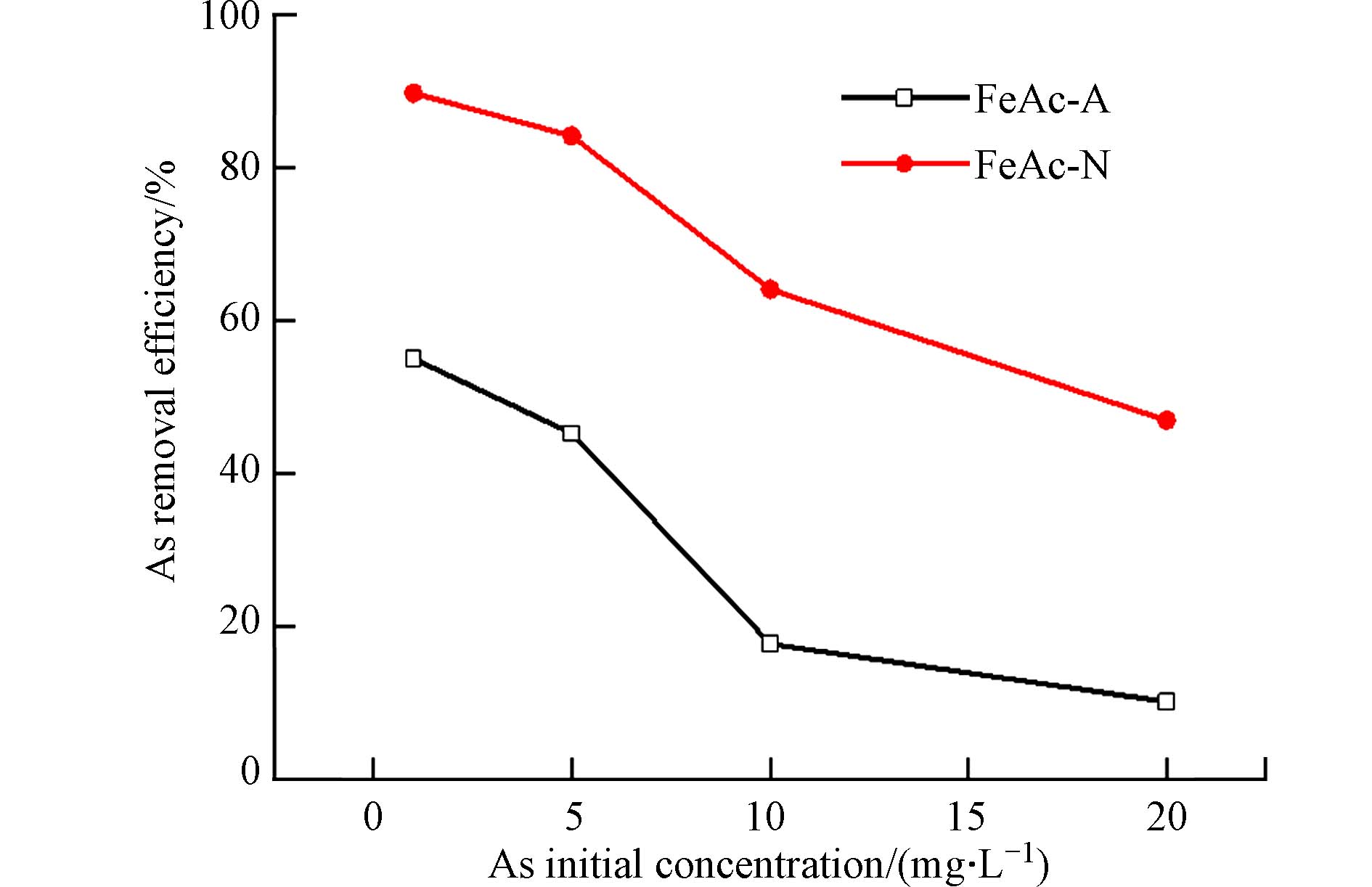
图5为中性条件、不同的As初始浓度下,0.4 g∙L−1的FeAc-N和FeAc-A对As的去除率. FeAc-N对As的去除率显著高于FeAc-A,这归因于前者具有更高的比表面积. 因此,选择FeAc-N进一步进行吸附性能研究.
-
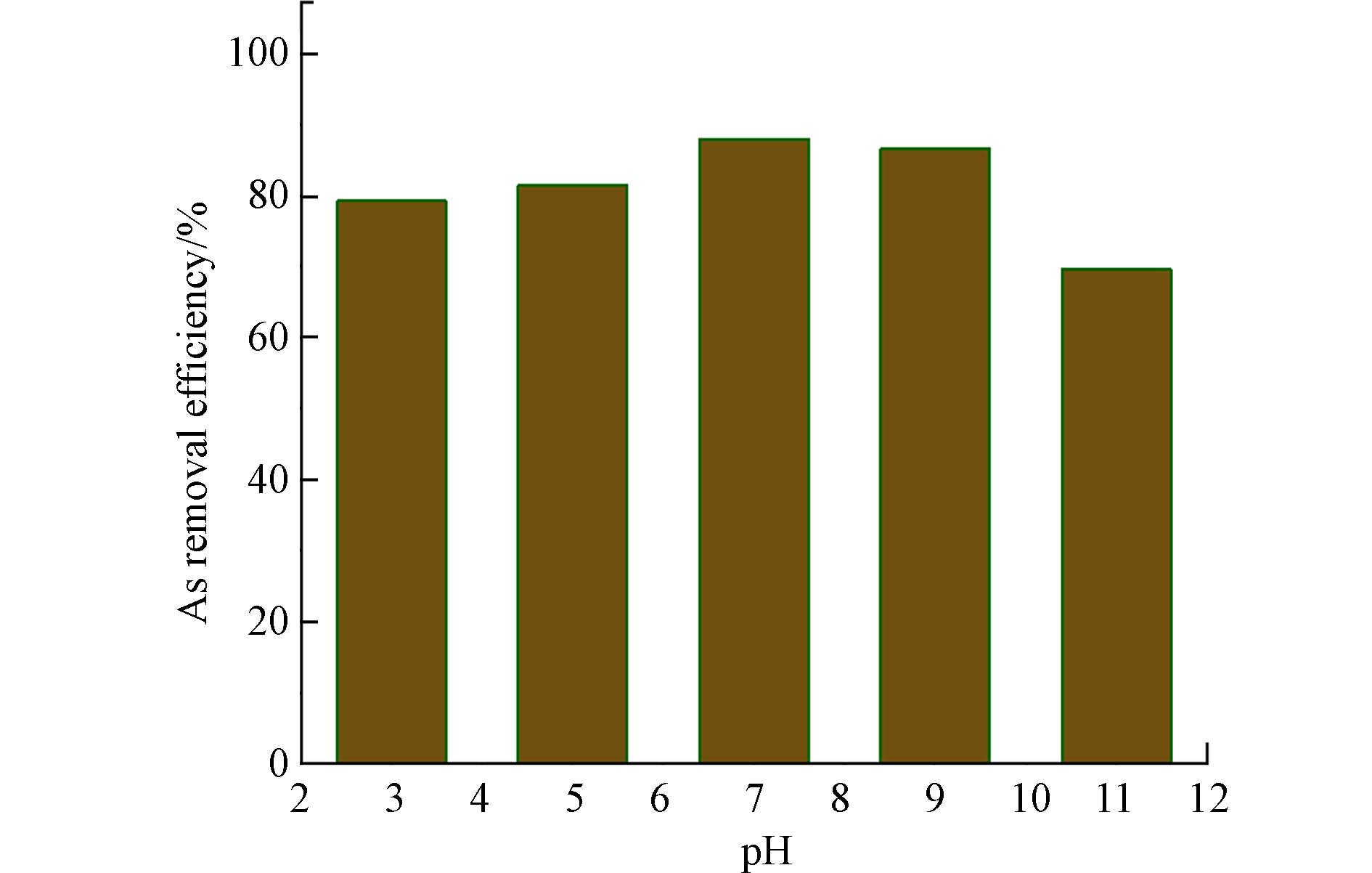
图6为不同pH下FeAc-N对As的去除率. 在pH 7时,去除效果最好. 研究表明,As的去除效率与吸附剂的表面化学和As的形态密切相关. H3AsO3的pKa为9.2,当pH < 9.2时,As主要以H3AsO3分子的形态存在,而当pH > 9.2时,H2AsO3−则成为主要的形态[19 − 20]. Fe3O4的等电点约为pH 6.5[26],在过高的pH下,Fe3O4表面发生去质子化而使净电荷为负,与H2AsO3−存在静电斥力,因而不利于As吸附. Goldberg等[27]总结了氧化铁和砷表面的羟基在吸附过程中形成内层络合物的表面反应过程,如式(9)和(10)所示. 在这些反应式中,氧化铁表面的羟基和砷分子的羟基参与了表面配位反应. 在等电点附近,吸附剂表面存在最多的电荷中性的表面羟基,这可能是pH 7时As的去除率最高的原因,先前研究中也观察到类似的现象[22].
-
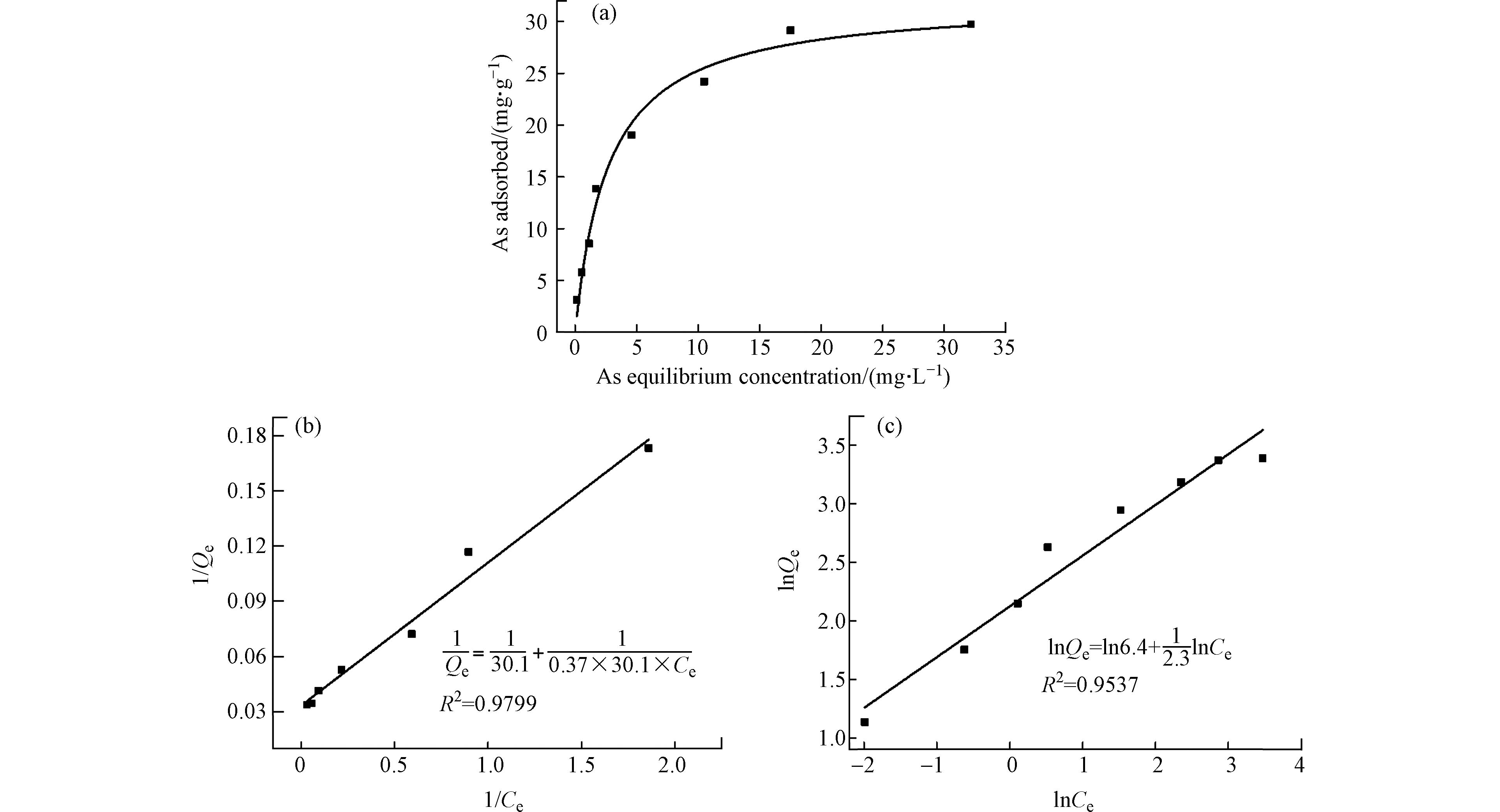
图7为pH 7、25 ℃条件下As在FeAc-N上的吸附等温线以及Langmuir和Freundlich等温线模型拟合.
等温线(图7a)显示,FeAc-N对As(Ⅲ)的最大吸附量约30 mg∙g−1. 对比两种等温线模型拟合的相关系数(R2),Langmuir模型(图7b)比Freundlich模型(图7c)的拟合度更高,说明Langmuir模型能更好的描述FeAc-N对As(Ⅲ)的吸附,即As吸附为单层吸附. 从Langmuir模型预测的FeAc-N对As的最大吸附量是30.1 mg∙g−1,与从等温线观察到的数据吻合.
Langmuir模型中As的吸附平衡常数b为0.37 L∙mg−1(即2.8 × 104 L∙ mol−1),根据公式(3)计算得到的As在FeAc-N上吸附的ΔG°为−25.5 kJ∙mol−1,该值为负值,说明吸附是不需要消耗外部能量的自发过程.
-
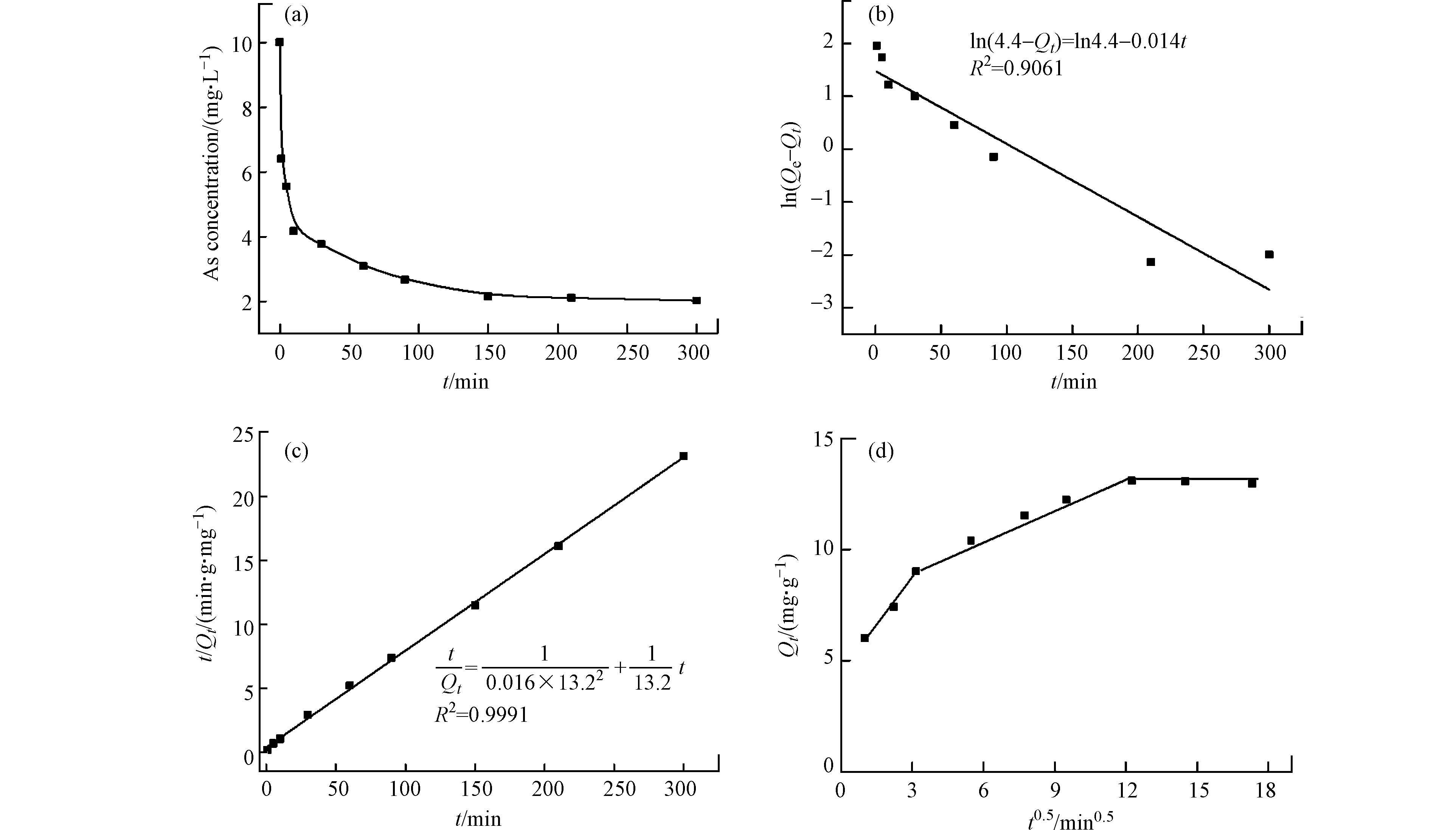
图8a是批吸附实验过程中As的浓度随时间的变化情况. 在前10 分钟,As浓度迅速下降,随后浓度下降速率变缓,约150 min后,浓度不再改变,达到吸附平衡. 图8b与图8c分别是动力学数据的准一级模型和准二级模型拟合的结果. 根据拟合的相关系数(R2),准二级动力学模型能更好的描述As在FeAc-N上的吸附动力学,符合准二级动力学常被当作化学吸附发生的标志[22 − 23]. 对于As在氧化物表面的吸附,砷酸分子与表面羟基之间发生配体交换形成内层络合物是常见的吸附机制(如式7和式8所示),该过程伴随中心原子配位水分子(羟基)的失去,为化学过程.
图8d为用颗粒内扩散模型对吸附动力学数据进行拟合的结果. 颗粒内扩散模型的拟合通常可以分为3个阶段,第一阶段的斜率较大,反映了吸附质被吸附到吸附剂外表面的过程,即As扩散到吸附剂的外表面快速占据表面吸附位点,对应吸附动力学曲线的前10 min(图8a),这个阶段中吸附质分子在边界层的扩散是决速步;第二阶段反映了吸附质被吸附到吸附剂内表面的过程,即As扩散到吸附剂的孔道中,对应吸附动力学曲线上As浓度缓慢下降阶段(图8a),这个阶段颗粒内扩散是决速步;第三段与X轴平行,表示吸附剂的外表面和内部孔道都占据了吸附质,吸附过程已达到平衡. 在本研究中,颗粒内扩散拟合曲线不过原点,说明As在FeAc-N上吸附过程中,颗粒内扩散不是唯一的决速步. 如前所示,FeAc-N有纳米颗粒堆积而成的较大孔,因而内扩散阻力小,这也是纳米吸附剂在应用中的优点之一[16].
-
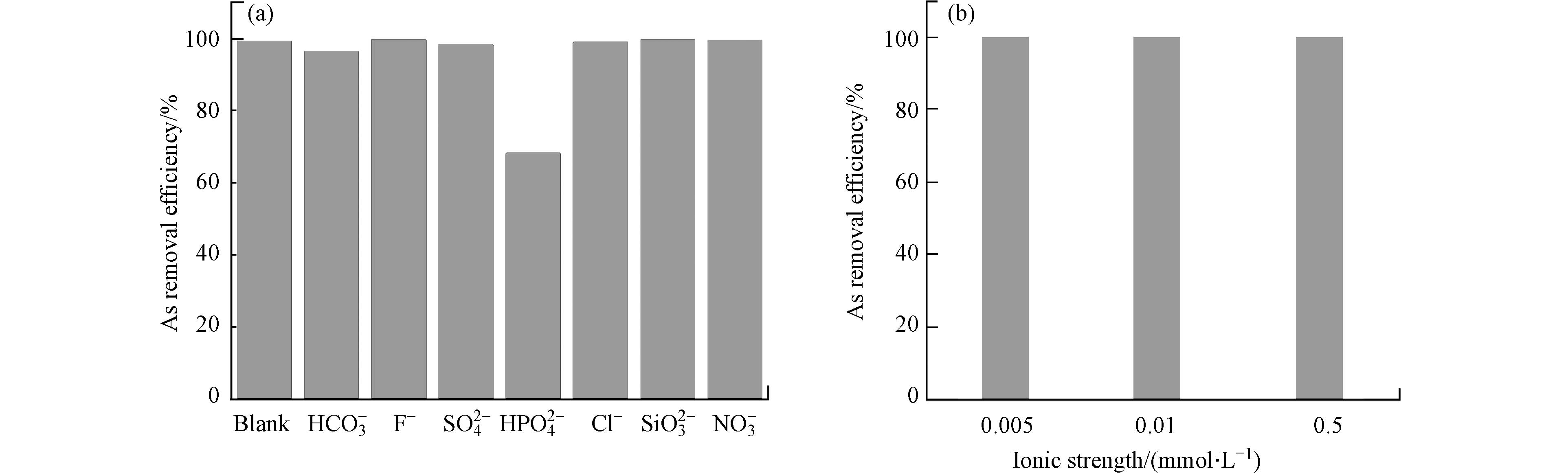
As污染的地下水中通常存在其他共存阴离子,其可能会与As竞争吸附剂表面的位点,从而抑制As的去除. 本工作中还研究了共存离子对吸附性能的影响. 向1 mg∙L−1(0.013 mmol∙L−1)的As溶液中加入1 mmol∙L−1的共存电解质,包括Na2SO4、NaHCO3、NaCl、Na2SiO3、NaF、Na2HPO4、NaNO3等,再开展批吸附实验(FeAc-N剂量0.6 g∙L−1),结果如图9a所示. 虽然共存离子的浓度远高于As的浓度,HCO3−、F−、SO42−、Cl−、SiO32−、NO3−等对As吸附几乎没有影响,只有HPO42−将As(Ⅲ)的去除率从99.1%降低到68.1%. P和As都位于元素周期表的第七主族,它们的离子形态相似,因此存在较强的竞争性吸附. 尽管如此,As的去除率仍然接近70%. 在地下水中,共存离子浓度不会远远超过As的浓度,因此不会严重干扰FeAc-N对As的吸附.
本工作也研究了离子强度对As吸附的影响. 向As溶液中加入5—500 mmol∙L−1的NaNO3,再开展批次吸附实验,结果如图9b所示. 离子强度的增加对砷的去除率没有影响. 离子强度会降低静电吸附形成的外层络合物的稳定性,但是不会减弱内层化学吸附[22 − 23]. 因此,离子强度的影响实验也表明,As在FeAc-N表面的吸附机制是通过表面化学配位形成了内层络合物.
-
通过在250 ℃焙烧乙酸铁,可以简单快捷的制备得到磁性纳米氧化铁,尤其是在氮气氛围下焙烧得到纳米颗粒粒径约10—12 nm,材料的BET比表面积约90 m2∙g−1,颗粒堆积孔较大,主要孔径分布在10—50 nm. 将材料用于水体中As的吸附,在pH 3—9范围内都有较好的去除率,其中在pH 7下的效果最好. 吸附等温线符合Langmuir模型,最大吸附量约30 mg∙g−1. 吸附动力学符合准二级模型,吸附机制为表面化学配位,离子强度对吸附没有影响. 水中的常见共存离子对As的吸附没有显著影响. 本论文方法制备的磁性纳米氧化铁有望作为低成本的水体除砷材料.
乙酸铁热分解制备磁性纳米氧化铁及对砷的吸附性能
Preparation of magnetic nano iron oxide by thermal decomposition of ferric acetate and its adsorption performance for arsenic
-
摘要: 磁性纳米氧化铁可以高效吸附去除水体中的砷(As),且可通过外加磁场进行分离,但是材料的制备过程一般较复杂. 本研究通过简单的乙酸铁热分解法制备了磁性纳米氧化铁,对其进行了表征,并通过批次吸附实验探究了其对As的吸附性能. 在氮气氛围中250 ℃热分解乙酸铁,得到的纳米颗粒粒径约10—12 nm,材料的BET比表面积约90 m2∙g−1,主要孔径分布为10—50 nm,为颗粒堆积孔结构. 材料在pH 3—9范围内都能高效去除水体中的As,其中在pH 7下的效果最好. 吸附等温线符合Langmuir模型,最大吸附量约30 mg∙g−1. 吸附动力学符合准二级模型,吸附机制为表面化学配位形成内层络合物,离子强度对吸附没有影响. 地下水中的常见共存离子对As的吸附没有显著影响. 乙酸铁热分解法可作为制备磁性纳米铁基除砷吸附剂的低成本方法.Abstract: Magnetic iron oxide nanoparticles can efficiently adsorb and remove arsenic from water, and can be separated by an external magnetic field. However, the preparation process of the material is generally complicated. In this study, magnetic iron oxide nanoparticles were prepared using a simple thermal decomposition method, and characterized with different techniques, and then their adsorption performance for As were investigated. The study showed that ferric acetate thermal decomposition at 250 ℃ under a nitrogen atmosphere produced nanoparticles with a particle size of about 10—12 nm. The BET specific surface area of the material is approximately 90 m2∙g−1, with a predominant pore size distribution of 10—50 nm, and possessing a particle aggregate pore structure. The synthesized adsorbents can efficiently remove As from water in the pH range of 3—9, with the best performance achieved at pH 7. The adsorption isotherm fits the Langmuir model, with a maximum adsorption capacity of approximately 30 mg∙g−1. The adsorption kinetics follow the pseudo-second order model, and the adsorption mechanism involves surface chemical coordination to form an innersphere complex, which is not affected by ionic strength. The common co-existing ions in groundwater have no significant effects on As removal. The ferric acetate thermal decomposition method can serve as a low-cost method for preparing magnetic iron-based arsenic adsorbents.
-
Key words:
- arsenic /
- nano iron oxide /
- magnetic adsorbent /
- water purification /
- adsorption.
-
目前,我国大气复合污染形势依然严峻,挥发性有机物(VOCs)排放量仍呈增长趋势[1-2],重点地区年排放量超过1×107 t[3-4]。2018年,我国打赢蓝天保卫战3年行动计划和“十三五”挥发性有机物污染防治工作方案要求实施VOCs专项整治活动,明确提出从源头控制VOCs的排放,大力发展水性涂料行业,推广水性涂料使用。但水性涂料使用过程会产生乙二醇乙醚有机废气[5],而乙二醇醚类废气具有血液毒性、生殖毒性、肝肾毒性、发育毒性和致畸毒性等[6],因此,研究水性涂料喷涂有机废气治理具有十分重要的现实意义。
生物法具有无二次污染、运行费用低等优点,近年来已逐步被应用于有机废气处理,而新型膜生物反应器[7](membrane biofilm reactor, MBfR)将膜分离技术与生物降解作用相结合,既充分利用纤维膜材料较大的比表面积作为气液吸收的传质界面和微生物附着,又可增强有机污染物的降解效果[8],在处理VOCs方面备受青睐。聚偏氟乙烯中空纤维膜生物反应器能有效处理二甲苯、乙酸乙酯单一废气以及双组分有机废气[9-10],乙酸乙酯废气[11]最大去除能力达225 g·(m3·h)−1;复合型平板膜生物反应器净化甲苯废气[12],可增强甲苯的生物降解[13];利用Pseudomonas putida为菌种挂膜的中空纤维膜生物反应器处理甲苯,通过中空纤维膜提高了氧的传质能力,能承受更高的负荷[14]。
膜生物反应器广泛应用于处理疏水性单一废气以及双组分有机废气方面,但用此技术处理水性涂料喷涂过程中产生的乙二醇乙醚有机废气鲜有报道。本研究采用膜生物反应器处理乙二醇乙醚有机废气,研究各种因素对去除效率的影响;通过16S rRNA和宏基因组测序技术研究反应器内微生物群落结构与功能,以期为膜生物反应器处理乙二醇乙醚废气的实际应用提供参考。
1. 材料与方法
1.1 实验原料
气相色谱(GC-1690,杭州捷岛科学仪器有限公司);玻璃转子流量计(LZB-3WB,余姚市舜寰流量仪表有限公司),pH计(pHB-3型,上海三信仪表厂)。
磷酸二氢钾(KH2PO4)、磷酸氢二钾(K2HPO4)、硫酸镁(MgSO4)、蛋白胨、氯化钠(NaCl);超纯氮气(N2,99.999 9%);实验室所用污泥取自广东省某生活污水处理厂的厌氧池和好氧池,接种的微生物类型有芽孢杆菌、陶厄氏菌属、噬氢菌属、蛭弧菌属等。
1.2 实验装置
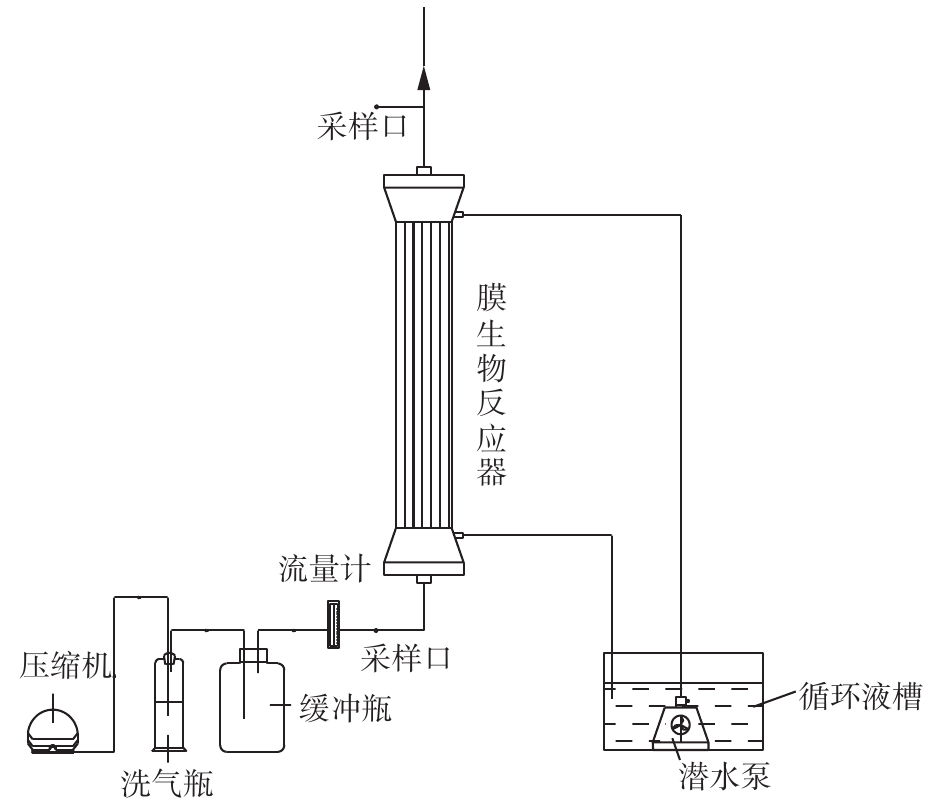
膜生物反应器处理乙二醇乙醚有机废气的实验装置流程如图1所示。膜生物反应器内膜组件为聚丙烯(PP)中空纤维膜,纤维内径为0.38 mm,外径为0.50 mm,纤维膜数量为2 400根,有效长度为300 mm,反应器有效体积为90 mL,废气处理量为0.1~0.6 L·min−1。乙二醇乙醚气体采用动态法配制,乙二醇乙醚经孟氏洗瓶后和压缩空气进入到缓冲瓶混合,混合后的气体从膜生物反应器底部进入,由膜内扩散传质至膜外的生物膜表面,与湿润生物膜接触被微生物降解,净化后的气体从反应器顶部排出;循环液体从顶部向下喷淋,在中空纤维膜外流动,由底部排出至循环液储槽。
1.3 实验方法
在膜生物反应器180 d的运行期间,每天采用气相色谱仪测定进出气中乙二醇乙醚浓度。在研究喷淋量和pH影响因素时,每次调整运行参数运行3 d后,监测进出气中乙二醇乙醚浓度;在研究气体停留时间和进气浓度影响因素时,每次调整运行参数运行1 d后,监测进出气中乙二醇乙醚浓度。定期向循环液槽中投加氮磷营养液。
1.4 分析方法
采用气相色谱测定乙二醇乙醚浓度,具体分析方法为:采用5%苯基-1%乙烯基聚甲基硅氧烷交联毛细管柱,初始柱温为100 ℃,升温速率为10 ℃·min−1,保持5 min;进样口温度为270 ℃,检测器温度为240 ℃,采用氢火焰离子化检测器检测;采用pHB-3型pH计测定循环液pH;采用16S rRNA技术分析第30、90、145天反应器内微生物群落结构;采用宏基因组测序技术分析反应器内微生物的功能基因。
2. 结果与讨论
2.1 膜生物反应器运行稳定性
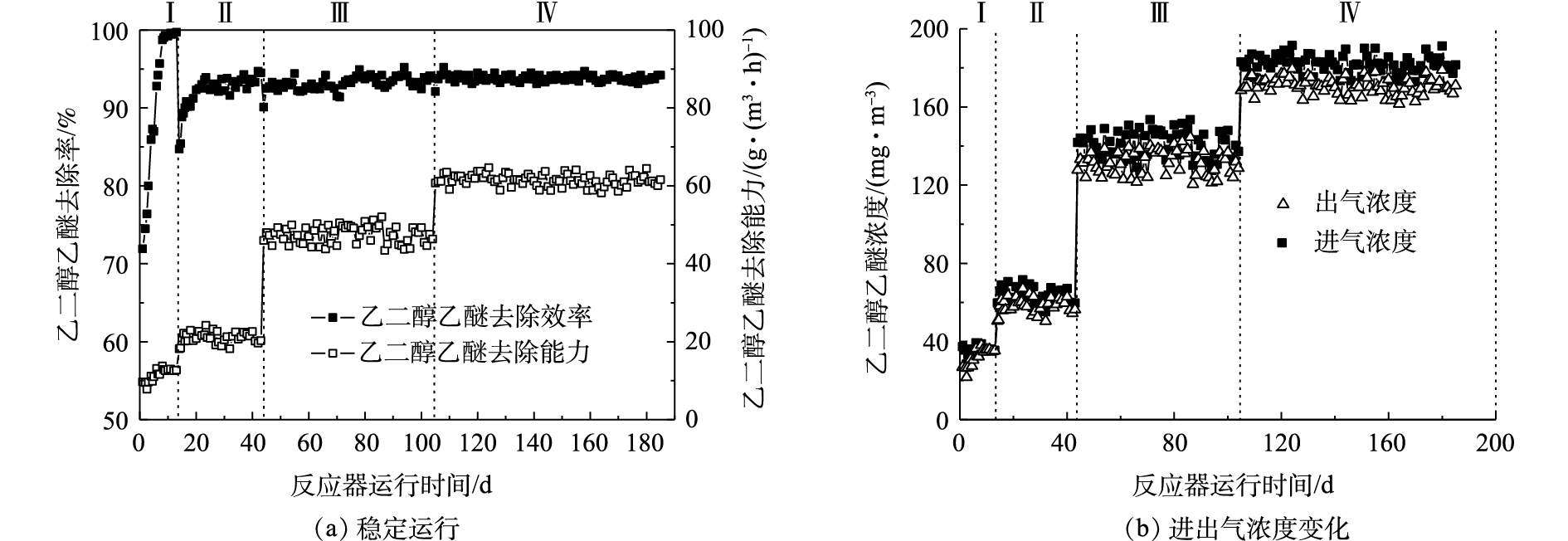
在气体停留时间为10 s、乙二醇乙醚进气浓度为35.0~200.0 mg·m−3、循环液pH为6.00~8.50、喷淋量为0.2~1.8 m3·(m2·h)−1的条件下,膜生物反应器处理乙二醇乙醚的运行稳定性如图2(a)所示,进出气浓度随时间变化如图2(b)所示。在膜生物反应器系统运行初期(1~13 d),进行低浓度(40.0±5.0) mg·m−3驯化。由于聚丙烯中空纤维膜高效分离和膜基水吸收乙二醇乙醚的作用,第1天乙二醇乙醚的去除率可达71.9%,随着纤维膜表面附着的微生物逐渐形成生物膜,第13天上升至99.0%。在驯化适应期(14~43 d),将进气浓度提高到(60.0±10.0) mg·m−3,乙二醇乙醚去除率先下降,再由84.7%升至94.0%,平均去除负荷为20.9 g·(m3·h)−1。为提高反应器抗冲击负荷能力,第44天将进气浓度增加到(140.0±10.0) mg·m−3,乙二醇乙醚去除率由92.2%下降至90.1%,然后升至93.8%,60 d的平均去除负荷达49.1 g·(m3·h)−1。这表明膜生物反应器具有抗冲击负荷的能力。为考察高负荷承受能力,第105天将乙二醇乙醚浓度提高到(180.0±10.0) mg·m−3,乙二醇乙醚去除率由93.8%下降至92.1%,第106天迅速恢复到93.7%,以后79 d维持稳定在94.0%左右。这表明膜生物反应器具有较强的抗冲击负荷能力和良好的稳定性。
2.2 进气浓度和停留时间的影响
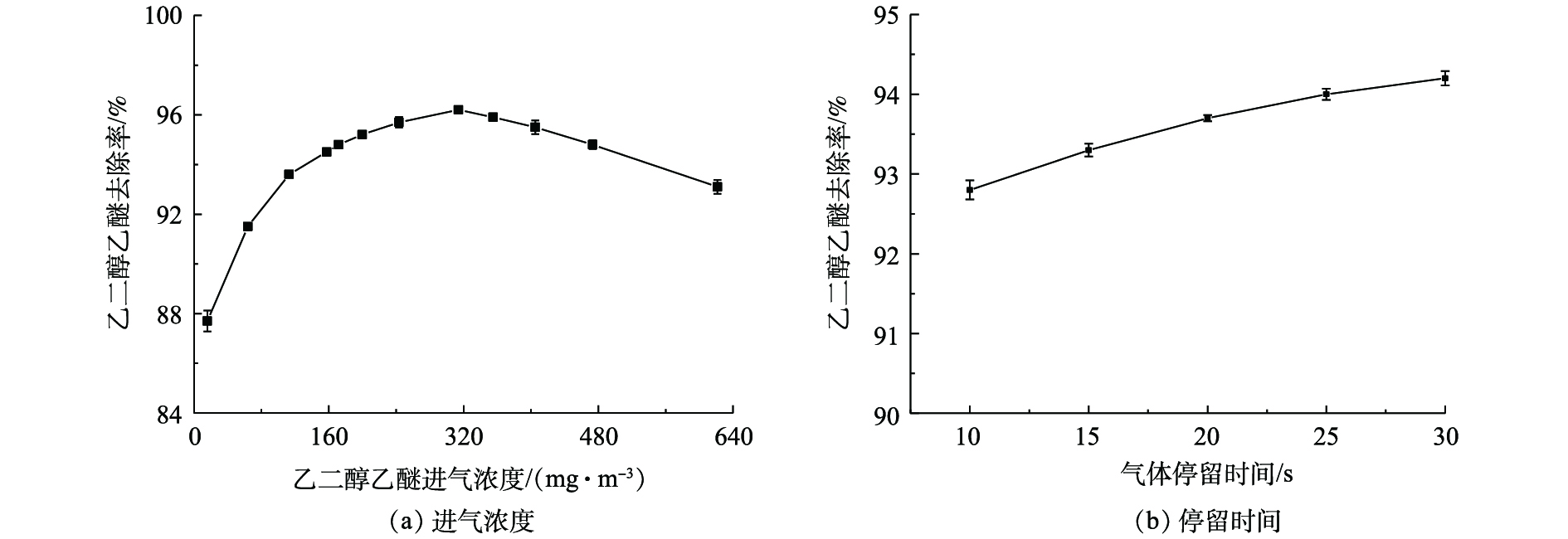
由图3(a)可知,在气体停留时间为10 s、循环液pH为7.65、喷淋量为1.3 m3·(m2·h)−1的条件下,随着进气浓度增加,乙二醇乙醚的去除率先升高后下降,由87.7%升至96.2%,再下降至93.1%;进气浓度为314.1 mg·m−3时,去除率最高,为96.2%。这可能是由于乙二醇乙醚从纤维膜内扩散到膜外的传质速率和微生物的活性随着进气浓度升高而增加,提高了微生物捕获降解能力[15-16],导致去除率逐渐升高;当进气浓度超过314.1 mg·m−3时,生物膜中有限的生物量在单位时间内无法通过代谢降解过量的乙二醇乙醚,导致去除率逐渐下降[17-18]。由图3(b)可知,在进气浓度为140.0 mg·m−3,循环液pH为7.50、喷淋量为1.3 m3·(m2·h)−1的条件下,随着气体停留时间由10 s延长至30 s,乙二醇乙醚的去除率由92.8%升至94.2%。延长停留时间有利于提高乙二醇乙醚的去除率,但增幅较小,同时会显著增加反应器体积,故选取适宜的气体停留时间为10 s。
2.3 循环液喷淋量和pH的影响
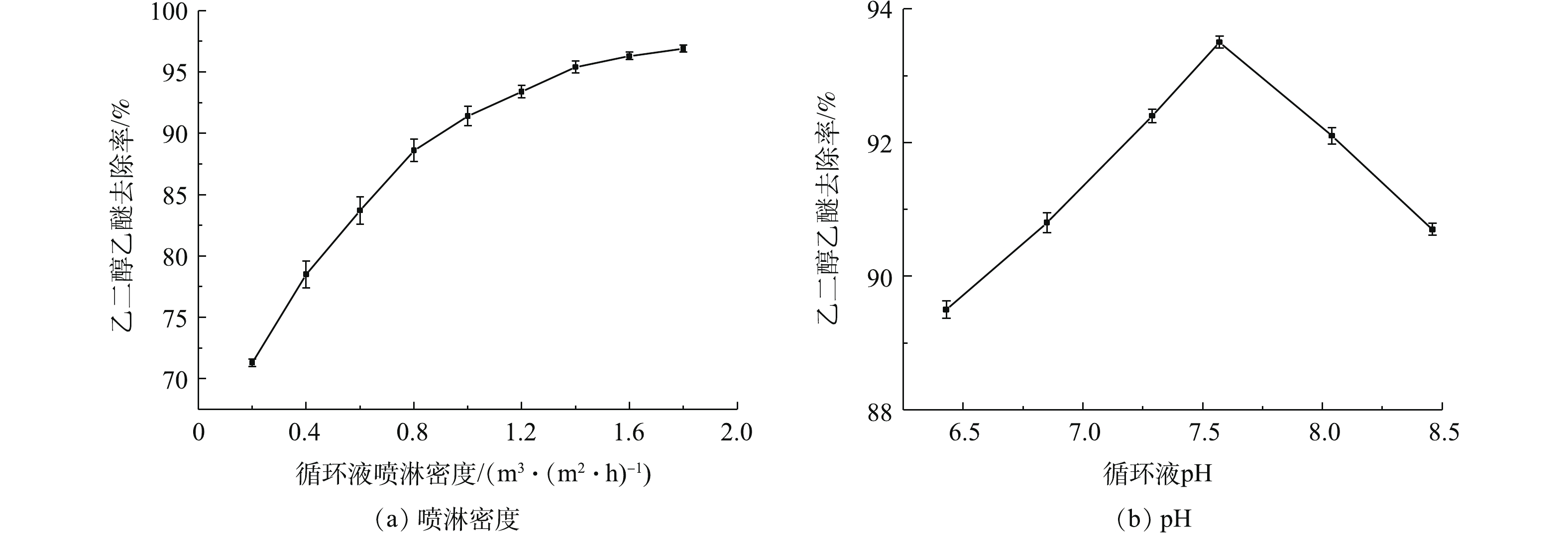
循环液喷淋量和pH对乙二醇乙醚去除率影响如图4所示。在气体停留时间为10 s,乙二醇乙醚进气浓度为140.0 mg·m−3,循环液pH稳定在7.52,设置不同喷淋密度,每个密度下反应器运行3 d。由图4(a)可知,当喷淋密度由0.2 m3·(m2·h)−1增大至1.8 m3·(m2·h)−1,乙二醇乙醚去除率由71.3%升至96.9%。这是由于乙二醇乙醚易溶于水,喷淋液能吸收乙二醇乙醚,增大喷淋量能增大循环液吸收乙二醇乙醚,循环液中有乙二醇乙醚的富集,进而增加液相中乙二醇乙醚与生物膜的接触,中空纤维膜表面的生物膜和循环液中的微生物共同降解乙二醇乙醚。当循环液喷淋量高于1.2 m3·(m2·h)−1时,乙二醇乙醚去除率增幅很小,同时会使运行成本增加,故选取适宜的循环液喷淋量为1.2 m3·(m2·h)−1。在气体停留时间为10 s,乙二醇乙醚进气浓度为140.0 mg·m−3,喷淋量为1.3 m3·(m2·h)−1的条件下,由图4(b)可知,乙二醇乙醚去除率随pH的升高呈现先升高后下降的趋势;当pH为7.57时,去除率最大为93.5%。这是因为体系pH过高或者过低都会影响微生物的活性,不利于其生长繁殖[19-20],进而影响乙二醇乙醚降解速率。因此,本实验循环液以磷酸氢二钾、磷酸二氢钾为缓冲物质,调节pH,适宜pH为7.60。
2.4 乙二醇乙醚的生物降解动力学
膜生物反应器处理乙二醇乙醚的本质是酶促反应,是利用体系中微生物产生的酶来降解乙二醇乙醚。Michaelis-Menten方程被广泛运用于研究酶催化反应动力学,因此,采用米门方程[21]式(1)拟合,得出生化降解乙二醇乙醚的最大反应速率和半饱和常数。
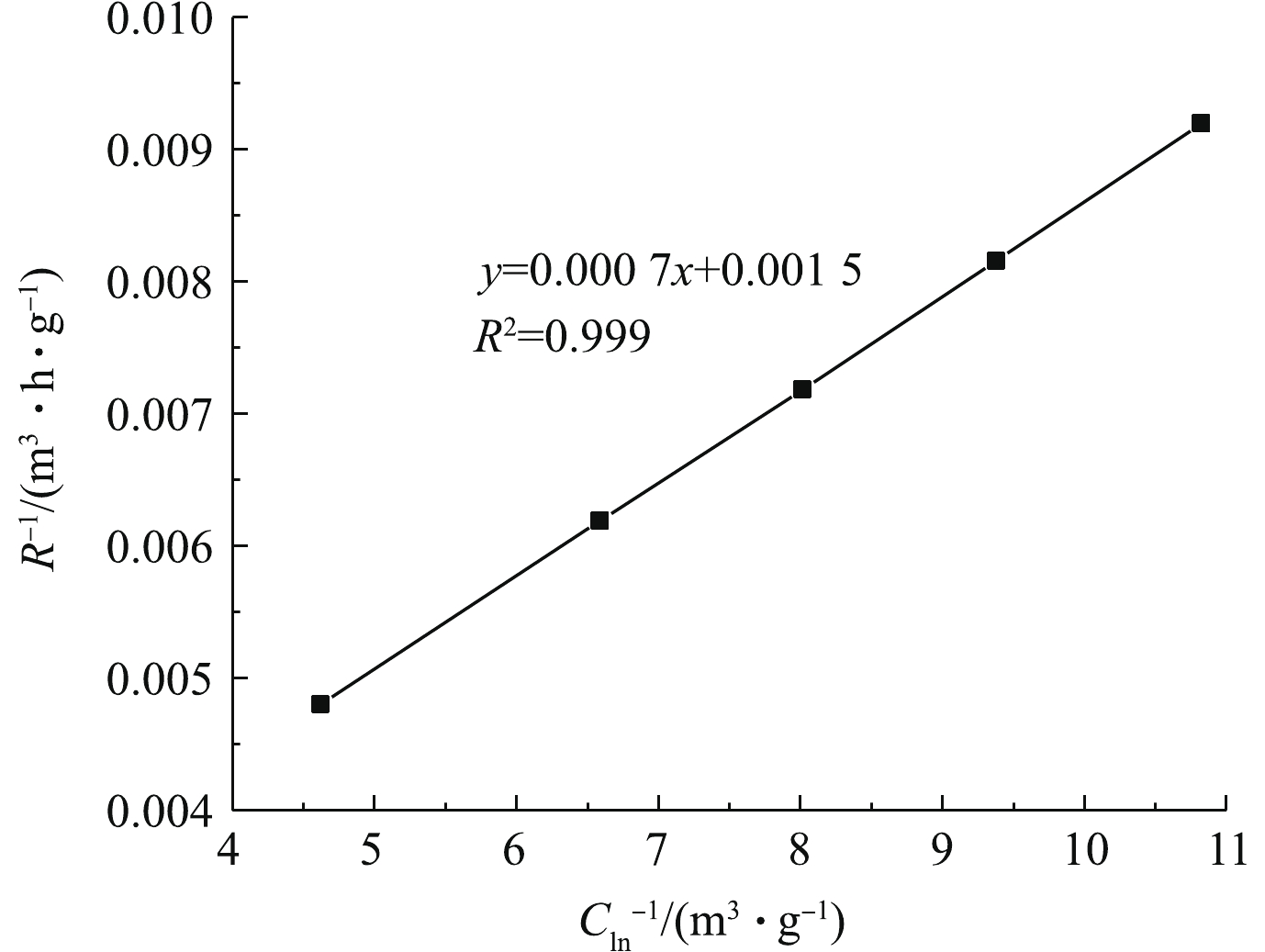
1R=KsVm1Cln+1Vm (1) 式中:R为表观去除率;Cln为进出气浓度的对数平均值;Vm为最大反应速率;Ks为半饱和常数。
将实验数据带入方程,结果如图5所示。拟合所得方程为y=0.000 7x+0.001 5,因此,本实验酶促反应的最大反应速率为666.67 g·(m3·h)−1,半饱和常数为0.47 g·m−3。
2.5 微生物群落结构与功能
采用16S rRNA技术分析膜生物反应器运行第30、90、145天的微生物群落结构变化,结果如图6所示。由图6(a)可知,在门分类水平上,反应器中的微生物在第30、90、145天的优势菌门均为Proteobacteria(54.4%,78.8%,34.2%)和Bacteroidetes(26.5%,7.9%,50.2%)。膜生物反应器在30~145 d,经过2次进气负荷的提高,微生物优势菌属、微生物群落结构发生了变化。在属分类水平上,膜生物反应器中的微生物群落结构变化如图6(b)所示,相对丰度在前10的优势菌属由第30天的OC32、Denitromonas、Methyloversatilis、OLB12、Chryseolinea、Bacillus、Thauera、Lewinella、Limnohabitans、Hydrogenophaga,第90天的Azospirillum、C39、Desulfovibrio、Blvii28, wastewater-sludge group、Sphaerochaeta、Desulfomicrobium、Lentimicrobium、Pseudomonas、SM1A02、Oceanimonas,变为第145天的Flavobacterium、Thauera、Blvii28, wastewater-sludge group、Oceanimonas、Azoarcus、Pseudomonas、Azospirillum、Desulfuromonas、Acinetobacter、Methyloversatilis。第30天微生物菌属相对丰度较大的OC32、Lewinella和Limnohabitans在装置运行到第90天后消失,Flavobacterium、Oceanimonas和Azoarcus等菌属在运行至第145天时,相对丰度有明显上升,分别为31.5%、5.5%和4.2%。Bacillus、Pseudomonas能够降解多种醚类物质[22];Pseudomonas和Hydrogenophag具有降解多种有机物的能力[23],包括酯类、醚氧化物等[24-25];Flavobacterium在降解2-乙基乙酸丁酯有机物中发挥重要作用,能够降解含氧有机物[26];Azoarcus和Thauera能共同参与酚类、吲哚等有机物的降解[27]。
膜生物反应器内乙二醇乙醚代谢主要功能基因如图7所示。乙二醇乙醚降解的功能基因分为加氧酶、醇脱氢、醛脱氢、乙酸氧化、乙醇酸氧化、乙二醇脱氢等6类。其中,NAD+、adhE、aldH能够将醛类物质氧化为羧酸类有机物[28],glcD能够代谢乙醇酸[29],adh能够将乙醇降解为乙醛,乙醛被aldB继续氧化为乙酸和水[30],dmpB、xyl属于加氧酶,能够在有机物的碳原子上加入氧键,与醚键的断裂相关[31]。宏基因组测序结果显示,微生物菌属Methyloversatilis含有功能基因aldB、xylQ、glcD、mdh2 mxaI、exaA、ACSS acs;Pseudomonas含有功能基因adh、aldH、glcD、catA;Azoarcus含有功能基因adhP、exaA、glcD;Thauera含有功能基因exaA、aldB、ACSS acs、frmB ESD fghA、pct;Hydrogenophaga含有功能基因puuC aldH、ACSS acs、glcD。这些菌属能将乙二醇乙醚降解为二氧化碳和水。
3. 结论
1)膜生物反应器处理乙二醇乙醚废气的最佳运行条件为:气体停留时间为10 s,循环液pH为7.60,循环液喷淋量为1.2 m3·(m2·h)−1。
2)采用米门方程和双倒数方程拟合得出生化降解乙二醇乙醚的最大反应速率为666.67 g·(m·h)−1,半饱和常数为0.47 g·m−3。
3)采用16S rRNA研究膜生物反应器内的微生物群落结构变化,经过2次进气负荷的提高,降解乙二醇乙醚的主要功能菌属由第30天的Methyloversatilis变为第90天的Methyloversatilis、Pseudomonas,最终变为第145天的Thauera和Flavobacterium。
4)宏基因组测序技术结果表明,adh、yiaY、adhP、gbsB、mah1,mxaf等是乙二醇乙醚代谢功能基因。
5)膜生物反应器能高效降解乙二醇乙醚废气,去除率可达99.6%。本研究结果为降解水性涂料生产使用过程中产生的有机废气提供了数据支持。
-
-
[1] PODGORSKI J, BERG M. Global threat of arsenic in groundwater[J]. Science, 2020, 368(6493): 845-850. doi: 10.1126/science.aba1510 [2] TYLER C R, ALLAN A M. The effects of arsenic exposure on neurological and cognitive dysfunction in human and rodent studies: A review[J]. Current Environmental Health Reports, 2014, 1(2): 132-147. doi: 10.1007/s40572-014-0012-1 [3] RODRÍGUEZ-LADO L, SUN G F, BERG M, et al. Groundwater arsenic contamination throughout China[J]. Science, 2013, 341(6148): 866-868. doi: 10.1126/science.1237484 [4] LIU R P, QU J H. Review on heterogeneous oxidation and adsorption for arsenic removal from drinking water[J]. Journal of Environmental Sciences, 2021, 110: 178-188. doi: 10.1016/j.jes.2021.04.008 [5] CHOWDHURY S R, YANFUL E K. Arsenic and chromium removal by mixed magnetite-maghemite nanoparticles and the effect of phosphate on removal[J]. Journal of Environmental Management, 2010, 91(11): 2238-2247. doi: 10.1016/j.jenvman.2010.06.003 [6] DICKSON D, LIU G L, CAI Y. Adsorption kinetics and isotherms of arsenite and arsenate on hematite nanoparticles and aggregates[J]. Journal of Environmental Management, 2017, 186: 261-267. [7] 赵雅光, 万俊锋, 刘奉滨, 等. 零价铁(ZVI)治理水体砷污染研究进展[J]. 环境化学, 2013, 32(10): 1943-1949. doi: 10.7524/j.issn.0254-6108.2013.10.018 ZHAO Y G, WAN J F, LIU F B, et al. Application of zero-valent iron(ZVI)technology for arsenic removal from aqueous environment[J]. Environmental Chemistry, 2013, 32(10): 1943-1949 (in Chinese). doi: 10.7524/j.issn.0254-6108.2013.10.018
[8] 胡一帆, 王文兵, 仵彦卿. 弱磁场强化零价铁去除水中砷的效果[J]. 环境化学, 2019, 38(5): 1074-1081. doi: 10.1002/etc.4383 HU Y F, WANG W B, WU Y Q. The role of weak magnetic field in accelerating the removal of arsenic by zero-valent iron[J]. Environmental Chemistry, 2019, 38(5): 1074-1081 (in Chinese). doi: 10.1002/etc.4383
[9] 罗灿钰, 张琢, 赵华甫. 施氏矿物的矿物学特征及其除砷研究进展[J]. 环境化学, 2021, 40(11): 3530-3543. doi: 10.7524/j.issn.0254-6108.2020070302 LUO C Y, ZHANG Z, ZHAO H F. The mineralogical characteristics of schwertmannite and its progress in arsenic removal[J]. Environmental Chemistry, 2021, 40(11): 3530-3543 (in Chinese). doi: 10.7524/j.issn.0254-6108.2020070302
[10] 吴川, 黄柳, 薛生国, 等. 赤泥对砷污染的调控研究进展[J]. 环境化学, 2016, 35(1): 141-149. doi: 10.7524/j.issn.0254-6108.2016.01.2015071004 WU C, HUANG L, XUE S G, et al. Review on the application of bauxite residue on As contamination remediation[J]. Environmental Chemistry, 2016, 35(1): 141-149 (in Chinese). doi: 10.7524/j.issn.0254-6108.2016.01.2015071004
[11] LI M, KUANG S P, KANG Y, et al. Recent advances in application of iron-manganese oxide nanomaterials for removal of heavy metals in the aquatic environment[J]. Science of the Total Environment, 2022, 819: 153157. doi: 10.1016/j.scitotenv.2022.153157 [12] 曾辉平, 于亚萍, 吕赛赛, 等. 基于铁锰泥的除砷颗粒吸附剂制备及其比较[J]. 环境科学, 2019, 40(11): 5002-5008. ZENG H P, YU Y P, LÜ S S, et al. Preparation and comparison of arsenic removal granular adsorbent based on iron-manganese sludge[J]. Environmental Science, 2019, 40(11): 5002-5008 (in Chinese).
[13] VIEIRA B R C, PINTOR A M A, BOAVENTURA R A R, et al. Arsenic removal from water using iron-coated seaweeds[J]. Journal of Environmental Management, 2017, 192: 224-233. [14] ABU-NADA A, McKAY G, ABDALA A. Recent advances in applications of hybrid graphene materials for metals removal from wastewater[J]. Nanomaterials, 2020, 10(3): 595. doi: 10.3390/nano10030595 [15] 韦婧, 刘昳晗, 涂晨, 等. 铁修饰生物炭的制备及在砷污染土壤修复中的应用[J]. 环境科学, 2023, 44(2): 965-974. WEI J, LIU Y H, TU C, et al. Preparation of iron modified biochar and its application in arsenic contaminated soil remediation[J]. Environmental Science, 2023, 44(2): 965-974 (in Chinese).
[16] SAMUEL M S, SELVARAJAN E, SARSWAT A, et al. Nanomaterials as adsorbents for As(III) and As(V) removal from water: A review[J]. Journal of Hazardous Materials, 2022, 424: 127572. doi: 10.1016/j.jhazmat.2021.127572 [17] JAIN R. Recent advances of magnetite nanomaterials to remove arsenic from water[J]. RSC Advances, 2022, 12(50): 32197-32209. doi: 10.1039/D2RA05832D [18] 芦琳, 颜利玲, 梁美娜, 等. 磁性氧化铁/桑树杆生物炭的制备及其对砷污染土壤溶解性有机碳和砷形态的影响[J]. 环境科学, 2022, 43(11): 5214-5223. LU L, YAN L L, LIANG M N, et al. Preparation of magnetic iron oxide/mulberry straw biochar and its effects on dissolved organic carbon and arsenic forms in arsenic contaminated soil[J]. Environmental Science, 2022, 43(11): 5214-5223 (in Chinese).
[19] MAGRO M, MOLINARI S, VENERANDO A, et al. Colloidal maghemite nanoparticles with oxyhydroxide-like interface and chiroptical properties[J]. Applied Surface Science, 2020, 534: 147567. doi: 10.1016/j.apsusc.2020.147567 [20] LIU Z M, WU S H, JIA S Y, et al. Novel hematite nanorods and magnetite nanoparticles prepared from MIL-100(Fe) template for the removal of As(V)[J]. Materials Letters, 2014, 132: 8-10. doi: 10.1016/j.matlet.2014.06.059 [21] DAS G K, BONIFACIO C S, de ROJAS J, et al. Ultra-long magnetic nanochains for highly efficient arsenic removal from water[J]. Journal of Materials Chemistry A, 2014, 2(32): 12974-12981. doi: 10.1039/C4TA02614D [22] CHENG W, XU J, WANG Y J, et al. Dispersion-precipitation synthesis of nanosized magnetic iron oxide for efficient removal of arsenite in water[J]. Journal of Colloid and Interface Science, 2015, 445: 93-101. doi: 10.1016/j.jcis.2014.12.082 [23] CHENG W, ZHANG W D, HU L J, et al. Etching synthesis of iron oxide nanoparticles for adsorption of arsenic from water[J]. RSC Advances, 2016, 6(19): 15900-15910. doi: 10.1039/C5RA26143K [24] FERREIRA L S, TRIERWEILER J O. Modeling and simulation of the polymeric nanocapsule formation process[J]. IFAC Proceedings Volumes, 2009, 42(11): 405-410. doi: 10.3182/20090712-4-TR-2008.00064 [25] 韩帅鹏, 唐李文, 刘勤, 等. 磁性含磷油茶壳生物炭对水中磺胺甲噁唑的吸附特性[J]. 环境科学,2024, 45(2): 898-908. HAN S P, TANG L W, LIU Q, et al. Adsorption properties of magnetic phosphorous oil tea shell biochar on sulfamethoxazole in water[J]. Environmental Science, 2024, 45(2): 898-908(in Chinese).
[26] MILONJIĆ S K, KOPEČNI M M, ILIĆ Z E. The point of zero charge and adsorption properties of natural magnetite[J]. Journal of Radioanalytical Chemistry, 1983, 78(1): 15-24. doi: 10.1007/BF02519745 [27] GOLDBERG S, JOHNSTON C T. Mechanisms of arsenic adsorption on amorphous oxides evaluated using macroscopic measurements, vibrational spectroscopy, and surface complexation modeling[J]. Journal of Colloid and Interface Science, 2001, 234(1): 204-216. doi: 10.1006/jcis.2000.7295 期刊类型引用(2)
1. 康晴晴,张志,牛涌祥,朱仁成,王树,李金亮,李顺义. VOC废气生物法净化工艺微生物气溶胶排放特征及暴露风险研究进展. 应用化工. 2024(03): 655-660 .  百度学术
百度学术
2. 刘玲玲. 复杂工业有机废气处理方法及装置. 天津化工. 2022(01): 103-106 .  百度学术
百度学术
其他类型引用(2)
-






 下载:
下载: