-
近年来,由水中抗生素超标导致的水体污染、生态毒害以及诱生超级耐药性基因(ARGs)等问题引起了广泛关注[1],有针对性的治理技术亟待开发. 在报道的水处理技术中,基于过硫酸盐活化的高级氧化技术(SR-AOPs)由于具有绿色环保、氧化效率高以及使用范围广等优点而被广泛应用于水中有机污染物的去除[2],其中高效且稳定的催化剂是该技术的关键所在.
金属有机框架(MOFs)是由金属离子中心和有机配体通过自组装形成的三维周期网格结构[3-4],具有比表面积大、结构性质可调和活性位点丰富等特点,有望在过硫酸盐活化体系中展现出优异的性能[5-6]. 例如,ZIF-8是由锌离子与2-甲基咪唑配位键形成的新型多孔材料,相比于其他MOFs材料具有良好的水热稳定性和化学稳定性[7-8]. 镍和锌位于元素周期表同一周期中,核外电子排列具有高度的结构相似性. 研究表明,将镍掺杂到ZIF-8中会影响sp2 C位点的电子结构、产生活化位点,从而改变催化活性[9].
粉末状MOFs还存在易团聚和难回收等问题[10]. 为此,有学者提出将电化学和膜过滤构筑在一个操作单元内形成电催化膜系统[11],以期产生一定的协同作用. 例如,Zheng等[12]提出利用比表面积大、导电性好的碳纳米管(CNT)作为载体对纳米材料进行妥善搭载的解决方案. CNT作为载体可以避免纳米催化剂的团聚,CNT、纳米催化剂和辅助电场之间发挥了显著的协同作用;然而,构筑金属有机骨架(MOFs)基的电催化膜材料用于活化过硫酸盐和降解有机微污染物的相关研究却鲜有报道.
本实验以CNT为载体,设计制备了CNT/Ni-ZIF-8纳米复合电催化膜,开展了活化过硫酸盐降解磺胺甲噁唑(sulfamethoxazole, SMX)的性能和机理研究,探究了制备条件与纳米复合膜理化性质间的构效关系,分析并优化了镍的掺杂量,考察了降解实验参数(如电压、流速和PMS用量等)对SMX降解动力学的影响,研究了CNT、MOFs催化剂和电场之间的相互作用,进一步通过自由基淬灭实验和EPR测试来明确反应体系中主要的活性物种,阐明了催化降解的内在工作机制.
-
实验中所有化学试剂均为分析纯,六水合硝酸锌(Zn(NO3)2·6H2O)、六水合硝酸镍(Ni(NO3)2·6H2O)、2-甲基咪唑(2-MeIm,C4H6N2)、过单硫酸氢钾(PMS,2KHSO5·KHSO4·K2SO4)、磺胺甲噁唑(SMX,C10H11N3O3S)、甲醇(CH3OH)、碳酸氢钠(NaHCO3)、氯化钠(NaCl)、磷酸氢二钠(Na2HPO4)、2, 2, 6, 6-四甲基-4-哌啶醇(TEMP,C9H19N)、5, 5-二甲基-1-吡咯啉-氧化物(DMPO,C6H11NO)、L-组氨酸(C6H9N3O2)、叔丁醇(TBA,C4H10O)均购自美国Sigma-Aldrich公司. 酸化碳纳米管(O-CNT)购自中国科学院成都有机化学有限公司. 所有溶液均用超纯水(18.25 MΩ·cm)配制,超纯水来自美国Millipore公司.
-
首先,将5 mmol·L−1 Zn(NO3)2·6H2O和20 mg酸化CNT(O-CNT)混合于50 mL甲醇溶液中,超声处理40 min. 随后,将50 mmol·L−1的2-甲基咪唑溶于40 mL甲醇溶液中(六水合硝酸锌与2-甲基咪唑的物质的量比为1:8),再添加到超声后的溶液中. 将混合溶液置于磁力搅拌器中等强度下搅拌24 h,通过真空抽滤将产物抽滤到PTFE支撑膜(孔径为0.45 μm)上,最后用甲醇和超纯水充分洗涤,制得CNT/ZIF-8催化膜.
除Zn(NO3)2·6H2O被Zn(NO3)2·6H2O和Ni(NO3)2·6H2O的混合物代替,同时保持金属源的总摩尔量相同之外,按照上述相同的步骤合成CNT/Ni-ZIF-8样品. 通过改变Ni在总金属(Ni + Zn)中的摩尔百分比(10%、20%、40%和80%)来制备4个不同镍掺杂量的CNT/Ni-ZIF-8样品. 催化膜的制备示意图如图1所示.
-
通过S-4800型场发射扫描电子显微镜对酸化CNT膜和CNT/20%Ni-ZIF-8复合膜的表面形貌进行表征分析. 利用 Escalab 250Xi 型 X 射线光电子能谱仪研究CNT/20% Ni-ZIF-8复合膜的元素组成和表面电子状态,并以 C 1s 284.8 eV作为标准进行荷电校正. 通过Talos F200S型场发射透射电子显微镜探究CNT/20% Ni-ZIF-8复合膜的微观结构. 测试前,将待测样品冷冻干燥过夜,并研磨至粉末状.
-
为消除物理吸附作用对SMX去除的影响,先将5 mg·L−1的SMX溶液以1.5 mL·min−1流速通过催化膜3 h达到吸附平衡后,再进行降解实验. 所用电过滤系统由多孔钛片、CNT/Ni-ZIF-8电催化膜、钛棒和绝缘硅胶片组成(图2). 以多孔钛片作阳极,CNT/Ni-ZIF-8电催化膜作阴极. 辅助电场则由直流电源(DH1766A-1)提供.
在实验条件下测试钛阳极电位为(1.0±0.2)V vs Ag/AgCl,低于Ti的腐蚀电位,不足以引发钛的氧化反应. 将含有一定量PMS的SMX溶液以1.5 mL·min−1通过反应系统. PMS作为自由基活化催化剂和溶液中的电解质. 在降解过程中,定期从反应器中收集反应后的溶液(1 mL),并立即与100 µL甲醇混合,以淬灭剩余的自由基. 测试时,所有样品均用0.45 μm针头过滤器过滤. 对比考察Ni掺杂量(0%、10%、20%、40%、80%)、电压(−2—0 V)、流速(0—2 mL·min−1)和PMS投加量(0—2 mmol·L−1)等参数对SMX降解效率的影响. SMX的降解率通过公式(1)计算.
其中,φ为SMX降解率,%;C0、Ct分别为初始时刻、t时刻的SMX浓度,mg·L−1; A0、At分别为液相色谱仪所测初始时刻、t时刻时SMX浓度下所占的峰面积,mAU·min.SMX的浓度利用高效液相色谱仪(HPLC,Ultimate 3000,Thermo-Fisher Scientific)进行测定. 流动相由甲醇和水(0.01%磷酸)(40:60,V/V)组成,流速为1.0 mL·min−1,检测波长为λ=257 nm. 所有实验重复3次以确保良好的再现性.
-
通过FESEM对O-CNT和镍掺杂量为20%的复合材料进行表观形貌分析. O-CNT表面含有丰富的含氧官能团,这不仅有利于其在甲醇中的分散,还为金属离子提供了充足的螯合位点. 如图3(a)所示,纯O-CNT呈现均匀的三维网络结构. 由于Ni2+离子与2-甲基咪唑连接剂之间的相互作用,已经证明Ni2+离子一旦加入到这些纳米晶体中,会破坏ZIF-8的结晶度[13]. 从图3(b)可以看出,当掺杂20%的镍后,ZIF-8的形貌转变为片状. 反应后的CNT/20% Ni-ZIF-8电催化膜仍基本维持原有的形貌特征(见图3c).
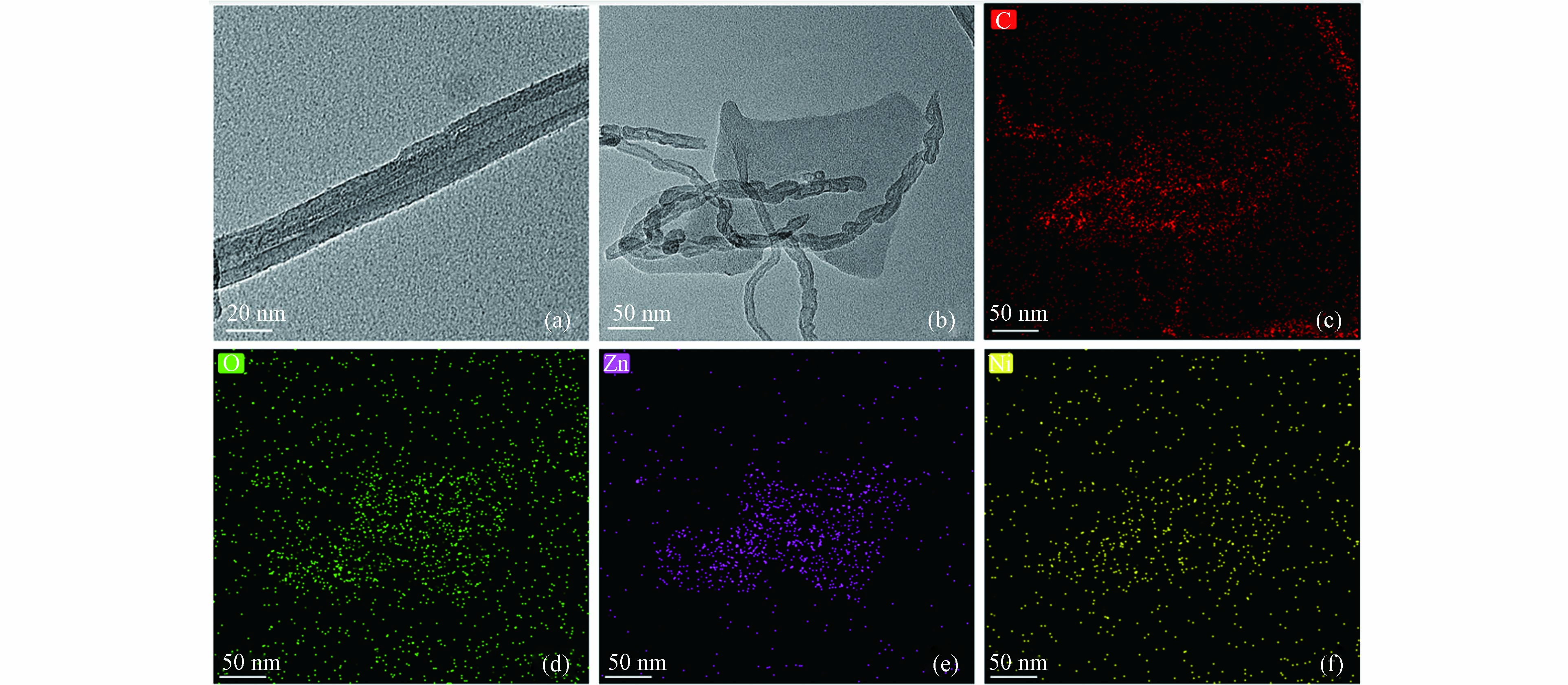
通过TEM和EDS分析了复合膜和O-CNT膜的微观结构和成分信息. 如图4(a)所示,O-CNT管直径为5—15 nm,表面平整光滑, CNT与20% Ni-ZIF-8片层均匀混合(图4(b)),这与FESEM表征结果相一致. 此外,图4(c-f)为(b)的EDS元素图结果显示C、O、Zn和Ni元素在复合膜表面上均匀分布,表明了镍元素的成功掺杂.
为研究复合膜的元素组成和表面电子状态,进行了XPS分析. 如图5(a)所示,XPS总扫描图中显示了C、O、Zn和Ni元素的存在. C 1s包含3个峰(图5(b)),结合能值为284.8 、285.7 、288.9 eV,分别对应于碳碳键(C—C/C=C)和碳有机连接体(C—O和C=O)[14]. Zn 2p光谱(图5(c)、(d))由两个反褶积峰组成,分别对应Zn 2p3/2 (1021.8 eV)和Zn 2p1/2 (1044.8 eV)[15]. 图5(e)中拟合结果表明,CNT/20% Ni-ZIF-8的Ni 2p XPS光谱归因于Ni2+和Ni3+两种价态的存在,即Ni(Ⅱ) 2p3/2 (857.1 eV)、Ni(Ⅲ) 2p3/2 (856.0 eV)、Ni(Ⅱ) 2p1/2 (873.9 eV)和Ni(Ⅲ) 2p1/2 (870.0 eV),这与文献报道一致[16].
-
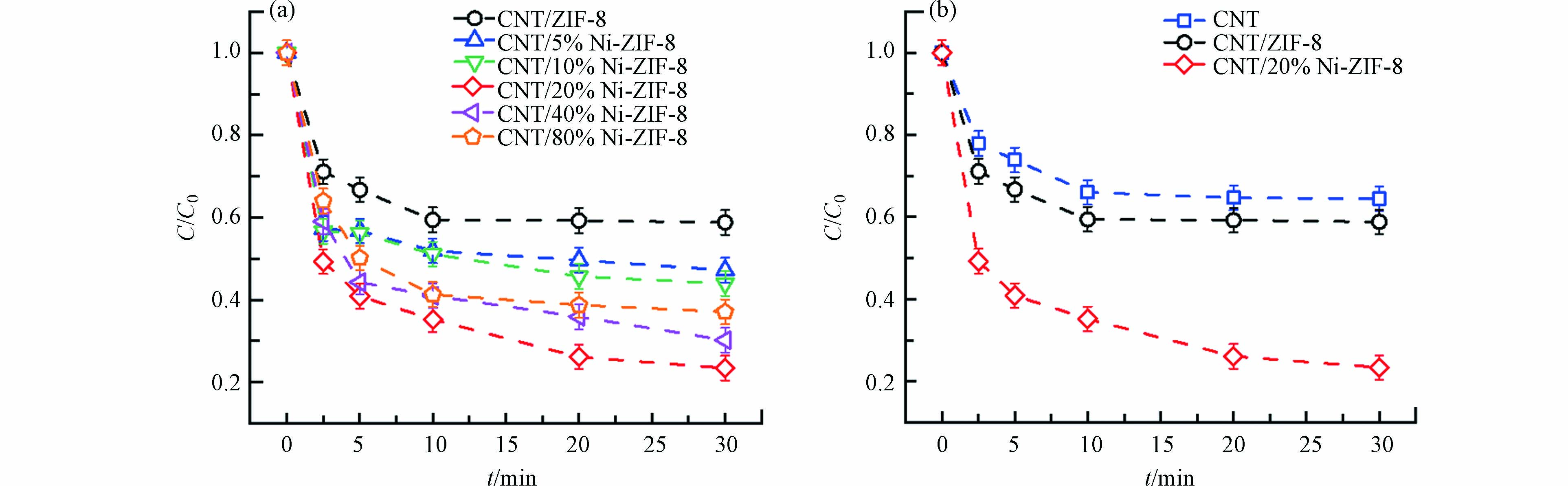
在中性pH、流速1.5 mL·min−1、电压−1.5 V和PMS投加量1.5 mmol·L−1的条件下,考察了不同镍掺杂量对SMX降解效果的影响. 如图6(a)所示,镍掺杂量从0%增至20%时,SMX单次流降解率由41.1%增至76.6%;当进一步提升镍掺杂量到80%时,SMX的降解率(62.9%)下降. 这是由于随着镍掺杂量的增加,催化活性位点增加,从而实现对SMX的高效降解. 而镍掺杂量进一步增加则可能导致团聚以及其他消耗自由基的副反应发生[17]. 因此,选择20%的镍掺杂量制备CNT/Ni-ZIF-8电催化膜,并用于后续实验研究.
为了证明CNT/Ni-ZIF-8电催化膜的优异性能,在相同实验条件下对比了不同催化膜降解磺胺甲噁唑的效果. 如图6(b)所示,纯CNT、CNT/ZIF-8和CNT/Ni-ZIF-8催化膜在30 min内SMX单次流的降解率分别为35.5%、41.1%、76.6%. 其中,CNT/Ni-ZIF-8催化膜对SMX的降解效果明显高于其他催化膜,表明体系中产生了活性氧物种,从而加速了SMX的降解.
-
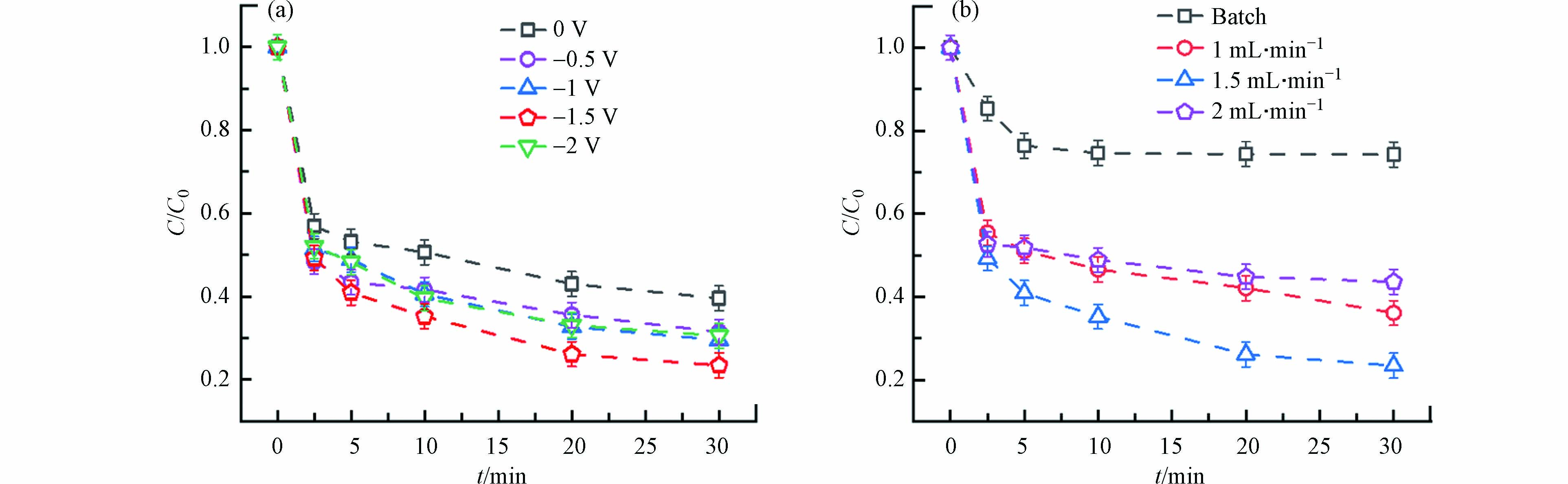
为探究实验操作参数对SMX降解效果的影响,考察在电压−2—0 V、流速0—2 mL·min−1实验条件下SMX的降解效果. 如图7(a)所示,随着电压从−0.5 V降低到−1.5 V,SMX去除率增加,这是由于外加电压的升高产生了更多的1O2,更有利于磺胺甲噁唑的降解. 然而,当外加电压进一步下降到−2 V时,SMX去除率下降,这可能是因为其他副反应的发生.
流速是影响污染物传质的重要因素之一. 如图7(b)所示,流速为1、1.5、2 mL·min−1时,SMX在30 min内的去除率分别为63.9%、76.6%和56.4%. 这是因为穿透式装置依靠对流进行传质,随着流速增加对流增强,相应地SMX分子向CNT/Ni-ZIF-8复合膜的质量传输也更快. 而进一步增加流速至2 mL·min−1,去除效果下降了20.2%,这是由于有限的停留时间导致SMX分子与过滤器活性部位接触不足. 相比之下,序批式处理模式下依靠扩散进行传质,30 min后仅实现25.7%的去除效果.
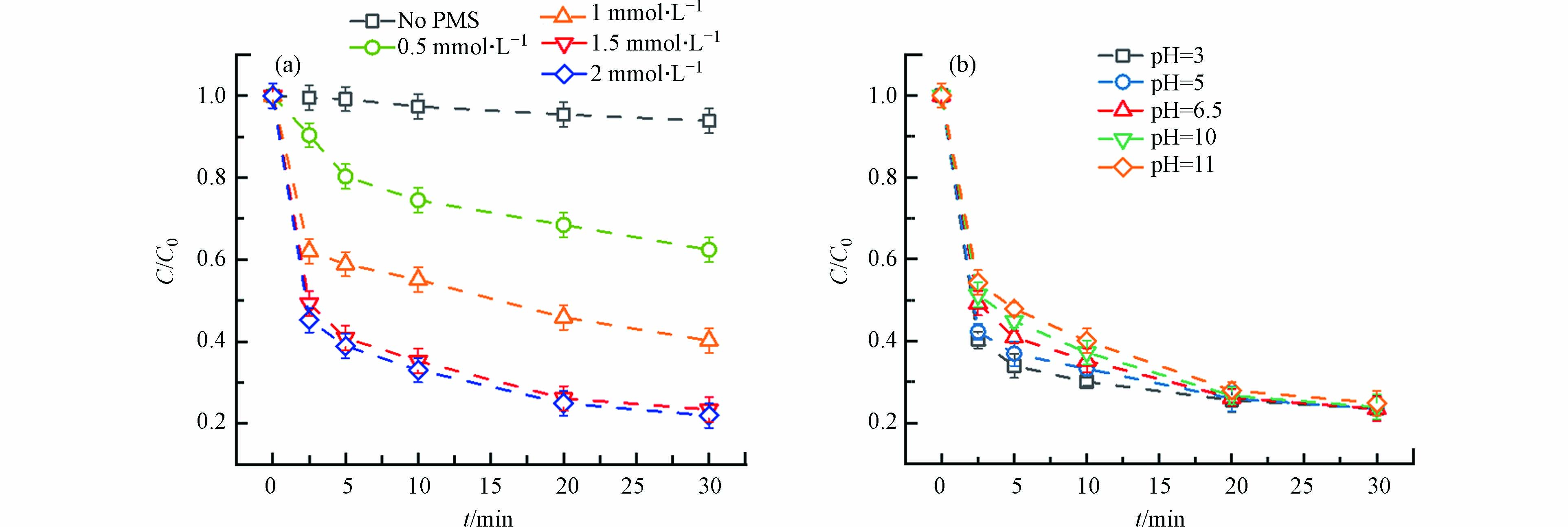
在电催化过滤系统中,PMS不仅充当反应的电解质,还是生成活性物种的前驱体物质,其浓度对SMX降解有很大影响. 从图8(a)中可以看出,随着PMS投加量从0 mmol·L−1增加到1.5 mmol·L−1,SMX降解率从6.1%提高到76.6%,说明随着PMS浓度提高,相应地产生的活性物种数量也会增多. 当PMS添加量从1.5 mmol·L−1增加到2 mmol·L−1时,SMX降解率没有明显提高,这归因于当PMS添加量较多时,一定量的催化剂没有更多的活性位点来活化PMS. 因此综合成本与催化效果最终选择添加1.5 mmol·L−1的PMS.
溶液pH值主要影响催化膜的表面电荷性质和PMS的存在状态,是活性物种生成和转化过程的重要因素[18]. 因此,为评价不同初始pH对SMX降解效果的影响,在pH=3.0—11.0的范围内进行了降解实验. 结果如图8(b)所示,溶液的pH值对CNT/Ni-ZIF-8体系的影响非常小,SMX的降解率变化不大,说明该体系在较宽的pH范围内对SMX均有良好的去除效果. 此外,目标污染物SMX的初始浓度也对去除效果有一定影响. 结果如图9(a)所示,SMX的去除率随着SMX浓度的增加而降低,当初始浓度为2.5 mg·L−1时,SMX在30 min内去除率达82.9%,而10 mg·L−1 SMX在30 min内仅去除73.3%. SMX的初始浓度越高,去除率越低. 可能由于体系中产生更多的中间产物或副产物与SMX竞争活性物种,导致SMX分子、中间产物和活性物种之间的竞争加剧,导致高浓度SMX的降解更为困难.
为探究水中不同无机阴离子对CNT/Ni-ZIF-8体系降解SMX的影响,向体系中分别加入5 mmol·L−1和10 mmol·L−1的无机阴离子(如Cl−、HCO3−、H2PO4−、NO3−). 如图9(b)所示,添加5 mmol·L−1Cl−时对SMX的降解影响并不明显,当其浓度为10 mmol·L−1时,降解效率得到一定提升. 这可能是因为在CNT/Ni-ZIF-8体系中,Cl−可与PMS反应生成HOCl[19],从而参与到SMX降解的过程中. H2PO4−和NO3−的降解效果没有明显变化,说明H2PO4−和NO3−对CNT/Ni-ZIF-8体系降解磺胺甲恶唑基本没有影响. HCO3−对磺胺甲恶唑的降解有一定抑制作用,这是因为碳酸盐对活性物种具有淬灭作用[20]. 结果说明,CNT/Ni-ZIF-8体系在实际水体中的应用性较强. 天然有机物也广泛存在于水体环境中,选取腐殖酸(HA)作为天然有机物的典型代表,如图9(b)所示,随着反应体系中HA浓度的增大,SMX的降解效果并没有受到影响. 因此CNT/Ni-ZIF-8体系具有很好的稳定性,适宜在实际水体中应用.
-
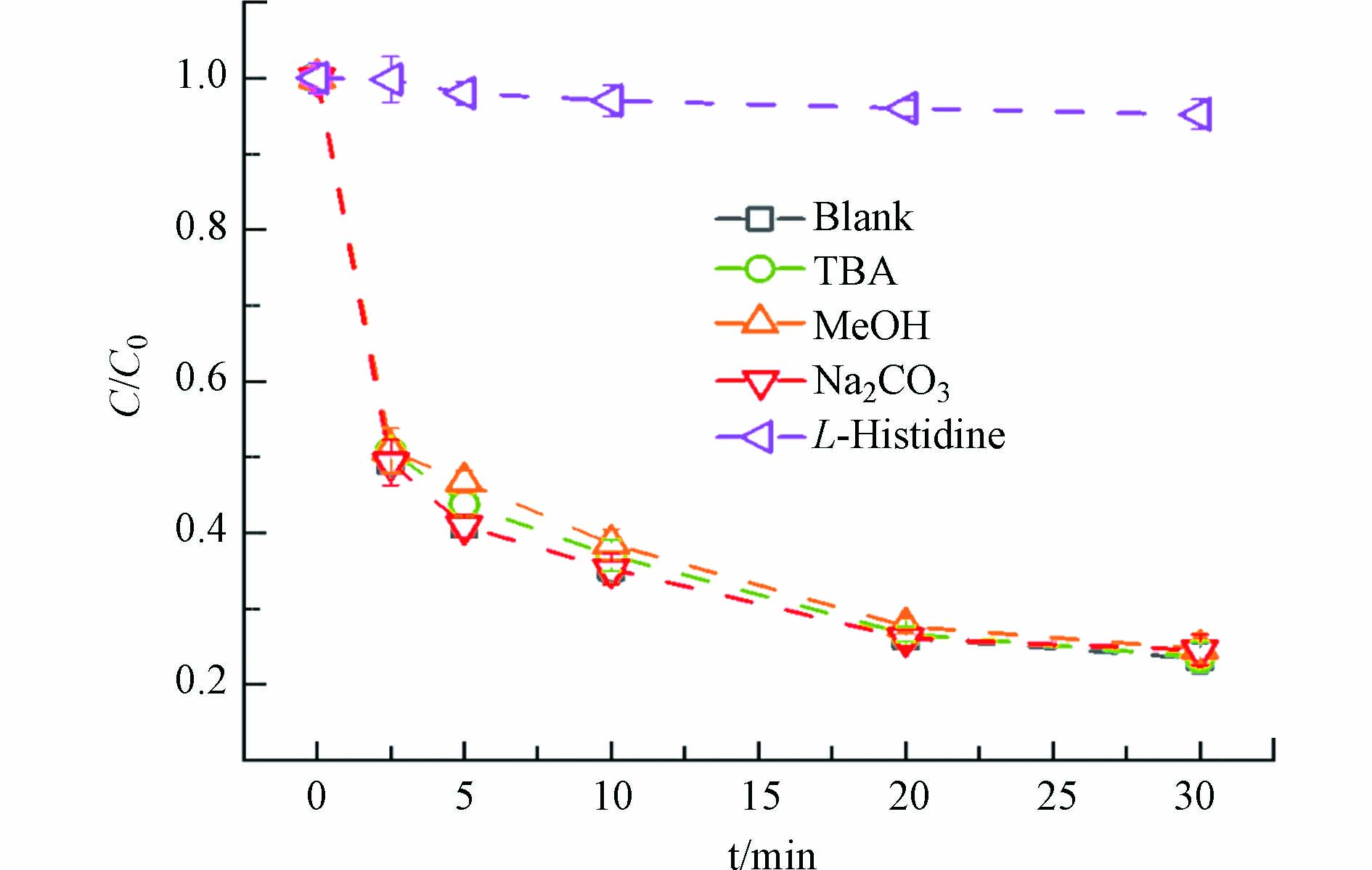
先前的研究表明PMS活化过程涉及自由基和非自由基途径[21,22]. 为确定CNT/Ni-ZIF-8系统中产生的活性物种,使用不同的自由基捕获剂进行淬灭实验. TBA可以淬灭反应体系中的羟基自由基(·OH),甲醇对·OH和SO4•−都具有淬灭作用[23]. 如图10所示,在体系中添加100 mmol·L−1 TBA和100 mmol·L−1甲醇,SMX的降解只受到轻微抑制,表明SO4•−和·OH不是反应体系中主要的活性物种,其他一些非自由基物种可能参与了这一过程. 利用Na2CO3作为特定的猝灭剂,探究超氧自由基(O2•−)的存在. 在体系中加入100 mmol·L−1 Na2CO3时,SMX的降解效果仍然没有抑制,说明O2•−也不是主要的反应物种. 用L-组氨酸(L-Histidine)进一步验证1O2的存在,当添加100 mmol·L−1 L-组氨酸时,71.6%的SMX降解被抑制,这表明1O2通过非自由基途径参与了有机物的降解,且是主导的反应活性物种.
-
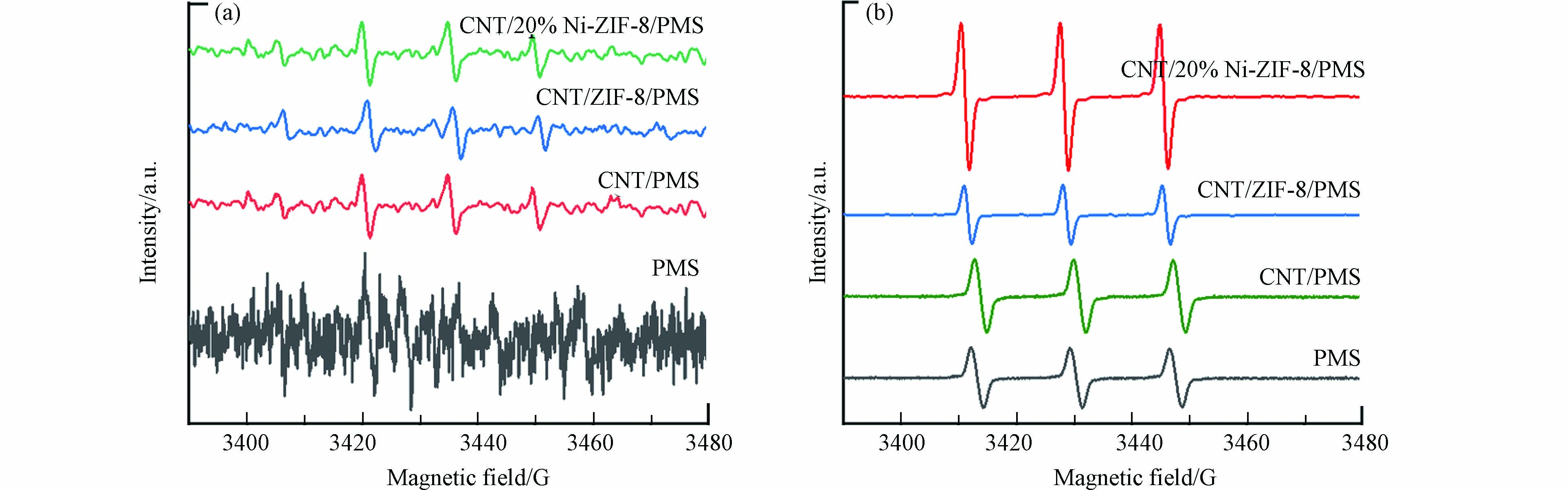
为了进一步证明CNT/Ni-ZIF-8体系中的活性物种以及阐明反应机理,使用5,5-二甲基-1-吡咯啉-N-氧化物(DMPO)和4-氨基-2,2,6,6-四甲基哌啶(TEMP)作为自由基捕获剂,分别捕获自由基(·OH、SO4•−)和1O2,进行电子顺磁共振(EPR)测试. 如图11(a)所示,在体系中加入DMPO出现了非常微弱的DMPO-OH信号(1:2:2:1),且没有检测到DMPO-SO4的特征信号. 图11(b)显示当体系中加入TEMP后出现了明显的1O2的三重态峰(1:1:1),且信号强度明显强于单独PMS和纯CNT时出现的信号峰,表明CNT/Ni-ZIF-8体系主要通过非自由基途径参与SMX的降解过程.
综上所述,结合自由基淬灭实验和EPR测试结果,可知CNT/Ni-ZIF-8体系中产生的·OH和SO4•−非常少,1O2是主要的活性氧物种.
-
由自由基淬灭实验和EPR测试结果可知,非自由基途径在CNT/Ni-ZIF-8活化PMS降解SMX的过程中占主要作用,自由基的作用较小. PMS自分解可产生少量1O2公式(2),但PMS产生1O2的分解率非常低,相应的贡献微不足道[24]. CNT上富电子的酮C=O基团也可以通过给电子活化PMS生成1O2,导致PMS中过氧化物O—O键的断裂公式(3—6)[25]. 同时,通过比较CNT/Ni-ZIF-8/PMS和CNT/PMS的EPR谱,发现产生1O2的驱动力是镍物种. 从XPS图中(图5(e)、(f))可以看出,反应后Ni(Ⅱ)的比例减少,Ni(Ⅲ)比例增加,推测来自HSO5−分解的SO5•−可能与Ni位结合,通过公式(7-8)生成1O2. 此外,CNT/Ni-ZIF-8活化PMS也能产生1O2,电子通过复合体从污染物(电子供体)转移到PMS(电子受体),PMS被消耗产生1O2(公式(9))[26],污染物则通过电子转移和1O2协同作用被矿化成H2O、CO2和小分子物质,这是降解SMX的非自由基途径. 因此,SMX最终通过1O2非自由基过程分解成小分子物质.
-
本文设计制备了不同镍掺杂量的CNT/Ni-ZIF-8电催化膜材料,结合多种先进表征手段明确了材料的理化特性. 以典型抗生素SMX为目标污染物,探究了复合材料活化PMS降解有机物的性能和机理. 主要结论如下:
1)以CNT为载体,成功制备了镍掺杂的ZIF-8复合催化材料. 表征结果显示Ni-ZIF-8均匀地分布于CNT表面.
2) 在电压−1.5V,流速1.5 mL·min−1,PMS投加量为1.5 mmol·L−1的最佳反应条件下,SMX的单次流去除率达76.6%.
3) 自由基淬灭实验和EPR测试结果表明,·OH和1O2均参与了SMX的降解过程.
金属有机框架(MOFs)基电催化膜活化过硫酸盐降解磺胺甲噁唑
Degradation of sulfamethoxazole by metal-organic framework (MOFs)-based electrocatalytic membrane activated by peroxymonosulfate
-
摘要: 基于过硫酸盐(peroxymonosulfate,PMS)活化的高级氧化技术在降解新污染物方面具有独特优势. 本实验利用碳纳米管(carbon nanotubes,CNT)搭载Ni-ZIF-8,设计制备了CNT/Ni-ZIF-8纳米复合电催化膜,开展了活化过硫酸盐降解磺胺甲噁唑(sulfamethoxazole,SMX)的性能和机理研究. 探究了制备条件与纳米复合膜理化性质间的构效关系,分析并优化了镍的掺杂量,考察了降解实验参数(如电压、流速和PMS用量等)对SMX降解动力学的影响. 研究表明,Ni-ZIF-8均匀地负载在碳纳米管表面. 在最佳条件时(镍掺杂量为20%、电压为−1.5 V、流速为1.5 mL·min−1和PMS用量为1.5 mmol·L−1),单次流模式下去除5 mg·L−1 SMX的效率为76.6%. 电子顺磁共振谱和淬灭实验结果表明,·OH和1O2均参与到SMX的降解过程中. 本研究为开发高效电催化膜催化材料提供了新的设计思路.Abstract: Peroxymonosulfate (PMS) activation-based advanced oxidation technology has attracted wide attention toward the decontamination of emerging contaminants. In this study, carbon nanotubes (CNT) were used to host Ni-ZIF-8 to construct CNT/Ni-ZIF-8 electrocatalytic membranes. Their catalytic performance and mechanism for persulfate activation and degradation of sulfamethoxazole (SMX) were studied systematically. The correlation between preparation parameters and physicochemical properties of the catalytic membranes were investigated. The doping amount of nickel was analyzed and optimized. The effects of operational parameters (such as voltage, flow rate and PMS dosage) on the SMX degradation kinetics were identified. Results suggested that Ni-ZIF-8 nanoparticles were uniformly loaded onto the CNT surface. Under optimal conditions (e.g., Ni doping of 20%, applied voltage of −1.5 V, flow rate of 1.5 mL·min−1 and PMS dosage of 1.5 mmol·L−1), 76.6% removal of 5 mg·L−1 SMX removal can be obtained under single-pass mode. Electron paramagnetic resonance(EPR) and radical quenching tests collectively suggested both ·OH and 1O2 were involved into the SMX degradation process. This study provides new insights on the development of high-performance electrocatalytic membranes for water treatment applications.
-
Key words:
- carbon nanotubes /
- metal-organic framework /
- peroxymonosulfate /
- advanced oxidation /
- sulfamethoxazole.
-
羟胺作为重要的活性氮化合物,在地球氮循环中起着至关重要的作用[1-3]. 大量研究表明多种氨氧化微生物催化的氨氧化[4-5],氮固化[6]、硝化和反硝化[7]等过程中均有羟胺化合物的产生,为了深入了解羟胺在地球氮循环中的作用,研究羟胺在环境中的迁移转化是十分必要的.
NOM作为环境中普遍存在的复杂有机混合物,包含羟基、酮基、羧基等多种活性基团[8-9],对多种含氮化合物的环境迁移转化有着重要影响. 例如,环境中的苯胺化合物可以共价结合NOM分子[10];氨作为农业土壤氮肥中含量最丰富的一种形式,可与NOM结合而被称之为氨固化[11]; 3,4-二氯苯胺是敌草隆除草剂降解过程中产生的主要代谢物,它能够不可逆地与NOM结合,从而降低其毒性[12]. 在NOM与上述含氮化合物的相互作用过程中,NOM的醛、酮官能团被认为是主要的作用位点.
羟胺也可以与羰基反应生成肟类产物[13],已有多篇研究报道了羟胺与NOM的相互作用以探究NOM对羟胺的吸收作用[14]或测定含羰基的NOM组分[15]. Thorn等通过液体15N NMR光谱法对羟胺衍生的NOM产物进行了表征,证明肟类化合物是其主要衍生物[16]. 然而,由于NOM组成极其复杂,传统的方法很难分离羟胺衍生的NOM组分从而获得更全面的分子信息. 因此,尽管羟胺衍生的NOM的分子组成对环境化学家更好地理解有机质对全球氮循环中羟胺转化的影响具有重要意义,但到目前为止尚未见报道.
FTICR-MS,因其具有超高的质量检测准确度和分辨率,目前已成为表征NOM[17]及其消毒副产物[18]分子组成的重要分析工具. 通过对NOM中存在的小分子有机物的精确质量数测定,从而获得其分子式信息,在此基础上,通过各种可视化图分析,可进一步区分NOM分子所属化合物种类,如脂类、木质素类、鞣酸类、稠环芳烃类等,还可进一步分析化合物的疏水性、芳香度、不饱和度等性质[19-20]. 基于此,本研究采用FTICR-MS对羟胺衍生的NOM产物进行分子表征,采用15N同位素标记的羟胺作为起始反应物,以保证所得到的15N同位素标记羟胺衍生NOM产物能排除NOM中其他组分的干扰,从而被特异性地识别检测;同时考察了时间对羟胺与NOM反应的影响.
1. 材料与方法(Materials and Methods)
1.1 试剂与样品制备
15N标记盐酸羟胺 (H215NOH.HCl, >98%) 购置于 Sigma-Aldrich 公司(Steinheim, Germany),NOM标准品购置于美国腐殖酸学会,超纯水制备于Milli-Q system (Millipore, Milford, MA, USA),甲醇 (色谱纯) 购置于Fisher Scientific 公司(Fair Lawn, N.J., USA),其他试剂均为国产分析纯试剂.
称取2.0 mg NOM标准品溶解于100 mL超纯水中制备成20.0 mg·L−1 NOM储备液. 取10 mL NOM储备液4份,分别加入50倍质量过量的15N标记盐酸羟胺,在室温条件分别振荡反应2、4、8、10 h,然后,采用全自动固相萃取装置(睿科公司,厦门)和安捷伦Bond Elut PPL固相萃取柱((0.5 g/6 mL, Varian, Palo Alto, CA, U.S.A.)对上述样品进行固相萃取以去除残留的15N标记盐酸羟胺并富集浓缩样品[21],具体操作步骤如下:(1)用甲酸调节反应样品 pH至2.0;(2)在固相萃取装置上安装好PPL柱,先后用 12 mL 甲醇(色谱纯)和 12 mL 0.1%的甲酸水溶液淋洗活化柱子;(3)PPL柱缓慢加入10 mL样品,样品以1 mL·min−1 的流速通过固相萃取柱以富集目标化合物;(4)样品流完后加入 12 mL 0.1% 甲酸水溶液淋洗柱子,以除去不保留成分;(5)氮吹干燥柱子,然后用 12 mL 甲醇洗脱,收集洗脱液;(6)氮吹洗脱液至甲醇完全挥发,FTICR-MS测定前用 1 mL甲醇溶解.
1.2 设备
FTICR-MS(Solarix 15T, Infinity cell,Bruker Daltonik, GmbH, Bremen, Germany)配备电喷雾/基质辅助激光解吸双离子源(ESI/MALDI). 本研究均采用ESI 源进行样品离子化,进样方式采用直接连续进样,进样流速为120 μL·h−1;离子源喷针电压设置为 4.0 kV,样品采用负离子宽谱扫描模式进行分析,离子累积时间设置为0.06 s,四百万字节时域采集瞬变模式,每个样品采集300扫描并叠加(每个样品重复测定3次); 质量扫描范围(m/z)100—1600. 仪器测定样品前,采用10 mmol·L−1 甲酸钠(50%异丙醇水溶液)校准液进行外标校准,样品测定后获得数据采用自制的NOM中常见已知CHO分子式列表作为内标校准文件进行进一步的内标校准,校准后的质量误差均小于百万分之0.5. 质谱数据采用Data Analysis软件进行分析 (Bruker Daltonics, version 5.3).
1.3 分子式匹配方法
采用Data Analysis (Bruker Daltonics, version 5.3)软件对所得数据进行质谱峰确认和可能分子式匹配,分子式匹配条件如下:,确认质谱峰信噪比(S/N)大于等于4,质量检测误差值小于等于百万分之0.5,仅考虑C、H、O、N、S元素,元素个数范围设置如下:12C (0—∞), 1H (0—∞), 16O (0—∞), 14N (0—3 ), 15N (0—2 ), and 32S (0—1);进一步采用如下规则[22] 对得到的可能分子式进行进一步筛选:氢碳比值(H/C)范围: 0.3<H/C<2.2,氧碳比值范围(O/C):O/C<1.2,不饱和度(DBE)值需为整数且小于40,分子式组成满足偶氮规则,同时H、C、N元素个数满足:H<=2C+2+N,如果一个质核比(m/z)离子有多个可能分子式时,采用杂元素之和最小规则[23]筛选出正确分子式(即选择N、S元素个数之和最小的分子式是正确的),保留3次重复测定结果中共同鉴定到的分子式结果并转换成Excel表数据进行作图分析.
根据已有文献报道,计算每个分子式的不饱和度减氧元素个数值(DBE-O)[24],修正芳香指数(AI-mod) [25];根据AI-mod 和 H/C 值范围将所得分子式分子划分为4类[26]: 第一类(Group 1)属于燃烧源稠环多环芳烃类化合物 (AI_mod > 0.66), 第二类(Group 2)属于维管植物源多酚类化合物 (0.66 ≥AI_mod > 0.5), 第三类(Group 3)属于高不饱和酚类化合物(AI_mod ≤ 0.50 and H/C <1.5), 第四类(Group 4)属于脂肪族化合物 (2.0 ≥ H/C ≥ 1.5).
2. 结果与讨论(Results and Discussion)
2.1 FTICR-MS检测15N同位素标记羟胺衍生化NOM产物
羟胺作为活性氮化合物可直接与NOM中的含羰基分子反应形成多种羟胺衍生化NOM产物[16],然而,由于NOM中本身含有的含氮化合物同分异构体的存在,导致羟胺衍生化NOM产物很难被FTICR-MS特异性识别检测. 本研究采用15N同位素标记羟胺作为反应物,当与NOM发生反应后形成15N同位素标记羟胺衍生化NOM产物,而NOM本身含氮分子的15N同位素峰通常掩盖在FTICR-MS的噪音信号以下,不会对15N同位素标记羟胺衍生化NOM产物的质谱信号造成干扰,从而能在FTICR-MS检测时特异性识别此类产物. 实验结果如图1 所示. 以质谱图标称m/z 389和m/z 460为例,可以看到,当NOM与15N同位素标记羟胺在室温条件下反应10 h后,与原NOM样品的质谱图相比(图1 A、C),明显有15N同位素标记羟胺衍生化NOM产物峰出现(图1 B、D),且这些质谱峰不受NOM中其他离子峰干扰,产物分子式种类主要包括CHO15N1, CHO15N2, CHOS115N1 和 CHON115N1等4类. 以上实验结果表明,当NOM与15N同位素标记羟胺反应10 h后,会明显产生15N同位素标记羟胺衍生化NOM产物,且这些产物峰可以被FTICR-MS特异性检测识别.
 图 1 NOM样品FTICR-MS质谱图Figure 1. Mass spectra of NOM at nominal m/z 389 (A) and m/z 460 (C); Mass spectra of NOM reacting with -labelled hydroxylamine in 10 h, at nominal m/z 389 (B), at nominal m/z 460(D). Molecular formulas of the detected 15N- labelled-hydroxylamine derivatized-NOM components were listed under the spectra(A)标称m/z 389, (C) 标称m/z 460;NOM与15N标记羟胺反应10 h后的样品FTICR-MS质谱图(B)标称m/z 389, (D) 标称m/z 460. 15N标记羟胺衍生NOM产物分子式标记在谱图下方
图 1 NOM样品FTICR-MS质谱图Figure 1. Mass spectra of NOM at nominal m/z 389 (A) and m/z 460 (C); Mass spectra of NOM reacting with -labelled hydroxylamine in 10 h, at nominal m/z 389 (B), at nominal m/z 460(D). Molecular formulas of the detected 15N- labelled-hydroxylamine derivatized-NOM components were listed under the spectra(A)标称m/z 389, (C) 标称m/z 460;NOM与15N标记羟胺反应10 h后的样品FTICR-MS质谱图(B)标称m/z 389, (D) 标称m/z 460. 15N标记羟胺衍生NOM产物分子式标记在谱图下方2.2 15N同位素标记羟胺衍生化NOM产物的分子组成分析
为了进一步分析羟胺衍生化NOM产物的分子组成,对整个质谱数据依据1.3节部分描述进行分子式匹配和筛选,得到所有检测到的15N同位素标记羟胺衍生化NOM产物的分子式结果. 分析结果如图2所示,共鉴定到2137个15N同位素标记羟胺衍生化NOM产物分子式(图2B),其中,包括CHO15N1分子式1346个(约占鉴定总数的63%),CHO15N2分子式194个(约占鉴定总数的9%),CHON115N1分子式221个(约占鉴定总数的10%),CHOS115N1分子式376个(约占鉴定总数的18%). 而对于反应前的NOM样品,共鉴定到CHO分子式2902个(约占鉴定总数的51%),CHON1分子式929个(约占鉴定总数的17%),CHOS1分子式1831个(约占鉴定总数的32%). 通过比较分析,可以看到,约40%以上的NOM中的CHO分子组分可以与15N同位素标记羟胺发生反应形成CHO15N1羟胺衍生NOM产物,而仅有低于7%的NOM中的CHO分子组分可以形成CHO15N2羟胺衍生NOM产物;对于NOM中的CHON1和CHOS1分子组分,仅有约23.7%的CHON1和约20.7%的CHOS1分子组分可与羟胺反应形成相应的CHON115N1 和CHOS115N1产物. 据此,可以推测,这些与羟胺反应的NOM分子中很可能至少含有一个羰基基团. Baluha等的研究表明,苏万尼河富里酸中约39%的CHO分子组分含有一到两个醛基或者酮基基团[27],此研究结果为本研究的推测提供了支持证据. 而形成CHO15N2羟胺衍生物的数目较少的原因可能是由于空间位阻、氢键作用或者电荷效应等导致NOM的CHO分子很难与两个羟胺分子连续发生反应.
 图 2 NOM与15N标记羟胺反应前(A)后(B)鉴定到的分子式数目和占比图;NOM样品(C)和NOM与15N标记羟胺反应10 h后(D)鉴定分子式的Van Krevelen图Figure 2. Number and percentage of molecular formulas identified in NOM (A) and NOM reacting with 15N-labelled hydroxylamine in 10 h (B); Van Krevelen diagrams of the identified formulas in NOM (C) and NOM reacting with 15N- labelled hydroxylamine in 10 h (D)
图 2 NOM与15N标记羟胺反应前(A)后(B)鉴定到的分子式数目和占比图;NOM样品(C)和NOM与15N标记羟胺反应10 h后(D)鉴定分子式的Van Krevelen图Figure 2. Number and percentage of molecular formulas identified in NOM (A) and NOM reacting with 15N-labelled hydroxylamine in 10 h (B); Van Krevelen diagrams of the identified formulas in NOM (C) and NOM reacting with 15N- labelled hydroxylamine in 10 h (D)通过Van Krevelen (VK)图分析,可以进一步推测化合物的理化属性和分子种类,通过AI_mod 和 H/C值的范围可以将化合物划分为4类[26] (如图2C、D所示). 可以看到,15N同位素标记羟胺衍生化NOM产物绝大部分属于维管植物源多酚类(Group 2)和高不饱和酚类化合物(Group 3)(图2D);与原始NOM样品的VK图(图2C)比较发现,NOM组分在VK图上的点分布范围几乎完全覆盖羟胺衍生化NOM产物组分的点分布,表明羟胺衍生化NOM产物组分的H/C 和O/C值与原NOM组分相比没有发生较大变化,对这一结果的可能解释是羟胺衍生化NOM产物很可能是通过羟胺与NOM组分所含的羰基发生肟化反应形成[16],因为发生肟化反应时,羟胺衍生化NOM产物分子式与原NOM分子相比H元素个数仅增加了1,O元素个数无变化,同时增加了1个15N元素. 为了进一步证明此推测,基于肟化反应,根据羟胺衍生化NOM产物分子式还原出相应的NOM反应物分子式,如果被还原出的分子式在原NOM样品中被鉴定到,则被定义为母-子分子对,同时认为此产物应该是通过肟化反应产生的. 通过数据分析发现(结果如图3A所示),对于CHO15N1羟胺衍生化NOM产物,可以找到1160个母-子分子对(约占总数的86.1%),对于CHO15N2羟胺衍生化NOM产物,共鉴定到172个母-子分子对 (约占总数的86.4%),对于CHON115N1羟胺衍生化NOM产物,共鉴定到198个母-子分子对 (约占总数的89.6%),对于CHOS115N1羟胺衍生化NOM产物,共鉴定到357个母-子分子对 (约占总数的94.9%). 此结果表明,86%以上的羟胺衍生化NOM产物很可能是通过肟化反应形成.
 图 3 (A)基于肟化反应的母子-分子对个数和百分比图;(B)NOM中CHO分子以及与羟胺反应10 h形成CHO15N1 和 CHO15N2产物的CHO分子的VK图,(C)NOM中CHON1分子以及与羟胺反应10 h形成CHON115N1产物的CHON1分子的VK图,(D)NOM中CHOS1分子以及与羟胺反应10 h形成CHOS115N1产物的CHOS1分子的VK图Figure 3. (A) Number and percentage of the precursor-product molecule pairs based on oximation reaction; (B) Van Krevelen diagrams of CHO formulas in NOM, precursors of CHO15N1 and CHO15N2 formulas obtained in NOM reacting with 15N-labelled hydroxylamine in 10 h; (C) Van Krevelen diagrams of CHON1 formulas in NOM and precursors of CHON115N1 formulas obtained in NOM reacting with 15N- labelled hydroxylamine in 10 h; (D) Van Krevelen diagrams of CHOS1 formulas in NOM and precursors of CHOS115N1 formulas obtained in NOM reacting with 15N- labelled hydroxylamine in 10 h
图 3 (A)基于肟化反应的母子-分子对个数和百分比图;(B)NOM中CHO分子以及与羟胺反应10 h形成CHO15N1 和 CHO15N2产物的CHO分子的VK图,(C)NOM中CHON1分子以及与羟胺反应10 h形成CHON115N1产物的CHON1分子的VK图,(D)NOM中CHOS1分子以及与羟胺反应10 h形成CHOS115N1产物的CHOS1分子的VK图Figure 3. (A) Number and percentage of the precursor-product molecule pairs based on oximation reaction; (B) Van Krevelen diagrams of CHO formulas in NOM, precursors of CHO15N1 and CHO15N2 formulas obtained in NOM reacting with 15N-labelled hydroxylamine in 10 h; (C) Van Krevelen diagrams of CHON1 formulas in NOM and precursors of CHON115N1 formulas obtained in NOM reacting with 15N- labelled hydroxylamine in 10 h; (D) Van Krevelen diagrams of CHOS1 formulas in NOM and precursors of CHOS115N1 formulas obtained in NOM reacting with 15N- labelled hydroxylamine in 10 h通过对上述鉴定到的羟胺衍生化NOM产物的母分子的VK图分析发现(图3B、C、D),H/C值范围在0.4—1.4同时O/C值范围在0.3—0.9的NOM CHO分子,H/C值范围在0.6—1.1同时O/C值范围在0.5—0.75的NOM CHON1分子,以及H/C值范围在0.7—1.5同时O/C值范围在0.42—0.9的NOM CHOS1分子更容易与15N同位素标记羟胺反应形成单肟产物,且这些分子大部分属于维管植物源多酚和高不饱和酚类化合物;而H/C 值范围在0.6—1.2同时O/C值范围在0.3—0.7的NOM CHO分子可以与羟胺形成双肟产物. 其他被检测到的NOM分子,如H/C值大于1.4或者O/C值大于0.9的NOM CHO分子,H/C值大于1.1或者O/C值大于0.75的NOM CHON1分子,以及H/C 值大于1.5或者O/C值大于0.9的NOM CHOS1分子,在此实验条件下不与羟胺发生反应形成肟化产物. 此实验结果表明,低H/C值和O/C值NOM组分可能具有较高的羟胺反应活性. 低H/C值和O/C值意味着分子具有较高的不饱和度和较低的氧化度,据此可以推测,这些分子可能含有更多的羰基基团和较少的羧基基团,从而导致其对羟胺的反应活性较高.
2.3 反应时间对15N同位素标记羟胺衍生化NOM产物的影响
为了进一步研究NOM组分对羟胺的反应活性,实验考察了反应时间对15N同位素标记羟胺衍生化NOM产物的影响,过量的羟胺与NOM在室温条件下分别反应0、2、4、8、10 h后,分别过固相萃取柱进行浓缩萃取并进行FTICR-MS检测. 本研究主要关注CHO15N1类羟胺衍生NOM产物,由于此类产物的占比较高. 所得质谱结果的部分质谱图如图4所示,可以看到,有一些15N同位素标记羟胺衍生化NOM产物的峰强度会随反应时间的增加而逐渐增大(图4A),对应其NOM反应物的峰强度随时间延长而降低(图4D),这一结果较容易解释,即随着反应时间的延长,反应物的量会随着产物量的增加而降低;有一些产物峰强度随反应时间延长没有发生明显变化(图4B),而对应NOM反应物的峰强度却随反应时间延长而降低(图4E),这一结果较为异常,正常情况下,反应物峰强度应该不会发生明显变化,造成此异常结果的原因可能是此类NOM反应物除了生成CHO15N1类产物,还有可能发生了其他化学反应,具体原因有待进一步研究验证;有一些产物峰强度随反应时间增加而降低(图4C),对于其NOM反应物的峰强度在反应2 h后几乎均降低到质谱噪音峰强度水平(图4F),这一结果表明此类NOM反应物在反应2 h后已经反应完全,对应产物峰强度在2 h后进一步降低,推测此类产物有进一步转化为其他产物的可能性. 总之,对于15N同位素标记羟胺衍生化NOM产物而言,在反应10 h后,产物峰强度几乎不再变化. 此结果表明,15N同位素标记羟胺与NOM的反应10 h后可能已达到平衡. CHO15N1类羟胺衍生化NOM产物的形成具有高度的时间依赖性,很可能是由于NOM组分对羟胺的反应活性不同所造成的.
 图 4 15N同位素标记羟胺与NOM反应0, 2, 4, 8 和 10 h后的FTICR-MS质谱图(A)m/z 411.142检测的质谱峰,(B)m/z 499.064检测的质谱峰, (C)m/z 469.127检测的质谱峰, (D) m/z 395.134检测的质谱峰, (E) m/z 483.056检测的质谱峰, (F) m/z 453.119检测的质谱峰Figure 4. Mass spectra of NOM reacting with 15N-labelled hydroxylamine in 0, 2, 4, 8 and 10 h (A) the detected peak at m/z 411.142, (B) at m/z 499.064, (C) at m/z 469.127, (D) at m/z 395.134, (E) at m/z 483.056, (F) at m/z 453.119
图 4 15N同位素标记羟胺与NOM反应0, 2, 4, 8 和 10 h后的FTICR-MS质谱图(A)m/z 411.142检测的质谱峰,(B)m/z 499.064检测的质谱峰, (C)m/z 469.127检测的质谱峰, (D) m/z 395.134检测的质谱峰, (E) m/z 483.056检测的质谱峰, (F) m/z 453.119检测的质谱峰Figure 4. Mass spectra of NOM reacting with 15N-labelled hydroxylamine in 0, 2, 4, 8 and 10 h (A) the detected peak at m/z 411.142, (B) at m/z 499.064, (C) at m/z 469.127, (D) at m/z 395.134, (E) at m/z 483.056, (F) at m/z 453.119本研究进一步比较了反应2 h和10 h的CHO15N1产物的分子组成,结果如图5所示. 可以看到,反应2 h单独鉴定到的CHO15N1类分子式数目为84个,而10 h单独鉴定到314个,两个时间点共同鉴定到的分子式数目为1032个(图5B);VK图结果(图5A)显示,大部分2 h单独鉴定到的分子的O/C值较低,而大部分10 h单独鉴定到的分子的O/C值较高;DBE-O对分子式数目图[24](图5C)显示,10 h单独鉴定到的分子中,DBE-O值偏负的分子数目占比明显高于2 h单独鉴定到的分子,DBE-O值偏负表明分子中氧个数大于双键和环的个数[28]. 此结果表明,一些高氧化且饱和的NOM的CHO化合物对羟胺可能具有较低的反应活性,只有当延长反应时间时才可能形成羟胺衍生化NOM产物.
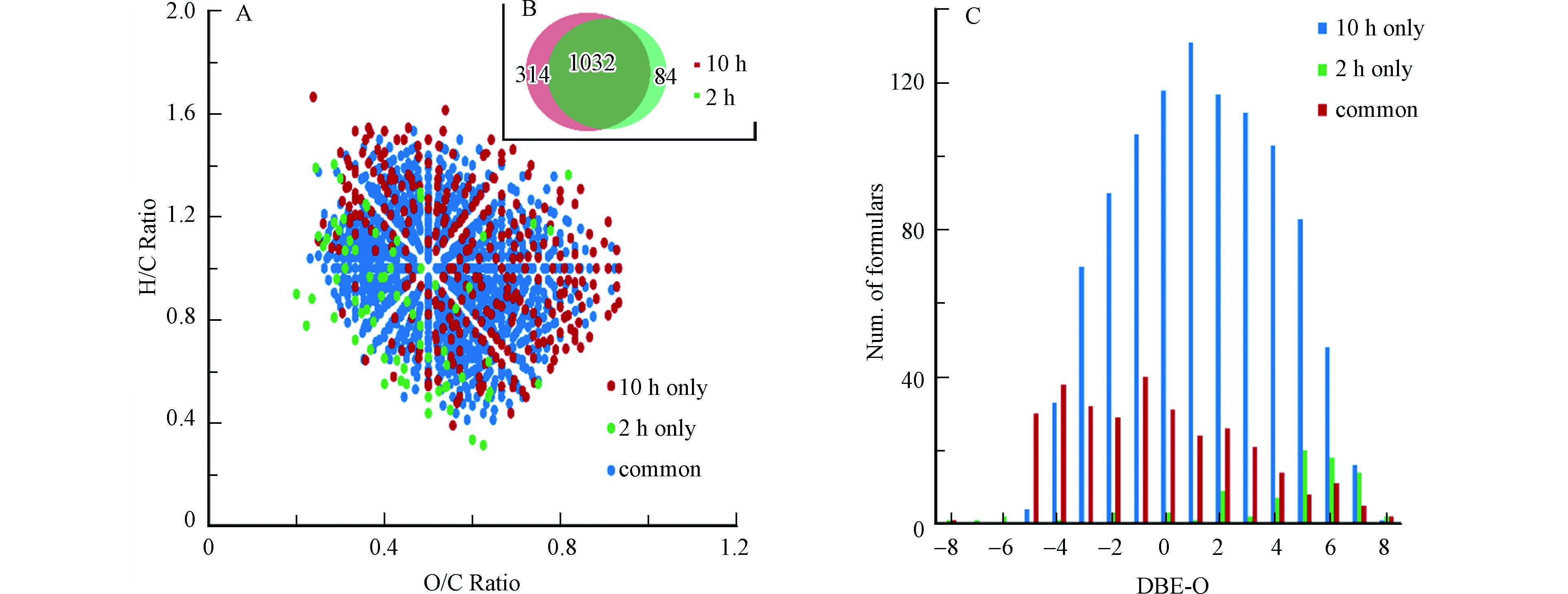 图 5 15N同位素标记羟胺与NOM反应2 h和10 h的CHO15N1产物的分子组成比较Figure 5. Comparison of the identified CHO15N1 formulas in NOM reacting with 15N-labelled hydroxylamine in 2 h and 10 h(A)VK图,(B)分子式数目比较图,(C)DBE-O对分子式数目图(A) Van Krevelen diagrams, (B) the number of the obtained formulas and (C) the plot of DBE-O vs. number of formulas
图 5 15N同位素标记羟胺与NOM反应2 h和10 h的CHO15N1产物的分子组成比较Figure 5. Comparison of the identified CHO15N1 formulas in NOM reacting with 15N-labelled hydroxylamine in 2 h and 10 h(A)VK图,(B)分子式数目比较图,(C)DBE-O对分子式数目图(A) Van Krevelen diagrams, (B) the number of the obtained formulas and (C) the plot of DBE-O vs. number of formulas对于反应2 h和10 h共同鉴定到的CHO15N1产物的分子,为了考察反应时间对其影响,同一产物离子在10 h的质谱峰强度除以其在2 h的质谱峰强度被定义为该离子的相对峰强度(RI),为了减小测定误差的影响,RI值小于等于0.8被定义为该离子的峰强度在反应10 h时明显小于反应2 h的峰强度,代表该类产物在反应10 h的产量低于其在2 h 的产量;RI值大于0.8且小于1.2被定义为该离子的峰强度在反应10 h时与其反应2 h的峰强度无明显差异,代表该类产物在反应10 h与在2 h 的产量相当;RI值大于等于1.2被定义为该离子的峰强度在反应10 h时明显大于其反应2 h的峰强度,代表该类产物在反应10 h的产量大于其反应2 h的产量. 通过分析发现,对于1032个共同鉴定到的CHO15N1产物的分子(结果如图6B所示),RI值大于等于1.2的分子式有613个(约占总数的60%),RI值在0.8—1.2之间的分子式有364个(约占总数的35%),而RI值小于等于0.8的分子式仅有55个(约占总数的5%). 此结果表明,有60%共同鉴定分子的产量随反应时间的延长而增大,说明产生此类产物的NOM反应物可能由于反应活性较弱,并不能在较短反应时间内与羟胺反应完全,而延长反应时间会增加羟胺衍生NOM产物的产量;有35%共同鉴定分子的产量随反应时间的延长无明显变化,说明产生此类产物的NOM反应物可能由于反应活性较强,在较短反应时间内便能与羟胺反应完全形成单肟化产物或随时间延长进一步形成其他产物;而仅有5%共同鉴定分子的产量随反应时间的延长而降低,说明产生此类产物的NOM反应物可能含有多个羰基基团,随反应时间延长可能进一步生成多肟化产物或其他不稳定产物,从而导致这些单肟化产物随反应时间延长而产量下降.
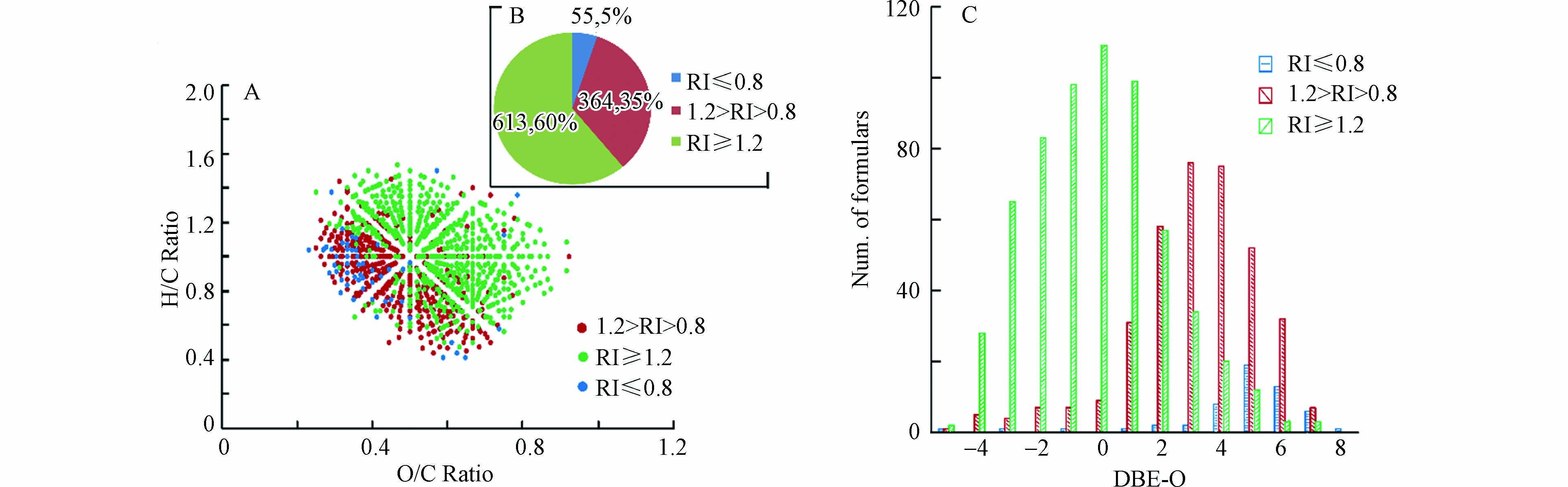 图 6 15N同位素标记羟胺与NOM反应2 h和10 h共同鉴定的不同RI值的CHO15N1产物的分子组成比较Figure 6. Comparison of the commonly identified CHO15N1 formulas with different RI values in NOM reacting with 15N-labelled hydroxylamine in 2 h and 10 h(A)VK图,(B)分子式数目比较图,(C)DBE-O对分子式数目图.(A) Van Krevelen diagrams, (B) the number and percentage of the obtained formulas and (C) the plot of DBE-O vs. number of formulas
图 6 15N同位素标记羟胺与NOM反应2 h和10 h共同鉴定的不同RI值的CHO15N1产物的分子组成比较Figure 6. Comparison of the commonly identified CHO15N1 formulas with different RI values in NOM reacting with 15N-labelled hydroxylamine in 2 h and 10 h(A)VK图,(B)分子式数目比较图,(C)DBE-O对分子式数目图.(A) Van Krevelen diagrams, (B) the number and percentage of the obtained formulas and (C) the plot of DBE-O vs. number of formulasVK图和DBE-O对分子式数目图结果(图6A、C)显示,RI值小于1.2的共同鉴定分子大部分具有较低的O/C值且DBE-O值偏正的分子式数目较多,而RI值大于等于1.2的共同鉴定分子大部分具有较高的O/C值且DBE-O值偏负的分子式数目较多,此结果说明高氧化度高饱和的NOM CHO分子对羟胺的反应活性相对较弱,需要较长的反应时间才能反应完全,而低氧化度高不饱和的NOM CHO分子对羟胺的反应活性相对较强,其反应完全时间较短甚至有些可以生成其他衍生产物.
事实上,RI值小于等于0.8的共同鉴定分子的进一步肟化产物确实在此研究实验中被检测到,图7A是检测质谱结果的一个举例;约有29%的此类分子可以进一步与羟胺反应形成双肟化产物,而其他71%的分子可能并不稳定或转化成其他产物(图7B).
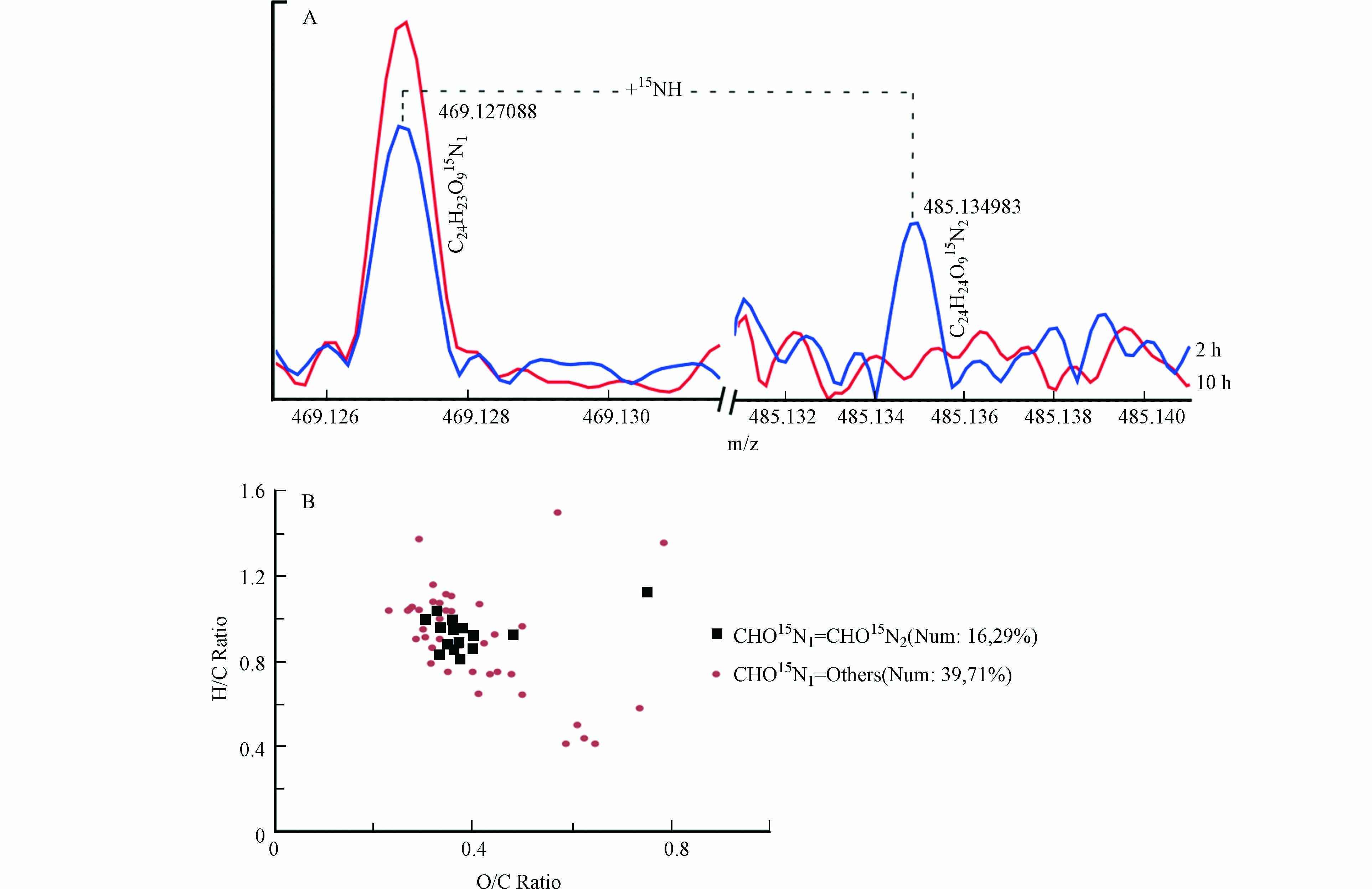 图 7 (A)15N同位素标记羟胺与NOM反应2、10 h后的FTICR-MS质谱图m/z 469.127和m/z 485.134;(B)形成双肟化产物或者其他产物的RI值小于等于0.8的共同鉴定CHO15N1产物的VK图Figure 7. (A) Mass spectra of NOM reacting with 15N-labelled hydroxylamine in 2 and 10 h at m/z 469.127 and m/z 485.134; (B) Van Krevelen diagrams of formulas with RI lower than 0.8 formed dioxime products and other products
图 7 (A)15N同位素标记羟胺与NOM反应2、10 h后的FTICR-MS质谱图m/z 469.127和m/z 485.134;(B)形成双肟化产物或者其他产物的RI值小于等于0.8的共同鉴定CHO15N1产物的VK图Figure 7. (A) Mass spectra of NOM reacting with 15N-labelled hydroxylamine in 2 and 10 h at m/z 469.127 and m/z 485.134; (B) Van Krevelen diagrams of formulas with RI lower than 0.8 formed dioxime products and other products3. 结论 (Conclusion)
羟胺作为地球氮循环过程中重要的活性氮化合物,可以与环境中普遍存在的NOM发生反应,从而转化成其他含氮产物. 本研究采用FTICR-MS超高分辨质谱结合15N同位素标记技术全面表征了羟胺与NOM在自然条件下发生反应的产物分子信息,共鉴定到2000多个羟胺衍生化NOM产物,主要包括CHO15N1、CHO15N2、CHOS115N1和CHON115N1 等4类分子产物,其中大部分产物可能属于维管植物源多分和高不饱和酚类化合物. 86%以上的产物可能是通过肟化反应形成,数据可视化分析表明,高氧化高饱和的NOM CHO化合物可能与羟胺的反应活性较弱,而低氧化高不饱和度的CHO化合物与羟胺的反应活性较强,其中部分可形成双肟化产物或其他产物. 本研究揭示了NOM不同组分对羟胺的反应活性以及相应产物的分子信息,可为深入探究羟胺在地球氮循环过程中的迁移转化和相应转化机制研究提供更全面的基础信息.
-
-
[1] 刘鹏霄, 王旭, 冯玲. 自然水环境中抗生素的污染现状、来源及危害研究进展 [J]. 环境工程, 2020, 38(5): 36-42. doi: 10.13205/j.hjgc.202005007 LIU P X, WANG X, FENG L. Occurrences, resources and risk of antibiotics in aquatic environment: A review [J]. Environmental Engineering, 2020, 38(5): 36-42(in Chinese). doi: 10.13205/j.hjgc.202005007
[2] 齐亚兵. 活化过硫酸盐高级氧化法降解抗生素的研究进展 [J]. 化工进展, 2022, 41(12): 6627-6643. QI Y B. Research progress on degradation of antibiotics by activated persulfate advanced oxidation [J]. Chemical Industry and Engineering Progress, 2022, 41(12): 6627-6643(in Chinese).
[3] DAI Y L, YAO Y, LI M H, et al. Carbon nanotube filter functionalized with MIL-101 (Fe) for enhanced flow-through electro-Fenton [J]. Environmental Research, 2022, 204: 112117. doi: 10.1016/j.envres.2021.112117 [4] 赵玲, 刘恒恒, 胡晴, 等. 金属有机骨架材料 MOF-5 催化吸附 SO2 [J]. 环境化学, 2017, 36(9): 1914-1922. doi: 10.7524/j.issn.0254-6108.2016110901 ZHAO L, LIU H H, HU Q, et al. Synthesis of MOF-5 catalysts and their catalytic oxidation of sulfur dioxide [J]. Environmental Chemistry, 2017, 36(9): 1914-1922(in Chinese). doi: 10.7524/j.issn.0254-6108.2016110901
[5] 李小娟, 廖凤珍, 叶兰妹, 等. 金属有机骨架及其衍生材料活化过硫酸盐在水处理中的应用进展 [J]. 化工进展, 2019, 38(10): 4712-4721. doi: 10.16085/j.issn.1000-6613.2019-0163 LI X J, LIAO F Z, YE L M, et al. Progress in the applications of metal-organic frameworks and derivatives activate persulfate in water treatment [J]. Chemical Industry and Engineering Progress, 2019, 38(10): 4712-4721(in Chinese). doi: 10.16085/j.issn.1000-6613.2019-0163
[6] LIU D, GU W Y, ZHOU L, et al. Recent advances in MOF-derived carbon-based nanomaterials for environmental applications in adsorption and catalytic degradation [J]. Chemical Engineering Journal, 2022, 427: 131503. doi: 10.1016/j.cej.2021.131503 [7] 穆寄林, 徐婕, 赵瑨云, 等. ZIF-8的制备及其光催化降解活性红研究 [J]. 化工新型材料, 2022, 50(8): 219-222. MU J L, XU J, ZHAO J Y, et al. Fabrication of ZIF-8 and its photocatalytic degradation of reactive red [J]. New Chemical Materials, 2022, 50(8): 219-222(in Chinese).
[8] 陈丽华, 杜建斌, 王茀学, 等. ZIF-8 复合物光催化去除水体污染物 [J]. 环境化学, 2022, 41(7): 2149-2161. doi: 10.7524/j.issn.0254-6108.2021031401 CHEN L H, DU J B, WANG F X, et al. Photocatalytic removal of water pollutants in ZIF-8 composites [J]. Environmental Chemistry, 2022, 41(7): 2149-2161(in Chinese). doi: 10.7524/j.issn.0254-6108.2021031401
[9] CHO J H, LEE C, HONG S H, et al. Transition metal ion doping on ZIF-8 enhances the electrochemical CO2 reduction reaction [J]. Advanced Materials (Deerfield Beach, Fla. ), 2022, 2208224. [10] REN L H, MA J X, CHEN M, et al. Recent advances in electrocatalytic membrane for the removal of micropollutants from water and wastewater [J]. IScience, 2022, 25(5): 104342. doi: 10.1016/j.isci.2022.104342 [11] JIN L M, YOU S J, DUAN X G, et al. Peroxymonosulfate activation by Fe3O4-MnO2/CNT nanohybrid electroactive filter towards ultrafast micropollutants decontamination: Performance and mechanism [J]. Journal of Hazardous Materials, 2022, 423: 127111. doi: 10.1016/j.jhazmat.2021.127111 [12] ZHENG W T, LIU Y B, LIU W, et al. A novel electrocatalytic filtration system with carbon nanotube supported nanoscale zerovalent copper toward ultrafast oxidation of organic pollutants [J]. Water Research, 2021, 194: 116961. doi: 10.1016/j.watres.2021.116961 [13] SAEEDIRAD R, GANJALI S T, RASHIDI A, et al. Experimental and computational study of organic sulfur removal proficiency of (Ni, Cu, Co)-doped ZIF-8 adsorbents [J]. ChemistrySelect, 2020, 5(1): 231-243. doi: 10.1002/slct.201903233 [14] WANG K D, WU C, WANG F, et al. In-situ insertion of carbon nanotubes into metal-organic frameworks-derived α- Fe2O3 polyhedrons for highly sensitive electrochemical detection of nitrite [J]. Electrochimica Acta, 2018, 285: 128-138. doi: 10.1016/j.electacta.2018.07.228 [15] ZHOU L, LI N, OWENS G, et al. Simultaneous removal of mixed contaminants, copper and norfloxacin, from aqueous solution by ZIF-8 [J]. Chemical Engineering Journal, 2019, 362: 628-637. doi: 10.1016/j.cej.2019.01.068 [16] SHEN B W, WANG B X, ZHU L Y, et al. Properties of cobalt- and nickel-doped zif-8 framework materials and their application in heavy-metal Removal from wastewater [J]. Nanomaterials (Basel, Switzerland), 2020, 10(9): 1636. doi: 10.3390/nano10091636 [17] LI Z Z, SHEN C S, LIU Y B, et al. Carbon nanotube filter functionalized with iron oxychloride for flow-through electro-Fenton [J]. Applied Catalysis B:Environmental, 2020, 260: 118204. doi: 10.1016/j.apcatb.2019.118204 [18] 张格红, 赵平歌, 廖志鹏, 等. 超声强化铋掺杂氧化铟降解偶氮染料废水 [J]. 环境化学, 2016, 35(3): 526-532. doi: 10.7524/j.issn.0254-6108.2016.03.2015080701 ZHANG G H, ZHAO P G, LIAO Z P, et al. Ultrasonic enhanced degradation of AZO dye wastewater by bismuth doped indium oxide [J]. Environmental Chemistry, 2016, 35(3): 526-532(in Chinese). doi: 10.7524/j.issn.0254-6108.2016.03.2015080701
[19] YANG Y, PIGNATELLO J J, MA J, et al. Comparison of halide impacts on the efficiency of contaminant degradation by sulfate and hydroxyl radical-based advanced oxidation processes (AOPs) [J]. Environmental Science & Technology, 2014, 48(4): 2344-2351. [20] YE Z H, PADILLA J A, XURIGUERA E, et al. A highly stable metal-organic framework-engineered FeS2/C nanocatalyst for heterogeneous electro-Fenton treatment: Validation in wastewater at mild pH [J]. Environmental Science & Technology, 2020, 54(7): 4664-4674. [21] DUAN X G, SUN H Q, WANG S B. Metal-free carbocatalysis in advanced oxidation reactions [J]. Accounts of Chemical Research, 2018, 51(3): 678-687. doi: 10.1021/acs.accounts.7b00535 [22] WANG Y, PAN T, YU Y F, et al. A novel peroxymonosulfate (PMS)-enhanced iron coagulation process for simultaneous removal of trace organic pollutants in water [J]. Water Research, 2020, 185: 116136. doi: 10.1016/j.watres.2020.116136 [23] ZHU L L, JI J H, LIU J, et al. Designing 3D-MoS2 sponge as excellent cocatalysts in advanced oxidation processes for pollutant control [J]. Angewandte Chemie (International Ed. in English), 2020, 59(33): 13968-13976. doi: 10.1002/anie.202006059 [24] LOU X Y, FANG C L, GENG Z N, et al. Significantly enhanced base activation of peroxymonosulfate by polyphosphates: Kinetics and mechanism [J]. Chemosphere, 2017, 173: 529-534. doi: 10.1016/j.chemosphere.2017.01.093 [25] MENG H, NIE C Y, LI W L, et al. Insight into the effect of lignocellulosic biomass source on the performance of biochar as persulfate activator for aqueous organic pollutants remediation: Epicarp and mesocarp of citrus peels as examples [J]. Journal of Hazardous Materials, 2020, 399: 123043. doi: 10.1016/j.jhazmat.2020.123043 [26] NIE G, HUANG J, HU Y Z, et al. Heterogeneous catalytic activation of peroxymonosulfate for efficient degradation of organic pollutants by magnetic Cu0/Fe3O4 submicron composites [J]. Chinese Journal of Catalysis, 2017, 38(2): 227-239. doi: 10.1016/S1872-2067(16)62566-4 -




 下载:
下载: