-
CO2、CH4和N2O作为主要的温室气体,对全球温室效应的贡献率达80%以上[1-2],内陆湖泊是其重要的来源之一[3-6]. 入湖河流输入的营养物质促进湖泊温室气体的产生和排放,同时也将水中溶存的温室气体输入到湖泊,进而影响湖泊中温室气体的溶存浓度[6-7]. 已有研究多关注自然水文状态下湖泊水体温室气体溶存浓度、源汇效应的时间变化特征及其影响因子[3-8],关于调水影响的研究主要关注引水对藻型湖泊N2O排放通量的影响[9],而对调水工程中的调蓄湖库在调水期温室气体的分布特征及影响因素的研究还未见报道. 调水工程调水期多处于枯水期,调水期湖泊水位、水质、水流流向和换水周期均较非调水期有较大变化,而水位和水质变化均会对水体温室气体产生和排放产生影响,同时水位的变化也会降低枯水期入湖河流对湖泊的影响.
南四湖是南水北调东线工程山东段最大的调蓄湖库,对区域环境和气候以及受水区水质安全影响显著. 调水不仅改变了南四湖湖水自北向南的自然流向,也对入湖区的水质造成一定的影响,进而影响温室气体的溶存和分布. 近年来有关南四湖水环境的研究主要集中于污染评价以及调水和区域发展对水环境的影响等方面[10-15],而对南四湖水体温室气体的研究较少,且仅有研究中采样点位较少[16-17]难以有效阐明其空间变化特征和影响因子. 本研究阐明了调水期南四湖及部分入湖河口表层水中温室气体浓度、饱和度和排放通量的空间变化特征,分析了各湖区以及河口区间温室气体的差异,并结合水质指标探讨了调水期南四湖表层水中温室气体溶存的影响因素,研究结果为深入理解调水期调蓄湖库表层水中温室气体的空间变化特征及其影响因子提供基础数据支撑.
-
南四湖由4个相连湖区(南阳湖、独山湖、昭阳湖、微山湖)组成,最大湖面积为1266 km2,兴利库容为63.7×108 m3,其中微山湖面积最大. 南四湖中部的二级坝将其分为上、下两级,上级湖为南阳湖、独山湖、昭阳湖,下级湖则为微山湖. 南四湖正常蓄水位下平均水深1.5 m,湖内分布有大量的水生植物,属典型的浅水草藻型湖泊. 2013年东线工程通水前南四湖富营养化严重,通水后富营养化程度有明显降低[18]. 东线工程一般在非汛期进行调水,2020—2021年度调水期为2020年12月底至2021年5月底,共调水入山东6.74×108 m3,由南四湖对其进行调蓄分配.
-
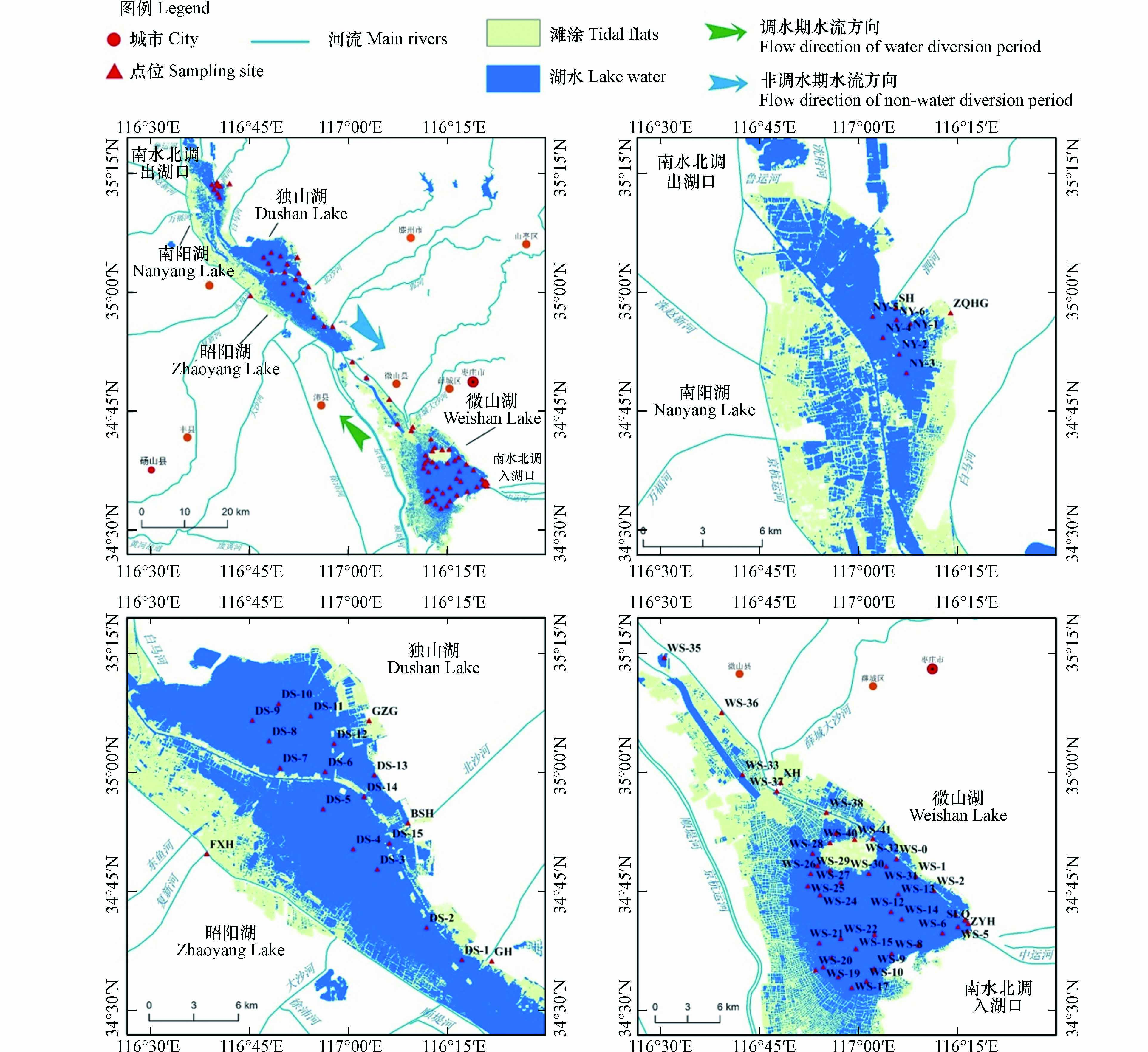
在南四湖布设63个采样点,其中微山湖(WS)42个,南阳湖(NY)6个,因独山湖与昭阳湖无明显分界线,故将两湖合并记作DS,共15个采样点;在9条主要入湖河流的河口布设采样点,分别为复新河(FXH)、北沙河(BSH)、胜利渠(SLQ)、泗河(SH)、薛河(XH)、郭河(GH)、中运河(ZYH)、仲浅横沟(ZQHG)和耿庄沟(GZG);各采样点具体分布见图1. 考虑水体的稳定性和均匀性并避开冰封期,于2021年3月11日—13日在各采样点采集水面下20 cm的表层水,现场采用顶空平衡法 [19]提取溶解气体,即将水样注入两头具有硅胶密封垫和密封螺帽的100 mL有机玻璃管内,并使其溢出一定体积的水后密封,从顶端用注射器注入50 mL高纯氮气,同时从底端通过针头排出同体积的水样,振荡10 min后静置1 h抽取顶空气体,储存于气体采样袋(大连海得)内;每个采样点采集3个平行,每次采样均重新采集表层水,同时使用气体采样袋直接采集现场1.0 m高度的空气样品;气体采样袋使用前经高纯N2多次清洗并抽真空;另取水样用于理化指标分析. 使用HI9145型DO仪(意大利HANNA公司)、pH400型pH计(美国SPECTRUM公司)、自制水深测量装置和塞氏盘现场测定水温(WT)、溶解氧(DO)、pH、水深(WD)和透明度(SD).
回实验室后,使用美国Agilent公司7890A型气相色谱仪测定气体中N2O、CO2和CH4的浓度,采用国家标准分析方法测定水中叶绿素a(Chl-a)、硝态氮(NO3−)、亚硝态氮(NO2−)、氨氮(NH3)、可溶性正磷酸盐(DIP)、高锰酸盐指数(CODMn)、总氮(TN)和总磷(TP)等[20],溶解性有机碳(DOC)采用德国Elementar公司的总TOC分析仪测定.
-
水中温室气体溶存浓度(CW, μmol·L−1)的计算公式为[21]:
式中,
CA1 为有机玻璃管中水—气交换平衡时顶空气体中温室气体浓度(μmol·L−1);VA1 为管中顶空空气体积(L);Vw 为管中水样的体积(L);α为布氏系数(mol·L−1·atm−1).温室气体水—气界面的排放通量(F)采用薄边界层扩散模型法计算,计算公式为[22-23]:
式中,
ΔC 为水—气界面温室气体浓度的差值,ΔC=Cw−CA2 ,CA2 为采样点大气中温室气体浓度(μmol·L−1);k为扩散系数[22]. F为正值代表气体自水向空气扩散.采用SPSS 25.0中Pearson相关模型探讨了影响温室气体浓度的主要因子;采样图和温室气体浓度和排放通量的空间分布图采用ArcGIS10.6绘制;采用Origin 2015拟合并绘制一元线性回归图.
-
如表1所示,调水期南四湖表层水中pH、DO、NH3、CODMn和NO3−平均含量均能达到其功能区域水质标准要求,且除CODMn外(仅微山湖有2个点位超标),pH、DO、NH3和NO3−达标率均为100%.
TP平均含量除独山湖+昭阳湖中略低于Ⅲ类水标准限值外,其余各湖区和河口区均超标,表现为河口区>南阳湖>微山湖,分别约为标准限值的2.2倍、1.9倍和1.5倍,河口区显著高于微山湖(P < 0.05),全湖TP超标率为80.6%. 各湖区和河口区TN平均含量均超标,超标率为97.2%,微山湖和独山湖+昭阳湖TN平均含量均显著高于南阳湖(P < 0.05). 河口区WD较大,且TN、NO3−、NO2−、TP、DIP和Chl-a量较高,反映了入湖河流营养物质输入作用的影响;而微山湖WD和SD均较低,DO含量显著高于其他湖区(P < 0.05),但作为下级湖,水中TN、NO3−、DIP含量亦较高. 各湖区和河口区pH、NH3、DOC和CODMn含量无显著性差异(P > 0.05).
-
如表2所示,南四湖表层水中N2O、CH4和CO2浓度分别为(23.0±6.13)nmol·L−1、(0.15±0.10)μmol·L−1和(52.4±11.4)μmol·L−1,饱和度分别为154%±44.6%、3878%±2668%和186%±46.2%,排放通量分别为(0.22±0.18)μmol·m−2·h−1、(3.95±2.73)μmol·m−2·h−1和(658±336)μmol·m−2·h−1. N2O、CH4和CO2均处于高度过饱和状态,表现为大气的“源”. 各湖区间表层水中CH4和CO2平均浓度不存在显著差异(P > 0.05);微山湖N2O平均浓度、饱和度和排放通量均显著低于河口区(P < 0.05),CO2平均饱和度和排放通量亦显著低于其他3个湖区(P < 0.05).
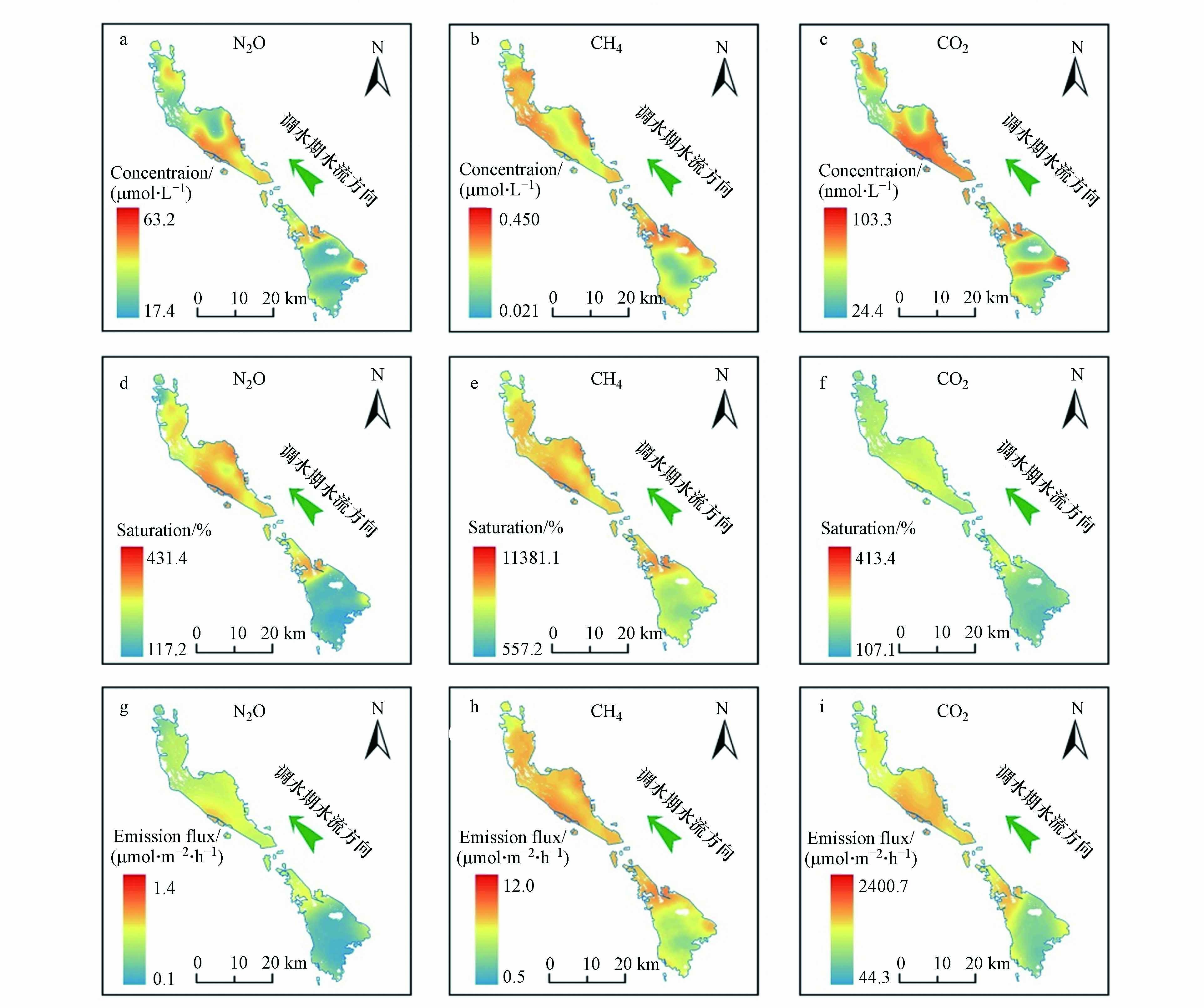
如图2所示,各温室气体溶存浓度、饱和度和排放通量均呈现自上级湖向下级湖降低的趋势,与南水北调水流方向相反,体现了调水对湖水中温室气体的稀释作用;且温室气体浓度在多个河口区和二级坝附近水域出现高值区,但在南水北调工程出水口(NY-6)附近区域,尽管受到泗河等入湖河流的影响但温室气体浓度并不高. 此外,N2O和CO2在微山湖湖心区出现带状高浓度区,而CH4则无此相对高值区且湖心区浓度相对较低. 入湖河口、二级坝上下及岸边区温室气体浓度较高可能是由于浅水湖泊中河流营养物质的输送及沉积的边缘效应所导致的[23],而微山湖湖心区N2O和CO2带状高浓度区的成因则需进一步探讨.
将南四湖温室气体溶存浓度和排放通量与冬季我国部分水体进行了对比分析,如表3所示. 南四湖表层水中N2O浓度与巢湖相当,但明显低于平原河网,而高于北京城市内湖;CH4浓度亦明显低于平原河网,但显著高于西北口水库,而较北京城市内湖低.
南四湖N2O饱和度明显低于平原河网,但CH4饱和度远高于平原河网. 南四湖N2O排放通量与巢湖和东平湖基本相当,高于梅梁湾和鄱阳湖,但显著低于平原河网;CH4排放通量与鄱阳湖相当,高于微山湖、梅梁湾和西北口水库,而显著低于平原河网以及部分城市内湖;与冬季梅梁湾表现为CO2的汇不同,南四湖表现为CO2的排放源,通量高于微山湖和鄱阳湖,但处于城市内湖的变化范围内.
-
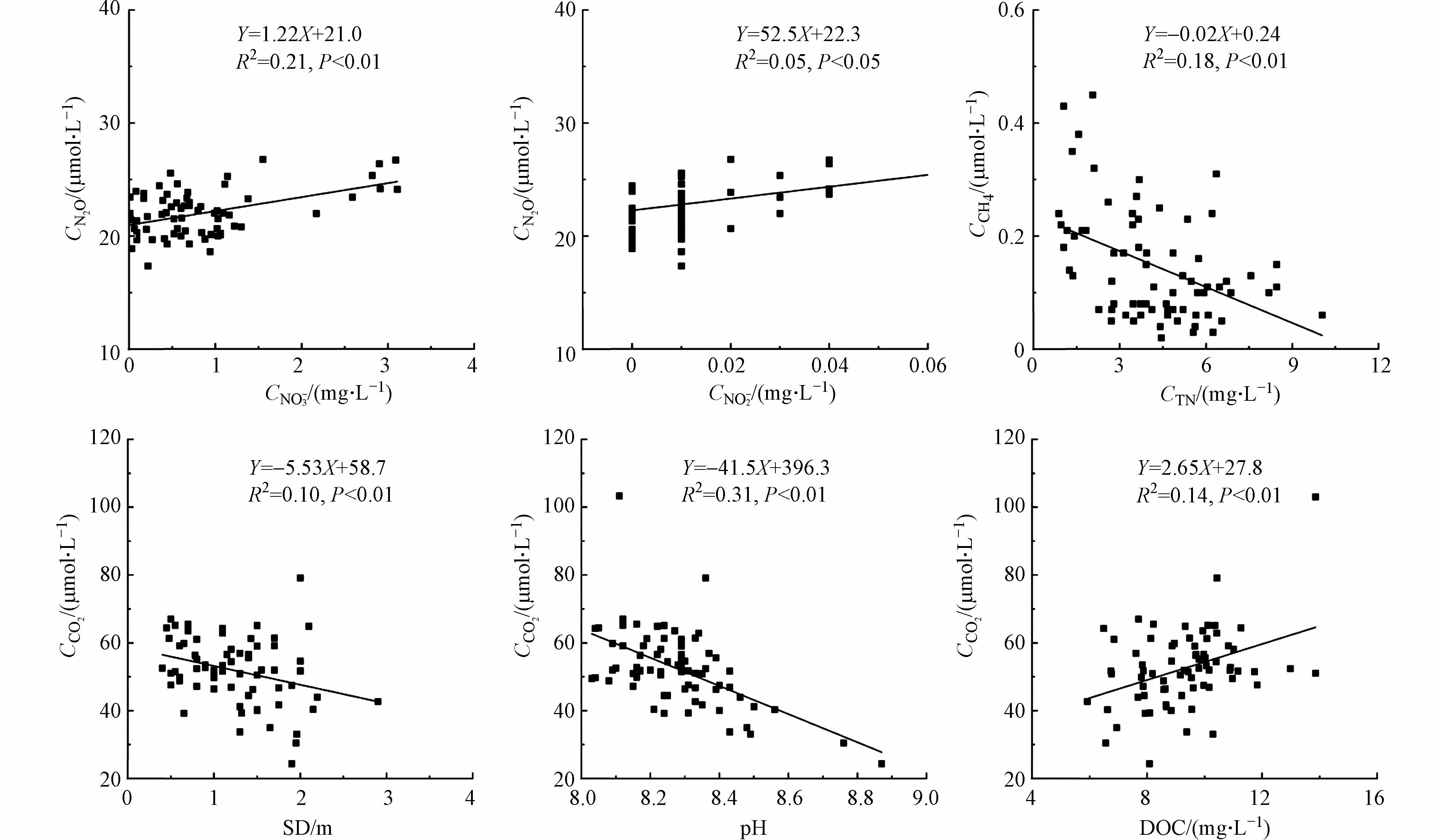
如图3和表4所示,南四湖表层水中各温室气体溶存浓度分别与不同的水质指标呈显著相关关系,且在微山湖湖区和河口区表层水中N2O溶存浓度的影响因子不同. 水体中N2O主要产生于硝化和反硝化过程中[6, 34],NO3−和NH3分别为反硝化作用和硝化作用的底物,NO2−是微生物氮转化过程的中间产物. 南四湖表层水中N2O浓度与NO3−、NO2−浓度呈显著正相关关系(图3),且NO3−和NO2−间呈显著正相关关系(R=0.417,P < 0.01)说明表层水中N2O可能主要来源于沉积物的反硝化过程. 在河口区由于河流带来较为丰富的NH3(表1),且河口区表层中NO2−与NH3呈显著正相关关系(R=0.556,P < 0.01),说明水中硝化作用强烈,推断该区域水体溶存的N2O主要产生于硝化过程;而在微山湖,N2O则主要来源于反硝化过程,水深增加导致水中DO降低有利于增强表层沉积物的反硝化作用,促进了水中N2O浓度增加,使二者呈显著正相关关系(表4);3月份南四湖水体中优势沉水植物-菹草正处于返青生长期,SD的增加会增强其光合作用,提高水中DO含量,抑制表层沉积物的反硝化作用,故二者呈显著负相关关系(表4);而在河口区中,SD的上升可通过影响菹草光合作用,增加水中DO含量,促进底层水和表层沉积物的硝化作用和N2O的产生,使二者呈正相关关系(表4).
水体中CH4浓度是由CH4产生和氧化的相对平衡决定[35]. 作为典型的草藻型湖泊,南四湖水生植物丰富,植物衰亡后残体沉积在底泥中,为产甲烷菌提供了丰富的底物[36],促进了水体深层和底泥中CH4的产生,并扩散进入上覆水,导致表层水中浓度较高[2];而TN的抑制作用则有可能与无机氮对产甲烷细菌的毒害作用有关[37],同时硝酸盐是更有利的末端电子受体[38],硝酸盐浓度亦影响CH4的产生.
水中CO2浓度主要受到水体碳酸平衡、光合作用以及呼吸作用等作用的影响. 3月份南四湖浮游藻类较少,SD大有利于菹草的生长,菹草的光合作用导致水中CO2浓度降低,使二者呈显著负相关关系(图3). DOC作为CO2产生的底物,含量增加会促进CO2的产生,故二者呈显著正相关关系(图3). 南四湖湖水最小pH为8.03,全湖水体为偏碱性,水中CO2易发生电离,使其浓度降低,两者呈显著负相关关系(图3),这与其他研究结果相一致[39-40].
-
(1)调水期南四湖表层水除TP和TN外,pH、DO、NH3和CODMn平均含量均可达到《地表水环境水质标准》Ⅲ类水标准,河流输入导致入湖河口区和下级湖微山湖营养盐含量较高.
(2)调水期南四湖各温室气体呈现过饱和状态,表现为大气的排放源,南水北调对湖水中温室气体具有一定的稀释作用,河口区和二级坝附近水域温室气体浓度较高,此外,微山湖湖心区N2O和CO2浓度较高,且呈带状分布.
(3)调水期南四湖表层水中温室气体浓度与氮浓度、pH、SD、DOC等水质指标间具有一定的显著相关性,各湖区N2O浓度与水中NO3−、NO2−浓度显著正相关,表明其可能主要受到反硝化作用的影响,而河口区N2O浓度与NH3显著正相关,可能主要受硝化作用的影响.
冬季调水期南四湖水体温室气体溶存浓度及其影响因素
Dissolved greenhouse gas concentrations and the influencing factors in Nansi Lake during winter water diversion period
-
摘要: 为了解冬季调水期南四湖表层水中温室气体的溶存浓度及其排放通量,采集南四湖各湖区和主要入湖河流的河口区表层水及气体样品,分析了水体的理化指标以及CO2、CH4和N2O的溶存浓度,采用薄边界层扩散模型法估算了水—气界面排放通量,并探讨了影响调水期南四湖温室气体溶存浓度的主要因子. 结果表明,调水期南四湖表层水中N2O、CH4和CO2浓度分别为(23.0±6.13) nmol·L−1、(0.15±0.10) μmol·L−1和(52.4±11.4) μmol·L−1,均处于高度过饱和状态,排放通量分别为(0.22±0.18) μmol·m−2·h−1、(3.95±2.73) μmol·m−2·h−1和(658±336) μmol·m−2·h−1;浓度和排放通量多与冬季其他湖泊相当,但低于平原河网. 各温室气体浓度、饱和度和排放通量整体呈现自上级湖向下级湖降低的趋势,且在河口区和二级坝附近水域浓度较高,同时N2O和CO2浓度在微山湖湖心区出现带状高值区,而CH4相对较低. 各温室气体浓度与水质参数间具有一定的相关性,其中,N2O浓度与NO3−、NO2−浓度呈显著正相关,CH4与TN呈显著负相关,CO2与pH、SD呈显著负相关,与DOC呈显著正相关,反映了水质对温室气体溶存浓度的影响. 研究结果为评估调蓄湖泊在调水期对大气温室气体的影响提供了基础数据支撑.Abstract: In order to understand the dissolved concentrations and emission fluxes of greenhouse gases (GHGs) in the surface water of Nansi Lake during the water diversion period, gas samples and surface water samples were collected at 63 sampling sites distributed in the four sub-lakes and the inlet area of the main rivers. Concentrations of carbon dioxide (CO2), methane (CH4) and nitrous oxide (N2O) and the physicochemical properties of surface water were analyzed, and the emission fluxes at the surface water-air interface were calculated by using the thin boundary layer equation (TBL). The influencing factors on the dissolved concentrations of GHGs were discussed by using the correlation analysis and linear regression analysis between the GHG concentrations and the water physicochemical properties. The average concentrations of CO2, CH4 and N2O were (23.0±6.13) nmol·L−1, (0.15±0.10) μmol·L−1 and (52.4±11.4) μmol·L−1, respectively. The GHGs were highly saturated, and the average emission fluxes were (0.22±0.18) μmol·m−2·h−1 for CO2, (3.95±2.73) μmol·m−2·h−1 for CH4 and (658±336) μmol·m−2·h−1 for N2O, respectively, indicating that Nansi Lake mainly acted as the source of GHGs during the water diversion period; moreover, the concentrations and fluxes were similar to those of other lakes, but lower than those of the plain river network in winter. In general, the concentrations, saturations and fluxes of the three GHGs showed a decreasing trend from the north (the Nanyang Lake) to the south (the Weishan Lake). Higher GHG concentrations were in the inlet area of the rivers and in the area near the second level dam, in addition, there were belt-shaped high concentrations of N2O and CO2 but lower CH4 concentrations in the center of Weishan Lake. The concentrations of GHGs had some significant correlations with the water quality parameters (P < 0.05) indicating that the water quality should have some impact on the dissolved concentrations of the GHGs. Specifically, N2O was positively correlated with NO3− and NO2−, and CH4 was negatively correlated with TN; while CO2 had negative correlations with pH and SD but positive correlation with DOC. The results provide basic data support for the assessment of the influence of the lake on atmospheric greenhouse gases during the water diversion period.
-
全(多)氟化合物(per- and polyfluoroalkyl substances,PFASs)是以烷基碳链结构为骨架、氢原子被氟原子全部或部分取代的一类全球性新型微污染物[1]. 自20世纪50年代以来,PFASs因具有良好表面活性、热/化学稳定性,以及疏水、疏油的“双疏特性”[2],被广泛应用于纺织品、食品包装、皮革、炊具等工业和商业产品[3-4]. 近年来,PFASs在全球多个地区的环境介质[5-7]、生物体[8-10]和人体[11-13]中被广泛检出,并被证实可能引起肝脏、生殖发育、免疫毒性和内分泌干扰等多种危害效应[14-16],与睾丸癌、乳腺癌等多种人体疾病和健康问题存在关联[17]. 鉴于其潜在环境风险与毒性效应[18-20],国内外政府、企业与学术界对PFASs污染的关注度越来越高. 2000年,全球氟化工重要企业美国3M公司宣布逐步淘汰C6、C8和C10长链全氟磺酸类化合物的生产[21];全氟辛烷磺酸(PFOS)及其盐类物质、全氟辛烷羧酸(PFOA)及其相关衍生物分别于2009年和2019年相继被纳入斯德哥尔摩公约附件B和附件A;至2020年,全氟己烷磺酸(PFHxS)也被提议纳入公约管控,目前正在接受进一步的研究评估[22].
目前,填埋仍是国内外处置固体废物的主要方式. 含有PFASs的工、商业产品在其使用寿命终结时大多以废物形式被弃置于填埋场[23],其携带的PFASs在物理、化学与生物等共同作用下释放、迁移、转化,并赋存于填埋渗滤液. 国内外学者已在世界多国填埋渗滤液中检出PFASs,其浓度跨越从ng·L−1到mg·L−1的6个数量级[24],并在填埋场附近环境介质(土壤、地下水、大气等)[25-27]检出PFASs,表明垃圾填埋场是PFASs重要的“汇”集场所与排放点“源”. 而今,关于渗滤液处理过程PFASs的迁移、转化与去除等归趋研究相对较少. 有限的研究表明,生物处理、膜处理、吸附、高级氧化等现场处理设施工段[28-29]对渗滤液赋存PFASs污染的控制具有特异性效果,但存在去除率参差不齐、机理机制不清、前体物污染转化与副产物环境归宿不明等问题[30-31];泡沫分离[32]、电絮凝[33]、等离子体反应器[34]的实验室规模探索对渗滤液赋存PFASs污染的控制具有显著研究成效,为处理PFASs等新微污染物提供创新借鉴意义. 鉴于数量众多的填埋场被认为是全球环境系统中重要的PFASs污染排放点源,本文系统综述了填埋场PFASs潜在来源与源强、渗滤液赋存PFASs特征、排放量及其可能影响因素,论述了不同渗滤液处理工艺/工段对PFASs的去除效果及存在问题,以期为全面和客观认识填埋渗滤液赋存PFASs及其处理现状,为明晰控制填埋工程系统包括PFASs在内的新型微污染物的研究方向提供重要参考.
1. 固体废物填埋系统PFASs的来源(Source of PFASs in solid waste landfill system)
大量研究已证实各类日常消费品赋存不同水平及组成的PFASs,在其使用寿命结束后往往被弃置于填埋场,构成填埋系统PFASs的主要来源. 欧洲学者Kotthoff等[35]在115种消费品中(以纺织品与纸类包装产品为代表)检出16种全氟烷基酸(PFAAs)及其5种前体物,其中纺织品和纸类包装的总PFASs(记为ΣPFASs)含量均超过100 µg·kg−1. 美国学者Schaider等[36]收集400多份食品包装样品,包括食品接触纸、非接触纸、纸杯等,运用粒子诱导γ射线发射光谱(PIGE)检出样品中总氟含量至少达到16 nmol·cm−2;运用液相色谱-飞行时间质谱(LC-TOF-MS)检出全氟羧酸(PFCAs,以PFOA和全氟己烷羧酸PFHxA为主)、全氟磺酸(PFSAs,以全氟丁烷磺酸PFBS为主)及前体物6∶2氟调聚磺酸(6∶2 FTS). 日本学者在9种纺织品中发现含量高达30 mg·kg−1的18种PFAAs,以及包括氟调聚羧酸FTCA、氟调聚不饱和羧酸FTUCA与6∶2 FTS等在内的14种PFAA前体物[37]. 此外,我国采样的纺织品、纸类、半导体等产品中也频繁检出PFASs[38-39].
除生活垃圾外,填埋场也通常是污水污泥、建筑垃圾、焚烧灰渣等其它类型废物的“最终归宿”,而这些废物已被直接或间接地证实对其填埋处置系统中PFASs的赋存水平及组成有所贡献. 美国32个州和1个特区的94个污水污泥样品被检出13种PFASs,其平均含量为539 ng·g−1(干重);据此推算,全美污泥每年携带释放ΣPFASs质量为2749—3450 kg[40]. Bečanová等[41]报道了54种建筑材料(木质装潢材料、外墙材料等)赋存15种PFAAs,其ΣPFAAs含量高达34.3 µg·kg−1. Solo-Gabriele等[30]近期在单独填埋建筑垃圾和焚烧灰渣的填埋单元渗滤液中检出11种PFASs,其ΣPFASs浓度分别达到16060 ng·L−1和3370 ng·L−1,间接证明建筑垃圾和焚烧灰渣携带PFASs进入填埋系统. 这些结果表明,除生活垃圾以外,污水污泥、建筑垃圾和垃圾焚烧灰渣等典型城镇固体废物,也是填埋系统PFASs的重要来源载体.
2. 国内外填埋渗滤液赋存PFASs特征(Characteristics of PFASs in landfill leachate at home and abroad)
2.1 PFASs物种类别
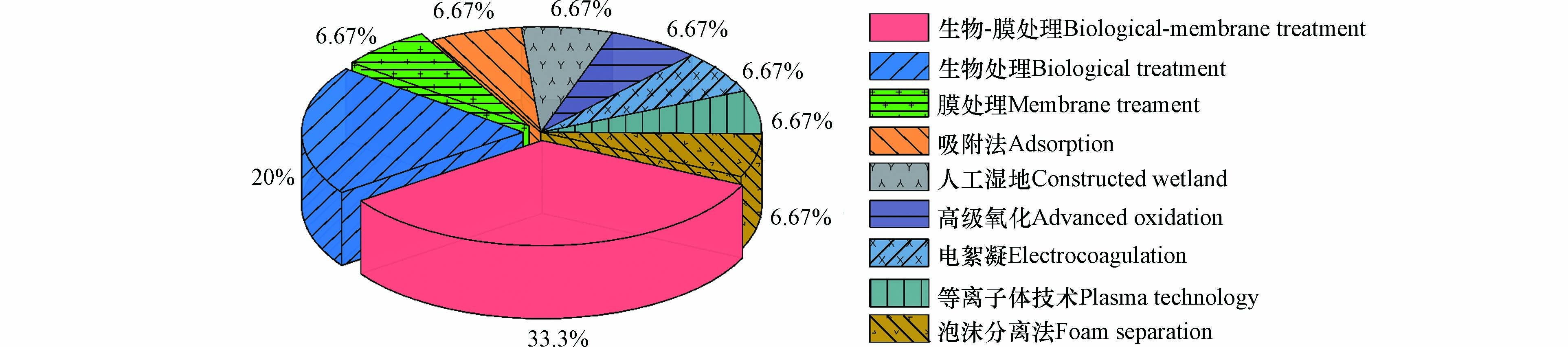
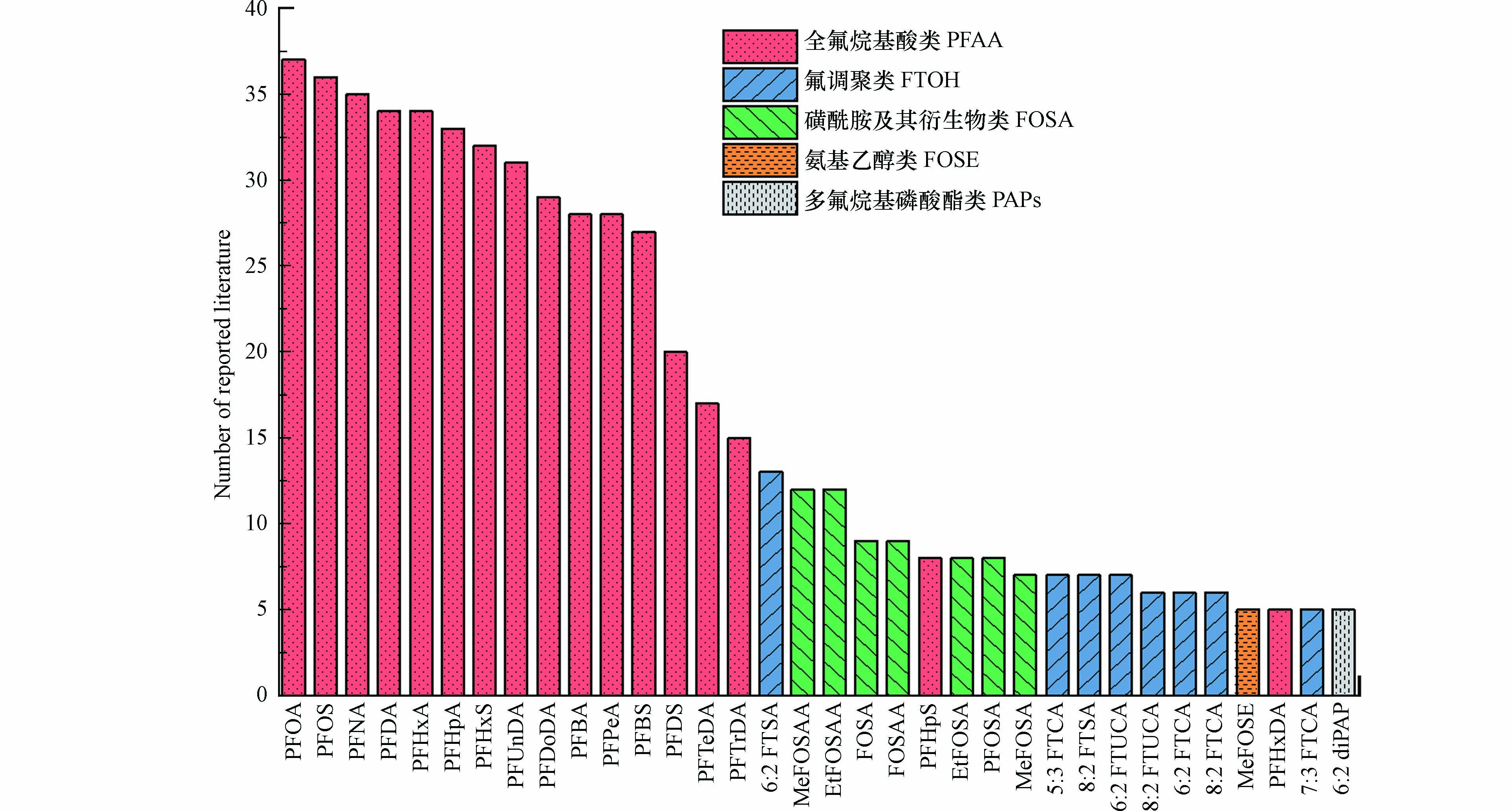
本文系统检索了国内外关于填埋渗滤液检出PFASs的文献报道,发现合计43篇文献(2008—2020)报道了渗滤液赋存上百种PFASs,主要包括全氟烷基酸类(PFAAs)、前体物氟调聚类(FTOHs、FTCAs等)、磺酰胺及其衍生物类(FOSA、PFOSA等)、氨基乙醇类(FOSE)和多氟烷基磷酸酯类(PAPs)5大类. 其中,PFAAs,包括12种全氟羧酸(PFCAs)和5种全氟磺酸(PFSAs),是已有研究关注的主要物种类别,占文献报道次数较多的34种PFASs中的50%(图1).
渗滤液真实赋存PFASs物种与浓度可能远远超过现有文献报道检出的物种与浓度. 一方面,文献报道定量检出的PFASs物种数量与分析测试标准品的可获得性有关. 现有研究主要采用目标分析方法(target analysis)进行比对定量,但目前市场上已发现4700多种PFASs,存在大量因缺乏标准品而难以定量的物种[42]. 另一方面,目标分析存在的局限性难以定性定量识别更多类别非目标PFASs,导致对PFASs物种与浓度的低估. 多国学者采用可疑(suspect)与非目标(non-target)筛查手段在土壤[5,43]、地表水[44]和生物体[45]内检出包括全氟醚基烷酸(PFEAs)、氯代多氟化合物(Cl-PFASs)和环状全氟烷酸(CYPFAAs)等多类非目标PFASs. Wang等[46]指出若只分析目标物质,ΣPFASs在渗滤液中的质量负荷可能被低估6.9%—49%.
2.2 渗滤液赋存PFASs水平与组成
表1总结了文献报道全球范围填埋场渗滤液赋存PFASs水平与组成. 目前仅14个国家对渗滤液中PFASs赋存特征进行了报道,发达国家如美国[47-48]、加拿大[49-50]和一些欧洲国家[51-54]开展研究较早,而我国近年来才逐步开展相关研究[31,46,55-56].
表 1 全球范围内填埋场渗滤液PFASs赋存水平Table 1. The occurrence level of PFASs in landfill leachates globally区域Region 国家/地区Country/region 发表年份Year of publication PFASs分析数Number of analytes 主要的PFASs类型ePrimary species ∑PFASs /(ng·L−1)f PFOA/(ng·L−1) PFOS /(ng·L−1) ∑PFASs排放量/(kg·a−1)Emission load 参考文献Reference 亚洲 中国/上海,广州,南京,苏州,常州 2015 14 PFOA, PFBS, PFPrA 7280—292000 281—214000 1150—6020 3110(全国) [31] 中国/北京 2019 10 PFPeA, PFBA, PFOA 407—2982 4—431 <LOQ—3 n.a. [55] 中国/重庆 2020 17 PFBS, PFBA, PFHxA, PFPeA, PFHxS, PFOS, PFHpA, PFOA 1805—43310 97—2350 139—3966 n.a. [56] 中国/天津 2020 29 PFPrA 22000—39000 330—820 37—130 0.02—0.4(阴离子PFASs) [46] 越南 2013 17 PFOA, PFUnDA, PFNA 360 100 11 n.a. [67] 新加坡 2017 18 PFOA 1269—7661 538—3458 123—439 0.05—0.25 [68] 北美洲 加拿大 2012 13 PFHxA, C4—C8 PFCAs 27—21300 439 279 n.a. [49] 加拿大a 2012 24 PFPeA, PFHxA 2500 210 80 8.5—25 [50] 加拿大 2013 7 PFOA, PFOS n.a. 50—1590 <9—744 n.a. [69] 美国/墨西哥湾沿岸a, 西海岸a, 太平洋西北地区, 大西洋沿岸中部各州a 2011 24 PFBA, PFPeA, PFBS, PFOS 2688—7415 380—1000 56—160 n.a. [47] 美国/明尼苏达州b 2013 14 PFOA, PFOS, PFHxA 178000 82000 31000 n.a. [48] 美国 2014 70 C4—C6 PFCAs 3200—160000 150—9200 14—590 n.a. [57] 美国 2017 70 5:3 FTCA 180—29311 30—4990 <LOD—801 563—638(全国) [58] 美国/佛罗里达州c 2020 11 PFHxA, PFHxS, PFOA, PFBS, 5:3 FTCA 2820—19970 259—2990 120—1230 n.a. [30] 欧洲 丹麦 2008 7 PFOA, PFOS n.a. <2—6 1—4 n.a. [51] 德国 2010 43 PFBA, PFBS, PFHxA, PFOA, PFPeA, PFHpA, 6:2 FTS, PFOS, PFHxS 31—12922 23 8 90(全国) [52] 荷兰 2013 17 PFOA, PFBA, PFHxA, PFHpA 74—4400 1—1800 10—110 n.a. [53] 芬兰 2013 4 PFOA, PFHxA, PFOS 214—614 76—270 87—140 n.a. [54] 西班牙 2017 16 PFOA, PFHxA, PFPeA, PFBA 639—1379 387—584 <LOD—43 1.2 [70] 瑞典 2018 26 PFHxA, PFOA 1300 338 n.a. n.a. [71] 挪威 2019 28 PFBA, PFPeA, PFHxA 320—11000 66—1800 15—160 3.2—110(全国) [62] 爱尔兰 2019 10 PFBS, PFOA, PFOS, PFHxS, PFNA 14—17524 9—11400 <0.1—7300 n.a. [72] 大洋洲 澳大利亚d 2016 14 PFHxA, PFHpA, PFOA 104—14989 19—2100 37—1100 n.a. [73] 澳大利亚d 2017 9 PFHxA, PFHxS, PFOA, PFHpA, PFOS 181—56328 17—7500 13—2700 0.02—31(全国) [61] 注:a.渗滤液回灌; b.接收3M公司污泥; c.接收生活垃圾,建筑垃圾,焚烧灰渣; d.接收生活垃圾,建筑垃圾,商业及工业垃圾; e.主要的PFASs类型是原文按质量百分比顺序给出; f.n.a.表示原文未给出,LOQ表示定量限,LOD表示检出限. a. leachate recirculation; b. receive sludge from 3M company; c. receive municipal solid waste(MSW), construction and demolition(C&D) and MSW ash; d. receive MSW, C&D and commercial and industrial(C&I); e. the dominant PFASs are shown in mass percent order in original literature; f. n.a. refers to not given in original literature, LOQ refers to the limits of quantification, LOD refers to the limits of detection. 如表1所示,渗滤液赋存PFASs水平存在显著的国际与地区差异,其浓度水平跨越6个数量级,从ng·L−1到mg·L−1不等. 据相关文献报道,中国上海是填埋渗滤液赋存PFASs水平最高的地区,赋存浓度高达292000 ng·L−1,其中PFOA和PFOS浓度分别达到214000 ng·L−1和6020 ng·L−1[31],该浓度也比中国其它地区渗滤液PFASs浓度高出4—40倍[46,55-56],这可能与上海城市化与工业化发展水平相关. 美国明尼苏达州某填埋渗滤液检出PFASs浓度高达178000 ng·L−1,仅次于上海,显著高于美国其它地区填埋场检出浓度(180—160000 ng·L−1)[30,47,57-58],这主要与该填埋场接收3M公司(全球最大氟化工制造商)的生产污泥有关.
尽管赋存水平呈现较大差异,但表1渗滤液中的PFASs,除最常见的PFOA与PFOS外,主要以短链物质为主. 推测其原因主要有两方面:一方面,2000年以来全球氟化工行业开始转向生产和使用短链化合物,造成短链PFASs逐渐替代长链PFASs[59];另一方面,短链PFASs被证实在水相中的溶解度高、辛醇/水分配系数低,更易被浸出分配于渗滤液液相而非废物固相颗粒[60].
2.3 PFASs排放量
除上述赋存水平及组成研究外,少量研究对特定国家废物填埋系统产生的渗滤液携带PFASs进入周边环境的质量进行了估算(表1). Lang[58]和Gallen等[61]分别调研了美国18座填埋场和澳大利亚27座填埋场,结合渗滤液产量与PFASs检出浓度情况,估算每年排放至美国和澳大利亚污水处理厂的PFASs质量分别为563—638 kg和0.02—31 kg. Busch等[52]调研德国22座填埋场,发现经生物、高级氧化、膜过滤等工艺处理后排入周围水环境中的PFASs约为90 kg. Knutsen等[62]估算挪威的填埋处置系统每年PFASs的排放量约为3.2—110 kg,其中55%排放至污水处理厂,45%经处理后直接排入环境. Yan等[31]也对我国可能渗漏污染地下水的PFASs质量进行了估算,推测我国由填埋系统渗入地下环境介质的PFASs质量可能高达3110 kg,远高于前述发达国家水平. 值得注意的是,这些研究可能显著低估排入环境介质的真实PFASs排放量,其原因与前文所述的目标分析手段的局限有关.
此外,随垃圾进入填埋场中的PFASs,除赋存于渗滤液中通过液相途径排放外,还存在分配到气相中发生挥发性释放的潜能. 已有研究在加拿大[63]、德国[64]和中国[30]垃圾填埋场上方空气中检出PFASs,浓度分别为2.8—26 ng·m−3、0.08—0.7 ng·m−3和1.6—33 ng·m−3,其中中性8∶2 FTOH为主要的物种,这是由于中性物质相比于离子型PFASs更具挥发性[58]. Tian[65]和Jin等[66]也在填埋场周围植物叶子或树皮上检出PFASs,浓度分别为48 µg·g−1和0.28 µg·g−1. Ahrens[63]和Wang[30]等分别采用简化的高斯扩散模型估算出PFASs向大气中的排放量分别为0.1—1 kg·a−1和0.04—0.57 kg·a−1. 这些结果表明,PFASs(尤其是FTOH、FTCA等挥发性PFASs)会通过挥发性释放从废物填埋系统排放至大气环境中,并因其具有持久性与远距离迁移潜能对大气环境及周边植物体等造成污染或损害. 因此,关于废物填埋系统衍生的逸散型PFASs排放方面的研究,值得重视.
3. 影响PFASs赋存特征的因素(Factors influencing the occurrence of PFASs)
在报道填埋渗滤液赋存PFASs水平与组成的同时,现有文献也尝试探讨影响PFASs赋存的自然与工程因素,及其与渗滤液特征理化性质之间的关联.
3.1 自然气候条件——降雨
自然降雨将造成渗滤液水质水量的波动,改变废物含水率,从而影响PFASs赋存水平,且影响机制较为复杂. 一方面,降雨带来的稀释作用可能使渗滤液赋存PFASs水平降低. Yin等[68]分别采集了湿润和干燥天气条件下的填埋渗滤液,发现短链PFASs在降雨量较高的湿润气候下显示出更低浓度水平. Benskin等[50]也发现,美国渗滤液PFASs赋存水平与24 h降雨量之间存在显著负相关(r=−0.87—−0.75). 然而,另一方面,降雨将增加废物含水率,促进微生物生长和废物降解,有利于PFASs从填埋废物渗出进而赋存于渗滤液,使得PFASs赋存水平有所提升. Lang等[58]对美国干燥(年降雨量<38 cm)、温和(年降雨量38—75 cm)、湿润(年降雨量>75 cm)地区的填埋场分别采样分析,发现湿润地区渗滤液中Σ6PFASs赋存水平显著高于干燥地区浓度水平. 另有个别研究发现渗滤液赋存PFASs水平与两周累积降雨量之间没有显著相关性[50]. 因此,自然气候条件(降雨)对渗滤液赋存PFASs特征存在的影响机制,尚未获得清晰一致的认识.
3.2 运行操作方式——渗滤液回灌
除降雨以外,渗滤液回灌也会显著影响填埋环境湿度,改变废物降解速率,对渗滤液赋存PFASs水平及组成造成潜在影响. Benskin等[50]在加拿大填埋场调研发现回灌渗滤液中ΣPFASs浓度比非回灌渗滤液浓度低1个数量级,且回灌渗滤液以赋存PFAAs为主,未发现前体物的显著存在,推测可能是由于回灌加速了PFAA前体物的生物转化. 相似地,Huset等[47]在美国回灌渗滤液中观测到PFASs赋存水平低于非回灌渗滤液水平3个数量级,但在此回灌渗滤液中检出FTS、FOSA等前体物,平均浓度达1340 ng·L−1,这可能与前体物降解半衰期有关[74]. 然而,目前关于渗滤液回灌影响PFASs赋存水平及组成的文献数据较少,且数据还受到填埋废物类型、填埋时间及其它环境条件等因素差异带来的干扰,因此尚难以得出其对赋存PFASs水平及组成影响的清晰认识.
3.3 填埋固相物质特征——废物类型与填埋时间
如第1小节所述,不同类型废物赋存PFASs特征存在差异,且已有研究者阐明填埋废物释放PFASs的行为存在组分特异性[75-76]. Lang等[76]通过实验室模拟厌氧填埋反应器研究地毯和成衣类纺织品释放PFASs规律,证实地毯释放PFASs主要以5∶3 FTCA和PFHxA为主,而填充纺织品的反应器则因释放积累了大量短链PFCAs、PFOA和8∶2 FTSA. Gallen等[61]调研发现,建筑垃圾填埋渗滤液中Σ9PFAAs浓度(平均12110 ng·L−1)显著高于生活垃圾渗滤液(平均3466 ng·L−1). 尽管Solo-Gabriele等[30]在建筑垃圾和生活垃圾填埋渗滤液中检出相似浓度水平的PFASs,但发现建筑垃圾渗滤液赋存PFHxS浓度明显高于生活垃圾填埋渗滤液,这可能是由于PFHxS常被用作建筑材料的密封剂和拒水剂;此外,还得出了焚烧灰渣填埋单元的渗滤液赋存PFASs水平相对较低这一结论. 由此可见,PFASs携带载体废物类型对其填埋渗滤液赋存PFASs水平及组成具有明显的影响,但具体影响及其机制仍需系统研究以获得进一步认识.
此外,现有的科学知识表明,废物填埋时间与渗滤液赋存PFASs特征之间存在复杂关系. Gallen等[61]从澳大利亚27座填埋场采集97个渗滤液样品,发现随着废物填埋时间增加(填埋45年),采集相应渗滤液样品所含Σ5PFASs浓度呈现指数级下降趋势. 然而,Lang等[58]通过独立样本t检验分析发现,13种PFASs在美国特定“老龄”填埋场(10—24 年)和“年轻”填埋场(6.5—10年)采集渗滤液中表现出相近浓度水平;同时推测填埋废物释放PFASs速度较慢,将会在较长的填埋时间内持续释放. 以上,带来这些复杂影响效应的原因可能有:(1)近年来短链PFASs作为长链化合物的替代品获得生产与使用,导致长链PFASs浓度显著降低;(2)研究者调研的废物类型不同,造成其赋存PFASs存在物种差异,随着填埋时间推移,前体物被生物降解,但其降解半衰期表现出物种特异性[74,77],导致填埋时间对PFASs赋存水平及组成的影响尚不清晰.
3.4 填埋液相特征——渗滤液理化性质
填埋渗滤液是一类具有特殊理化性质的高浓度有机废水,其特征水质参数pH值、离子强度、总有机碳(TOC)等与PFASs从其载体废物的溶出释放,以及在固、液相间的分配与转化等行为可能存在关联. 不少研究已提及,渗滤液赋存PFASs的形态与pH值相关. 在弱酸/中性渗滤液基质背景下,PFAAs(pKa<0.52)往往以阴离子形态存在,而氟调聚类PFASs(pKa—6.24)会以中性分子形态存在[78].Yan、Benskin和Gallen等[31,50,61]研究发现,pH值的升高有助于PFASs的迁移,推测该现象可能与吸附废物表面的静电排斥特性变化及质子化与去质子化作用有关. 此外,离子强度被发现与渗滤液赋存PFASs水平存在正面[50]或负面[31]的相关性,而TOC含量与PFASs浓度仅存在中等偏弱的相关性[46,58]. 这些复杂且不一致的影响及其机制,尚需进一步的观测证实与深入研究.
然而,值得注意的是,这些影响因素之间可能存在共线性的问题,即各因素之间仍存在尚未清晰的关联,这对于探讨影响PFASs赋存水平及组成的因素及明晰其影响机制带来了潜在挑战.
4. 渗滤液赋存PFASs的去除(Removal of PFASs in leachates)
研究者们在关注渗滤液中PFASs的来源、赋存及其影响因素的同时,也在不断认识和探索对渗滤液所含PFASs的有效去除[28-29]. 传统的渗滤液处理方式主要是将其直接排往城市污水处理厂进行合并处理. Arvaniti等[79]综述了PFASs在城市污水处理过程的转归趋势,发现二级生物处理无法有效降解PFASs,反而使其富集于污水污泥,并可能随之被填埋或用于土壤改良,对土壤、植物等带来潜在污染[23];而膜过滤、吸附和高级氧化等深度处理工艺对PFASs的去除效率相对较高.
近年来,随着城镇污水处理厂的“拒收”以及对排放标准的严格要求,越来越多的渗滤液采用单独处理的方式,即采用物化(预处理)-生化-物化(深度处理)的组合工艺实现达标排放[80-81]. 然而,目前关于渗滤液单独处理过程中PFASs迁移转化去除的文献报道尚显匮乏,仅检索获取10篇. 这些有限的研究关注的处理系统工艺或单元技术(图2),除泡沫分离[32]、电絮凝[33]、等离子体[34]属于实验室规模的研究外,其它包括生物处理[30-31,46,52,55]、膜处理[31,46,52,70]、吸附[52]、高级氧化[52]、人工湿地[68]等研究,均是在渗滤液处理设施现场采样进行. 关于生物处理与膜处理效果的研究,约占已有文献报道的60%,表2对其报道的去除率数据进行了汇总.
表 2 生物处理和膜处理对渗滤液PFASs的去除情况Table 2. Removal of PFASs in leachates by the biological treatment and membrane treatment国家/地区Country/region 处理工艺/构筑物aTreatment process/structure 进水ΣPFASs/(ng·L−1)Influent 出水ΣPFASs/(ng·L−1)Effluent ΣPFASs去除率/%Removal rate 参考文献Reference 中国/上海,广州,南京,苏州,常州 生物反应器 7280—292000 4570—111000 19.4—62.0 [31] 超滤-纳滤 4570—111000 122—859 81.2—97.8 超滤-反渗透 4570—111000 98—190 99.3—99.8 中国/北京 生物法-纳滤 407—4276 744—3657 −136.1—51.9 [55] 中国/天津 好氧/厌氧/好氧池-厌氧/好氧池-超滤-纳滤-反渗透 22000b 10000 54.5 [46] 生物池-曝气池-生物沉淀池-膜生物反应器 32000 46000 −43.8 调节池-厌氧池-反硝化池-硝化池-二次硝化池-纳滤-反渗透 39000 1600 95.9 西班牙 膜生物反应器(两级生物处理-超滤) 1045—1379 856—3162 −129.3—18.1 [70] 美国/佛罗里达州 连续流生物曝气 8450—8730 8570—8600 −1.4—1.5 [30] 序批式生物曝气 15610—15840 19920—19970 −27.9—−25.8 注:a. 本文已将原文分工段分析PFASs去除的处理工艺分段整理,未分段的则为原文中只分析了进出水浓度; b. 该数值源于原文中µg·L−1转化所得. a. in this study, the treatment process section of PFASs removal has been segmented and sorted out as long as it was analyzed by each section in original literature, in contrast, it has not been segmented and sorted out if only concentrations of influent and effluent were analyzed in original literature; b. this value is derived from the conversion of µg·L−1 in original literature. 4.1 生物处理
生物处理是目前渗滤液处理的重要工艺段,具有操作简单、运行费用低及二次污染小等优点[80],但如表2所示,现有生物处理工艺难以有效去除、甚至会造成处理出水PFASs浓度上升的结果,导致表2中去除率出现负值的异常情况. Solo-Gabriele等[30]检出渗滤液原液赋存PFASs浓度为15610—15840 ng·L−1,经生物曝气处理后,出水浓度为19920—19970 ng·L−1,增幅达到25.8%—27.9%(即去除率=−27.9%—−25.8%). Wang等[46]发现生物处理出水PFASs浓度(46000 ng·L−1)高于进水浓度(32000 ng·L−1),去除率为−43.8%. 此外,尽管联合深度膜处理,但仍能在渗滤液出水中观测到显著的浓度上升趋势,导致负去除率高达−136.1%[55]和−129.3%[70]. 分析其原因:一方面,在分子水平上,氟原子具有极高的电负性,从而产生极稳定的C—F键(解离能:536 kJ·mol−1),致使PFASs难以生物降解而具有持久性[82]. 另一方面,渗滤液含有的非目标前体物经过生物转化为目标PFASs,对出水浓度水平升高具有“贡献”.Wang等[46]首次运用总可氧化前体测定法(TOP)研究垃圾渗滤液生物处理前后赋存PFASs污染水平,定量阐明出水C2—C12 PFCAs浓度升高了40 µg·L−1,且未知C4—C12 PFAA前体物对渗滤液中ΣPFASs贡献介于10%—97%(以mol浓度计),未知C2—C3 PFAA前体物贡献介于12%—93%. 另有研究表明,代表性前体物FTOH和FTS在好氧土壤[83-84]、污泥[85-86]、沉积物[87-88]和渗滤液[74]等不同环境基质下,可被生物转化为最终产物PFAAs.
4.2 膜处理
膜处理是目前渗滤液处理常用的深度处理工艺段,可以有效去除渗滤液中大分子难降解有机物和总氮,具有污染物去除率高、出水水质稳定等优点[81,89]. 与单独生物处理相比,Wang等[46]发现经过纳滤-反渗透的深度膜处理后渗滤液出水PFASs去除率显著升高(生物处理:−43.8%,联合膜处理:54.5%—95.9%)(表2). 此外,膜处理根据膜材料孔径大小可分为反渗透(RO)、纳滤(NF)、超滤(UF)、微滤(MF),其中MF由于孔径过大,处理效果不佳,因此很少应用于渗滤液处理;UF常作为NF/RO的前处理工艺应用于渗滤液处理[31,46]. 由表2可看出膜处理去除PFASs效果明显,且与其孔径存在关联. Yan等[31]采集经UF预处理后的NF/RO渗滤液样品,发现孔径较小的RO工艺处理渗滤液后PFASs去除率高达99.3%—99.8%,高于NF工艺(81.2%—97.8%).
尽管膜处理对渗滤液中PFASs的去除效果显著,但这种方法并没有真正解决PFASs污染问题,而主要是通过物理截留将其分离富集于膜浓缩液. Yan等[31]观测到NF/RO工艺处理渗滤液产生膜浓缩液,其赋存PFASs浓度分别高达5610—7580 ng·L−1和19100—282000 ng·L−1,其中苏州某填埋场经RO工艺处理后浓缩液赋存PFASs水平甚至高出进水渗滤液赋存水平102%,表明膜浓缩液很大程度上会成为渗滤液所含PFASs的“汇”. 目前对膜浓缩液的处理,主要采用回灌、蒸发、高级氧化等单一或组合工艺[90],但在这些工艺过程中PFASs的最终环境归宿,亟待获得清晰的科学认识.
4.3 其他处理
除生物处理、膜处理的主流处理工艺段外,研究者们还在其它渗滤液处理设施工段观测到不一致的去除效果(表3). 针对活性炭(AC)和湿式氧化(WAO)处理工艺,有学者[52]研究了处理前后渗滤液赋存PFASs水平,分析发现,经AC物理吸附工段,渗滤液赋存PFASs浓度从31—12819 ng·L−1降低至9—4079 ng·L−1,去除率达到68.2%—99.8%,表明物理吸附能有效去除PFASs;相反,经WAO化学氧化工段,渗滤液处理出水PFASs浓度1993 ng·L−1略高于进水浓度1889 ng·L−1,可能由于PFASs具有难以被氧化降解的化学稳定性,且PFAA前体物在处理过程中生物转化为PFAAs,导致出水浓度呈现5.5%的增幅. 相关研究[68]报道了人工湿地系统中各构筑物(调节池、曝气池、沉淀池、芦苇床和深度处理塘)处理渗滤液过程对PFASs的去除情况. 该研究表明,人工湿地通过微生物降解、植物修复和土壤吸附等协同作用致使出水PFASs浓度降低到619 ng·L−1(原液:1570 ng·L−1),去除率达到61%,其中44%主要源于芦苇床的植物吸收.
表 3 其它渗滤液处理工艺(段)对渗滤液PFASs的去除情况Table 3. Removal of PFASs in leachates by other treatment processes(sections)近年来,基于PFASs具有良好热/化学稳定性、难以被生物降解矿化的特性,国内外学者在实验室研究中探索采用泡沫分离、电絮凝、等离子体等创新方法对渗滤液中PFASs进行分离、沉淀、去除(表4). 采用泡沫分离处理渗滤液中PFASs,主要是利用PFASs的表面活性剂特性,通入空气诱导渗滤液起泡,使PFASs富集浓缩于泡沫层,随即分离泡沫与渗滤液以达到去除PFASs的目的. Robey等[32]开展泡沫分离实验分析了PFASs从渗滤液液相中分离去除的效果,发现69%的PFASs从渗滤液分配富集至泡沫中,且前体物和长链PFASs的去除率(>80%)显著高于短链PFASs(<40%). Zhang等[33]选择铝电极电絮凝研究渗滤液中C6—C12 PFCAs的去除效率,通过外加电压使阳极金属板溶出铝离子,与电解反应产生的OH−形成氢氧化铝絮状物,吸附捕获、沉淀去除PFASs,实验发现C6—C10 PFCAs的去除率为33.8%—75.2%,C11—C12 PFCAs浓度水平反而增加18.6%—20.2%,这与前文所述的前体物可能生物转化为PFAAs的推测一致. 也有研究揭示了等离子体处理受PFASs污染的垃圾渗滤液的可行性. Singh等[34]首次探究在外加电场作用下,等离子体反应器内产生的大量携能电子轰击PFASs分子,使其发生一系列物理化学反应(如电离、解离和激发),从而得以脱氟、降解的潜能. 研究表明,前体物在120 min内去除率为44%—99.9%,长链PFAAs在75 min内去除率就高达99.9%,相比之下,多数短链PFAAs在120 min内去除率较低(10%—50%),但通过添加阳离子表面活性剂CTAB,使其与短链PFAAs产生静电/疏水相互作用,促使结合分子更易转移至等离子体-液体界面,提高短链PFAAs电离去除率(40%—95%). 然而,以上研究均是实验室规模的初步探索,将其应用于实际渗滤液中去除PFASs仍有待进一步工程验证.
表 4 实验室研究渗滤液PFASs的去除情况Table 4. Removal of PFASs in leachates(Laboratory-scale)国家/地区Country/region 处理技术Treatment technology PFASs分析数Analytes 去除率Removal rate 参考文献Reference 美国/佛罗里达州 泡沫分离 36(18种前体物,10种长链PFAAs,8种短链PFAAs) ΣPFASs:69%(平均)PFAAs前体物:>80%长链PFASs:>80%短链PFASs:<40% [32] 中国/北京 电絮凝 7(C6—C12 PFCAs) ΣPFASs:70.8%(平均)C6—C10 PFCAs:33.8%—75.2%C11—C12 PFCAs:−20.2%—−18.6% [33] 美国 等离子体 27(10种前体物,11种长链PFAAs,6种短链PFAAs) PFAAs前体物:44%—99.9%长链PFAAs:>99.9%短链PFAAs:40%—95% [34] 5. 结论与展望(Conclusion and prospect)
(1)除生活垃圾以外,建筑垃圾、污水污泥、焚烧灰渣等填埋处置废物也被证实是填埋场PFASs的来源. 现有研究对生活垃圾以外的固体废物在填埋环境释放PFASs的行为关注较少. 这些行为值得进一步研究,以期为全面评估废物填埋系统PFASs的释放源强提供基础数据支持.
(2)世界多国填埋渗滤液中检出上百种PFASs,浓度在ng·L−1—mg·L−1水平. 然而目前主要采用的目标分析技术仅能定量分析渗滤液赋存的少数类别PFASs,未来有必要结合TOP、可疑与非目标筛查等多种分析测试方法更加全面的识别渗滤液赋存PFASs物种类别、浓度及前体物转化“贡献”等,从而正确评估渗滤液携带PFASs污染特征及强度.
(3)PFASs的迁移释放过程受到自然降雨、渗滤液回灌、填埋废物类型与填埋时间、渗滤液理化性质等多因素的综合影响,尚需开展系统研究阐明这些因素的影响程度及其作用机制,以加强填埋系统PFASs及其它新微污染物的防控.
(4)生物处理与膜处理相结合是我国当前垃圾渗滤液单独处理的主流工艺,尽管其对于控制处理出水赋存PFASs浓度的效果明显,但膜处理副产物(浓缩液)富集残留PFASs的最终环境归宿尚未得到清晰准确的认识. 此外,为避免渗滤液处理出水所含PFASs对土壤、水体等生态环境造成潜在风险,应加强研发高效低耗的降解转化处理PFASs的技术.
-
表 1 南四湖各湖区和部分河口水环境参数
Table 1. The water environment parameters of Nansi Lake
区域Region 理化指标Physical and chemical indexes WD/m SD/m WT/℃ pH DO/(mg·L−1) TN/(mg·L−1) NO3--N/(mg·L−1) NO2--N/(mg·L−1) NH3-N/(mg·L−1) TP/(mg·L−1) DIP/(mg·L−1) DOC/(mg·L−1) CODMn/(mg·L−1) Chl-a/(μg·L−1) 微山湖(n=42)WS 平均值 2.02b 1.13b 5.26b 8.27a 11.34a 4.48a 1.02ac 0.010b 0.43a 0.075b 0.029a 8.98a 3.52a 2.10b 标准偏差. 0.87 0.58 0.47 0.18 1.16 1.71 0.78 0.010 0.14 0.031 0.025 1.83 1.13 2.51 独山湖+昭阳湖(n=15)DS+ZY 平均值 2.74a 1.54a 6.39a 8.31a 10.51b 4.80a 0.31b 0.008b 0.55a 0.046c 0.014b 9.67a 3.87a 1.42b 标准偏差 0.56 0.35 0.88 0.07 0.19 1.56 0.22 0.008 0.20 0.026 0.015 0.66 0.50 1.14 南阳湖(n=6)NY 平均值 2.21ab 1.37ab 5.18b 8.32a 10.65b 1.25b 0.37bc 0.008b 0.44a 0.097ab 0.010b 9.30a 3.76a 2.01b 标准偏差 0.24 0.34 0.40 0.11 0.14 0.32 0.42 0.003 0.19 0.040 0.006 1.41 0.65 0.47 河口(n=9)Estuary 平均值 4.83a 1.20ab 6.52a 8.21a 11.13ab 3.91ab 2.77a 0.046a 0.44a 0.111a 0.028a 10.08a 3.78a 4.46a 标准偏差 4.73 0.60 1.32 0.08 1.40 3.19 2.99 0.064 0.20 0.050 0.017 1.68 0.59 2.98 全湖(含河口,n=72)The whole lake 平均值 2.51 1.25 5.65 8.28 11.08 4.21 1.03 0.014 0.46 0.075 0.024 9.29 3.64 2.21 标准偏差 1.90 0.54 0.90 0.15 1.06 2.04 1.38 0.026 0.17 0.038 0.022 1.63 0.94 2.36 最小值 0.70 0.40 4.80 8.03 10.20 0.88 0.005 0.002 0.12 0.009 0.001 5.92 0.56 0.013 最大值 15.00 2.90 9.30 8.87 14.90 10.04 8.65 0.213 0.92 0.190 0.103 13.86 6.62 11.18 GB3838-2002Ⅲ类水标准 — — — 6—9 ≥5 ≤1.0 ≤10* — ≤1.0 ≤0.05 — — ≤6 — 注:* NO3−-N标准为GB 3838—2002集中式生活饮用水地表水源地补充项目标准限值. 同列不同小写字母表示具有显著差异(P < 0.05). 下文同. Notes: * NO3−-N standard value is the standard limit of GB 3838—2002 supplementary items of centralized drinking water surface water source. Different lowercase letters in the same column have significant difference (P < 0.05) The same below. 表 2 南四湖表层水中N2O、CH4和CO2溶存浓度、饱和度和排放通量的参数统计
Table 2. The parametric statistics of concentrations, saturation and emission fluxes of N2O, CH4 and CO2 in surface water of Nansi Lake
参数Parameter N2O CH4 CO2 浓度Concentration 饱和度Saturation 排放通量Emission flux 浓度Concentration 饱和度Saturation 排放通量Emission flux 浓度Concentration 饱和度Saturation 排放通量Emission flux 微山湖WS 平均值 21.5b 140b 0.16b 0.14a 3595a 3.63a 50.3a 170b 551.7b 最小值 17.4 117 0.07 0.02 557 0.46 24.4 107 44.3 最大值 26.7 170 0.27 0.45 11206 12.0 67.0 241 1035.3 标准偏差 2.08 14.5 0.06 0.10 2688 2.72 10.1 36.8 262.0 独山湖+昭阳湖DS+ZY 平均值 22.3ab 156a 0.22a 0.12a 3148a 3.23a 54.2a 199a 757.2a 最小值 19.7 142 0.18 0.05 1457 1.35 41.7 171 497.9 最大值 24.6 174 0.26 0.24 6327 6.69 65.1 235 1005.1 标准偏差 1.35 10.1 0.03 0.06 1647 1.77 7.34 19.2 157.3 南阳湖NY 平均值 23.3ab 153ab 0.21ab 0.22a 5655a 5.82a 56.4a 207a 782.7a 最小值 20.7 136 0.14 0.13 3322 3.37 41.2 142 330.8 最大值 25.6 171 0.28 0.43 11381 11.7 79.1 301 1425.6 标准偏差 2.02 12.6 0.05 0.11 2953 3.06 12.9 56.8 383.5 河口Estuary 平均值 30.8a 217a 0.46a 0.19a 5235a 5.42a 56.6a 224a 902a 最小值 20.7 140 0.16 0.06 1498 1.47 39.2 151 356 最大值 63.2 431 1.34 0.38 10444 10.5 103.3 413 2411 标准偏差 15.0 104 0.42 0.11 3179 3.23 19.1 75.9 601 全湖(含河口)The whole lake 平均值 23.0 154 0.22 0.15 3878 3.95 52.4 186 658 最小值 17.4 117 0.07 0.02 557 0.46 24.4 107 44.3 最大值 63.2 431 1.34 0.45 11381 12.0 103.3 413 2411 标准偏差 6.13 44.6 0.18 0.10 2668 2.73 11.4 46.2 336 注:CO2和CH4浓度单位为μmol·L−1,N2O为nmol·L−1;饱和度单位是%;排放通量单位是μmol·m−2·h−1. 下文同. Notes: The unit for CO2 and CH4 is μmol·L−1, N2O: nmol·L−1; Saturation: %; Emission flux: μmol·m−2·h−1. The same below. 表 3 南四湖表层水中温室气体平均溶存浓度、饱和度和排放通量与其他水体的比较
Table 3. The comparison of average concentrations, saturation and emission fluxes of greenhouse gases in surface water of Nansi Lake with those in other water bodies
N2O CH4 CO2 浓度Concentration 饱和度Saturation 排放通量Emission flux 浓度Concentration 饱和度Saturation 排放通量Emission flux 浓度Concentration 饱和度Saturation 排放通量Emission flux 南四湖(本研究) 23.0③ 154② 0.22④ 0.15③ 3878① 3.95⑤ 52.4 186 658④ 巢湖[6] 23.4② 0.26③ 微山湖[16−17] 2.13⑦ 628.2⑤ 平原河网[24] 86.8① 448① 2.28① 0.86② 758② 24.1② 西北口水库[25] 0.079④ 0.44—1.44⑧ 东平湖[26] 0.33② 梅梁湾[27] −0.05⑦ 2.5⑥ −41.1⑧ 鄱阳湖[28] 0.05⑤ 4.38④ 165.5⑥ 北京内湖[29] 17.1④ 0.023⑥ 北京内湖[30] 1.1① 29.2① −8.3⑦ 五里湖[31] 1041.7③ 荷兰人工湖[32] 3409.1① 东湖[33] 17.5③ 1336.4② 注:CO2和CH4浓度单位为μmol·L−1,N2O为nmol·L−1;饱和度%;排放通量μmol·m−2·h−1. 平均值后带圈数字表示同列数据的大小排序. 北京内湖数据均为年平均数据. Notes: The unit for CO2 and CH4 is μmol·L−1, N2O: nmol·L−1; Saturation: %; Emission flux: μmol·m−2·h−1. The circled number after the average indicates the order of the data in the same column. The data of inner lakes in Beijing are annual average data. 表 4 微山湖与河口区表层水中N2O浓度与水质参数间的Pearson相关系数
Table 4. The Pearson correlation coefficients between N2O concentrations and the water quality parameters in Weishan Lake
湖区 WD SD WT pH DO TN NO3- NO2- NH3 TP DIP DOC CODMn Chl-a 微山湖(n=42) 0.322 b -0.474 a 0.059 -0.258 0.156 0.186 0.730 a 0.781 a -0.006 0.017 -0.104 0.396 a -0.076 -0.199 河口(n=9) -0.257 0.622 0.173 0.480 -0.195 0.212 0.235 -0.064 0.672 b 0.072 0.518 -0.191 -0.309 -0.519 注Note:a:P < 0.01;b:P < 0.05. -
[1] KARLÉN W. Global temperature forced by solar irradiation and greenhouse gases? [J]. Ambio, 2001, 30(6): 349-350. doi: 10.1579/0044-7447-30.6.349 [2] IPCC, 2013. Climate Change 2013: The Physical Science Basis. Contribution of Working Group I to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change[R]. Cambridge University Press, Cambridge, United Kingdom and New York, NY, USA. [3] XIAO Q T, XU X F, DUAN H T, et al. Eutrophic Lake Taihu as a significant CO2 source during 2000-2015 [J]. Water Research, 2020, 170: 115331. doi: 10.1016/j.watres.2019.115331 [4] BARTOSIEWICZ M, MARANGER R, PRZYTULSKA A, et al. Effects of phytoplankton blooms on fluxes and emissions of greenhouse gases in a eutrophic lake [J]. Water Research, 2021, 196: 116985. doi: 10.1016/j.watres.2021.116985 [5] SANTOSO A B, HAMILTON D P, SCHIPPER L A, et al. High contribution of methane in greenhouse gas emissions from a eutrophic lake: A mass balance synthesis [J]. New Zealand Journal of Marine and Freshwater Research, 2021, 55(3): 411-430. doi: 10.1080/00288330.2020.1798476 [6] MIAO Y Q, HUANG J, DUAN H T, et al. Spatial and seasonal variability of nitrous oxide in a large freshwater lake in the lower reaches of the Yangtze River, China [J]. Science of the Total Environment, 2020, 721: 137716. doi: 10.1016/j.scitotenv.2020.137716 [7] 闫兴成, 张重乾, 季铭, 等. 富营养化湖泊夏季表层水体温室气体浓度及其影响因素 [J]. 湖泊科学, 2018, 30(5): 1420-1428. doi: 10.18307/2018.0523 YAN X C, ZHANG Z Q, JI M, et al. Concentration of dissolved greenhouse gas and its influence factors in the summer surface water of eutrophic lake [J]. Journal of Lake Sciences, 2018, 30(5): 1420-1428(in Chinese). doi: 10.18307/2018.0523
[8] 邓焕广, 张菊, 刘浩志, 等. 不同营养水平城市水体温室气体溶存特征及影响因素研究[J]. 聊城大学学报(自然科学版), 2022, 35(5):103-110. DENG H G, ZHANG J, LIU H Z, et al. Characteristics and the influencing factors of dissolved concentrations of greenhouse gases in urban water bodies at different nutrient levels[J]. Journal of Liaocheng University (Natural Science Edition), 2022, 35(5):103-110(in Chinese).
[9] 刘臻婧, 肖启涛, 胡正华, 等. 引江济太对太湖贡湖湾氧化亚氮通量的影响 [J]. 中国环境科学, 2020, 40(12): 5229-5236. LIU Z J, XIAO Q T, HU Z H, et al. Effects of water diversion from Yangtze River to Lake Taihu on N2O flux in Gonghu Bay, Lake Taihu [J]. China Environmental Science, 2020, 40(12): 5229-5236(in Chinese).
[10] 张萍, 张菊, 邓焕广, 等. 南四湖菹草对上覆水和表层沉积物中汞和砷的富集特征 [J]. 环境化学, 2022, 41(11): 3589-3598. doi: 10.7524/j.issn.0254-6108.2021071402 ZHANG P, ZHANG J, DENG H G, et al. Enrichment characteristics of mercury and arsenic by Potamogeton crispus in the overlying water and surface sediment of Nansi Lake [J]. Environmental Chemistry, 2022, 41(11): 3589-3598(in Chinese). doi: 10.7524/j.issn.0254-6108.2021071402
[11] 曹起孟, 刘涛, 张菊, 等. 春季南四湖表层沉积物中生物硅的分布及其影响因素 [J]. 环境化学, 2022, 41(7): 2299-2308. doi: 10.7524/j.issn.0254-6108.2021112203 CAO Q M, LIU T, ZHANG J, et al. Study on the distribution and influencing factors of biogenic silica in surface sediments of Nansi Lake in spring [J]. Environmental Chemistry, 2022, 41(7): 2299-2308(in Chinese). doi: 10.7524/j.issn.0254-6108.2021112203
[12] 张慧, 郭文建, 刘绍丽, 等. 南四湖和东平湖表层水体中抗生素污染特征和风险评价 [J]. 环境化学, 2020, 39(12): 3279-3287. doi: 10.7524/j.issn.0254-6108.2019091002 ZHANG H, GUO W J, LIU S L, et al. Contamination characteristics and risk assessment of antibiotics in surface water of Nansi Lake and Dongping Lake [J]. Environmental Chemistry, 2020, 39(12): 3279-3287(in Chinese). doi: 10.7524/j.issn.0254-6108.2019091002
[13] LIU Y, YANG L Y, JIANG W. Qualitative and quantitative analysis of the relationship between water pollution and economic growth: A case study in Nansi Lake catchment, China [J]. Environmental Science and Pollution Research International, 2020, 27(4): 4008-4020. doi: 10.1007/s11356-019-07005-w [14] DIVYA K R, ZHAO S S, CHEN Y S, et al. A comparison of zooplankton assemblages in Nansi Lake and Hongze Lake, potential influences of the East Route of the South-to-North Water Transfer Project, China [J]. Journal of Oceanology and Limnology, 2021, 39(2): 623-636. doi: 10.1007/s00343-020-9288-1 [15] ZHANG B L, CUI B H, ZHANG S M, et al. Source apportionment of nitrogen and phosphorus from non-point source pollution in Nansi Lake Basin, China [J]. Environmental Science and Pollution Research International, 2018, 25(19): 19101-19113. doi: 10.1007/s11356-018-1956-8 [16] 陈永根, 白晓华, 李香华, 等. 中国8大湖泊冬季水-气界面甲烷通量初步研究 [J]. 湖泊科学, 2007, 19(1): 11-17. doi: 10.18307/2007.0102 CHEN Y G, BAI X H, LI X H, et al. A primary study of the methane flux on the water-air interface of eight lakes in winter, China [J]. Journal of Lake Sciences, 2007, 19(1): 11-17(in Chinese). doi: 10.18307/2007.0102
[17] 陈永根, 李香华, 胡志新, 等. 中国八大湖泊冬季水-气界面CO2通量 [J]. 生态环境, 2006, 15(4): 665-669. CHEN Y G, LI X H, HU Z X, et al. Carbon dioxide flux on the water-air interface of the eight lakes in China in winter [J]. Ecology and Environment, 2006, 15(4): 665-669(in Chinese).
[18] 张晓翠, 武周虎, 王瑜, 等. 南四湖湖区富营养化变化趋势与影响因素分析 [J]. 青岛理工大学学报, 2020, 41(1): 81-87. ZHANG X C, WU Z H, WANG Y, et al. Analysis of the eutrophication variation trends and influencing factors in Nansi Lake area [J]. Journal of Qingdao University of Technology, 2020, 41(1): 81-87(in Chinese).
[19] 邓焕广, 张智博, 刘涛, 等. 城市湖泊不同水生植被区水体温室气体溶存浓度及其影响因素 [J]. 湖泊科学, 2019, 31(4): 1055-1063. doi: 10.18307/2019.0409 DENG H G, ZHANG Z B, LIU T, et al. Dissolved greenhouse gas concentrations and the influencing factors in different vegetation zones of an urban lake [J]. Journal of Lake Sciences, 2019, 31(4): 1055-1063(in Chinese). doi: 10.18307/2019.0409
[20] 魏复盛主编. 国家环境保护总局, 水和废水监测分析方法编委会编. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002. WEI F S. State Environmental Protection Administration, Water and wastewater monitoring and analysis methods[M]. 4thed. Beijing: China Environmental Science Press, 2002(in Chinese).
[21] WANG D Q, CHEN Z L, SUN W W, et al. Methane and nitrous oxide concentration and emission flux of Yangtze Delta plain river net [J]. Science in China Series B:Chemistry, 2009, 52(5): 652-661. doi: 10.1007/s11426-009-0024-0 [22] YU Z J, DENG H G, WANG D Q, et al. Nitrous oxide emissions in the Shanghai River network: Implications for the effects of urban sewage and IPCC methodology [J]. Global Change Biology, 2013, 19(10): 2999-3010. doi: 10.1111/gcb.12290 [23] DEEMER B R, HOLGERSON M A. Drivers of methane flux differ between lakes and reservoirs, complicating global upscaling efforts [J]. Journal of Geophysical Research:Biogeosciences, 2021, 126(4): e2019JG005600. [24] 胡蓓蓓, 谭永洁, 王东启, 等. 冬季平原河网水体溶存甲烷和氧化亚氮浓度特征及排放通量 [J]. 中国科学:化学, 2013, 43(7): 919-929. HU B B, TAN Y J, WANG D Q, et al. Methane and nitrous oxide dissolved concentration and emission flux of plain river network in winter [J]. Scientia Sinica(Chimica), 2013, 43(7): 919-929(in Chinese).
[25] 王雪竹, 刘佳, 牛凤霞, 等. 基于走航高频监测的水库冬季水体溶解甲烷浓度分布: 以湖北西北口水库为例 [J]. 湖泊科学, 2021, 33(5): 1564-1573. doi: 10.18307/2021.0524 WANG X Z, LIU J, NIU F X, et al. Dissolved methane concentration distribution of reservoir in winter based on the underway high-resolution monitoring: A case study of the Xibeikou Reservoir in Hubei Province [J]. Journal of Lake Sciences, 2021, 33(5): 1564-1573(in Chinese). doi: 10.18307/2021.0524
[26] 刘涛. 东平湖优势水生植物对水体氮转化的影响[D]. 聊城: 聊城大学, 2021. LIU T. Effects of dominant aquatic plants on nitrogen transformation in lake Dongping[D]. Liaocheng: Liaocheng University, 2021(in Chinese).
[27] 李香华. 太湖水-气界面温室气体通量及时空变化特征研究[D]. 南京: 河海大学, 2005. LI X H. Study of the greenhouse gas flux of water-air interface and its spatio-temporal change in Taihu Lake[D]. Nanjing: Hohai University, 2005(in Chinese).
[28] 林茂. 鄱阳湖水-气界面温室气体通量研究[D]. 北京: 北京林业大学, 2012. LIN M. Greenhouse gas fluxes on the water-air interface of Poyang Lake[D]. Beijing: Beijing Forestry University, 2012(in Chinese).
[29] WANG G Q, XIA X H, LIU S D, et al. Distinctive patterns and controls of nitrous oxide concentrations and fluxes from urban inland waters [J]. Environmental Science & Technology, 2021, 55(12): 8422-8431. [30] WANG G Q, XIA X H, LIU S D, et al. Intense methane ebullition from urban inland waters and its significant contribution to greenhouse gas emissions [J]. Water Research, 2021, 189: 116654. doi: 10.1016/j.watres.2020.116654 [31] XIAO Q T, DUAN H T, QI T C, et al. Environmental investments decreased partial pressure of CO2 in a small eutrophic urban lake: Evidence from long-term measurements [J]. Environmental Pollution, 2020, 263: 114433. doi: 10.1016/j.envpol.2020.114433 [32] VAN BERGEN T, BARROS N, MENDONCA R, et al. Seasonal and diel variation in greenhouse gas emissions from an urban pond and its major drivers [J]. Limnology and Oceanography, 2019, 64(5): 2129-2139. doi: 10.1002/lno.11173 [33] XING Y P, XIE P, YANG H, et al. Methane and carbon dioxide fluxes from a shallow hypereutrophic subtropical Lake in China [J]. Atmospheric Environment, 2005, 39(30): 5532-5540. doi: 10.1016/j.atmosenv.2005.06.010 [34] FREYMOND C V, WENK C B, FRAME C H, et al. Year-round N2O production by benthic NOx reduction in a monomictic south-alpine lake [J]. Biogeosciences, 2013, 10(12): 8373-8383. doi: 10.5194/bg-10-8373-2013 [35] 杨平, 仝川, 何清华, 等. 闽江口养殖塘水-大气界面温室气体通量日进程特征 [J]. 环境科学, 2012, 33(12): 4194-4204. YANG P, TONG C, HE Q H, et al. Diurnal variations of greenhouse gas fluxes at the water-air interface of aquaculture ponds in the Min River Estuary [J]. Environmental Science, 2012, 33(12): 4194-4204(in Chinese).
[36] 张力, 张振华, 高岩, 等. 不同水生植物对富营养化水体释放气体的影响 [J]. 生态与农村环境学报, 2014, 30(6): 736-743. ZHANG L, ZHANG Z H, GAO Y, et al. Effect of aquatic plants on emission of gases from eutrophic water [J]. Journal of Ecology and Rural Environment, 2014, 30(6): 736-743(in Chinese).
[37] KLÜBER H D, CONRAD R. Effects of nitrate, nitrite, NO and N2O on methanogenesis and other redox processes in anoxic rice field soil [J]. FEMS Microbiology Ecology, 1998, 25(3): 301-318. doi: 10.1111/j.1574-6941.1998.tb00482.x [38] 曾从盛, 王维奇, 仝川. 不同电子受体及盐分输入对河口湿地土壤甲烷产生潜力的影响 [J]. 地理研究, 2008, 27(6): 1321-1330. ZENG C S, WANG W Q, TONG C. Effects of different exogenous electron acceptors and salt import on methane production potential of estuarine marsh soil [J]. Geographical Research, 2008, 27(6): 1321-1330(in Chinese).
[39] MA Y C, SUN L Y, LIU C Y, et al. A comparison of methane and nitrous oxide emissions from inland mixed-fish and crab aquaculture ponds [J]. Science of the Total Environment, 2018, 637/638: 517-523. doi: 10.1016/j.scitotenv.2018.05.040 [40] PEACOCK M, AUDET J, BASTVIKEN D, et al. Small artificial waterbodies are widespread and persistent emitters of methane and carbon dioxide [J]. Global Change Biology, 2021, 27(20): 5109-5123. doi: 10.1111/gcb.15762 -




 下载:
下载: