-
山东省是我国的渔业大省,海洋资源丰富,水域滩涂辽阔,有着巨大的开发潜力,水产品总产量、渔业经济总产值位居全国前列. 从水产养殖面积构成来看,目前山东海水养殖面积远超淡水养殖面积. 2018年以来,山东省海水养殖面积占总面积的比重维持在70%以上;到2020年海水养殖面积为580.35千公顷,占总面积的77.9%,可见海水养殖在山东省的经济发展中占据重要地位[1]. 传统的粗放式养殖模式对水体造成的污染越来越严重,不利于水产养殖业的可持续发展,而循环水养殖系统具有高效、节水、节能、减排等优点,成为当前最具前景的养殖模式之一,对渔业绿色可持续发展有着突出贡献,并且现阶段循环水的健康养殖将是水产养殖产业绿色高质量发展及实现绿色水产品的重要途径. 2021年中央一号文件中明确指出,推进水产品绿色健康养殖,要加强农产品和食品安全监管,发展绿色、有机农产品.
有些重金属元素进入水体时,生物会通过摄取、吸附与积累等过程,对重金属进行传递和富集,最终造成水产品的重金属污染,再通过食物链富集传递给人类,一旦食用污染的水产品,长期积累将引起器官中毒,威胁人体健康. 重金属不仅会损害人体的神经系统、肝脏、肾脏和其他解毒器官,还会导致免疫系统的削弱,甚至诱发癌症[2]. 循环水养殖系统中虽然对养殖废水进行了一系列循环处理,但由于该系统水体交换率低且几乎封闭循环的特性,仍存在一定的风险性[3]. 如果对于源水的处理不够完善,养殖用水也会受到污染,加上投喂饲料等影响因素也可能有一定累积风险,重金属等危害物质一旦进入循环水养殖系统,就不容易被排出,从而导致养殖生物体内重金属的累积,直接捕捞食用可能会出现至关重要的食品安全问题[4-5].
国内外关于水产品重金属污染的研究主要集中在近岸海域、池塘淡水的人工养殖以及捕捞野生的水产品等方面 [6],关于循环水养殖系统中水产品的重金属等污染风险以及评估的研究较少. 本文选取山东省烟台市某水产公司海水循环水养殖系统中的重要经济鱼类牙鲆(Paralichthys olivaceus)和珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂)作为研究对象进行重金属检测分析,了解系统中水体、鱼体的重金属分布特征,并采用单因子污染指数法、综合污染指数法、目标危险系数法评估其重金属污染程度和重金属污染的健康风险,为循环水养殖产业绿色可持续发展和模式的优化提供科技支撑. 同时,为食用此养殖企业循环水系统中牙鲆和珍珠龙胆石斑鱼的居民提供食品安全的数据,对居民身体的健康保障也具有重要意义.
-
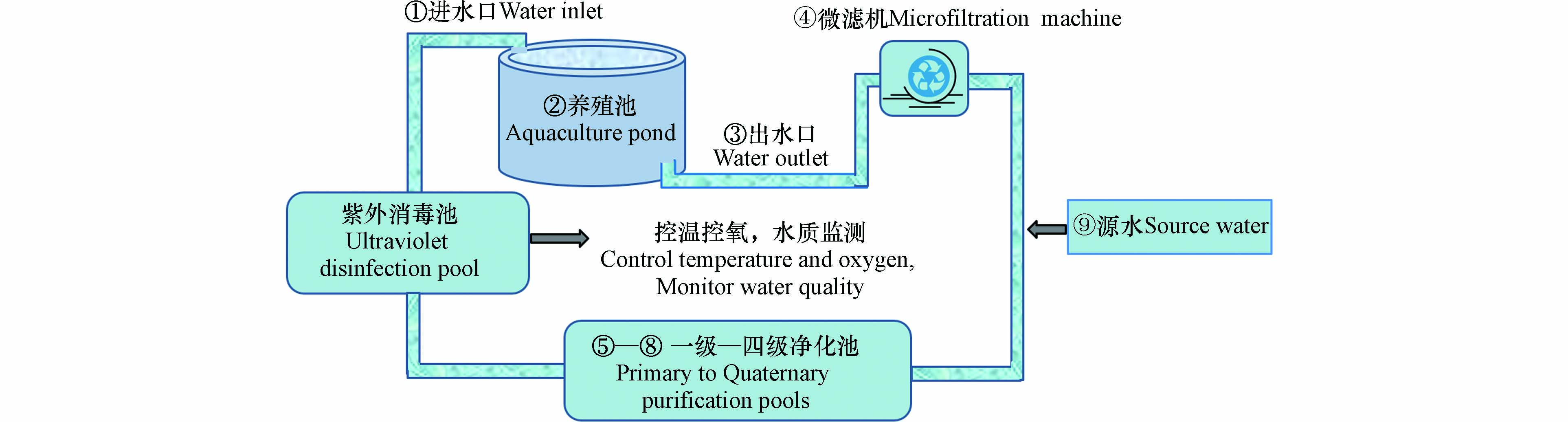
本实验选取山东省烟台市某水产公司牙鲆和珍珠龙胆石斑鱼海水循环水养殖系统的进水口、养殖池、出水口、微滤机、牙鲆养殖系统一级—四级净化池、珍珠龙胆石斑鱼养殖系统一级和二级净化池以及源水口等15个站点的水样和2021年不同生长周期的5、6、9、10月份可上市销售的牙鲆、珍珠龙胆石斑鱼,采集的水体样品各1 L装于聚乙烯瓶内和各3条鱼体装于泡沫箱内,标记后运回实验室冷冻备用. 同时,带回喂养实验鱼体的海水鱼饲料. 其中采集的牙鲆体长范围大致为25—30 cm;珍珠龙胆石斑鱼体长范围为21—27 cm. 其中,循环水养殖系统的结构如图1所示.
-
主要设备:电热消解仪(型号:ED54-iTouch,美国LabTech)、原子吸收光谱仪(型号:PinAAcle900T,美国PerkinElmer)、原子荧光分光光度计(型号:AFS-933,北京吉天)、可见分光光度计(型号:EV-2200,上海昂拉)等.
主要试剂:硝酸、高氯酸、盐酸、甲基异丁酮、环己烷、冰乙酸、硫脲(国药集团化学试剂有限公司)、铜(Cu)、铅(Pb)、锌(Zn)、镉(Cd)、汞(Hg)、砷(As)、铬(Cr)单元素标准溶液(1000 mg·L−1,国家有色金属及电子材料分析测试中心)等,且试剂的纯度选择均按国标.
-
鱼体:将所采集的鱼类样品室温下解冻,用去离子水冲洗干净鱼体和不锈钢刀,后用不锈钢刀做解剖,取鱼体肌肉可食用部分,用搅拌机制成泥状,装入聚乙烯密封袋等待后续消解工作. 测定鱼肉中的铜、铅、锌、镉、汞、砷,采用国标中的湿法消解. 重金属的前处理方法:称取试样(1.50±0.02)g(鲜重)于消解管中,加入8.0 mL硝酸和2.0 mL高氯酸,加盖放置12 h左右是为了能达到充分消解的效果,然后放石墨消解仪上,温度参考条件(120 ℃/0.5—1 h;升至180 ℃/2—4 h、升至200—220 ℃),消解至冒白烟(赶酸),无色透明或略带黄色停止,取出消解管冷却定容10 mL至容量瓶内,混匀备用,同时做空白试验和生物体分析标准物质实验. 其他具体过程以及分析方法均参照GB/T5009.12—2017《食品中铅的测定》,GB/T5009.13—2017《食品中铜的测定》,GB/T5009.14—2017《食品中锌的测定》,GB/T5009.15—2014《食品中镉的测定》,GB/T5009.11—2014《食品中总砷及无机砷的测定》,GB/T5009.17—2014《食品中总汞及无机汞的测定》.
水体:首先对水体进行过滤,取50 mL水样调节pH值至5.0,采用无火焰原子吸收分光光度法测定铜、铅和镉;另取50 mL水样调节pH值至4.0,采用火焰原子吸收分光光度法测定锌;采用原子荧光分光光度法测定汞和砷;其余详细步骤均按照GB17378.4—2007《海洋监测规范》第4部分 海水分析 进行有机萃取等前处理和分析检测工作.
-
评价方法采用单因子污染指数法和综合污染指数法进行.
单因子污染指数法计算公式(1)如下:
其中,Pi表示鱼肉中重金属i的污染指数;Ci表示鱼肉中重金属i的实测含量;Si表示鱼肉中重金属i的标准限值. Pi<0.2为正常背景值;0.2≤Pi<0.6为轻微污染;0.6≤Pi<1.0为中污染;Pi≥1.0为重污染. 本研究标准限量值参考依据GB2762—2017《食品安全国家标准 食品中污染物限量》、NY/T 842—2021《绿色食品 鱼》、FAO和参考文献中的限量指标为标准限值,Cu、Pb、Zn、Cd、Hg、As的限量指标分别为 50、0.5、40.0、0.1、0.5、0.1 mg·kg-1[7-9].
综合污染指数法计算公式(2)如下:
其中,P综表示鱼类重金属综合污染指数;Pave表示鱼类各单个污染指数Pi的平均值;Pmax为鱼类各单个污染指数中的最大值. 当P综≤1.0时,为正常背景水平;1.0< P综≤2.0 时,为轻度污染;2.0< P综≤3.0 时,为中度污染;P综>3.0 时,为重度污染[10-11].
-
本文以目标危险系数法(target hazard quotient,THQ)对重金属健康风险进行评价. 选用美国环保署(USEPA)推荐的健康风险评价常用方法模型[12-13],用于评估人体通过食物摄取重金属的风险. 该方法将鱼肉中重金属人体摄入剂量与其标准限值的比用来风险评价,可以综合评价单一或多种重金属的健康风险,计算公式见式(3—4). 当THQ>1,说明暴露人群存在潜在非致癌健康风险,THQ 值越大表明有害重金属对人体健康的非致癌风险越严重,同理也适用于TTHQ多种重金属复合健康风险[12,14].
式中,EF为人群暴露频率(d·a−1);一般设定为365 d·a−1;ED为暴露时间(a),通常等于人均寿命,常取70 a;FIR为食物摄入率g∙(d∙人)−1,成人平均每人每天摄入水产品分别为 0.029 kg;Ci为食物中重金属含量水平,mg·kg−1;RFDi为重金属入口参考剂量,mg∙(kg∙人)−1,Cu、Pb、Zn、Cd、Hg、As的RFD分别为 0.04、0.0035、0.3、0.0010、0.0005、0.0003 mg∙ (kg∙人)−1;BW为人体平均体重(kg),成人平均体重取 61.8 kg;AT为非致癌性暴露平均时间,(365 d·a−1×暴露年限70 a)取25550 d;10−3为单位换算[11-17] .
当THQ<1 时,暴露人群无明显健康风险;当 THQ ≥1 时,则认定暴露人群存在健康风险。
-
实验数据采用Microsoft Office Excel 2010和Orange 8.5进行图表统计与制作,运用Microsoft Office Excel 2010中的数据分析进行双因素方差显著性分析.
-
按照采样标准进行采样并检测其重金属,标准曲线相关性系数>0.995,回收率控制在85%—120%. 采样时用美国YSI 556型便携多参数水质监测仪对水体进行温度、盐度、pH值和溶解氧的测量,并记录数据,以确保实验对象是在适应的生长条件下成长的可供食用的正常健康鱼类,具备能够对重金属元素有良好的吸收和排出的能力.
牙鲆养殖系统中温度范围是16.6—18.9 ℃;盐度范围23.9‰—29.0‰;pH值范围6.53—7.94;溶解氧范围4.58—8.11 mg·L−1.
珍珠龙胆石斑鱼养殖系统中温度范围是19.8—27.0 ℃;盐度范围28.6‰—29.7‰;pH值范围6.01—8.11;溶解氧范围4.11—9.60 mg·L−1.
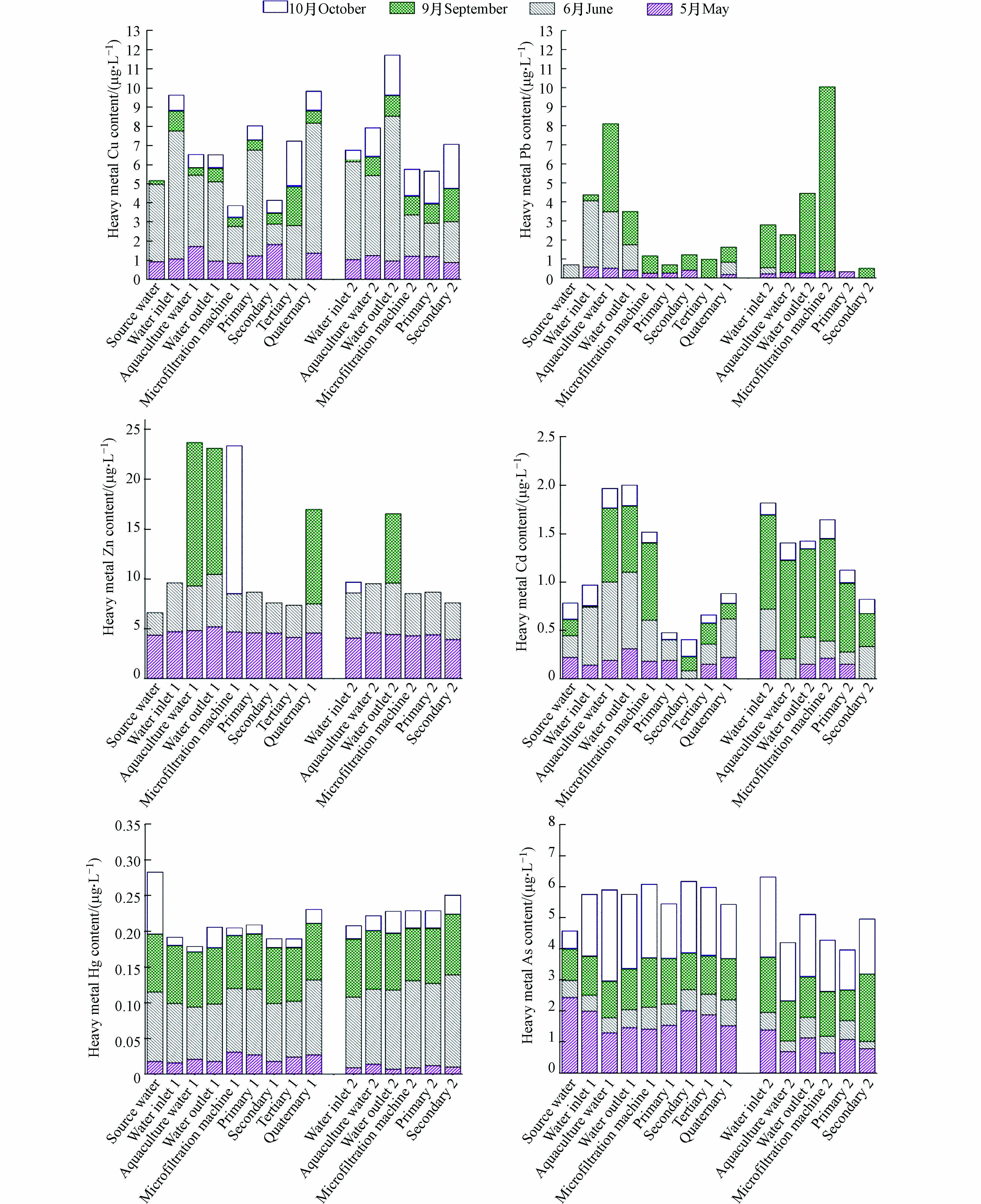
由图2可知,Cu含量相比来说较高的为珍珠龙胆石斑鱼养殖池出水,Cd含量较高的为牙鲆养殖池出水,养殖用水在循环水系统中对养殖生物至关重要,因为有研究发现池塘中重金属Cu的主要来源为养殖用水,其次才与饲料的投入等其他原因有关[18-19],说明循环水系统因有封闭循环等特征,养殖水中可能会存在一定的重金属元素[3].
4个月份中,Pb的含量水平9月最高,其中,微滤机净化池中的水Pb含量大,考虑是循环净化过程中,水中的Pb积累被过滤进入了微滤机净化池内的原因[3-5]. 可见运用循环水系统能够把水质里沉积的重金属进行有效吸附在微滤机过滤池中,养殖场应该提高其运行效率,把有害物质做出更好的排出处理[14]. 5月份每个水样的Hg含量较持平,6月份Hg的含量最高;10月的As含量最高,除了源水和珍珠龙胆石斑鱼的二级过滤池水外,每个水样都是10月的数值最大,6月的Cu总体含量最高,且4个月份中源水重金属的含量也有波动. 说明重金属元素含量可能与季节变化有关,根据其他研究发现,重金属元素会随季节因素影响呈现增大或减小的情况,Cu、Zn含量大致为春夏高于秋冬,Pb含量为春秋较高,Hg、As含量为夏秋较高,Cd含量为秋季较高[20],与本研究结果也大体一致,而且重金属含量也没有随着时间的推迟而累积,呈现持续上升等特定的规律性,循环水系统实际的换水率为10%左右,投喂量为1% (每日两次),所以可能是由换水频率的不固定性以及饲料的投喂量不同等多种原因造成的,其相关的结论在其他研究中也有说明[3].
由于六价铬对水生生物有致死作用,六价铬及其化合物受到各国主管当局严格的法规监管控制[21],所以本研究对水质六价铬进行了检测,5、6、9、10月的范围分别是0.22—0.82 μg·L−1、ND—2.40 μg·L−1、ND—4.30 μg·L−1、1.93—7.39 μg·L−1(ND为未检出). 依据GB 11607—1989 《渔业水质标准》Cu、Zn、Pb、Cd、Hg、As、Cr6+的标准限量分别是:10、100、50、5、0.5、50、100 μg·L−1,所测水体均符合标准限量.
同时,实验测出的喂养两种鱼的海水鱼饲料中重金属含量分别为:Cu 3.01 mg·kg−1、Pb 1.75 mg·kg−1、Zn 1.90 mg·kg−1、Cd 0.22 mg·kg−1、Hg 0.01 mg·kg−1、As 0.30 mg·kg−1. 结合GB 13078—2017《饲料卫生标准》 和NY 5072—2002《无公害食品 渔用配合饲料安全限量标准》,得到Pb、Cd、Hg、As的限量值分别为5.0、1.0、0.5、3.0 mg·kg−1,Cu和Zn没有标准限量,所有重金属均在标准限量内. 水体中Cu和Zn的值较大,其中Cu的含量范围是0.89—2.93 μg·L−1,Zn的范围是3.31—7.89 μg·L−1,最大值与最小值跨度也较大,可能是与水体中掺杂未被食用的饲料成分有关[22].
-
分别对每个月份采集的牙鲆和珍珠龙胆石斑鱼体肌肉组织做3个平行样,对其进行重金属含量测定,取其平均值. 标准曲线相关性系数>0.995,回收率介于 85%—120%.
由前文可知鱼体中Cu、Pb、Zn、Cd、Hg、As的限量指标分别为 50、0.5、40.0、0.1、0.5、0.1 mg·kg−1. 结合表1、表2来看,所有重金属都未超标. 4个月份中重金属没有呈现规律性的增大和减少的状况,可能是随着时间的变化,重金属在鱼体内吸收和排出产生的波动影响. 两种鱼类重金属含量大小表现均为Zn>Cu>As>Pb>Cd>Hg,且都为Cu、Zn的值明显大于其他重金属. 对比表1和表2,两种鱼类中的Pb、As、Cd、Hg重金属含量对比均值相差10%左右,可见牙鲆和珍珠龙胆石斑鱼对Pb、As、Cd、Hg的吸收和积累能力相似,大多研究结果也都表明这些元素在鱼体内的含量较Cu、Zn等元素低[12-14,23]. 重金属离子可划分为营养和非营养类两种,Cu、Zn 作为鱼类生长的必要微量元素,参与构成鱼体内的酶,具有促进鱼骨发育、免疫、鱼类代谢调节等功能. 营养元素Cu和 Zn 等较非营养元素 As、Hg 等更能与机体吸收融合[24],而且不同重金属之间有着协同和竞争作用,某些金属元素有共用一个离子通道的情况,多种离子在同一环境中碰撞时,竞争效应会出现在生物体富集过程中,从而影响吸收[3]. 实验表明除Cu外,Zn富集能力相对较高,但Hg含量可以忽略不计,在这两种鱼体内基本无富集,说明它们对一些重金属元素的富集具有选择性,重金属Cu、Zn等在不同鱼类中更容易积累在肌肉中,类似的结果在其他研究中也有说明[18,25-26]. 重金属Cd的含量在6月最高,考虑到水体重金属的含量与季节变化有关,其温度变化可能也会对鱼体中重金属的吸收与代谢产生影响,根据文献[27]得知,夏季温度高会影响藻类的生长,使得硅藻对Cd的敏感性增强,说明鱼类食用水中藻类也会使体内重金属Cd的含量增加.
同一种鱼体的同一种重金属含量在不同月份之间也有显著的差异(P<0.05). 水体Hg含量水平6月份的最大,其结果与珍珠龙胆石斑鱼肌肉中Hg的含量规律一致,对于水体环境中的重金属,即使不参与鱼体的生长代谢,生物体通过摄食、呼吸等也有在体内产生累积的可能,所以养殖水体中重金属的含量可能会影响水产品健康,对于养殖鱼类而言,它们不仅可以通过体表的渗透功能把外来物质带来的重金属渗进肌肉中,还会通过鳃膜吸收溶解在水中的重金属离子[17,28];水体中6月的Cu和9月的Pb在4个月中含量较高,但此月份两种鱼体中的含量水平却不是最大. 考虑到换水率的阶段性波动和投喂的饲料残渣等没被及时排出形成的沉淀,长此以往可能会使水中重金属的沉淀累积至底层,两种鱼类又属于底栖生物,如果长期暴露在养殖池中更会有污染的风险,相关研究表明不同水产品的重金属含量特征存在很大差异,中上层洄游性鱼类的Cu、Zn含量就比近底层鱼类的高,而Pb、Cd含量相反,且本研究中两种鱼类的重金属含量也有一定的差别 [12-14],牙鲆和珍珠龙胆石斑鱼重金属含量(除Hg为P>0.05无显著差异)均值差异显著(P<0.05). 以上结果说明了影响水产品重金属含量的因素除了水源以外,还会与饲料的投喂、投入水产品的品种等情况有关[29]. 水产品的来源不同其体内重金属的含量也会有不一样的结果,依据非循环水养殖模式中牙鲆的重金属含量[30]得出表3,与本研究中牙鲆4个月均值对比可看出循环水养殖系统中的鱼类重金属含量最小,循环水养殖模式下的鱼类比其他生长模式中的鱼类要更加清洁.
-
牙鲆和珍珠龙胆石斑鱼的重金属污染结果评价见表4所示,两种鱼类Pb的Pi值均为5月最高, As的Pi 值均为9月最高,Pi平均都表示为Hg<Cu<Cd<Pb<Zn<As,牙鲆Zn的Pi值为10月最高;Cd的Pi 值为6月最高,而珍珠龙胆石斑鱼Zn的Pi 值为6月最高;Cd的Pi 值为5月最高,由单一污染指数可知,两种鱼类Cu、Pb、Cd、Zn、Hg的风险指数小于0.2均为正常背景值,没有遭受污染. As在0.2≤Pi<0.6之间,属于轻度污染,但5月份牙鲆和6月的珍珠龙胆石斑鱼As的Pi小于0.2为正常范围. 近年来,一些沿海地区的工农业生产及城市建设的加速,人为因素使重金属污染物汇入海洋,养殖用水从海水中抽取,所以会对水体洁净度产生一定影响[14],建议相关部门要引起重视,加强对近岸海域环境的监管. 本实验鱼体的综合污染指数表明,两种鱼类的P综均小于1,为正常背景值. 单一重金属污染指数有少许污染的情况并不会代表鱼类真正受到重金属的污染,许多关于养殖鱼类中重金属评估的相关文献中,也有单一污染指数为轻度甚至中度,而综合污染指数为正常背景值的情况[11,13,25,31],表明此循环水养殖系统中的牙鲆和珍珠龙胆石斑鱼无重金属超标情况且卫生质量符合标准.
-
由单一(THQ)及复合(TTHQ)重金属摄入的健康风险表5可知,每个月的单一和多金属的目标危险系数均小于1,可见暴露人群不存在潜在的重金属健康风险,安全性较好,其系数越小越安全. 其中,牙鲆的THQ4个月平均值的大小排序为:Hg<Cd<Cu<Pb<Zn<As;珍珠龙胆石斑鱼的THQ4个月平均值大小排序为:Hg<Pb<Cd<Cu<As<Zn,两种鱼类的THQ平均排列大小和单因子污染指数Pi 值的排列大小不同,两种鱼类9月的TTHQ均为最高.
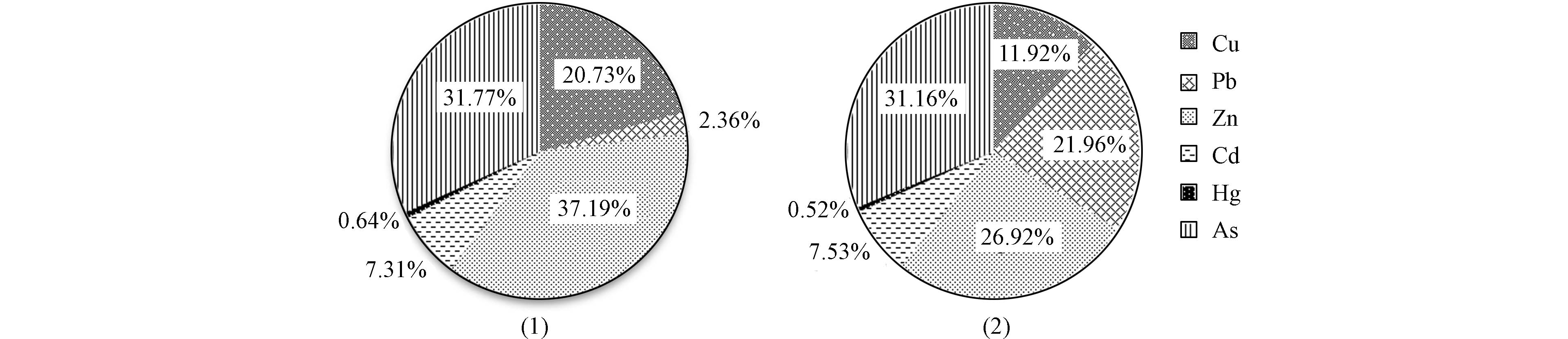
不同的重金属有着不一样的复合健康风险贡献率,比较不同重金属元素 THQ 占 TTHQ的平均比值如图3所示,Cu、Zn、As的数值占比较大,其中Cu、Zn占比为所有复合重金属系数的50%左右,为主要风险贡献者,适当的微量Cu、Zn等元素可以提高人体免疫力及调节血糖,所以食用适量此种鱼肉可以补充人体中所需的Cu、Zn微量元素且也是安全的. 由于不同重金属在不同鱼类中富集程度也不同[21-24],表中Hg的值最低,Zn的值最高,两种鱼类Pb的值接近. 虽然As单因子污染指数存在个别轻微污染,但根据综合污染指数以及单一及复合目标危险系数来看,都符合正常背景值且重金属含量未超标,所以可说明食用其循环水养殖系统中的牙鲆和珍珠龙胆石斑鱼不会存在重金属污染的健康风险.
-
(1)水体和鱼体内的重金属含量没有特定的规律性,没有随着月份的变化而发生累积增大的情况. 同一鱼体的重金属含量在不同生长周期存在显著差异(P<0.05),不同种类鱼体重金属含量均值差异显著(Hg除外),牙鲆和珍珠龙胆石斑鱼重金属含量大小均表现为Zn>Cu>As>Pb>Cd>Hg,所测实验对象均未超过它们的限量标准,所以是安全的.
(2)综合污染指数研究发现,两种鱼类的指数均小于1,为正常背景值,均未受到重金属Cu、Pb、Zn、Cd、Hg、As的污染,所以是无风险的.
(3)目标危害污染系数的评估方法,其单一和多金属的目标危险系数均小于1,证明暴露人群不存在潜在的重金属健康风险,所以食用此循环水养殖系统中的牙鲆和珍珠龙胆石斑鱼不会对人的身体造成有关重金属的健康风险,但长期的监测管理也是必不可少的.
循环水养殖系统重金属的分布特征及鱼体风险评估
Distribution characteristics of heavy metals in recirculating aquaculture system and risk assessment of fish
-
摘要: 为研究海水循环水养殖系统中水体及养殖鱼体重金属的分布特征和评估鱼体的污染状况及健康风险,本文以2021年山东省烟台市某水产公司两个海水循环水养殖系统中15个站点的水样和不同生长周期的牙鲆、珍珠龙胆石斑鱼(Paralichthys olivaceus、Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂)为研究对象,选用原子吸收光谱法和原子荧光光谱法测定分析其中重金属铜(Cu)、铅(Pb)、锌(Zn)、镉(Cd)、汞(Hg)和砷(As)的含量,并评估鱼体重金属的污染状况和健康风险. 结果显示,循环水养殖系统水体的重金属含量均未超标,在生物体中的含量均符合国家限量标准. 水体中Cu、Zn含量最大,Pb、Cd含量在9月最高,微滤机净化池水中的Pb含量大,Hg、Cu含量为6月最高,As含量为10月最大,水体中重金属含量可能与换水率、季节变化等情况有关. 鱼体中牙鲆和珍珠龙胆石斑鱼重金属含量均表现为Zn>Cu>As>Pb>Cd>Hg,Cu、Zn 作为鱼类生长的必要微量元素其含量最大;同一鱼体的重金属含量在不同生长周期存在显著差异,不同种类鱼体重金属含量均值差异显著(Hg除外). 根据综合污染指数法,鱼体肌肉内的重金属污染状况均属于无污染清洁状态,目标危险系数证明其膳食暴露风险都较低. 综合表明,此循环水养殖系统中的水体和鱼体是安全的,人类食用此系统中的鱼体不会存在相关风险.Abstract: In order to study the distribution characteristics of heavy metals in water body and cultured fish of the seawater recirculating aquaculture system and evaluate the pollution status and health risk of fish, this paper selected the water samples from 15 sites in two seawater recirculating aquaculture system and the Paralichthys olivaceus and Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂ with different growth period of an aquaculture company in Yantai City, Shandong Province in 2021 as the research objects. Atomic absorption spectrometry and atomic fluorescence spectrometry were used to determine and analyze the contents of copper (Cu), lead (Pb), zinc (Zn), cadmium (Cd), mercury (Hg) and arsenic (As), and we also evaluated the pollution status and health risks of heavy metals in fish. The results showed that the content of heavy metals in water body of the recirculating aquaculture system did not exceed the standard, and the content in organisms met the national limit standard. The content of Cu and Zn in water body were the highest, and the content of Pb and Cd were highest in September. The content of Pb was high in the water of the microfilter purification pool, the content of Hg and Cu were highest in June, and the content of As was highest in October. The content of heavy metals in water body may be related to the water exchange rate, seasonal changes, etc. The contents of heavy metals in Paralichthys olivaceus and Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂ were all followed the order: Zn>Cu>As>Pb>Cd>Hg, Cu and Zn were the essential trace elements for fish growth and their contents were the highest. The content of heavy metals in the same fish had significant differences in different growth period, and the mean content of heavy metals in different kinds of fish has significant differences (except Hg). According to the comprehensive pollution index method, the heavy metal in the muscle of fish belonged to the clean state without pollution. The method of target risk coefficient proved that the dietary exposure risk of fish was low. The comprehensive results showed that the water body and fish body in this circulating aquaculture system were safe, and there was no risk associated for human to eat the fish in this system.
-
Key words:
- recirculating aquaculture /
- heavy metals /
- fish /
- risk assessment.
-
山东省是我国的渔业大省,海洋资源丰富,水域滩涂辽阔,有着巨大的开发潜力,水产品总产量、渔业经济总产值位居全国前列. 从水产养殖面积构成来看,目前山东海水养殖面积远超淡水养殖面积. 2018年以来,山东省海水养殖面积占总面积的比重维持在70%以上;到2020年海水养殖面积为580.35千公顷,占总面积的77.9%,可见海水养殖在山东省的经济发展中占据重要地位[1]. 传统的粗放式养殖模式对水体造成的污染越来越严重,不利于水产养殖业的可持续发展,而循环水养殖系统具有高效、节水、节能、减排等优点,成为当前最具前景的养殖模式之一,对渔业绿色可持续发展有着突出贡献,并且现阶段循环水的健康养殖将是水产养殖产业绿色高质量发展及实现绿色水产品的重要途径. 2021年中央一号文件中明确指出,推进水产品绿色健康养殖,要加强农产品和食品安全监管,发展绿色、有机农产品.
有些重金属元素进入水体时,生物会通过摄取、吸附与积累等过程,对重金属进行传递和富集,最终造成水产品的重金属污染,再通过食物链富集传递给人类,一旦食用污染的水产品,长期积累将引起器官中毒,威胁人体健康. 重金属不仅会损害人体的神经系统、肝脏、肾脏和其他解毒器官,还会导致免疫系统的削弱,甚至诱发癌症[2]. 循环水养殖系统中虽然对养殖废水进行了一系列循环处理,但由于该系统水体交换率低且几乎封闭循环的特性,仍存在一定的风险性[3]. 如果对于源水的处理不够完善,养殖用水也会受到污染,加上投喂饲料等影响因素也可能有一定累积风险,重金属等危害物质一旦进入循环水养殖系统,就不容易被排出,从而导致养殖生物体内重金属的累积,直接捕捞食用可能会出现至关重要的食品安全问题[4-5].
国内外关于水产品重金属污染的研究主要集中在近岸海域、池塘淡水的人工养殖以及捕捞野生的水产品等方面 [6],关于循环水养殖系统中水产品的重金属等污染风险以及评估的研究较少. 本文选取山东省烟台市某水产公司海水循环水养殖系统中的重要经济鱼类牙鲆(Paralichthys olivaceus)和珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂)作为研究对象进行重金属检测分析,了解系统中水体、鱼体的重金属分布特征,并采用单因子污染指数法、综合污染指数法、目标危险系数法评估其重金属污染程度和重金属污染的健康风险,为循环水养殖产业绿色可持续发展和模式的优化提供科技支撑. 同时,为食用此养殖企业循环水系统中牙鲆和珍珠龙胆石斑鱼的居民提供食品安全的数据,对居民身体的健康保障也具有重要意义.
1. 材料与方法(Materials and methods)
1.1 实验材料
本实验选取山东省烟台市某水产公司牙鲆和珍珠龙胆石斑鱼海水循环水养殖系统的进水口、养殖池、出水口、微滤机、牙鲆养殖系统一级—四级净化池、珍珠龙胆石斑鱼养殖系统一级和二级净化池以及源水口等15个站点的水样和2021年不同生长周期的5、6、9、10月份可上市销售的牙鲆、珍珠龙胆石斑鱼,采集的水体样品各1 L装于聚乙烯瓶内和各3条鱼体装于泡沫箱内,标记后运回实验室冷冻备用. 同时,带回喂养实验鱼体的海水鱼饲料. 其中采集的牙鲆体长范围大致为25—30 cm;珍珠龙胆石斑鱼体长范围为21—27 cm. 其中,循环水养殖系统的结构如图1所示.
1.2 实验设备和试剂
主要设备:电热消解仪(型号:ED54-iTouch,美国LabTech)、原子吸收光谱仪(型号:PinAAcle900T,美国PerkinElmer)、原子荧光分光光度计(型号:AFS-933,北京吉天)、可见分光光度计(型号:EV-2200,上海昂拉)等.
主要试剂:硝酸、高氯酸、盐酸、甲基异丁酮、环己烷、冰乙酸、硫脲(国药集团化学试剂有限公司)、铜(Cu)、铅(Pb)、锌(Zn)、镉(Cd)、汞(Hg)、砷(As)、铬(Cr)单元素标准溶液(1000 mg·L−1,国家有色金属及电子材料分析测试中心)等,且试剂的纯度选择均按国标.
1.3 重金属的测定
鱼体:将所采集的鱼类样品室温下解冻,用去离子水冲洗干净鱼体和不锈钢刀,后用不锈钢刀做解剖,取鱼体肌肉可食用部分,用搅拌机制成泥状,装入聚乙烯密封袋等待后续消解工作. 测定鱼肉中的铜、铅、锌、镉、汞、砷,采用国标中的湿法消解. 重金属的前处理方法:称取试样(1.50±0.02)g(鲜重)于消解管中,加入8.0 mL硝酸和2.0 mL高氯酸,加盖放置12 h左右是为了能达到充分消解的效果,然后放石墨消解仪上,温度参考条件(120 ℃/0.5—1 h;升至180 ℃/2—4 h、升至200—220 ℃),消解至冒白烟(赶酸),无色透明或略带黄色停止,取出消解管冷却定容10 mL至容量瓶内,混匀备用,同时做空白试验和生物体分析标准物质实验. 其他具体过程以及分析方法均参照GB/T5009.12—2017《食品中铅的测定》,GB/T5009.13—2017《食品中铜的测定》,GB/T5009.14—2017《食品中锌的测定》,GB/T5009.15—2014《食品中镉的测定》,GB/T5009.11—2014《食品中总砷及无机砷的测定》,GB/T5009.17—2014《食品中总汞及无机汞的测定》.
水体:首先对水体进行过滤,取50 mL水样调节pH值至5.0,采用无火焰原子吸收分光光度法测定铜、铅和镉;另取50 mL水样调节pH值至4.0,采用火焰原子吸收分光光度法测定锌;采用原子荧光分光光度法测定汞和砷;其余详细步骤均按照GB17378.4—2007《海洋监测规范》第4部分 海水分析 进行有机萃取等前处理和分析检测工作.
1.4 牙鲆和珍珠龙胆石斑鱼重金属污染评价方法
评价方法采用单因子污染指数法和综合污染指数法进行.
单因子污染指数法计算公式(1)如下:
stringUtils.convertMath(!{formula.content}) (1) 其中,Pi表示鱼肉中重金属i的污染指数;Ci表示鱼肉中重金属i的实测含量;Si表示鱼肉中重金属i的标准限值. Pi<0.2为正常背景值;0.2≤Pi<0.6为轻微污染;0.6≤Pi<1.0为中污染;Pi≥1.0为重污染. 本研究标准限量值参考依据GB2762—2017《食品安全国家标准 食品中污染物限量》、NY/T 842—2021《绿色食品 鱼》、FAO和参考文献中的限量指标为标准限值,Cu、Pb、Zn、Cd、Hg、As的限量指标分别为 50、0.5、40.0、0.1、0.5、0.1 mg·kg-1[7-9].
综合污染指数法计算公式(2)如下:
stringUtils.convertMath(!{formula.content}) (2) 其中,P综表示鱼类重金属综合污染指数;Pave表示鱼类各单个污染指数Pi的平均值;Pmax为鱼类各单个污染指数中的最大值. 当P综≤1.0时,为正常背景水平;1.0< P综≤2.0 时,为轻度污染;2.0< P综≤3.0 时,为中度污染;P综>3.0 时,为重度污染[10-11].
1.5 牙鲆和珍珠龙胆石斑鱼重金属健康风险评价方法
本文以目标危险系数法(target hazard quotient,THQ)对重金属健康风险进行评价. 选用美国环保署(USEPA)推荐的健康风险评价常用方法模型[12-13],用于评估人体通过食物摄取重金属的风险. 该方法将鱼肉中重金属人体摄入剂量与其标准限值的比用来风险评价,可以综合评价单一或多种重金属的健康风险,计算公式见式(3—4). 当THQ>1,说明暴露人群存在潜在非致癌健康风险,THQ 值越大表明有害重金属对人体健康的非致癌风险越严重,同理也适用于TTHQ多种重金属复合健康风险[12,14].
stringUtils.convertMath(!{formula.content}) (3) stringUtils.convertMath(!{formula.content}) (4) 式中,EF为人群暴露频率(d·a−1);一般设定为365 d·a−1;ED为暴露时间(a),通常等于人均寿命,常取70 a;FIR为食物摄入率g∙(d∙人)−1,成人平均每人每天摄入水产品分别为 0.029 kg;Ci为食物中重金属含量水平,mg·kg−1;RFDi为重金属入口参考剂量,mg∙(kg∙人)−1,Cu、Pb、Zn、Cd、Hg、As的RFD分别为 0.04、0.0035、0.3、0.0010、0.0005、0.0003 mg∙ (kg∙人)−1;BW为人体平均体重(kg),成人平均体重取 61.8 kg;AT为非致癌性暴露平均时间,(365 d·a−1×暴露年限70 a)取25550 d;10−3为单位换算[11-17] .
当THQ<1 时,暴露人群无明显健康风险;当 THQ ≥1 时,则认定暴露人群存在健康风险。
1.6 数据统计与分析
实验数据采用Microsoft Office Excel 2010和Orange 8.5进行图表统计与制作,运用Microsoft Office Excel 2010中的数据分析进行双因素方差显著性分析.
2. 结果与讨论(Results and discussion)
2.1 牙鲆和珍珠龙胆石斑鱼养殖水体和饲料重金属含量分析
按照采样标准进行采样并检测其重金属,标准曲线相关性系数>0.995,回收率控制在85%—120%. 采样时用美国YSI 556型便携多参数水质监测仪对水体进行温度、盐度、pH值和溶解氧的测量,并记录数据,以确保实验对象是在适应的生长条件下成长的可供食用的正常健康鱼类,具备能够对重金属元素有良好的吸收和排出的能力.
牙鲆养殖系统中温度范围是16.6—18.9 ℃;盐度范围23.9‰—29.0‰;pH值范围6.53—7.94;溶解氧范围4.58—8.11 mg·L−1.
珍珠龙胆石斑鱼养殖系统中温度范围是19.8—27.0 ℃;盐度范围28.6‰—29.7‰;pH值范围6.01—8.11;溶解氧范围4.11—9.60 mg·L−1.
由图2可知,Cu含量相比来说较高的为珍珠龙胆石斑鱼养殖池出水,Cd含量较高的为牙鲆养殖池出水,养殖用水在循环水系统中对养殖生物至关重要,因为有研究发现池塘中重金属Cu的主要来源为养殖用水,其次才与饲料的投入等其他原因有关[18-19],说明循环水系统因有封闭循环等特征,养殖水中可能会存在一定的重金属元素[3].
4个月份中,Pb的含量水平9月最高,其中,微滤机净化池中的水Pb含量大,考虑是循环净化过程中,水中的Pb积累被过滤进入了微滤机净化池内的原因[3-5]. 可见运用循环水系统能够把水质里沉积的重金属进行有效吸附在微滤机过滤池中,养殖场应该提高其运行效率,把有害物质做出更好的排出处理[14]. 5月份每个水样的Hg含量较持平,6月份Hg的含量最高;10月的As含量最高,除了源水和珍珠龙胆石斑鱼的二级过滤池水外,每个水样都是10月的数值最大,6月的Cu总体含量最高,且4个月份中源水重金属的含量也有波动. 说明重金属元素含量可能与季节变化有关,根据其他研究发现,重金属元素会随季节因素影响呈现增大或减小的情况,Cu、Zn含量大致为春夏高于秋冬,Pb含量为春秋较高,Hg、As含量为夏秋较高,Cd含量为秋季较高[20],与本研究结果也大体一致,而且重金属含量也没有随着时间的推迟而累积,呈现持续上升等特定的规律性,循环水系统实际的换水率为10%左右,投喂量为1% (每日两次),所以可能是由换水频率的不固定性以及饲料的投喂量不同等多种原因造成的,其相关的结论在其他研究中也有说明[3].
由于六价铬对水生生物有致死作用,六价铬及其化合物受到各国主管当局严格的法规监管控制[21],所以本研究对水质六价铬进行了检测,5、6、9、10月的范围分别是0.22—0.82 μg·L−1、ND—2.40 μg·L−1、ND—4.30 μg·L−1、1.93—7.39 μg·L−1(ND为未检出). 依据GB 11607—1989 《渔业水质标准》Cu、Zn、Pb、Cd、Hg、As、Cr6+的标准限量分别是:10、100、50、5、0.5、50、100 μg·L−1,所测水体均符合标准限量.
同时,实验测出的喂养两种鱼的海水鱼饲料中重金属含量分别为:Cu 3.01 mg·kg−1、Pb 1.75 mg·kg−1、Zn 1.90 mg·kg−1、Cd 0.22 mg·kg−1、Hg 0.01 mg·kg−1、As 0.30 mg·kg−1. 结合GB 13078—2017《饲料卫生标准》 和NY 5072—2002《无公害食品 渔用配合饲料安全限量标准》,得到Pb、Cd、Hg、As的限量值分别为5.0、1.0、0.5、3.0 mg·kg−1,Cu和Zn没有标准限量,所有重金属均在标准限量内. 水体中Cu和Zn的值较大,其中Cu的含量范围是0.89—2.93 μg·L−1,Zn的范围是3.31—7.89 μg·L−1,最大值与最小值跨度也较大,可能是与水体中掺杂未被食用的饲料成分有关[22].
2.2 牙鲆和珍珠龙胆石斑鱼中重金属含量分析
分别对每个月份采集的牙鲆和珍珠龙胆石斑鱼体肌肉组织做3个平行样,对其进行重金属含量测定,取其平均值. 标准曲线相关性系数>0.995,回收率介于 85%—120%.
由前文可知鱼体中Cu、Pb、Zn、Cd、Hg、As的限量指标分别为 50、0.5、40.0、0.1、0.5、0.1 mg·kg−1. 结合表1、表2来看,所有重金属都未超标. 4个月份中重金属没有呈现规律性的增大和减少的状况,可能是随着时间的变化,重金属在鱼体内吸收和排出产生的波动影响. 两种鱼类重金属含量大小表现均为Zn>Cu>As>Pb>Cd>Hg,且都为Cu、Zn的值明显大于其他重金属. 对比表1和表2,两种鱼类中的Pb、As、Cd、Hg重金属含量对比均值相差10%左右,可见牙鲆和珍珠龙胆石斑鱼对Pb、As、Cd、Hg的吸收和积累能力相似,大多研究结果也都表明这些元素在鱼体内的含量较Cu、Zn等元素低[12-14,23]. 重金属离子可划分为营养和非营养类两种,Cu、Zn 作为鱼类生长的必要微量元素,参与构成鱼体内的酶,具有促进鱼骨发育、免疫、鱼类代谢调节等功能. 营养元素Cu和 Zn 等较非营养元素 As、Hg 等更能与机体吸收融合[24],而且不同重金属之间有着协同和竞争作用,某些金属元素有共用一个离子通道的情况,多种离子在同一环境中碰撞时,竞争效应会出现在生物体富集过程中,从而影响吸收[3]. 实验表明除Cu外,Zn富集能力相对较高,但Hg含量可以忽略不计,在这两种鱼体内基本无富集,说明它们对一些重金属元素的富集具有选择性,重金属Cu、Zn等在不同鱼类中更容易积累在肌肉中,类似的结果在其他研究中也有说明[18,25-26]. 重金属Cd的含量在6月最高,考虑到水体重金属的含量与季节变化有关,其温度变化可能也会对鱼体中重金属的吸收与代谢产生影响,根据文献[27]得知,夏季温度高会影响藻类的生长,使得硅藻对Cd的敏感性增强,说明鱼类食用水中藻类也会使体内重金属Cd的含量增加.
表 1 牙鲆重金属含量(mg·kg−1)Table 1. Contents of heavy metals in Paralichthys olivaceus重金属含量/(mg·kg−1)Heavy metals content 5月May 6月June 9月September 10月October 平均值Average Cu 0.165±0.054 0.200±0.020 0.216±0.029 0.153±0.009 0.184 Pb 0.043±0.008 0.025±0.004 0.024±0.007 0.026±0.007 0.030 Zn 2.597±0.503 3.220±1.076 2.734±0.336 3.892±0.144 3.110 Cd 0.002±0.000 0.006±0.004 0.003±0.001 0.003±0.000 0.003 Hg 0.001±0.001 0.001±0.001 0.000±0.000 0.000±0.000 0.001 As 0.005±0.001 0.036±0.009 0.058±0.016 0.046±0.004 0.036 表 2 珍珠龙胆石斑鱼重金属含量(mg·kg−1)Table 2. Contents of heavy metals in Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂重金属含量/(mg·kg−1)Heavy metals content 5月May 6月June 9月September 10月October 平均值Average Cu 0.247±0.014 0.086±0.047 0.286±0.007 0.424±0.071 0.261 Pb 0.046±0.024 0.018±0.013 0.018±0.001 0.021±0.001 0.026 Zn 2.950±0.101 4.707±1.901 3.972±0.249 2.424±1.392 3.512 Cd 0.004±0.000 0.004±0.003 0.001±0.000 0.001±0.000 0.002 Hg 0.000±0.000 0.001±0.000 0.000±0.000 0.000±0.000 0.001 As 0.040±0.013 0.001±0.000 0.070±0.048 0.037±0.003 0.053 同一种鱼体的同一种重金属含量在不同月份之间也有显著的差异(P<0.05). 水体Hg含量水平6月份的最大,其结果与珍珠龙胆石斑鱼肌肉中Hg的含量规律一致,对于水体环境中的重金属,即使不参与鱼体的生长代谢,生物体通过摄食、呼吸等也有在体内产生累积的可能,所以养殖水体中重金属的含量可能会影响水产品健康,对于养殖鱼类而言,它们不仅可以通过体表的渗透功能把外来物质带来的重金属渗进肌肉中,还会通过鳃膜吸收溶解在水中的重金属离子[17,28];水体中6月的Cu和9月的Pb在4个月中含量较高,但此月份两种鱼体中的含量水平却不是最大. 考虑到换水率的阶段性波动和投喂的饲料残渣等没被及时排出形成的沉淀,长此以往可能会使水中重金属的沉淀累积至底层,两种鱼类又属于底栖生物,如果长期暴露在养殖池中更会有污染的风险,相关研究表明不同水产品的重金属含量特征存在很大差异,中上层洄游性鱼类的Cu、Zn含量就比近底层鱼类的高,而Pb、Cd含量相反,且本研究中两种鱼类的重金属含量也有一定的差别 [12-14],牙鲆和珍珠龙胆石斑鱼重金属含量(除Hg为P>0.05无显著差异)均值差异显著(P<0.05). 以上结果说明了影响水产品重金属含量的因素除了水源以外,还会与饲料的投喂、投入水产品的品种等情况有关[29]. 水产品的来源不同其体内重金属的含量也会有不一样的结果,依据非循环水养殖模式中牙鲆的重金属含量[30]得出表3,与本研究中牙鲆4个月均值对比可看出循环水养殖系统中的鱼类重金属含量最小,循环水养殖模式下的鱼类比其他生长模式中的鱼类要更加清洁.
表 3 不同生长模式下牙鲆中重金属含量对比Table 3. Comparison of metal contents in Paralichthys olivaceus body weight under different growth modes模式 Pattern 重金属含量/(mg·kg−1) Heavy metal content Pb Cd Cu 循环水养殖Circulating aquaculture 0.030 0.003 0.184 近海养殖Inshore aquaculture 0.260 0.030 1.630 近海野生Inshore wild 0.250 0.030 1.670 2.3 牙鲆和珍珠龙胆石斑鱼的重金属污染风险评估
牙鲆和珍珠龙胆石斑鱼的重金属污染结果评价见表4所示,两种鱼类Pb的Pi值均为5月最高, As的Pi 值均为9月最高,Pi平均都表示为Hg<Cu<Cd<Pb<Zn<As,牙鲆Zn的Pi值为10月最高;Cd的Pi 值为6月最高,而珍珠龙胆石斑鱼Zn的Pi 值为6月最高;Cd的Pi 值为5月最高,由单一污染指数可知,两种鱼类Cu、Pb、Cd、Zn、Hg的风险指数小于0.2均为正常背景值,没有遭受污染. As在0.2≤Pi<0.6之间,属于轻度污染,但5月份牙鲆和6月的珍珠龙胆石斑鱼As的Pi小于0.2为正常范围. 近年来,一些沿海地区的工农业生产及城市建设的加速,人为因素使重金属污染物汇入海洋,养殖用水从海水中抽取,所以会对水体洁净度产生一定影响[14],建议相关部门要引起重视,加强对近岸海域环境的监管. 本实验鱼体的综合污染指数表明,两种鱼类的P综均小于1,为正常背景值. 单一重金属污染指数有少许污染的情况并不会代表鱼类真正受到重金属的污染,许多关于养殖鱼类中重金属评估的相关文献中,也有单一污染指数为轻度甚至中度,而综合污染指数为正常背景值的情况[11,13,25,31],表明此循环水养殖系统中的牙鲆和珍珠龙胆石斑鱼无重金属超标情况且卫生质量符合标准.
表 4 4个月的重金属单因子污染指数(Pi)和综合污染指数(P综)Table 4. Single factor pollution index (Pi) and comprehensive pollution index (P综)Cu Pb Zn Cd Hg As P综 牙鲆(Paralichthys olivaceus) 5月 0.003 0.087 0.065 0.020 0.002 0.050 0.354 6月 0.004 0.051 0.081 0.039 0.002 0.360 0.474 9月 0.004 0.048 0.068 0.030 0.001 0.580 0.592 10月 0.003 0.052 0.097 0.027 0.000 0.460 0.532 Pi平均 0.004 0.059 0.078 0.029 0.002 0.360 0.474 珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂) 5月 0.005 0.092 0.074 0.040 0.001 0.400 0.500 6月 0.002 0.037 0.118 0.035 0.002 0.010 0.276 9月 0.006 0.036 0.099 0.013 0.001 0.430 0.514 10月 0.008 0.042 0.061 0.006 0.001 0.370 0.475 Pi平均 0.005 0.050 0.088 0.023 0.002 0.300 0.435 2.4 牙鲆和珍珠龙胆石斑鱼的重金属健康风险评估
由单一(THQ)及复合(TTHQ)重金属摄入的健康风险表5可知,每个月的单一和多金属的目标危险系数均小于1,可见暴露人群不存在潜在的重金属健康风险,安全性较好,其系数越小越安全. 其中,牙鲆的THQ4个月平均值的大小排序为:Hg<Cd<Cu<Pb<Zn<As;珍珠龙胆石斑鱼的THQ4个月平均值大小排序为:Hg<Pb<Cd<Cu<As<Zn,两种鱼类的THQ平均排列大小和单因子污染指数Pi 值的排列大小不同,两种鱼类9月的TTHQ均为最高.
表 5 单一(THQ)及复合(TTHQ)重金属摄入的健康风险指数Table 5. Health risk index of single (THQ) and complex (TTHQ) heavy metal intakeCu Pb Zn Cd Hg As TTHQ 牙鲆(Paralichthys olivaceus) 5月 0.0074 0.0222 0.0155 0.0036 0.0004 0.0030 0.0520 6月 0.0090 0.0130 0.0192 0.0070 0.0004 0.0215 0.0700 9月 0.0097 0.0123 0.0163 0.0054 0.0002 0.0556 0.0995 10月 0.0069 0.0132 0.0233 0.0048 0.0001 0.0275 0.0757 THQ平均 0.0082 0.0152 0.0186 0.0052 0.0004 0.0269 0.0744 珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂) 5月 0.0110 0.0024 0.0176 0.0072 0.0001 0.0239 0.0622 6月 0.0039 0.0010 0.0281 0.0063 0.0004 0.0006 0.0402 9月 0.0128 0.0009 0.0237 0.0023 0.0001 0.0257 0.0656 10月 0.0190 0.0011 0.0145 0.0011 0.0001 0.0221 0.0579 THQ平均 0.0117 0.0013 0.0210 0.0041 0.0004 0.0179 0.0564 不同的重金属有着不一样的复合健康风险贡献率,比较不同重金属元素 THQ 占 TTHQ的平均比值如图3所示,Cu、Zn、As的数值占比较大,其中Cu、Zn占比为所有复合重金属系数的50%左右,为主要风险贡献者,适当的微量Cu、Zn等元素可以提高人体免疫力及调节血糖,所以食用适量此种鱼肉可以补充人体中所需的Cu、Zn微量元素且也是安全的. 由于不同重金属在不同鱼类中富集程度也不同[21-24],表中Hg的值最低,Zn的值最高,两种鱼类Pb的值接近. 虽然As单因子污染指数存在个别轻微污染,但根据综合污染指数以及单一及复合目标危险系数来看,都符合正常背景值且重金属含量未超标,所以可说明食用其循环水养殖系统中的牙鲆和珍珠龙胆石斑鱼不会存在重金属污染的健康风险.
3. 结论(Conclusion)
(1)水体和鱼体内的重金属含量没有特定的规律性,没有随着月份的变化而发生累积增大的情况. 同一鱼体的重金属含量在不同生长周期存在显著差异(P<0.05),不同种类鱼体重金属含量均值差异显著(Hg除外),牙鲆和珍珠龙胆石斑鱼重金属含量大小均表现为Zn>Cu>As>Pb>Cd>Hg,所测实验对象均未超过它们的限量标准,所以是安全的.
(2)综合污染指数研究发现,两种鱼类的指数均小于1,为正常背景值,均未受到重金属Cu、Pb、Zn、Cd、Hg、As的污染,所以是无风险的.
(3)目标危害污染系数的评估方法,其单一和多金属的目标危险系数均小于1,证明暴露人群不存在潜在的重金属健康风险,所以食用此循环水养殖系统中的牙鲆和珍珠龙胆石斑鱼不会对人的身体造成有关重金属的健康风险,但长期的监测管理也是必不可少的.
-
表 1 牙鲆重金属含量(mg·kg−1)
Table 1. Contents of heavy metals in Paralichthys olivaceus
重金属含量/(mg·kg−1)Heavy metals content 5月May 6月June 9月September 10月October 平均值Average Cu 0.165±0.054 0.200±0.020 0.216±0.029 0.153±0.009 0.184 Pb 0.043±0.008 0.025±0.004 0.024±0.007 0.026±0.007 0.030 Zn 2.597±0.503 3.220±1.076 2.734±0.336 3.892±0.144 3.110 Cd 0.002±0.000 0.006±0.004 0.003±0.001 0.003±0.000 0.003 Hg 0.001±0.001 0.001±0.001 0.000±0.000 0.000±0.000 0.001 As 0.005±0.001 0.036±0.009 0.058±0.016 0.046±0.004 0.036 表 2 珍珠龙胆石斑鱼重金属含量(mg·kg−1)
Table 2. Contents of heavy metals in Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂
重金属含量/(mg·kg−1)Heavy metals content 5月May 6月June 9月September 10月October 平均值Average Cu 0.247±0.014 0.086±0.047 0.286±0.007 0.424±0.071 0.261 Pb 0.046±0.024 0.018±0.013 0.018±0.001 0.021±0.001 0.026 Zn 2.950±0.101 4.707±1.901 3.972±0.249 2.424±1.392 3.512 Cd 0.004±0.000 0.004±0.003 0.001±0.000 0.001±0.000 0.002 Hg 0.000±0.000 0.001±0.000 0.000±0.000 0.000±0.000 0.001 As 0.040±0.013 0.001±0.000 0.070±0.048 0.037±0.003 0.053 表 3 不同生长模式下牙鲆中重金属含量对比
Table 3. Comparison of metal contents in Paralichthys olivaceus body weight under different growth modes
模式 Pattern 重金属含量/(mg·kg−1) Heavy metal content Pb Cd Cu 循环水养殖Circulating aquaculture 0.030 0.003 0.184 近海养殖Inshore aquaculture 0.260 0.030 1.630 近海野生Inshore wild 0.250 0.030 1.670 表 4 4个月的重金属单因子污染指数(Pi)和综合污染指数(P综)
Table 4. Single factor pollution index (Pi) and comprehensive pollution index (P综)
Cu Pb Zn Cd Hg As P综 牙鲆(Paralichthys olivaceus) 5月 0.003 0.087 0.065 0.020 0.002 0.050 0.354 6月 0.004 0.051 0.081 0.039 0.002 0.360 0.474 9月 0.004 0.048 0.068 0.030 0.001 0.580 0.592 10月 0.003 0.052 0.097 0.027 0.000 0.460 0.532 Pi平均 0.004 0.059 0.078 0.029 0.002 0.360 0.474 珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂) 5月 0.005 0.092 0.074 0.040 0.001 0.400 0.500 6月 0.002 0.037 0.118 0.035 0.002 0.010 0.276 9月 0.006 0.036 0.099 0.013 0.001 0.430 0.514 10月 0.008 0.042 0.061 0.006 0.001 0.370 0.475 Pi平均 0.005 0.050 0.088 0.023 0.002 0.300 0.435 表 5 单一(THQ)及复合(TTHQ)重金属摄入的健康风险指数
Table 5. Health risk index of single (THQ) and complex (TTHQ) heavy metal intake
Cu Pb Zn Cd Hg As TTHQ 牙鲆(Paralichthys olivaceus) 5月 0.0074 0.0222 0.0155 0.0036 0.0004 0.0030 0.0520 6月 0.0090 0.0130 0.0192 0.0070 0.0004 0.0215 0.0700 9月 0.0097 0.0123 0.0163 0.0054 0.0002 0.0556 0.0995 10月 0.0069 0.0132 0.0233 0.0048 0.0001 0.0275 0.0757 THQ平均 0.0082 0.0152 0.0186 0.0052 0.0004 0.0269 0.0744 珍珠龙胆石斑鱼(Epinephelus fuscoguttatus♀×Epinephelus lanceolatus♂) 5月 0.0110 0.0024 0.0176 0.0072 0.0001 0.0239 0.0622 6月 0.0039 0.0010 0.0281 0.0063 0.0004 0.0006 0.0402 9月 0.0128 0.0009 0.0237 0.0023 0.0001 0.0257 0.0656 10月 0.0190 0.0011 0.0145 0.0011 0.0001 0.0221 0.0579 THQ平均 0.0117 0.0013 0.0210 0.0041 0.0004 0.0179 0.0564 -
[1] 2020年全国渔业经济统计公报[J]. 中国水产, 2021(8): 11-12. Statistical bulletin of national fishery economy in 2020[J]. China Fisheries, 2021(8): 11-12(in Chinese).
[2] 蔡深文, 倪朝辉, 刘斌, 等. 赤水河主要经济鱼类重金属含量及风险评价 [J]. 淡水渔业, 2017, 47(3): 105-112. doi: 10.3969/j.issn.1000-6907.2017.03.016 CAI S W, NI Z H, LIU B, et al. Concentration and risk assessment of heavy metals in the main economic fishes from Chishui River [J]. Freshwater Fisheries, 2017, 47(3): 105-112(in Chinese). doi: 10.3969/j.issn.1000-6907.2017.03.016
[3] 万慧珊, 程波, 宋晓红, 等. 循环水养殖欧洲鲈鱼(Dicentrarchus labrax)重金属污染状况与富集分布特征 [J]. 渔业科学进展, 2017, 38(5): 83-91. doi: 10.11758/yykxjz.20160826001 WAN H S, CHENG B, SONG X H, et al. Contamination and accumulation of heavy metals in Dicentrarchus labrax cultured in recirculating aquatic systems [J]. Progress in Fishery Sciences, 2017, 38(5): 83-91(in Chinese). doi: 10.11758/yykxjz.20160826001
[4] SALAM M A, DAYAL S R, SIDDIQUA S A, et al. Risk assessment of heavy metals in marine fish and seafood from Kedah and Selangor coastal regions of Malaysia: A high-risk health concern for consumers [J]. Environmental Science and Pollution Research, 2021, 28(39): 55166-55175. doi: 10.1007/s11356-021-14701-z [5] HAN J L, PAN X D, CHEN Q, et al. Health risk assessment of heavy metals in marine fish to the population in Zhejiang, China [J]. Scientific Reports, 2021, 11: 11079. doi: 10.1038/s41598-021-90665-x [6] 王炫凯, 赵彤, 岳扬, 等. 循环水养殖红鳍东方鲀的重金属污染状况与健康风险评价[J]. 大连海洋大学学报. DOI:10.16535/j.cnki.dlhyxb.2021-280. WANG X K, ZHAO T, YUE Y, et al. Heavy metals contamination and health risk assessment in recirculating aquaculture Takifugu rubripes[J]. Journal of Dalian Ocean University,DOI:10.16535/j.cnki.dlhyxb.2021-280 (in Chinese).
[7] NAUEN C E, . Compilation of legal limits for hazardous substances in fish and fishery products[C]. FAO Fisheries Circular, 1983. [8] 中华人民共和国卫生部. GB 2762—2017 食品安全国家标准 食品中污染物限量(S). 北京: 中国标准出版社, 2017. Ministry of Health of PRC. GB 2762—2017 National food safety standard-Maximum levels of contaminants in foods(S). Beijing: China Standards Press, 2017(in Chinese).
[9] GAO Y, FANG L, XIANG Q Q, et al. Ecological risk assessment of heavy metals in fish from the Dianchi Lake, China using the integrated biomarker response approach [J]. Environmental Science and Pollution Research, 2020, 27(36): 45712-45721. doi: 10.1007/s11356-020-10434-7 [10] LIU J H, CAO L, DOU S Z. Bioaccumulation of heavy metals and health risk assessment in three benthic bivalves along the coast of Laizhou Bay, China [J]. Marine Pollution Bulletin, 2017, 117(1/2): 98-110. [11] 罗钦, 吴建衍, 潘葳. 3种养殖淡水鱼重金属含量测定及健康风险评价 [J]. 食品安全质量检测学报, 2020, 11(18): 6568-6574. doi: 10.19812/j.cnki.jfsq11-5956/ts.2020.18.056 LUO Q, WU J Y, PAN W. Determination of heavy metal content of 3 kinds of cultured freshwater fish and health risk assessment [J]. Journal of Food Safety & Quality, 2020, 11(18): 6568-6574(in Chinese). doi: 10.19812/j.cnki.jfsq11-5956/ts.2020.18.056
[12] 刘洋, 林彩, 陈金民, 等. 南海游泳动物重金属含量特征及风险评价 [J]. 海洋环境科学, 2021, 40(3): 401-406,416. doi: 10.12111/j.mes.20200110 LIU Y, LIN C, CHEN J M, et al. Distribution and risk assessment of heavy metal in nekton of South China Sea [J]. Marine Environmental Science, 2021, 40(3): 401-406,416(in Chinese). doi: 10.12111/j.mes.20200110
[13] 盛蒂, 朱兰保. 蚌埠市场食用鱼重金属含量及安全性评价 [J]. 食品工业科技, 2014, 35(22): 49-52,56. doi: 10.13386/j.issn1002-0306.2014.22.001 SHENG D, ZHU L B. Heavy metal content and safety evaluation of fish in Bengbu market [J]. Science and Technology of Food Industry, 2014, 35(22): 49-52,56(in Chinese). doi: 10.13386/j.issn1002-0306.2014.22.001
[14] 白晨, 郝天琦, 赵心悦, 等. 辽西沿海地区4种海鱼重金属富集特征与污染风险评价 [J]. 现代畜牧兽医, 2021(3): 70-73. BAI C, HAO T Q, ZHAO X Y, et al. Bioaccumulation characteristics and pollution risk assessment of four marine fishes in the coastal area of western Liaoning [J]. Modern Journal of Animal Husbandry and Veterinary Medicine, 2021(3): 70-73(in Chinese).
[15] 中华人民共和国国家卫生和计划生育委员会. 中国居民营养与慢性病状况报告(2015) (R). 中华人民共和国国家卫生健康委员会, 2015. National Health and Family Planning Commission of PRC. Report on nutrition and chronic diseases of Chinese residents (2015) (R). National Health Commission of the People's Republic of China, 2015(in Chinese).
[16] 郑娜, 王起超, 郑冬梅. 基于THQ的锌冶炼厂周围人群食用蔬菜的健康风险分析 [J]. 环境科学学报, 2007, 27(4): 672-678. doi: 10.3321/j.issn:0253-2468.2007.04.022 ZHENG N, WANG Q C, ZHENG D M. Health risk assessment of heavy metals to residents by consuming vegetable irrigated around zinc smelting plant based THQ [J]. Acta Scientiae Circumstantiae, 2007, 27(4): 672-678(in Chinese). doi: 10.3321/j.issn:0253-2468.2007.04.022
[17] 张晓文, 邵柳逸, 连宾. 4种太湖水产品体内重金属富集特征及食用安全性评价 [J]. 食品科学, 2018, 39(2): 310-314. doi: 10.7506/spkx1002-6630-201802049 ZHANG X W, SHAO L Y, LIAN B. Accumulation characteristics and safety evaluation of heavy metals in four kinds of aquatic products from lake Taihu [J]. Food Science, 2018, 39(2): 310-314(in Chinese). doi: 10.7506/spkx1002-6630-201802049
[18] LACERDA L D, SANTOS J A, MADRID R M. Copper emission factors from intensive shrimp aquaculture [J]. Marine Pollution Bulletin, 2006, 52(12): 1823-1826. doi: 10.1016/j.marpolbul.2006.09.012 [19] SOW A Y, ISMAIL A, ZULKIFLI S Z, et al. Survey on heavy metals contamination and health risk assessment in commercially valuable Asian swamp eel, Monopterus albus from Kelantan, Malaysia [J]. Scientific Reports, 2019, 9: 6391. doi: 10.1038/s41598-019-42753-2 [20] 车琳萍, 上官魁星, 于彩芬. 辽东湾北部近海渔业水域中重金属污染的季节和年际变化 [J]. 河北渔业, 2018(5): 44-49. doi: 10.3969/j.issn.1004-6755.2018.05.013 CHE L P, SHANGGUAN K X, YU C F. Seasonal and interannual changes of heavy metal pollution in offshore fishery waters of northern Liaodong Bay [J]. Hebei Fisheries, 2018(5): 44-49(in Chinese). doi: 10.3969/j.issn.1004-6755.2018.05.013
[21] 杨冬梅. 铬与人体健康 [J]. 科技创新导报, 2008, 5(30): 179. doi: 10.3969/j.issn.1674-098X.2008.30.176 YANG D M. Chromium and human health [J]. Science and Technology Innovation Herald, 2008, 5(30): 179(in Chinese). doi: 10.3969/j.issn.1674-098X.2008.30.176
[22] 吴伟, 范立民. 水产养殖环境的污染及其控制对策 [J]. 中国农业科技导报, 2014, 16(2): 26-34. doi: 10.13304/j.nykjdb.2014.076 WU W, FAN L M. Pollution and control measures of aquaculture environment [J]. Journal of Agricultural Science and Technology, 2014, 16(2): 26-34(in Chinese). doi: 10.13304/j.nykjdb.2014.076
[23] 吴丹, 张小军, 曾军杰, 等. 嵊泗区域贻贝重金属污染研究及健康风险评估 [J]. 安徽农业科学, 2021, 49(22): 164-169. doi: 10.3969/j.issn.0517-6611.2021.22.041 WU D, ZHANG X J, ZENG J J, et al. The pollution and health risk assessment of heavy metals in mussels in Shengsi area [J]. Journal of Anhui Agricultural Sciences, 2021, 49(22): 164-169(in Chinese). doi: 10.3969/j.issn.0517-6611.2021.22.041
[24] 王明华, 王桂忠, 李少菁. 重金属在海洋甲壳动物中的吸收和代谢[J]. 福建农业学报, 2005, 20(S1): 51-56. WANG M H, WANG G Z, LI S J. Assimilation and metabolism of heavy metals in marine crustacean[J]. Fujian Journal of Agricultural Sciences, 2005, 20(Sup 1): 51-56(in Chinese).
[25] WEI Y H, ZHANG J Y, ZHANG D W, et al. Metal concentrations in various fish organs of different fish species from Poyang Lake, China [J]. Ecotoxicology and Environmental Safety, 2014, 104: 182-188. doi: 10.1016/j.ecoenv.2014.03.001 [26] USMAN Y M, NASIRU Y P, MODIBBO U U. Health risk assessment on humans by contamination of heavy metals in some edible crops and fish at Galena mining area of Nahuta, Alkaleri Local Government Area, Bauchi State, Nigeria [J]. African Journal of Pure and Applied Chemistry, 2020, 14(3): 42-50. doi: 10.5897/AJPAC2019.0814 [27] 徐笠, 陆安祥, 王纪华. 温度变化对重金属植物有效性影响的研究进展 [J]. 江苏农业科学, 2016, 44(10): 26-30. doi: 10.15889/j.issn.1002-1302.2016.10.006 XU L, LU A X, WANG J H. Research progress on the effect of temperature change on the availability of heavy metal plants [J]. Jiangsu Agricultural Sciences, 2016, 44(10): 26-30(in Chinese). doi: 10.15889/j.issn.1002-1302.2016.10.006
[28] 张小磊, 王晶晶, 安春华, 等. 郑州沿黄地区养殖鱼类中重金属污染与健康风险评价 [J]. 生态环境学报, 2018, 27(2): 350-355. doi: 10.16258/j.cnki.1674-5906.2018.02.020 ZHANG X L, WANG J J, AN C H, et al. Pollution characteristics and health risk assessment of heavy metals in cultured fish species along the Yellow River in Zhengzhou [J]. Ecology and Environmental Sciences, 2018, 27(2): 350-355(in Chinese). doi: 10.16258/j.cnki.1674-5906.2018.02.020
[29] LE N D, HOANG T T H, PHUNG V P, et al. Evaluation of heavy metal contamination in the coastal aquaculture zone of the Red River Delta (Vietnam) [J]. Chemosphere, 2022, 303: 134952. doi: 10.1016/j.chemosphere.2022.134952 [30] 王际英, 马晶晶, 李宝山, 等. 野生与人工养殖褐牙鲆亲鱼微量元素组成的差异比较 [J]. 渔业科学进展, 2012, 33(2): 29-34. doi: 10.3969/j.issn.1000-7075.2012.02.005 WANG J Y, MA J J, LI B S, et al. A comparison study of trace elements in wild and cultured Japanese flounder Paralichthys olivaceus [J]. Progress in Fishery Sciences, 2012, 33(2): 29-34(in Chinese). doi: 10.3969/j.issn.1000-7075.2012.02.005
[31] HASAN M, RAHMAN M, AHMED A A, et al. Heavy metal pollution and ecological risk assessment in the surface water from a marine protected area, Swatch of No Ground, north-western part of the Bay of Bengal [J]. Regional Studies in Marine Science, 2022, 52: 102278. doi: 10.1016/j.rsma.2022.102278 期刊类型引用(5)
1. 刘倩,吕少梁,陈宁,王学锋. 基于鱼类生长特征和营养成分视角分析豹纹鳃棘鲈增殖放流水域的适宜性. 水产学报. 2025(02): 163-173 .  百度学术
百度学术
2. 李奇龙,夏斌,隋琪,曲克明,朱琳,李玉. 渤海渔业生物重金属污染及风险评价. 渔业科学进展. 2024(02): 39-49 .  百度学术
百度学术
3. 庞巧珠,陈晓慧,谢海群,梁计林,邢孔敏. 万宁小海海域重金属分布特征研究及其风险评价. 广西科学. 2024(03): 554-564 .  百度学术
百度学术
4. 刘忠艳,杨俊杰,乔沐溪,刘瑶. 基于高光谱技术的重金属污染蛤仔快速无损鉴别. 生物学杂志. 2024(06): 104-110 .  百度学术
百度学术
5. 陈倩,谢青,李游镒,吕红健,李佳佳,王永敏,王定勇. 三峡库区短颌鲚重金属累积特征及来源解析. 中国环境科学. 2023(08): 4360-4369 .  百度学术
百度学术
其他类型引用(3)
-






 下载:
下载: