-
随着经济的发展,环境污染问题日益严重. 在众多污染物里抗生素危害极大,它会诱导产生抗药菌和抗药基因,从而危害人和动物的健康. 其中,四环素(tetracycline)作为一种典型的抗生素,广泛应用于医药工业中,经常在废水中被监测到 [1]. 在过去几年中,物理化学技术,如氧化[2]、膜技术[3]和光催化[4]已被应用于处理抗生素废水. 其中,半导体光催化被认为是一种有效、绿色、节能的技术,而获得了广泛的关注.
二氧化钛(TiO2)作为典型的光催化剂,因其无毒、稳定性好和成本低,而被广泛应用[5]. 它有两种主要的晶型:锐钛矿、金红石. 其中,锐钛矿被广泛认为拥有良好的光催化性能[6];金红石的带隙宽度稍小于锐钛矿, 在光催化产H2中比锐钛矿效果更好[7]. 然而, Kawahara等认为混合晶型的TiO2比单一晶型拥有更高的光催化活性[8]. 为解决TiO2的带隙宽度大,可见光下效果差,光生电子和空穴复合速度快,光催化活性低等劣势. 研究者们采用复合其他材料来改善这些缺点. Wang等制备了TiO2/g-C3N4复合材料, 提高了光生载流子的迁移效率,减少复合率,增强了光催化降解四环素的效果[9];Hajipour 等用一种简单沉淀法制备出了TiO2/CuO复合材料,减小了带隙宽度,使材料可以在可见光下快速降解阿莫西林[10]; Ali 等将SBA 15和TiO2进行复合,使得TiO2的比表面积变大,反应活性位点增加,光催化性能提升[11].
碳量子点(CQDs)是一种碳基零维材料,被广泛用于光催化、生物传感和生物成像等技术领域[12-14]. CQDs可以作为复合材料的电子库,提高光生电子-空穴对的分离,拥有上转换光致发光特性,与其他半导体复合后可提高材料对可见光的利用率. 表面的官能团可以通过在光催化剂表面提供更高的吸附容量来增强光催化活性[15]. Wang等的研究表明,锐钛矿相二氧化钛在与碳量子复合后,在光催化下的产H2能力是以前的9. 7倍,复合材料表现出极高的光催化活性[16]; Muhammad等发现,当初始溶液pH 11时,CQD/TiO2对甲基橙废水的降解率是TiO2的3倍[17].
本研究研制了一种全新的CQDs/TiO2:首先制备了锐钛矿与金红石混相的TiO2,以葡萄糖为碳源制备了CQDs,后将两者合成了CQDs/TiO2纳米复合材料. 在可见光条件下降解四环素废水. 探究了不同条件下,复合材料对四环素废水的降解性能,并探究降解机理.
-
四异丙醇钛、乙醇、葡萄糖、氢氧化钠、氨水、四环素、对苯醌、四氯化碳、异丙醇、草酸铵、去离子水,0. 22 μm滤膜,透析袋(3500 MW),所用试剂均为分析纯.
-
TiO2纳米颗粒的制备 先将四异丙醇钛(4 mL)与乙醇(20 mL)混合,磁力搅拌1 h,超声30 min.与含H2O(4 mL)和乙醇(10 mL)的溶液混合,并将混合物保持在恒速下搅拌(1 h). 将混合物在水热反应釜中以180 ℃加热12 h. 收集的粉末用水和乙醇清洗,90 ℃干燥后在530 ℃下煅烧5 h.
CQDs的制备方法 首先,0.15 g葡萄糖加入40 mL水中,加入一定浓度的氨水并搅拌. 将溶液转移至100 mL聚四氟乙烯反应器中,然后以180 ℃在干燥箱中加热10 h. 再将其冷却至室温,用0.22 μm微孔膜去除大颗粒物质,通过透析袋(3500 MW)透析2 d,去除杂质离子. 即可得CQDs溶液,通过冷冻干燥可得到CQDs粉末.
CQDs/TiO2的制备方法. 先前制备的TiO2(0.64 g)分散于CQDs溶液中,加入20 mL蒸馏水,超声30 min,磁力搅拌3 h,使其混合均匀. 随后将溶液在烘箱中80 ℃干燥10 h,用去离子水离心洗涤4次并再次干燥,即获得CQDs/TiO2. 用不同葡萄糖含量(0.1 g、0.15 g、0.2 g)合成的复合材料分别记作为CT1、CT2、CT3.
-
采用X射线衍射仪(日本D/Max 2500)进行催化剂的晶体结构分析; X射线光电子能谱仪(美国Thermo Scientific K-Alpha)研究了催化剂中各种元素的表面化学成分和价态;透射电子显微镜 (日本JEOL JEM-F200)观察了材料形貌和晶格间距;全自动比表面及孔隙度分析仪(康塔Autosorb-IQ-MP)探究了复合材料的比表面积;傅里叶红外变换光谱仪(德国Bruker VERTEX70)分析了材料的化学键和官能团;紫外-可见分光光度计(日本Shimadzu UV-3600i Plus)探究了光学特征.
-
50 mg催化剂分散到50 mL四环素水溶液(10 mg·L−1)中. 在光催化实验开始之前,溶液在黑暗中搅拌30 min,以达到吸附-解吸平衡. 之后,开启氙灯,光催化反应开始. 定期从上清液中取出试样,并在12000 r·min−1下离心3 min,以去除固体颗粒,使用紫外-可见分光光度计测定四环素浓度.
为了评估纳米复合材料和嵌入在TiO2表面CQDs的稳定性,进行5次循环重复测试. 每次光催化反应后,以6000 r·min−1的转速离心4 min,收集光催化剂,用去离子水清洗,后在烘箱中60 ℃干燥,收集的光催化剂在相同条件下重复实验4次.
-
淬灭实验常用于探究光催化机理. 在其他条件不变的情况下,加入异丙醇(IPA,5 mmol)、四氯化碳(CCl4,5 mmol)、苯醌(BQ,1.5 mmol)、草酸铵(AO,5 mmol)分别作·OH、 e-、·O2-、h+的清除剂[18-21].
-
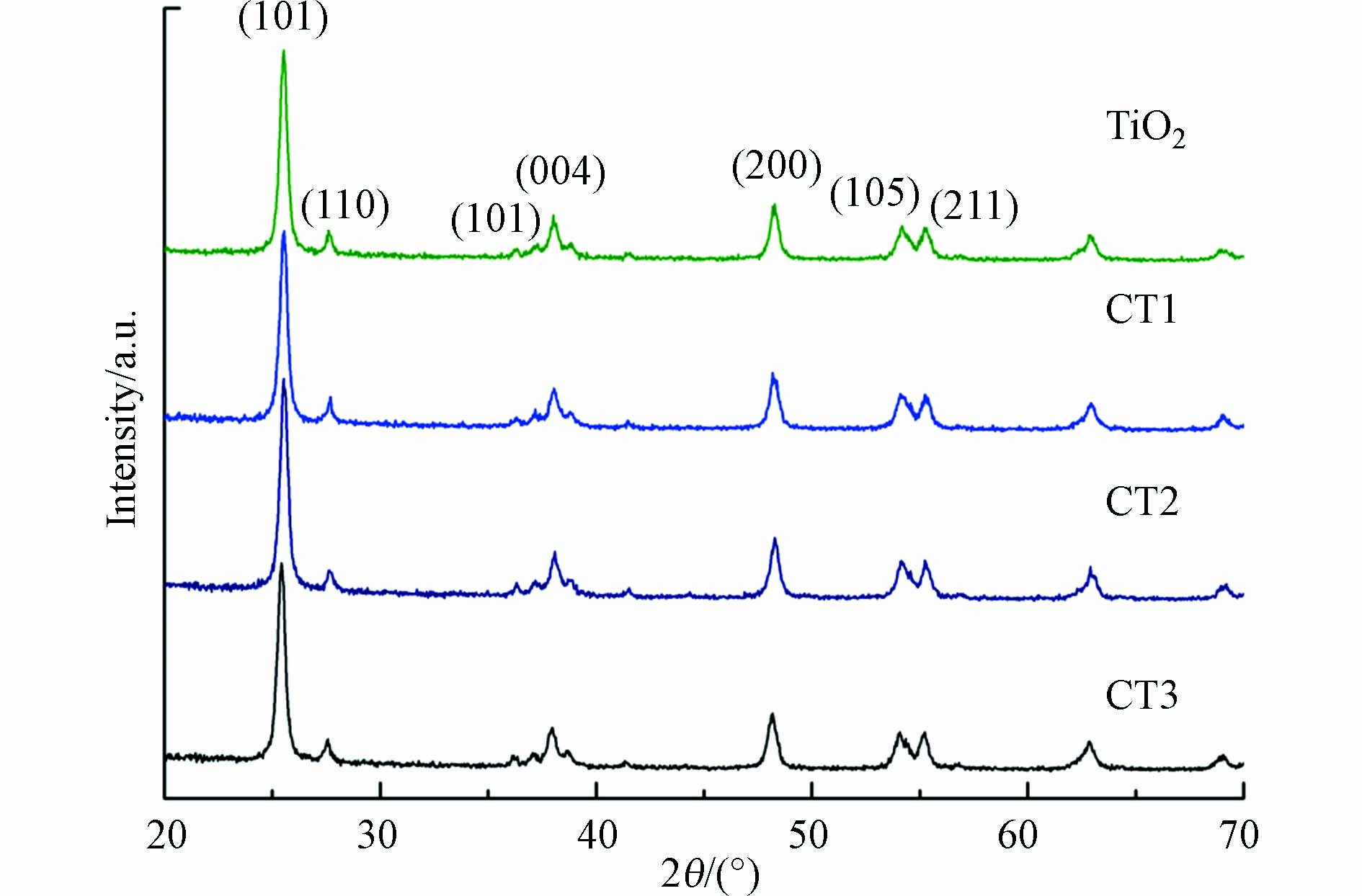
XRD分析如图1所示,对比PDF卡片,在TiO2和不同配比的CQDs/TiO2复合材料谱图中均检测到对应的晶面信息. 其中属于锐钛矿的峰有:25.3°(101)、37. 8°(004)、48.0°(200)、54.0°(105)、55.1°(211),属于金红石的峰有:27.4°(110)、36.1°(101). 证明混相TiO2制备成功. TiO2与CQDs/TiO2的峰形都没有明显的变化,说明CQDs的负载没有改变TiO2的晶体结构. 复合材料峰的位置几乎未发生偏移,这表明CQDs分散在TiO2表面,没有进入TiO2晶格[22]. 在复合材料的XRD图中没有检测到CQDs的衍射峰,表明掺杂没有导致生成其他物质. 也与CQDs掺杂量较低、结晶度差有关.
通过TEM和HR-TEM分析了CQDs和CQDs/TiO2纳米复合材料的形态外观. 图2a为通过水热法获得的CQDs的TEM图像. 这些制备的碳点呈球状,通过对此TEM图像测量后,发现直径为3.4 nm到5 nm. 图2b中显示CQDs的高分辨率HR-TEM图像,经过测量,晶格间距约为0.205 nm,对应的是石墨碳的(102)晶面[23]. 图2c为CQDs/TiO2纳米复合材料的TEM图像. 当负载在TiO2表面时,CQDs形态为如图2d所示,绿色箭头指向CQDs. 值得注意的是,添加CQD对TiO2的比表面积有影响,但对其孔径几乎没有影响(表1),这意味着CQDs位于TiO2的表面,而不是其孔中,这与图2d观察到的形貌相同. 在图2e中,晶面间距为0.345 nm对应于TiO2锐钛矿的(101)晶面[24],而为0.25 nm晶面间距对应着石墨烯的100晶面[25],表明CQDs/TiO2成功复合.
通过X射线光电子能谱(XPS)研究了合成材料中各元素的表面化学成分和价态. 图3a显示,复合材料含有碳、氧、钛和氮元素. C1s的XPS光谱(图3b)主要包含4个特征峰,位于288.2、286.05、284.6 eV.
分别归属于C=O、C—O和C—C&C=C,这证明了复合材料CQDs/TiO2中碳量子点的存在[25]. 在O1s的XPS光谱(图3c)中,特征峰529.7、531.4、532.3 eV分别归因于Ti-O、C—O和O—H键,揭示了CQD和TiO2纳米颗粒通过形成Ti—O—C键结合在一起[25]. 此外,在Ti2p的高分辨XPS图像(图3d)中Ti2p3/2和Ti2p1/2的特征峰位于458.4 eV和464.2 eV,与纯TiO2相比有轻微位移,这表明TiO2和CQDs之间强烈的相互作用.
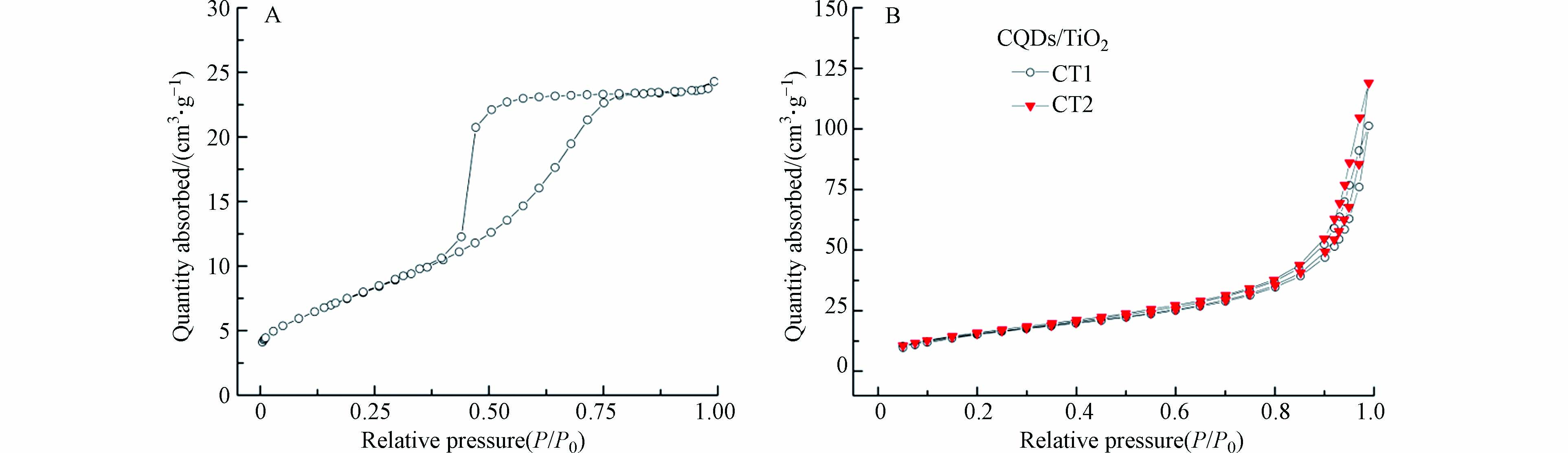
BET. 氮吸附分析用于研究材料的结构特性,图4为材料的N2吸附-脱附等温线图. 根据IUPAC分类,TiO2和CQDs/TiO2均为IV型吸附等温线,TiO2为H2型回滞环(图4A),而CQDs/TiO2为H3型回滞环(图4B). 表1中,CQDs的负载略微减少了复合材料的孔体积,但大幅度地增加了材料的比表面积,这与其表面的特殊官能团有关,从而提供了更多的表面活性中心,有利于污染物的降解,使得CQDs/TiO2表现出优异的降解性能.
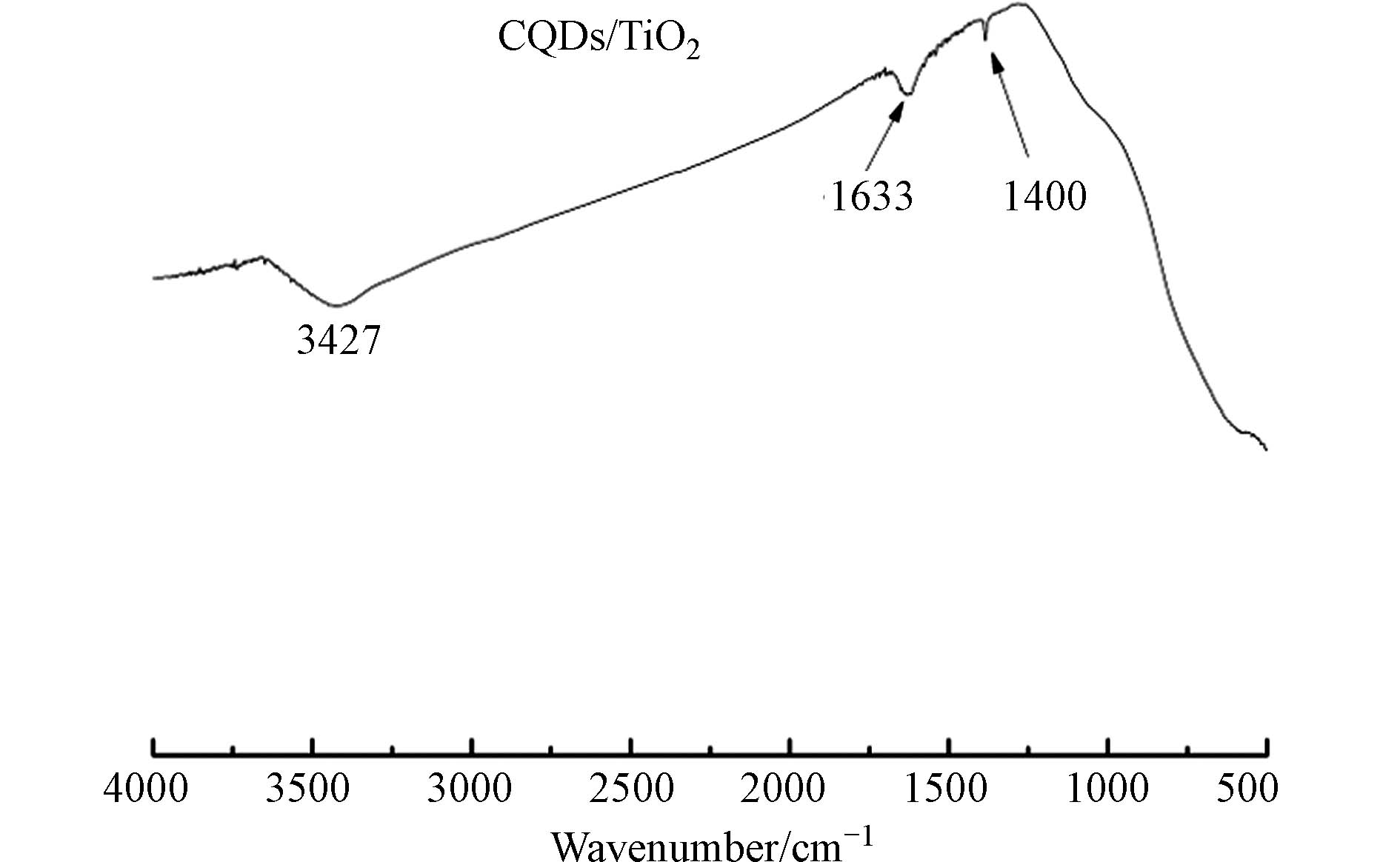
FTIR 分析. 利用CQDs/TiO2 (CT2)的FTIR光谱(图5)研究了复合材料化学键的组成和官能团. 3427、1633、1400 cm−1处有明显的特征峰. 其中,3427 cm−1对应—OH的伸缩振动吸收峰,是由于对水吸附造成的现象;1633 cm−1是C=O的振动峰,1400 cm−1是C=C键的对称拉伸振动峰,属于碳量子点的拉伸振动峰[26],这表明CQDs成功负载在TiO2.
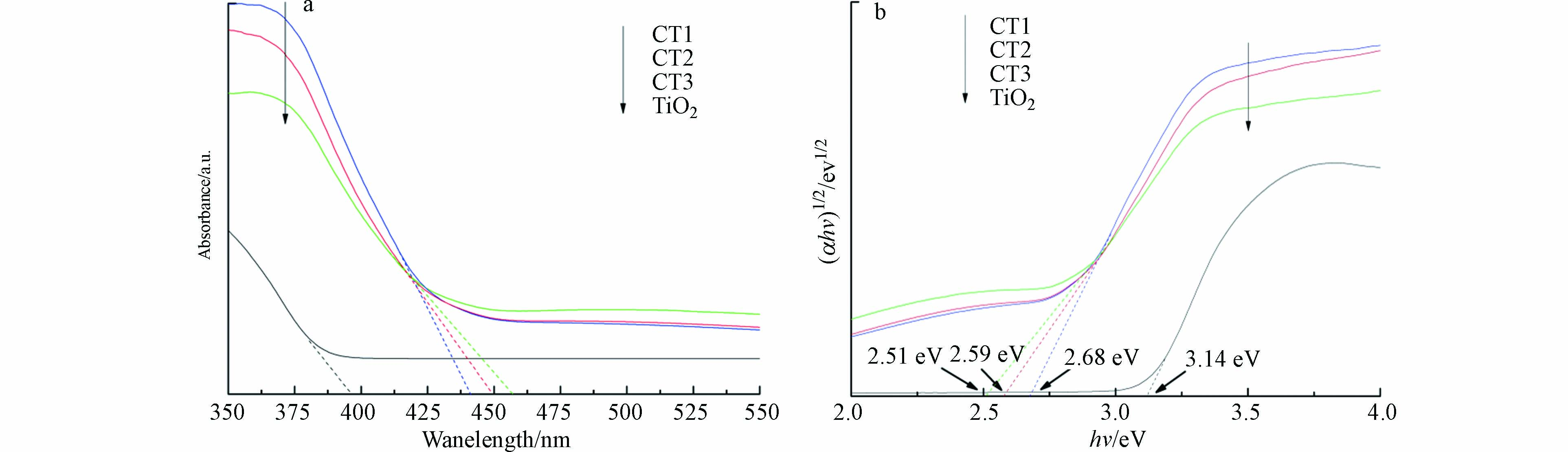
UV-vis DRS漫反射. 为了探究CQDs/TiO2的光学性质,通过UV-vis DRS对复合材料进行表征(图6). 其中,图6a中吸收带关系为TiO2(395 nm)<CT1(441 nm)<CT2(450 nm)<CT3(457 nm). 很明显CQDs的负载显著地延长了光吸收,复合材料的吸收带边缘出现了明显的红移现象[27],说明CQDs/TiO2更容易实现电子跃迁,拓宽了光的吸收范围,增强了材料在可见光下的催化效果;图6b中通过Tauc公式,按照间接带隙半导体直接计算,绘制(αhv)1/2-hv曲线图,估算的带隙宽度关系为TiO2(3.14 eV)>CT1(2.68 eV)>CT2(2.59 eV)>CT3(2.51 eV). 结果表明,掺杂降低了带隙宽度,对比单一材料,复合材料对可见光的响应能力更强. 实验发现当碳量子点掺杂量增高时,吸收边带增大,CQDs/TiO2的带隙能变窄[28]. 但实际的光催化能力并没有增加,这是因为过多的CQDs沉积在TiO2上,使复合材料的比表面积减小,阻碍光催化反应的进行而造成的.
-
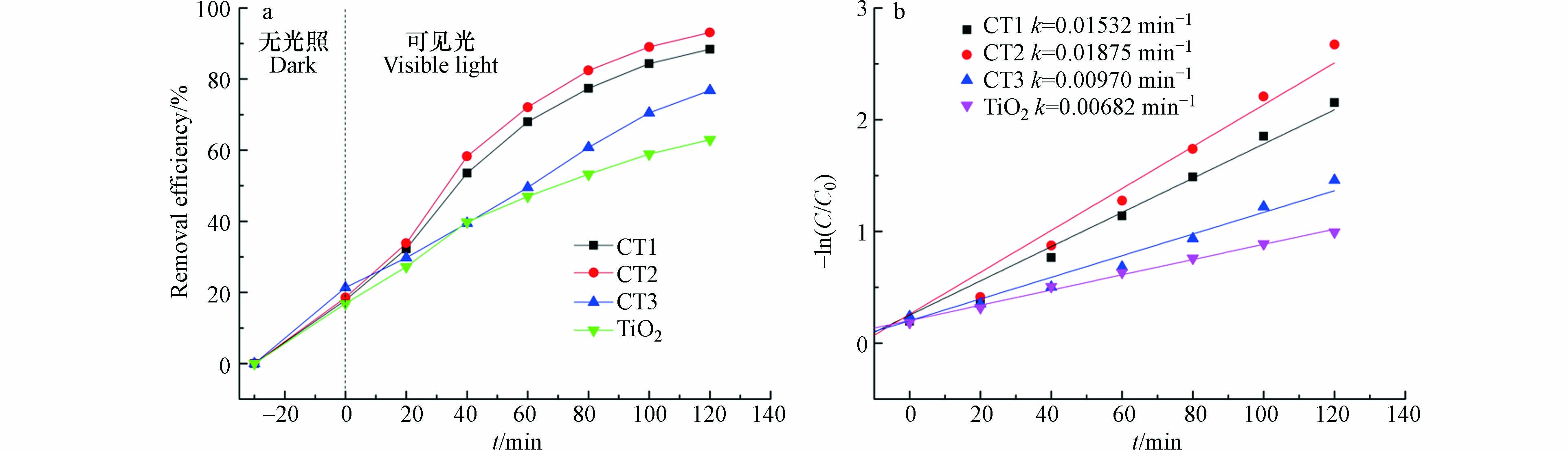
掺杂量的影响. 如图7a所示,显示了在光照条件下,四环素的降解率随时间的变化曲线(pH=5.6,四环素浓度10 mg·L−1,光照强度为300 W). 将1 mg·L−1的催化剂投入溶液中,光照120 min后,纳米复合材料的降解率均高于TiO2,且CT2的降解率最高,达到了93.1%,而TiO2仅为62.9%. CQDs/TiO2的降解效果优于纯TiO2,体现了CQDs/TiO2复合材料优异的光催化性能. 结果表明,添加一定量的CQDs(CT2)可以提高CQDs/TiO2的光催化性能. 当掺杂量过多时(CT3),复合材料的降解率反而下降. 是因为CQDs相对TiO2粒径较小,当大量覆盖在材料表面时,会减小二氧化钛的有效受光面积,电子和空穴的复合速率加快,导致光催化反应降低. 由-ln(C/C0)与降解时间t之间的线性关系可以推断,四环素的光降解动力学拟合曲线遵循准一级动力学模型. 图7b是根据反应时间绘制的反应速率图,为了获得速率常数,进行了线性拟合. 经计算,TiO2光催化剂的恒定速率为0.00682 min−1,而CT2为0.01875 min−1,是TiO2的2. 75倍,效果极佳.
四环素初始浓度的影响. 从图8a可以直观看出,随着四环素浓度的增加,其降解效率逐渐降低(pH=5.6,催化剂投加量1 mg·L−1,光照强度为300 W). 当初始浓度为5、10、15、20、25 mg·L−1时,降解率分别为99.5%、93.1%、88.6%、82.3%、75.5%. 图8b显示了各个浓度的反应速率,反应速率也随着浓度的增加而增加,浓度越低反应速率越快,其中5 mg·L−1的速率远大于其他高浓度. 这是因为当初始浓度较低时,四环素分子与其降解的中间产物(如脱水四环素、差向四环素)之间,对光催化活性物质(如·O2-、·OH)的争夺较弱,从而让更多的活性物质与四环素反应,使去除效率增高. 当较高浓度时,四环素会和其中间产物产生反应竞争[29],导致没有足够多的活性物质与四环素反应,反应速率降低.
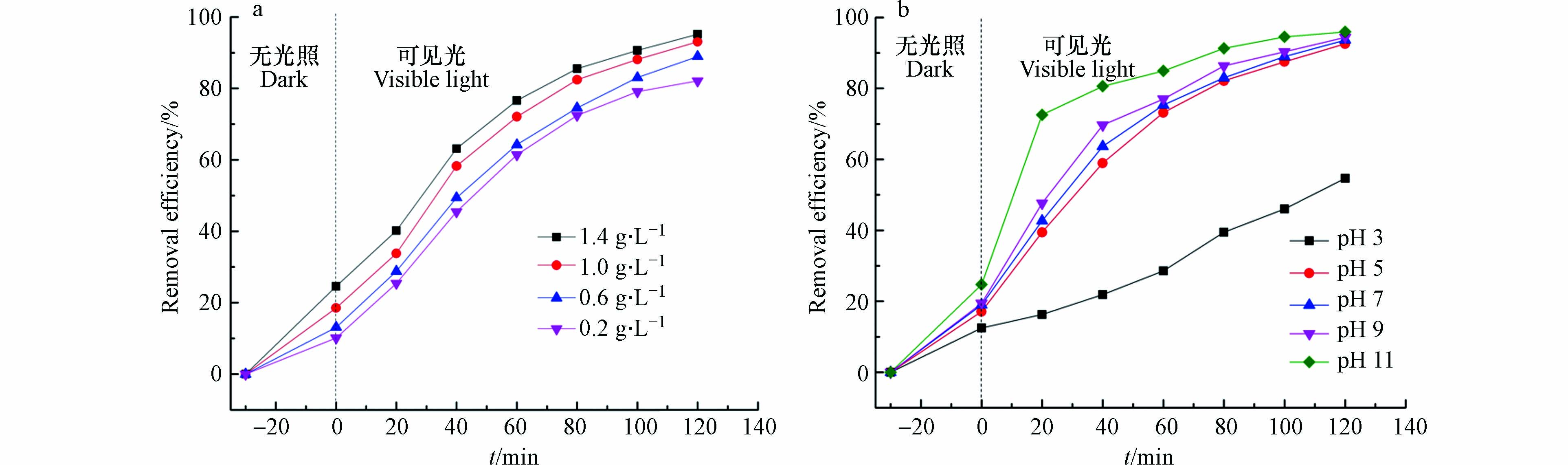
催化剂投加量的影响. 在25 ℃,pH为5.6,光照强度为300 W的条件下,分别以不同的CQDs/TiO2投加量(0.2—1.4 g·L−1)处理10 mg·L−1的四环素溶液,结果如图9a所示. 四环素去除率随着催化剂投加量的增加而增加,当投加量从1 g·L−1增加到1.4 g·L−1时,降解率仅从93.1%轻微增加到95.2%,这是因为高浓度的催化剂彼此之间发生团聚,表面积减小,反应速率减慢;催化剂量增多,也会造成它们相互叠加,到达复合材料表面的光照强度减弱,使去除率没有达到预期水平.
溶液初始pH的影响. pH是影响光催化反应的重要因素. 以CT2为例研究了pH对CQDs/TiO2降解四环素的影响(四环素浓度为10 mg·L−1,催化剂投加量为1 mg·L−1,光照强度为300 W). 在图9b中显示了溶液pH对四环素降解率的影响,当pH从3升高到11时,降解率从54.6%增加到95.9%. 可以看出,在碱性条件有利于四环素的降解. 这是由于pH值较大时,溶液中大量的OH-转化为·OH[30],而·OH恰好是与四环素反应的最主要活性物质之一(后面通过实验证明),所以四环素的降解效率有了很大提高. 在酸性条件中,四环素带正电荷,与CQDs/TiO2的正电荷相互排斥,两者之间巨大的静电斥力阻碍了污染物的吸附. 而且反应生成的·O2-容易与溶液中丰富的H+结合,消耗了大量反应活性物质,从而影响反应速率[30]. 因此当pH值较低时,CQDs/TiO2对四环素的降解效率低.
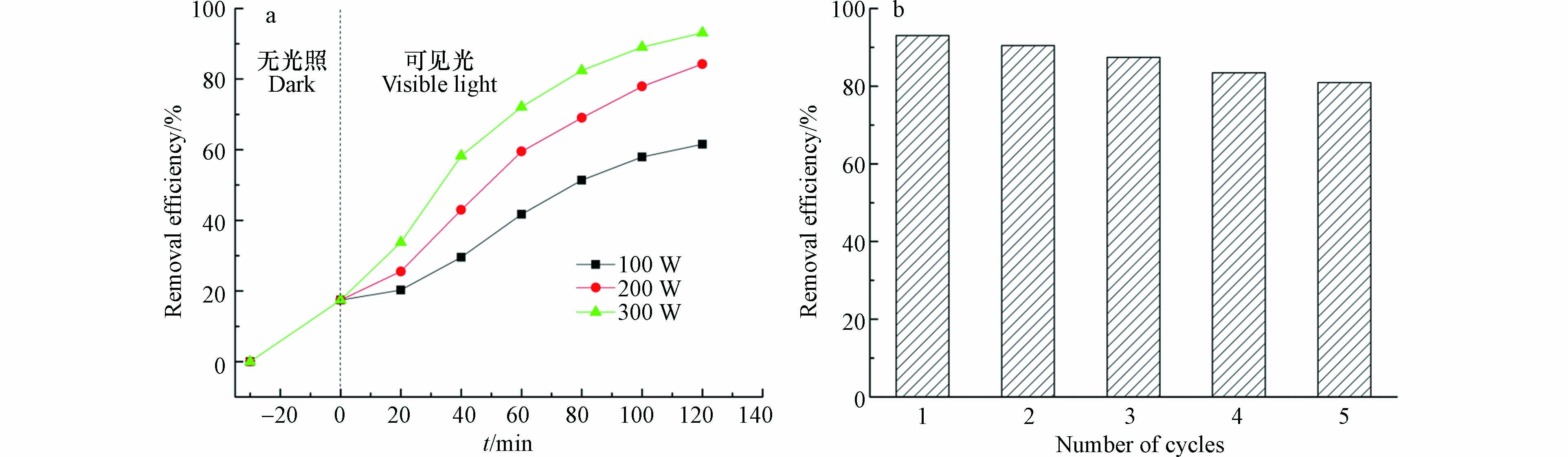
光照强度的影响及稳定性分析. 利用可调节功率电源对氙灯进行功率调节,分别为100、200、300 W. 图10a描绘了不同输入功率下降解率的变化趋势(pH=5.6,四环素浓度为10 mg·L−1,催化剂投加量为1 mg·L−1). 如图所示,当氙灯的功率为从100 W增加到300 W时,降解率从61.5%增加到了93.1%. 降解效率随着氙灯的输入功率的增加而提高,这归因于高的输入功率会产生离子风,导致水中与污染物反应的活性物质的数量增加[31]. ARA等通过构建数学模型证明了·OH、·O2-的产率和光照强度有关[32],光照强度越高这些活性物质的产率就越高. 图10b中,CQDs/TiO2在5个周期后降解率仍能达到80%以上,损失的少量活性可能是Ti—O—C键的断裂造成的[33]. 显然,CQDs/TiO2不仅具有优异的性能,还是一种环保,可循环利用的优质光催化剂.
-
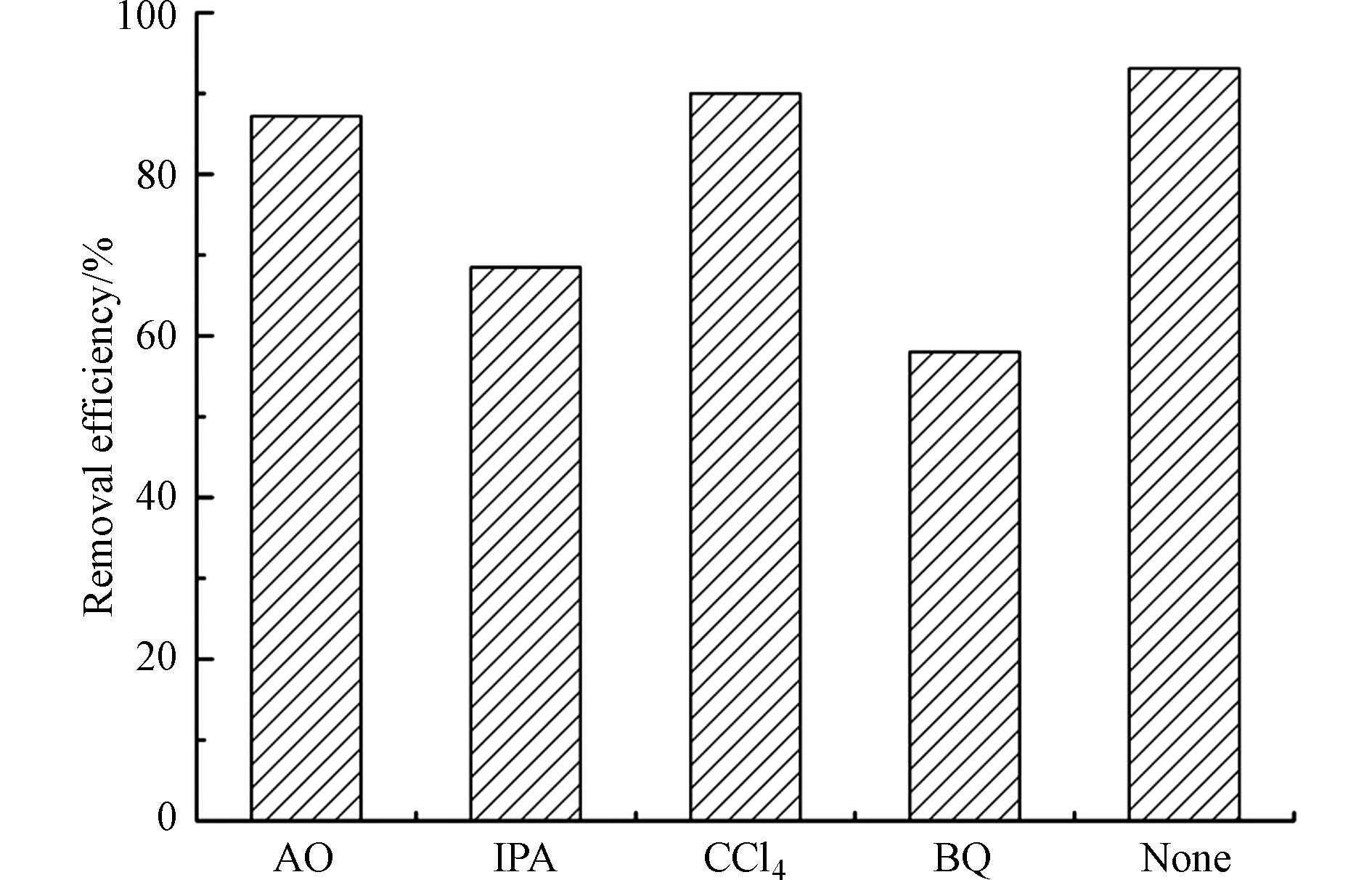
为了检测CQDs/TiO2在四环素光降解过程中的主要活性物质,进行了淬灭实验(图11). 在分别添加对苯醌、异丙醇、四氯化碳、草酸铵的溶液中,四环素的光催化降解性能从93.1%分别降低到58.0%、68.5%、90.0%和87.2%. 很明显对苯醌和异丙醇对降解过程影响最大,这就说明·OH、 ·O2-是四环素降解过程中最重要的两个活性物种. 主要涉及反应的公式如下(1—7):
其中,(4)、(5)反应产生的HO2·、H2O2活性较弱,对反应的影响可以忽略不记.
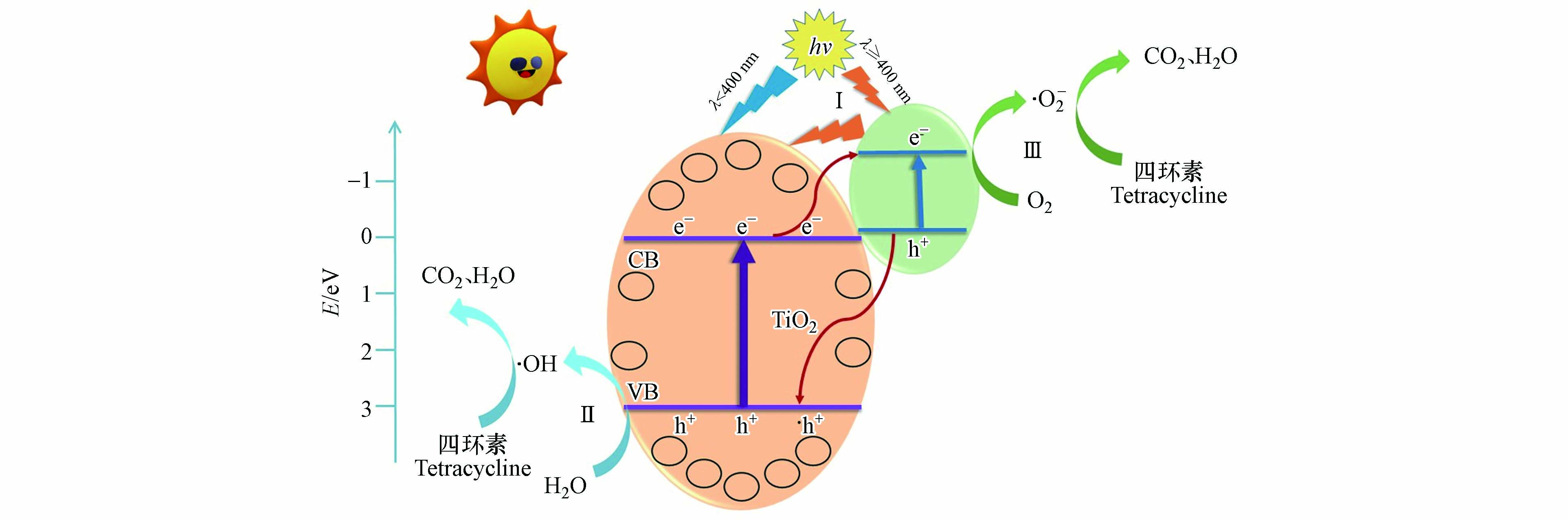
根据以上结果,分析了CQDs/TiO2降解四环素过程中的反应机制(图12). 光线照射到催化剂时,因CQDs的上转换光致发光特性[34],进一步激发了TiO2(过程Ⅰ),产生光生电子和空穴. 此外,CQDs还可以作为电子储存器. 在共轭π键的作用下,它可以捕获从TiO2的导带中迁移的电子. TiO2导带中的电子会转移到CQDs上,与氧分子反应,产生·O2-(过程Ⅲ). 同时,CQDs价带上的空穴会迁移到TiO2的表面,然后与H2O反应,生成·OH(过程Ⅱ). 这些高活性的自由基拥有很强的氧化能力,可以与吸附在TiO2表面的四环素分子发生反应,最终生成CO2和H2O.
-
(1)运用了一种简便新颖的水热超声法,用混合相的TiO2为原料,制备了全新CQDs/TiO2. CQDs负载在TiO2纳米颗粒表面,不仅增大材料的比表面积,增强了可见光的利用率,而且有助于电子和空穴的分离. 在模拟光照120 min后,CQDs/TiO2(CT2)对四环素的降解速率是TiO2的2.75倍.
(2)探究了CQDs掺杂量、溶液初试浓度、催化剂投加量、溶液pH、光照强度对CQDs/TiO2复合材料光催化降解四环素的影响. 其中,过大的掺杂量与过低的pH均不利于光催化的进行,这可为后续处理抗生素废水的研究提供帮助.
(3)该催化剂具有良好的重复使用性和稳定性,5次重复性实验后活性只轻微下降. 通过淬灭实验,得到·OH、·O2-为CQDs/TiO2在四环素光降解过程中的两个主要活性物质. 分析了CQDs/TiO2在可见光下光降解四环素的反应机制.
CQDs/TiO2复合材料的制备及光催化降解抗生素
Preparation of CQDs/TiO2 composites and photocatalytic degradation of antibiotic wastewater
-
摘要: 以四异丙醇钛和葡萄糖为原料,制备全新的CQDs/TiO2复合材料并用于降解四环素废水. 使用XRD、XPS、TEM、HR-TEM、BET、FT-IR、UV-vis DRS等方法进行表征,探究了在不同掺杂量、溶液初始浓度、催化剂投加量、pH、光照强度等条件下的降解效果. 实验结果表明,在pH=5. 6、催化剂投加量1 g·L−1、四环素溶液浓度10 mg·L−1,光照120 min后,CQDs/TiO2对四环素的去除率可达93.1%,复合材料大幅度提升了降解效率. 通过淬灭实验,发现降解过程主要起作用的活性物种为·OH、·O2−,并分析了CQDs/TiO2降解四环素的反应机制. 进行5次循环利用实验,降解率仍能达到80%以上,表现出CQDs/TiO2是一种稳定、可循环利用的复合材料.Abstract: Novel CQDs/TiO2 composites were prepared from titanium tetraisopropoxide and glucose and used to degrade tetracycline wastewater. XRD, XPS, TEM, HR-TEM, BET, FT-IR, and UV-vis DRS were used for characterization. The degradation effects were also investigated under different doping amounts, initial concentration of the solution, catalyst dosing, pH, and light intensity. The experimental results showed that the removal rate of tetracycline by CQDs/TiO2 could reach 93.1% at pH=5. 6, catalyst dosage of 1 g·L−1, tetracycline solution concentration of 10 mg·L−1, and 120 min of light exposure, and the composite material substantially improved the degradation efficiency. Through quenching experiments, it was found that the main active species acting in the degradation process were ·OH and ·O2−, and the reaction mechanism of CQDs/TiO2 in degrading tetracycline was analyzed. Five recycling experiments were carried out and the degradation rate still reached over 80%, demonstrating that CQDs/TiO2 is a stable and recyclable composite material.
-
Key words:
- CQDs/TiO2 /
- photocatalysis /
- tetracycline /
- wastewater treatment.
-
地下水是地球水资源的重要组成部分,是地球上一切生物生存及人类生产活动中不合或缺的自然资源,是支撑经济可持续发展的重要战略资源,也是构成并影响生态环境的重要因素[1-4]. 根据中国水利统计年鉴数据,从2013年至2020年我国地下水资源占总供水量的比例逐年减少,北方城市地下水供用量较南方高. 在2020年全国地下水资源占总供水量的15.35%,而内蒙古占41.98%. 随着经济的不断发展和工业化、现代化程度的不断提高,我国地下水开采量日益上升,同时由于人类不当的活动导致环境中的污染物入渗,使地下水遭受污染[5-6]. 由于地下水污染具有隐蔽性、滞后性及较弱的自净能力,地下水一旦发生污染就很难恢复,同时对居民饮水安全和社会经济可持续发展构成了严重威胁[7-8]. 因此,进行地下水环境风险评估,对于防治地下水污染、科学规划和可持续利用具有一定的参考价值.
目前,对盐湖盆地蒸发特征、植被生长特征、土壤污染特征有较多的研究,杨宇娜等[9]揭示了吉兰泰及周边地区蒸散发的时空变化规律;迟旭等[10]探明吉兰泰盐湖绿洲防护林带同一建植年限柽柳灌丛形态大小与阻沙能力之间存在一定关系;张阿龙等[11]运用不同的评价方法对吉兰泰盐湖盆地土壤重金属中铬、汞、砷污染展开评价工作. 目前,对盐湖盆地地下水的风险评价较少,高瑞忠等[12]采用单因子指数法、内梅罗指数法和USEPA健康风险评价模型对吉兰泰盐湖盆地地下水中Cr、As、Hg重金属污染开展了一些健康风险评价工作. 评价方法常以单项指标评价法[13]、综合评价法[14-16]、模糊综合评价法[17-21]和集对分析法等为主[22]. 然而这些方法都有各自的缺点,例如单项指标评价法不能给出水体整体的质量状况,综合评价法只突出某单项评价指标对水体质量的影响,模糊数学法、集对分析法存在评价指标权重不唯一等问题[23]. 在实际的地下水质量评价工作中,需要根据研究区实际情况,选择恰当的评价方法并加以改进,方可得到切合实际的评价结果.
本文针对地处西北旱区荒漠边缘的盐湖盆地,结合当地生态环境脆弱、降水量少、水质恶化、污染物种类与来源复杂等诸多问题. 运用李小牛等[24]提出的地下水风险评价概念模型,以盐湖盆地土壤作为风险源,以地下水系统作为风险受体展开风险评价,将地下水脆弱性[25-27]、地下水毒性污染物容量[28]及土壤毒性污染物潜在生态危害[29-32]有机结合起来,并借助ArcGIS技术进行污染分区表征[33-35],分析盐湖盆地地下水污染状况,以期为吉兰泰盐湖盆地地下水资源合理开发利用、地下水污染防控以及保障农牧民生活饮水安全、社会经济和自然环境相协调发展提供科学依据.
1. 材料和方法(Materials and methods)
1.1 研究区概况
吉兰泰盐湖盆地(38°35'—40°35'N,104°50'—106°40'E)位于内蒙古自治区阿拉善左旗吉兰泰镇,是地处乌兰布和沙漠西南边缘的贺兰山与巴彦乌拉山之间的断陷盆地. 盐湖盆地面积为20025 km2左右,高程1013—3159 m,地形向盐湖中心呈明显的环带状分布. 巴音乌拉山、贺兰山分别位于盐湖盆地的西北、东南方向,盐湖盆地的东南部和东北部分别为腾格里沙漠和乌兰布和沙漠. 盐湖盆地属于典型的大陆性干旱气候,多年平均气温8.6 ℃,常年蒸发强烈、降水稀少,多年平均蒸发量达2983.30 mm,平均降水量仅为108.80 mm,蒸发量为降水量的30倍左右. 由于降水主要集中在6—9 月份,且主要以暴雨形式出现,其时空分布又比较集中,洪水的特点表现为历时短、洪量集中、陡涨陡落,在降雨时期山区沟产流,滩地沟不产流等空间分布不均匀现象. 该研究区域处于山区地下水溶滤带,水质良好,矿化度一般小于0.50 g·L−1,水化学类型为单一的重碳酸钙水或重碳酸钙钠水. 根据多年测量数据显示地下水水位动态变化范围为4—7 m,含水介质主要为粗砂、细砂、砂砾石、卵砾石及一些砂质粘土. 土壤以粘土和不同类型亚粘土为主. 包气带主要以粘土、沙土、砾石为主. 吉兰泰盐湖(120 km2)属于中型盐湖,是我国西北荒漠区重要的盐业生产基地,盐的开采量居全国之首,同时也拥有国内规模最大的钠生产企业. 由于人类活动的干扰,导致盐湖盆地地区人地关系具有极端脆弱性和风险性. 盐湖盆地有着极端恶劣的气候条件,导致水资源呈现严重短缺态势,浅层地下水作为该区域的主要水资源,对维护该区域人地关系稳定、生物多样性、生态安全及当地农牧民生活饮用水安全具有重要的意义.
1.2 采样与测定
由于土壤与浅层地下水之间重金属会发生迁移,在地表高温蒸发条件下,地下水通过毛细作用不断向地表运移,重金属向土壤富积,当地表发生积水后,土壤与水发生离子交换吸附和溶滤等作用,故土壤采样点与地下水采样点布设尽量吻合. 2020年6月—8月布点采集样品,根据《土壤环境监测技术规范》(HJ/T 166—2004)及结合盆地的地貌特征和土壤类型,确定以吉兰泰盐湖为中心向四周呈放射状均匀布设土壤采样点,采集土壤表层(0—10 cm)样品,研究区共布设56个采样点(见图1). 在采样过程中,每个采样点取土样1 kg左右,装入聚乙烯塑料袋中,防止交叉污染. 水样点的布设中充分考虑盐湖盆地地形特点和地下水汇流方向,在吉兰泰盐湖周边分散分布,共选取了127口取样井(参见图1). 取样井选取浅层饮用水井和灌溉井. 将采集的水样装于洁净的规格为1 L的聚乙烯塑料取样瓶中,加入3 mL 65% HNO3,将水样pH调至2以下,封口于4 ℃的便携式冷藏箱保存,送至内蒙古自治区水资源保护与利用重点实验室测定.
测试前土壤样品采用王水-高氯酸(HNO3-HCI-HCIO4)开放式消煮法,空白和标准样品同时消解,以确保消解及分析测定的准确性. 水样使用0.45 μm的微孔过滤膜对水样进行过滤预处理. 样品中重金属测试参考《地下水污染地质调查评价规范》(DD 2008—01),使用电感耦合等离子体质谱仪(ICP-MS)分析测定,F−、NO3−、NO2−采用离子色谱仪进行测定. 为保证分析的准确性,标准曲线的绘制采用国家标准中心提供的标准物质,分析过程中试剂均为优级纯,样品测定全程做空白样,每个样品设3 组平行实验,取平均值作为样品测定的最终值. 保证待测物质的相对标注偏差(RSD)均低于15%,符合美国国家环境保护局(USEPA)的要求(RSD<30%).
1.3 评价方法
本文以盐湖盆地土壤作为风险源,以地下水系统作为风险受体,首先结合当地自然条件采用地下水脆弱性评价方法来分析地下水环境变化,从而判断地下水水质易受到污染的可能性和地下水水量衰减的可能性. 通过采用地下水特征污染物容量指数分析地下水污染物容量和允许污染的程度,进而应用潜在生态危害指数评价研究区域土壤重金属潜在生态危害程度,最后将三者结合对地下水污染风险展开评价.
1.3.1 地下水脆弱性评价
目前国内外使用最广泛的地下水脆弱性评价方法是美国环境保护署于1987年提出的DRASTIC方法[36-39]. 地下水脆弱性DRASTIC指标体系,包含6个指标,其中,D-地下水位埋深,权重为5;R-降雨补给量,权重为4;A-含水层介质,权重为3;S-土壤类型,权重为2;T-地形坡度,权重为1;I-包气带介质,权重为5;C-地下水开采系数,权重为3.
DRASTIC=∑ni=1ωi×Ri 式中,
DRASTIC ωi Ri 表 1 DRASTIC指标体系评分标准Table 1. DRASTIC index system scoring criteria埋深/mBurial depth D 净补给量/mm Net replenishment R 含水层介质Aquifer media(A) 土壤Soli(S) 包气带类型Type of aeration zone(I) 地形坡度/%Topographic gradient(T) 渗透系数/(m·d−1)Permeability coefficient(C) 评分Score >30.5 ≤51 粘土 卵砾石 粘土为主(50%) >18 ≤4.1 1 26.7—30.5 51—72 亚粘土 砂砾石 亚粘土为主 17—18 4.1—12.2 2 22.9—26.7 72—92 亚砂土 泥炭 亚砂土为主 15—17 12.2—20.3 3 15.2—22.9 92—117 粉砂 胀缩或凝聚性粘土 粉砂为主 13—15 20.3—28.5 4 12.1—15.2 117—148 粉细砂 砾质亚粘土 粉细砂为主 11—13 28.5—34.6 5 9.1—12.1 148—178 细砂 亚粘土 细砂为主 9—11 34.6—40.7 6 6.8—9.1 178—216 中砂 粉砾质亚粘土 中砂为主 7—9 40.7—61.5 7 4.6—6.8 216—235 粗砂 粘土质亚粘土 粗砂为主 4—7 61.5—71.6 8 1.5—4.6 235—255 砂砾石 垃圾 砂砾石为主 2—4 71.6—81.5 9 <1.5 >255 卵砾石 非胀缩和非凝聚性粘土 卵砾石为主 <2 >81.5 10 1.3.2 地下水污染物容量指数
地下水中含有大量的可溶性物质,但同时也含有一定量对人体危害较大的污染物质,各类污染物质的容量有不同程度的差别[29]. 为了有效描述地下水中各组分所处的容量状态,提出了综合容量指数
TCD TCDi TCDi TCDi=(Cis−Ci)Cis (1) ¯TCDi=1nn∑i=1TCDi (2) TCD=√(¯TCDi2+TCD2g+TCD2m)3 (3) 式中,
TCDi Cis Ci TCD −TCDi TCD TCDm TCDi TCDg TCDi TCD 表 2 容量指数评分标准Table 2. Scoring criteria for capacity indexTCD 等级Rank 水环境状态Water environment status 分值Score 0—0.2 Ⅰ 极易恶化 5 0.2—0.4 Ⅱ 极易污染 4 0.4—0.6 Ⅲ 易污染 3 0.6—0.8 Ⅳ 较易污染 2 >0.8 Ⅴ 不易污染 1 1.3.3 潜在生态危害指数法
瑞典学者Hakanson提出了潜在生态危害指数法,该方法用于评价重金属污染及其生态危害 [40-41]. 将重金属的生态效应、环境效应与毒理学有机结合在一起,用来综合反映重金属对生态环境的潜在危害程度. 公式如式(4):
Ei=Tir×(Ci/C0i) (4) 式中,Ci,C0i分别为重金属i的实测值和参比值;
Tir 综合潜在生态危害指数,见公式(5):
RI=n∑i=1Ei (5) 式中:RI为研究区域多种重金属的综合潜在生态危害指数;Ei为某种待测重金属i的潜在生态危害指数,生态危害程度划分见表3.
表 3 潜在生态危害系数与综合潜在生态危害指数等级划分Table 3. Classification of potential ecological hazard index and comprehensive potential ecological hazard index等级Rank 潜在生态危害指数Potential ecological hazard index 综合潜在生态危害指数Comprehensive potential ecological hazard index 潜在生态危害程度Potential ecological hazard level 1 Ei≤40 RI ≤150 轻微生态危害 2 40<Ei≤80 150<RI≤300 中等生态危害 3 80<Ei≤160 300<RI≤600 强生态危害 4 160<Ei≤320 RI>600 很强生态危害 5 Ei≥320 — 极强生态危害 1.3.4 地下水污染风险评价指数
将地下水脆弱性指数DRASTIC、地下水污染物容量指数TCD和综合潜在生态危害指数RI相结合,通过整合处理得出研究区地下水污染风险指数R[24],然后采用自然分级法对地下水污染风险指数进行统计分析. 将地下水污染风险划分为低风险、较低风险、中等风险、较高风险和高风险5个等级,并依此绘制和划定研究区地下水污染风险分区图,如公式(6).
R=DRASTIC×TCD×RI (6) 2. 结果与讨论(Results and discussion)
2.1 盐湖盆地浅层地下水脆弱性评价及分区
根据采样过程中的实际测试,结合对研究区地质环境综合分析,依照地下水脆弱性评价表赋予地下水脆弱性各指标相应的值. 运用DRASTIC公式求得盐湖盆地地下水脆弱性指数范围为4.80—5.30. 指数越大,防污性能越低,地下水越容易受到污染;指数越小,防污性能越高. 根据地下水脆弱性和受污染程度分类标准,可判定盐湖盆地整体为中等脆弱性,属于中等受污染程度. 运用ArcGIS软件进行相应数据处理,绘制出研究区地下水脆弱性分区图(见图2a).
研究区降水量时空分布极不均匀,夏季的降水量占全年的60%以上,多呈暴雨形式,冬季各月的降水量仅约占全年的1%,冬季呈现干旱少雨的特征. 由于贺兰山和巴乌拉山高原的地形作用,降水从东到西逐渐减少,贺兰山地区的降水超过400 mm,而西边的荒漠地区低于150 mm. 蒸发量从东边到西边呈上升趋势,是年降水量的4—12倍. 盐湖盆地的深度蒸发使得地下水出现盐渍化现象,地下水ρ(TDS)范围达到156—12140 mg·L−1之间,Cl−/(Cl−+HCO3−)质量浓度比值全部>0.90,Na+/(Na++Ca2+)质量浓度比值范围在0.34—0.98之间,仅4个水样点Na+/(Na++Ca2+)比值<0.50,绝大多数水样点集中在右上角的虚线框内(见图3). 说明蒸发浓缩作用是决定吉兰泰盐湖盆地地下水主要离子含量的重要机制,而岩石风化、降水控制作用对研究区内地下水主要离子的含量影响十分微弱.
采用自然分级法对地下水脆弱性指数进行统计分析,将中等脆弱性细化为5个类型,由图2a可见,在中等脆弱性的区域内吉兰泰盐湖西南部和吉兰泰镇东北部的地下水脆弱性最高,该区域土壤以沙土和细砂为主,含水层介质粒径大于细砂,地表污染物较易下渗到含水层对地下水造成影响. 吉兰泰盐湖附近地下水脆弱性相对较高,该地区位于盐湖附近地下水位较高,又由于该地区蒸发量大的特点,浅层地下水通过蒸发浓缩后污染物易得到富集,致使该地区地下水脆弱性相对较高. 贺兰山、宗别立镇、古拉本敖包镇的脆弱性处于相对较低的水平具有较高的防污能力,是由于该地区位于山区,地形坡度较大,含水层较深,地表污染物不易下渗到含水层,对地下水造成污染.
2.2 盐湖盆地浅层地下水污染物容量指数
对研究区采集的127个浅层地下水样品中部分重金属元素和毒性离子检测结果进行统计和汇总,见表4.
表 4 盐湖盆地浅层地下水特征毒性元素含量统计分析Table 4. Statistical analysis of characteristic toxic elements in shallow groundwater in the Salt Lake Basin元素Element 含量范围/(mg·L−1)Content range 平均值/(mg·L−1)Average value 标准差Standard deviation 变异系数/%Coefficient of variation 地下水质量标准(GBT14848-2017)/(mg·L−1)Groundwater Quality Standards 超标率/%Exceeding rate Cr 0.0012—0.27 0.038 0.048 125.40 0.050 22.05 Hg 0.0000020—0.0010 0.00020 0.00020 98.70 0.0010 0 As 0.00011—0.066 0.0047 0.0086 183.50 0.010 11.02 F- 0—46.18 2.77 4.95 178.70 1.00 62.20 NO2- 0—11.06 0.64 1.59 248.70 1.00 14.17 NO3- 0—48.47 3.12 8.76 280.70 20.00 4.72 由表4可见,研究区被测浅层地下水样品中Cr、Hg、As、F−、NO2−、NO3−共6种元素的平均含量分别为0.038、0.00020、0.0047、2.77、0.64、3.12 mg·L−1. 与《地下水质量标准》(GBT 14848-2017) 中Ⅲ类水水质指标相比较,被测的127个地下水采样点,除重金属Hg的含量在标准范围内外,其他元素均有个别点位超出标准限值. 其中,样品中F−超标率最高,超标率为62.20%. 变异系数可反映采样总体中各样点之间的平均差异程度,被测采样点浅层地下水中Cr、Hg、As、F−、NO2−、NO3−变异程度分别为125.40%、98.70%、183.50%、178.70%、248.70%、280.70%,Cr、As、F−、NO2−、NO3−为强变异性,Hg为中等变异性,表明这6种元素含量值波动幅度大,连续性变化较差,受外界因素干扰较为明显. 通过采用公式(1—3)计算127个采样点浅层地下水特征污染物单组分容量评价指数和多组分容量评价指数. 以表4多组分容量评价指数划分标准为依据,运用ArcGIS软件克里格插值法计算和划定研究区的容量评价等级范围,见图2b. 由图 2b 可见,研究区浅层地下水特征污染物容量评价指标值均大于 0.60,即对应水环境风险等级为良好以上.锡林高勒镇西北部,吉兰泰镇东北部地下水易污染,巴音乌拉山、乌兰布和沙漠、贺 兰山、吉兰泰湖为山脉和湖泊,受人为因素干扰较小,地下水呈现不易被污染状态.
2.3 土壤重金属潜在生态危害评价
研究区域干旱少雨,土壤类型属于其他,表层土壤样品pH大于7.5,重金属含量的描述性统计分析见表5. 由表5可知,土壤中重金属Cr、Hg、As的平均含量分别为26.32、0.17、11.77 mg·kg−1,与内蒙古当地土壤背景值相比较[32],Cr的平均含量在背景值范围内,Hg、As的平均含量分别超出背景值的4.25、1.57倍. 在56个采样点中,重金属Cr、Hg、As的超标率分别为5.36%、73.21%、73.21%. Cr、Hg、As含量的最大值高于背景值,而最小值低于背景值,表明研究区域土壤存在局部超标点或超标区域,与国家土壤标准值相比较,3种重金属元素含量均未超过《土壤环境质量 农用地土壤污染风险管控标准》(GB 15618-2018)风险筛选值的限值范围. Cr、Hg、As元素的变异系数分别为37.46%、94.12%、50.81%,3种重金属变异系数均在中等变异性范围内. 因此,可推断该区域重金属的累积不排除是受人为因素干扰所致. 注:(CV<10%为弱变异性,10%≤CV≤100%为中等变异性,CV>100%为强变异性).
表 5 盐湖盆地土壤特征毒性元素含量统计分析(mg·kg−1)Table 5. Statistical analysis of soil characteristic toxic elements in the Salt Lake Basin毒性元素Toxic element 最小值Min 最大值Max 均值Average 标准差Standard deviation 变异系数/%Coefficient of variation 内蒙古自治区背景值Inner Mongolia Autonomous region background 国家标准(GB15618-2018)National standard 背景值Background 超标率Exceeding rate 标准值Standard 超标率Exceeding rate Cr 2.90 55.21 26.32 9.86 37.46 41.40 5.36% 250.00 0 Hg 0.00 0.60 0.17 0.16 94.12 0.04 73.21% 3.40 0 As 0.00 21.74 11.77 5.98 50.81 7.50 73.21% 25.00 0 以内蒙古土壤环境背景值为评价标准,3种重金属潜在生态危害系数
Ei 表 6 潜在生态危害指数评价结果Table 6. Evaluation results of potential ecological hazard index元素Element Ei ˉEi 样品比例 Sample ratio 轻微危害Minor hazard 中等危害Moderate hazard 强危害Strong hazard 很强危害Very hazard 极强危害Extremely hazard Cr 0.14—2.67 1.27 100% 0 0 0 0 Hg 1.59—601.48 171.36 26.79% 14.29% 19.64% 14.29% 25% As 0—28.98 15.69 100% 0 0 0 0 RI ¯RI 样品比例 Sample ratio 轻微危害Minor hazard 中等危害Moderate hazard 强危害Strong hazard 很强危害Very hazard — RI 21.89—609.47 188.32 58.93% 14.29% 25% 1.79% — 由表6可见,Cr、Hg、As的潜在生态危害系数平均值由大到小依次为Hg>As>Cr,土壤中Hg的平均潜在生态危害系数为171.36,呈中等、强、很强、极强危害程度样品数占总数的73.21%,潜在危害性较大,这与Hg毒性系数较大和污染程度严重相关,Cr、As的潜在生态危害系数均小于40,对土壤生态环境的危害属于轻微. Cr、Hg、As平均综合潜在生态危害系数为188.32,属于中等潜在生态危害程度,在盐湖盆地中有41.07%的样品点属于中等、强、很强潜在生态危害. 因此,应当注重土壤重金属污染源的控制以及土壤重金属的污染监测.
运用ArcGIS及克里格插值法绘制单种重金属潜在生态危害指数和综合潜在生态危害指数分布图(见图4),进行研究区潜在生态危害的空间变化特征分析. 由图4可以看出,盐湖盆地Cr的生态危害系数由吉兰泰湖西南部向东北部呈梯度递增,巴音乌拉山周围和敖伦布拉格镇强度相对较高,其最大值为2.67,属于轻微生态危害,这可能与巴音乌拉山岩石风化水土流失有关. 吉兰泰盐湖盆地东南方向的锡林高勒镇和巴彦浩特镇附近Hg的生态危害系数较高,达到中等潜在生态危害,与张阿龙等对吉兰泰盐湖盆地土壤重金属研究结果相一致[11]. As生态风险系数整体处于轻微生态危害,强度较高的区域主要分布在锡林高勒镇、宗别立镇、吉兰泰镇、敖伦布拉格镇. 因此,可初步推断出As的潜在生态危害可能与当地居民人为活动因素干扰影响较为密切. 综合潜在生态危害程度由东北向西南部呈扇形递增,吉兰泰盐湖东南方向指数较大,这与Hg的生态危害系数空间分布相似,且与Hg潜在危害指数较大,在综合潜在生态危害中贡献率大有关.
2.4 盐湖盆地浅层地下水污染风险分区
运用ArcGIS空间分析功能,将图2、3、5以概念模型(6)作为运算规则,进行整合处理得到各个区域的地下水污染危险指数R;运用自然分级方法对盐湖盆地地下水环境质量进行统计分析,并将其污染风险划分为低风险、较低风险、中等风险、较高风险和高风险5个级别,并绘制盐湖盆地地下水污染风险分区图,结果见图5.
由图5可以发现,研究区域内吉兰泰盐湖西南部地下水风险等级呈梯度逐渐递增,锡林高勒镇西部处于高风险区域,较高风险区位于贺兰山西部和锡林高勒镇附近,贺兰山区域降水主要在该区域形成地表径流,在地表径流过程中累积了大量物质,由于该地区蒸发量大,径流污染物通过蒸发浓缩后入渗地下导致该区域地下水处于较高风险,其中较高风险及以上的面积占研究区总面积的25.77%,该区域内地下水脆弱性、地下水污染物容量指数、土壤毒性污染物风险指数均相对较高. 贺兰山的西南部、古拉本敖包镇、巴音乌拉山西南部处于中风险地段,面积占比为11.49%. 巴音乌拉山和贺兰山西南部附近地下水属于较低风险,面积占比为33.06%. 低风险区域主要分布在乌兰布和沙漠和吉兰泰镇,面积占比为29.68%,此区域主要处于沙漠地带,受人为干预较弱,同时此区域地下水容量指数和土壤毒性污染物潜在危害性处于相对较低的水平. 盐湖盆地处于西北寒旱区,面临严峻的水资源短缺问题. 因此,需要进一步加强地下水水位、水质、开采量、气候条件等监测监管工作. 在制定和实施地下水治理措施时,应当结合当前面临的地下水资源问题,充分考虑当地地理条件和当地的经济发展,设计直接且明确的可持续发展方案.
3. 结 论(Conclusion)
(1)吉兰泰盐湖盆地下水脆弱性指数范围为4.80—5.30属于中等脆弱性,为中等受污染程度,盐湖西南部和东北部的地下水脆弱性相对较高,贺兰山、宗别立镇、古拉本敖包镇的脆弱性相对较低.
(2)地下水样品中重金属Hg的含量在标准限值范围内,Cr、Hg、As、F−、NO2−、NO3−元素均有超标现象,其中F−超标率最高,达62.20%. 地下水特征污染物容量评价指标值均大于0.60,即对应水环境风险等级为良好以上. 锡林高勒镇西北部,吉兰泰镇东北部地下水易污染.
(3)盐湖盆地土壤中Hg的平均潜在生态危害系数为171.36,达到中等生态危害程度,Hg呈中等以上危害程度样品数占总数的73.21%,潜在危害性较大. 综合潜在生态危害系数为188.32,属于中等潜在生态危害,在盐湖盆地中有41.07%的样品点属于中等、强、很强潜在生态危害. 土壤重金属对环境的影响具有一定的历史承载性和实际的连续性,未来应加强地表土壤重金属纵向迁移对地下水的影响.
(4)应用地下水风险评价概念模型,对研究区域地下水进行污染风险评价,吉兰泰盐湖西南部地下水风险等级呈梯度逐渐递增,锡林高勒镇西部地下水整体处于较高风险及高风险. 其中,中风险区域面积占研究区域的11.49%,较高风险以上的面积占研究区域的25.77%. 建议加强对该区域地下水的监测并采取适当措施进行防治,必要时开展盐湖盆地地下水环境、地质环境、生态环境健康等方面研究,确保地下水可持续开发利用.
-
表 1 不同材料的比表面积、孔径
Table 1. Specific surface area and pore size of different materials
样品 Samples 比表面积/(m2·g−1) Specific surface area 平均孔径/nm Average pore size TiO2 29.66 10.46 CT1 57.66 10.12 CT2 59.28 10.1 CT3 50.06 10.16 -
[1] LIU X H, LU S Y, MENG W, et al. Occurrence, source, and ecological risk of antibiotics in Dongting Lake, China [J]. Environmental Science and Pollution Research International, 2018, 25(11): 11063-11073. doi: 10.1007/s11356-018-1290-1 [2] KURNIAWAN T A, LO W H, CHAN G Y S. Radicals-catalyzed oxidation reactions for degradation of recalcitrant compounds from landfill leachate [J]. Chemical Engineering Journal, 2006, 125(1): 35-57. doi: 10.1016/j.cej.2006.07.006 [3] QIU G L, CHEN H, SRINIVASA RAGHAVAN D S, et al. Removal behaviors of antibiotics in a hybrid microfiltration-forward osmotic membrane bioreactor for real municipal wastewater treatment [J]. Chemical Engineering Journal, 2021, 417: 129146. doi: 10.1016/j.cej.2021.129146 [4] YANG X R, CHEN Z, ZHAO W, et al. Recent advances in photodegradation of antibiotic residues in water [J]. Chemical Engineering Journal, 2021, 405: 126806. doi: 10.1016/j.cej.2020.126806 [5] BAYAN E M, PUSTOVAYA L E, VOLKOVA M G. Recent advances in TiO2-based materials for photocatalytic degradation of antibiotics in aqueous systems [J]. Environmental Technology & Innovation, 2021, 24: 101822. [6] MURDOCH M, WATERHOUSE G I N, NADEEM M A, et al. The effect of gold loading and particle size on photocatalytic hydrogen production from ethanol over Au/TiO2 nanoparticles [J]. Nature Chemistry, 2011, 3(6): 489-492. doi: 10.1038/nchem.1048 [7] LI R G, WENG Y X, ZHOU X, et al. Achieving overall water splitting using titanium dioxide-based photocatalysts of different phases [J]. Energy & Environmental Science, 2015, 8(8): 2377-2382. [8] KAWAHARA T, OZAWA T, IWASAKI M, et al. Photocatalytic activity of rutile-anatase coupled TiO2 particles prepared by a dissolution-reprecipitation method [J]. Journal of Colloid and Interface Science, 2003, 267(2): 377-381. doi: 10.1016/S0021-9797(03)00755-0 [9] WANG W, LIU X L, FANG J J, et al. TiO2@g-C3N4 heterojunction with directional charge migration behavior for photodegradation of tetracycline antibiotics [J]. Materials Letters, 2019, 236: 622-624. doi: 10.1016/j.matlet.2018.11.025 [10] HAJIPOUR P, ESLAMI A, BAHRAMI A, et al. Surface modification of TiO2 nanoparticles with CuO for visible-light antibacterial applications and photocatalytic degradation of antibiotics [J]. Ceramics International, 2021, 47(23): 33875-33885. doi: 10.1016/j.ceramint.2021.08.300 [11] ALI A, SHOEB M, LI Y, et al. Enhanced photocatalytic degradation of antibiotic drug and dye pollutants by graphene-ordered mesoporous silica (SBA 15)/TiO2 nanocomposite under visible-light irradiation [J]. Journal of Molecular Liquids, 2021, 324: 114696. doi: 10.1016/j.molliq.2020.114696 [12] HENG Z W, CHONG W C, PANG Y L, et al. An overview of the recent advances of carbon quantum dots/metal oxides in the application of heterogeneous photocatalysis in photodegradation of pollutants towards visible-light and solar energy exploitation [J]. Journal of Environmental Chemical Engineering, 2021, 9(3): 105199. doi: 10.1016/j.jece.2021.105199 [13] LI T X, LI Z, HUANG T Z, et al. Carbon quantum dot-based sensors for food safety [J]. Sensors and Actuators A:Physical, 2021, 331: 113003. doi: 10.1016/j.sna.2021.113003 [14] YUE J, ZHANG K, YU H, et al. Mechanism insights into tunable photoluminescence of carbon dots by hydroxyl radicals [J]. Journal of Materials Science, 2019, 54(8): 6140-6150. doi: 10.1007/s10853-018-03254-1 [15] CHEN P, WANG F L, CHEN Z F, et al. Study on the photocatalytic mechanism and detoxicity of gemfibrozil by a sunlight-driven TiO2/carbon dots photocatalyst: The significant roles of reactive oxygen species [J]. Applied Catalysis B:Environmental, 2017, 204: 250-259. doi: 10.1016/j.apcatb.2016.11.040 [16] WANG J, GAO M M, HO G W. Bidentate-complex-derived TiO2/carbon dot photocatalysts: in situ synthesis, versatile heterostructures, and enhanced H2 evolution [J]. Journal of Materials Chemistry A, 2014, 2(16): 5703. doi: 10.1039/c3ta15114j [17] SHAFIQUE M, MAHR M S, YASEEN M, et al. CQD/TiO2 nanocomposite photocatalyst for efficient visible light-driven purification of wastewater containing methyl orange dye [J]. Materials Chemistry and Physics, 2022, 278: 125583. doi: 10.1016/j.matchemphys.2021.125583 [18] ZHUANG J D, DAI W X, TIAN Q F, et al. Photocatalytic degradation of RhB over TiO2 bilayer films: Effect of defects and their location [J]. Langmuir, 2010, 26(12): 9686-9694. doi: 10.1021/la100302m [19] LIU Y, YUAN X Z, WANG H, et al. Solvothermal synthesis of graphene/BiOCl0.75Br0.25 microspheres with excellent visible-light photocatalytic activity [J]. RSC Advances, 2015, 5(42): 33696-33704. doi: 10.1039/C5RA02852C [20] CHEN Y, LIU K R. Preparation and characterization of nitrogen-doped TiO2/diatomite integrated photocatalytic pellet for the adsorption-degradation of tetracycline hydrochloride using visible light [J]. Chemical Engineering Journal, 2016, 302: 682-696. doi: 10.1016/j.cej.2016.05.108 [21] LI T T, ZHANG S J, MENG S G, et al. Amino acid-assisted synthesis of In2S3 hierarchical architectures for selective oxidation of aromatic alcohols to aromatic aldehydes [J]. RSC Advances, 2017, 7(11): 6457-6466. doi: 10.1039/C6RA28560K [22] LYU J Z, ZHOU Z, WANG Y H, et al. Platinum-enhanced amorphous TiO2-filled mesoporous TiO2 crystals for the photocatalytic mineralization of tetracycline hydrochloride [J]. Journal of Hazardous Materials, 2019, 373: 278-284. doi: 10.1016/j.jhazmat.2019.03.096 [23] ZHAN Y, SHANG B, CHEN M, et al. One-step synthesis of silica-coated carbon dots with controllable solid-state fluorescence for white light-emitting diodes [J]. Small (Weinheim an Der Bergstrasse, Germany), 2019, 15(24): e1901161. doi: 10.1002/smll.201901161 [24] MAHATO D, KHARWAR Y P, RAMANUJAM K, et al. S, N co-doped graphene quantum dots decorated TiO2 and supported with carbon for oxygen reduction reaction catalysis [J]. International Journal of Hydrogen Energy, 2021, 46(41): 21549-21565. doi: 10.1016/j.ijhydene.2021.04.013 [25] CONG Y, LI X K, QIN Y, et al. Carbon-doped TiO2 coating on multiwalled carbon nanotubes with higher visible light photocatalytic activity [J]. Applied Catalysis B:Environmental, 2011, 107(1/2): 128-134. [26] LI F, TIAN F, LIU C J, et al. One-step synthesis of nanohybrid carbon dots and TiO2 composites with enhanced ultraviolet light active photocatalysis [J]. RSC Advances, 2015, 5(11): 8389-8396. doi: 10.1039/C4RA14865G [27] WANG J, WANG C F, CHEN S. Amphiphilic egg-derived carbon dots: Rapid plasma fabrication, pyrolysis process, and multicolor printing patterns [J]. Angewandte Chemie (International Ed. in English), 2012, 51(37): 9297-9301. doi: 10.1002/anie.201204381 [28] PHANG S J, TAN L L. Recent advances in carbon quantum dot (CQD)-based two dimensional materials for photocatalytic applications [J]. Catalysis Science & Technology, 2019, 9(21): 5882-5905. [29] XU Y G, LIU J, XIE M, et al. Construction of novel CNT/LaVO4 nanostructures for efficient antibiotic photodegradation [J]. Chemical Engineering Journal, 2019, 357: 487-497. doi: 10.1016/j.cej.2018.09.098 [30] HUNGE Y M, YADAV A A, KANG S W, et al. Photocatalytic degradation of tetracycline antibiotics using hydrothermally synthesized two-dimensional molybdenum disulfide/titanium dioxide composites [J]. Journal of Colloid and Interface Science, 2022, 606: 454-463. doi: 10.1016/j.jcis.2021.07.151 [31] FENG J W, ZHENG Z, SUN Y B, et al. Degradation of diuron in aqueous solution by dielectric barrier discharge [J]. Journal of Hazardous Materials, 2008, 154(1/2/3): 1081-1089. [32] RANJBARI A, DEMEESTERE K, VERPOORT F, et al. Novel kinetic modeling of thiabendazole removal by adsorption and photocatalysis on porous organic polymers: Effect of pH and visible light intensity [J]. Chemical Engineering Journal, 2022, 431: 133349. doi: 10.1016/j.cej.2021.133349 [33] SHARMA S, DUTTA V, SINGH P, et al. Carbon quantum dot supported semiconductor photocatalysts for efficient degradation of organic pollutants in water: A review [J]. Journal of Cleaner Production, 2019, 228: 755-769. doi: 10.1016/j.jclepro.2019.04.292 [34] YU X J, LIU J J, YU Y C, et al. Preparation and visible light photocatalytic activity of carbon quantum dots/TiO2 nanosheet composites [J]. Carbon, 2014, 68: 718-724. doi: 10.1016/j.carbon.2013.11.053 -





 下载:
下载: