吡啶类离子液体对青海弧菌Q67的混合毒性评估
Evaluation on the Combined Toxicity of Pyridium-Based Ionic Liquids to Vibrio Qinghaiensis sp. -Q67
-
摘要: 混合污染物产生的累积与毒性相互作用具有潜在的环境与健康风险。以6种吡啶类离子液体(IL):丁基溴化吡啶([Bpy]Br)、己基溴化吡啶([Hpy]Br)、辛基溴化吡啶([Opy]Br)、丁基氯化吡啶([Bpy]Cl)、己基氯化吡啶([Opy]Cl)和辛基氯化吡啶([Opy]Cl)为混合物组分,应用直接均分射线法(EquRay)和均匀设计射线法(UD-Ray)分别设计4组二元IL混合物和2组三元混合物,每组混合物包括5条具有不同浓度配比的混合物射线。应用微板毒性分析法测定6种IL及其30条混合物射线对青海弧菌Q67的发光抑制毒性,以浓度加和(CA)为加和参考模型分析混合物毒性相互作用。结果表明,Logit函数能有效地拟合6种吡啶IL及其30条混合物射线的浓度-效应数据。若以半数效应浓度的负对数(pEC50)为毒性指标,6个吡啶IL对Q67的毒性与烷基链上碳原子数目正相关,且每增加2个碳原子,其毒性约增加1。IL的阴离子(Br-或Cl-)对毒性没有影响。除己基氯化吡啶([Hpy]Cl)和辛基氯化吡啶([Opy]Cl)的二元混合物呈现明显拮抗作用外,其他二元及三元混合物都为加和作用。Abstract: The cumulative toxicity and toxicity interaction of mixtures have potential hazards and risks to the environment and human health. Selecting six pyridium-based ionic liquids (ILs), 1-butyl pyridinium bromide, 1-hexyl pyridinium bromide, 1-octyl pyridinium bromide, 1-butyl pyridinium chloride, 1-hexyl pyridinium chloride, and 1-octyl pyridinium chloride as mixture components, we employed the direct equipartition ray design and uniform design ray methods to design four groups of binary mixtures and two groups of ternary ones, respectively. Every group of mixture contains five mixture rays with different concentration ratios. The toxicities of the six single ILs and 30 binary and ternary mixture rays to Vibrio qinghaiensis sp.-Q67 (Q67) were determined by using the microplate toxicity analysis, and the mixture toxicity interaction was identified by selecting the concentration addition (CA) as an additive reference model. It was shown that concentration -response curves (CRCs) of six ILs as well as 30 binary and ternary mixture rays can be effectively described by the Logit function. Selecting the negative logarithm of median effective concentration (pEC50) as a toxicity index, the toxicity of six ILs to Q67 has a positive relationship with the length of alkyl chain in IL. Every two-carbon augment on the alkyl chain almost makes the toxicity (pEC50) of IL increasing one. The anion, Br-or Cldoes not affect the toxicity of ILs on Q67. Except that the group of binary mixtures between 1-hexyl pyridinium chloride and 1-octyl pyridinium chlorides produces significant antagonism, the other five groups of binary and ternary mixtures display the concentration additive action.
-
厌氧氨氧化(anaerobic ammonium oxidation, anammox)工艺相较于传统硝化-反硝化脱氮工艺,具有曝气量少、不消耗有机物及污泥产率低等特点[1-3],并已成功应用于城市污水处理厂污泥水及与此类似的含有高浓度氨氮废水[4-6]。在厌氧氨氧化技术成功应用于处理高浓度含氮废水后,研究重点则从处理水量小、浓度高的污泥水(侧流)转变到处理水量大、浓度低的城镇污水(主流)处理[7-10]。
厌氧氨氧化反应的功能菌为厌氧氨氧化菌(AnAOB),而温度是AnAOB生长和代谢的一个重要参数,大多数厌氧氨氧化菌的最适生长温度为30~35 ℃[11]。而在实际污水处理厂主流的水温基本处于10~25 ℃。有研究[12-13]表明,温度每降低5 ℃,厌氧氨氧化菌的比生长速率下降30%~40%,从而影响反应器的脱氮效能。MA等[14]在利用厌氧氨氧化UASB反应器在中低温条件下处理低浓度废水时发现,当反应器温度由30 ℃降至16 ℃时,总氮去除率下降62%。因此,研究厌氧氨氧化菌活性随温度变化的规律对anammox技术应用于城市污水主流处理具有重要意义。
近年来,相比于传统活性污泥工艺,基于生物膜或颗粒污泥的主流工艺表现突出[15]。有研究表明,相较于活性污泥,在温度低于15 ℃的条件下,好氧颗粒污泥可长期稳定进行亚硝化过程并表现出0.63~0.7 kg·(m3·d)−1(以氮素计)的处理能力[16-17]。这说明不同形态的污泥在遭受温度变化时微生物响应特征存在差异。LOTTI等[18]在温度为10~30 ℃条件下,研究了以游离态和颗粒态存在的厌氧氨氧化菌的反应活化能,结果表明,以游离态存在的厌氧氨氧化菌对温度变化的敏感程度大于厌氧氨氧化颗粒污泥。这说明厌氧氨氧化菌的存在形态影响其对温度的适应性。随着以颗粒污泥和生物膜形式的厌氧氨氧化技术拟在城市污水处理厂主流工艺应用中的推进,厌氧氨氧化菌在不同温度和污泥形态条件下的反应活性和特性亟需了解和研究。
本研究以培养成熟的厌氧氨氧化颗粒污泥和生物膜为研究对象,通过测定anammox菌在不同温度(15~35 ℃)和不同形态下(游离态、颗粒污泥和生物膜)的活性,探讨了厌氧氨氧化反应的活化能和温度系数的变化,以期为厌氧氨氧化技术在主流系统脱氮的应用提供参考。
1. 材料与方法
1.1 实验装置及污泥
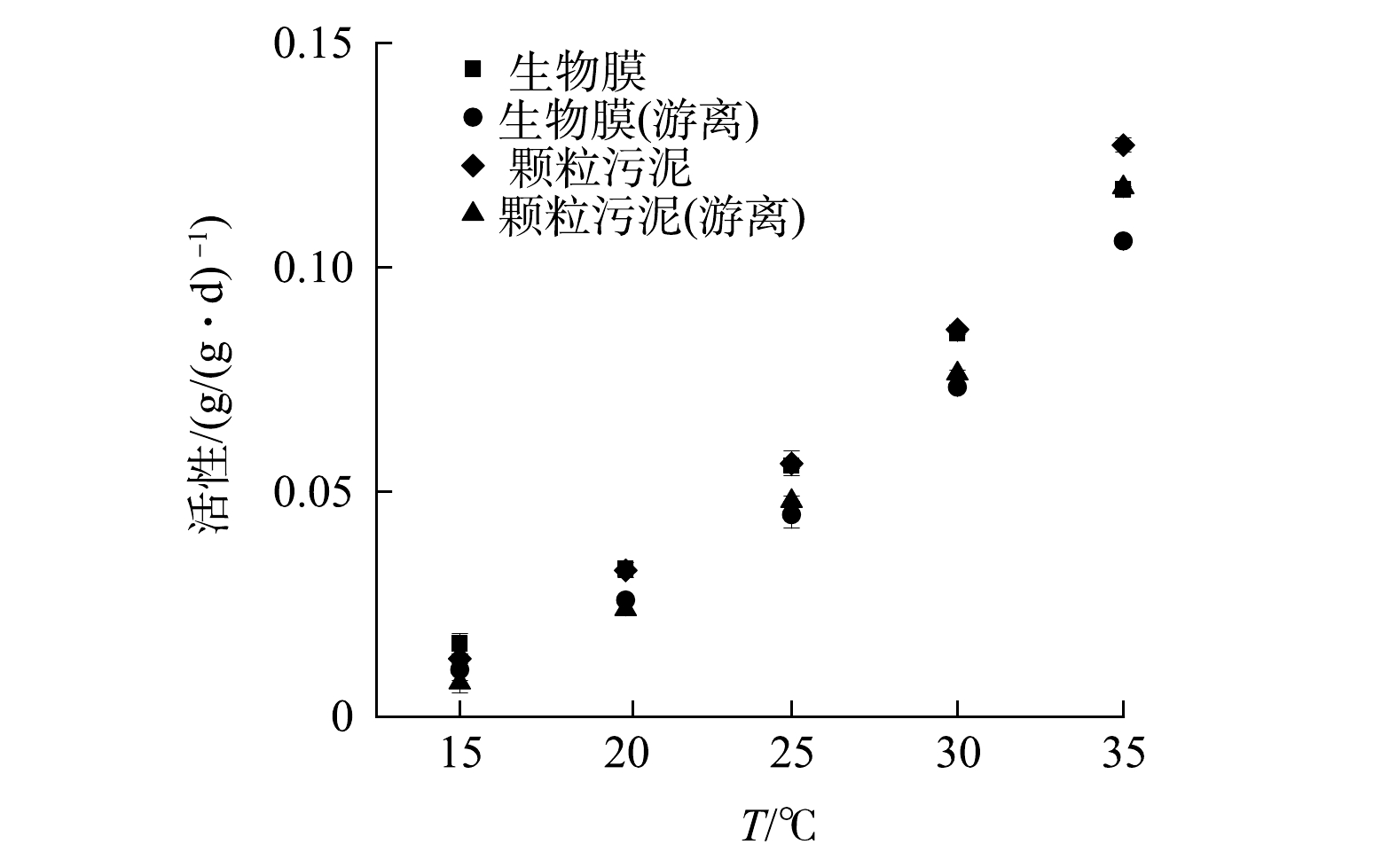
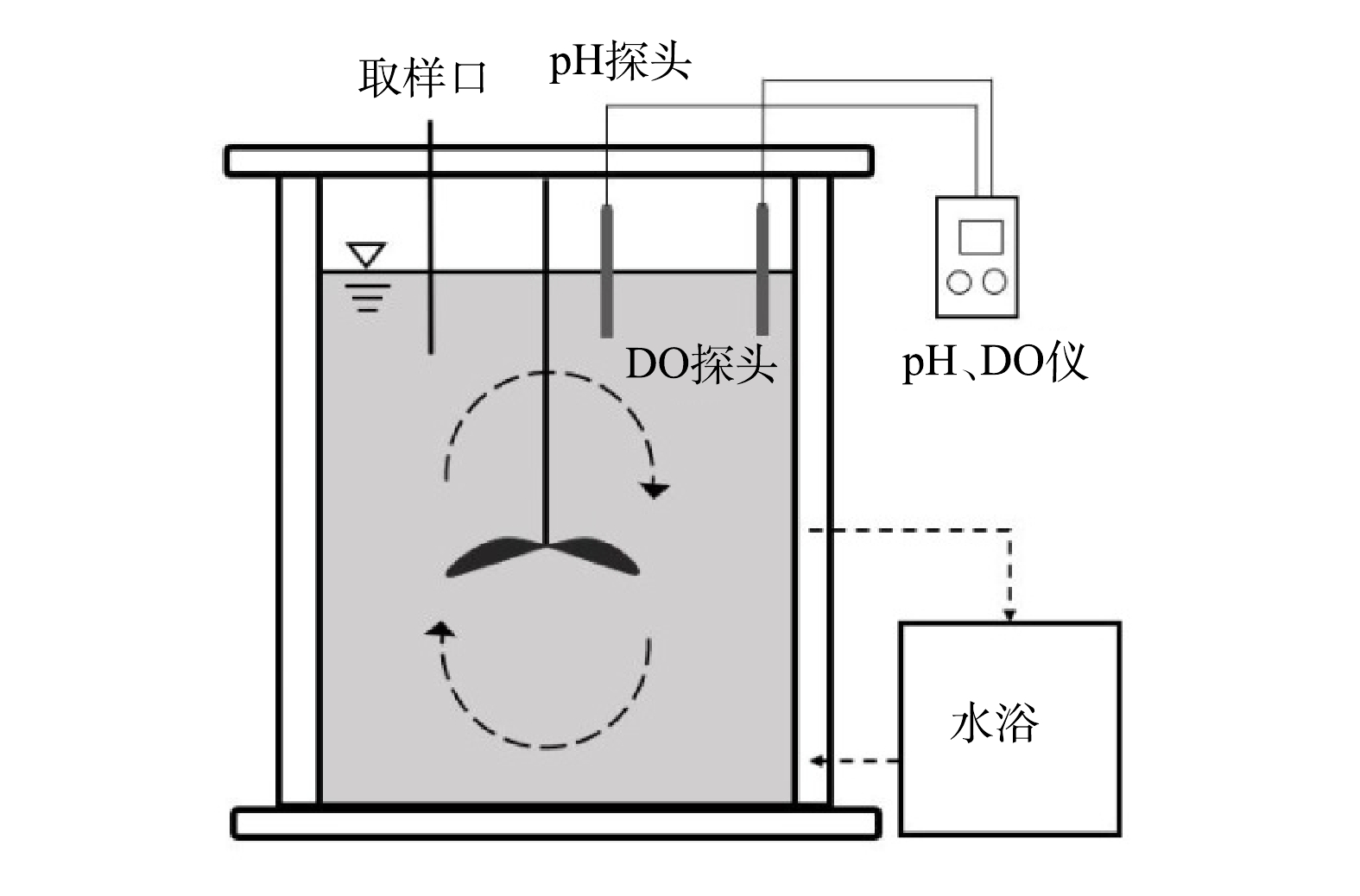
厌氧氨氧化活性(specific anammox activity, SAA)采用基质消耗速率法进行测定,测定装置如图1所示。反应器有效容积为7 L,内置推进器且在顶部设置进出水及取样口,温度由外部水浴控制,pH控制为7.5~8.1,DO控制在0.1 mg·L−1以下。活性测定过程中NH4+-N和NO2−-N由NH4Cl和NaNO2提供,质量浓度分别为30 mg·L−1和40 mg·L−1,每隔15~50 min(根据不同温度进行设定)取样并测定NH4+-N、NO2−-N和NO3−-N质量浓度,按式(1)计算厌氧氨氧化菌活性。
ki=dcidt⋅1X (1) 式中:ki为颗粒污泥、生物膜或游离状态厌氧氨氧化菌的厌氧氨氧化活性,g·(g·d)−1;ci为氮浓度变化(NH4+-N、NO2−-N及NO3−-N),mg·L−1;X为污泥浓度(mixed liquid volatile suspended solid,MLVSS),g·L−1。
厌氧氨氧化颗粒污泥取自实验室已稳定运行的厌氧氨氧化反应器,温度控制为35℃,进水负荷(nitrogen loading rate, NLR)为2.508 g·(L·d)−1,总氮(total nitrogen,TN)去除率为(87.77±1.59)%,MLVSS为(12.45±0.37) g·L−1,MLVSS/MLSS比值为0.67±0.04。厌氧氨氧化颗粒污泥呈红棕色且颗粒形态良好,直径为2 mm左右,SAA颗粒污泥为0.129 g·(g·d)−1。
厌氧氨氧化生物膜取自实验室已稳定运行的移动床生物膜反应器(moving bed biofilm reactor, MBBR),反应器温度控制为35 ℃,NLR为5.446 g·(L·d)−1,TN去除率为(73.15±5)%,填料型号为K3(比表面积为500 m2·m−3),生物膜厚度为2~3 mm,外观呈现红棕色,SAA生物膜为0.117 g·(g·d)−1 。
游离状态的厌氧氨氧化菌为实验所用颗粒污泥和生物膜通过磁力搅拌分散,以1 000 r·min−1搅拌时间3 min。由Microtrac Sync粒度仪(SYNC,美国)测定分散后的污泥粒径约为7.02~30.36 μm(≤30 μm),此时可认为污泥中的anammox处于游离态[19]。
1.2 水质指标测定
NH4+-N、NO2−-N和NO3−-N的测定参照标准方法[20]进行。NH4+-N使用纳氏试剂分光光度法测定;NO2−-N使用N-(1-萘基)-乙二胺光度法测定;NO3−-N使用紫外分光光度法测定。MLSS和MLVSS使用标准重量法测定;pH使用雷磁PH-3C pH计测定;DO使用便携式溶氧仪测定。
1.3 活化能及温度系数的计算
厌氧氨氧化菌的生物反应速率(活性)和温度的关系通过Arrhenius方程(式(2))表示,对式(2)进行积分可得式(3)。
dlnkdT=EaRT2 (2) 式中:k为厌氧氨氧化活性,g·(g·d)−1;Ea为反应所需活化能,J·mol−1;T为热力学温度,K;R为气体常数,8.314 J·(K·mol)−1。
lnk=−EaRT+lnA (3) 式中:A为Arrhenius常数。通过测定不同温度下的k,做lnk与1/T的关系图,直线的斜率为-Ea/R,由此可确定相应形态下的厌氧氨氧化活化能Ea。若温度分别为T1和T2时,反应速率分别为k1和k2,将其分别代入式(3),得式(4)和式(5)。将式(4)和式(5)相减可得式(6),再进一步换算可得式(7)。
lnk1=−EaRT1+lnA (4) lnk2=−EaRT2+lnA (5) lnk2k1=−EaR⋅T1−T2T1T2 (6) k2=k1⋅eEaRT1T2⋅(T2−T1) (7) 令Ea/(R·T1·T2)=KT (温度影响因子),e^(KT)=θ (温度系数),则(7)式可改为式(8)
k2=k1⋅θ⋅(T2−T1) (8) 根据不同温度下的Ea,计算温度影响因子KT,从而确定温度系数θ。
1.4 Anammox种群结构分析
对实验污泥采用高通量测序,确定污泥中anammox菌的种群结构。取一定数量的生物膜及颗粒污泥,经去离子水淘洗离心后按照试剂盒E.Z.N.A.® soil DNA Kit (Omega Bio-tek,Norcross GA, U.S.)规定的方法对DNA进行提取。以提取的DNA为PCR模板,采用V3-V4引物(序列为338F:5'-ACTCCTACGGGAGGCAGCAG-3'和806R:5'-GGACTACHVGGGTWTATAAT-3'),在ABI Gene Amp® 9700 PCR thermo-cycler(ABI, CA,USA)上进行PCR反应。将同一样本的PCR产物混合后使用2%琼脂糖凝胶回收PCR产物,利用AxyPrep DNA Gel Extraction Kit (Axygen Biosciences,Union City,CA,USA)进行回收产物纯化,2%琼脂糖凝胶电泳检测,并用Quantus™ Fluorometer (Promega,USA)对回收产物进行检测定量。使用NEXTflexTM Rapid DNA-Seq Kit (Bioo Scientific,美国)进行建库,利用Illumina公司的Miseq PE300/NovaSeq PE250平台进行测序(上海美吉生物医药科技有限公司,www.majorbio.com)。
2. 结果与讨论
2.1 厌氧氨氧化颗粒污泥和生物膜微生物群落结构分析
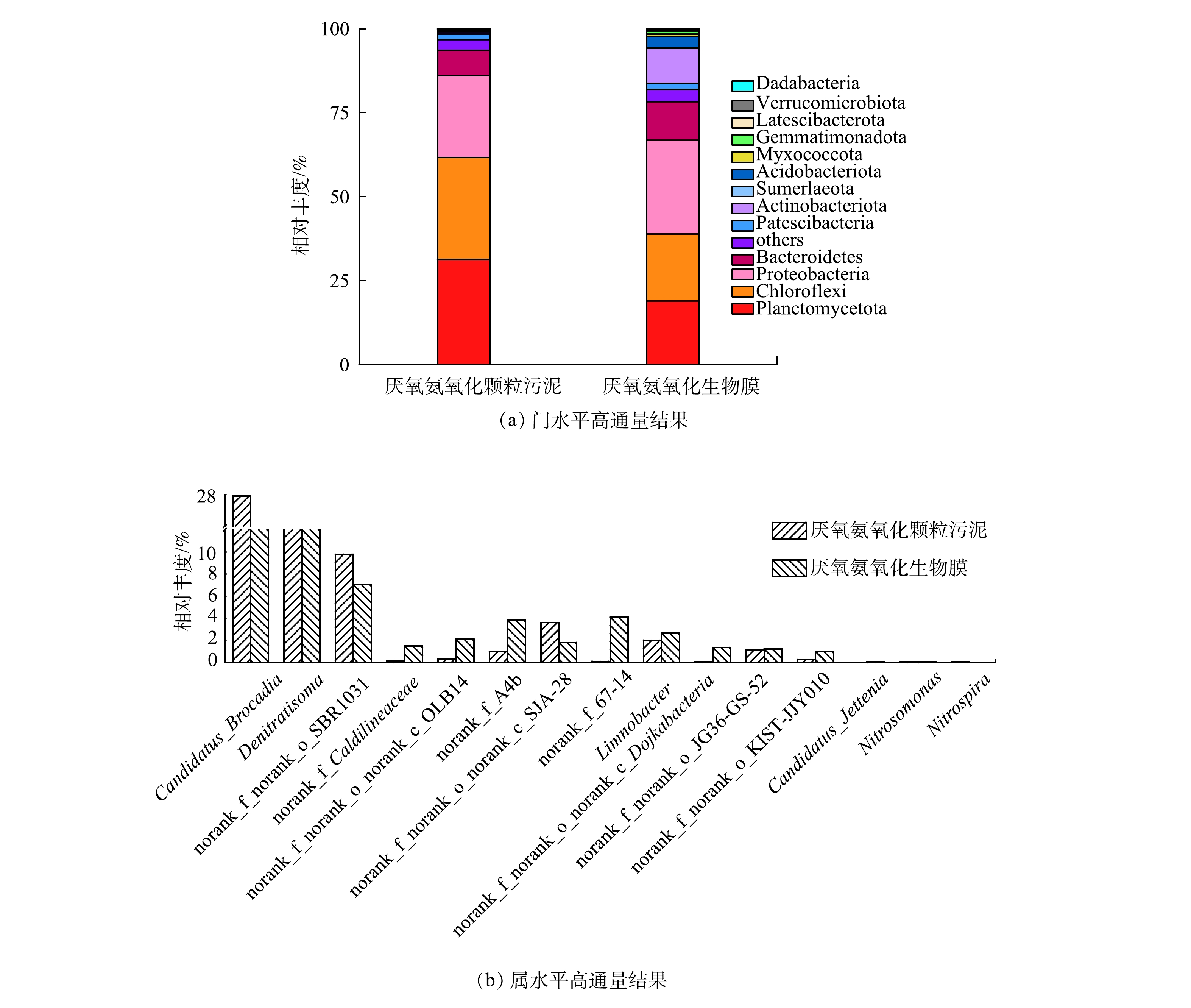
由图2可见,从门水平上来看,Planctomycetes门的微生物相对丰度分别为31.36%和18.86%,而Planctomycetes门中包含所有已知的anammox菌[21-22]。在属水平上,颗粒污泥和生物膜上探明的主要anammox菌属为Ca. Brocadia,此结果和主流系统内已探明的典型种属相同[23-24],相对丰度达到27.96%和17.52%。该结果表明anammox菌在颗粒污泥上和生物膜上均占据主导地位。除此之外,污泥中还含有Chloroflexi、Proteobacteria、Bacteroidetes。这些微生物的存在对颗粒污泥颗粒化及颗粒形态维持的过程中具有重要的作用[25]。因此,以上述2种污泥样品进行不同温度条件下的厌氧氨氧化活性特性研究是可行的。
2.2 颗粒污泥和生物膜的SAA
图3为不同温度条件下SAA的测定结果。SAA颗粒污泥随温度的下降而下降,当温度由35 ℃降至15 ℃时,SAA颗粒污泥由0.128 g·(g·d)−1下降至0.013 g·(g·d)−1,活性损失了89.89%。在对颗粒污泥进行分散处理后,SAA颗粒污泥(游离)由0.118 g·(g·d)−1(35 ℃)下降至0.008 g·(g·d)−1(15 ℃),活性损失增至93.58%。同样,当温度由35 ℃降至15 ℃时,SAA生物膜由0.117 g·(g·d)−1下降至0.016 g·(g·d)−1,活性损失为86.19%。在对生物膜进行分散处理后,SAA生物膜(游离)由0.106 g·(g·d)−1(35 ℃)下降至0.010 g·(g·d)−1(15 ℃),活性损失升至90.17%。由此可见,随着温度降低,SAA颗粒污泥和SAA生物膜均有不同程度的减小,但生物膜抵抗温度变化的能力较强。
2.3 厌氧氨氧化反应Ea
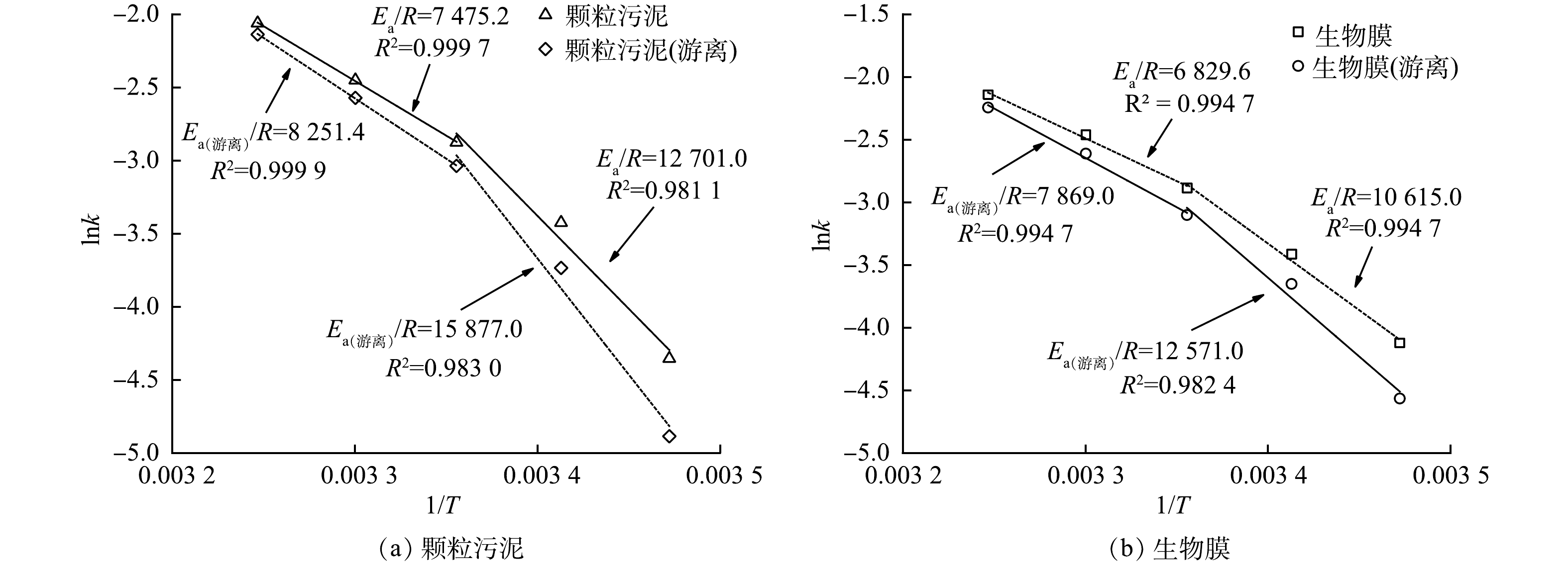
Ea值越大,说明反应过程中要跨越的能垒越大,该反应越难进行;反之,Ea值越小,则说明反应过程中要跨越的能垒越小,反应则越容易进行。由图4可见,不论颗粒污泥还是生物膜,若以15~35 ℃进行拟合,lnk和1/T线性关系较差,而若分别以15~25 ℃和25~35 ℃拟合,则能取得较好的线性关系。这表明颗粒污泥和生物膜的厌氧氨氧反应在不同温度范围内的活化能不同。谭锡诚等[26]在运行厌氧氨氧化反应器时也有相同发现。针对厌氧氨氧化活性存在拐点这一现象,ISAKA等[27]认为可能是由于厌氧氨氧化反应在不同温度区间酶活性存在差异所致。因此,将15~35 ℃分为15~25 ℃和25~35 ℃ 2个区间更符合anammox对温度的效应。由图4(a)可见,在15~25 ℃和25~35 ℃的活化能Ea-颗粒污泥分别为105.60 kJ·mol−1和62.15 kJ·mol−1;在15~25 ℃和25~35 ℃ Ea-颗粒污泥(游离)分别为132.00 kJ·mol−1和68.60 kJ·mol−1。由图4(b)可见,对生物膜而言,在15~25 ℃和25~35 ℃的活化能Ea-生物膜分别为88.25 kJ·mol−1和56.78 kJ·mol−1;在15~25 ℃和25~35 ℃ Ea-生物膜(游离)分别为104.52 kJ·mol−1和65.42 kJ·mol−1。以上数据说明不同形态的厌氧氨氧化菌活化能在不同温度区间有明显差异,温度较高时(25~35 ℃)的活化能明显小于温度较低时(15~25 ℃)的活化能。因此,厌氧氨氧化反应在温度较高时更容易进行。LOTTI等[18]的研究结果也证实了这一点。颗粒污泥和生物膜在进行分散处理后,Ea值均有不同程度的升高,说明Anammox菌的Ea与其存在状态有关。当Anammox菌以颗粒污泥和生物膜形态存在时,Anammox菌被胞外聚合物(EPS)包裹,这有助于抵抗外界温度变化[28];而当anammox菌以游离态存在时,由于缺少EPS的保护,anammox菌对温度变化就变得敏感。王淑莹等[29]研究温度对硝化反应的影响时也发现,同一温度范围内颗粒污泥的硝化反应Ea值低于絮状污泥。这说明颗粒污泥或生物膜空间结构的确有助于微生物抵抗外界的温度变化。除分散前后Ea发生变化外,生物膜所得Ea值与颗粒污泥所得Ea值两者存在差异,推测其原因可能是颗粒污泥与生物膜内EPS的含量不同。有研究表明,厌氧氨氧化颗粒污泥EPS含量为71.82~140.3 mg·g−1[30-34](以EPS计),而生物膜中EPS含量可高达300.84 mg·g−1[35]。此外,郭静[36]发现厌氧氨氧化生物膜中的EPS总量略高于颗粒污泥。这可能是造成生物膜Ea值与颗粒污泥Ea值存在差异的主要原因,但还需进一步研究。
表1比较了本研究与文献报道的厌氧氨氧化反应Ea值。本研究颗粒污泥和生物膜中的厌氧氨氧化菌在25~35 ℃下的反应活化能分别为62.15 kJ·mol−1和56.78 kJ·mol−1,上述数值与STROUS等[13]报道的Ca. Brocadia在20~43 ℃下的Ea为70 kJ·mol−1 相近。此外,LOTTI等[18]报道,厌氧氨氧化菌活化能为68 kJ·mol−1(25~30 ℃),这也与本研究获得的Ea值相近。颗粒污泥中的厌氧氨氧化菌在15~25 ℃下的反应活化能为105.60 kJ·mol−1。PARK等[37]利用厌氧氨氧化颗粒污泥在13~23 ℃下获得Ea为89.6 kJ·mol−1,略低于本研究的结果。这可能是因为实验所用anammox菌不同而存在差异。本研究中Anammox菌为Ca. Brocadia菌,而PARK等[37]研究的anammox菌是Ca. Kuenenia菌。
表 1 不同实验厌氧氨氧化反应Ea值Table 1. Ea values for anaerobic ammonia oxidation reactions in different tests污泥形态 anammox种属 Ea/(kJ·mol−1) 参考文献 生物膜 Ca. Brocadia 88.25(15~25 ℃);56.78(25~35 ℃) 本研究 生物膜(游离) 104.52(15~25 ℃);65.42(25~35 ℃) 颗粒污泥 Ca. Brocadia 105.60(15~25 ℃); 62.15(25~35 ℃) 本研究 颗粒污泥(游离) 132.00(15~25 ℃);68.60(25~35 ℃) 颗粒污泥 Ca. KueneniaCa.Jettenia 93~94(6~28 ℃);33(28~37 ℃) [27] 颗粒污泥 Ca.Brocadia 230(10~15 ℃);105(15~20 ℃)68(20~25 ℃);46(25~30 ℃) [18] 颗粒污泥 Ca. Kuenenia 89(20~43 ℃) [37] 颗粒污泥 Ca. Kuenenia. 72.8(10~30 ℃) [37] 颗粒污泥 Ca.Brocadia 89.6(13~23 ℃);16.4(23~33 ℃) [37] 活性污泥 Ca. Brocadia 107.4(10~25 ℃) [37] 活性污泥 Ca. Brocadia 70(20~43 ℃) [13] 活性污泥 Ca.Brocadia 293(10~15 ℃);131(15~20 ℃)79(20~25 ℃);68(25~30 ℃) [18] 2.4 温度系数θ
依据各温度区间所得Ea,可得出不同形态下anammox污泥的温度系数θ。结果表明,颗粒污泥在15~25 ℃和25~35 ℃下的温度系数θ分别为1.14和1.09;生物膜在15~25 ℃和25~35 ℃的θ分别1.12和1.08。
在污水处理中,温度系数可以衡量系统温度对反应速率和净化能力的影响,θ值越大,表明温度变化对该微生物活性的影响越大。我国城市污水处理厂生物池中温度通常为15~25 ℃,且厌氧氨氧化过程必须与亚硝化或部分反硝化配合使用,因此,对比15~25 ℃厌氧氨氧化工艺中各功能微生物的KT和θ是必要的。表2为本研究和文献报道的厌氧氨氧化工艺中功能微生物的KT和θ值。可见,当温度为15~25 ℃时,各功能微生物的θ值大致为θ反硝化<θAOB<θanammox。这可能与3种功能菌的最适温度有关。Anammox菌、氨氧化菌(ammonium oxidizing bacteria, AOB)和反硝化菌的适宜温度依次为30~40、20~30和15~35 ℃,使得anammox菌的θ值较大,即anammox菌对低温环境的适应性弱于其他2种微生物。相比于反硝化菌,AOB温度系数θ值略小,这表明AOB抵抗温度变化的能力较强。因此,在主流系统内采用亚硝化厌氧氨氧化工艺比部分反硝化厌氧氨氧化工艺更有优势。
表 2 厌氧氨氧化工艺中功能微生物的KT和θTable 2. KT and θ of functional microorganisms in anammox process3. 结论
1)当温度由35 ℃降至15 ℃时,以颗粒污泥形态存在的anammox菌活性由0.128 g·(g·d)−1下降至0.013 g·(g·d)−1,以生物膜形态存在的anammox菌活性由0.117 g·(g·d)−1下降至0.016 g·(g·d)−1。
2)以颗粒污泥形态存在的anammox菌在15~25 ℃和25~35 ℃的Ea分别为105.60 kJ·mol−1和62.15 kJ·mol−1;以生物膜形态存在的anammox菌在15~25 ℃和25~35 ℃的活化能分别为88.25 kJ·mol−1和56.78 kJ·mol−1。这表明以生物膜形态存在的anammox菌对于温度变化的抵抗能力较强。
3)以颗粒污泥形态存在的anammox菌在15~25 ℃和25~35 ℃的θ分别为1.14和1.09;以生物膜形态存在的anammox菌在15~25 ℃和25~35 ℃的θ分别为1.12和1.08。与硝化菌或反硝化菌相比,本实验所获得的厌氧氨氧化菌的温度系数θ偏大。这表明,厌氧氨氧化菌对温度的变化更为敏感,使得厌氧氨氧化在低温条件下首先将成为限制步。
-

 点击查看大图
点击查看大图
计量
- 文章访问数: 2172
- HTML全文浏览数: 2172
- PDF下载数: 34
- 施引文献: 0



 下载:
下载: