生物扰动对沉积物中污染物环境行为与生物可利用性的影响
Influence of Bioturbation on Fate and Bioavailability of Sediment-Associated Contaminants
-
摘要: 疏水性有机污染物进入环境水体后易于与沉积物结合,对沉积物中的底栖动物造成危害。底栖动物引起的生物扰动作用可以通过改变沉积物的地球化学性质,对其中污染物的赋存形态、迁移转化和生物可利用性产生重要影响。在综述了国内外生物扰动影响沉积物中污染物环境行为和生物可利用性的最新研究进展基础上,重点讨论了沉积物颗粒交换、水体环境条件改变、疏水有机污染物解吸释放过程以及对生物扰动影响的定量化表征。最后对该研究方向进行了展望,指出应重点研究多种污染物及不同生物共存条件下的生态效应,以及造成沉积物扰动的影响因素的定量化表征等。Abstract: Hydrophobic organic contaminants and heavy metals tend to bind to the solid phases including bed sediments and suspended particles, in aquatic ecosystems. Sediment-associated contaminants may be released to water body under certain conditions. Bioturbation caused by the activities of benthic organisms is one of the factors affecting fate of chemicals in sediment. By altering sediment geochemistry characteristics, the bioturbation influenced on distribution, transport, bioavailability and toxicity of contaminants in sediment. This paper reviewed the recent studies on how bioturbation affects environmental fate and risks of sediment-associated contaminants, with a focus on movements of sediment particles, alteration of characteristics of water body, desorption of contaminants from sediment, and quantitative characterization of bioturbation. In the future, more studies will be required to better understand the effects of bioturbation on multiple classes of contaminants, the influence of bioturbation on bioavailability and toxicity of contaminants to the co-exposed organisms, as well as the quantitative characterization of bioturbation.
-
Key words:
- bioturbation /
- hydrophobic contaminants /
- sediment /
- environmental fate /
- bioavailability
-
地热资源作为一种集水、矿和热为一体的清洁能源,还兼具医疗和旅游价值,是极具开发潜力的一种新型能源. 在经过补给后进入深部的地热水其赋存环境、运移规律和反应过程相当复杂,同时受到热力、水力以及化学等多种因素的影响;地热水复杂的形成过程也导致了难以对地热系统进行全面系统的了解,而开展地热系统成因模式、水岩相互作用过程研究对推进地热系统的了解有极大帮助[1]. 海南岛的地热资源呈现出以中低温为主、出露点多、储量大的特点,开发利用潜力巨大,具有代表性的琼海官新地热田、儋州兰洋温泉、保亭七仙岭温泉都得到了不同程度的开发利用. 随着地热资源的大面积开发,地热水高氟的特点而导致的氟污染问题受到越来越多的关注[2].
氟作为自然界中常见的元素,主要来源于深部地壳和地幔,以吸附态氟离子、固体氟化物以及氟矿石颗粒等赋存形态广泛分布于岩石圈、水圈、土壤圈中[3]. 氟是人体生长发育过程中必不可少的微量元素,在人体微量元素含量的第三位,摄入适量的氟能够预防龋齿和骨质疏松,但是人体对氟的最佳摄入量的范围十分小[4]. 当氟浓度的摄入量过大时,会导致矿化过度或异位矿化的病理现象,即地方性氟中毒. 地方性氟中毒广泛分布于中国各个地区,患病人数超过1亿,为降低患病人数国家政府投入了大量的人力物力,但效果并不是很理想. 过量的氟对土壤中各类微生物和植物的生长会造成一定程度的危害,同时也会造成人体肾上腺素功能紊乱[5].
地下热水的含氟量通常高于同地区的地表水和地下水,含量通常介于3—10 mg·L−1,远高于中国饮用水标准中规定的1 mg·L−1. 在地热资源当前大规模应用的情况下,高氟含量尾水的排放对于水、土壤环境中氟含量的影响将成为一个不容忽视的问题. 20世纪以来,有关于水环境中氟的研究日益增多,吕晓立[6]对新疆塔城盆地的含氟地下水的分布特征和富集规律进行了分析,李成城[7]总结了运城盆地的高氟地下水的成因机制,但地下热水中氟的研究却比较少. 琼北地区温泉出露点多,地热水中氟含量高,在开发过程中对环境的潜在威胁大. 针对这一问题,本文通过对琼北地区的地质资料、水化学数据、同位素数据进行分析,探究地热水的富集规律和分布特征. 探究内容可以为研究区防治地热水污染提供参考,同时对地热资源合理开发具有重要的指导意义.
1. 材料与方法(Materials and Methods)
1.1 研究区域
如图1(a)所示,研究区位于中国海南岛的中北部,四面环海,与雷州半岛相隔琼州海峡,是中国第二大海岛. 地理位置坐标为东经109°23′31″—110°41′17″,北纬19°6′48″—20°03′52″,包括琼海市、屯昌县、儋州市、昌江黎族自治县、澄迈县、琼中黎族苗族自治县、海口市和文昌市. 研究区地处热带,属于热带季风性气候,夏季长冬季短,平均气温约为25℃. 海南岛降雨充足,雨季一般分布于5—10月,降水量约占全年的80%. 整个海南岛地势呈现出中部高、四周低平的特点,地势以中部五指山、七仙岭为代表的高点向海岛四周逐渐降低. 地表水含量丰富,水库、河流和湖泊众多,其中河流大多起源于中部山区或者丘陵区,呈放射状分流入海. 琼北地区地下水大多分布于厚度大、岩性稳定的第三系海相碎屑砂、砂砾层,地下水类型丰富,含水层厚度约为30—100 m,距离顶板埋深一般大于100 m[8].
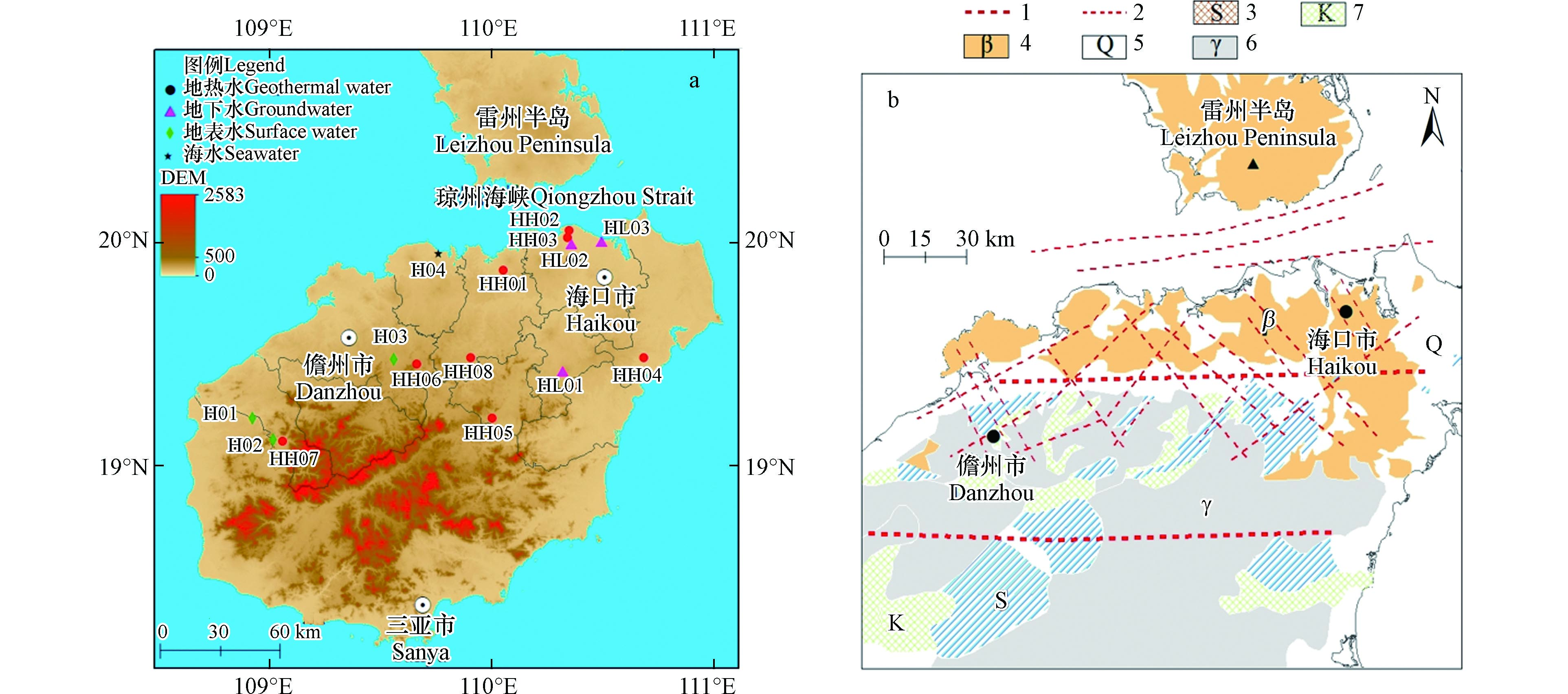 图 1 研究区采样分布图(a),地质构造图(b)Figure 1. Sampling distribution map of the study area (a), Geological structure map (b)1-大断裂,2-小断裂,S-志留系,Q-第四系砂土、粘土,γ-中生代花岗岩,K-白垩系石英碎屑岩,β-新生代玄武岩1-large fault, 2-small fault, S-Silurian, Q-quaternary sand, clay, γ-Mesozoic granite, K-Cretaceous quartz clastic rock, β-Cenozoic basalt
图 1 研究区采样分布图(a),地质构造图(b)Figure 1. Sampling distribution map of the study area (a), Geological structure map (b)1-大断裂,2-小断裂,S-志留系,Q-第四系砂土、粘土,γ-中生代花岗岩,K-白垩系石英碎屑岩,β-新生代玄武岩1-large fault, 2-small fault, S-Silurian, Q-quaternary sand, clay, γ-Mesozoic granite, K-Cretaceous quartz clastic rock, β-Cenozoic basalt琼北地区是指海南岛中北部昌江-琼海大断裂以北的陆域部分,从大地构造上分析属于雷琼凹陷. 自新生代以来区内出现了强烈、频繁的火山活动,北部地区地表覆盖有相当厚度的新生代玄武岩[8]. 图1(b)中表明,研究区中部广泛出露花岗岩,其中以中生代为主,基底为元古代的变质火山岩系,花岗岩良好的透水性特点更有利于地下水补给和出露. 沿海地带主要发育第四系的砂岩、粘土和亚砂土,呈带状环岛分布,泥盆系、三叠系碎屑岩广泛分布于儋州市、琼海市境内.
区域内构造发育良好,基本可以将断裂分为近东西向、南北向、北东向和北西向四组,近东西向类断裂规模最大、数量最多,以区内的昌江-琼海大断裂和王五-文教大断裂为代表[9]. 王五-文教大断裂地理坐标约为19°45′,全长达到210 km,横跨临高县、澄迈县、儋州市、海口市等地,沿该断裂带热泉大量出露. 昌江-琼海大断裂约位于19°15′,沿着断裂分布着大量的山脉与河流,横跨昌江、白沙、东方等地,全长达90 km. 在研究区内北部各向断裂相互交叉,产生汇水汇热效应更有利于热水出露于地表[10].
1.2 样品的采集与测试
为了探究琼北地区地热水中氟的富集规律,在2019年7月前往海南岛进行实地勘探和地热水、河水和地下水等的采集. 采样点的具体分布见图1(a),总共采集15个水样,其中海水由于测试仪器无法承受高浓度的氯离子,因此将其稀释10倍. 样品的采集均采用50 mL的聚乙烯瓶,采样前用目标水样清洗3次再进行采样. 采样过程中利用0.45 μm的醋酸纤维脂膜与注射器过滤水样,过滤后的水样为了防止其产生变化,用注射器装满水样品,防止产生气泡. 阳离子和微量元素的样品,加入浓硫酸酸化至pH<2对其进行保护. 在现场使用精度为0.1℃的温度计测量温度,使用德国WTW Multi 3400i多参数水质分析仪器测定其pH值、TDS.
采集样品的测试工作于2019年9月在国土资源部岩溶地质资源检测中心进行. 阴阳离子的测试工作于26℃、湿度69%的条件下采用Seven Multi pH/电导率/离子综合测试仪、883 离子色谱仪、FP6410 火焰分光光度计和Thermo iCE 3500 原子吸收光谱仪等仪器进行;δ2H、δ18O同位素的测试工作则于24.2℃、湿度48.9的环境下采用MAT253型稳定同位素质谱仪进行.
2. 结果与讨论 (Results and discussion)
2.1 地热水水环境特征
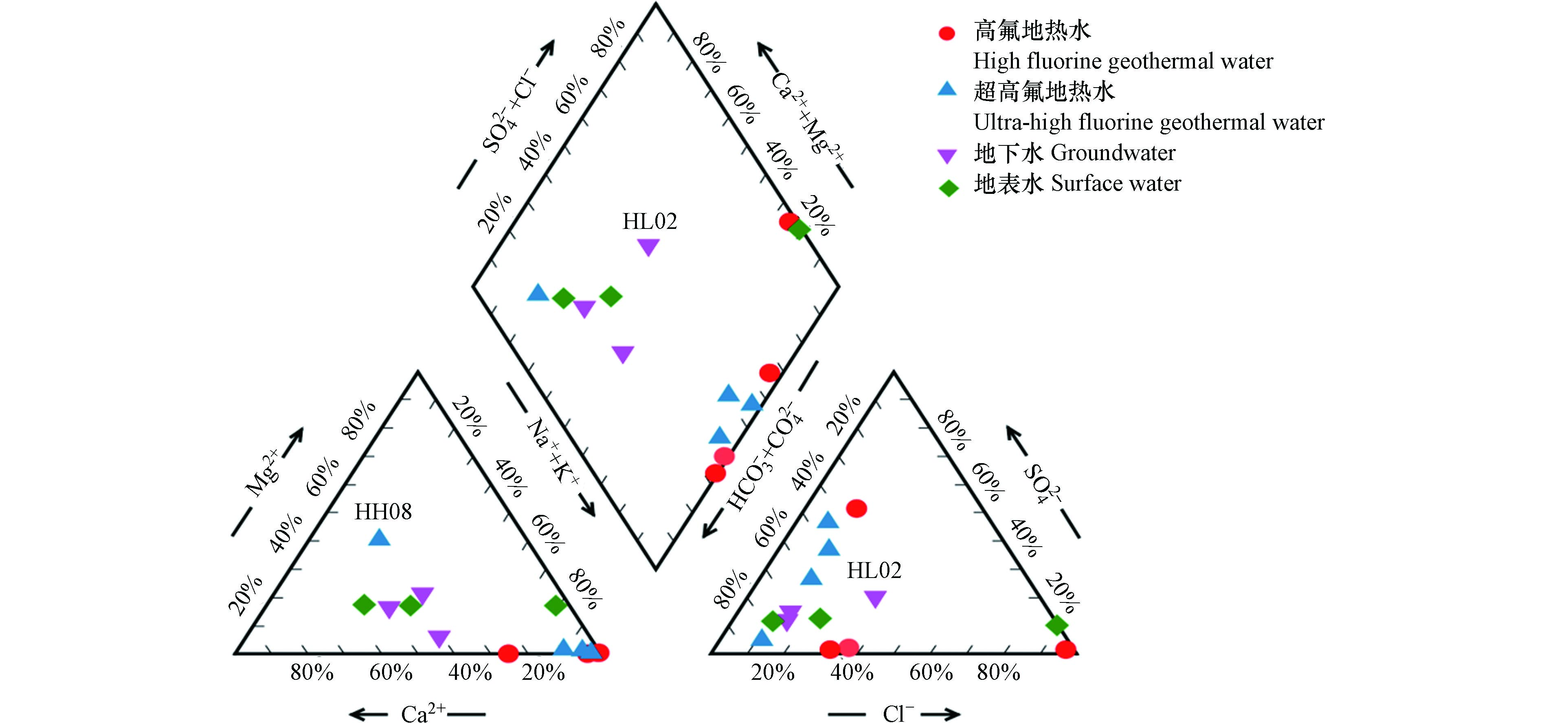
琼北地区所采集的样品的水化学组分如表1所示,地热水pH含量变化范围为7.59—9.07,平均值为8.31,呈弱碱性;温度变化范围为35.1—83.5℃,依据《地热资源地质勘探规范》(GB/T1615-2010)的分类属于典型的中低温型热水. TDS的波动范围较大,均值为962.25 mg·L−1,最高值HH04兰洋温泉可达到3096.00 mg·L−1. 主要阳离子Na+、Ca2+变化范围分别为110.50—960.00 mg·L−1和2.39—293.42 mg·L−1,主要阴离子为Cl-和HCO3-, 平均值分别为376.31 mg·L−1和472.04 mg·L−1. 地下水和地表水的水化学组分极为相似,pH值为6.85—7.85,呈中性且波动范围小,温度平均值为27.11℃. TDS除HL03样品外均值为403.80 mg·L−1,明显小于地热水的TDS;这可能是由于地热水在高温下经历了更长时间的循环过程,导致出露的热泉水含有更多的溶解性物质[11]. HL03位于琼州市境内,地层中含有的盐岩层,使得地热水在循环过程中有更高的TDS含量[12]. 相对于地热水的主要离子,地下水和地表水的离子含量显著更小,Na+和Ca2+含量平均值分别为6.90 mg·L−1和10.06 mg·L−1,Cl-和HCO3-含量变化范围为2.99—12.97 mg·L−1和32.74—102.77 mg·L−1.
表 1 研究区水样水化学组分特征Table 1. Water chemical composition characteristics of water samples in the study area采样点Sample 类型Type pH T/℃ TDS/(mg·L−1) K+/(mg·L−1) Na+/(mg·L−1) Ca2+/(mg·L−1) Mg2+/(mg·L−1) Cl−/(mg·L−1) SO42−/(mg·L−1) HCO3−/(mg·L−1) F−/(mg·L−1) δ2H/‰ δ18O/‰ HH01 高氟地热水 8.10 35.1 746 5.1 778.1 4.8 1.5 310.3 38.6 1122.3 6.32 −49.4 −6.53 HH02 高氟地热水 7.99 43.8 1430 6.0 681.3 4.2 2.2 383.4 30.1 1106.0 7.36 −43.6 −6.48 HH03 高氟地热水 8.47 38.7 1306 4.9 653.8 3.0 1.1 290.6 19.2 1058.7 8.29 −42.7 −6.37 HH04 高氟地热水 7.59 70.1 3096 63.3 960.0 293.4 0.1 1957.3 42.6 71.9 5.30 −46.9 −6.18 HH05 超高氟地热水 8.92 47.3 266 3.1 125.5 4.2 0.1 19.1 94.5 83.7 22.00 −52.8 −7.38 HH06 超高氟地热水 8.18 83.5 281 5.8 114.8 10.8 1.1 21.5 78.0 125.5 20.40 −54.8 −6.98 HH07 超高氟地热水 9.07 40.1 442 2.6 110.5 2.4 0.4 8.7 63.6 77.3 23.10 −65.5 −8.92 HH08 超高氟地热水 8.19 55.4 131 3.0 112.0 4.8 0.7 19.7 49.6 131.0 21.25 −55.3 −7.41 HL01 地下水 6.89 26.1 221 1.0 9.2 17.9 10.9 8.1 5.0 102.8 0.02 −44.9 −6.7 HL02 地下水 6.93 26.3 668 3.6 4.0 4.2 0.4 3.0 4.2 32.7 0.02 −23.5 −3.42 HL03 地下水 7.85 26.5 3490 3.5 9.5 9.6 3.3 13.0 10.3 36.4 0.42 −36.5 −5.1 H01 地表水 7.59 28.7 421 2.7 6.9 10.8 2.2 5.4 5.7 46.4 0.44 −39.2 −5.45 H02 地表水 7.25 27.6 380 0.1 4.7 9.6 1.8 3.2 4.5 40.0 0.26 −38.8 −5.51 H03 地表水 6.85 27.5 329 2.6 7.2 8.4 2.0 7.2 5.3 38.2 0.32 −34.4 −4.97 H04 海水 7.15 27.1 1001 14.1 488.8 19.7 57.3 857.8 131.0 10.9 0.02 − − 研究区地下热水的氟含量变化范围为5.30—23.10 mg·L−1,平均值为14.25 mg·L−1,F−含量远高于《生活饮用水卫生标准》(GB5749-2006)规定的1 mg·L−1. 将研究区地下热水的含氟量分为两个等级,20 mg·L−1>F−>1mg·L−1为高氟地热水,F−>20 mg·L−1为超高氟地热水. HH05-HH08地热水水样位于海南岛内陆地区,其F−含量均超过20 mg·L−1,而其余沿海地区的地热水F−含量均值为6.82 mg·L−1,说明研究区从沿海向内陆地区地热水的F−含量呈增大趋势. 地下水和地表水的F−含量较低,变化范围为0.02—0.44 mg·L−1,均值为0.25 mg·L−1,含量能够达到《生活饮用水卫生标准》(GB5749-2006)的要求. 地热水水化学类型有HCO3-Na、SO4-Na、HCO3-Mg、Cl-Na,其中HCO3-Na是主要的水化学类型;地下水和地表水的水化学类型主要以重碳酸根型为主(图2).
2.2 地热水氢氧同位素特征
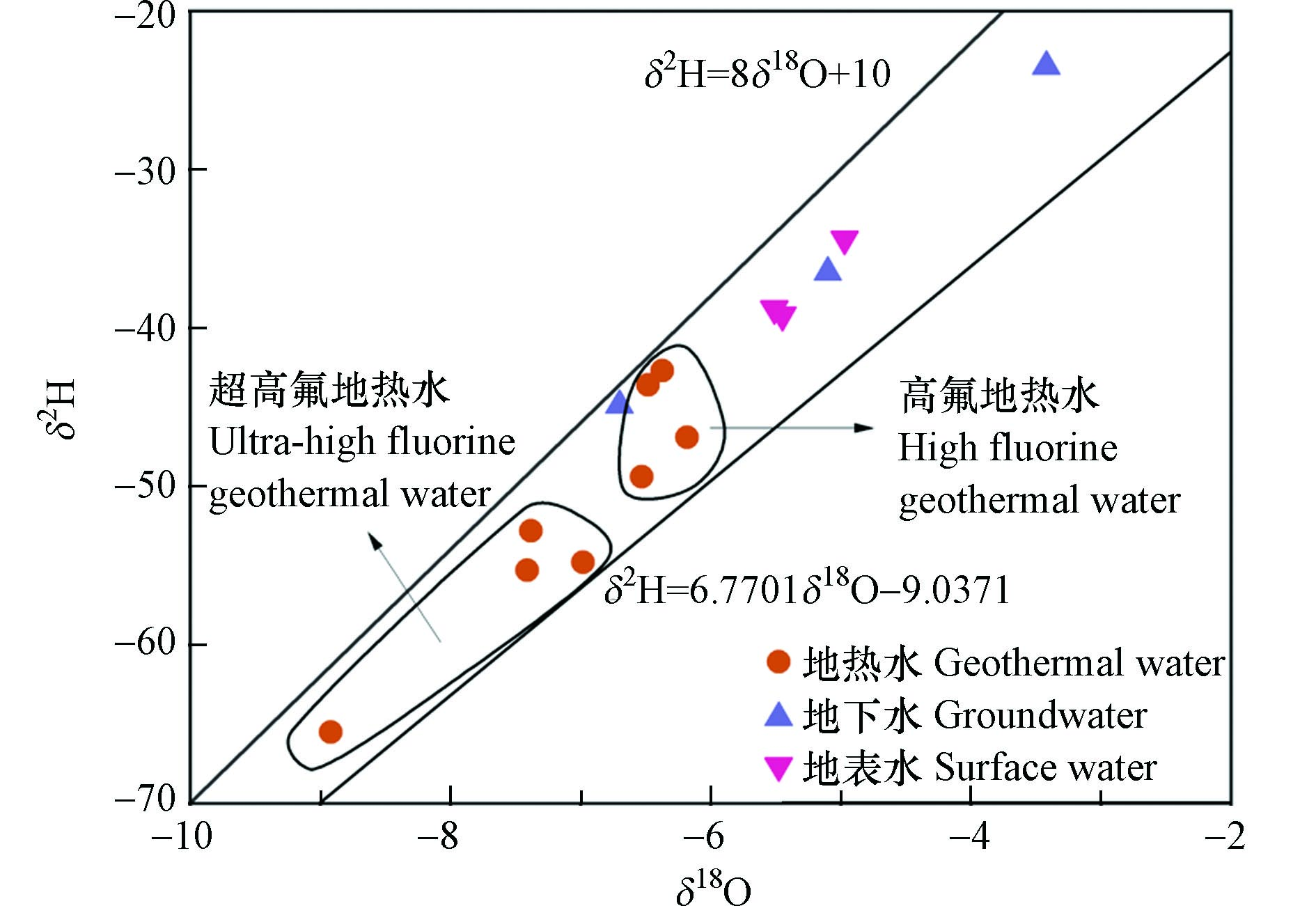
研究区地下热水的δ2H、δ18O含量分别为−65.5‰—−42.7‰和−8.92‰—−6.37‰,平均值分别为−51.38‰和−7.03‰; 而地下水与河水的δ2H、δ18O含量则相对较低,平均值分别为−36.22‰和−5.19‰. 高氟和超高氟地下热水的δ2H、δ18O平均含量分别为−45.65‰、−57.10‰和−6.39‰、−7.67‰,可以发现高氟地热水的δ2H、δ18O含量显著高于超高氟地热水.
将采集样点的数据投影在全球大气降水线GMWL:δ2H=8δ18O+10和当地大气降水线LMWL:δ2H=8δ18O+10[12]上. 由图3可以发现,所有地热水、地下水和地表水样点均偏离大气降雨曲线,表明研究区地热水存在轻微的“氧漂移”现象,这可能是由于地下热水受到了不同程度的蒸发及浓缩作用. 一方面,地表水受到强烈蒸发的影响导致δ2H和δ18O增加;另一方面,当地热水沿断层上升至地表时,围岩中的含氧矿物与地下水发生同位素交换反应,导致δ18O同位素消耗[13]. “氧漂移”现象表明地热水不是直接来源于大气降水,而是大气降水降落到高海拔地区后经过长时间的径流后形成的地热水. 高氟地热水的氢氧同位素值显著高于超高氟地热水主要可能存在两方面原因:一方面沿断裂带出露的地热水,氢氧同位素的值与循环深度大致成反比,因此可以推断超高氟地热水的循环深度更大,与围岩作用更充分导致更高的氟含量;另一方面高氟地热水位于滨海地带,含水层主要包括海相和河流相交互沉积层,地热水形成过程可能受到高δ2H、δ18O含量的地下水和海水影响,导致氢氧同位素含量高[14].
不同地区的大气降雨在形成的过程中的水气来源和周围环境的差异,导致了气、液同位素分馏的差异性,这种差异性被量化为氘过量参数. 1984年Dansgaard首次提出氘过量参数的概念,并且定义其公式为 d =δ2H−8δ18O [15]. 对于地热水的d值,其变化主要受到停留时间、围岩和水体的物理化学特征等的影响,一般d值越小,说明水文地质环境越封闭,地下水径流速度越慢,水岩相互作用程度更高. 研究区地热水的d值介于8.26‰和1.04‰之间,平均值为4.88‰,略低于地下水和地表水平均值5.32‰,表明地热水均是由当前气候条件下的大气降雨补给形成的. 地热水相对于地下水和地表水径流速度更慢,停留时间更长,与围岩中的含氟矿物相互作用程度更高,因此地热水的氟含量远高于地下水和地表水[16].
2.3 氟的富集过程
2.3.1 溶解沉淀作用
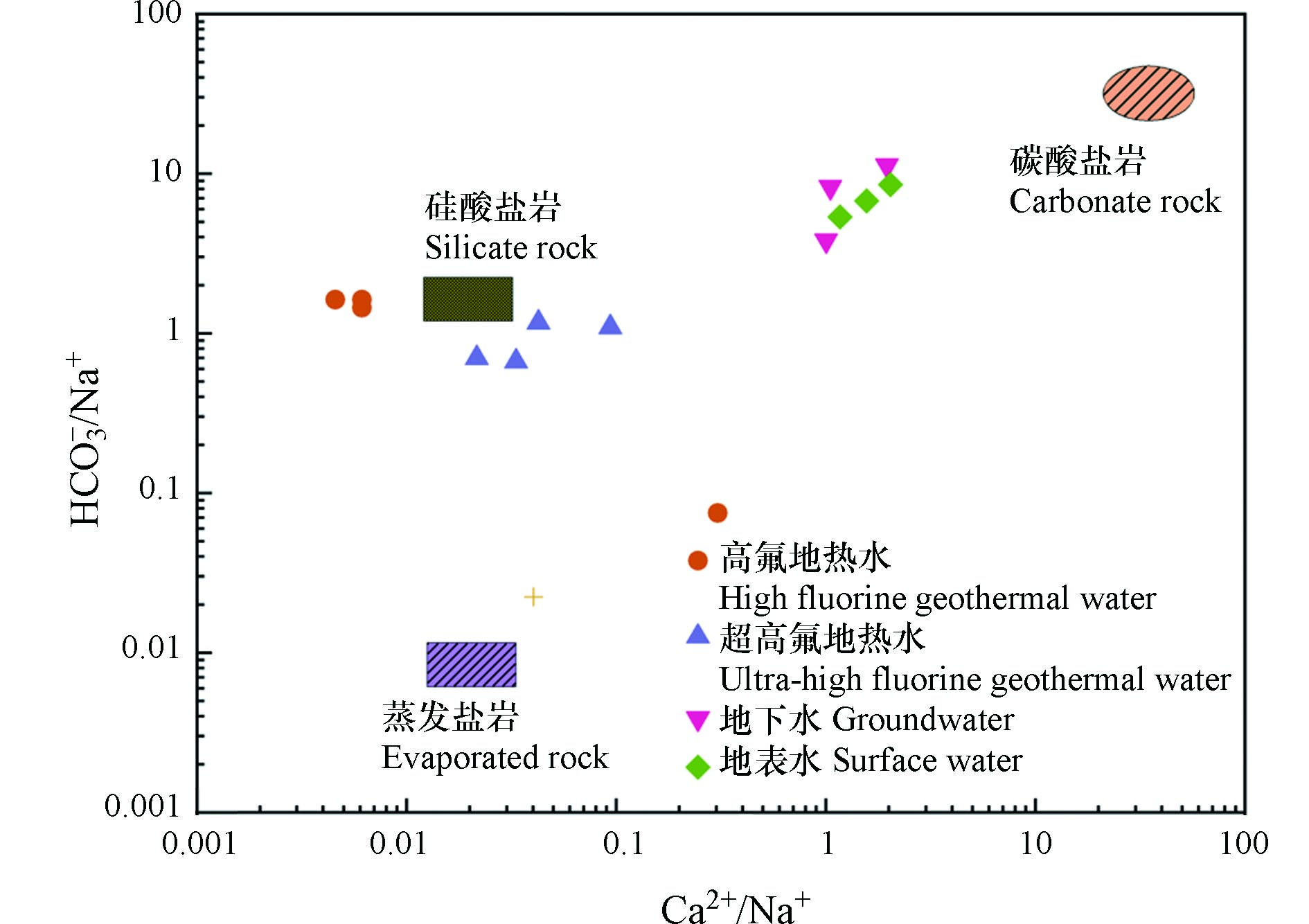
研究区地热水的补给主要为现代大气降水,补给后的水体经过沿断裂下渗至深部地热源进行加热,被加热后的热水向上渗流在盖层薄弱处出露地表[17]. 在地热水下渗、渗流、径流过程中,围岩矿物在水体中发生溶滤作用,围岩矿物中的氟多以难溶化合物的形式存在,主要包括萤石、氟磷灰石和黑云母[18]. 地热水中Ca2+/Na+、HCO
−3 萤石作为硅酸盐矿物中最主要的含氟矿物,含氟量高达48%[19];运用PHREEQC对地下热水中涉及氟富集矿物的矿物饱和指数(SI)计算,结果表明地热水中萤石、方解石、白云石均处于饱和状态,部分地下水中萤石处于非饱和状态. 涉及的相关反应为:
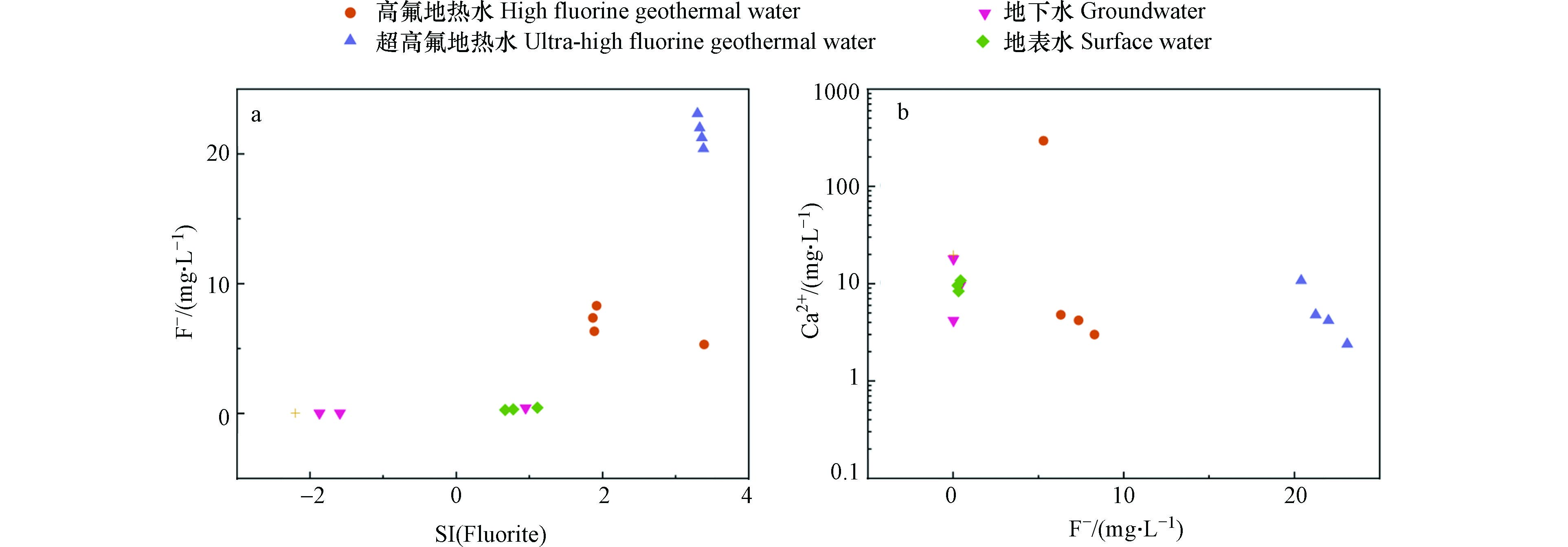
CaF2(萤石)=Ca2++2F− (1) Ca2++Mg2++2HCO3−+2OH−=CaMg(CO3)2↓(文石)+H2O (2) Ca2++HCO−3+OH−=CaCO3↓(方解石)+H2O (3) 一般情况下萤石十分稳定,当外部环境的条件发生变化时,含氟矿物的稳定性随之发生变化,矿物中的氟溶解进入水体中,这也是研究区地热水中氟浓度变化的主要影响因素[20]. 如图5所示,Ca2+和F−呈现出明显的负相关关系,而萤石的矿物饱和指数随F−浓度增加而增加. 地热水中的白云石、方解石的矿物饱和指数均大于0,水体中钙离子不断发生沉淀反应形成这两类矿物;进而Ca2+浓度降低,促进萤石发生溶解反应,水体中F−含量增加. 文石、方解石的沉淀促进了萤石的溶解,当萤石在水中溶解达到饱和状态时,固液两相之间的物质与能量交换处于平衡,并且共存于溶液中,达到动态平衡状态.
2.3.2 络合解离作用
在地下围岩矿物中,氟离子是一种非常活泼的离子,在一定条件下能够与矿物中的Al3+、Fe3+等一些金属水合离子发生配位体反应[21]. Al3+在研究区地热水中含量丰富,含量为3.60—133.00 μg·L−1, 均值为24.45 μg·L−1. 氟离子是除氢氧根之外和铝离子结合能力最强的离子,尤其是在酸性和中性条件下,能够形成大量的AlF、AlF2+、AlF4−等络合物. 在研究区弱碱性地热水的条件下,原有的络合-解离平衡会破坏,氟离子和Al-F络合物以及氢离子缔合的氟进行转化,进而导致地热水的氟浓度发生改变. 氟离子不仅能够和金属离子形成络合物,还能和土壤中的一些有机配位体形成各种络合物,包括氨基酸、碳水化合物和酚类物质等. 络合反应形成的络合物在流体中是具有可溶性和迁移性,并且能够增强研究区的含氟矿物溶解作用,导致氟浓度的增加.
2.3.3 离子交换作用
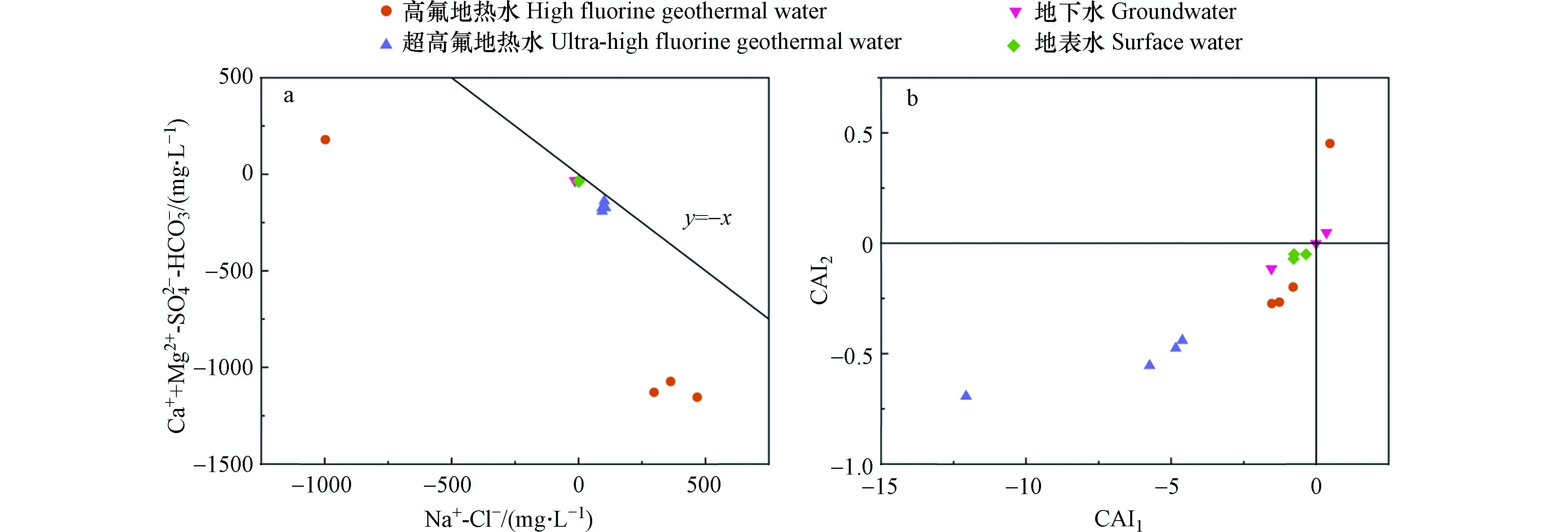
离子交换作用是影响地热水水化学组分的主要水文地球化学特征之一,离子比值法常用来判断地热水是否盛行离子交换作用. 当离子交换作用强烈时,Ca2++Mg2+-HCO
−3 2−4 CAI1=Cl−−Na+−K+Cl (4) CAI2=Cl−−Na+−K+HCO−3+SO2−4+CO2−3+NO−3 (5) 图6(b)表明研究区钠碱指数大多为负数,矿物中的Ca2+、Mg2+被Na+、K+置换出. 在离子交换作用的影响下导致研究区的Na+大量富集,Ca2+含量降低. Ca2+含量的降低促进了萤石的溶解,进而导致氟浓度的增加.
2.4 影响氟富集的因素
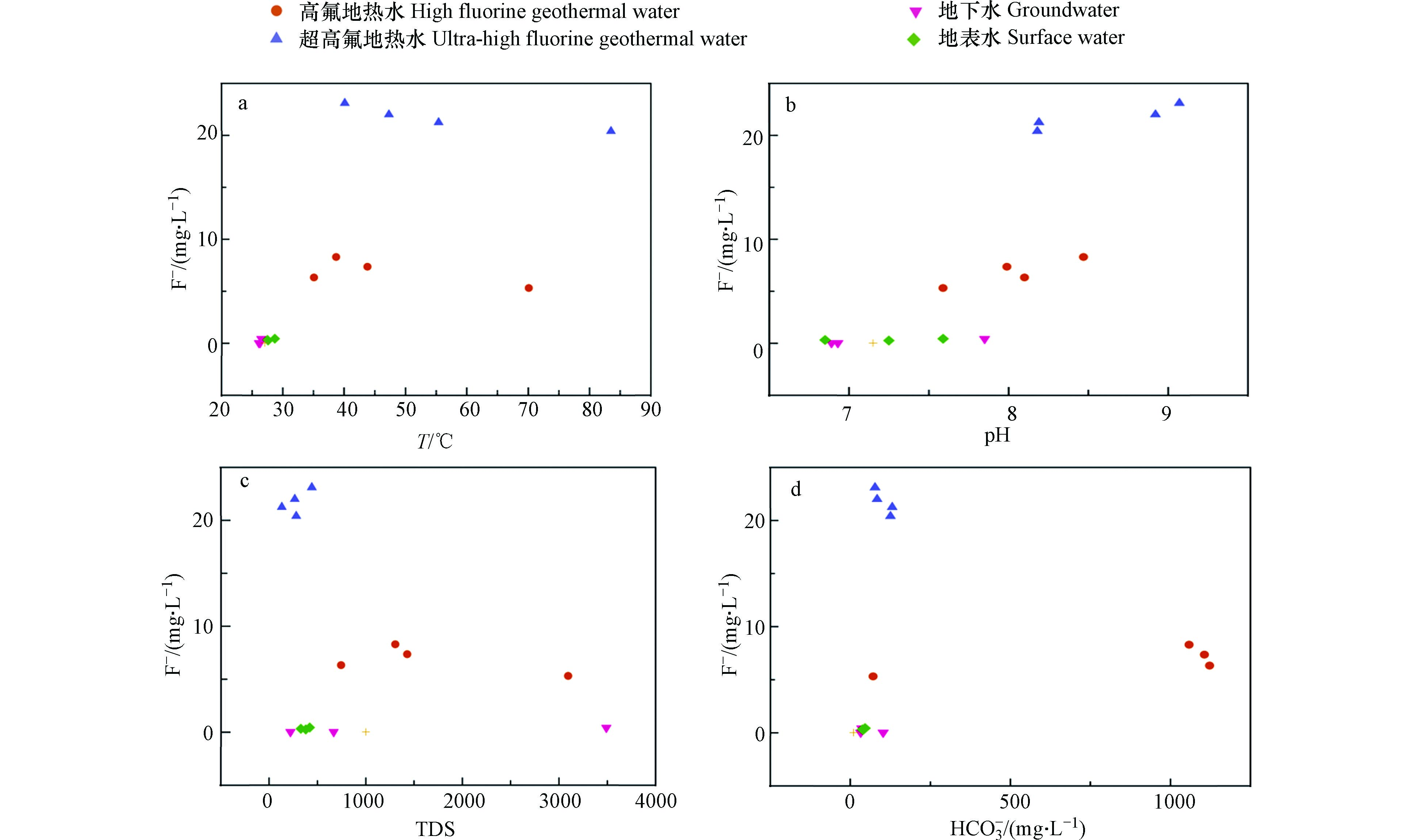
地下水中氟主要来源于围岩的矿物,而围岩矿物中氟进入地下水的过程受到多种因素的影响,对这类影响因素的分析能够进一步探究氟的富集规律. 在前人研究的基础上已经证实地下水中的氟含量和温度成正比关系,高温条件更有利于围岩中的含氟矿物的溶解,同时岩石、土壤表面大量吸附态的氟解吸进入地下水中,进而导致氟含量增加[23-24]. 图7(a)中表明温度更高的地热水的含氟量显著高于地下水和地表水,而地热水的含氟量和温度并未有明显相关性,这可能还和循环深度、水文地质封闭程度有关.
研究区地热水呈弱碱性,pH集中分布在8.5附近,该弱碱性环境更有利于F−的富集,而地下水和地表水约呈中性. 在弱碱条件下氟的赋存形态主要是氟离子,水体中大量的氢氧根离子和氟离子拥有相似的化学半径和电荷数,将取代围岩含氟矿物中的氟离子而使其进入水体,使水体中的氟含量增加. 如图7(b)所示,地热水中的氟含量随pH的增大而增大,而地下水中的氟含量几乎不受pH的影响;表明在地热水中pH是氟含量变化的控制因子,这与大部分地区的结果相一致[7,24]. 高氟地热水位于滨海地区,地层中存在相当厚度的盐岩层,导致高氟地热水的TDS含量显著高于超高氟地热水,其平均值分别为1644 mg·L−1和280 mg·L−1. 地热水氟含量和TDS相关性不大,表明蒸发浓缩等作用造成的TDS变化对琼北地区地热水氟含量影响不大. F−的化学性质相当活泼,能和诸多金属、非金属类元素作用形成化合物,因此地热水中的离子组分是影响氟含量变化的重要因素. HCO
−3 −3 −3 地热水中的氟主要来源于地下围岩中的含氟矿物中,地层的岩性是影响氟含量的分布重要因素. 高氟地热水分布于沿海地区,主要出露第四系砂岩、粉砂岩和粘土这类沉积岩. 沉积岩含氟量通常低于其它类型的岩石,其主要的含氟矿物为萤石、氟磷灰石,一般含氟量为220—940 mg·L−1 [26]. 超高氟地热水主要分布于内陆地区,岩性较为复杂,其主要出露年代较为古老的玄武岩、花岗岩等岩浆岩和变质岩,这类岩石的氟含量一般远高于沉积岩. 研究区北部大量出露的玄武岩中富含萤石、黑云母、角闪石和氟磷灰石等富氟矿物,变质岩广泛出露中部,出露的地热水具有更高的氟含量[20].
3. 结论(Conclusion)
(1)琼北地区地热水中的F−含量均超标,平均值高达14.25 mg·L−1;而地下水和地表水的F−含量未超标,变化范围为0.02—0.44 mg·L−1. 在空间分布上,由沿海地区到内陆地区F−含量呈现逐渐增大的趋势,尤其是内陆地区,平均含量为21.69 mg·L−1,远高于沿海地区地热水.
(2)研究区地热水水化学类型有HCO3-Na、SO4-Na、HCO3-Mg、Cl-Na,其中HCO3-Na是主要的水化学类型. pH、温度和地层中的含氟矿物类型对地热水中的氟富集过程有重要的影响.
(3)氢氧同位素数据表明研究区地下热水补给来源为现代大气降水,并且存在轻微的“氧漂移”现象,受到一定程度的蒸发浓缩的影响. 高氟地热水的氢氧同位素值显著高于超高氟地热水,可能是由于超高氟地热水的循环深度更大,与围岩作用更充分. 高氟地热水形成过程可能受到高含量的δ2H、δ18O地下水和海水影响,进而导致氢氧同为素含量更高.
(4)溶解沉淀作用、络合解离作用、离子交换作用是影响研究区F−富集的主要水文地球化学过程. 文石、方解石的沉淀反应、络合反应形成的络合物以及Na+、K+置换出Ca2+、Mg2+的离子交换反应,使得地热水中氟含量增加.
-

 点击查看大图
点击查看大图
计量
- 文章访问数: 2139
- HTML全文浏览数: 2139
- PDF下载数: 27
- 施引文献: 0





 下载:
下载: