-
厌氧氨氧化(anaerobic ammonium oxidation bacteria,anammox)自养生物脱氮工艺是以氨氮(NH4+-N)为电子供体,亚硝氮(NO2−-N)为电子受体的自养脱氮工艺[1],因其具有脱氮效率高、无需额外补充碳源等优点,在老龄垃圾渗滤液为代表的低C/N比污水脱氮处理中受到广泛关注[2, 3]。但anammox菌生长和富集速度缓慢,环境敏感性强[4],且垃圾渗滤液含有高浓度氨氮、有机物及重金属等污染物对anammox菌具有强烈抑制作用,使得anammox工艺在垃圾渗滤液脱氮应用中受到极大的制约。因此,寻找一种快速启动anammox的污泥接种策略,及实现anammox自养脱氮工艺在垃圾渗滤液处理过程中稳定运行的方法,对该自养工艺的工程化应用具有重大意义。
Anammox工艺的启动是淘汰劣势菌种,富集anammox菌的过程。有研究表明,混合接种反硝化污泥与anammox污泥能减少反应器启动所需时间,CHEN等[5]将接种反硝化污泥与接种Anammox污泥:反硝化污泥=1:3的混合污泥启动效果进行比较,发现接种反硝化污泥反应器氮去除速率达0.54 kg·(m3·d)−1需98 d,而后者氮去除速率达到0.55 kg·(m3·d)−1仅需40 d。但WANG等[6]接种厌氧颗粒污泥:anammox污泥=20:1启动反应器却未能成功,这可能与anammox污泥接种比例有关。因此,其他污泥与anammox污泥混合接种的比例对anammox反应器启动影响还有待深入探究。本研究将垃圾渗滤液常规处理中的短程硝化污泥、反硝化污泥以及实验室前期培养的anammox污泥为接种对象,探究一种最优的污泥接种策略来减少anammox工艺启动时间。此外,由于anammox工艺在实际处理垃圾渗滤液时,往往受到渗滤液中NH4+-N,NO2−-N和有机污染物浓度变化影响,导致anammox脱氮效果降低[7, 8]。其中,垃圾渗滤液中NH4+-N对anammox活性的影响主要源于游离氨(free ammonium,FA),JUNG等[9]a研究中发现当进水FA达到1.7 mg·L−1以上时开始对anammox产生抑制,当FA达到32 mg·L−1时anammox会完全停止反应。而垃圾渗滤液中NO2−-N本身具有一定的生物毒性,STROUS等[10]发现当NO2−-N质量浓度超过100 mg·L−1时anammox反应会受到抑制,且在该浓度下持续12 h会完全失活。高浓度有机污染物会造成反应器anammox种群丰度下降,TANG等[11]探究有机物对anammox长期运行影响中发现当进水中COD达800 mg·L−1时,有机环境中的anammox活性仅为无机环境的1/4,反应器内异养菌丰度大幅度提高。因此,在anammox自养脱氮工艺实际应用中,需要一种能维持anammox高效脱氮性能,保证anammox菌在反应器中始终占据主导地位的方法。联氨(N2H4)是anammox反应过程的中间产物,可在联氨脱氢酶的作用下转化为N2,该过程中释放的部分电子会用于ATP的合成[12],适量投加N2H4可强化anammox脱氮性能[13],但N2H4也是一种强还原剂,具有生物毒性,过量投加反而会抑制Anammox反应[14]。目前对N2H4研究主要集中在污染物浓度较低的水体(如模拟废水或城市污水)中anammox的反应过程和活性恢复方面。如MIODONSKI等[15]在污泥消化废水中通过投加N2H4促进Anammox活性,投加N2H4反应器的氮去速率较未添加N2H4的对照组高出0.256 kg·(m3·d)−1。而如何通过N2H4促进anammox菌快速适应高污染及生物抑制性强的垃圾渗滤液,以及其对渗滤液中脱氮菌群活性变化的影响研究却鲜有报道。
鉴于此,本研究在选择出anammox工艺最优污泥接种启动策略的基础上,讨论N2H4在anammox工艺中对垃圾渗滤液脱氮的影响,通过对比运行中的脱氮性能、比厌氧氨氧化活性、胞外聚合物以及微生物群落结构变化等,以确定促进anammox运行的最适N2H4浓度。结合最优污泥接种策略与适合的N2H4浓度实现anammox在垃圾渗滤液中的快速启动以及长期稳定运行,解决anammox工艺受垃圾渗滤液抑制脱氮性能不佳的困扰,为该工艺在实际工程运用中提供科学的技术支持。
-
实验一:采用序批式反应器(sequencing batch reactor,SBR)对anammox快速启动最优污泥接种策略进行研究,如装置图1(a)所示。反应器采用容积为1 L的柱状玻璃瓶,外缠遮光布,内置磁力转子,顶口由橡胶塞密封,橡胶塞顶部设进/出水口。运行周期为24 h,其中进水0.5 h、搅拌22 h、沉淀1 h、排水0.5 h,搅拌速度90 r·min−1,水浴保温在(30±1) ℃下运行。
实验二:采用升流式厌氧污泥床反应器(up-flow anaerobic sludge bed reactor,UASBR)探究不同N2H4浓度对anammox工艺垃圾渗滤液脱氮稳定性的影响,装置如图1(b)所示。反应器内径6 cm,高45 cm,有效容积为1.2 L,外设水浴保温层调节温度为(30±1) ℃,水力停留时间为24 h。
-
实验一:进水采用模拟废水,NH4+-N和NO2−-N来自NH4Cl及NaNO2,质量浓度分别为(35±5) mg·L−1和(45±5) mg·L−1,其他主要成分:MgSO4·7H2O(0.3 g·L−1)、CaCl2(0.0056 g·L−1)和KH2PO4(0.01 g·L−1);微量元素Ⅰ (1 mg·L−1)和微量元素Ⅱ (1 mg·L−1)[16]。
实验二:anammox无法独立处理仅含氨氮的垃圾渗滤液,需要与短程硝化工艺耦合,将NH4+-N部分转化为NO2−-N,以满足anammox工艺对进水中NO2−-N与NH4+-N比例要求。因此,本实验将经短程硝化反应后的渗滤液作为处理对象。采用模拟废水与短程硝化出水渗滤液混合并逐步提高渗滤液占比的进水方式,最后完全以短程硝化出水渗滤液为进水。其中短程硝化出水渗滤液来自于佛山市某中试短程硝化反应器。
-
Anammox工艺快速启动最优污泥接种策略,所接种短程硝化污泥与反硝化污泥均来自于广东省佛山市某中试工程硝化池与反硝化池;anammox颗粒污泥由实验室前期培养,污泥颜色呈红棕色。实验采用5个反应器分别接种短程硝化污泥;反硝化污泥;短程硝化污泥:anammox颗粒污泥(W:W)=9:1;反硝化污泥:anammox颗粒污泥(W:W)=9:1;短程硝化污泥:反硝化污泥:anammox颗粒污泥(W:W)=4.5:4.5:1,其中W表示接种污泥浓度(MLVSS),反应器MLVSS为(3 000±100) mg·L−1,反应器命名为A1、A2、A3、A4、A5。
探究不同N2H4浓度对anammox工艺垃圾渗滤液脱氮稳定性的影响,采用反硝化污泥:anammox颗粒污泥(W:W)=9:1的接种策略,根据N2H4浓度将反应器命名为B1、B2、B3、B4、B5。各反应器进水条件相同,设置独立进水桶,进水桶中N2H4浓度每日根据实验要求进行配置,分别为0、3、6、9、12 mg·L−1,反应器MLVSS均为(10 000±800) mg·L−1。
-
NH4+-N、NO2−-N、NO3−-N、MLSS、MLVSS根据《水和废水监测方法》标准方法测定[17],pH和DO采用便携式水质多参数测定仪(上海SANXIN-SX825)测定。
比厌氧氨氧化活性(Specific anammox activity,SAA)分析方法:当每阶段连续7 d过程中TN去除率波动在±5%以内时,认为该阶段已达到稳定,通过批次实验测定SAA,测定前反应器污泥用0.1 M磷酸盐缓冲溶液清洗3次,随后加入相应阶段渗滤液进水,pH调节至7.5,温度为(30±1) ℃,反应器关闭进水仅开启内循环。间隔取样分析,根据式(1)计算SAA。
式中:k为厌氧氨氧化菌的厌氧氨氧化活性,kg·(kg·d)−1;ci为氮浓度变化(NH4+-N、 NO2−-N),mg·L−1;w为污泥浓度(MLVSS),g·L−1。
污泥胞外聚合物(extracellular polymeric substance,EPS)采用热提法提取,EPS中的多糖和蛋白质分别用考马斯亮蓝法和蒽酮—硫酸法测定[18-19],污泥EPS中的有机物变化通过三维激发发射矩阵(three-dimensional fluorescence spectrum,3D-EEM)荧光光谱法测定。
微生物群落结构分析,DNA提取由北京百迈克生物公司完成,选用16S rRNA高可变区V3~V4进行扩增,用通用引物27F(5'-AGRGTTTGATYNTGGCTCAG-3')和1492R(5'-TASGGHTACCTTGTTASGACTT-3')进行PCR扩增,最后采用PacBio测序平台完成测序,并将微生物DNA序列上传至NCBI,BioProject accession number :PRJNA948566。
-
A1~A5脱氮效果如图2所示,本实验中根据NH4+-N、NO2−-N的进/出水质量浓度变化将启动过程分为菌体自溶期、活性迟滞期、活性提升期等3个时期[20]。首先,菌体自溶期的主要表现为出水NH4+-N浓度增加甚至高于进水。由图2(a)可见,A1、A2、A5接种污泥启动初期出现明显菌种自溶现象,即出水NH4+-N质量浓度高于进水。而A3、A4接种污泥菌种自溶程度较低,出水NH4+-N质量浓度虽然有升高趋势,但始终低于进水。汪瑶琪等[21]的研究也发现反应器接种污泥启动初期存在菌体自溶现象,出水中NH4+-N浓度高于进水。这是因为接种污泥中不能适应自养环境的菌体死亡后溶解释放一部分NH4+-N[22],导致反应器中出水NH4+-N质量浓度高于进水。当接种污泥适应环境后,菌体结束自溶进入活性迟滞期,表现为出水NH4+-N质量浓度低于进水且缓慢降低,并伴有NO2−-N的少量去除。关于anammox的启动研究中菌体自溶期、活性迟滞期普遍出现,如何快速度过这2个关键时期是anammox快速启动的关键[23, 24]。
A1(短程硝化污泥)、A2(反硝化污泥)采用单一污泥来源接种启动的菌种自溶期时长分别为25 d、39 d。A1在第26天进入活性迟滞期,出水中NH4+-N较之前有所下降,但NO2−-N、NO3−-N持续增长,直至实验运行结束,A1未见有明显厌氧氨氧化反应,TN去除率仅为4.1%。而A2在第40天进入活性迟滞期,直至运行结束时也未能进入活性提升阶段,运行末期的TN去除率保持在8%左右。上述结果表明,A1与A2采用单一短程硝化或反硝化污泥的接种策略无效。与A1、A2相比,接种少量anammox颗粒污泥A3、A4、A5均能进入活性提升期,菌体自溶期和活性迟滞期总耗时长顺序为A5(42 d)>A3(30 d)>A4(28 d)。这一结果表明,接种10%的anammox颗粒污泥能快速度过菌体自溶和活性迟滞阶段,加速anammox启动。这是因为anammox菌较其他菌种更适应无机环境,在接种初期可快速富集,反应器能更快表达厌氧氨氧化活性。
A3、A4、A5进入活性提升期后,微生物已经适应环境,厌氧氨氧化活性逐渐增强,活性提升期的表现为出水NH4+-N、NO2−-N快速降低,TN去除率逐渐升高。在运行100 d后发现,A3、A4、A5的TN去除率分别提升至62.5%、75.1%、47.8%。其中采用反硝化污泥:anammox颗粒污泥(W:W)=9:1接种策略的A4不仅菌体自溶期和活性迟滞期总耗时最短(28 d),较A3、A5分别少2 d、14 d,而且进入活性提升期后A4的TN去除效果最佳,比A3、A5分别高出12.6%、27.3%。这是因为A4接种污泥中反硝化菌的存在极大的促进了anammox活性表达[25]。
-
实验一结果表明,反硝化污泥:anammox颗粒污泥(W:W)=9:1为最优污泥接种策略,基于此结果进行不同浓度(0、3、6、9、12 mg·L−1)N2H4对垃圾渗滤液中anammox脱氮稳定性的影响研究,实验共分5个阶段(表1)。阶段Ⅰ进水方式采用模拟废水与垃圾渗滤液混合,通过逐步提高进水NH4+-N、NO2−-N浓度,考察不同浓度N2H4对anammox的耐氮负荷冲击能力的影响。阶段Ⅱ~Ⅳ逐步提高进水中垃圾渗滤液的占比,探究不同浓度N2H4对anammox垃圾渗滤液脱氮稳定性的影响。阶段Ⅴ停止投加N2H4,观察无N2H4影响下的脱氮性能变化。
如图3所示,阶段Ⅰ第1~12天进水TN平均质量浓度为140.1 mg·L−1时,各反应器运行稳定,TN平均去除率均在90%以上,表明该阶段中垃圾渗滤液未对anammox产生明显抑制。但在第13~24天,进水TN质量浓度提高到200.0 mg·L−1以上时,各反应器脱氮性能骤降,第18天B1~B5反应器的TN去除率分别降至32.5%、33.6%、41.7%、37.9%、39.0%,表明该阶段的anammox脱氮性能主要受到进水基质浓度变化的影响。其中,未添加N2H4的anammox反应器B1的TN去除率降幅明显,且活性恢复缓慢,直到第24天的TN去除率仅恢复至60.6%。同期投加N2H4的反应器均已恢复至80%以上,特别是添加3 mg·L−1的N2H4反应器表现最佳,TN去除率由33.6%恢复至83.2%。第42天后,进水TN质量浓度达230.0 mg·L−1以上,未添加N2H4的B1及添加高浓度N2H4的B4与B5脱氮效果随进水总氮浓度提升而下降,TN平均去除率为62.8%、65.2%和44.9%。而添加低浓度N2H4的B2和B3脱氮效果则较为稳定,后续TN平均去除率为83.4%和81.7%,较未添加N2H4的B1高出20.6%和18.9%。上述结果表明,适量N2H4(3、6 mg·L−1)能削弱进水基质的抑制,加速活性恢复,保证运行稳定,而高浓度N2H4对微生物有明显的抑制效果,会阻碍anammox反应的进行,降低脱氮效果。
阶段Ⅱ~Ⅳ提高进水中垃圾渗滤液比例时,有机物和毒性物质浓度激增,微生物受到抑制,导致阶段Ⅱ~Ⅳ初期各反应器脱氮效果短期下降。未添加N2H4的B1在阶段Ⅱ~Ⅳ稳定运行时的TN平均去除率为61.8%、62.5%、61.7%,与阶段Ⅰ(61.9%)相差不大,表明B1已适应垃圾渗滤液水质,但未能有良好脱氮效果。添加高浓度N2H4的B4与B5受较高N2H4浓度与垃圾渗滤液的共同抑制,脱氮效果低于未投加N2H4的B1,阶段Ⅱ~Ⅳ的TN平均去除率分别为69.8%、26.3%、53.9%与48.6%、12.2%、20.8%。而添加低浓度N2H4的B2与B3较同阶段未添加N2H4的B1有更良好的脱氮性能,阶段Ⅱ~Ⅳ的TN平均去除率分别达到85.9%、81.6%、75.5%和84.4%、82.1%、90.6%。值得一提的是,N2H4质量浓度为6 mg·L−1的anammox反应器能在完全以垃圾渗滤液为进水,TN负荷为338.3 g·(m3·d)−1时,TN平均去除率达90.6%,较杨盈盈等[26]在相似渗滤液水质中的anammox脱氮效果有显著提升(TN负荷为15.4 g·(m3·d)−1时,TN平均去除率为67.7%)。上述结果表明6 mg·L−1的N2H4可较好地削弱渗滤液抑制效果,能促进anammox在垃圾渗滤液中稳定脱氮。
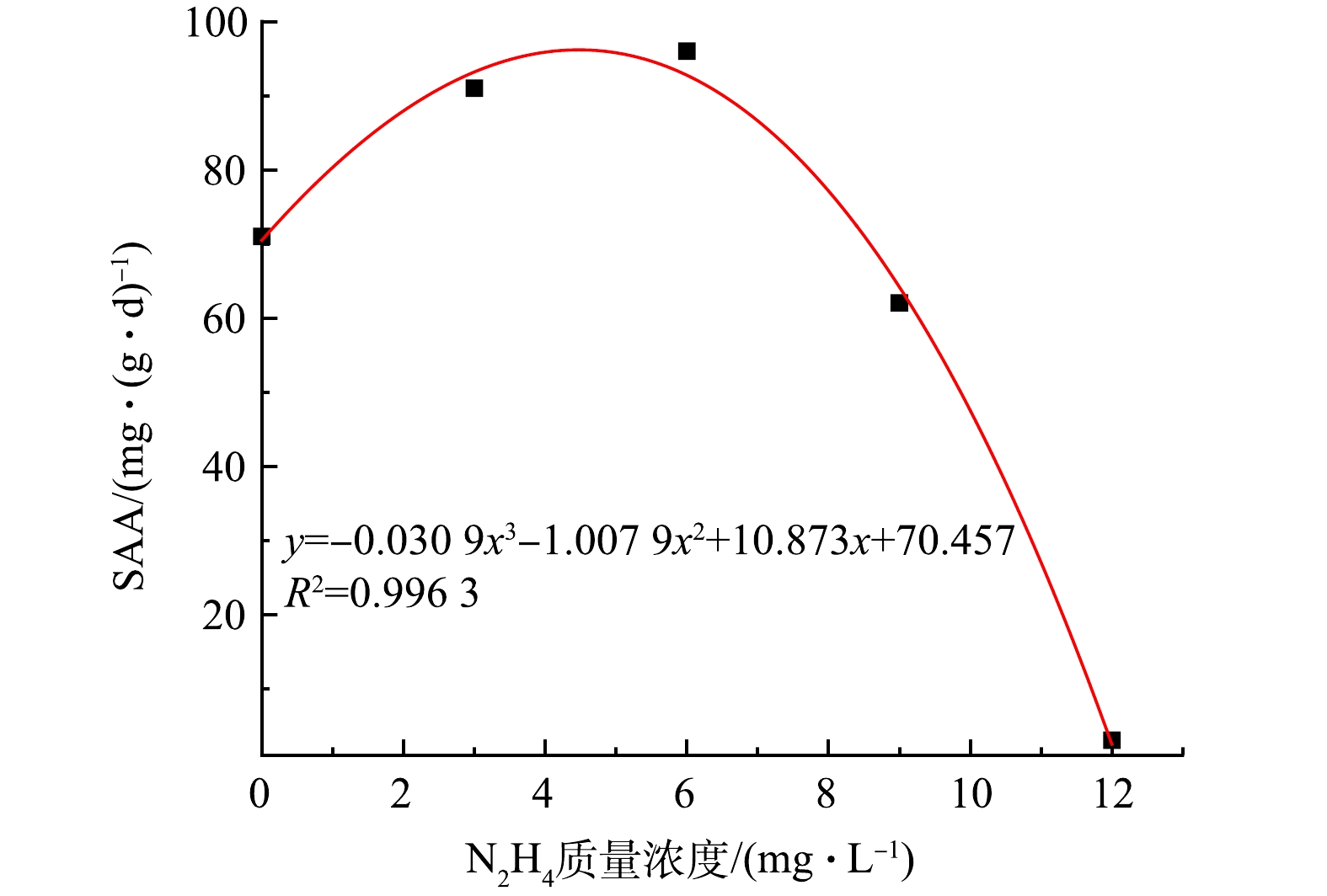
本研究中,适宜N2H4浓度对anammox脱氮性能产生较好的促进作用,而12 mg·L−1的N2H4对anammox产生明显的抑制效果,其原因在于以下3点:1)外源N2H4能通过式(2)所示反应被anammox菌氧化利用[27],从而释放电子参与ATP的合成,为anammox菌的代谢提供能量,强化anammox菌对NH4+-N、NO2−-N去除;2)N2H4具有一定的生物毒性,但由于N2H4是anammox菌脱氮过程的中间产物,因此,与其他菌种相比,anammox菌对N2H4毒性有更强耐受性,适宜浓度的N2H4可实现强化anammox菌的同时抑制其他异养微生物的生长,减少底物竞争;3)但anammox菌对N2H4毒性耐受能力有限,超过阈值水平会抑制anammox过程。不少学者[28-29]已对N2H4浓度影响anammox动力学进行分析。蔡庆等[30]研究发现anammox反应中N2H4的半饱和质量浓度为0.68 mg·L−1,抑制质量浓度为26.96 mg·L−1。而本实验中,由图4中的拟合结果可知,N2H4促进anammox的半饱和质量浓度约为1.4 mg·L−1,N2H4的半抑制质量浓度在8~12 mg·L−1,因此,N2H4质量浓度为12 mg·L−1的anammox反应器受抑制效果显著。这与鲍林林等[31]的研究结果相似,当N2H4质量浓度由4 mg·L−1提升至10 mg·L−1后,反应器TN平均去除率由60%降至35%。
阶段Ⅴ停止投加N2H4后,添加N2H4的B2~B5反应器脱氮性能出现明显下降,但随后脱氮效果均有所恢复。特别是N2H4浓度为6 mg·L−1的B3反应器脱氮性能恢复较快,仅历时4 d,TN去除率由64.2%恢复到了81.3%,且后续阶段Ⅴ第230~252天内反应器脱氮性能稳定,TN平均去除率为87.0%,较阶段Ⅳ时的90.6%仅下降了3.6%。而添加高浓度N2H4的B4与B5停止投加N2H4后,厌氧氨氧化活性恢复较慢,直至第252天,TN去除率分别由39.3%和20.7%升至71.9%和73.7%。N2H4质量浓度为6 mg·L−1的反应器停止投加N2H4后依然能达到85%以上的脱氮率。这是由于anammox反应器在阶段Ⅰ~Ⅳ内,微生物在N2H4影响下,已经适应高毒性的垃圾渗滤液水质,并通过N2H4确保反应器中anammox菌占据优势地位。因此,停止投加N2H4后反应器仍具有较高anammox活性可实现垃圾渗滤液NH4+-N与NO2−-N的同步去除。
上述结果表明,通过结合最优污泥接种策略及适量投加N2H4可实现垃圾渗滤液anammox工艺的快速启动及稳定运行,因此,本研究对anammox在高生物抑制性的垃圾渗滤液及低C/N废水自养脱氮处理中具有较高的实际工程应用价值。但本研究也存在一定不足,未对反应过程中的N2H4浓度实时检测。这是由于本实验开展于中试工程现场,实验设备条件有限,仅可通过紫外可见分光光度计测量N2H4浓度,但渗滤液的较高色度会对N2H4浓度测定结果准确性有较大影响,不利于对反应过程中N2H4的消耗及生成进行分析。未来研究中可通过联氨探针或联氨分析仪等设备探索适宜垃圾渗滤液中的N2H4浓度测试方法,进一步揭示渗滤液中N2H4对anammox的促进或抑制机理。
-
垃圾渗滤液中的有机物会促使反硝化菌快速繁殖,其细胞产率高于厌氧氨氧化菌,大量繁殖后会与anammox菌争夺基质,影响anammox脱氮效果,并出现NO2−-N去除量、NO3−-N生成量偏离anammox理论值的情况[32]。N2H4对亚硝酸盐氧化菌和反硝化菌有一定抑制效果,能提高anammox活性的同时减少NO3−-N生成,影响anammox氮素转化比例,其对渗滤液中anammox反应化学计量比影响如表2所示。
根据式(3)可知,anammox过程中ΔNO2−-N/ΔNH4+-N的理论值为1.32,ΔNO3−-N/ΔNH4+-N为0.26,但实际运行中会因为反硝化去除部分NO2−-N、NO3−-N而导致ΔNO2−-N/ΔNH4+-N及ΔNO3−-N/ΔNH4+-N与理论值出现偏差,根据偏差情况可以判断各反应器中反硝化的脱氮贡献占比大小。由表(2)可知,未添加N2H4的anammox反应器B1在阶段Ⅰ~Ⅴ的ΔNO2−-N/ΔNH4+-N均大于理论值1.32,ΔNO3−-N/ΔNH4+-N低于理论值0.26,而阶段Ⅰ~Ⅳ投加N2H4反应器的ΔNO2−-N/ΔNH4+-N均低于未添加N2H4的anammox反应器,表明添加N2H4的anammox反应器B2~B5中反硝化的脱氮贡献占比低于未投加N2H4的B1,而阶段Ⅴ停止投加N2H4后,B2~B5的ΔNO2−-N/ΔNH4+-N有所升高,最终高于理论值1.32,表明无N2H4抑制的情况下,反硝化活性有所提升,消耗了更多的NO2−-N。而ΔNO3−-N/ΔNH4+-N在N2H4投加时期(阶段Ⅰ~Ⅳ)低于理论值0.26,这是因为投加N2H4减少NO3−-N的生成。已有研究[33]证实外源N2H4可直接参与anammox反应过程,外源N2H4在联氨脱氢酶的作用下释放电子强化anammox菌的增殖;同时外源N2H4可对anammox菌合成代谢消耗电子进行补充,减少anammox副产物NO3−-N生成。由图3(c)可知,本研究也出现相似变化,添加外源N2H4的反应器出水NO3−-N质量浓度低于未添加N2H4的对照组B1。各反应器的化学计量比变化表明,长期运行中投加N2H4对反硝化菌有一定抑制效果,可以保证anammox的主导地位,并减少NO3−-N的生成量。
-
各阶段不同N2H4浓度的anammox反应器SAA变化情况如图5所示。受垃圾渗滤液影响,未添加N2H4的Anammox反应器B1的SAA整体呈下降趋势,由阶段Ⅰ的0.071 kg·(kg·d)−1(以VSS计)降至阶段Ⅴ的0.059 kg·(kg·d)−1。受高浓度N2H4影响,N2H4质量浓度分别为9 mg·L−1和12 mg·L−1的anammox反应器各阶段SAA均低于未添加N2H4的anammox反应器,阶段Ⅴ停止N2H4投加后,9 mg·L−1和12 mg·L−1的anammox反应器的SAA由阶段Ⅳ的0.031 kg·(kg·d)−1和0.008 kg·(kg·d)−1快速恢复到0.054 kg·(kg·d)−1和0.029 kg·(kg·d)−1,表明高浓度N2H4对anammox活性抑制效果显著。但N2H4质量浓度为3 mg·L−1和6 mg·L−1的反应器在阶段Ⅰ~Ⅳ的anammox活性明显提高,SAA均高于未添加N2H4的anammox反应器。其中N2H4浓度为6 mg·L−1的anammox反应器的SAA在各阶段均高于其他反应器,且始终保持增长趋势,由从阶段Ⅰ时0.096 kg·(kg·d)−1提升到阶段Ⅳ的0.143 kg·(kg·d)−1,较同阶段未添加N2H4的anammox反应器高出134.4%,停止投加N2H4后也能保持最高活性,阶段Ⅴ的SAA达0.118 kg·(kg·d)−1。上述结果表明,适量N2H4可有效提高anammox反应器的SAA,其中以6 mg·L−1的N2H4对anammox反应器的SAA提升效果最为显著,同时高浓度N2H4(9、12 mg·L−1)对SAA的抑制是可逆的。鲍林林等[31]研究中发现向HABR-CANON反应器中投加10 mg·L−1的N2H4后TN去除率降至35%,停止投加N2H43 d后,TN去除率恢复至84.7%,实现高浓度N2H4抑制后的活性恢复。
-
接种污泥中的EPS含量为12.8 mg·g−1(以VSS计),PN和PS分别为7.2 mg·g−1和5.6 mg·g−1,PN/PS为1.29。由图6可见,阶段V不同N2H4浓度的anammox反应器污泥EPS浓度较接种污泥有显著增长,分别提高了107.0%、142.9%、164.8%、92.2%、61.7%,其中N2H4质量浓度为6 mg·L−1的anammox反应器中EPS提升最大。同时,anammox污泥的EPS提高主要以PN含量增长为主,B1~B5的anammox反应器中PN含量分别增长至15.5、18.3、21.5、16.9、15.5 mg·g−1。
PN携带正电荷,可有效减少污泥表面负电荷,降低静电斥力,使增加细胞表面的疏水性,有利于微生物的聚集,因此PN含量提高表明各反应器anammox污泥颗粒化程度增强[34]。然而,B1~B5的anammox反应器相较于PN含量增长,PS含量增长较少。其中B1~B4的PS含量由5.6 mg·g−1分别增长至阶段V的11、12.8、12.4、7.7 mg·g−1,B5反应器PS含量先上升后下降,最高在阶段Ⅱ达到7.6 mg·g−1,最后降至阶段V的5.2 mg·g−1。PN为疏水性物质,PS为亲水性物质,anammox污泥EPS中PN/PS上升说明污泥相对疏水性提高,anammox污泥颗粒化程度得到了增强[35],本实验不同N2H4浓度的anammox反应器污泥EPS中PN/PS的比值随N2H4浓度增加而增加,N2H4质量浓度分别为0、3、6、9及12 mg·L−1时,PN/PS为1.41、1.43、1.73、2.19及2.98。上述结果表明,N2H4的补充不仅能促进anammox污泥EPS中PN含量的增加,且能有效提高PN/PS的比值,从而促进反应器中污泥的颗粒化,使污泥沉降性能逐渐增强[36]。
由于anammox菌分泌的EPS含有荧光特性,可以利用三维荧光法分析EPS的组成,接种污泥和不同N2H4浓度的anammox反应器阶段Ⅴ的三维荧光光谱如图7所示。荧光谱图中主要包含4个特征峰:A峰Ex/Em位于280~290 nm/335~370 nm,为溶解性微生物副产物;B峰Ex/Em位于300~320 nm/425~455 nm和C峰Ex/Em位于340~360 nm/435~455 nm,为腐殖酸类;D峰Ex/Em位于220~235 nm/290~325 nm,为酪氨酸蛋白类物质[37]。
由图7可观察到B1~B5的anammox反应器污泥EPS中A峰荧光强度均为最强,表明溶解性微生物副产物为EPS的主要成分。B峰和C峰为腐殖酸,可能来源于EPS对垃圾渗滤液中有机物的吸附,长期处理垃圾渗滤液后,各anammox反应器中的B峰和C峰荧光强度均有所增加。而anammox反应器污泥EPS中新出现的酪氨酸蛋白类物质(D峰),该物质有利于污泥聚集[38],各反应器D峰荧光强度较接种污泥均有显著增强,表明较接种污泥各反应器的污泥颗粒化程度有所增强。其中N2H4质量浓度为6 mg·L−1的anammox反应器中的D峰荧光强度最高,表明此浓度下的N2H4对促进EPS及酪氨酸蛋白类物质分泌效果最佳[39]。
-
由表3结果可知,生物样品中的覆盖率(coverage)均大于98%。B1~B5反应器相较于接种污泥,operational taxonomic units (OTUs)数明显增长。此外,Simpson指数、Shannon指数、Ace指数和Chao1指数在处理垃圾渗滤液后均增长。上述结果表明,垃圾渗滤液的复杂水质对微生物群落多样性有一定促进作用,可构成更适应垃圾渗滤液水质的脱氮微生物种群体系。
图8(a)为接种污泥和阶段V时不同N2H4浓度的anammox反应器门水平上微生物群落结构分布。结果表明,接种污泥门水平的微生物主要包括变形菌门(Proteobacteria)、栖热菌门(Deinococcota)、拟杆菌门(Bacteroidota)、浮霉菌门(Planctomycetes),相对丰度分别为75.9%、10.7%、9.5%、2.0%。而在阶段Ⅴ时,不同N2H4浓度的anammox反应器中的浮霉菌门及拟杆菌门相对丰度有显著提高,B1~B5的浮霉菌门相对丰度由接种污泥的2%分别提高至8%、8.6%、11.9%、9.0%和2.9%,拟杆菌门由9.5%分别提升至39.4%和37.1%、45.1%、42.0%和53.5%。但B1~B5反应器中的变形菌门相对丰度大幅下降,由接种污泥的75.9%分别降至23.1%、19.1%、13.2%、11.6%和13.8%。上述结果表明,6 mg·L−1的N2H4能更好的提高浮霉菌门的相对丰度[40]。此外,与接种污泥相比,不同N2H4浓度的anammox反应器中新检测出了髌骨菌门(Patescibacteria)及绿弯菌门(Chloroflexi)。髌骨菌门在B1~B5中的相对丰度分别为12.9%、15.1%、9.4%、14.3%和9.2%,髌骨菌门在anammox系统中为共存细菌提供乳酸盐和甲酸盐,促进厌氧氨氧化菌生长,对anammox系统稳定起到重要作用[41]。而绿弯菌多为丝状菌可以增强anammox菌的聚集,且绿弯菌会则利用死亡细胞作为碳源,减轻凋亡细胞组织对anammox菌的影响,在anammox菌与异养菌之间产生负相互作用时保持anammox系统功能稳定[42]。
属水平菌群结构分析,图8(b)为接种污泥和阶段V时不同N2H4浓度的anammox反应器属水平上微生物群落结构分布。各反应器浮霉菌门中的Candidatus Kuenenia成为优势菌,其为anammox反应器中最常见菌属[43]。有研究表明该菌属为淡水中最嗜盐菌属,一定程度上的盐度提升有利于其丰度增长[44],本研究中逐步提升垃圾渗滤液浓度的过程致使盐度增加,这可能是该菌属占比较大的原因,其在B1~B5的相对丰度为4.2%、5.5%、10.6%、5.8%和2.1%,较接种污泥中的0.2%有显著提升,N2H4浓度6 mg·L−1的条件下,Candidatus Kuenenia丰度提升最为明显,表明6 mg·L−1的N2H4促进anammox的生长效果最佳。而12mg·L−1的N2H4浓度的Candidatus Kuenenia丰度最低,可能是过量N2H4抑制anammox菌的增殖。
-
1)以不同污泥接种策略启动anammox反应器运行100 d,发现少量投加anammox颗粒污泥能够实现反应器快速启动,以反硝化污泥:anammox颗粒污泥=9:1的接种组合为最佳污泥接种策略,其菌体自溶和活性迟滞阶段耗时最短,运行100 d后TN去除率可达75.1%。
2) Anammox工艺中6 mg·L−1的N2H4浓度能削弱高浓度进水基质和垃圾渗滤液对anammox的不利影响,抑制异养反硝化菌的活性。N2H4质量浓度为6 mg·L−1的anammox反应器在完全以垃圾渗滤液为进水时的TN平均去除率可达90.6%,较未添加N2H4的anammox反应器高出28.9%。
3)适量N2H4浓度对SAA、EPS的分泌及anammox菌繁殖有较好的促进作用,在N2H4质量浓度6 mg·L−1时,anammox反应器的SAA最高达到0.143 kg·(kg·d)−1,EPS总含量由12.8 mg·g−1增长到33.9 mg·g−1,Candidatus Kuenenia相对丰度由0.2%提升到10.6%。
污泥接种策略与联氨促进垃圾渗滤液厌氧氨氧化工艺快速启动及其运行效果
Sludge inoculation strategy and hydrazine promoting rapid start-up and operational effectiveness of anaerobic ammonia oxidation process for landfill leachate
-
摘要: 针对厌氧氨氧化工艺启动速度慢及在垃圾渗滤液中脱氮效率低的问题,探究了厌氧氨氧化工艺在处理高氨氮、低C/N比垃圾渗滤液中的快速启动及稳定运行策略。结果表明,厌氧氨氧化工艺接种反硝化污泥:anammox颗粒污泥=9:1的启动效果最佳,100 d时TN去除率可达75.1%。但由于垃圾渗滤液中COD较高,异养反硝化菌生长迅速且严重影响厌氧氨氧化菌活性。通过投加6 mg·L−1的N2H4之后,异养反硝化菌活性受到抑制,反应器内厌氧氨氧菌占据主导地位,Candidatus Kuenenia菌相对丰度由0.2%提升到10.6%,TN去除率及氮去除速率分别达90.6%和0.143 kg·(kg·d)−1以上。在厌氧氨氧化工艺中投加适量N2H4可实现垃圾渗滤液的稳定高效自养脱氮。Abstract: Aiming at the problems of slow start-up and low denitrification efficiency of anammox process in landfill leachate, the strategy of rapid start-up and steady operation of anammox process in treating landfill leachate with high ammonia nitrogen and low C/N ratio was investigated. The results showed that the anammox process inoculated with denitrifying sludge: anammox granular sludge = 9:1 had the optimal start-up effect, and TN removal rate could reach 75.1% at 100 d. However, due to the high COD in landfill leachate, heterotrophic denitrifying bacteria grew rapidly and seriously affected the activity of anammox bacteria. After the addition of 6 mg·L−1 N2H4, the activity of heterotrophic denitrifying bacteria was inhibited and the abundance of anammox bacteria dominated. The relative abundance of Candidatus Kuenenia increased from 0.2% to 10.6%, and TN removal rate and nitrogen removal rate reached over 90.6% and 0.143 kg·(kg·d)−1, respectively. The stable and efficient autotrophic denitrification of landfill leachate could be achieved by adding an appropriate amount of N2H4 to the anammox process.
-
Key words:
- autotrophic denitrification /
- anammox /
- landfill leachate /
- N2H4
-

-
表 1 B1~B5反应器各阶段进水水质
Table 1. Influent water quality of B1~B5 reactors during different phases.
阶段 渗滤液占比/% COD/(mg·L−1) NH4+-N/(mg·L−1) NO2−-N/(mg·L−1) NO3−-N/(mg·L−1) Ⅰ (第1~116天) 25 497~728 58.5~156.6 76.5~201.2 0~13.0 Ⅱ(第117~144天) 50 1 226~1 422 168.4~189.5 232.0~252.3 1.3~9.6 Ⅲ(第145~184天) 75 2 184~2 316 147.4~168.4 183.3~249.5 ND Ⅳ(第185~222天) 100 2 510~2 632 167.1~185.5 191.5~264.1 0~0.9 Ⅴ(第223~252天) 100 2 504~2 892 163.2~165.8 210.4~214.4 2.0~8.1 表 2 B1~B5反应器各阶段化学计量变化
Table 2. The stoichiometric change of B1~B5 reactors during different phases
反应器 阶段Ⅰ 阶段Ⅱ 阶段Ⅲ 阶段Ⅳ 阶段Ⅴ ΔNO2−-N/
ΔNH4+-NΔNO3−-N/
ΔNH4+-NΔNO2−-N/
ΔNH4+-NΔNO3−-N/
ΔNH4+-NΔNO2−-N/
ΔNH4+-NΔNO3−-N/
ΔNH4+-NΔNO2−-N/
ΔNH4+-NΔNO3−-N/
ΔNH4+-NΔNO2−-N/
ΔNH4+-NΔNO3−-N/
ΔNH4+-NB1 1.37 0.13 1.53 0.24 1.44 0.26 1.40 0.08 1.43 0.05 B2 1.31 0.12 1.46 0.18 1.27 0.17 1.28 0.10 1.37 0.08 B3 1.32 0.11 1.44 0.21 1.24 0.20 1.20 0.13 1.34 0.11 B4 1.31 0.11 1.46 0.18 1.21 0.15 1.08 0.10 1.34 0.13 B5 1.30 0.04 1.44 0.22 1.20 0.02 1.21 0.11 1.28 0 表 3 接种污泥及阶段Ⅴ B1~B5的Alpha多样性指数
Table 3. Alpha diversity index of inoculation sludge and B1~B5 reactors in phase Ⅴ
样品 OTUs Shannon Simpson Ace Chao 1 谱系多样性 覆盖率 接种污泥 86 2.933 0.770 5 126.224 3 119.214 3 10.862 0.996 8 B1 310 4.753 7 0.889 4 432.124 9 419 31.7412 0.985 9 B2 460 5.516 3 0.927 7 579.214 7 568.370 4 40.487 8 0.986 1 B3 375 4.954 6 0.918 2 521.858 9 537.018 2 36.746 8 0.988 8 B4 500 5.57 3 0.923 5 602.091 5 603.2 42.287 2 0.988 4 B5 366 4.621 7 0.878 2 489.403 9 467.283 6 33.491 0.989 0 -
[1] KARTAL B, MAALCKE W J, DE ALMEIDA N M, et al. Molecular mechanism of anaerobic ammonium oxidation[J]. Nature, 2011, 479(7371): 127-130. doi: 10.1038/nature10453 [2] DENG W, WANG L, CHENG L, et al. Nitrogen removal from mature landfill leachate via anammox based processes: A Review[J]. Sustainability, 2022, 14(2): 995. doi: 10.3390/su14020995 [3] REN S, ZHANG L, ZHANG Q, et al. Anammox-mediated municipal solid waste leachate treatment: A critical review[J]. Bioresource Technology, 2022, 361: 127715. doi: 10.1016/j.biortech.2022.127715 [4] 宋韶华, 刘永军, 杨璐, 等. 厌氧氨氧化技术在废水处理中的研究与应用进展[J]. 水处理技术, 2022, 48(10): 6-12. [5] CHEN H, HU H, CHEN Q, et al. Successful start-up of the anammox process: Influence of the seeding strategy on performance and granule properties[J]. Bioresource Technology, 2016, 211: 594-602. doi: 10.1016/j.biortech.2016.03.139 [6] WANG Q, WANG Y, LIN J, et al. Selection of seeding strategy for fast start-up of Anammox process with low concentration of Anammox sludge inoculum[J]. Bioresource Technology, 2018, 268: 638-647. doi: 10.1016/j.biortech.2018.08.056 [7] WANG Y, XIE H, WANG D, et al. Insight into the response of anammox granule rheological intensity and size evolution to decreasing temperature and influent substrate concentration[J]. Water Research, 2019, 162: 258-268. doi: 10.1016/j.watres.2019.06.060 [8] NI S Q, NI J Y, HU D L, et al. Effect of organic matter on the performance of granular anammox process[J]. Bioresource Technology, 2012, 110: 701-705. doi: 10.1016/j.biortech.2012.01.066 [9] KIM J, GUO X, PARK H. Comparison study of the effects of temperature and free ammonia concentration on nitrification and nitrite accumulation[J]. Process biochemistry, 2008, 43(2): 154-160. doi: 10.1016/j.procbio.2007.11.005 [10] STROUS M, KUENEN J G, JETTEN M S. Key physiology of anaerobic ammonium oxidation.[J]. Applied and Environmental Microbiology, 1999, 65(7): 3248-3250. doi: 10.1128/AEM.65.7.3248-3250.1999 [11] TANG C J, ZHENG P, WANG C H, et al. Suppression of anaerobic ammonium oxidizers under high organic content in high-rate Anammox UASB reactor[J]. Bioresource Technology, 2010, 101(6): 1762-1768. doi: 10.1016/j.biortech.2009.10.032 [12] VAN DER STAR W R L, DIJKEMA C, DE WAARD P, et al. An intracellular pH gradient in the anammox bacterium Kuenenia stuttgartiensis as evaluated by 31P NMR[J]. Applied Microbiology and Biotechnology, 2010, 86(1): 311-317. doi: 10.1007/s00253-009-2309-9 [13] XIANG T, GAO D, WANG X. Performance and microbial community analysis of two sludge type reactors in achieving mainstream deammonification with hydrazine addition[J]. Science of the Total Environment, 2020, 715(C): 136377. [14] ZEKKER I, ARTEMCHUK O, RIKMANN E, et al. Start-Up of anammox SBR from non-specific inoculum and process Acceleration Methods by Hydrazine[J]. Water, 2021, 13(3): 350. doi: 10.3390/w13030350 [15] MIODOŃSKI S, MUSZYŃSKI-HUHAJŁO M, ZIĘBA B, et al. Fast start-up of anammox process with hydrazine addition[J]. SN Applied Sciences, 2019. [16] van de GRAAF A A, de BRUIJN P, ROBERTSON L A, et al. Autotrophic growth of anaerobic ammonium-oxidizing micro-organisms in a fluidized bed reactor[J]. Microbiology, 1996, 142(8): 2187-2196. doi: 10.1099/13500872-142-8-2187 [17] 编委会国家环境保护总局水和废水监测分析方法. 水和废水监测分析方法 (第四版)[M]. 水和废水监测分析方法 (第四版), 2002. [18] BRADFORD M. A Rapid and Sensitive Method for the Quantitation of Microgram Quantities of Protein Utilizing the Principle of Protein-Dye Binding[J]. Analytical Biochemistry, 1976, 72(1/2): 248-254. [19] GAUDY A F. Colorimetric determination of protein and carbohydrate[J]. Water Wastes, 1962, 7(1): 17-22. [20] 唐崇俭. 厌氧氨氧化工艺特性与控制技术的研究[D]. 杭州: 浙江大学, 2011. [21] 汪瑶琪, 张敏, 姜滢, 等. 厌氧氨氧化启动过程及微生物群落结构特征[J]. 环境科学, 2017, 38(12): 5184-5191. [22] CHAMCHOI N, NITISORAVUT S. Anammox enrichment from different conventional sludges[J]. Chemosphere (Oxford), 2007, 66(11): 2225-2232. doi: 10.1016/j.chemosphere.2006.09.036 [23] 丁爽, 郑平, 唐崇俭, 等. 三种接种物启动Anammox-EGSB反应器的性能[J]. 生物工程学报, 2011, 27(4): 629-636. [24] 闾刚, 李田, 徐乐中, 等. 基于不同接种污泥复合型厌氧氨氧化反应器的快速启动特征[J]. 环境科学, 2017, 38(10): 4324-4331. [25] XU L Z, ZHANG Q, FU J J, et al. Deciphering the microbial community and functional genes response of anammox sludge to sulfide stress[J]. Bioresource Technology, 2020, 302(C): 122885. [26] 杨盈盈, 陈奕, 李明杰, 等. 进水渗滤液总氮和BOD_5/TN对填埋场反应器反硝化和厌氧氨氧化协同脱氮的影响[J]. 环境科学, 2015, 36(4): 1412-1416. [27] 姚宗豹. Anammox新体系: 外加N2H4的影响、NO的脱出和Fe(Ⅲ)氧化NH4+[D]. 重庆: 重庆大学, 2015. [28] XIANG T, LIANG H, GAO D. Effect of exogenous hydrazine on metabolic process of anammox bacteria[J]. Journal of Environmental Management, 2022, 317: 115398. doi: 10.1016/j.jenvman.2022.115398 [29] YAO Z, LU P, ZHANG D, et al. Stoichiometry and kinetics of the anaerobic ammonium oxidation (Anammox) with trace hydrazine addition[J]. Bioresource Technology, 2015, 198: 70-76. doi: 10.1016/j.biortech.2015.08.098 [30] 蔡庆, 丁佳佳. N2H4强化厌氧氨氧化机理及动力学特性[J]. 水处理技术, 2015, 41(5): 73-77. [31] 鲍林林, 李晓珍, 李孙林, 等. 联氨对HABR全程自养脱氮系统的影响[J]. 中国给水排水, 2020, 36(5): 26-32. [32] 陈佼, 陆一新, 李滨伶, 等. CRI系统厌氧氨氧化协同反硝化脱氮的启动及性能[J]. 环境科学与技术, 2021, 44(9): 86-92. doi: 10.19672/j.cnki.1003-6504.0639.21.338 [33] MA J, YAO H, YU H, et al. Hydrazine addition enhances the nitrogen removal capacity in an anaerobic ammonium oxidation system through accelerating ammonium and nitrite degradation and reducing nitrate production[J]. Chemical engineering journal (Lausanne, Switzerland:1996), 2018, 335: 401-408. [34] 范丹, 李冬, 梁瑜海, 等. 生活污水SNAD颗粒污泥快速启动及脱氮性能研究[J]. 中国环境科学, 2016, 36(11): 3321-3328. doi: 10.3969/j.issn.1000-6923.2016.11.015 [35] 杨明明, 刘子涵, 周杨, 等. 厌氧氨氧化颗粒污泥EPS及其对污泥表面特性的影响[J]. 环境科学, 2019, 40(5): 2341-2348. [36] 高梦佳, 王淑莹, 王衫允, 等. 生活污水对成熟厌氧氨氧化颗粒污泥的影响[J]. 化工学报, 2017, 68(5): 2066-2073. [37] MIAO L, ZHANG Q, WANG S, et al. Characterization of EPS compositions and microbial community in an Anammox SBBR system treating landfill leachate[J]. Bioresource Technology, 2018, 249: 108-116. doi: 10.1016/j.biortech.2017.09.151 [38] LIU S, LIN C, DIAO X, et al. Interactions between tetracycline and extracellular polymeric substances in anammox granular sludge[J]. Bioresource Technology, 2019, 293: 122069. doi: 10.1016/j.biortech.2019.122069 [39] CHEN Z, ZHOU S, WANG J, et al. Recovery of anaerobic ammonium oxidation via hydrazine following sulfate inhibition[J]. Environmental Science: Water Research & Technology, 2022. [40] FUERST J A, SAGULENKO E. Beyond the bacterium: Planctomycetes challenge our concepts of microbial structure and function[J]. Nature Review Microbiology, 2011, 9(6): 403-413. doi: 10.1038/nrmicro2578 [41] HOSOKAWA S, KURODA K, NARIHIRO T, et al. Cometabolism of the superphylum patescibacteria with anammox bacteria in a long-term freshwater anammox column reactor[J]. Water (Basel), 2021, 13(2): 208. [42] HE S, CHEN Y, QIN M, et al. Effects of temperature on anammox performance and community structure[J]. Bioresource Technology, 2018, 260: 186-195. doi: 10.1016/j.biortech.2018.03.090 [43] HU B L, ZHENG P, TANG C J, et al. Identification and quantification of anammox bacteria in eight nitrogen removal reactors[J]. Water Research, 2010, 44(17): 5014-5020. doi: 10.1016/j.watres.2010.07.021 [44] JIANG X, HOU L, ZHENG Y, et al. Salinity-driven shifts in the activity, diversity, and abundance of anammox bacteria of estuarine and coastal wetlands[J]. Physics and chemistry of the earth. Parts A/B/C, 2017, 97: 46-53. doi: 10.1016/j.pce.2017.01.012 -




 下载:
下载: