-
我国污泥产量基数大、增速快,2019年已超过6×107 t (以80%含水率计) ,预计2025年将达到9×107 t[1]。据统计,污泥处理的碳排放量约占污水处理行业的65%~76%,是不可忽视的减排领域[2]。污泥与煤的掺烧是污泥协同焚烧的常见工艺,能实现最大程度的减量化和无害化,焚烧后的灰渣可回收利用。在“双碳”背景下,碳排放水平成为评估污泥干化焚烧-灰渣综合利用路径效果的一个重要指标。
污泥处理处置产生的直接碳排放主要有化石源CO2、CH4和N2O等温室气体。根据联合国气候变化政府间专家委员会 (IPCC) 清单计算方法,化石源CO2应纳入碳排放核算清单中,而生物源CO2则不纳入[3]。且IPCC认为污泥化石碳质量分数为0,因焚烧或生物降解产生的CO2被视为生物成因,因此核算直接碳排放时仅考虑CH4和N2O排放量[3]。但随着人们生活水平提高,多数以石油加工化学品为原材料的食品添加剂、洗涤剂、化妆品、药物等在生产使用过程中将化石碳引入到了污泥中。KANG等[4]采用放射性碳测年法得出污水污泥化石碳质量分数为14.00%~34.24%。因此,实际污泥化石碳质量分数不可忽略。纪莎莎等[5]将污泥化石碳质量分数视为0%,得到污泥焚烧的直接碳排放因子 (以CO2eq/DS计,下同) 为0.31 t·t−1;李哲坤等[6]代入的化石碳质量分数为12%,得到污泥焚烧的直接碳排放因子为0.46 t·t−1;李欢等[7]认为,污泥化石碳质量分数为100%,计算得到污泥焚烧的直接碳排放因子为1.56 t·t−1。由此可见,污泥焚烧的直接碳排放量与化石碳质量分数呈正相关。测定实际污泥化石碳质量分数对提高污泥处理处置路径碳排放强度评估的准确性具有重要意义。
目前,在碳排放核算时,测定污泥化石碳质量分数的研究较为缺乏,导致碳排放评估风险增加。本研究基于浙江省某污泥能源化利用热电联产项目,拟采用放射性碳测年法测定污泥总有机碳中化石碳的质量分数,构建碳排放和碳补偿计算方法,以更准确地核算污泥干化焚烧-灰渣综合利用路径的碳排放因子,并与深度脱水-应急填埋路径的理论碳排放水平比较。
-
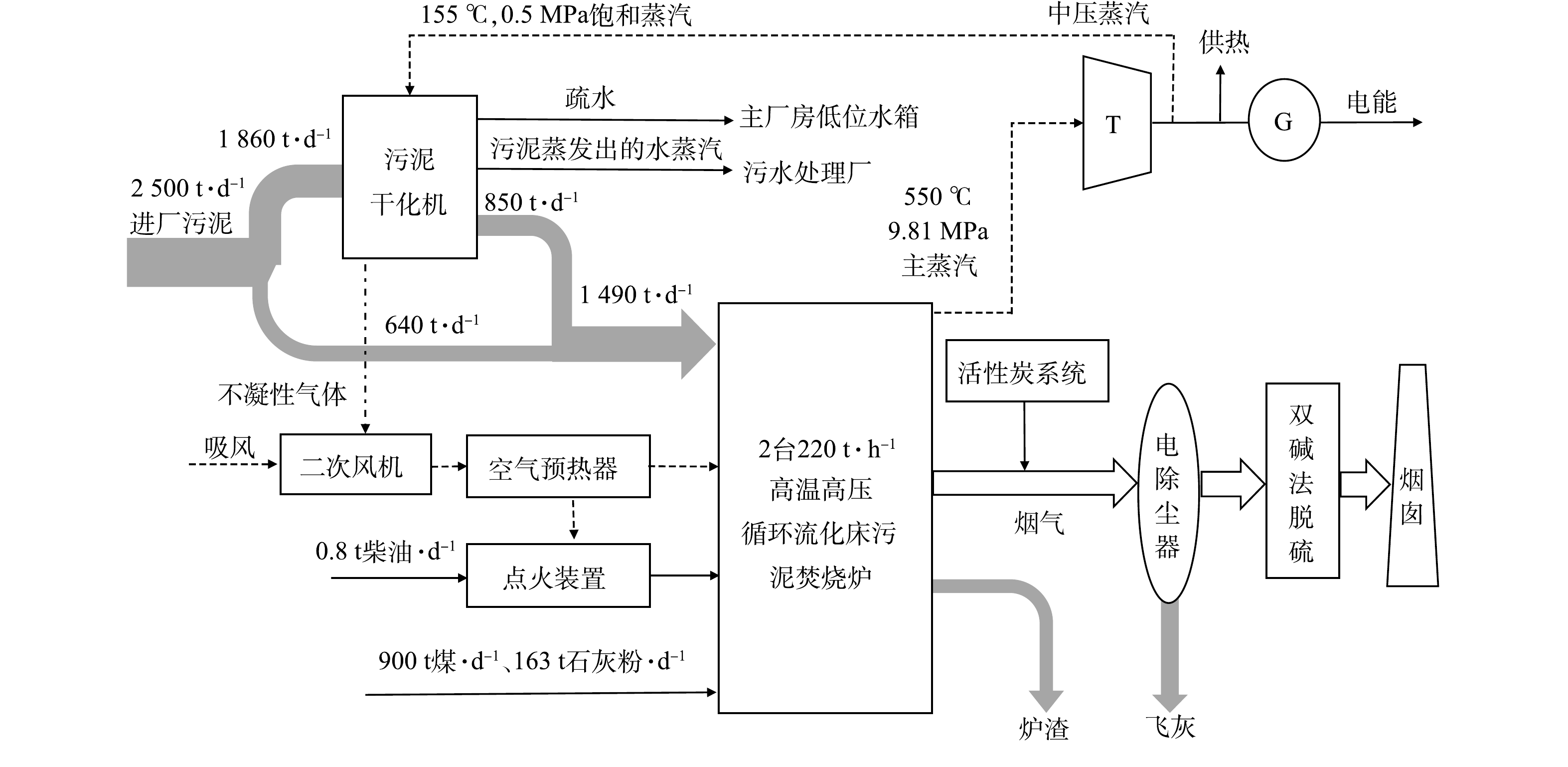
本研究采用的污泥产自项目附近的市政污水处理厂、印染纺织厂、皮革厂和工业区,来源稳定。焚烧时,干污泥与煤炭的掺混比例约为0.623∶0.377。干污泥、煤炭及其2者的混合物的收到基工业分析、元素分析和低位发热量结果见表1。项目工艺流程如图1所示,污泥和煤的化学能转化为蒸汽的热能,部分发电供热,部分用于污泥干燥。项目2021年1-4月的运营情况见表2。
-
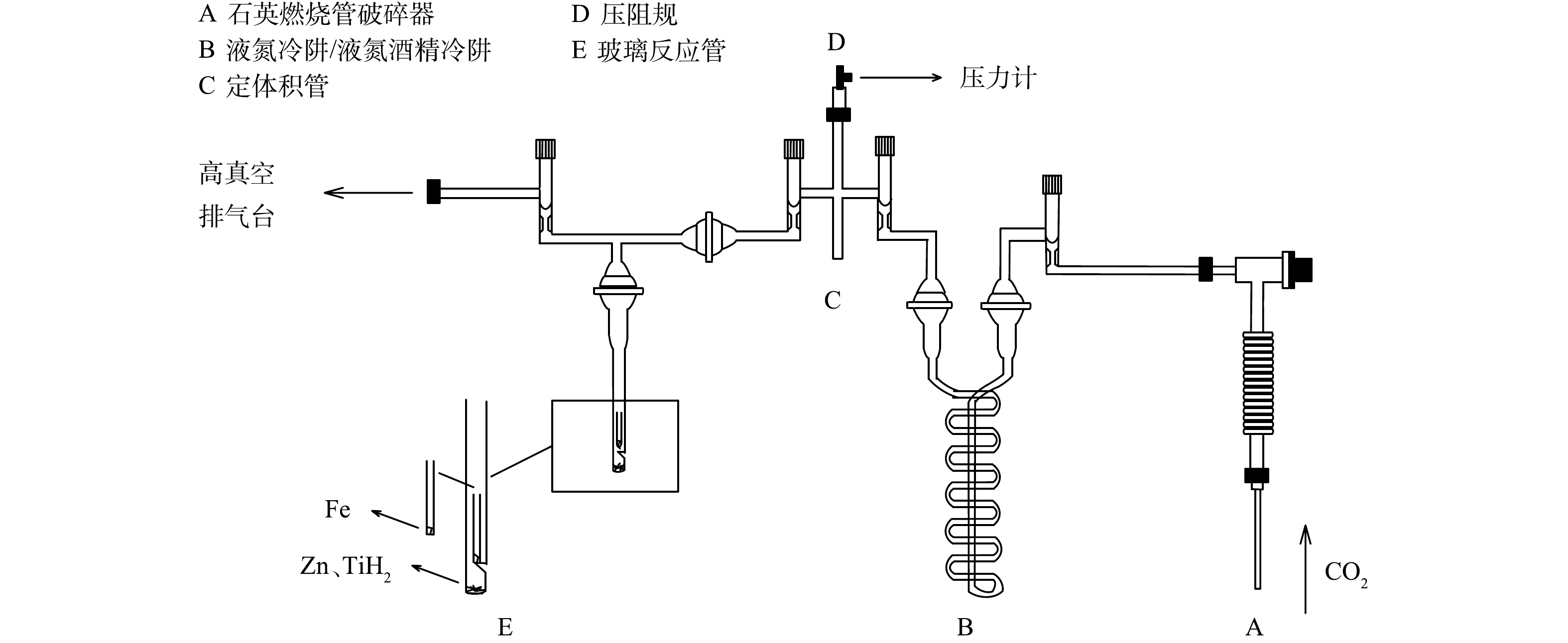
采用加速器质谱仪测定化石碳质量分数需先将污泥制备成石墨样品。石墨样品制备实验台如图2所示,该实验台由石英燃烧管破碎器、冷阱、定体积管、圧阻规和玻璃反应管组成,整体装置抽真空。污泥预处理时先除去样品自身含有的无机碳[8]。制备石墨样品的实验方法参照刘圣华等[9]的研究。所用0.5 MV 1.5SDH-1型加速器质谱仪14C/12C长期测试精度优于0.3%,机器本底现代碳比值为0.000 4,相当于14C年龄为63 764 a。
根据同位素两端元混合模型计算污泥有机碳中化石碳的质量分数,样品中生物碳与化石碳质量分数之和为100%。由于生物碳与现代大气保持平衡的同位素特征,化石碳中14C衰变完全,因此Fmf=0,Fmb=Fmatm,计算如式(1)~式(3)所示。
式中:Fms为样品现代碳比值;Fmb为生物质基现代碳比值;wb为生物碳质量分数;Fmf为化石基现代碳比值;wf为化石碳质量分数;Fmatm为大气现代碳比值监测值。
-
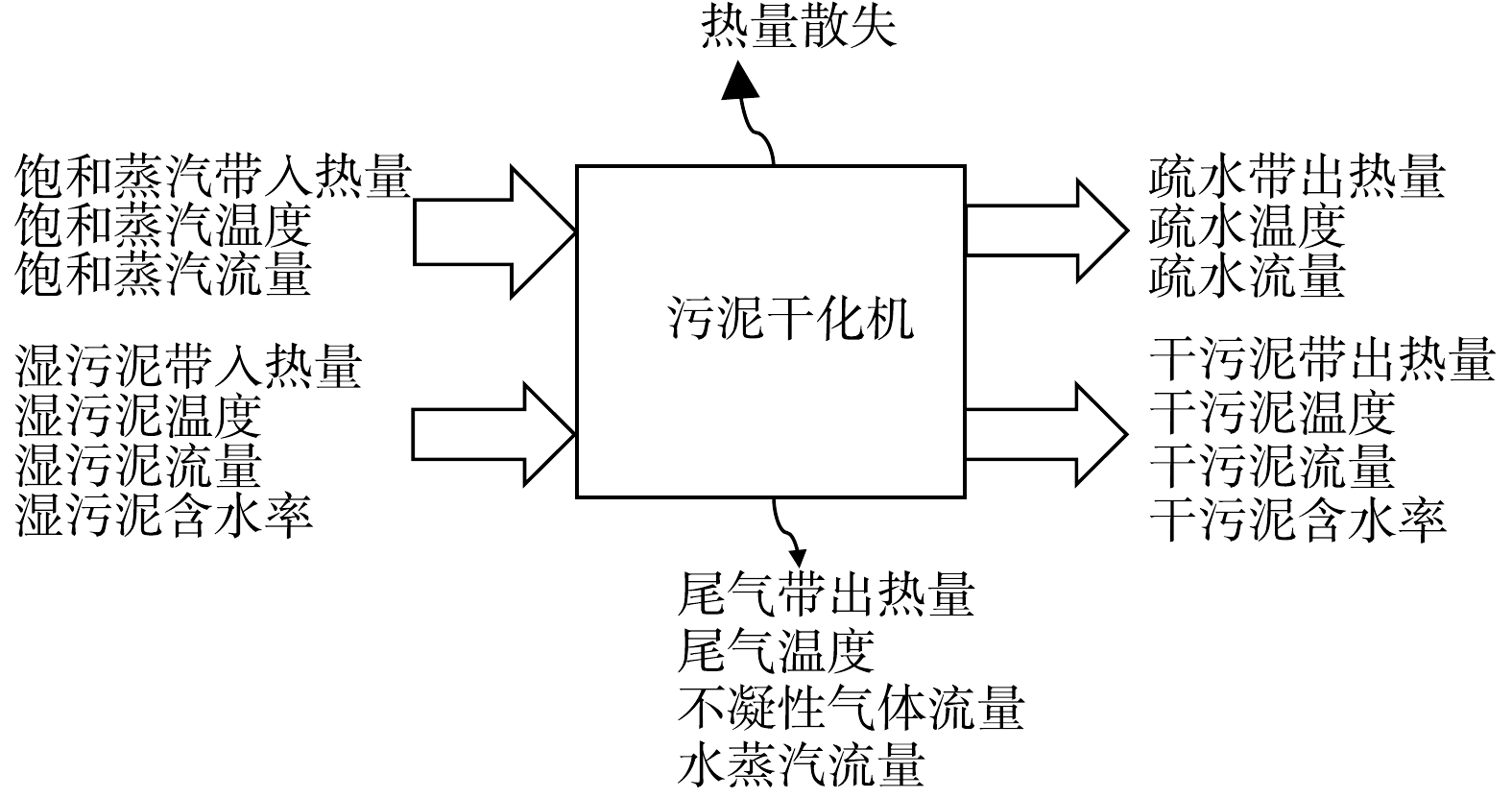
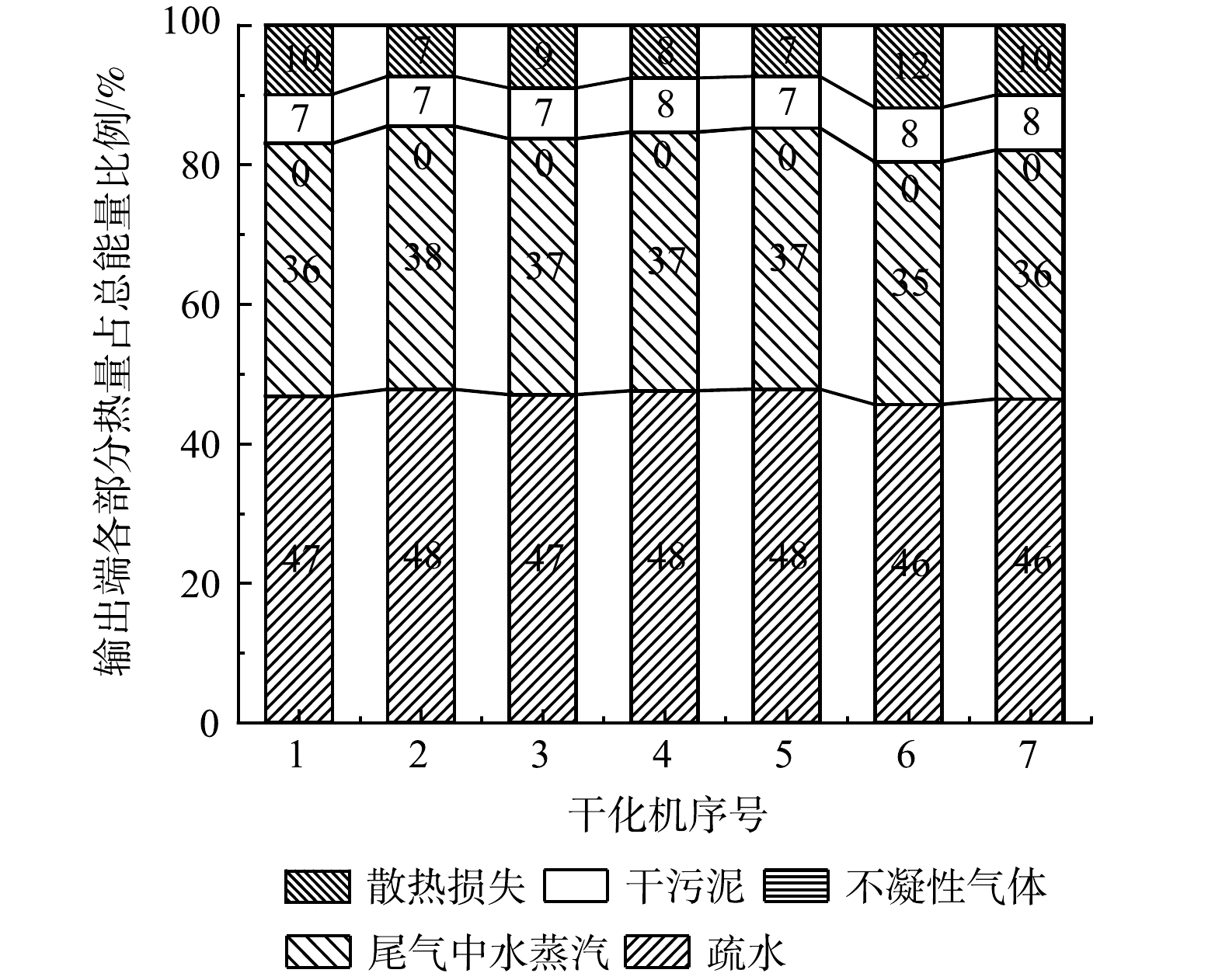
污泥干化机的质量和能量平衡见图3,计算如式(4)~式(6)所示。
式中:qm,q1为饱和蒸汽质量流量,kg·h−1;qm,q2为疏水质量流量,kg·h−1;qm,wn1为湿污泥质量流量,kg·h−1;qm,wn2为干污泥质量流量,kg·h−1;qm,q3为尾气中水蒸汽质量流量,kg·h−1;qm,g为不凝性气体质量流量,kg·h−1;Qq1为饱和蒸汽带入热量,kJ·h−1;Qwn1为湿污泥带入热量,kJ·h−1;Qwn2为干污泥带出热量,kJ·h−1;Qq2为疏水带出热量,kJ·h−1;Qq3为水蒸汽带出热量,kJ·h−1;Qg为不凝性气体带出热量,kJ·h−1;Qs为散热损失,kJ·h−1。
饱和蒸汽和疏水携带热量计算如式(7)~式(8)所示。
式中:hq1为饱和蒸汽比焓,kJ·kg−1;hq2为疏水比焓,kJ·kg−1。
湿污泥和干污泥携带热量计算如式(9)~式(10)所示。
式中:twn1为湿污泥温度, ℃;cDS为污泥干基比热,1.3 kJ·(kg· ℃)−1[10];cw为水的比热容,4.187 kJ·(kg· ℃)−1[10];xwn1为湿污泥含水率;twn2为干污泥温度, ℃;xwn2为干污泥含水率。
不考虑化学反应吸放热,尾气中水蒸汽及不凝性气体带出热量计算如式(11)~式(13)所示[11]。
式中:tq3为水蒸汽温度, ℃;r0为0 ℃时水的汽化潜热,2 491 kJ·kg−1[11];cq3为水蒸汽比热容,1.866 kJ·(kg· ℃)−1[11];cg为不凝性气体定压比热容,kJ·(kg· ℃)−1;tg为不凝性气体温度, ℃。
污泥干化机热效率计算如式(14)所示。
式中:ηh为污泥干化机热效率。
项目中7台污泥干化机的运行情况见表3。采用GASMET-DX4000型烟气分析仪检测不凝性气体,结果见表4。实验发现不凝性气体的主要成分为NH3、C3H8、HCN、CH4和CH3COOH。经加权计算,7台污泥干化机排出的不凝性气体比热容相差不大,分别为2.077、2.075、2.075、2.073、2.074、2.073、2.073 kJ·(kg· ℃)−1。
-
污泥掺烧可减少煤炭使用量,但相比于燃煤锅炉,锅炉效率会下降。根据文献[12]计算2种燃料分别焚烧时的理论锅炉效率,如式(15)~式(18)所示。
式中:q4,i为固体不完全燃烧热损失,i为f时,燃料为煤炭,i为m时,燃料为污泥掺煤,下同;Aar为收到基灰分;adz为底渣占燃料灰分份额;Cdz为底渣含碳量;afh为飞灰占燃料灰分份额;Cfh为飞灰含碳量;Qb,i为锅炉输入热量,GJ;q2,i为排烟热损失;hpy为排烟焓,kJ·kg−1;αpy为排烟处过量空气系数;hlk0为冷空气焓,kJ·m−3;q6,i为灰渣物理显热损失;Qpz为返渣补砂热损失,kJ·kg−1;apz为排渣率;hpz为排渣焓,kJ·kg−1;afz为返渣率;hfz为返渣焓,kJ·kg−1;abz为补砂率;hbz为补砂焓,kJ·kg−1;ηb,i为锅炉效率;q3,i为气体不完全燃烧热损失;q5,i为散热损失。
取锅炉运行现场的飞灰和炉渣进行元素分析,含碳量分别为2.02%和1.35%。煤粉炉中气体不完全燃烧热损失一般不超过0.5%,取q3,i为0.5%[12]。由于散热损失测量非常困难,工程上根据锅炉额定容量查取散热损失,取q5,i为0.6%[12]。其余物理量根据锅炉运行实际情况取值如表5所示。
燃料理论消耗量计算如式(19)~式(20)所示。单位干基污泥焚烧替代的标煤量计算如式(21)所示。
式中:Q为主蒸汽热量,GJ;D为主蒸汽量,t;h为主蒸汽比焓,kJ·kg−1;mi为燃料理论消耗量,t;Qnet,ar,i为燃料低位发热量,kJ·kg−1;mce为每t干基污泥焚烧替代的标煤量 (以ce/DS计) ,t·t−1;mwn为污泥理论消耗量,t;Qnet,ar,wn为污泥低位发热量,kJ·kg−1;Qnet,ar,ce为标煤低位发热量,29 271.2 kJ·kg−1;m为入炉干污泥量,t。
-
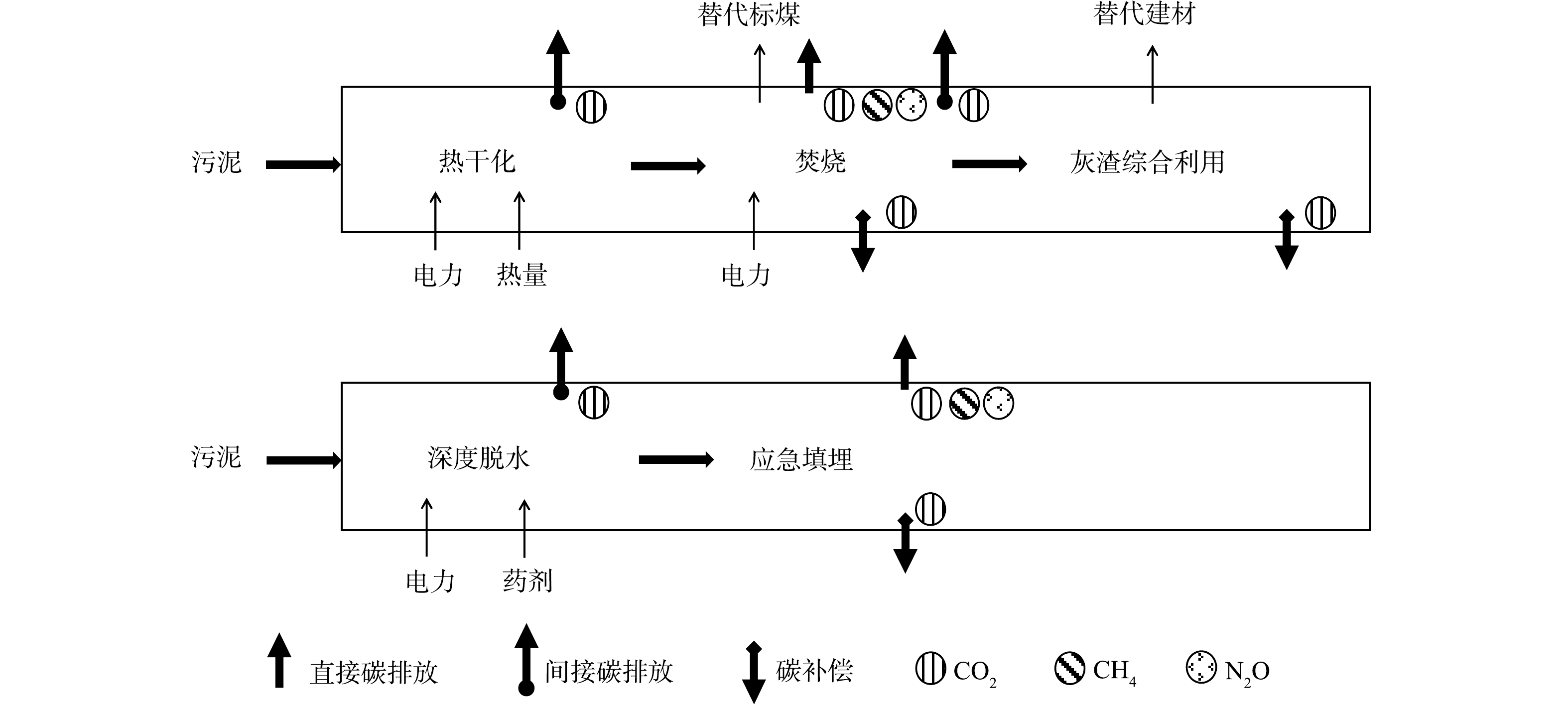
两种污泥处理处置路径的碳排放核算边界见图4,碳排放因子的计算如式(22)~式(23)所示。
式中:EFIC为污泥干化焚烧-灰渣综合利用路径的碳排放因子,t·t−1;EIC1为污泥焚烧直接碳排放量,t;EIC2为干化焚烧间接碳排放量,t;EIC3为污泥焚烧和灰渣综合利用的碳补偿量,t;EFLF为污泥深度脱水-应急填埋路径的碳排放因子,t·t−1;ELF1为污泥填埋直接碳排放量,t;ELF2为污泥深度脱水和填埋的间接碳排放量,t;ELF3为填埋气利用的碳补偿量,t;mS为湿污泥处理总量,t。
-
该路径的直接碳排放量包括焚烧时产生的化石源CO2、CH4和N2O,如式(24)~式(27)所示。
式中:EIC1,CO2为焚烧化石源CO2排放量,t;EIC1,CH4为焚烧CH4排放量,t;EIC1,N2O为焚烧N2O排放量,t;GWPCH4为CH4的100年全球增温潜势,为25[13];GWPN2O为N2O的100年全球增温潜势,为298[13];CF为干基污泥含碳量;FCF为化石碳在总碳中的质量分数;OF为碳氧化率;44/12为CO2与C的分子量之比;EFIC1,CH4为污泥焚烧CH4排放因子 (以CH4/DS计,下同) ,取0.024 25 kg·t−1[14];EFIC1,N2O为污泥焚烧N2O排放因子 (以N2O/DS计) ,取0.99 kg·t−1[14]。
假设污泥和煤的碳氧化率相同,计算如式(28)~式(29)所示。
式中:OFwn为污泥碳氧化率;OFf为煤碳氧化率;mz为炉渣产量,t;Cz为炉渣平均含碳量;mh为飞灰产量,t;Ch为飞灰平均含碳量;η为除尘系统平均除尘效率;FC为干污泥和煤混合燃料消耗量,t;NCV为污泥掺煤平均低位发热量,kJ·kg−1;CC为污泥掺煤单位热值含碳量 (以碳元素计) ,t·TJ−1。
该路径的间接碳排放量由污泥干化热耗以及干化焚烧等主要用电环节电耗产生,核算如式(30)~式(32)所示。
式中:EIC2,h为热耗产生的间接碳排放量,t;EIC2,e为干化焚烧电耗产生的间接碳排放量,t;Qh为干化时蒸汽携带热量,kJ;qce为标准煤热值,29.27 MJ·kg−1[15];EFce为标准煤碳排放因子 (以CO2/ce计) ,2.493 t·t−1[15];Qe,h为每t干基污泥干化耗电量 (以DS计,下同) ,取0.05 MW h·t−1[14];Qe,IC为每t干基污泥焚烧耗电量,取0.4 MW·h·t−1[16];EFe为电力碳排放因子,取0.792 t·(MW·h)−1[17]。
该路径通过污泥焚烧替代煤炭和灰渣综合利用产生碳补偿,计算如式(33)~式(35)所示。
式中:EIC3,B为替代标煤的碳补偿量,t;EIC3,hz为灰渣综合利用的碳补偿量,t;mhz,IC为污泥焚烧灰渣产量,t;EFhz为灰渣综合利用碳排放因子,0.52 t·t−1[18]。
-
微生物降解污泥有机质时产生填埋气,而我国填埋场大多无专门的填埋气收集装置,填埋气直接逸散于大气中。根据PAN等[19]研究结果,污泥填埋气无组织排放参数如表6所示,核算理论直接碳排放量时取各参数的中值计算,生物源CO2不计入,如式(36)~式(39)所示。
式中:ELF1,CO2为填埋化石源CO2排放量,t;EFLF1,CO2为填埋化石源CO2排放因子 (以CO2/DS计) ,t·t−1;ELF1,CH4为填埋CH4排放量,t;EFLF1,CH4为填埋CH4排放因子,t·t−1;ELF1,N2O为填埋N2O排放量,t;EFLF1,N2O为填埋N2O排放因子 (以N2O/Nd计) ,t·t−1;Nd为污泥干基含氮量。
该路径的间接碳排放量由电耗和药耗产生。污泥深度脱水常用的药剂为聚丙烯酰胺 (PAM) 、FeCl3、CaO,脱水后泥饼含水率为45%~60%[20]。核算如式(40)~式(42)所示。
式中:ELF2,e为深度脱水电耗产生的间接碳排放量,t;ELF2,m为药耗产生的间接碳排放量,t;Qe,d为每t干基污泥深度脱水耗电量,取0.125MW·h·t−1[21];mm.j为每t干基污泥深度脱水不同药剂的消耗量,t·t−1。EFm.j为不同药剂的碳排放因子,t·t−1。PAM、FeCl3、CaO投加率分别为0.01 t·t−1、6%、10%[22],其碳排放因子分别为25[23]、8.3[21]、1.4 t·t−1[21]。
污泥填埋中填埋气收集困难,因此假设甲烷回收率为0,即
ELF3=0 。 -
近年大气现代碳比值监测值见表7[24],本研究中将2022年的数值代入计算。经测定,污泥现代碳比值为0.350 6,则化石碳占总碳的质量分数为64.94%。该结果远大于以往文献[4]中污水污泥化石碳质量分数14.00%~34.24%。这是因为,本研究中的污泥除了来自市政污水处理厂,还有一部分来自印染纺织厂、皮革厂和工业区。工业行业使用的化学品大多来自石油及其衍生物;纺织印染行业在织物染色过程中广泛使用的合成染料主要由煤焦油 (或石油加工) 分馏后经化学加工而成[25]。因此,污泥来源不同,其化石碳质量分数存在较大差异。
-
7台干化机输出端的能量分配情况见图5。经热平衡计算,污泥干化机的平均热效率为80.51%,在一般污泥干化机热效率70%~90%范围内[26-28],运行工况良好。污泥干化机输出端疏水带出热量约占总能量的46.98%,因此回收利用疏水余热十分必要。
-
2种燃料的锅炉热平衡情况见表8,2021年1-4月的理论消耗量见表9。污泥掺煤混烧时,锅炉效率为89.46%;煤炭为燃料时,锅炉效率为91.52%。经计算,平均焚烧1 t干基污泥可替代0.21 tce。
-
污泥干化焚烧-灰渣综合利用路径的碳排放核算结果见图6。该路径呈碳源性,碳排放因子为0.32 t·t−1。不同的污泥处理环节中,污泥焚烧直接碳排放>电耗间接碳排放>热耗间接碳排放。1 t干基污泥焚烧时产生的直接碳排放为0.85 t,介于0.46~1.56 t·t−1[6-7]。焚烧时产生的化石源CO2、CH4和N2O折合的碳排放当量分别占65.27%、0.07%、34.66%。若污泥焚烧产生的CO2均视为生物成因,则该路径呈碳汇性,碳排放因子为-0.24 t·t−1。因此,虽然测定实际污泥化石碳质量分数对评估污泥处理处置路径的碳排放水平具有负面影响,但可切实提高核算工作的准确性。在污泥焚烧项目中可通过增加碳捕集装置,优化干化机运行工况,提高干化机平均热效率等方法降低碳排放水平。该路径核算结果的不确定性可能来自污泥收到基含碳量、低位发热量的测定误差,计算干化机热效率和替代煤量时的数据误差,以及所取参考值的不准确性,如污泥干化和焚烧单位耗电量、灰渣碳排放因子等。
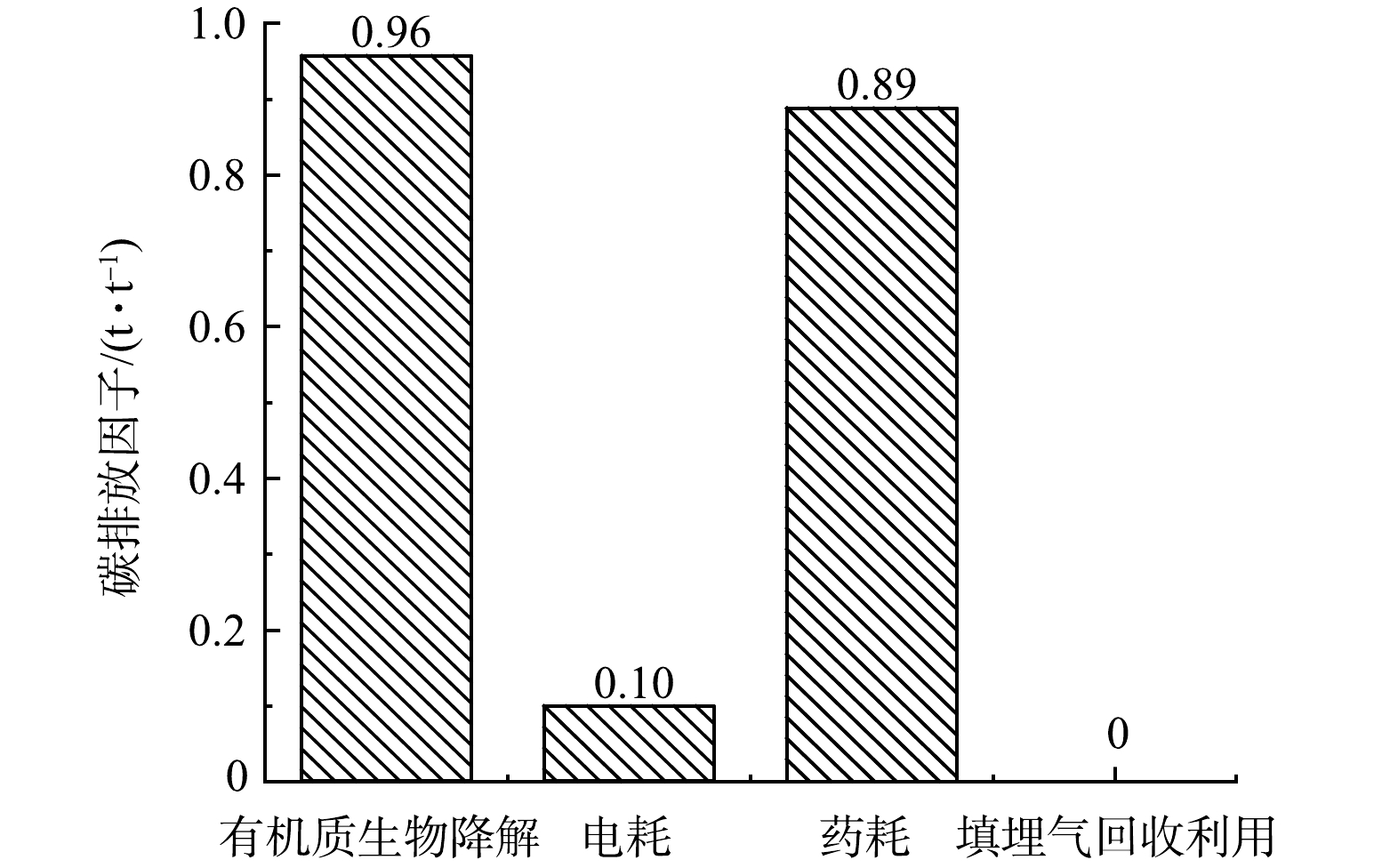
污泥深度脱水-应急填埋路径的碳排放核算结果见图7。该路径的理论碳排放因子为1.95 t·t−1,约为焚烧路径的6倍。不同的污泥处理环节中,污泥有机质降解产生的碳排放>药耗产生的间接碳排放>电耗产生的间接碳排放。填埋时1 t干基污泥因有机物生物降解产生的碳排放为0.96 t,其中化石源CO2、CH4和N2O折合的碳排放当量分别占2.14%、91.87%、5.99%,可见该路径下化石源CO2排放量较小。根据表6,填埋气中的CO2,生物源占94.3%左右,化石源仅占5.7%左右。这是因为,相比于生物碳,化石碳通常不易降解[29]。研发和普及污泥填埋气收集技术,避免填埋气逸散于空气,资源化利用填埋气产生碳补偿,对降低该路径的碳排放强度具有重要意义。该路径核算结果存在不准确性的原因在于填埋气无组织排放参数存在一定的范围,而为使结果更具有代表性,计算时仅代入中值。
-
1) 在评估污泥处理处置路径的碳排放强度时,测定化石碳质量分数可提高数据准确性,但也会增大碳排放水平。污泥干化焚烧-灰渣综合利用路径的碳排放因子为0.32 t·t−1,约为深度脱水-应急填埋路径的1/6,具有更大的减排潜力与推广价值。但污泥填埋成本低,短期内仍可作为一种应急措施。
2) 相关部门应投入人力、物力和财力开发高效污泥深度脱水技术,加强污泥干化系统优化和智能化水平,进一步节能减耗。应尽量降低电耗、药耗等高碳排放工艺的密集程度,有选择地耦合多种污泥低碳处理工艺,加强污泥资源化利用,降低碳排放水平。
3) 污泥掺煤混烧能够实现较为稳定的燃烧和较大的污泥处置量。但相比于单独焚烧,混烧会导致飞灰中磷的质量分数降低,还会引入杂质。因此从磷回收的角度出发,建议污泥单独焚烧。
基于化石碳的污泥干化焚烧处置碳排放分析
Analysis on carbon emissions of sludge drying and incineration treatment based on fossil carbon
-
摘要: 通常认为,污泥焚烧产生的CO2是生物成因,不计入碳排放核算清单。但石油加工化学品的广泛使用会导致污泥化石碳质量分数增加。为符合实际情况,采用放射性碳测年法测定污泥化石碳质量分数。基于浙江省某2 500 t·d−1污泥能源化利用热电联产项目运营数据,以1 t干基污泥 (DS) 为核算对象,构建碳排放及碳补偿核算方法,得出污泥干化焚烧-灰渣综合利用路径的碳排放因子,并与深度脱水-应急填埋路径的理论碳排放水平比较。结果表明,污泥有机碳中化石碳质量分数为64.94%,并非100%的生源碳。因此,污泥焚烧时计入碳排放核算清单的直接碳排放会增大,同时数据准确性和可靠度也有所增加。干化焚烧-灰渣综合利用路径中,1 t干基污泥的碳排放为0.32 tCO2eq,约为深度脱水-应急填埋路径的1/6,更具减排潜力。本研究结果可为污泥低碳化处理处置提供参考。Abstract: CO2 from sludge incineration is commonly considered biogenic and thus excluded from the carbon emission accounting list. However, the widespread use of petroleum processing chemicals would lead to an upward trend in sludge’s fossil carbon mass proportion. To adjust for the current circumstances, the radiocarbon dating technique was employed to quantify the mass fraction of fossil carbon in sludge. Based on the operation data of a 2500 t·d−1 sludge energy utilization cogeneration project in Zhejiang Province, carbon emissions and compensation accounting methods were built using 1 t dry base sludge (DS) as the accounting object. The carbon emission factor of the sludge drying incineration - comprehensive utilization of ash and slag path was calculated and compared with the theoretical carbon emission level of the deep dewatering - emergency landfill path. The results revealed that the mass proportion of fossil carbon in sludge organic carbon was 64.94%, indicating that the carbon was not entirely biogenic. As a result, the direct carbon emissions integrated into the carbon emission inventory when incinerating sludge would increase, simultaneously improving the data’s accuracy and dependability. The carbon emission (in terms of CO2-equivalent) of 1 t dry base sludge in the path of drying incineration - comprehensive utilization of ash and slag was 0.32 t, about 1/6 of that in the route of deep dehydration - emergency landfill, which had better emission reduction potential. This research could serve as a reference for sludge low-carbonization treatment and disposal.
-
Key words:
- sludge treatment /
- drying /
- incineration /
- landfill /
- fossil carbon /
- carbon emissions
-
近年来,我国一些发达地区的村落建设了分散式农村污水处理设施,并取得了较好的环境效益,但这些村落污水的治理,仍以COD、氨氮、总磷等污染物的降解为考核目标,而农村居民生活水平和医疗条件在不断提高,村落水环境中EDCs浓度水平也相应增加,其对水环境生态和人类健康危害日益严重[1],尤其是农村地区,EDCs通过灌溉形式,直接被稻、麦、瓜果等农作物吸收,进而进入食物链。EDCs是一种能扰乱生物体新陈代谢平衡的化学物质,主要分为天然产生(E1、E2、E3)及人工合成(EE2)[2]。据报道,各种环境基质中均检测到不同浓度的EDCs,水体中其质量浓度可低至10−6(1 μg·L−1)量级和10−9(1 ng·L−1)量级,而EDCs在极低浓度下就可引起水生生物的生殖发育障碍[3-4]。主要原因在于,EDCs与生物体内的雌激素受体结合而干扰生物内分泌系统正常代谢[5]。Legler等[6]研究发现,当自然水体中E2浓度达到1.0 ng·L−1时,可引起生物体内分泌紊乱。Cappiello等[7]发现不少猝死婴儿体内残留的EDCs含量相对普通新生婴儿较高;Clarke等[8]研究表明,妊娠期女性若接触过量EE2,则将増加母女患乳腺癌的风险。由此可见,当EDCs进入动物食物链,再经过层层传递,最终在人类体内积累,对人体健康损害威胁相应不断增大。
国内外众多学者研究表明,耕作型稻田复合生态系统通过“微生物-稻田湿地”耦合的复合系统对村落污水中的有机污染物进行生物降解,其主要依靠水稻复杂的根系及其附着的生物膜协同净化作用,不但可以达到净化村落污水的效果,还可以产生水稻增肥的效益[9]。但存在类固醇类激素(EDCs)环境污染及生态危害问题。现阶段,人为去除环境中雌激素类污染物主要通过吸附[10]、光催化氧化[11]、生物降解[12]的3种途径使EDCs在环境中迁移、降解。阳春等[10]研究表明,污泥对雌激素的吸附主要来自于污泥中的活性成分,而被生物表面所吸附的雌激素才能被生物降解。光解与氧化作用是EDCs真正的分解过程,因为它不可逆的改变了分子结构,强烈影响其在环境中的归趋,但光降解类固醇雌激素极易受pH的影响,近期有一些研究表明类固醇雌激素光氧化降解后产生的代谢产物仍具有雌激素活性[11]。生物降解通过微生物新陈代谢和自身与周围环境进行物质交换,达到将污染物去除或转化为无害无毒的物质[12],日益受到人们的重视。
本文针对村落污水中的类固醇类激素(EDCs)环境污染及生态危害问题,构建耕作型稻田湿地[13],并以本课题组筛选的农药降解菌HD为EDCs生物强化降解菌[14],考察其对EDCs的降解效能,以期为村落水环境中的EDCs降解机制及环境生态影响评价提供参考。
1. 材料与方法(Materials and methods)
1.1 试验装置与进水水质
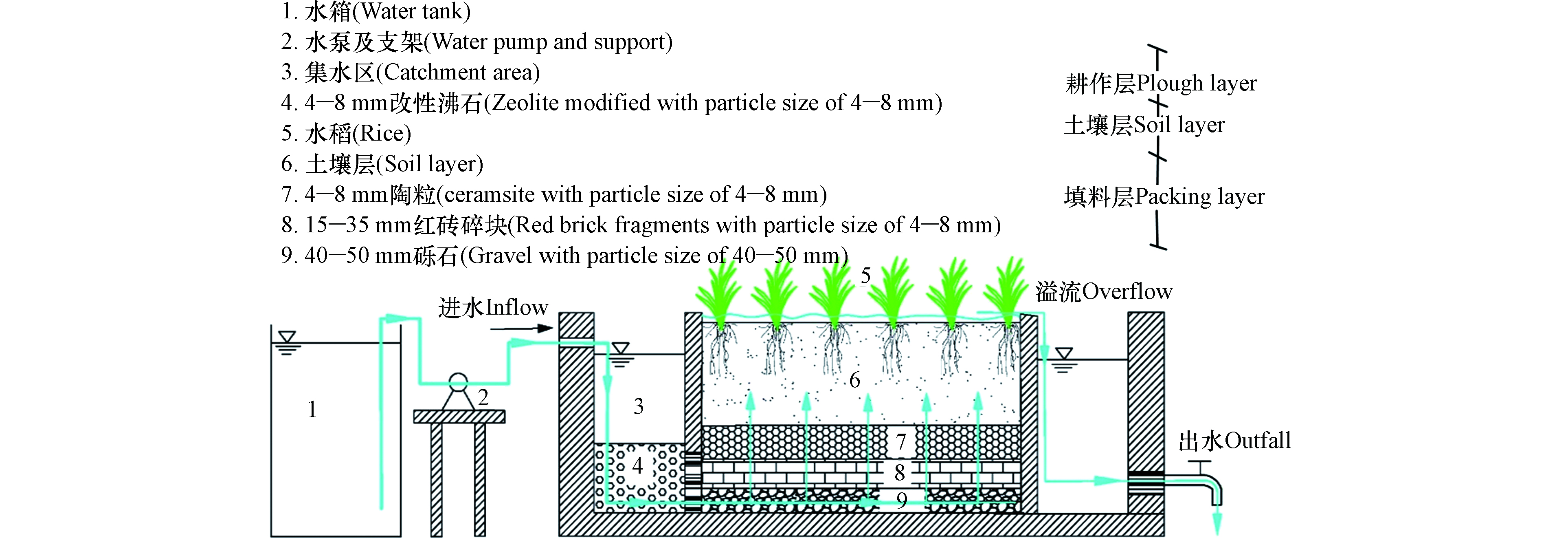
耕作型稻田湿地试验装置分2组,A组为空白对照组,B组为HD菌剂强化组。试验装置如图1所示,整个耕作型稻田湿地装置采用PP板(L×B×H=1 m×0.4 m×0.65 m),由集水区、湿地处理区和出水区3部分所组成,集水区沸石[15]层厚度200 mm,湿地填料层厚度300 mm,自下而上由40—50 mm砾石、15—35 mm红砖碎块、4—8 mm陶粒组成,孔隙率约30.8%;试验进水通过恒流水泵抽入集水区,经集水区的沸石层有效拦截后,再进入稻田湿地。装置内的土壤,取自常州洛阳镇薛家河周边稻田表层15—20 cm处土壤,所取土壤为该地区连年种植水稻土,装置内土壤层厚度为20 cm。耕作层厚度10 cm。水稻秧苗取自常州市洛阳镇薛家河周边水稻田中,种植密度为45株·m−2。
菌剂投加:A、B二组均采用自然进水法生物膜培养,当镜检可见填料上有褐色生物膜和原生动物及COD降解率超过60%时,认为生物挂膜成功。此时在B组中投加HD菌剂,配制100 mL的基础液体培养基(氯化钠:0.5 g,七水合硫酸镁:0.5 g,七水合硫酸亚铁:0.002 g,硫酸铵:1.5 g,氯化钙:0.04 g,磷酸氢二钾:1.5 g,磷酸二氢钾:1.5 g,蒸馏水:1 L,琼脂粉:20 g,pH:7.2—7.4),按照体积分数2.5%的比例接入菌种HD,培养48 h,将菌液混合后,再按照1%的投加比例混入进水中,随进水进入B组耕作型稻田湿地系统,连续投加2周,进行菌剂强化挂膜。A组不投菌,在正常条件下进行生物挂膜,为试验对照组。
农药降解菌HD筛选自南京某废弃农药厂的土壤中,是一株具有降解2,4-二氯苯酚能力的菌,现保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号:CGMCC No. 15123。经理化特性和分子鉴定判断属于摩式假单胞菌属(Pseudomonas mosselii)。
试验进水水质如表1所示。在生活污水的基础上添加少量内分泌干扰物,模拟进水内分泌干扰物浓度波动,如表2所示。
表 1 试验进水水质Table 1. Test water quality指标Index CODcr/(mg·L−1) 总磷/(mg L−1)TP 氨氮/(mg·L−1) NH+4 总氮/(mg·L−1)TN pH 范围 87—156 2.23—5.69 8.75—16.34 10.86—18.33 7.39—7.84 表 2 进水内分泌干扰物浓度(μg·L-1)Table 2. Concentration of endocrine disruptors in water inlet(μg·L-1)类固醇Steroid estrogen E1 Estrone E2 Estradiol EE2 17-α-ethinylestradiol E3 Estriol 原水浓度 10.13—15.25 0.79—1.1 0.88—1.82 6.31—9.58 模拟进水浓度 38.69—60.13 9.86—14.32 10.89—13.21 33.28—54.36 1.2 试验仪器与试剂
表 3 主要试验试剂Table 3. Main experimental reagents药品名称Drug names 分子式Molecular formula 规格Specification 生产单位Production unit E1 C18H22O2 — 阿拉丁 E2 C18H24O2 — 阿拉丁 E3 C18H24O3 — 阿拉丁 EE2 C20H24O3 — 阿拉丁 BSTFA C8H18F3NOSi2 — 阿拉丁 吡啶 C5H5N AR 永华化学科技(江苏) 丙酮 CH3COCH3 AR 国药 正己烷 C6H14 AR 江苏强盛功能化学 二氯甲烷 CH2Cl2 AR 永华化学科技(江苏) 雄烷 C19H23 — 北京谱析科技有限公司 表 4 试验主要仪器Table 4. Experimental main instruments仪器设备Instrument and equipment 型号Model number 生产单位Production unit 多用途高速离心机 SORVALL Thermo electron corporation 行星式球磨机 QM-1SP2 南京大学仪器厂 超声波细胞粉碎机 JY96-Ⅱ 宁波新芝生物科技股份有限公司 气质联用 Trace ISQLT 美国赛默飞科技有限公司 1.3 水样预处理
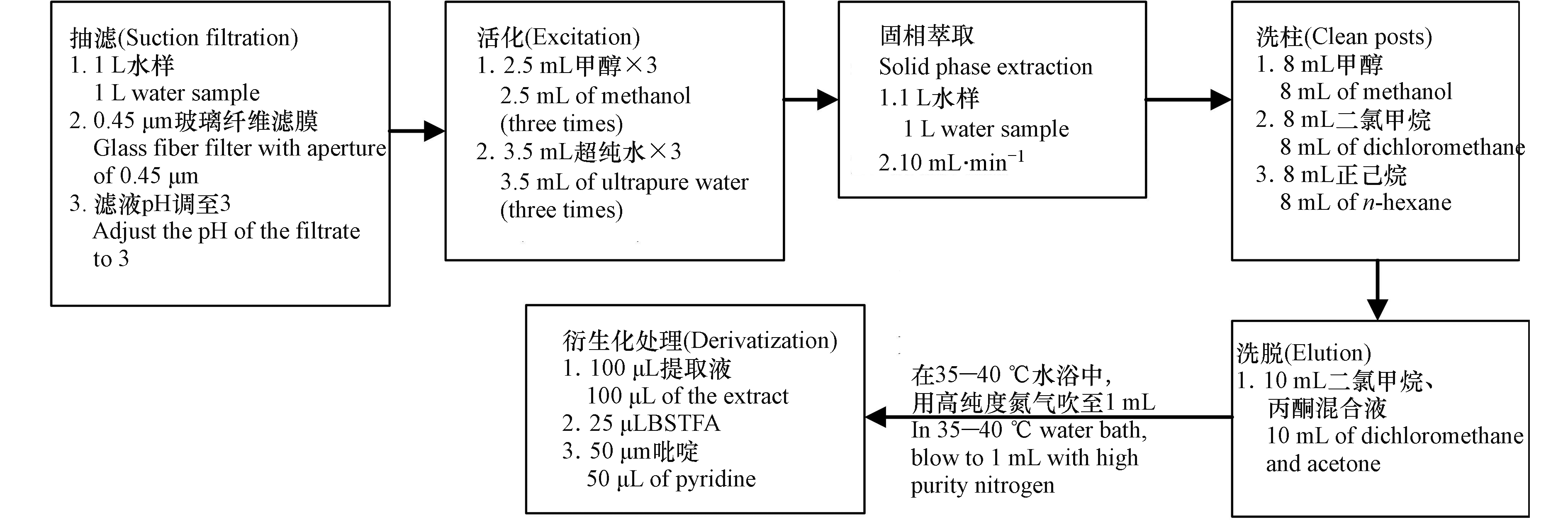
采集1 L水样,GF/F(0.45 μm)滤膜抽滤,滤液用99%的浓硫酸调节至pH3以下。
固相萃取:利用Simon Acti-Carb SPE柱进行固相萃取,首先活化SPE,分别加入2.5 mL甲醇3次,3.5 mL超纯水3次,控制流速在10 mL min−1,进行萃取,待水样萃取完,再分别加入8 mL甲醇、8 mL二氯甲烷、8 mL正己烷进行洗柱,最后用10 mL的二氯甲烷和丙酮的混合溶液淋洗,收集淋洗液,在35—40 ℃的水浴中,用高纯度氮气吹至1 mL,放入冰箱待用,具体步骤见图2。
1.4 土样预处理
稻田土壤采集后,自然风干,去除杂石杂草,用球磨机在400 r·min−1的条件下充分研磨,过20目筛网,混匀后放入冰箱待用。预处理时,称取1 g的样品,放入10 mL的离心管中,加入5 mL溶剂(甲醇∶丙酮=1∶1),超声波萃取10 min,随后以5000 r·min−1转速离心10 min,收集上清液至25 mL离心管中。重复以上步骤2次,合并上清液后,经高纯度氮气吹至1 mL后,定容至20 mL。最后按照图2水样预处理的方法,进行固相萃取。
1.5 衍生化处理
环境中类固醇类EDCs的含量相对较低,且由于这类化学物质都含有—OH官能团,极性较强,若直接采用气质联用测定,在测定过程中容易被色谱柱所吸附,从而造成实测浓度小于实际浓度,因此为降低该类物质的极性,提高其热稳定性,增加了衍生化步骤,即在正常衍生化的步骤中,又增添了吡啶,可以有效降低EE2的衍生产物转变为E1的衍生产物。黄成等[16]对某制药厂污水样品中E1、E2、E3和EE2衍生化后使用气相色谱/质谱法(GC-MS)分析表明,4种目标化合物的加标回收率达到(94.0%±2.9%)—(101.0%±3.8%),说明GC-MS法可应用于污水中雌激素化合物定量检测。
衍生化方法是在1.5 mL色谱进样瓶中加入100 μL的混合标液,通入高纯度氮气将其缓慢吹干,接着在进样瓶中加入25 μL BSTFA和50 μL吡啶,待其反应一定时间后吹干,最后加入V(二氯甲烷)∶V(正己烷)=1∶4的进样溶剂和10 μL 0.01 g·L−1的内标,取1 μL注入GC-MS分析,在空白污水样品中添加100,300、500 ng·L−1 等3个浓度水平的目标物,测定回收率。衍生化的具体反映结构变化如下:

1.6 EDCs的测定条件
试验中E1、E2、EE2、E3选用气质联用进行测定,色谱柱为TG-5MS(30 m×0.25 mm×0.25 μm),气相条件如下:
GC:以氦气为载气,流速1 mL·min−1;不分流方式进样,进样口温度280 ℃,进样体积1 μL;柱初始温度为50 ℃,保持2 min,以12 ℃·min−1程序升温至260 ℃,保持8 min,再以3 ℃·min−1升温至280 ℃,保持5 min;
MS:接口温度280 ℃,传输线温度300 ℃,离子源为EI源,温度250 ℃,电子轰击能量70 eV,溶剂延迟时间12 min,以全扫描模式定性,扫描范围50—600 m/z,以选择离子扫描模式定量;
根据其衍生产物的特征碎片离子分布特征来确定目标产物的实际浓度,衍生产物实际参数如表5所示。
表 5 衍生产物的相应参数Table 5. corresponding parameters of derivative products衍生产物Derivative product 保留时间/min Retention time 特征碎片离子(m/z)Characteristic fragment ion 线性回归方程Equation of linear regression TMS-E1 24.28 342、327、285 Y=(9.43×108)x+(1.02×109);R2=0.91 di-TMS-E2 25.43 416、401、285 Y=(1.08×107))x+(7.55×106);R2=0.91 di-TMS-EE2 27.03 440、425、285 Y=(1.90×107))x+(3.92×106);R2=0.92 Tri-TMS-E3 28.43 504、489、285 Y=(1.14×106)x+(2.38×106);R2=0.90 注:x为目标产物的实际浓度,单位mg·L−1,Y为色谱峰面积. Note:x is the actual concentration of the target product, unit: mg·L−1, Y is the peak area. 2. 结果与讨论(Results and discussion)
2.1 耕作型稻田湿地去除EDCs效能分析
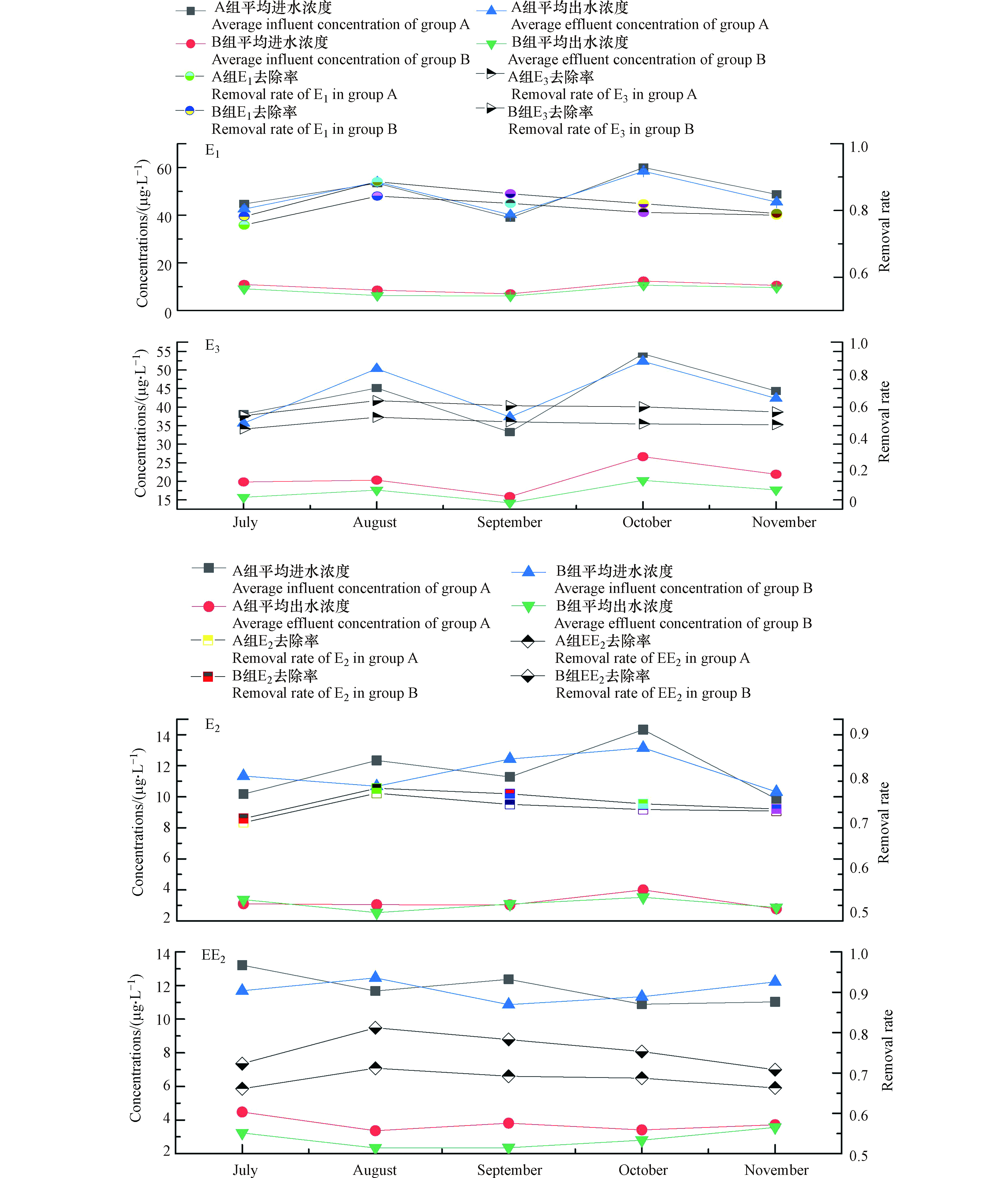
图3是2018年7月至11月,水稻生长过程中,耕作型稻田湿地对EDCs中E1、E2、EE2、E3的去除效果图。从图3可以看出,生活污水中EDCs通过耕作型稻田湿地吸附降解后,A组的E1、E2、EE2、E3的平均去除率为80.1%、72.4%、68.3%、51.4%,B组的平均去除率为82.6%、73.4%、75.6%、60.5%,除了E3外,其余各目标污染物的去除率均在65%以上,Baronti[17]在试验过程中发现E2在生物降解过程中,一部分的E2较易氧化转化成E1,遵循典型的醇氧化为酮原则,而E1通过水和作用又转化为E3,随着中间产物的不断产生,进而导致了出水E3浓度偏高。B组投加HD菌后,可能是假单胞菌HD诱导产生了羟基酶[18],相比A组E1、E2去除率未发生明显变化,EE2和E3去除率增高7%—9%,Huang等[19]发现,在BPA(双酚A)降解的河流底泥中,假单胞菌和鞘单胞菌占据了原有细菌群落的73%,由此可见,向湿地中投加假单胞菌HD有助于提高EDCs的去除率。
湿地经过5个月的连续运行后,投菌组B中的EDCs残留量明显低于未投菌组A。由图3中的实测数据,经计算B组湿地出水中E1、E2、E3和EE2含量相比A组分别降低约26.6%、17.1%、30.3%、13.3%。试验时间跨秋夏两季,夏季EDCs的去除效果要明显优于秋季,这主要是因为夏季正值水稻生长期,水稻根系对EDCs有一定吸收作用,夏季温度较高,微生物活性较强,微生物新陈代谢较为旺盛,运行至秋季时,温度降低,水稻收割,微生物活性逐渐降低,EDCs的降解率并未大幅下降,说明人工湿地中填料层及土壤层对EDCs的去除起到了一定作用。
2.2 HD菌剂强化后耕作型稻田湿地各生物单元对EDCs去除分析
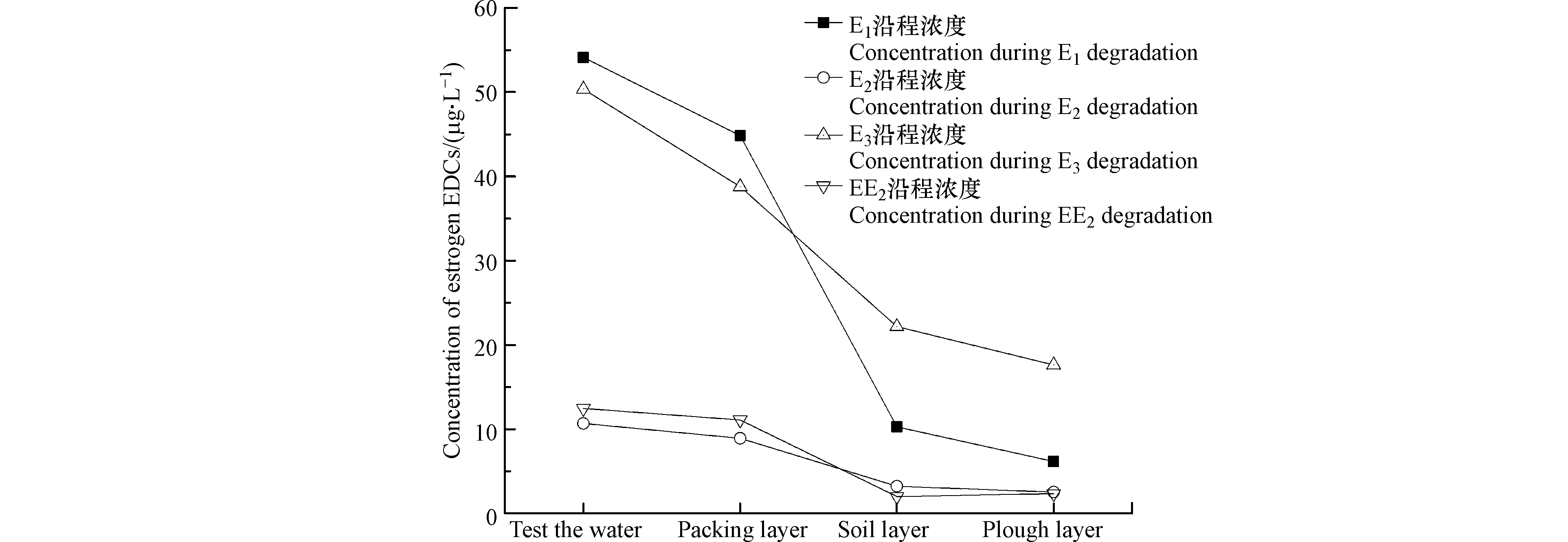
图4为耕作型稻田湿地经HD菌剂强化后EDCs浓度变化趋势图,沿程对E1、E2、E3和EE2的总去除率分别为88.6%、76.3%、64.8%和81.2%。3个生物单元填料层、土壤层、耕作层对E1去除率分别为16.2%、75.1%、28.2%,对E2去除率分别为14.5%、61.8%、18.7%,对E3去除率分别为20.6%、49.8%、10.4%,对EE2去除率分别为8.9%、43.4%、-8.1%,显然土壤层对EDCs的去除贡献占比相对最大,主要是因为土壤中微生物种群丰度要远高于填料层孔隙中生物膜上的微生物种群丰度,同时,土壤中还有分布广泛的水稻根系,通过其根系的泌氧作用,刺激微生物活性,促进微生物新陈代谢,进而加强了微生物降解能力,而填料层的填料作为微生物的代谢场所[20],其主要作用有二:一是直接吸附EDCs,二是作为微生物的载体,在其表面形成微生物集聚(生物膜),为生物膜微生物吸附、吸收、降解EDCs提供平台。其中E1、E2、E3的降解沿程越往后,目标污染物浓度越低,但EE2在经过土壤层的降解后,其浓度却略有提升,一方面,据Ascenzo等[21]研究显示,EE2的生物降解只发生在好氧段,因为EE2拥有乙炔基,从空间结构上来看,这对基团基质和受体的结合有阻碍作用,使得酶活性表达受阻,且在厌氧阶段,会使其由结合态变为游离态,导致EE2不易被降解,另一方面,Li等[22]研究发现,EE2在厌氧条件下更有利用吸附,耕作层分布有植物根系,植物根系的泌氧作用使得填料层吸附作用相比土壤层较弱。同时在降解过程中E3的含量在进水时略低于E1,但随着沿程越往后E3出水浓度高于E1,因为E2在生物降解过程中,一部分的E2较易氧化转化成E1,而E1通过水和作用又转化为E3,随着中间产物的不断产生,进而导致出水E3浓度偏高。
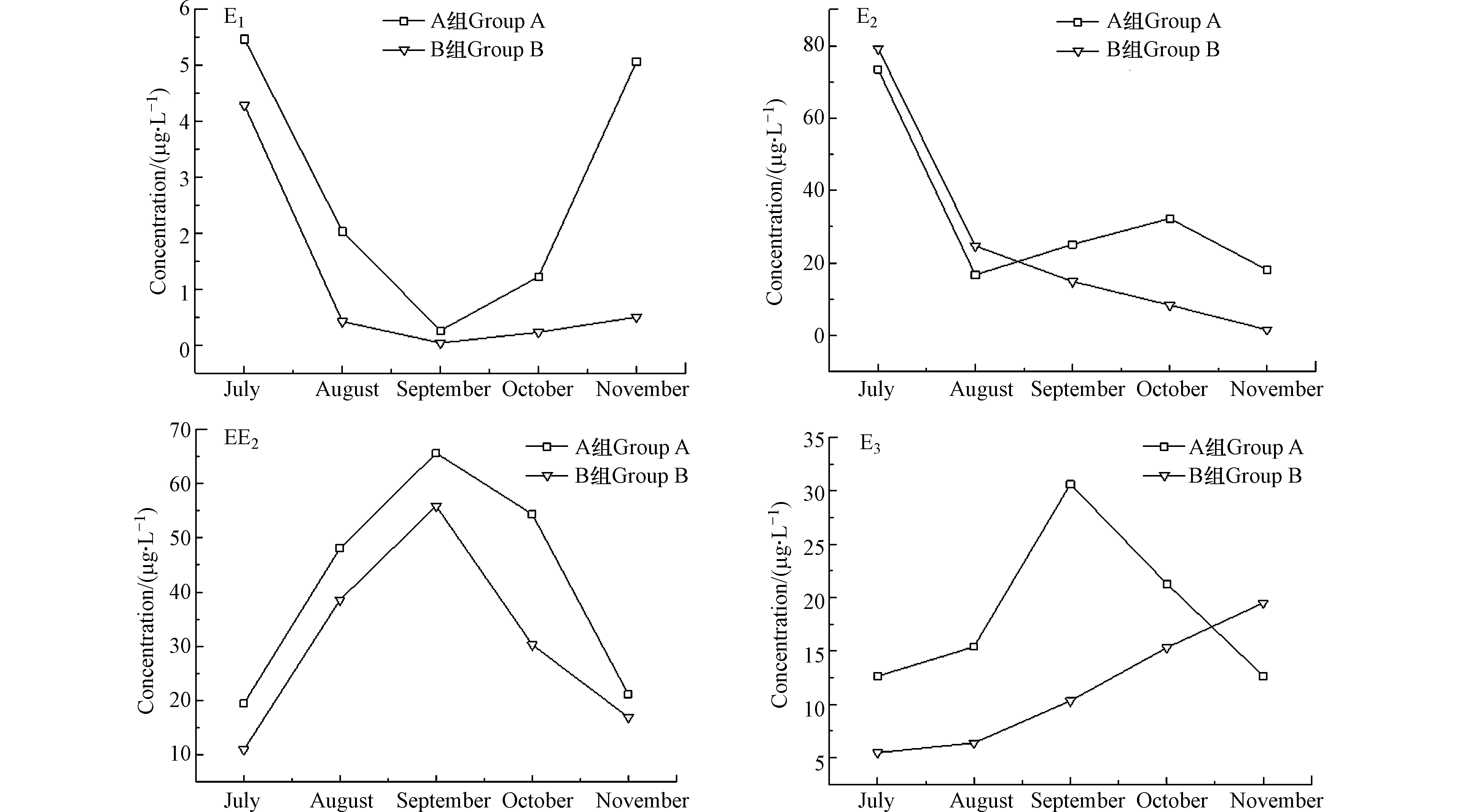
2.3 耕作型稻田湿地水芹种植期土壤中残留EDCs的变化特征
类固醇类EDCs多半有亲脂疏水的特性,易被土壤所吸附,一般类固醇类EDCs在环境中的半衰期为5—25 d不等,土壤中残留的EDCs会在一定时期,通过迁移、浸出到水体中,所以稻田湿地水体中EDCs含量通常偏高[23]。图5反应了耕作型稻田湿地净化过程中,土壤中残留EDCs含量的变化趋势,可看出投菌组B中E1、E2、EE2残留量明显小于A组,可见稻田湿地微生物对EDCs进行生物降解时,反硝化假单胞菌[24]使得反硝化细菌种群丰度提升,有利于E1的生物降解,说明HD菌促进了土壤层中羟基酶的产生,提高了其对EDCs的去除效率。从图5可看出,EE2浓度是先增后减,可能是由于EE2较为稳定不易降解。Ternes等[25]研究EE2的生物降解特性,发现1 mg·L−1的EE2经24 h后几乎无降解。10月水稻收割后,新种植了水芹,据Schroeder等[26]研究发现水芹在24 h内便能通过茎部富集近0.9 ng·L−1的EE2,所以后期EE2浓度又显下降趋势。B组中E3浓度一直呈上升趋势,任海燕等[27]研究发现,对EE2降解中间产物进行质谱分析推测,EE2在降解过程中首先被氧化为E1,后经过一系列生物催化作用生成2-羟基-2,4-二烯-戊酸和2-羟基-2,4-二烯-1,6-己二酸两种中间代谢产物,E1通过水合作转化为E3,又E2在生物降解过程中部分较易被氧化转化为E1,E1通过水合作用又转化为E3,故而导致土壤中E3浓度不断增高。湿地运行初期E1、E2浓度分别增加了85%、25%,EE2、E3浓度下降了60%、30%,这主要是因为生活污水中EDCs的构成主要以天然雌激素中的E1、E2为主,且其主要为结合态形式,极性更强,更易被土壤所吸收[28],且溶解性有机物的共轭物在经细菌酶分解时,亦会产生E1的衍生产物[29],进而导致E1浓度提高。虽然土壤层对于EDCs的降解效果较好,但初期由于土壤中生物种群尚未稳定,所以导致E1、E2的处理效果受限。
3. 结论(Conclusions)
(1)未投菌的A组对雌酮(E1)、雌二醇(E2)、雌三醇(E3)及17α-乙炔基雌二醇(EE2)的平均去除率分别为80.1%、72.4%、51.4%、68.3%,投加HD菌剂强化的B组平均去除率分别为82.6%、73.4%、60.5%、75.6%,A、B两组耕作型稻田湿地对E3去除率相比E1、E2、EE2最低。E2在生物降解过程中较易氧化转化成E1,而E1通过水和作用又转化为E3,随着中间产物的不断产生,出水E3浓度增大。A、B两组耕作型稻田湿地中,除E3外E1、E2、EE2去除率均在65%以上,EE2的生物降解只发生在好氧段,EE2拥有乙炔基,从空间结构上来看,这对基团基质和受体的结合有阻碍作用,使得酶活性表达受阻,且在厌氧阶段,会使其由结合态变为游离态,致使EE2不易被降解。
(2)投加HD菌后,耕作型稻田湿地对E1、E2、E3和EE2的总去除率分别为88.6%、76.3%、64.8%和81.2%。耕作层、土壤层、填料层3个生物单元对EDCs(E1、E2、E3、EE2)去除效果均有提升,其中:对E1去除率分别为16.2%、75.1%、28.2%;对E2去除率分别为14.5%、61.8%、18.7%;对E3去除率分别为20.6%、49.8%、10.4%;对EE2去除率分别为8.9%、43.4%、−8.1%。HD菌对耕作型稻田湿地中微生物群落产生影响,诱导产生的羟基酶有利于降解EDCs,从而提高了EDCs的去除效率。耕作型稻田湿地经HD菌剂强化后,3个生物单元中明显土壤层对EDCs去除贡献相对较大,土壤层微生物种群丰度更大,且土壤层中还分布有广泛的水稻根系,不仅为微生物代谢提供营养物质和氧气,还进一步提高了其生物分解能力。
(3)湿地运行初期,耕作型稻田背景土壤中残留的EDCs含量相对较高,经过5个月的连续运行后,土壤中EDCs含量明显下降,投菌组B中的EDCs残留量要明显低于未投菌组A,B组湿地出水中E1、E2、E3和EE2含量相比A组可分别降低约26.6%、17.1%、30.3%、13.3%。表明HD菌剂能强化耕作型稻田湿地土壤中EDCs的降解。本研究对于村落水环境中的EDCs降解机制及环境生态影响评价有一定的参考价值。
-
表 1 污泥、煤炭及混合样收到基工业、元素及低位热值分析
Table 1. Analysis of proximate, element and low calorific value of sludge, coal and mixed samples as received basis
样品种类 工业分析/% 元素分析/% 低位发热量/(kJ·kg−1) 水分 灰分 挥发分 固定碳 C H N S O 干污泥 35.27 32.89 30.71 1.19 15.22 2.46 1.83 2.83 9.50 6 137.93 煤炭 10.76 10.72 28.80 49.74 65.46 3.78 0.92 0.29 8.09 25 669 干污泥与煤混合物 26.03 24.53 29.99 19.50 34.16 2.96 1.49 1.87 8.97 13 501.14 表 2 2021年1-4月项目运营情况
Table 2. Project operation from January to April 2021 t
月份 进厂污泥量 干化机湿污泥进料量 干化机干污泥出料量 干污泥焚烧量 主蒸汽量 1 74 800 51 642 28 403 51 561 140 290 2 37 800 27 055 14 880 25 625 83 523.25 3 72 700 53 220 29 271 48 751 382 427.75 4 81 000 56 626 31 144 55 518 379 050.75 表 3 7台污泥干化机运行参数
Table 3. Operating parameters of 7 sludge dryers
序号 饱和蒸汽温度/℃ 饱和蒸汽压力/MPa 饱和蒸汽流量/(t·h−1) 湿污泥温度/℃ 湿污泥流量/(t·h−1) 疏水温度/℃ 疏水流量/(t·h−1) 干污泥温度/℃ 干污泥流量/(t·h−1) 尾气温度/℃ 不凝性气体流量/(t·h−1) 水蒸汽流量/(t·h−1) 1 155.50 0.55 4.11 16.00 5.06 108.21 4.11 68.01 1.67 102.01 0.010 3.38 2 154.10 0.53 3.92 16.00 4.93 107.23 3.92 64.50 1.64 101.39 0.018 3.27 3 154.10 0.53 3.83 16.00 4.83 107.12 3.83 64.10 1.65 101.10 0.009 3.17 4 154.10 0.53 3.80 16.00 4.86 107.05 3.80 64.90 1.68 100.10 0.014 3.17 5 154.10 0.53 3.84 16.00 4.89 107.10 3.84 63.11 1.68 100.61 0.004 3.21 6 153.40 0.52 3.42 16.00 4.41 106.99 3.42 62.24 1.61 100.24 0.013 2.79 7 153.40 0.52 3.41 16.00 4.40 107.01 3.41 63.12 1.59 100.12 0.005 2.80 表 4 不凝性气体组分及体积分数
Table 4. Composition and volume fraction of non-condensable gases
组分 体积分数/% NH3 75.38 C3H8 9.72 HCN 6.63 CH4 4.58 CH3COOH 2.75 HCOOH 0.51 HF 0.32 HCl 0.11 表 5 锅炉效率计算中部分物理量取值
Table 5. Values of some physical quantities in boiler efficiency calculation
符号 单位 数值 adz — 0.3 afh — 0.7 apz — 2.0% hpz kJ·kg-1 767.0 afz — 1.0% hfz kJ·kg-1 125.0 abz — 1.0% hbz kJ·kg-1 40.5 表 6 污泥填埋气无组织排放参数表[19]
Table 6. Unorganized discharge parameter table of sludge landfill gas[19]
t·t−1 气体种类 中值 最小值 最大值 化石源CO2 0.020 5 0.013 5 0.037 生物源CO2 0.341 9 0.086 8 0.597 CH4 0.035 2 0.013 4 0.090 2 N2O 0.006 8 0 0.025 1 表 7 近年大气现代碳比值监测值[24]
Table 7. Monitoring values of atmospheric modern carbon ratio in recent years[24]
监测年份 Fmatm 2017 1.010 2018 1.005 2019 1 2020 1 2021 1 2022 1 表 8 2种燃料种类下的锅炉热平衡表
Table 8. Boiler heat balance table under 2 fuel types %
燃料种类 q4,i q3,i q2,i q5,i q6,i ηb,i 干污泥∶煤炭=0.623∶0.377 1.01 0.50 7.75 0.60 0.68 89.46 煤炭 0.23 0.50 6.98 0.60 0.16 91.52 表 9 燃料理论消耗量对比表
Table 9. Comparison of theoretical fuel consumption
参数名称 单位 燃料种类 煤炭 干污泥∶煤炭=0.623∶0.377 锅炉效率 % 91.52 89.46 燃料理论消耗量 ×104 t 14.94 29.06 煤炭理论消耗量 ×104 t 14.94 10.96 干污泥理论消耗量 ×104 t 0 18.10 -
[1] 戴晓虎. 我国污泥处理处置现状及发展趋势[J]. 科学, 2020, 72(6): 30-34. [2] 赵刚, 唐建国, 徐竟成, 等. 中美典型污泥处理处置工程能耗和碳排放比较分析[J]. 环境工程, 2022, 40(12): 9-16. [3] IPCC. 2019 refinement to the 2006 IPCC guidelines for national greenhouse gas inventory[EB/OL]. [2022-08-18]. https://www.ipcc.ch/report/2019-refinement-to-the-2006-ipcc-guidelines-for-national-greenhouse-gas-inventories/, 2019. [4] KANG S, CHO C, KIM K H, et al. Fossil carbon fraction and measuring cycle for sewage sludge waste incineration[J]. Sustainability, 2018, 10(8): 2790. doi: 10.3390/su10082790 [5] 纪莎莎. 污泥干化焚烧工艺碳排放研究及优化策略[J]. 环境科技, 2019, 32(1): 49-53. [6] 李哲坤, 张立秋, 杜子文, 等. 城市污泥不同处理处置工艺路线碳排放比较[J]. 环境科学, 2023, 44(2): 1181-1190. [7] 李欢, 金宜英, 李洋洋. 污水污泥处理的碳排放及其低碳化策略[J]. 土木建筑与环境工程, 2011, 33(2): 117-121. [8] 杨旭冉, 庞义俊, 何明, 等. 用于AMS测量的~(14)C样品制备方法[J]. 同位素, 2015, 28(2): 65-68. [9] 刘圣华, 杨育振, 徐胜, 等. 加速器质谱~(14)C制样真空系统及石墨制备方法研究[J]. 岩矿测试, 2019, 38(3): 270-279. [10] 王丽花, 吕国钧, 王飞, 等. 污泥干化焚烧系统的节能降耗研究[J]. 中国给水排水, 2021, 37(4): 29-36. [11] 孙奇, 余辉, 朱方兵, 等. 圆盘干燥深度脱水污泥的中试研究[J]. 环境工程, 2016, 34(10): 118-123. [12] 周强泰, 周克毅, 冷伟, 等. 锅炉原理[J]. 3版. 北京:中国电力出版社, 2013: 150-156. [13] 宋宝木, 秦华鹏, 马共强. 污水处理厂运行阶段碳排放动态变化分析: 以深圳某污水处理厂为例[J]. 环境科学与技术, 2015, 38(10): 204-209. [14] 次瀚林, 王先恺, 董滨. 不同污泥干化焚烧技术路线全链条碳足迹分析[J]. 净水技术, 2021, 40(6): 77-82. [15] 全国能源基础与管理标准化技术委员会. 综合能耗计算通则: GB/T 2589-2020[S]. 北京: 中国标准出版社, 2020. [16] 陈莉佳, 许太明, 卢宇飞. 市政污泥脱水-干化-焚烧不同工艺路线碳排放分析[J]. 净水技术, 2019, 38(S1): 155-159. [17] 中华人民共和国生态环境部. 《2019年度减排项目中国区域电网基准线排放因子》[EB/OL]. [2022-08-18]. https://www.mee.gov.cn/ywgz/ydqhbh/wsqtkz/202012/t20201229_815386.shtml. [18] 刘立涛, 张艳, 沈镭, 等. 水泥生产的碳排放因子研究进展[J]. 资源科学, 2014, 36(1): 110-119. [19] PAN Y R, WANG X, REN Z J, et al. Characterization of implementation limits and identification of optimization strategies for sustainable water resource recovery through life cycle impact analysis[J]. Environment International, 2019, 133(Part B): 105266. [20] 刘鹏, 朱乃若, 熊唯, 等. 污泥深度脱水处理与处置工艺的COD及碳减排分析[J]. 环境卫生工程, 2012, 20(1): 9-12. [21] 王琳, 李德彬, 刘子为, 等. 污泥处理处置路径碳排放分析[J]. 中国环境科学, 2022, 42(5): 2404-2412. [22] 蒋玲燕. 上海某污水处理厂污泥深度脱水运行优化探索[J]. 给水排水, 2019, 55(9): 25-28. [23] 林文聪, 赵刚, 刘伟, 等. 污水厂污泥典型处理处置工艺碳排放核算研究[J]. 环境工程, 2017, 35(7): 175-179. [24] ASTM International. Standard test methods for determining the biobased content of solid, liquid, and gaseous samples using radiocarbon analysis: ASTM D6866[S]. United States, 2021. [25] 颜永全, 王玉君, 曾祥梅. 纺织工业与化学工业——分析潍坊纺织业[J]. 山东纺织经济, 2021(10): 22-25. [26] 李博, 王飞, 朱小玲, 等. 污泥干化焚烧联用系统最佳运行工况研究[J]. 环境污染与防治, 2014, 36(8): 29-33. doi: 10.3969/j.issn.1001-3865.2014.08.005 [27] 程晓波, 李博, 王飞, 等. 上海市竹园污泥干化焚烧系统的能量平衡分析[J]. 节能, 2011, 30(10): 15-18. doi: 10.3969/j.issn.1004-7948.2011.10.004 [28] 陈少卿. 污泥在桨叶干燥机内干燥的模拟和试验研究[D]. 杭州: 浙江大学, 2018. [29] LAW Y, JACOBSEN G E, SMITH A M, et al. Fossil organic carbon in wastewater and its fate in treatment plants[J]. Water Research, 2013, 47(14): 5270-5281. doi: 10.1016/j.watres.2013.06.002 -






 下载:
下载: