-
水质安全是污水排放与再生回用的关键。病原微生物风险是保障水质安全需要优先控制的问题。总大肠菌群、粪大肠菌群和大肠埃希氏菌(E.coli)常被作为粪便污染的指示微生物,被国内外学者广泛用于评价水的生物安全性[1]。大肠菌群主要以粪口途径传播、通过侵染肠道系统引发疾病,甚至危及人的生命[2]。污水处理厂既是各种污水的汇集地,又是污水经过处理达到一定标准后重新回到生态系统或加以再生利用的重要环节[3]。污水处理厂被认为是大肠菌群的重要来源及传播场所[4]。消毒作为污水处理的最后一道工序,在灭活病原微生物、减少水传染疾病的传播等方面发挥着重要作用。在污水处理厂中,通常采用UV或NaClO消毒对大肠菌群进行灭活[5]。
有研究表明,NaClO消毒可有效灭活细菌,同时水中残留的氯具有持续消毒作用,可保证消毒后水的生物稳定性,但次氯酸钠消毒会产生消毒副产物(DBPs),威胁再生水的用水安全[6]。UV消毒可以在较低剂量下有效灭活病原微生物[7],但UV消毒无持续杀菌能力,且经UV消毒后部分细菌难以被完全杀灭而处于亚致死或活的但不可培养状态[8],这些细菌可在一定条件下通过光复活或暗修复的方式重新获得活性,进而增加再生水储存和输送过程中病原微生物二次滋生的潜在风险。
迄今为止,已有学者在UV-NaClO顺序消毒灭活病原微生物方面开展了相关的研究工作[9-10],但达到与UV或NaClO相同的消毒效果时,UV-NaClO顺序消毒在投加量的优势,消毒后水在输送,储存及再生利用过程中UV-NaClO顺序消毒控制大肠菌群二次滋生的研究却相对较少。本研究以青岛市某市政污水处理厂消毒前的深度处理出水为研究对象,分别采用UV、NaClO以及UV-NaClO顺序消毒,对比分析了在达到排放要求以及再生水不同回用标准时,UV-NaClO顺序消毒对微生物光复活与暗修复的抑制能力及其对DBPs生成量的削减作用。本研究结果可为强化污水消毒,降低污水排放与再生回用的生物安全风险提供参考。
-
本实验原水取自青岛市某市政污水处理厂,该厂进水主要为生活污水,生物处理采用A2O+MBBR工艺,深度处理工艺为混凝/沉淀/过滤及UV消毒工艺,实验期间该厂过滤后出水,水质的pH为6.93~7.17、PO43--P为0.11~0.19 mg·L−1、NH4+-N为2.26~3.40 mg·L−1、COD为27.00~30.00 mg·L−1、TOC为9.01~11.10 mg·L−1和浊度为1.69~2.94 NTU。采用经过灭菌处理的取样设备取该厂过滤后出水,将水样于4 ℃下保存并尽快进行消毒实验。
-
通过系列实验研究了不同消毒方式消毒后污水中大肠菌群的灭活效果、复活特性和DBPs生成的影响。每个实验均设3次重复。
1) UV消毒实验。UV消毒实验在自制的平行光束仪下进行。平行光束仪上部有2个功率为20 W的UV灯管,开启UV灯30 min后,用紫外辐照计检测紫外线强度。每次实验时将300 mL水样注入500 mL灭菌后的烧杯中,放入灭菌后的转子,将烧杯置于磁力搅拌器上均匀接受UV辐射,通过调节紫外强度和照射时间确定紫外辐射剂量[11]。
2) NaClO消毒实验。将一定量的NaClO溶液投加到已盛装一定体积水样的500 mL灭菌烧杯中,在磁力搅拌器的搅拌作用下接触反应30 min,用硫代硫酸钠终止反应,取消毒反应前后的水样测定其中的大肠菌群类微生物的数量。
3) UV-NaClO顺序消毒实验。将水样先经一定剂量的UV消毒后,再向其中投加一定量的NaClO溶液,在磁力搅拌器的搅动作用下消毒反应30 min,用硫代硫酸钠终止反应。
4)光复活和暗修复实验。取一定剂量消毒后的水样,分别在日光灯照射(光复活)或避光(暗修复)条件下于25 ℃恒温搅拌放置一定时间,期间定时取样,测定细菌的菌落数。
-
采用孔径为0.45 μm的滤膜对消毒前后的水样进行预处理,之后采用滤膜法对大肠菌群进行测定。截留了菌体的滤膜分为3份,1份置于品红亚硫酸钠培养基上,于37 ℃下培养24 h后转至乳糖蛋白胨半固体培养基上,于37 ℃下培养6~8 h,测定总大肠菌群的数量;1份置于M-FC培养基上,于45 ℃下培养24 h后测定粪大肠菌群的数量;1份置于品红亚硫酸钠培养基上,于37 ℃下培养24 h后转至MUG培养基上,于37 ℃下继续培养4 h后,计算大肠埃希氏菌(E.coli)的菌落数。采用顶空气相色谱法测定水中DBPs的浓度[12]。
-
采用对数灭活率来评价消毒后细菌的灭活效果,灭活率根据式(1)进行计算。利用复活百分比来表征光复活和暗修复程度,复活率百分比根据式(2)进行计算。
式中:A为灭活率,%;B为复活百分比,%;N0和N分别为消毒前和消毒后水样中的大肠菌群数量,CFU·L−1;NP 为光复活或暗修复后水样中的大肠菌群数量,CFU·L−1。
-
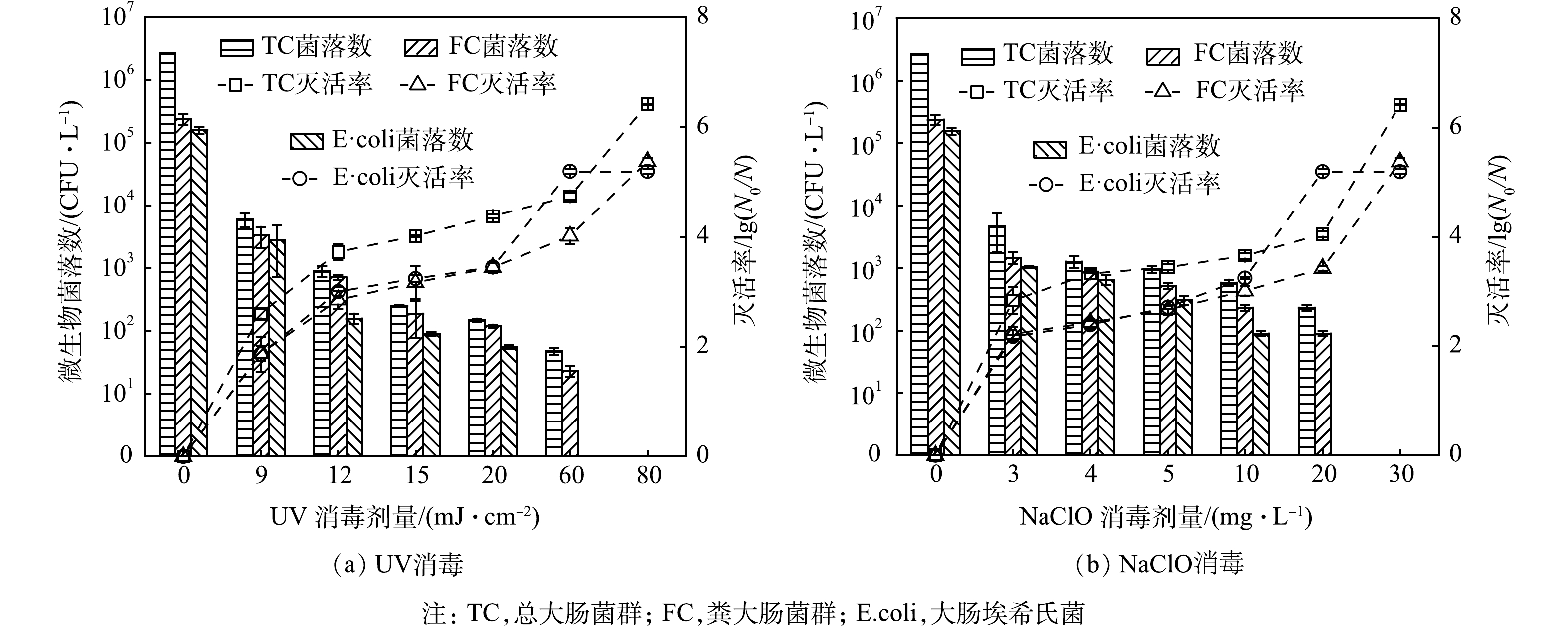
不同剂量下单独UV消毒或NaClO消毒对总大肠菌群、粪大肠菌群和大肠埃希氏菌(E.coli)的灭活情况如图1所示。消毒剂量对大肠菌群类微生物的灭活影响较大,随着UV剂量或NaClO投加量的增加,大肠菌群数量随之下降。当UV剂量仅为12 mJ·cm−2时,大肠菌群类微生物的灭活率即可达到接近或超过3个对数级;当NaClO投加量仅为3 mg·L−1时,大肠菌群类微生物可达到2个对数级的灭活率。此后,进一步增加消毒剂量,微生物数量下降幅度趋缓,如当UV剂量由12 mJ·cm−2增加到60 mJ·cm−2时,总大肠菌群和粪大肠菌群的灭活率仅提高不足1个对数级,当NaClO的投加量从3 mg·L−1增加到20 mg·L−1时,总大肠菌群的灭活率也仅增加了1.22个对数级。相较于其他的粪大肠菌,E.coli更易被灭活,当UV剂量达到60 mJ·cm−2时,已检测不到E.coli。完全灭活总大肠菌群或粪大肠菌群需要80 mJ·cm−2 UV或30 mg·L−1 NaClO。
当UV消毒剂量达到12 mJ·cm−2和20 mJ·cm−2时,粪大肠菌群数量可分别满足《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A排放标准[13](简称“一级A标准”)中“≤1 000 CFU·L−1”以及《城市污水再生利用绿地灌溉水质》(GB/T 25499-2010)(简称“绿地灌溉标准”)中非限制性绿地的“≤200 CFU·L−1”的要求[14]。当UV消毒剂量达到60 mJ·cm−2时,E.coli可满足《城市污水再生利用 城市杂用水水质》(GB/T 18920-2020)中“大肠埃希氏菌不得检出”的要求[15](简称“杂用水标准”)[16]。消毒后的水样要达到一级A标准、绿地灌溉标准以及杂用水标准,NaClO投加量分别需达到4、10和20 mg·L−1。
-
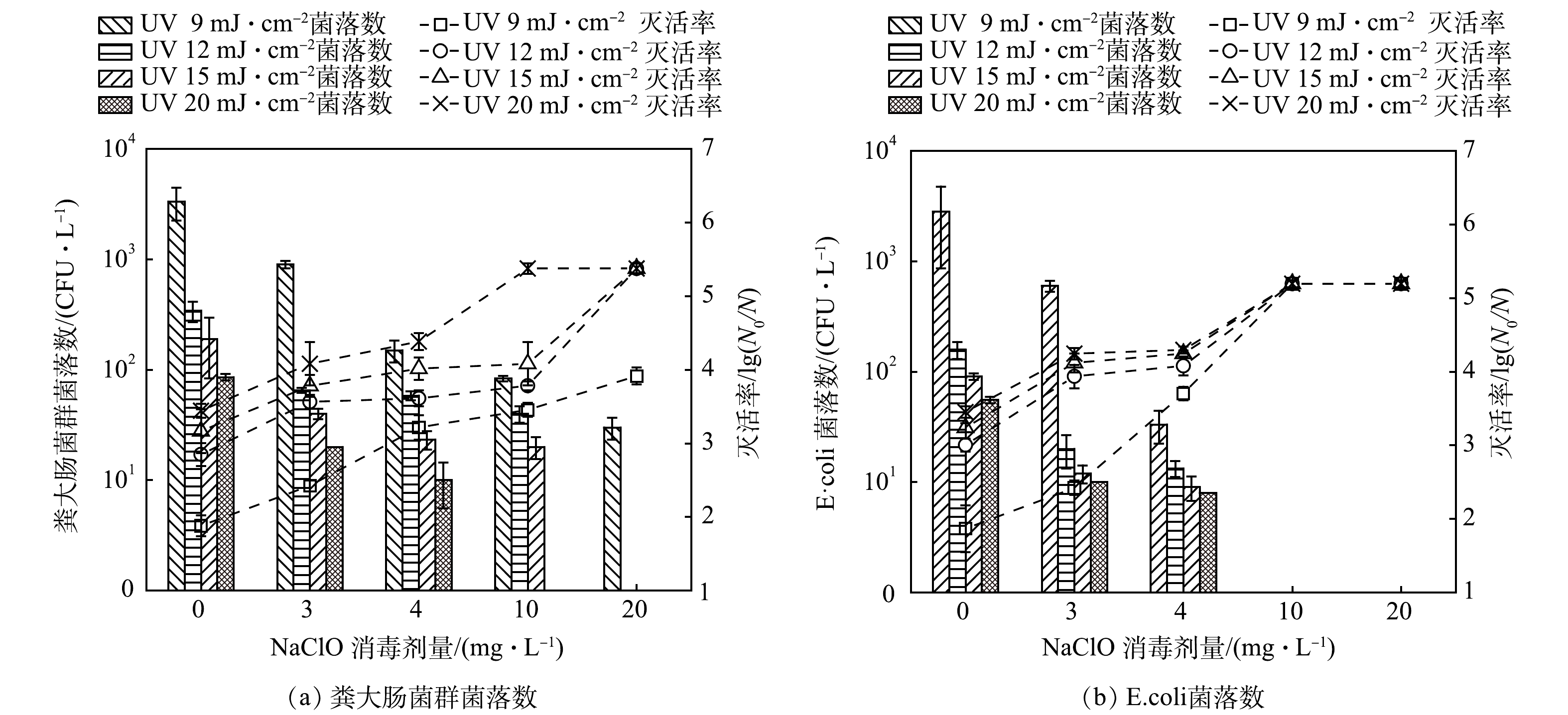
为探究UV-NaClO顺序消毒应用于污水消毒的可行性,在不同UV和NaClO剂量组合条件下分析了UV-NaClO顺序消毒对水样中大肠菌群的灭活效果,结果如图2所示。UV-NaClO顺序消毒更有利于大肠菌群的灭活,顺序消毒的效果好于UV或NaClO单独消毒的效果。仅采用UV消毒,当UV剂量为9 mJ·cm−2时,粪大肠菌群的菌落数可由2.4×105 CFU·L−1降至3.4×103 CFU·L−1;仅采用NaClO消毒,当NaClO投加量为3 mg·L−1时,消毒后粪大肠菌群的数量降为1.5×103 CFU·L−1;若采用UV-NaClO 顺序消毒,UV和NaClO的剂量分别为9 mJ·cm−2和3 mg·L−1时,消毒后粪大肠菌群的数量可降至9.0×102 CFU·L−1,与单独UV或单独NaClO消毒相比,粪大肠菌群的数量分别降低了73.5%和40.0%。
表1对比了达到不同处理效果时不同消毒方式所需消毒剂的最低投加量。由对比结果可知,采用UV-NaClO顺序消毒,可以在相对较低的消毒剂投加量下就可达到单一消毒剂在较高剂量下所达到的消毒效果,尤其是当需要达到的排放标准较高时,采用UV-NaClO顺序消毒的优势更加明显。例如,当出水仅需满足一级A标准,即粪大肠菌群数量≤1000 CFU·L−1时,采用UV-NaClO顺序消毒需要的UV及NaClO剂量分别为9 mJ·cm−2和3 mg·L−1,同单独UV或NaClO消毒在消毒剂投加量上相比未表现出较大优势;若出水需满足杂用水标准规定的E.coli不得检出的要求,单独UV或NaClO消毒需要的UV或NaClO剂量分别为60 mJ·cm−2或20 mg·L−1,而采用UV-NaClO顺序消毒则仅需9 mJ·cm−2 UV和10 mg·L−1 NaClO。若达到完全灭活粪大肠菌群的目标,UV-NaClO顺序消毒在投加量上的优势则更加明显。
UV-NaClO顺序消毒相比单一消毒剂所具有的优势,可能是由于微生物对不同消毒方式的耐受程度不同。有研究表明,经UV消毒后磺胺类抗生素耐药菌的比例显著升高,而低剂量的NaClO消毒则能有效降低此类细菌的比例[17-18],因而投加低剂量的NaClO即可达到或超过高剂量UV消毒所达到的效果。同样有一些细菌(Cryptosporidium)对氯消毒具有很强的耐受能力[19],对于这类细菌采用低剂量的UV辐射也可能达到较好的灭活效率。因而,UV-NaClO顺序消毒中UV和NaClO具有协同效应,可以灭活单一消毒剂所不能完全灭活的微生物,且可以在UV和NaClO剂量均不高的组合方式下即可达到更优的消毒效果。
-
在满足相同出水标准时,经UV-NaClO顺序消毒后微生物的复活能力明显低于单独UV消毒(图3),尤其是当NaClO的投加量较高时,对微生物复活的抑制作用更为明显。在满足一级A排放标准的消毒剂投加量下,单独UV(12 mJ·cm−2)消毒后分别经24 h光复活和暗修复后,粪大肠菌群的复活率为7.97%和4.96%,而经UV-NaClO(UV剂量9 mJ·cm−2和3 mg·L−1 NaClO )顺序消毒后粪大肠菌群复活率仅为3.21%和0.84%,较单独UV消毒分别减少了4.76%和4.12%。当UV剂量不变,NaClO投加量增加到4 mg·L−1时,UV-NaClO顺序消毒后在相同的复活时间内,粪大肠菌群的复活率仅为0.3%(光复活)和0.01%(暗修复),虽然NaClO投加量仅增加了1 mg·L−1,但细菌复活率明显降低。
当UV剂量为60 mJ·cm−2时,单独UV消毒可完全灭活E.coli,但在光照下经3 h复活后,E.coli的数量即可增加为33 CFU·L−1;经24 h的暗修复,E·coli可增加至66 CFU·L−1(图3(e))。采用UV-NaClO顺序消毒,当UV剂量为9 mJ·cm−2和NaClO投加量10 mg·L−1也可完全灭活E.coli,但是,消毒后的水样无论是在光照下还是在暗处,24 h内均未出现细菌复活的现象。因而,在UV消毒后,继续投加少量的NaClO可以减小微生物复活的概率。UV-NaClO顺序消毒之所以可以抑制微生物的复活主要是由于NaClO作为强氧化剂,其对微生物的灭活作用是通过氧化细胞中的酶、阻止蛋白质合成这一途径实现的,这种对细胞的破坏作用不具有可逆性,因此,被NaClO灭活的微生物不会出现复活的现象。
当处理后出水再生回用于绿地灌溉时,仅采用UV消毒,在光照条件下,3 h后再生水中的粪大肠菌群数即会超标,采用UV-NaClO顺序消毒,6 h后粪大肠菌群数可能会超标;当处理后出水再生回用于城市杂用时,仅采用UV消毒,在光照条件下,3 h后E.coli的数量超标,而采用UV-NaClO顺序消毒,24 h后E·coli数量仍然可以满足标准要求。同光复活相比,细菌暗修复的能力较弱,如仅采用UV消毒满足绿地灌溉或城市杂用标准时,经24 h暗修复后,细菌数量才出现超标的现象,采用UV-NaClO顺序消毒后的水样,在暗处放置24 h后,细菌数量均未出现超标的现象。因而,考虑到再生水输配管网的长度以及再生水使用的非连续性特点,采用UV-NaClO顺序消毒更有利于保证再生水的水质安全。同时在实际工程中,再生水的输送及储存应尽量采用密闭式系统,以降低消毒后细菌复活的可能性。
通过本研究可知,单独 UV 消毒不能有效的防止大肠菌群从污水处理厂向环境中传播,而采用UV-NaClO顺序消毒可在一定程度上抑制大肠菌群的二次滋生,减少了消毒后水在输送,储存及再生利用过程中潜在的生物风险。
-
为考察UV-NaClO顺序消毒对DBPs生成的影响,采用顶空气相色谱法分析了不同方式消毒后三氯甲烷、四氯化碳、二溴一氯甲烷和一溴二氯甲烷的生成量,并计算了DBPs的总生成量,结果如表2所示。在满足相同出水标准时,UV-NaClO顺序消毒DBPs的生成量明显低于单独NaClO消毒。尤其是当需要达到的出水标准越高时优势越明显。满足一级A排放标准时,采用UV-NaClO顺序消毒产生的总DBPs比单独NaClO消毒可减少24.53%;达到绿地灌溉标准时,单独NaClO消毒生成的总DBPs量为11.56 μg·L−1,UV-NaClO顺序消毒生成的总DBPs为5.79 μg·L−1,比NaClO消毒DBPs生成量降低了49.91%;满足杂用水标准时,UV-NaClO顺序消毒总DBPs的生成量比单独NaClO消毒可降低76.87%;在达到完全灭活粪大肠菌群的条件下,DBPs的减量可高达77.85%。
DBPs的生成量同氯的投加量密切相关,随着氯投加量的增加,DBPs的生成量显著增加[20]。采用UV-NaClO顺序消毒之所以可以降低DBPs的生成量,主要是由于在达到相同消毒效果时UV-NaClO顺序消毒所需的NaClO投加量低于单独NaClO消毒时的投加量,而且,当需要达到的消毒标准越高时,所需NaClO投加量低的优势越明显,如完全灭活粪大肠菌群时,单独NaClO消毒需要的NaClO投加量为30 mg·L−1,而采用UV-NaClO顺序消毒则只需投加10 mg·L−1的NaClO,因而,采用UV-NaClO顺序消毒可大幅降低DBPs的生成量。
大部分DBPs具有潜在的致癌、致畸和致突变毒性,较高浓度DBPs排入水体或再生利用时会威胁生态系统安全,并对人体健康具有潜在危害[21],UV-NaClO顺序消毒可避免大量的DBPs排入水体或进入再生水利用系统,因而,其在保护人体健康与生态环境等方面更具优势。
-
1) UV和NaClO对大肠菌群的灭活具有协同效应,采用UV-NaClO顺序消毒,在UV和NaClO投加量均不高的组合方式下即可达到单独UV或单独NaClO高剂量下的消毒效果,且当需要达到的消毒标准越高时,UV-NaClO顺序消毒的优势越明显。
2)经UV-NaClO顺序消毒后,大肠菌群的光复活和暗修复能力相比单独UV消毒有所下降,NaClO投加量越高下降幅度越明显,因而,采用UV-NaClO顺序消毒可在一定程度上抑制大肠菌群的二次滋生。
3)由于在达到相同消毒效果的前提下,UV-NaClO顺序消毒可以有效降低NaClO的投加量,因而,采用UV-NaClO顺序消毒可以降低DBPs的生成量,从而降低消毒对人体健康与生态环境的潜在危害。
UV-NaClO顺序消毒对污水中大肠菌群的灭活效果
Inactivation of coliforms in wastewater by UV- NaClO disinfection
-
摘要: 紫外(UV)和次氯酸钠(NaClO)消毒广泛应用于城市污水处理中,但目前2种消毒方式均存在不足。为实现既可高效消毒又能同时降低消毒所带来负面影响的目的,通过对比研究,分析了达到与UV或NaClO相同的消毒效果时,紫外-次氯酸钠(UV-NaClO)顺序消毒所需的消毒剂量以及UV-NaClO顺序消毒对微生物复活和消毒副产物(DBPs)生成的影响。结果表明:当UV剂量为9 mJ·cm−2,NaClO投加量为3、4和10 mg·L−1时,UV-NaClO顺序消毒可达到与单独UV消毒时(剂量为12、20或60 mJ·cm−2)以及单独NaClO消毒时(NaClO投加量为4、10或20 mg·L−1)的相同消毒效果;且当需要的微生物灭活效率越高时,UV-NaClO 顺序消毒的优势越明显。同单独UV消毒相比,UV-NaClO顺序消毒后微生物的光复活率和暗修复率明显降低。当达到与单独NaClO消毒相同的微生物灭活效果时,UV-NaClO顺序消毒可有效降低DBPs的生成量,例如完全灭活E.coli,采用UV-NaClO顺序消毒,DBPs的生成量可较单独NaClO消毒降低了76.87%。本研究可为污水排放与再生利用消毒技术的选择提供参考。Abstract: Ultraviolet (UV) and sodium hypochlorite (NaClO) disinfection are widely used in wastewater treatment, but both disinfection methods have deficiencies. In order to achieve efficient disinfection while reducing the negative impact of disinfection, a comparative study was conducted to analyze the disinfectant amount required for combined UV-NaClO disinfection with the same disinfection effect as UV or NaClO and the effect of UV-NaClO disinfection on microbial reactivation and disinfection by-products (DBPs) formation. The results showed that at UV dosage of 9 mJ·cm−2 and NaClO dosages of 3, 4 and 10 mg·L−1, UV-NaClO disinfection was as effective as UV disinfection alone at UV dosages of 12, 20 or 60 mJ·cm−2 and NaClO disinfection alone at NaClO dosages of 4, 10 or 20 mg·L−1. The higher the desired microbial inactivation efficiency, the more obvious the advantages of UV-NaClO disinfection. Compared to UV disinfection alone, UV-NaClO disinfection showed significantly lower rates of microbial photo-reactivation and dark repair. Achieving the same microbial inactivation effect as NaClO disinfection alone, UV-NaClO disinfection could effectively reduce the production of DBPs, for example, achieving complete inactivation of E.coli, the production of DBPs decreased by 76.87% using UV-NaClO disinfection compared with NaClO disinfection alone. This study can provide a theoretical basis for the selection of disinfection technology for wastewater discharge and recycling.
-
Key words:
- ultraviolet /
- sodium hypochlorite /
- disinfection /
- coliforms /
- reactivation /
- disinfection by-products
-
高铁酸盐(Fe(Ⅵ))是一种环境友好的氧化剂[1],与含有富电子基团的有机微污染物(例如胺类[2-3]、硫醇硫酯类[4]、酚类[5])具有较高的反应活性. 与二氧化氯、高锰酸盐、臭氧和次氯酸盐等常见氧化剂相比[6],Fe(Ⅵ)在酸性pH值下具有最高的氧化还原电位,且会减少溴代和氯代消毒副产物的生成[7]. 然而,Fe(Ⅵ)生产成本较高、在水溶液中的稳定性较低,这阻碍了其在水处理中的广泛应用. 因此,通过催化Fe(Ⅵ)氧化,提高Fe(Ⅵ)的利用效率具有重要意义.
在各种催化剂中,钌(Ru)因其多功能性而占有特殊的地位. ZSM-5(一种具有规整结构的微孔晶态硅铝酸盐分子筛)、TiO2和CeO2作为钌基催化剂的载体,在高锰酸盐氧化体系中性能稳定,钌能很好地附着到载体表面. 另外,ZSM-5、TiO2和CeO2作为载体,本身不会对催化效果产生影响. 因此本文选择ZSM-5、TiO2和CeO2作为载体. 已有研究证明在常见水处理pH范围内,催化剂Ru/ZSM-5、Ru/TiO2或Ru/CeO2能显著提高高锰酸盐氧化速率[8-9]. 此外,Ru/CeO2和Ru/TiO2具有良好的稳定性,在连续6次重复试验中其催化活性基本保持不变[8];但在连续10次重复试验中,Ru/ZSM-5的催化效能迅速下降,其稳定性比Ru/CeO2和Ru/TiO2差[9]. Ru作为催化剂在高铁酸盐氧化中的应用却鲜有报道. 因此,本研究以CeO2、TiO2和 ZSM-5为载体的非均相钌催化剂,并考察了其在不同pH条件下催化Fe(Ⅵ)氧化苯酚的性能,提出了Ru催化Fe(Ⅵ)氧化中的机理并评估了催化剂的稳定性.
1. 材料与方法 (Materials and methods)
1.1 试验药剂
水合三氯化钌(RuCl3·xH2O, 37% Ru)购自J&K化学公司;CeO2、TiO2、苯酚以及甲醇、甲酸等有机溶剂购自国药化学试剂有限公司;咖啡因购自Sigma公司;ZSM-5购自南开大学催化剂厂. 实验中所有溶液均使用超纯水配制.
采用湿式化学合成法[10]制备固体高铁酸钾(K2FeO4,纯度>95%). 将固体K2FeO4溶解在超纯水中制备K2FeO4储备溶液,然后用0.45 μm亲水性滤头过滤,通过紫外分光光度计在510 nm测量浓度,并在30 min内使用,以减少其自分解的影响.
1.2 实验流程
将装有200 mL一定浓度有机物和一定量催化剂的溶液调节至指定pH值,投加高铁酸钾储备液后,反应开始计时,定时取样,采用硫代硫酸钠或者盐酸羟胺淬灭,水样经醋酸纤维膜(孔径0.22 μm)过滤后定量分析.
1.3 催化剂的制备与表征
将RuCl3的干固体溶于pH 2.0的盐酸溶液中,配置成浓度为1 mol·L−1的RuCl3酸性溶液,弱酸环境可以有效防止三价钌被空气氧化为四价钌. 然后在室温条件下(约20 ℃)向RuCl3酸溶液投加载体,在磁力搅拌器上进行剧烈搅拌,使之达到均匀混合的状态,搅拌过程持续4 h. 然后通过高速离心机将固体从溶液中分离开来,用超纯水对催化剂进行反复冲洗,直至冲洗液的pH约为近中性,再将最终离心的固体置于温度为40 ℃的真空干燥箱中进行干燥. 待催化剂彻底干燥以后,即可进行实验. 利用场发射扫描电子显微镜(SEM,型号HITACHIS-4800)观察催化剂的表面形貌. 采用高分辨透射电子显微镜(TEM,型号为JEM-2100)和能量色散X射线光谱仪(EDAX)对催化剂表面的钌氢氧化物的颗粒形貌进行观察,同时对选定区域进行元素分析. 采用 Coulter SA 3100 吸附分析仪进行氮吸附-解吸,测定催化剂的比表面积和孔体积. 新合成的催化剂和使用后的催化剂分别经硝酸微波消解,采用电感耦合等离子体发射光谱法(ICP-AES)测定其Ru含量.
1.4 分析方法
采用超高效液相色谱仪(UPLC,型号H-Class)测定苯酚和咖啡因的浓度. 采用BEH C18柱子,柱温控制在35 ℃;测定苯酚时流动相为水:甲醇=65:35,测定咖啡因时流动相为水(0.1%甲酸):甲醇=70:30;检测波长是254 nm(苯酚)和273 nm(咖啡因).
2. 结果与讨论 (Results and discussion)
2.1 非均相钌催化剂的表征
新合成的Ru/ZSM-5、Ru/CeO2和Ru/TiO2催化剂中Ru的含量分别为0.69‰、0.80‰和0.94‰. SEM、TEM和EDAX的结果均证明载体上存在Ru颗粒(图1). 图1表面ZSM-5和TiO2为球形,CeO2为立方体形状. TEM结果表明,在Ru/ZSM-5、Ru/CeO2和Ru/TiO2中,Ru以粒径约为2.5 nm的颗粒存在于ZSM-5、TiO2和CeO2的表面. 制备过程中载体与RuCl3酸溶液反应结束后,通过离心将固体从溶液中分离,然后用超纯水对催化剂进行反复冲洗,因此在冲洗过程中RuCl3可能会发生水解,生成相应的氢氧化钌,推测载体表面的纳米颗粒为氢氧化钌的颗粒 [8]. 在Ru/ZSM-5中,ZSM-5的比表面积较高,通过TEM观测到Ru在ZSM-5表面的分散性也更好(表1). Ru/ZSM-5的区域EDAX分析表明Ru被成功负载(图1b).
 图 1 (a) Ru/ZSM-5的TEM图,(b)Ru/ZSM-5表面黄色方框内的EDAX图,(c) Ru/CeO2的TEM图,(d) Ru/TiO2的TEM图;载体的SEM图像显示在(a)、(c)和(d)的插图中.Figure 1. (a) TEM image of Ru/ZSM-5, (b) EDAX image of Ru/ZSM-5 surface in the yellow box, (c) TEM image of Ru/CeO2, and (d) TEM image of Ru/TiO2. The SEM images of supports were shown in the insets of (a), (c) and (d).表 1 催化剂及其载体的性质Table 1. Characteristics of synthesized catalysts and supports
图 1 (a) Ru/ZSM-5的TEM图,(b)Ru/ZSM-5表面黄色方框内的EDAX图,(c) Ru/CeO2的TEM图,(d) Ru/TiO2的TEM图;载体的SEM图像显示在(a)、(c)和(d)的插图中.Figure 1. (a) TEM image of Ru/ZSM-5, (b) EDAX image of Ru/ZSM-5 surface in the yellow box, (c) TEM image of Ru/CeO2, and (d) TEM image of Ru/TiO2. The SEM images of supports were shown in the insets of (a), (c) and (d).表 1 催化剂及其载体的性质Table 1. Characteristics of synthesized catalysts and supports平均粒径/μmAverage diameter 比表面积/(m2·g−1)BET Surface area 微孔表面积/(m2·g−1)Micropore surface area 外比表面积/(m2·g−1)External surface area 孔径/nmPore size 孔体积/(m3·g−1)Pore volume 微孔体积/(m3·g−1)Micropore volume ZSM-5 0.5 461 323 138 0.5 0.386 0.132 Ru/ZSM-5 0.5 407 280 127 0.5 0.272 0.088 TiO2 0.15 4.87 — — — — — Ru/TiO2 0.15 4.70 — — — — — CeO2 30 4.53 — — — — — Ru/CeO2 30 4.87 — — — — — 2.2 非均相钌催化剂的催化性能
已有研究证明Fe(Ⅵ)氧化有机微污染物符合二级反应动力学,因此本研究假设在有催化剂或没有催化剂的情况下,Fe(Ⅵ)氧化苯酚的反应在初始阶段遵循二级反应. 苯酚降解可能发生在溶液中(即非催化反应)和/或催化剂表面(即催化反应). 反应动力学方程1为简化的动力学模型,该模型同时考虑了催化反应和非催化反应.
−d[phenol]dt=ku[Fe(Ⅵ)][phenol]+kc[Fe(Ⅵ)][catalyst][phenol]=(ku+kc[catalyst])[Fe(Ⅵ)][phenol]=kT[Fe(Ⅵ)][phenol]=kobs[phenol] (1) 式中,ku(L·mol−1·min−1)为非催化反应的二级速率常数,kc(L·mol−1·min−1)为催化反应的二级速率常数;kT(L·mol−1·min−1)是整个反应的表观二级速率常数;kobs(min−1)等于kT[Fe(Ⅵ)]. 在以前的研究中,Fe(Ⅵ)浓度随时间的变化是通过紫外分光光度计在510 nm测量的,但在本研究中,由于固体催化剂的干扰,无法测定溶液中Fe(Ⅵ)的浓度.
如图2所示,Ru/ZSM-5、Ru/CeO2和Ru/TiO2催化剂加入后,kobs随催化剂用量的增加呈线性增加. 当Ru/ZSM-5的投加量从0增加到0.5 g·L−1时,kobs几乎增加了10倍. Ru/ZSM-5的Ru载量最低(0.69‰),但其催化效能与另外两种催化剂相当。由于ZSM-5比表面积远高于TiO2和CeO2,且钌纳米颗粒在ZSM-5载体上有良好分散性. 已有研究证明CeO2、TiO2和 ZSM-5作为载体,本身不会对钌催化效果产生影响[11]. 虽然载体本身对非均相钌催化剂的性能影响不大,但决定了钌纳米颗粒的分散性[8],而钌的分散性对其催化性能起着决定性作用。
2.3 pH值的影响
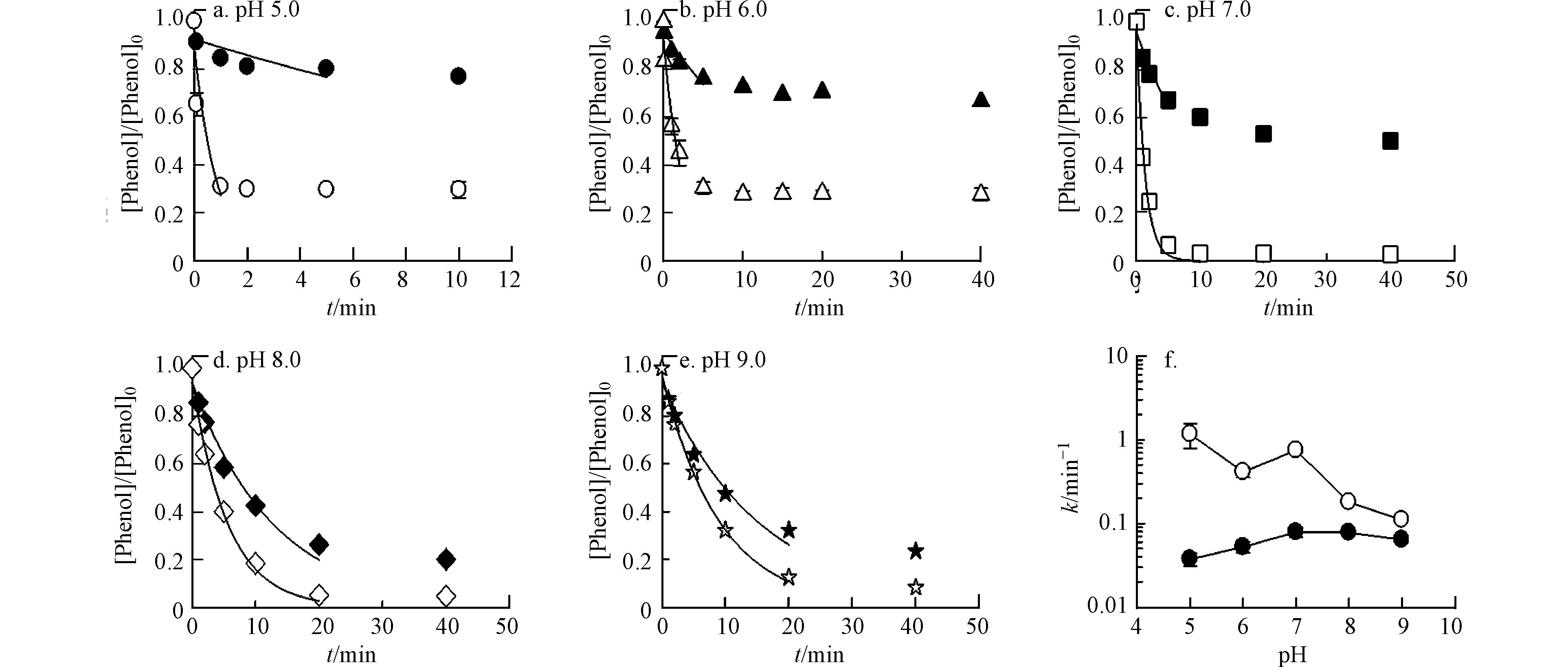
不同pH值下,Fe(Ⅵ)存在不同酸碱形态(pKa1 = 3.5,pKa2 = 7.3)[12],且不同形态的Fe(Ⅵ)活性不同. 苯酚(PhOH)也存在分子态和电离态(pKa = 10),在pH 5.0—9.0范围内,苯酚主要以分子态PhOH存在,因此可以忽略其电离态. 假设不同形态的Fe(Ⅵ)通过平行反应对PhOH进行氧化(反应 2—4):
H2FeO4+PhOHkα1,β1→products (2) HFeO−4+PhOHkα2,β1→products (3) FeO2−4+PhOHkα3,β1→products (4) 在不投加催化剂的情况下,当pH从5.0升高到7.0时,kobs从3.74×10−2 min−1增加到7.89×10−2 min−1,随着pH进一步升高到9.0,kobs从7.89×10−2 min−1下降到6.40×10−2 min−1(图3). 以往的研究证明HFeO4−比FeO42−的反应活性更高,但在pH 5.0和6.0下kobs相对较低,这可能是由于在低pH条件下Fe(Ⅵ)会快速自分解[12].
在3种催化剂中,选择Ru/ZSM-5作为模型催化剂来评估pH对Fe(Ⅵ)氧化苯酚性能的影响. 如图3所示,Ru/ZSM-5催化Fe(Ⅵ) 氧化苯酚的动力学也表现出很强的pH依赖性. 在pH 5.0—9.0范围内,Ru/ZSM-5极大地提高了苯酚的去除速率. 除pH 7.0外,Ru/ZSM-5催化Fe(Ⅵ)氧化苯酚的kobs (min−1)随pH升高而降低. 这是由于随着pH的升高,Fe(Ⅵ)氧化电位逐渐降低,因此生成的Rux+的量也就相应逐渐下降,最终使得催化效果下降. 在pH 7.0时,Ru/ZSM-5催化效能升高,这可能是因为在pH 7.0时,钌的催化活性较高[13].
2.4 催化机理
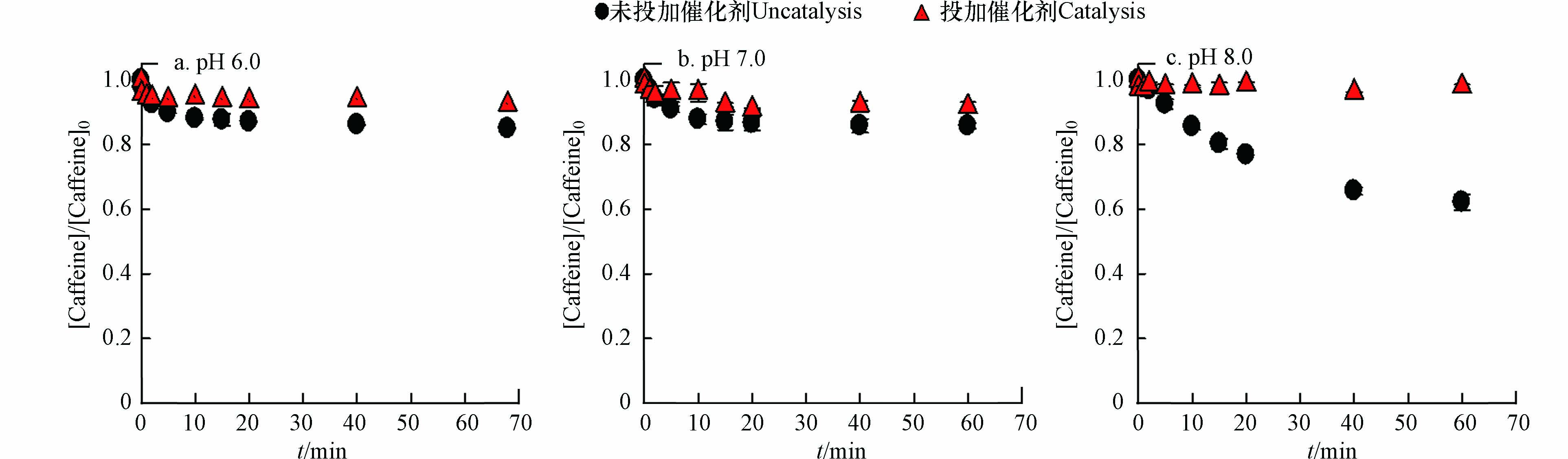
研究表明,在Fe(Ⅵ)氧化过程中,可能有中间态Fe(Ⅳ)、Fe(Ⅴ)和羟基自由基(HO·)等反应活性中间体[14]. 高铁酸盐氧化咖啡因过程中,主要是中间价态铁Fe(Ⅴ)和Fe(Ⅳ)在发挥氧化效能,而Fe(Ⅵ)不能降解咖啡因[15]. 因此,本文选择咖啡因作为探针化合物,检测和评估Fe(Ⅴ)和Fe(Ⅳ)对Fe(Ⅵ)-Ru/ZSM-5体系的贡献. 如图4所示,由于Ru/ZSM-5的存在,Fe(Ⅵ)对咖啡因的降解被完全抑制. 因此,可以排除 Fe(Ⅵ)-Ru/ZSM-5体系中Fe(Ⅴ)和Fe(Ⅳ)的贡献. 已有研究证明[16],Fe(Ⅵ)氧化过程中产生的HO·对有机物的降解作用可以忽略不计. 因此,排除了HO·对苯酚降解的贡献.
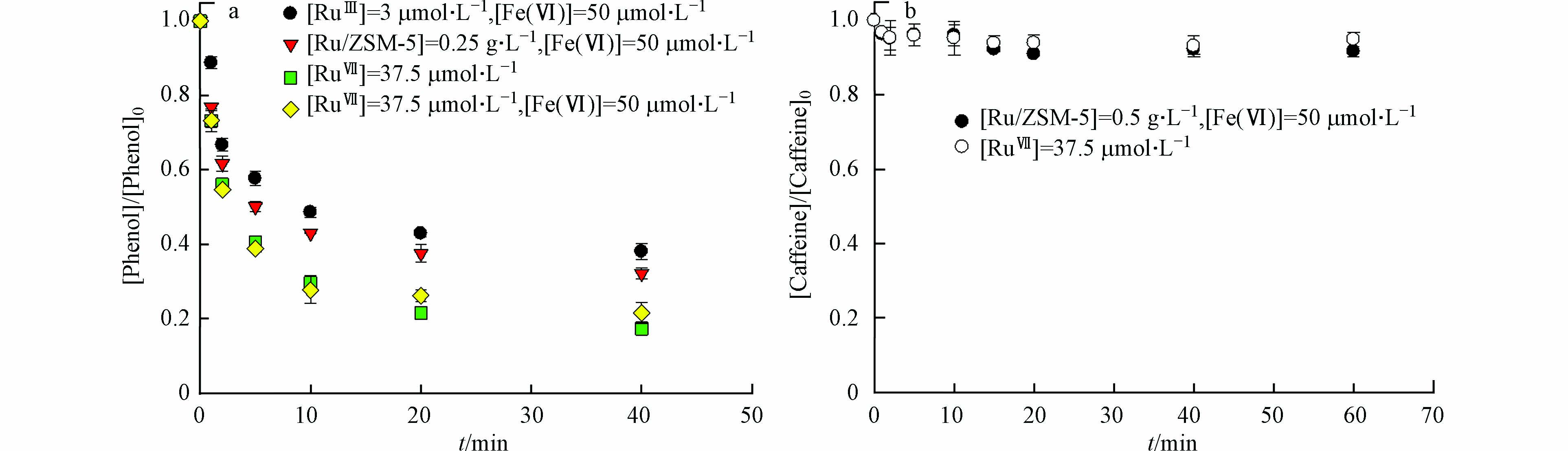
在高锰酸钾氧化的过程中,钌纳米颗粒具有电子穿梭的作用[8]. 简而言之,RuⅢ被高锰酸盐氧化成更高的氧化态RuⅦ,其作为氧化物种被有机微污染物还原到其初始状态RuⅢ. 因此,本研究假设Ru催化Fe(Ⅵ)氧化过程中的活性物种也是RuⅦ. 本文通过投加KRuO4,评估了RuⅦ对Fe(Ⅵ)氧化苯酚的影响. 在pH 7.0下,单独RuⅦ降解苯酚速率比Fe(Ⅵ)更高,但其对咖啡因的降解几乎没有影响(图5). Fe(Ⅵ)/RuⅢ降解苯酚的动力学规律与Fe(Ⅵ)/RuⅦ相同,但Fe(Ⅵ)/RuⅦ的反应速率常数更大. 这是因为Fe(Ⅵ)/RuⅦ中的Fe(Ⅵ)和RuⅦ都参与苯酚降解,而Fe(Ⅵ)/RuⅢ中部分Fe(Ⅵ)用于转化RuⅢ为中间态RuⅦ. 可以确定RuⅦ是Ru催化Fe(Ⅵ)氧化的主要活性物种,也是降解有机微污染物的选择性氧化剂[12].
2.5 催化剂的稳定性
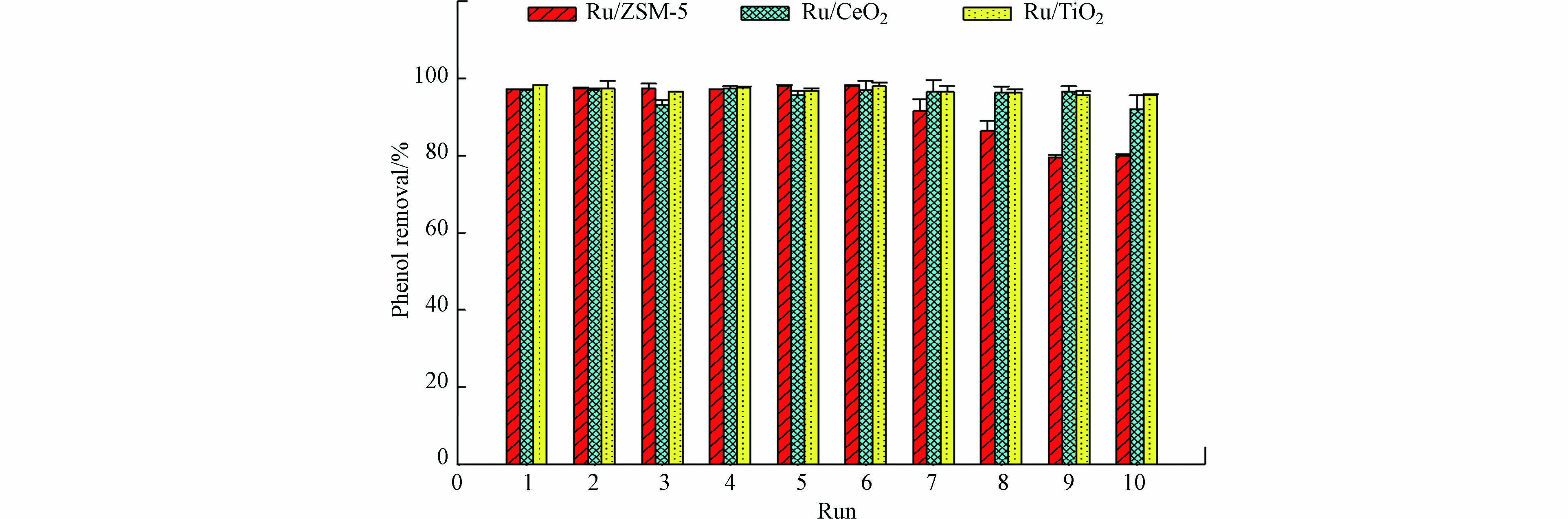
在催化反应和工业应用中,催化剂的可重复使用性和稳定性至关重要. 因此本文评估了Ru/CeO2、 Ru/TiO2和Ru/ZSM-5连续使用10次的稳定性(图6). 在Ru/CeO2和Ru/TiO2催化体系中,苯酚的去除率始终高于92%;而当催化剂为Ru/ZSM-5时,在前6次实验中苯酚的去除率保持不变,但从第6次到第10次循环实验中,苯酚的去除率从98.1%逐渐下降到80.0%. 经过10次循环使用后,Ru/ZSM-5、Ru/CeO2和Ru/TiO2中Ru负载量分别从0.69‰降至0.65‰、0.80‰至0.77‰、0.94‰至0.84‰. 因此,Ru的泄露并不是Ru/ZSM-5性能下降的主要原因. Fe(Ⅵ)的主要还原产物是Fe(Ⅲ),即氢氧化铁沉淀物,这些沉淀物可能吸附在催化剂表面,导致催化剂部分活性位点被覆盖. ZSM-5是一种中孔沸石,具有较高的表面积,因此对氢氧化铁的吸附能力更高(表1). ICP结果证实在使用后的Ru/ZSM-5上存在Fe元素,质量占比为0.04‰,而Ru/CeO2和Ru/TiO2上的Fe可以忽略不计. 因此,Ru/ZSM-5 性能下降可能主要与沉积的氢氧化铁掩盖了Ru/ZSM-5表面的活性位点有关. Ru/TiO2和Ru/CeO2稳定性好,有利于其工程或中试应用,但应尽量避免氢氧化铁在催化剂表面沉积.
3. 结论(Conclusion)
Ru/ZSM-5、Ru/CeO2和Ru/TiO2可以有效催化Fe(Ⅵ)氧化降解苯酚,且催化效能随催化剂用量线性增加. 钌纳米颗粒的良好分散性是其获得较好催化性能的关键,因此,在未来研究中,单原子钌基催化剂具有广阔前景. Ru催化Fe(Ⅵ)氧化降解苯酚的动力学表现出很强的pH依赖性. Ru催化Fe(Ⅵ)氧化降解苯酚过程中的主要活性物质为RuⅦ和Fe(Ⅵ). Ru/TiO2和Ru/CeO2的稳定性优于Ru/ZSM-5,有利于其中试或工程实践中的应用.
-
表 1 不同污水排放标准下不同消毒方式所需的最小消毒剂量
Table 1. Minimum disinfection dosage required by different disinfection methods for different sewage discharge standards
出水标准 限值要求/(CFU·L−1) UV消毒/(mJ·cm−2) NaClO消毒/(mg·L−1) UV- NaClO顺序消毒UV(mJ·cm−2)/NaClO(mg·L−1) 一级A标准 FC≤1000 12 4 9/3 绿地灌溉标准 FC≤200 20 10 9/4 杂用水标准 E.coli 不得检出 60 20 9/10 完全灭活FC 80 30 20/10 表 2 NaClO和UV-NaClO顺序消毒时DBPs生成量的比较
Table 2. Comparison of DBPs generation after NaClO and UV-NaClO disinfection
出水标准 NaClO消毒/(mg·L−1) DBPs生成量/(μg·L−1) UV- NaClO顺序消毒UV(mJ·cm−2)/NaClO(mg·L−1) DBPs生成量/(μg·L−1) 一级A标准 4 3.18±2.14 9/3 2.4±1.68 绿地灌溉标准 10 11.56±2.03 9/4 5.79±1.76 杂用水标准 20 52.27±2.65 9/10 12.09±2.23 完全灭活FC 30 65.32±2.87 20/10 14.47±1.89 -
[1] 杨蓉, 李垒, 霍晓芹, 等. 水质标准中指示微生物的发展及现状[J]. 中国环境监测, 2020, 36(4): 1-10. doi: 10.19316/j.issn.1002-6002.2020.04.01 [2] 潘均悦. 粪大肠菌群检测方法探究[J]. 生物化工, 2020, 6(4): 152-155. doi: 10.3969/j.issn.2096-0387.2020.04.043 [3] LAPARA T M, BURCH T R, MCNAMARA P J, et al. Tertiary-treated municipal wastewater is a significant point source of antibiotic resistance genes into Duluth-Superior Harbor[J]. Environmental Science & Technology, 2011, 45(22): 9543-9549. [4] BEN W W, WANG J, CAO R K, et al. Distribution of antibiotic resistance in the effluents of ten municipal wastewater treatment plants in China and the effect of treatment processes[J]. Chemosphere, 2017, 172: 392-398. doi: 10.1016/j.chemosphere.2017.01.041 [5] WANG H C, WANG J, LI S M, et al. Synergistic effect of UV/chlorine in bacterial inactivation, resistance gene removal, and gene conjugative transfer blocking[J]. Water Research, 2020, 185: 116290-116290. doi: 10.1016/j.watres.2020.116290 [6] MAZHAR M A, KHAN N A, AHMED S, et al. Chlorination disinfection by-products in Municipal drinking water : A review[J]. Journal of Cleaner Production, 2020, 123159: 226-239. [7] 蔡璇, 张云, 李然, 等. 饮用水紫外线消毒研究进展[J]. 中国公共卫生, 2012, 28(4): 562-564. doi: 10.11847/zgggws2012-28-04-64 [8] GUO M T, HUANG J J, HU H Y, et al. Growth and repair potential of three species of bacteria in reclaimed wastewater after UV disinfection[J]. Biomedical and Environmental Sciences, 2011, 24(4): 400-407. [9] 孔秀娟, 马军, 文刚, 等. 紫外-氯对细菌的协同消毒效果[J]. 水处理技术, 2016, 42(1): 41-44. doi: 10.16796/j.cnki.1000-3770.2016.01.008 [10] 张天阳, 魏海娟, 姚杰, 等. 污水处理厂不同紫外/氯化组合工艺的消毒效能对比[J]. 中国给水排水, 2021, 37(17): 19-24. doi: 10.19853/j.zgjsps.1000-4602.2021.17.003 [11] BOLTON J R, LINDEN K G. Standardization of methods for fluence (UV Dose) determination in bench-scale UV experiments[J]. Journal of Environmental Engineering, 2003, 129(3): 209-215. doi: 10.1061/(ASCE)0733-9372(2003)129:3(209) [12] 国家环境保护总局. HJ 620-2011 水质挥发性卤代烃的测定顶空气相色谱法[S]. 北京: 中国环境科学出版社, 2011. [13] 国家环境保护总局. 城镇污水处理厂污染物排放标准: GB 18918-2002[S]. 北京: 中国环境科学出版社, 2002. [14] 国家质量检验检疫总局. 城市污水再生利用绿地灌溉水质: GB/T 25499-2010, [S]. 北京: 中国环境科学出版社, 2010. [15] 国家质量检验检疫总局. 城市污水再生利用城市杂用水水质: GB/T 18920-2020, [S]. 北京: 中国环境科学出版社, 2020. [16] 李腾, 胡静, 宋海旺, 等. 污水厂二级出水中抗生素抗性细菌的紫外灭活与复活特性[J]. 环境工程, 2022, 40(2): 14-19. doi: 10.13205/j.hjgc.202202003 [17] ZHANG Z G, LI B X, LI N, et al. Effects of UV disinfection on phenotypes and genotypes of antibiotic-resistant bacteria in secondary effluent from a municipal wastewater treatment plant[J]. Water Research, 2019, 157: 546-554. doi: 10.1016/j.watres.2019.03.079 [18] PING Q, YAN T T, WANG L, et al. Insight into using a novel ultraviolet/peracetic acid combination disinfection process to simultaneously remove antibiotics and antibiotic resistance genes in wastewater: Mechanism and comparison with conventional processes[J]. Water Research, 2022, 210: 118019-118019. doi: 10.1016/j.watres.2021.118019 [19] WEI F Q, LU Y, SHI Q, et al. A dose optimization method of disinfection units and synergistic effects of combined disinfection in pilot tests[J]. Water Research, 2022, 211: 118037-118037. doi: 10.1016/j.watres.2022.118037 [20] 邰晓晖, 李轶, WANG C S, 等. 操作条件及水质对海水氯消毒过程中消毒副产物生成的影响[J]. 环境工程, 2016, 34(3): 6-10. doi: 10.13205/j.hjgc.201603002 [21] CHOWDHURY S, MAZUMDER M A J, ALHOOSHANI K, et al. Reduction of DBPs in synthetic water by indoor techniques and its implications on exposure and health risk[J]. Science of the Total Environment, 2019, 691: 621-630. doi: 10.1016/j.scitotenv.2019.07.185 -





 下载:
下载: