-
溴系阻燃剂因其具有环境持久性、生物蓄积性和生物毒性等而被禁止使用[1]。与溴系阻燃剂相比,有机磷阻燃剂(organophosphorus flame retardants,OPFRs)具有较好的润滑、阻燃、增塑效果而被广泛应用,成为溴系阻燃剂的替代品[2]。有机磷阻燃剂作为一种人工合成的工业有机添加剂[3-4],广泛应用在各种商业及工业领域中,如电子设备,建筑材料,纺织品,油漆,家具等[5-7]。OPFRs主要以物理形式添加到材料中,在使用过程中通过挥发、磨损和溶解等方式进入环境[8],导致OPFRs广泛存在于水[9]、灰尘[10]、空气[11]和沉积物[12]等各种介质中。毒理学研究表明,多种OPFRs具有致畸、致癌、致突变风险以及神经毒性作用,即使暴露在低浓度下,长期积累也会对人体造成潜在危害[13]。现阶段,针对多种OPFRs的检测方法较少,因此,研究水体中OPFRs的污染特征并采用科学的方法对其进行检测和风险评价具有重要意义。
本研究筛选出环境中含量较高的27种OPFRs作为研究对象,通过优化固相萃取前处理条件、高效液相色谱-串联质谱仪和气相色谱-质谱联用仪的参数,建立了27种OPFRs的定性和定量分析方法,并对北京市潮白河流域地表水和地下水中OPFRs进行检测;同时,基于美国环境保护局(USEPA)推荐的健康风险评价模型对地表水和地下水中的OPFRs进行人体健康风险评价,旨在为地表水和地下水水体中OPFRs的检测及风险评价提供参考。
-
本研究共检测出27种OPFRs标准品,包括10种烷基磷酸酯阻燃剂、3种氯代磷酸酯阻燃剂和14种苯基磷酸酯阻燃剂。
10种烷基磷酸酯阻燃剂包括磷酸三(2-乙基己基)酯(TEHP)、磷酸二(2-乙基己基)酯(BEHP)、磷酸三异丁酯(TiBP)、磷酸三丁酯(TnBP)、磷酸三丙酯(TnPP)、磷酸三异丙酯(TiPP)、磷酸三乙酯(TEP)、磷酸三(2-丁氧基乙基)酯(TBEP)、磷酸三己酯(THP)、磷酸三戊酯(TPeP)。3种氯代磷酸酯阻燃剂包括磷酸三(1,3-二氯异丙基)酯(TDCPP)、磷酸三(2-氯乙基)酯(TCEP)、磷酸三(2-氯异丙基)酯(TCPP)。14种苯基磷酸酯阻燃剂包括磷酸二苯基甲苯酯(MDPP)、磷酸叔丁基苯二苯酯(BPDP)、磷酸二苄酯(DBPP)、磷酸三邻甲苯酯(o-TTP)、磷酸三间甲苯酯(m-TTP)、磷酸三对甲苯酯(p-TTP)、磷酸三(3,5-二甲基苯基)酯(TDMPP)、磷酸异癸基二苯酯(IDPP)、2-乙基己基二苯基磷酸酯(EHDPP)、磷酸三苯酯(TPhP)、三苯基氧化膦(TPPO)、磷酸异丙基二苯酯(IDDP)、磷酸三(2-异丙基苯)酯(TIPPP)、磷酸三(二甲苯)酯(TXP)。
内标TnBP-d27和TPhP-d15购自上海甄准生物科技有限公司,纯度>99%,使用甲醇配制成标准储备溶液。甲醇、乙腈、二氯甲烷、正己烷、甲酸均是HPLC级,0.45 μm玻璃纤维滤膜购自上海安谱公司。HLB和MCX固相萃取柱(柱体体积为6 mL,柱填料质量为500 mg)购自美国Waters公司,Envi-18固相萃取柱(柱体体积为6 mL,柱填料质量为500 mg)购自美国Supelco公司。
-
仪器与设备包括:高效液相色谱-串联质谱仪(LC-MS8040,日本岛津)、气相色谱(7890A)-质谱(5975C)联用仪(美国安捷伦)、固相萃取仪(Supelco-24位,美国Supelco公司)、旋转蒸发仪(RE-52AA,上海亚荣)和氮吹浓缩仪(KL512J,北京康林公司)。
-
2021年4月,采集北京市潮白河4种地表水样品(编号为S1、S2、S3、S4)和4种地下水样品(编号为1#、2#、3#、4#,取自地下30 m),置于棕色玻璃瓶内,避光运送至实验室进行前处理。准确量取经0.45 μm玻璃纤维滤膜过滤后的水样2 L,并加入内标物TnBP-d27和TPhP-d15(500 ng·L−1)。
高效液相色谱-串联质谱仪检测样品固相萃取过程:HLB和MCX固相萃取柱使用前依次用5 mL乙腈、甲醇和超纯水进行活化,水样以5~10 mL·min−1的流速通过固相萃取柱。富集结束后,用10 mL的乙腈分两次洗脱,洗脱液经过16 g无水硫酸钠进行脱水,并于50 ℃下旋转蒸发和氮吹浓缩至0.5 mL,保存在4 ℃冰箱中待测。
气相色谱-质谱联用仪检测样品固相萃取过程:HLB和Envi-18固相萃取柱使用前依次用5 mL二氯甲烷、甲醇、超纯水进行活化,水样以5~10 mL·min−1的流速通过固相萃取柱。富集结束后,HLB固相萃取柱用二氯甲烷和甲醇混合液(体积比9∶1)10 mL分2次进行洗脱,Envi-18固相萃取柱用正已烷和二氯甲烷混合液(体积比7∶3)10 mL分2次进行洗脱。洗脱液经过20 g无水硫酸钠进行脱水,并于40 ℃下用旋转蒸发仪和氮吹仪浓缩至0.2 mL,保存在4 ℃冰箱中待测。
-
LC-MS8040条件:高效液相色谱柱(C18柱,Inert Suatain C18 column,150 mm×4.6 mm,5 μm,Tokyo,Japan);柱温40 ℃,进样体积10 μL,流动相为甲醇和含10 mmol·L−1甲酸的水溶液。梯度洗脱程序为:0~6 min,甲醇由80%升至95%,6~15 min,甲醇由95%降至80%。质谱条件选用正离子模式电喷雾离子源(ESI+),多反应监测模式(MRM),雾化气流速为3 L·min−1,干燥气流速为15.0 L·min−1,去溶剂温度为250 ℃,加热区温度为400 ℃。在ESI+模式下确定20种OPFRs的母离子,并在MRM模式下优化质谱参数,20种目标物的主要参数如表1所示。
高效液相色谱-串联质谱仪采用二级质谱,与气相色谱-质谱联用仪采用单级质谱相比具有更低的检测限。但是,磷酸三(2-乙基己基)酯和磷酸二(2-乙基己基)酯在上述梯度洗脱条件下有残留,磷酸叔丁基苯二苯酯未出峰,磷酸二苄酯检测限较高,而磷酸三邻甲苯酯、磷酸三间甲苯酯、磷酸三对甲苯酯3种同分异构体母离子和定量离子相同,出峰时间相同,无法区分,故不能检测,这7种OPFRs采用GC-MS进行检测。
GC-MS条件:HP-5MS色谱柱(30 m×0.25 mm×0.25 μm),载气为高纯氦气,流量为1.0 mL·min−1。进样口温度为280 ℃,进样量为1 µL,不分流进样。采用程序升温:初始温度40 ℃,保持2 min;以5 ℃·min−1升温至290 ℃,保持8 min,总运行时间为60 min。质谱条件为电子轰击离子源(EI),选择离子监测模式(SIM),离子源温度为230 ℃,四极杆温度为280 ℃。7种OPFRs在GC-MS中的参数如表2所示。
-
在实验过程中配制不同浓度梯度的混合标准溶液(0、10、40、100、200、400 ng·L−1),用固相萃取柱富集后进行检测,以OPFRs峰面积作为横坐标,浓度作为纵坐标,绘制标准曲线。所有目标化合物在此范围内线性良好,可决系数(R2)均大于0.99。方法检出限(LODs)和方法定量限(LOQs)分别以3倍信噪比(S/N=3)和10倍信噪比(S/N=10)进行计算。27种OPFRs的方法检出限为0.02~2.53 ng·L−1;定量限为0.06~8.43 ng·L−1;回收率为65.82%~108.48%;RSD为2.4%~10.6%,结果见表3。
-
采用美国环境保署(USEPA)提出的健康风险评价模型[14-15],对北京市潮白河地表水和地下水中的OPFRs的健康风险进行评价。
人群通过饮用水摄入OPFRs 的日均暴露量(ADD),计算方法[16]如式(1)所示。
式中:EADD为OPFRs的日均暴露量,ng·(kg·d)−1;c为水体中的OPFRs的浓度,ng·L−1;QIR 为日均饮水量,L·d−1;SAP 为饮水摄入量的吸收率,取 SAP 为100%;mBW为平均人体质量,kg。水中OPFRs的成人暴露风险计算参数引自《中国人群暴露参数手册(成人卷):概要》[17],儿童暴露风险指标来源于已有研究中的参数[18]。
危害商(HQ)表示人群通过饮用水摄入OPFRs的非致癌风险,计算方法如式(2)所示。
式中:RHQ为人群通过饮用水摄入OPFRs的非致癌风险值;NRfD为USEPA对每个OPFRs的参考剂量值, ng·(kg·d)−1,表示在单位时间、单位质量摄取的不会引起人体不良反应的污染物最大量,用无不良反应水平(NOVEL)除以安全系数(10 000)计算[19]。当RHQ>1时,表示存在非致癌健康风险;当RHQ<0.1时,认为非致癌风险较小或忽略不计。
人群通过饮用水摄入OPFRs的致癌风险(CR)计算方法如式(3)所示。
式中:HCR为人群通过饮用水摄入OPFRs的致癌风险值;CSFO为致癌斜率因子,ng·(kg·d)−1,用来评估与接触致癌物或潜在致癌物相关的致癌风险[20]。当HCR>1×10−6时,表示存在致癌风险;当HCR<1×10−6时,表示致癌风险可以忽略不计;当HCR为10−6~10−4时,具有潜在的致癌风险;当HCR>10−4时,则认为具有高致癌风险。
-
目前,固相萃取柱包括OasisHLB、OasisMCX、Envi-18、C18、PEP等不同型号[21]。HLB和MCX固相萃取柱对于极性较强的物质萃取效果更好,并且MCX柱对碱性化合物具有较好的保留作用,Envi-18含有大量的十八烷基,含碳量大于17%,对弱极性物质有较好的富集效果。因此,选取HLB和MCX作为LC-MS/MS的前处理SPE柱,选取HLB和Envi-18作为GC-MS的前处理SPE柱。
HLB和MCX单个固相萃取柱以及两者串联之后的实验结果见图1。由图1可以看出,回收率分别为54.33%~93.40%、65.82%~102.14%、70.60%~110.27%,HLB柱串联MCX柱对OPFRs的萃取效果相对较好,其次是MCX固相萃取柱。单个MCX柱和两者串连起来的回收率相差不大,故本实验水样前处理选择MCX柱。
HLB和Envi-18单个固相萃取柱以及两者串联之后的GC-MS实验结果见图2。由图2可以看出,7种OPFRs的富集效果均较好,回收率分别为72.52%~88.29%、76.86%~94.90%、86.38%~108.48%。HLB和Envi-18串联后的回收率明显高于单个固相萃取柱,故选择HLB串联Envi-18用于水样前处理。
-
本研究分别以等度洗脱(80%甲醇-水、90%甲醇-水、100%甲醇)和梯度洗脱作为流动相进行检测,结果如图3所示。100%甲醇等度洗脱与80%甲醇-水和90%甲醇-水等度洗脱相比,12种OPFRs的响应强度提高了2~4倍。采用0~6 min甲醇由80%升至95%,6~15 min甲醇由95%降至80%的梯度洗脱,7种OPFRs的响应强度比100%甲醇等度洗脱提高了2~4倍。通常,LC-MS/MS在正离子模式下,加酸可以提高其响应强度 [22],因此,本研究探讨了含10 mmol·L−1甲酸的水溶液作为流动相进行梯度洗脱的实验效果,发现15种OPFRs的响应强度进一步提高了2~4倍,故选择甲醇和含10 mmol·L−1甲酸的水溶液作为流动相进行检测。
-
在北京市潮白河流域地表水和地下水进行布点采样,采用表3中所列OPFRs检测方法对水样中的OPFRs进行了检测。除TIPPP、IDPP、BPDP和DBPP等4种物质未检出外,其余23种OPFRs均有检出,质量浓度为0~973.17 ng·L−1,测定结果如表4所示。地表水S1、S2、S3、S4的总质量浓度分别为1071.26、762.20、262.39和722.10 ng·L−1,其中S4的TEP(459.90 ng·L−1)质量浓度相对较高,其次是S1的TnPP(315.47 ng·L−1)和TiPP(298.41 ng·L−1)。在地下水1#、2#、3#、4#监测井中,OPFRs的总质量浓度分别为772.16、1 913.40、749.60、1 101.24 ng·L−1,其中1#(376.85 ng·L−1)和2#(973.17 ng·L−1)的TEHP质量浓度相对较高,其次是2#的TnPP(208.83 ng·L−1)。在8个采样点中,TEHP、TEP、TnPP、TiPP质量浓度相对较高,分别为23.04~973.17、7.48~459.90、29.30~315.47和10.34~298.41 ng·L−1。TnPP和TEP主要用于建筑材料中的阻燃剂,其易溶于水,极性强,辛醇水分配系数
(lgKow) 分别为1.87和0.80[23],这可能导致其在水体中的质量浓度偏高。李栋等[24]对长江南京段水源水中13种OPFRs进行过检测,ƩOPFRs质量浓度为85.21~1 557.96 ng·L−1 。XING等[6]的检测结果表明,骆马湖地表水水样中12种 ƩOPFRs质量浓度为97.1~1 066.00 ng·L−1,此结果与本研究结果接近。 -
目前,有13种OPFRs能查到其RfD值,包括TEP、TnBP、TDCPP、TPHP、EHDPP、o-TTP、m-TTP、p-TTP、TCEP、TCPP、TBEP、TPPO和TEHP。有4种OPFRs能查到其SFO值,包括TCEP、TCPP和TnBP、TEHP [14]。年龄段和性别的不同导致人群通过饮用水摄入OPFRs的日均暴露剂量也不一样,男性略高于女性,男性儿童略高于女性儿童。按照男性儿童、男性成人、女性儿童、女性成人分别计算健康风险,计算参数如表5和表6所示。由式(1)~式(3)计算得出,13种OPFRs的非致癌风险值为0~6.17×10−4,4种致癌风险值为1.37×10−9~1.07×10−7。同时,以平均暴露(8个样点平均质量浓度)和高暴露(8个样点最大质量浓度)分别计算其致癌风险和非致癌风险。
由图4可知,男性儿童、男性成人、女性儿童、女性成人在平均暴露和高暴露条件下,OPFRs非致癌风险值(HQ)分别为6.41×10−6~1.99×10−4和1.61×10−5~6.17×10−4。在高暴露条件下,TBEP是非致癌风险最高的物质,按照男性儿童、男性成人、女性儿童、女性成人分类,分别为6.07×10−4、6.17×10−4、5.95×10−4、5.30×10−4;在平均暴露条件下,TnBP非致癌风险值相对较高,分别为3.93×10−4、3.99×10−4、3.84×10−4、3.43×10−4。TnBP极性较弱,其疏水性较高、吸附性较强,易吸附于悬浮物进入水体中,从而在水体中容易富集[25]。TBEP和TCPP非致癌风险值分别为1.32×10−4~1.54×10−4和1.22×10−4~1.42×10−4。TBEP主要作为橡胶制品中的改性剂和增塑剂,在我国地表水中检测频率较高,具有一定的生殖毒性,会对激素受体基因表达产生一定的干扰[13]。虽然氯代有机磷阻燃剂对人体的非致癌风险值小于阈值,但是其具有神经毒性、内分泌干扰性、致癌性等多种毒性,对人体健康有着较高的危害,已被WHO列为致癌物之一 [26-27],并且在环境中不易降解、污水处理厂无法有效去除、环境中持续时间更长 [28]。在平均暴露和高暴露条件下,非致癌风险值小于风险阈值,表明北京潮白河地表水和地下水中OPFRs对人体非致癌风险较低。但是,OPFRs在环境中会通过皮肤、灰尘、呼吸等方式进入体内,同时OPFRs之间可能具有毒性加和效应,仍然需要继续关注其不同途径的暴露情况[19]。
如图5所示,在平均暴露和高暴露条件下,OPFRs致癌风险值分别为5.24×10−9~2.32×10−8和1.00×10−8~1.07×10−7,其致癌风险值明显低于致癌(CR)风险阈值(1.0×10−6)。在高暴露条件下,TEHP较其他3种OPFRs致癌风险值最高,为9.18×10−8~1.07×10−7,其次是TnBP,为3.10×10−8~3.60×10−8。由此可知,在高暴露条件下,虽然致癌风险值和非致癌风险值小于风险阈值,但是TEHP致癌风险值已经达到1×10−7,需要对其进行重点监控[29]。
-
1)在27种OPFRs中,有20种OPFRs采用LC-MS/MS进行检测,定量限为0.08~1.04 ng·L−1,回收率为65.82%~110.27%;有7种OPFRs采用GC-MS进行检测,回收率为86.38%~108.48%,定量限为1.31~8.43 ng·L−1。27种OPFRs检测方法线性关系良好,可决系数(R2)均大于0.99,RSD为2.4%~10.6%。
2)在8种水样中,除TIPPP、IDPP、BPDP和DBPP未检出外,其余23种OPFRs均有不同程度检出。其中TEHP、TEP、TnPP、TiPP质量浓度相对较高,分别为23.04~973.17、7.48~459.90、29.30~315.47和10.34~298.41 ng·L−1。
3) 13种OPFRs的非致癌风险值为0~6.17×10−4,4种OPFRs致癌风险值为1.37×10−9~1.07×10−7,OPFRs产生的人体健康风险处于较低水平。在高暴露条件下,TBEP非致癌风险值为6.17×10−4, TEHP致癌风险值为1×10−7,非致癌风险和致癌风险均处于较低水平。
水体中27种有机磷阻燃剂(OPFRs)的检测及风险评价
Determination and risk assessment of 27 organophosphorus flame retardants (OPFRs) in water
-
摘要: 有机磷阻燃剂(organophosphorus flame retardants,OPFRs)具有致畸、致癌、致突变风险以及神经毒性作用。为了更好地研究其存在水平和健康风险,建立了固相萃取与高效液相色谱-串联质谱仪和气相色谱-质谱联用仪检测水体中27种OPFRs的分析方法,并对OPFRs进行了健康风险评价。20种OPFRs采用MCX固相萃取柱预处理和LC-MS/MS进行检测,以甲醇和含10 mmol·L−1的甲酸水溶液作为流动相进行梯度洗脱,7种OPFRs采用HLB串联Envi-18固相萃取柱进行预处理并利用GC-MS进行检测。检测结果表明,27种OPFRs的检出限为0.02~2.53 ng·L−1;定量限为0.06~8.43 ng·L−1;回收率为65.82%~108.48%。2021年4月份,采集北京市潮白河地表水和地下水8个水样并检测其OPFRs。实测结果表明:除磷酸三(2-异丙基苯)酯、磷酸异癸基二苯酯、磷酸叔丁基苯二苯酯、磷酸二苄酯外,其余23种OPFRs均有不同程度检出,质量浓度为0~973.17 ng·L−1;磷酸三(2-乙基己基)酯、磷酸三乙酯、磷酸三丙酯、磷酸三异丙酯含量相对较高,分别高达973.17、459.90、315.47、298.41 ng·L−1。采用USEPA模型对水样中的OPFRs进行了健康风险评价, 13种OPFRs的非致癌风险值为0~6.17×10−4,4种OPFRs致癌风险值为1.37×10−9~1.07×10−7;在高暴露条件下,OPFRs的非致癌风险值为1.61×10−5~6.17×10−4,致癌风险值为1.00×10−8~1.07×10−7,均低于风险阈值。上述结果说明,水体中OPFRs产生的健康风险处于较低水平。此次采集的潮白河地表水和地下水水中OPFRs的致癌风险和非致癌风险均处于较低水平。本研究结果可为地表水和地下水水体中OPFRs的检测及风险评价提供参考。
-
关键词:
- 有机磷阻燃剂(OPFRs) /
- 高效液相色谱-串联质谱仪 /
- 气相色谱-质谱联用仪 /
- 固相萃取 /
- 风险评价
Abstract: Organophosphorus flame retardants (OPFRs) have been demonstrated to be teratogenic, carcinogenic, mutagenic and neurotoxic. In order to better study its existing level and health risks, the analytical methods with solid-phase extraction (SPE) pretreatment followed by liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) and gas chromatography-mass spectrometry (GC-MS) were developed to determine 27 OPFRs in the surface and ground water, and their health risk assessment was performed. Twenty OPFRs were determined by MCX cartridge pretreatment coupled by LC-MS/MS method, and gradient elution was performed using methanol and 10 mmol·L−1 formic acid as the mobile phases in the positive mode. Seven OPFRs were determined by GC-MS method with HLB and Envi-18 double cartridge pretreatment. The results showed that the detection limit (LODs), quantitation limit (LOQs) and recoveries for the 27 OPFRs were 0.02~2.53 ng·L−1, 0.06~8.43 ng·L−1, and 65.82%~108.48%, respectively. In April 2021, eight samples from the surface and ground water in Chaobai River, Beijing were collected, and the concentrations of 27 OPFRs in these samples were analyzed. in which only 4 kinds of OPFRs, namely Tri-(2-isopropyl phenyl) phosphate(TIPPP), Isodecyl diphenyl phosphate(IDPP), Tertbutyl phenyl diphenyl phosphate(BPDP) and Dibenzyl phosphate(DBPP) were undetectable, the rest of 23 OPFRs was detected with the concentration range of 0~973.17 ng·L−1, and relative high concentrations for Tris (2-ethylhexyl) phosphate(TEHP), Tri-ethyl phosphate(TEP), Tri-propyl phosphate(TnPP), Tri-isopropyl phosphate(TiPP) were 973.17, 459.90, 315.47, 298.41 ng·L−1, respectively. The health risks posed by OPFRs in Chaobai River water environment were evaluated using the USEPA health risk assessment model. The non-carcinogenic risk values of 13 OPFRs were in the range of 0~6.17×10−4, whereas the carcinogenic risk values of 4 OPFRs were in the range of 1.37×10−9~1.07×10−7. At the high exposure concentrations, the non-carcinogenic risk values of the above 13 OPFRs were in the range of 1.61×10−5~6.17×10−4, the carcinogenic risk values of 4 OPFRs were in the range of 1.00×10−8~1.07×10−7, they were below the low risk threshold, indicating that the health risk caused by OPFRs in Chaobai River surface and ground water was at a low level. The carcinogenic risk and non-carcinogenic risk of OPFRs in Chaobai River surface water and groundwater collected are at a low level. This study can provide a reference for the detection and risk assessment of OPFRs in surface water and groundwater. -
柠檬酸是有机酸中的第一大酸,其在医药和化工等工业领域应用广泛,主要生产原料为木薯和玉米。行业统计数据表明,每生产1 t柠檬酸可产生7.5 t废水[1]。柠檬酸废水中的主要污染物为淀粉、蛋白质、各种有机酸等有机物和N、P、S等无机物[2],且其有机物含量较高,直接排放容易带来水体富营养化风险目前。国内柠檬酸行业普遍采用生物法[3-5]对废水进行处理,然而生化后的出水仍然具有色度深(90~100倍)、COD高(100~120 mg·L−1)和出水生化性(BOD5/COD)低等特点。近年来,国家加大了对污染行业的整治力度,工业废水排放标准也逐渐提高,故研究新型高效的污水深度处理技术已经迫在眉睫。
高级氧化技术是一种新型的污水处理技术,其原理是在电、超声、光照、外加催化剂或高温高压等反应条件下生成具有强氧化性的羟基自由基(·OH),利用·OH将难降解的大分子有机物分解成小分子物质甚至完全矿化[6]。根据自由基生成途径和反应条件的不同,可将其分为臭氧催化氧化[7]、光催化氧化[8]、高铁酸盐(Fe(Ⅵ))氧化[9]等。与其他高级氧化技术相比,臭氧催化氧化法具有独特的优势[10-11]。其操作步骤简单易行、占地面积小、无二次污染、无额外药剂的投入,因而在工业废水处理领域具有广阔的应用前景。
然而,单独采用臭氧催化氧化法降解柠檬酸生化尾水需要投加大量臭氧和催化剂,会增加处理成本,从而大大限制了其实际应用。有研究[12-14]表明,可将臭氧催化氧化技术作为预处理手段,在臭氧催化适度改善废水生化性的基础上耦合生物处理,能够显著降低废水处理的综合成本并提升处理效率[15-18]。作为一种新型高效的污水生物处理法,移动床生物膜反应器(MBBR)工艺兼具传统流化床和生物接触氧化法两者的优点[19]。相较于生物曝气滤池(BAF)等传统的生物处理工艺[20],MBBR工艺负荷高、不需要填料支架和反冲洗设备、操作简便,明显降低了污水的运行成本且可以达到深度处理的效果[21]。将臭氧催化氧化技术与MBBR系统组合,可以形成一种低能耗、低成本、高效率的联合处理工艺,以充分发挥2种工艺的独特优势,提高其在柠檬酸生化尾水处理中的应用价值。
本研究采用臭氧催化氧化-MBBR组合工艺,以某柠檬酸厂生化尾水作为原水进行中试研究,考察了臭氧催化氧化系统对柠檬酸生化尾水的生化性改善情况;在此基础上,进一步研究了臭氧催化氧化-MBBR组合工艺深度降解柠檬酸生化尾水的可行性、运行参数及运行效率,旨在为厂区污水处理系统的升级提供参考。
1. 材料和方法
1.1 实验水质
中试研究所用水来自某柠檬酸废水处理厂二级生化处理后的出水,该废水可生化性差,出水颜色呈深黄色,出水成分复杂。具体水质情况为:COD为100~120 mg·L−1,BOD为8~10 mg·L−1(B/C=0.08~0.09),pH为7.4~7.8。
1.2 中试设备与流程
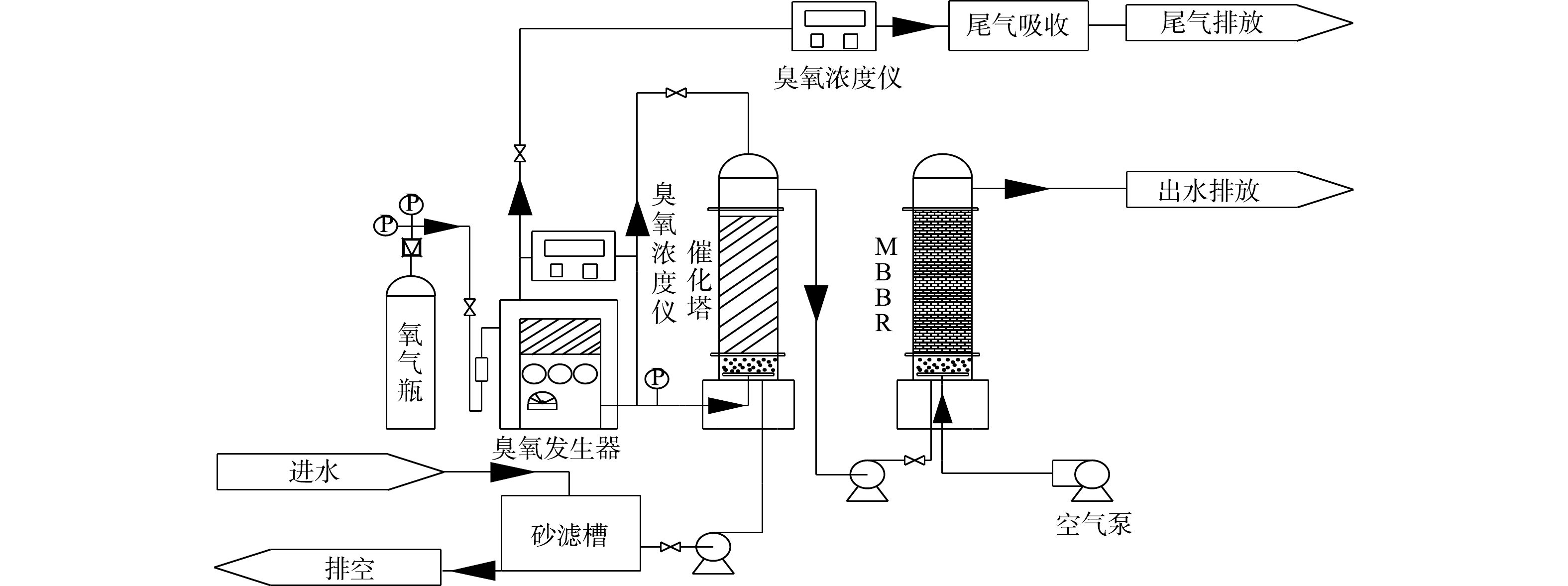
臭氧催化氧化-MBBR中试系统流程图如图1所示。主要包括臭氧催化塔和MBBR生物处理单元2个部分。所用臭氧催化塔由不锈钢加工而成,管径为75 cm,高度为4.5 m,内部填充催化剂,填充率为50%。废水通过立式泵从底部进入催化塔,臭氧发生器以氧气为气源,通过调节阀门使臭氧以1 m3·h−1的流速进入催化塔。生物处理单元的主要反应装置为MBBR,其反应器由有机玻璃加工而成,管径为50 cm,高度为3 m,内部填充有填料,填充比约为40%。反应器在设计流量为0.08 m3·h−1的条件下经立式泵完成连续进水。MBBR运行时所需的空气来自空气泵,接种污泥为柠檬酸厂活性污泥,质量浓度约为4 000 mg·L−1。
1.3 催化剂与填料
在臭氧催化体系中,所填充的催化剂为实验室自制的MnOx-CeOx复合双金属氧化物[22]。该催化剂经高温煅烧制得,具有机械强度高、吸附性能强和催化性能好等优点。在MBBR系统中,所用填料为圆柱体聚乙烯塑料,直径约为10 mm,高为8~9 mm。圆柱体中有十字支撑,具有较高的比表面积(160~500 m2·m−3),密度略小于水(0.92~0.97 g·cm−3)。该填料的特有性质有利于微生物在填料上富集和生长,形成比较稳定的生物膜,并且在反应器中易呈现流化状态。
1.4 实验方法
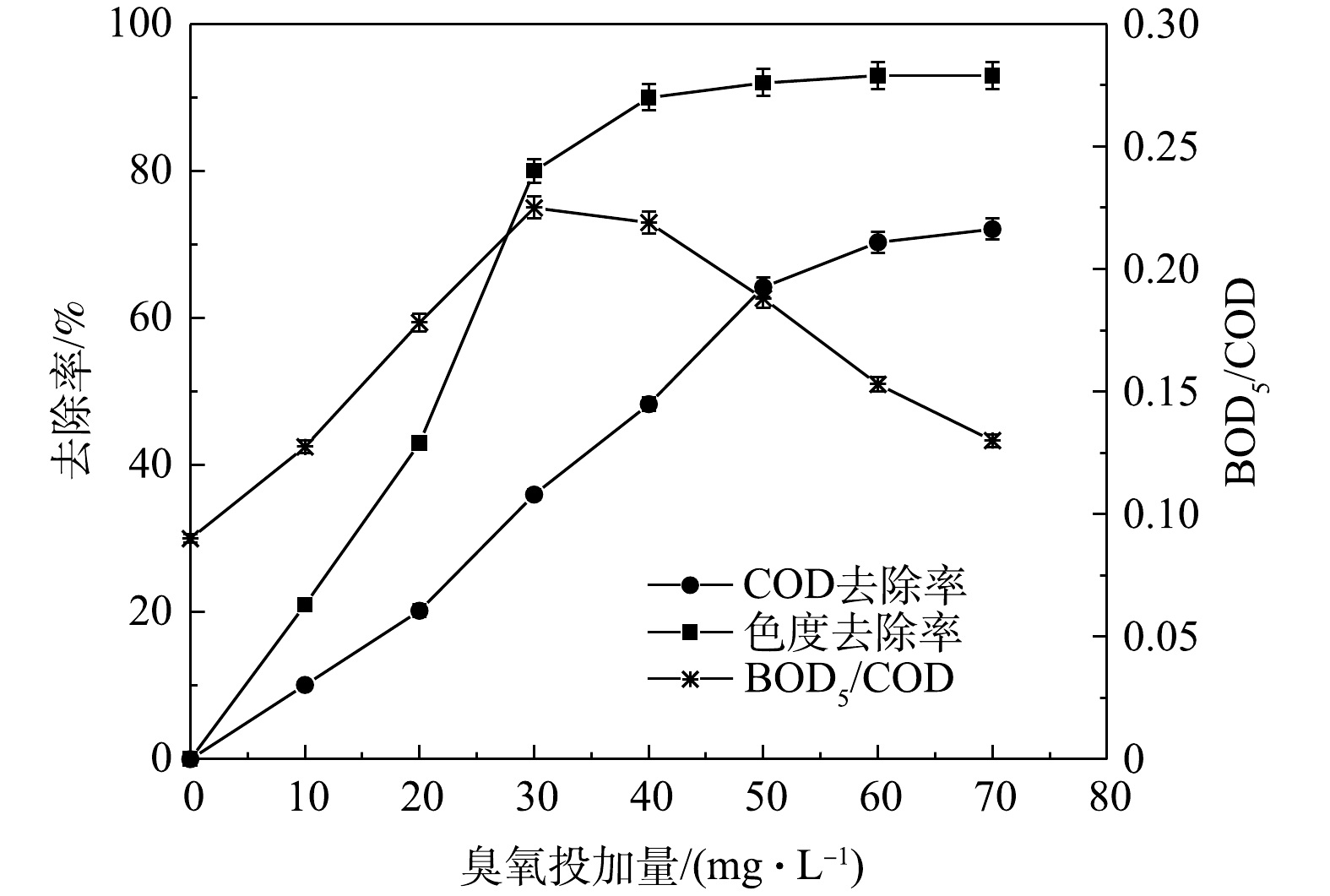
1)臭氧催化氧化段。在进水平均COD、色度和BOD5/COD分别为110 mg·L−1、90倍和0.08的条件下,首先对臭氧投加量进行优化。在臭氧反应时间为60 min,进气流量为1 m3·h−1的条件下,连续运行,分别调整臭氧投加量为10、20、30、40、50、60、70 mg·L−1,比较在不同臭氧投加量下COD、色度的去除率以及出水BOD5/COD的变化特征,选取最佳的臭氧投加量。在获得最佳臭氧投加量的基础上,固定最佳臭氧投加量,进气流量为1 m3·h−1,连续运行,分别调整水力停留时间(HRTo)为30、40、50、60、70、80 min,比较在不同的HRTo下COD、色度的去除率以及出水BOD5/COD的变化特征,获得最佳的HRTo。
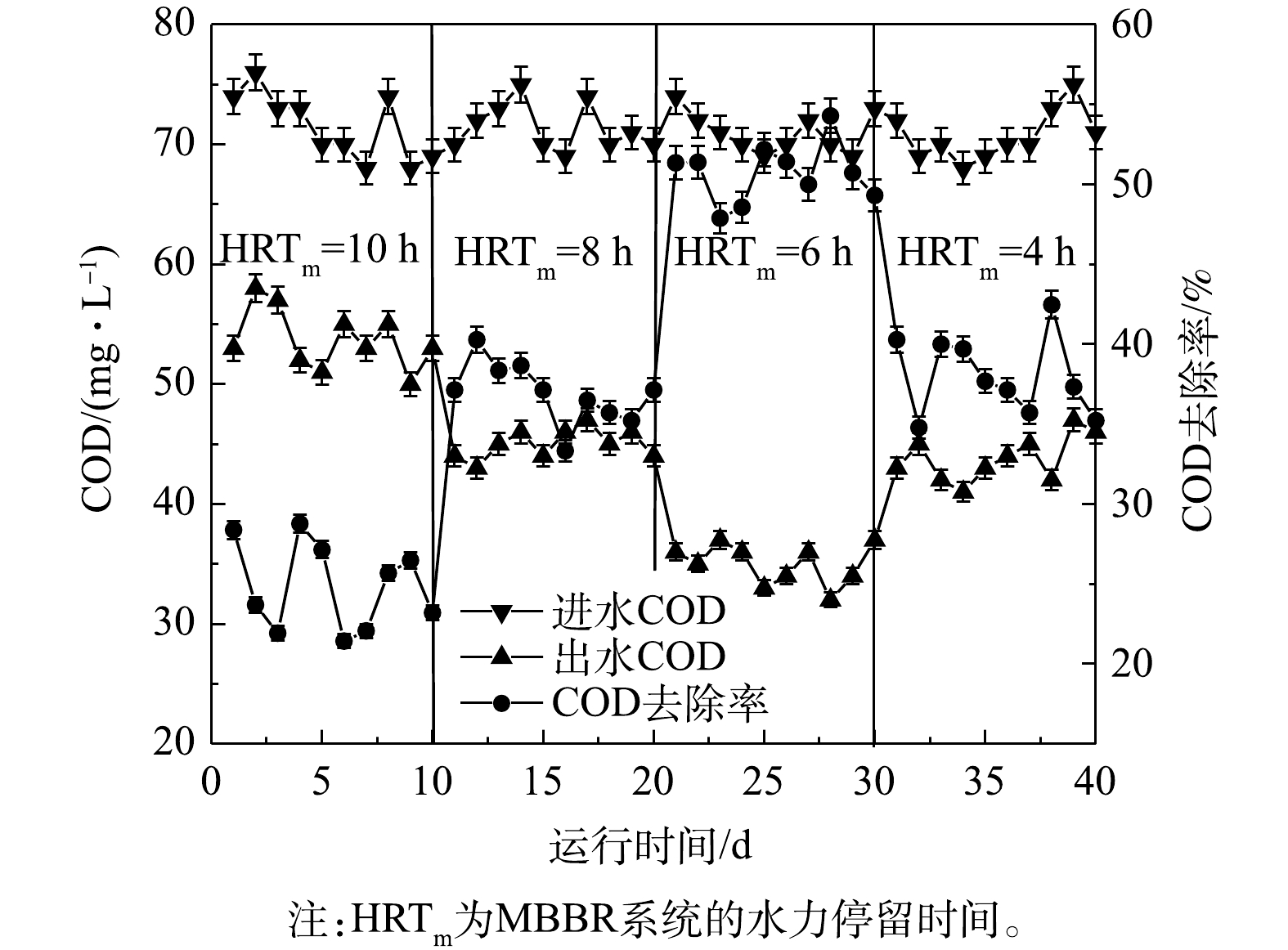
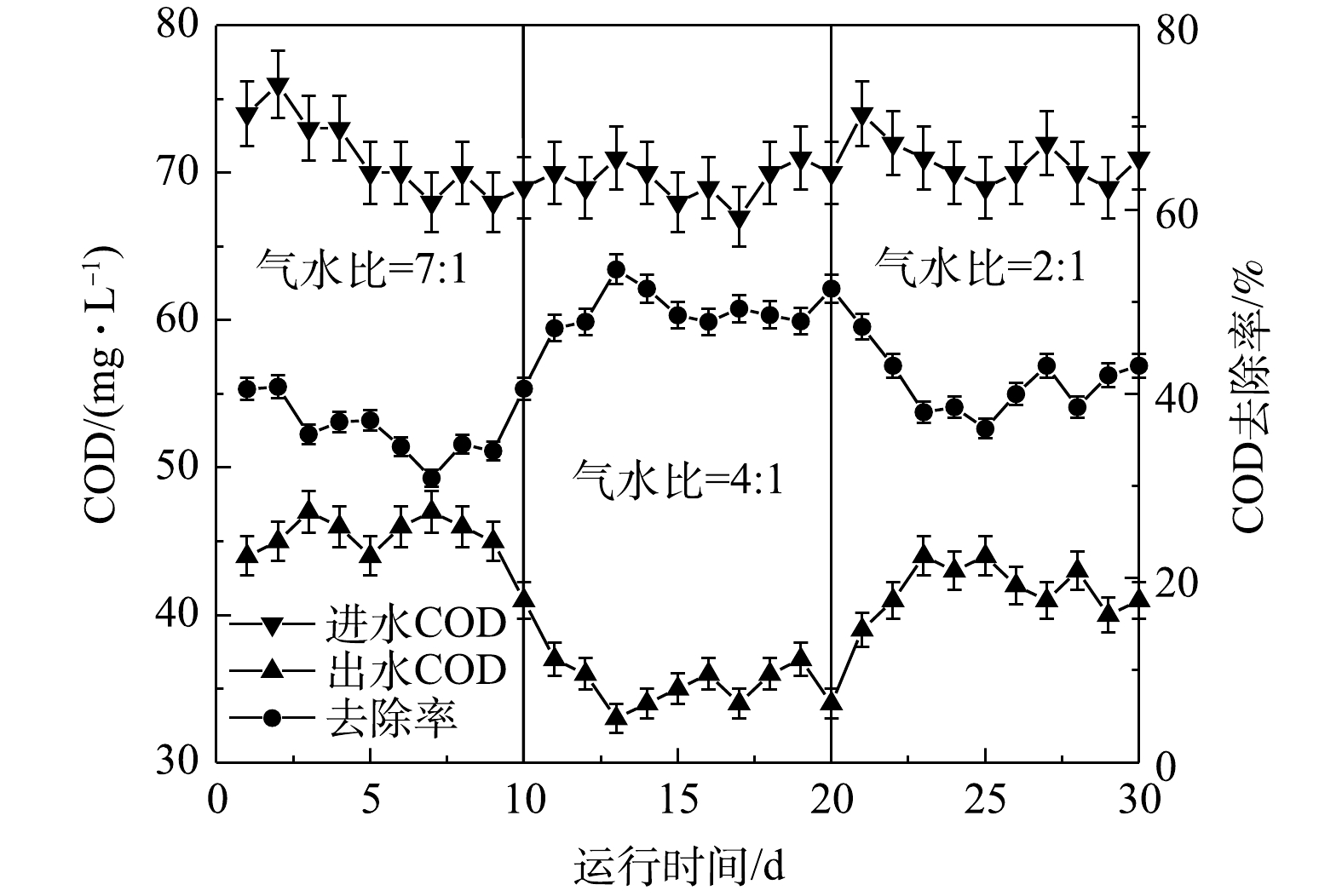
2) MBBR段。将0.4 m3左右的泥水混合物倒入反应器中,静置2 h,使污泥能够充分地与填料接触,然后加入臭氧催化氧化处理后的废水闷曝48 h。在48 h后,采用连续进水的方式,启动挂膜阶段控制气水比为4∶1,分别调整水力停留时间(HRTm)为10、8、6、4 h,每个条件运行10 d,比较不同HRTm下COD的去除率,选取最佳的HRTm;在获得最佳HRTm的基础上,分别调整气水比为7∶1、4∶1、2∶1,比较在不同气水比的条件下COD的去除率,获得最佳气水比。
1.5 分析方法
采用标准方法[23]测定COD和SS;采用稀释倍数法测定色度;采用五日生化法测定BOD5;采用YSI DO200型溶解氧温度仪测量DO;采用同林科技ZX-01测定臭氧浓度;采用气相色谱质谱仪(GC/MS,7890B+5977A)测定污水中有机物的种类。
2. 结果与讨论
2.1 臭氧催化氧化系统的运行
1)臭氧投加量对臭氧催化氧化的影响。由图2可知,随着臭氧投加量的增加,出水COD、色度去除率和出水BOD5/COD均不断提高,当臭氧投加量为30 mg·L−1时,COD和色度去除率分别为36.0%和80.0%,出水BOD5/COD值则达到最大值0.23。这表明此时废水中的有机成分在臭氧及羟基自由基作用下发生分解,生成大量中间产物和小分子有机物,导致生化性明显改善;继续增加臭氧投加量,COD去除率继续提高,色度的去除率趋于平稳,出水BOD5/COD开始下降。显然,这是因为·OH进一步矿化废水中的部分中间产物所导致的。因此,为保证MBBR段的进水生化性和处理效率,确定最佳臭氧投加量为30 mg·L−1。
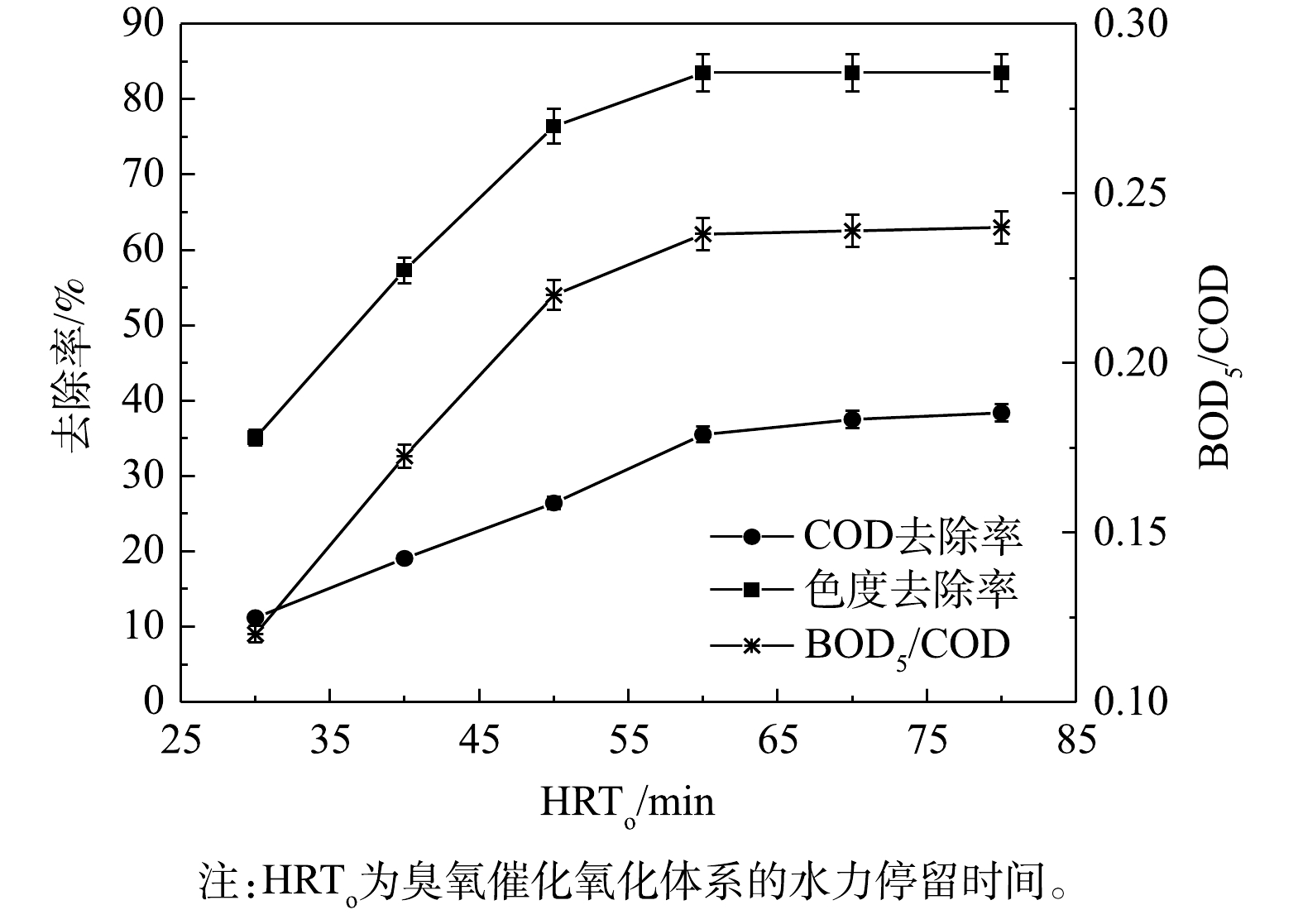
2) HRTo对臭氧催化氧化的影响。图3反映了COD、色度去除率和出水BOD5/COD随HRTo的变化情况。当HRTo为30 min时,COD、色度去除率和出水BOD5/COD分别11.2%、35.1%和0.12;当HRTo为60 min时,COD、色度去除率分别为35.4%和83.3%,出水生化性BOD5/COD由0.12提升至0.24;继续延长HRTo,COD、色度去除率和出水的BOD5/COD都趋于平缓,且反应时间越长,臭氧投加量增加,会导致运行成本升高。上述结果表明,在本实验条件下,将HRTo控制在60 min可确保臭氧催化氧化的效果,有效地改善柠檬酸生化尾水的可生化性,从而有利于后续MBBR单元的生物降解。综合考虑能耗和成本,确定最佳HRTo为60 min。
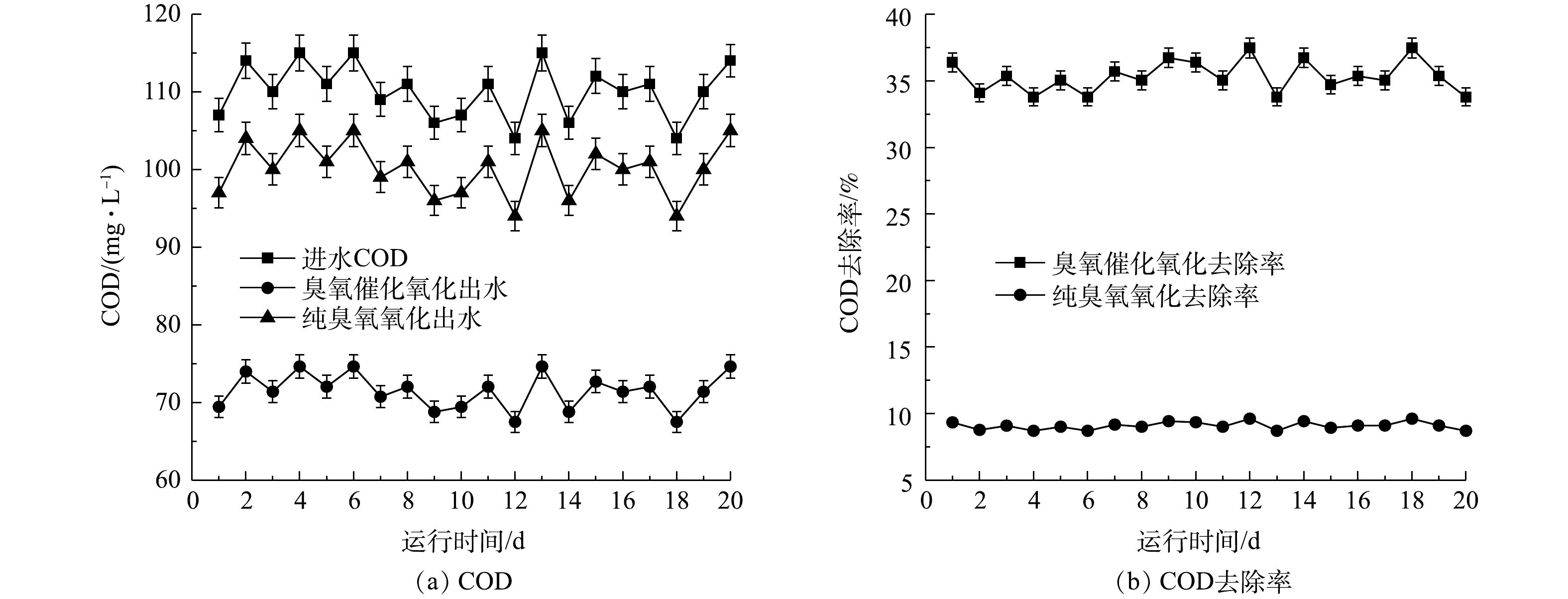
3)不同反应体系对COD去除的影响。在臭氧投加量为30 mg·L−1,水力停留时间为60 min,进气量1 m3·h−1的条件下,考察纯臭氧氧化体系和臭氧催化氧化体系对COD的去除效果,结果如图4所示。由图4可知,在臭氧催化氧化体系中,平均COD去除率为35.5%,相较于纯臭氧氧化体系中,平均COD去除率提高了24%。这是因为在纯臭氧氧化体系中,主要以臭氧直接参与反应为主,臭氧的选择性氧化和气液传质较差导致去除率较低;而在臭氧催化氧化体系中,催化剂的存在使得系统中产生了大量·OH,增强传质,进而可提高废水COD去除率。
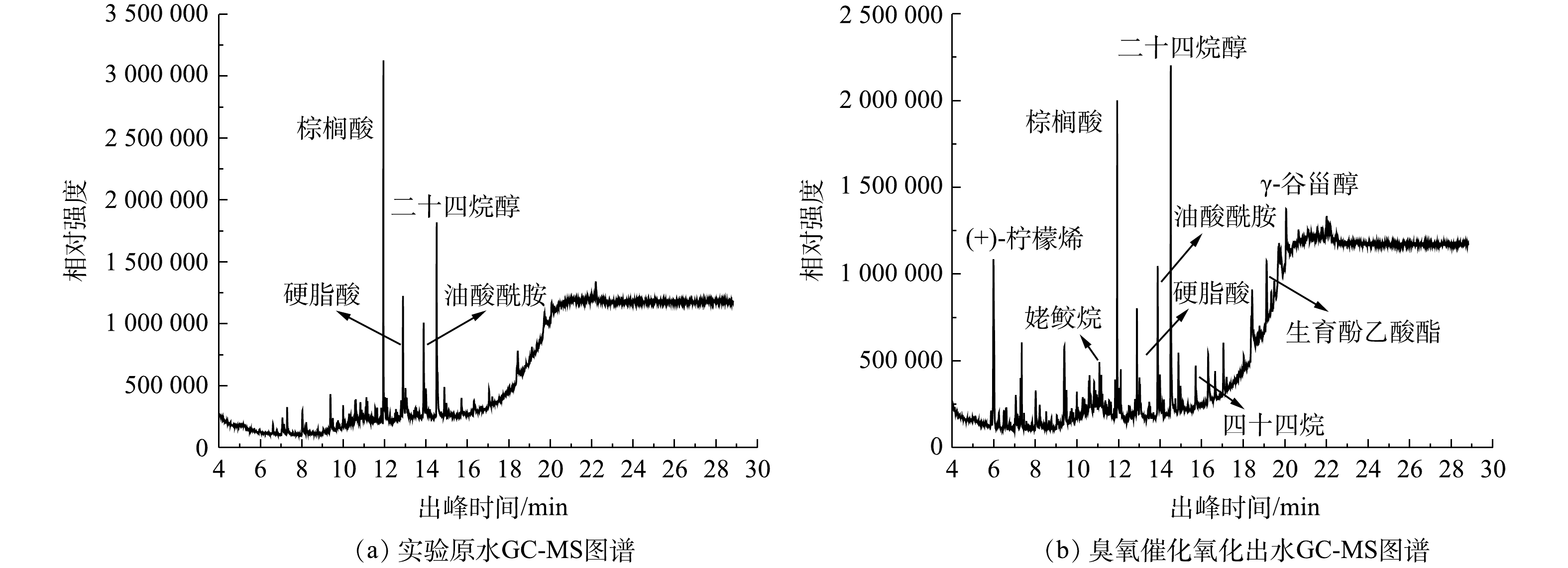
4)水质成分分析。为了进一步验证臭氧催化氧化技术能够改善柠檬酸生化尾水的生化性,在臭氧投加量为30 mg·L−1,水力停留时间为60 min,进气量1 m3·h−1的条件下,对实验原水和臭氧催化氧化出水进行GC-MS分析,分析结果如图5所示。结果表明,实验原水中的主要污染物为11种,其中脂肪酸、酰胺类等物质为主要污染物,在其他类有机物中,部分有机物含有乙烯基、羰基、苯环等发色基团,故导致柠檬酸废水呈现颜色。经臭氧催化预处理后的出水中主要污染物可达到20种,其主要为烷烃类、酯类和醇类。由此可见,在臭氧催化氧化处理后,废水中的脂肪酸类和其他类有机物被分解成简单的酯类和部分链状烷烃类,使柠檬酸生化尾水的生化性得到了显著改善,色度明显降低。
2.2 MBBR生化系统运行情况
1) HRTm对MBBR系统处理效果的影响。以优化后的臭氧催化氧化工艺段的出水作为MBBR系统的进水,设定气水比为4∶1,探究HRTm对MBBR系统运行的影响。由于进水色度较低,改变运行条件对色度去除不明显,因此,主要以COD去除率为指标优化运行参数。由图6可知,当HRTm由10 h降至6 h,COD平均去除率由24.9%升高至50.7%;继续缩短HRTm,COD去除率反而开始下降。当HRTm为10 h时,系统中有机负荷较低,系统处于驯化启动阶段,COD去除效果相对较差;随着HRTm的缩短,MBBR系统的有机负荷提高,微生物大量繁殖,污染物得到充分降解,从而使得COD去除效果得到改善;继续缩短HRTm,MBBR系统中的微生物没有充分吸收和降解废水中的有机物,导致COD去除效果变差。根据上述结果,本研究确定MBBR系统的最佳HRTm为6 h。
2)气水比对MBBR系统处理效果的影响。设定HRTm为6 h,探究气水比对MBBR系统处理效果的影响。由图7可知,将气水比由7∶1减小到4∶1后,COD平均去除率由36.5%增加到49.3%。继续减小气水比,COD平均去除率开始下降。这是因为初始系统中气水比过高,导致生物膜受到冲刷而脱落[24],不利于污染物的截留和微生物的生长繁殖,导致COD去除效果较差。随着气水比的降低,填料在水中逐渐呈现流化态,此时系统中气、水、填料三者充分接触,加速了生物膜的生长,从而改善了COD的去除效果。当气水比过低时,填料在水中的流化状态受到影响,同时废水中的溶解氧不足导致好氧微生物活性受到抑制,不利于废水中有机污染物的去除。根据上述实验结果,确定最佳气水比为4∶1。
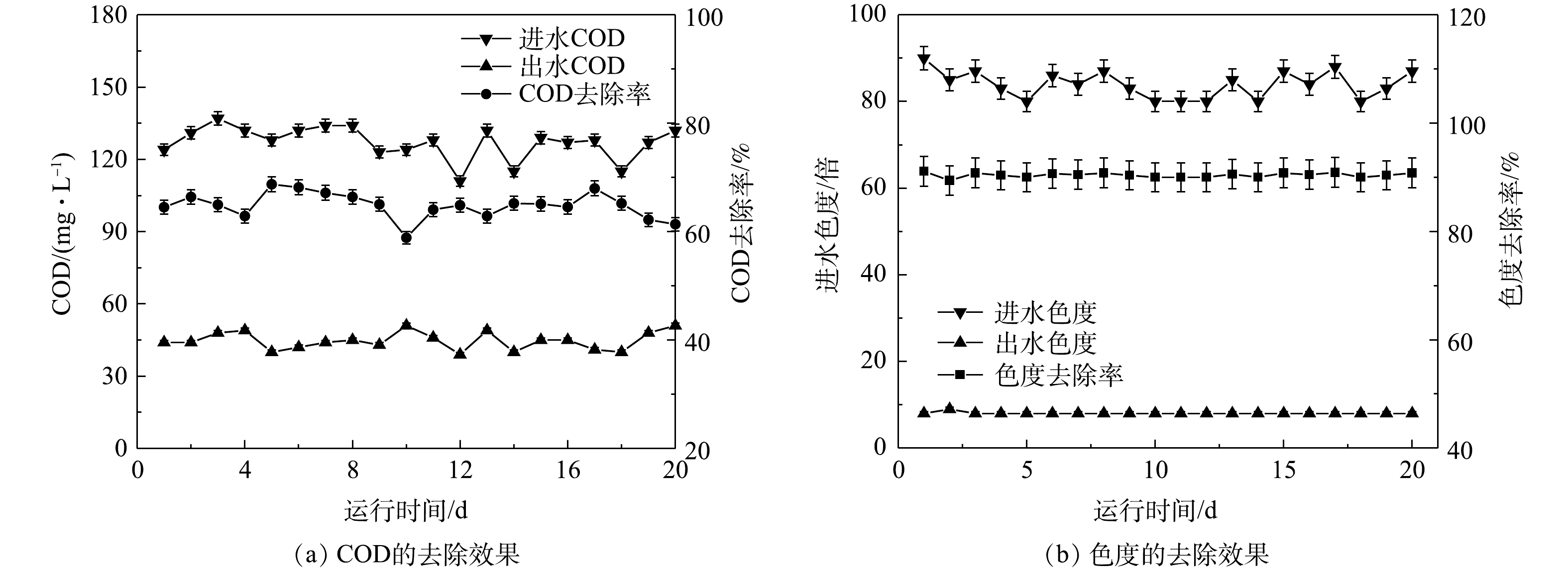
3)最优条件下连续运行效果。在确定最优的条件下将2种工艺组合运行20 d,每天定时采样测试以探究工艺连续运行的效果,结果如图8所示。在连续运行20 d期间,臭氧催化氧化-MBBR组合工艺处理效果良好,系统出水COD由100~120 mg·L−1降至32~40 mg·L−1,COD去除率维持在66.2%~74.7%,出水色度由90~100倍降至10倍左右,色度去除率维持在90.0%~94.0%。此外,该组合工艺的出水不会返色且表观清澈透明,填料上的生物膜生长良好(图9),反应器中始终维持着较高的生物量。以上结果表明,臭氧催化氧化-MBBR组合工艺对柠檬酸生化尾水深度降解有显著效果。
2.3 运行成本初步分析
采用臭氧催化氧化-MBBR组合工艺处理柠檬酸生化尾水的运行成本主要来自臭氧催化单元中臭氧和生化处理单元的能耗2个方面。其中,当臭氧投加量为30 mg·L−1,进气量为1 m3·h−1时,每克臭氧耗电量为20 W,处理每吨水的耗电量为0.6 kW。电费按0.70 元·(kW·h)−1计,则臭氧单元的电费为0.42 元·t−1。MBBR单元处理[25]能耗按0.07 元·t−1计,该组合工艺的运行成本约为0.49 元·t−1。工业级液氧价格大约800 元·t−1,产生30 g臭氧所需要的费用约为0.24 元。催化剂折旧费用约为0.06 元·t−1,该组合工艺总费用约为0.79 元·t−1。单独使用臭氧催化氧化技术,要达到相同的处理效果需要臭氧投加量为50 mg·L−1,则需要总费用约为1.16 元·t−1。综合上述结果可知,臭氧催化氧化-MBBR组合工艺处理柠檬酸生化尾水经济效益更高。
3. 结论
1)本研究以MnOx-CeOx复合双金属氧化物为催化剂,采用臭氧催化氧化法对柠檬酸生化尾水进行预处理。在臭氧投加量为30 mg·L−1、HRTo为60 min、进气量为1 m3·h−1的条件下,臭氧催化预处理生化尾水的COD和色度去除率分别35.4%和83.3%,出水生化性由0.08提升至0.23,显著提高了废水的生化性。
2)采用MBBR对臭氧催化氧化单元的出水进行处理,在HRTm为6 h、气水比为4∶1的条件下,出水COD为32~40 mg·L−1,色度能够稳定在10倍左右。
3)臭氧催化氧化-MBBR组合工艺的运行成本约为0.79 元·t−1,较单独使用臭氧催化氧化技术(1.16 元·t−1)节约运行成本。采用臭氧催化氧化-MBBR组合工艺减少了臭氧的投加量,在降低废水处理成本的同时提高了对柠檬酸生化尾水的处理效率。
-
表 1 20种OPFRs的LC-MS/MS参数
Table 1. LC-MS/MS parameters of 20 OPFRs
化合物 出峰时间/min 母离子质荷比 定量离子质荷比 四极杆电压1 (Q1)/V 碰撞室电压(CE)/V 四极杆电压2 (Q3)/V 第1次 第2次 第3次 第1次 第2次 第3次 第1次 第2次 第3次 TEP 2.143 183.10 98.90 126.90 154.90 −20 −20 −14 −12 −19 −23 −30 TCEP 2.164 285.00 63.00 98.90 222.80 −19 −27 −23 −13 −26 −19 −25 TPPO 2.775 278.90 200.95 76.95 173.00 −19 −26 −48 −33 −23 −27 −12 TCPP 2.928 327.00 99.00 174.85 250.90 −15 −21 −13 −9 −18 −19 −28 TiPP 3.089 225.20 98.95 140.95 80.90 −17 −16 −10 −48 −19 −16 −30 TnPP 3.095 225.20 98.95 141.00 192.95 −16 −17 −10 −7 −18 −26 −13 IDDP 3.594 293.10 251.00 76.95 153.05 −14 −11 −41 −25 −26 −29 −29 TDCPP 3.778 430.90 98.90 208.90 210.85 −20 −29 −18 −17 −19 −23 −22 TPhP 4.198 327.10 77.00 151.90 214.90 −11 −45 −39 −28 −14 −28 −23 TiBP 4.593 267.20 98.95 155.00 80.85 −20 −15 −9 −55 −20 −11 −30 TnBP 4.594 267.20 98.95 154.95 211.10 −20 −21 −11 −9 −19 −30 −24 MDPP 4.833 341.10 152.00 165.00 90.90 −12 −34 −33 −36 −30 −30 −17 TBEP 4.954 399.30 199.00 299.15 45.00 −27 −16 −14 −25 −14 −22 −17 TPeP 6.683 309.30 99.00 169.00 239.00 −11 −20 −11 −9 −19 −12 −27 EHDPP 6.689 363.20 251.05 76.90 151.90 −18 −10 −49 −45 −18 −14 −26 IDPP 7.787 391.30 251.00 76.95 148.90 −14 −14 −45 −24 −28 −30 −30 TXP 8.240 411.20 104.95 179.05 194.00 −14 −34 −42 −31 −18 −19 −20 TDMPP 8.255 411.20 178.95 194.00 79.05 −28 −47 −30 −50 −18 −22 −14 TIPPP 8.414 453.30 327.00 411.10 369.10 −16 −30 −18 −22 −23 −21 −27 THP 8.540 351.30 99.10 182.95 267.15 −12 −20 −12 −10 −19 −21 −30 表 2 7种OPFRs的 GC-MS参数
Table 2. GC-MS parameters of 7 kinds of OPFRs
化合物 出峰时间/min 基峰 定性峰1 定性峰2 BEHP 43.559 99 113 55 TEHP 43.566 99 113 57 BPDP 47.459 367 368 382 DBPP 48.373 91 92 277 o-TTP 45.352 165 368 179 m-TTP 46.273 368 367 165 p-TTP 47.577 368 367 107 表 3 27种PPCPs的参数对比
Table 3. Parameter comparison of 27 PPCPs
化合物 可决系数R2 回收率/% 相对标准偏差RSD/% 检出限/(ng·L−1) 定量限/(ng·L−1) 检测方法 TDMPP 0.991 75.99 5.6 0.19 0.64 LC-MS/MS TCEP 0.996 81.37 3.5 0.28 0.93 LC-MS/MS TiBP 0.999 98.35 6.3 0.37 1.23 LC-MS/MS TnPP 0.992 94.68 5.7 0.05 0.18 LC-MS/MS TiPP 0.994 98.25 4.6 0.03 0.11 LC-MS/MS MDPP 0.996 66.30 3.6 0.31 1.04 LC-MS/MS IDPP 0.996 74.88 3.1 0.37 1.24 LC-MS/MS TIPPP 0.999 97.57 7.8 0.31 1.02 LC-MS/MS TPeP 0.999 90.51 6.5 0.04 0.14 LC-MS/MS EHDPP 0.998 95.03 9.3 0.07 0.23 LC-MS/MS TEP 0.999 76.20 5.1 0.1 0.32 LC-MS/MS TCPP 0.998 65.82 2.4 0.03 0.11 LC-MS/MS TBEP 0.999 74.48 10.6 0.05 0.16 LC-MS/MS TnBP 0.999 102.14 8.3 0.02 0.06 LC-MS/MS THP 0.994 81.16 9.4 0.13 0.44 LC-MS/MS TPhP 0.996 80.91 8.0 0.13 0.42 LC-MS/MS TPPO 0.998 94.59 10.1 0.02 0.08 LC-MS/MS IDDP 0.994 75.96 8.3 0.08 0.25 LC-MS/MS TDCPP 0.999 70.54 6.3 0.29 0.96 LC-MS/MS TXP 0.996 77.14 5.1 0.10 0.32 LC-MS/MS BEHP 0.993 95.36 4.2 0.55 1.83 GC-MS TEHP 0.999 101.36 4.2 0.49 1.62 GC-MS BPDP 0.999 103.35 6.4 2.53 8.43 GC-MS DBPP 0.994 86.38 5.2 0.74 2.45 GC-MS o-TTP 0.999 95.80 6.3 0.39 1.31 GC-MS m-TTP 0.999 92.76 8.2 0.59 1.96 GC-MS p-TTP 0.997 108.48 6.1 0.68 2.28 GC-MS 表 4 23种OPFRs在8个采样点中的质量浓度
Table 4. Mass concentrations of 23 kinds of OPFRs in 8 sampling points
化合物 地表水/(ng·L−1) 地下水/(ng·L−1) S1 S2 S3 S4 1# 2# 3# 4# TDMPP 1.83 1.98 0 6.56 72.23 105.33 46.54 61.75 TCEP 40.05 37.07 4.37 7.06 29.31 8.03 11.41 25.88 TiBP 16.23 15.99 12.19 8.15 13.25 32.58 27.64 34.35 TnPP 315.47 192.76 46.46 44.67 29.30 208.83 191.06 201.69 TiPP 298.41 189.09 64.68 46.72 10.34 116.51 105.91 102.14 MDPP 0.57 0.48 0.52 1.25 2.24 2.39 0 12.22 TPeP 0.43 0 0 0 0 0.46 0 2.03 EHDPP 1.44 1.03 1.05 0.88 0.88 8.96 2.88 6.15 TEP 136.53 133.21 17.38 459.90 7.48 80.94 113.56 71.21 TCPP 61.23 45.63 9.54 26.56 17.75 65.76 21.81 83.39 m-TTP 2.31 2.67 2.49 6.41 11.63 9.97 1.60 87.27 o-TTP 0.49 0.68 1.01 1.20 2.28 4.75 8.93 15.39 TBEP 27.01 5.74 1.21 0.62 1.33 8.01 2.52 7.35 TnBP 51.34 41.09 14.49 31.80 64.99 116.36 57.86 86.04 THP 1.11 0.66 1.01 0.92 0.67 0.76 0 1.60 TPhP 2.32 0 3.27 2.78 3.06 4.93 3.36 9.11 TPPO 70.60 53.56 55.84 12.26 37.41 30.29 27.60 53.75 p-TTP 0.84 0.96 0.72 2.94 1.74 3.38 0 23.86 IDDP 2.98 0.64 0.89 2.83 0.97 1.13 2.88 5.63 TDCPP 8.06 9.88 1.50 2.36 2.47 4.83 5.80 10.96 TXP 1.24 1.86 0.49 5.34 82.13 116.10 38.16 64.94 BEHP 0.31 0.27 0.24 0.51 3.85 9.93 0.81 1.36 TEHP 30.46 26.95 23.04 50.38 376.85 973.17 79.27 133.17 ƩOPFRs 1 071.26 762.2 262.39 722.1 772.16 1 913.4 749.6 1 101.24 表 5 OPFRs 暴露风险计算参数
Table 5. Parameters for the exposure risk calculation to OPFRs
性别 儿童或成人 饮水量/(L·d-1) 人体质量/kg 男性 儿童 0.81 24 成人 2.23 65 女性 儿童 0.76 23 成人 1.65 56 表 6 OPFRs的参考剂量值和斜率致癌因子参数值
Table 6. Chronic oral reference dose and oral slope factor values of OPFRs
化合物 参考剂量值/(ng·(kg·d)−1) 致癌斜率因子/(ng·(kg·d)−1) TEP 125 000 — TnBP 10 000 9.00×10−9 TDCPP 20 000 3.10×10−8 TPHP 7 000 — EHDPP 15 000 — o-TTP 20 000 — m-TTP 20 000 — p-TTP 20 000 — TCEP 7 000 2.00×10−8 TCPP 10 000 — TBEP 15 000 — TPPO 20 000 — TEHP 100 000 3.10×10−9 -
[1] LI S H, ZHU F F, ZHANG D R, et al. Seasonal concentration variation and potential influencing factors of organophosphorus flame retardants in a wastewater treatment plant[J]. Environmental Research, 2021, 199: 111318. doi: 10.1016/j.envres.2021.111318 [2] LIU Y H, SONG N H, GUO R X, et al. Occurrence and partitioning behavior of organophosphate esters in surface water and sediment of a shallow Chinese freshwater lake (Taihu Lake): Implication for eco-toxicity risk[J]. Chemosphere, 2018, 202: 255-263. doi: 10.1016/j.chemosphere.2018.03.108 [3] LEE S, JEONG W, KANNAN K, et al. Occurrence and exposure assessment of organophosphate flame retardants (OPFRs) through the consumption of drinking water in Korea[J]. Water Research, 2016, 103: 182-188. doi: 10.1016/j.watres.2016.07.034 [4] 杨露敏, 宋晓翠, 张颖, 等. 自来水给水系统中有机磷酸酯的污染特征及健康风险评价[J]. 环境科学学报, 2021, 41(8): 3268-3278. [5] CHEN Y X, LIU Q Y, MA J, et al. A review on organophosphate flame retardants in indoor dust from China: Implications for human exposure[J]. Chemosphere, 2020, 260: 127633. doi: 10.1016/j.chemosphere.2020.127633 [6] XING L Q, ZHANG Q, SUN X, et al. Occurrence, distribution and risk assessment of organophosphate esters in surface water and sediment from a shallow freshwater Lake, China[J]. Science of the Total Environment, 2018, 636: 632-640. doi: 10.1016/j.scitotenv.2018.04.320 [7] LI W H, WANG Y, ALEXANDROS G A, et al. Organophosphate esters in indoor dust from 12 countries: Concentrations, composition profiles, and human exposure[J]. Environment International, 2019, 133: 105178. doi: 10.1016/j.envint.2019.105178 [8] ZHONG M Y, TANG J H, MI L J, et al. Occurrence and spatial distribution of organophosphorus flame retardants and plasticizers in the Bohai and Yellow Seas, China[J]. Marine Pollution Bulletin, 2017, 121: 331-338. doi: 10.1016/j.marpolbul.2017.06.034 [9] LI J, YU N Y, ZHANG B B, et al. Occurrence of organophosphate flame retardants in drinking water from China[J]. Water Research, 2014, 54: 53-61. doi: 10.1016/j.watres.2014.01.031 [10] NADEEM A, ALIN C D, NELE V D E, et al. Occurrence of alternative flame retardants in indoor dust from New Zealand: Indoor sources and human exposure assessment[J]. Chemosphere, 2012, 88(11): 1276-1282. doi: 10.1016/j.chemosphere.2012.03.100 [11] HAN X, HAO Y F, LI Y M, et al. Occurrence and distribution of organophosphate esters in the air and soils of Ny-Ålesund and London Island, Svalbard, Arctic[J]. Environmental Pollution, 2020, 263: 114495. doi: 10.1016/j.envpol.2020.114495 [12] TAN X X, LUO X J, ZHENG X B, et al. Distribution of organophosphorus flame retardants in sediments from the Pearl River Delta in South China[J]. Science of the Total Environment, 2016, 544: 77-84. doi: 10.1016/j.scitotenv.2015.11.089 [13] CHEN M H, MA W L. A review on the occurrence of organophosphate flame retardants in the aquatic environment in China and implications for risk assessment[J]. Science of the Total Environment, 2021, 783: 147064. doi: 10.1016/j.scitotenv.2021.147064 [14] United States Environment Protection Agency. Atlantic Risk Assessment, Regional Screening Levels (RSLs)-Generic Tables[M/OL]. (2017-01-19)[2022-01-20]. Washington, 2017. https://www.epa.gov/region9/superfund/prg. [15] LI J F, HE J H, LI Y N, et al. Assessing the threats of organophosphate esters (flame retardants and plasticizers) to drinking water safety based on USEPA oral reference dose (RfD) and oral cancer slope factor (SFO)[J]. Water Research, 2019, 154: 84-93. doi: 10.1016/j.watres.2019.01.035 [16] DING J J, SHEN X L, LIU W P, et al. Occurrence and risk assessment of organophosphate esters in drinking water from Eastern China[J]. Science of the Total Environment, 2015, 538: 959-965. doi: 10.1016/j.scitotenv.2015.08.101 [17] 赵秀阁, 段小丽. 中国人群暴露参数手册(成人卷): 概要[M]. 北京: 中国环境科学出版社, 2014. [18] SHI W, ZHANG F X, ZHANG X W, et al. Identification of trace organic pollutants in freshwater sources in Eastern China and estimation of their associated human health risks[J]. Ecotoxicology, 2011, 20(5): 1099-1106. doi: 10.1007/s10646-011-0671-8 [19] 董政, 马玉龙, 李珺琪, 等. 潍坊滨海经济技术开发区饮用水中有机磷酸酯的水平及人体暴露风险评估[J]. 环境科学, 2017, 38(10): 4212-4219. [20] LI J F, ZHANG Z Z, MA L Y, et al. Implementation of USEPA RfD and SFO for improved risk assessment of organophosphate esters (organophosphate flame retardants and plasticizers)[J]. Environment International, 2018, 114: 21-26. doi: 10.1016/j.envint.2018.02.027 [21] 高立红. 北京市城市环境有机磷酸酯污染水平和分布特征研究[D]. 北京: 北京科技大学, 2016. [22] 陈玫宏, 徐怀洲, 宋宁慧, 等. 高效液相色谱-串联质谱法同时测定水体和沉积物中12种有机磷酸酯类化合物[J]. 分析化学, 2017, 45(7): 987-995. doi: 10.11895/j.issn.0253-3820.170180 [23] SHI Y L, GAO L H, LI W H, et al. Occurrence, distribution and seasonal variation of organophosphate flame retardants and plasticizers in urban surface water in Beijing. China[J]. Environmental Pollution, 2016, 209: 1-10. doi: 10.1016/j.envpol.2015.11.008 [24] 李栋, 张圣虎, 张芹, 等. 长江南京段水源水中有机磷酸酯的污染特征与风险评估[J]. 环境科学, 2020, 41(1): 205-212. [25] 王艺璇, 张芹, 宋宁慧, 等. 南京市雪水中有机磷阻燃剂的污染特征及健康风险评价[J]. 中国环境科学, 2019, 39(12): 5101-5109. [26] STEPIEN D K, REGNERY J, MERZ C, et al. Behavior of organophosphates and hydrophilic ethers during bank filtration and their potential application as organic tracers: A field study from the Oderbruch, Germany[J]. Science of the Total Environment, 2013, 458-460: 150-159. doi: 10.1016/j.scitotenv.2013.04.020 [27] CAO Z G, XU F C, COVACI A, et al. Distribution patterns of brominated, chlorinated, and phosphorus flame retardants with particle size in indoor and outdoor dust and implications for human exposure[J]. Environmental Science & Technology, 2014, 48(15): 8839-8846. [28] REEMTSMA T, JOSE B Q, RODIL R, et al. Organophosphorus flame retardants and plasticizers in water and air I. Occurrence and fate[J]. Trends in Analytical Chemistry, 2008, 27(9): 727-737. [29] 朱舟, 顾炜旻, 安伟, 等. 基于umu遗传毒性效应的饮用水致癌风险评价的尝试[J]. 生态毒理学报, 2008, 3(4): 363-369. doi: 10.1016/j.trac.2008.07.002 -




 下载:
下载: