-
好氧颗粒污泥是微生物在好氧条件下自凝聚形成的一种结构紧密的颗粒状活性污泥[1-2]。与传统活性污泥相比,好氧颗粒污泥具有沉降性能优良、微生物种类多样、生物量高、单级同步脱氮除磷等优点[3-5]。自1991年首次在连续流反应器中培养得到好氧颗粒污泥报道以来[6],有研究[7-8]发现,以葡萄糖或乙酸钠为单一碳培养好氧颗粒污泥存在污泥易膨胀和颗粒污泥结构松散等问题。王芳等[9]采用以葡萄糖和乙酸钠为混合碳源培养的好氧颗粒污泥表面光滑、结构紧密。培养过程中SBR调控方法的不同会导致培养结果也有差异。赵霞等[10]采用调控表面上升气速的方法培养出结构密实且表面有大量丝状菌存在的颗粒污泥;但是通过增大耗氧有机污染物浓度和表面上升气速的方式培养出的好氧颗粒污泥表面光滑且无丝状菌存在[9]。郭承元等[11]以容积负荷和沉降时间为调控参数培养出了表面凹凸不平、内部出现空洞且表面以杆菌为主的好氧颗粒污泥。以上研究在好氧颗粒污泥的培养过程中均采用调控单一条件,同时调控多因素的好氧颗粒污泥培养研究鲜有报道。
因此,本实验在SBR中,采用以葡萄糖和乙酸钠为混合碳源,通过提高进水COD值、表面上升气速,缩短污泥沉降时间的方法培养好氧颗粒污泥,研究污泥颗粒化过程中污泥特性以及污染物去除效果的变化,以期为好氧颗粒污泥培养技术提供理论依据。
全文HTML
-
1)接种污泥。实验所用接种污泥取自广州市猎德污水处理厂四期二沉池的回流污泥,接种前曝气24 h,接种污泥体积为3.7 L。接种污泥为絮状,灰褐色,含水率为99.14%,沉降速度为12.36 m·h−1、SVI30为110.7 mL·g−1、MLSS为7 588 mg·L−1、MLVSS/MLSS为0.41。
2)实验用水。进水水质采用人工配制的模拟废水,以葡萄糖和乙酸钠为混合碳源,用NaHCO3 调节进水pH为7.5左右,并向进水添加1 mL·L−1的微量元素溶液。模拟废水组成:葡萄糖为500~1 200 mg·L−1、乙酸钠为300~600 mg·L−1、NH4Cl为40~90 mg·L−1、KH2PO4为8~18 mg·L−1、CaCl2为100 mg·L−1、MgSO4·7H2O为30 mg·L−1、FeSO4·7H2O为30 mg·L−1、EDTA为20 mg·L−1。微量元素溶液组成:FeCl3·6H2O为500 mg·L−1、CuCl2·2H2O为30 mg·L−1、MnCl2·4H2O为120 mg·L−1、ZnCl2·6H2O为120 mg·L−1、H3BO3为150 mg·L−1、KI为30 mg·L−1、Na2MoO4·2H2O为60 mg·L−1、CoCl2·6H2O为150 mg·L−1。
-
1)实验装置。好氧颗粒污泥培养采用SBR,反应器主体是由有机玻璃制成的圆柱体,其内径D为9.8 cm,总高度为 100 cm,有效高度H为98 cm,有效高径比(H∶D)为 10,反应器有效容积为 7.39 L,实验装置如图1所示。SBR运行过程包括进水、曝气、沉淀、排水和闲置5个阶段,各阶段均通过时间控制器进行全自动控制。
2)运行方式。在污泥颗粒化过程中,以有机污染物浓度,表面上升气速和污泥沉降时间为主要调控参数,各阶段进水碳、氮和磷的质量浓度比控制在130∶10∶1~100∶5∶1,SBR运行周期为6 h,其中包括进水4 min、曝气338~351 min、沉淀2~15 min、排水1 min、闲置2 min,SBR排出比为0.5。采用水浴加热的方法使反应器温度控制在25 ℃。SBR运行的具体参数如表1所示。
-
MLSS、MLVSS、SVI30、含水率、COD、TN、TP等均采用标准方法[12]测定,粒径分布采用湿式筛分法[13]确定,污泥沉降速度采用重力沉降法[14]测定,利用生物显微镜(BK 500 奥特光学)观测好氧颗粒污泥形态变化。好氧颗粒污泥微观形貌和组成元素采用FIB-SEM双束电镜(LYRA 3 XMU)观察和分析。EPS采用热提取法[15],EPS含量由PN和PS含量之和表示,PS含量采用苯酚-硫酸法[16]测定;PN含量采用BCA分光光度法[17]测定。
1.1. 接种污泥和实验用水
1.2. 实验装置和运行方式
1.3. 分析指标和分析方法
-
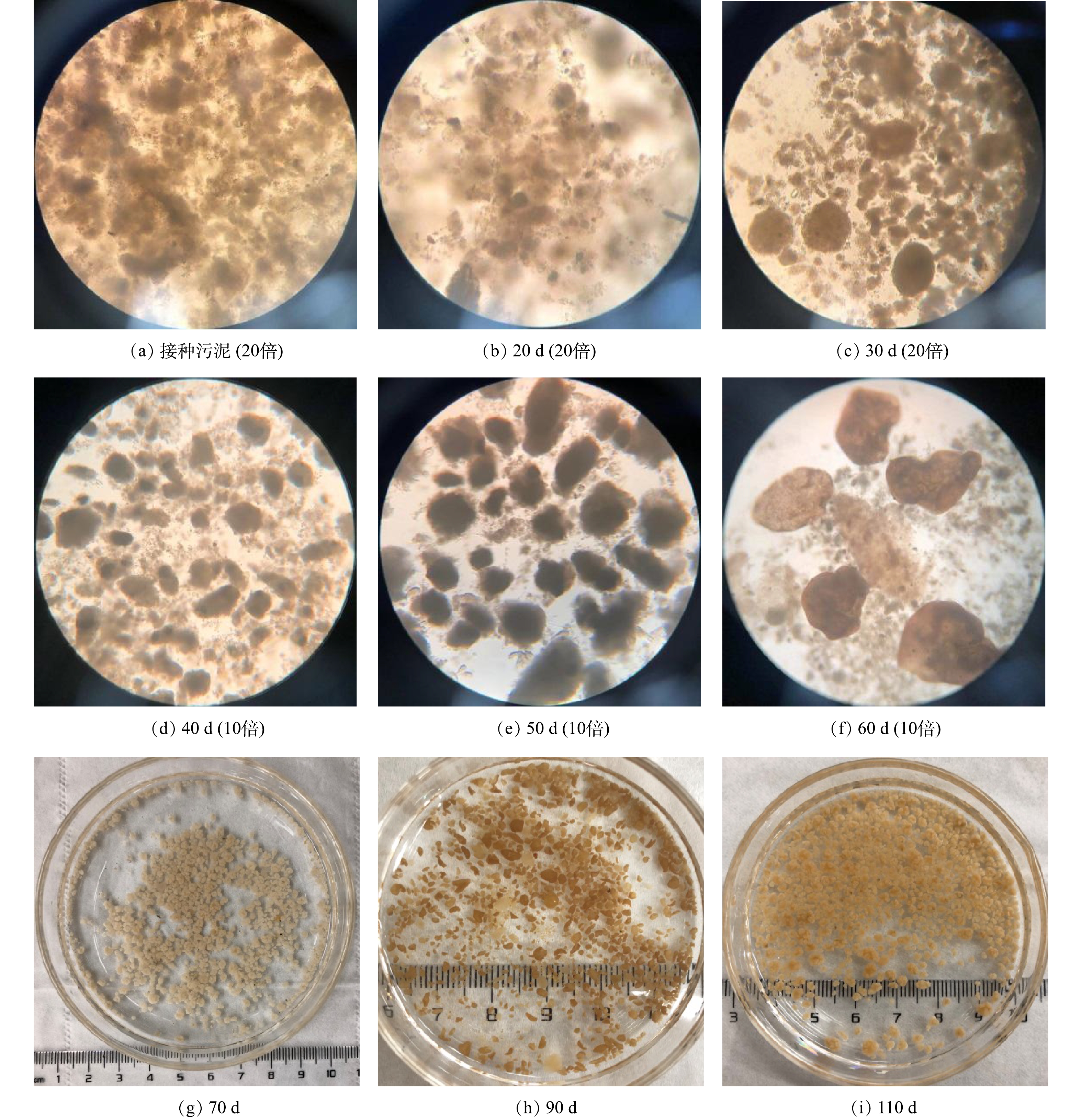
由图2可知,接种污泥外观为灰褐色、絮状,结构松散,SVI30为110.7 mL·g−1,沉降速度为12.36 m·h−1,MLVSS/MLSS仅为0.41。当SBR运行30 d后,出现少量细小的污泥颗粒,但絮状污泥占主体。第50天,初期好氧颗粒污泥形成,粒径较小,主要呈现椭球状或棒状,SVI30下降为41.66 mL·g−1,沉降速度增大到35.74 m·h−1,MLVSS/MLSS为0.57。随着SBR内选择压不断增强,沉降性能较差的颗粒污泥被筛选出反应器,第70天,好氧颗粒污泥外观呈淡黄色,表面有一层绒毛,颗粒粒径主要集中在1~1.5 mm。第110天,好氧颗粒污泥为橙黄色,外形较为光滑,整体呈球状或椭球状的立体结构,大多数颗粒粒径分布在1.43~2.26 mm,SVI30为28 mL·g−1,沉降速度为94 m·h−1,MLSS达到17 400 mg·L−1,MLVSS/MLSS为0.72,以上测定结果标志着好氧颗粒污泥培养成功。与其他研究结果[18]相比,该实验培养得到的好氧颗粒污泥沉降性能、微生物量以及微生物活性均较高。
-
好氧颗粒污泥微观形貌如图3所示。由图3(a)可知:好氧颗粒污泥呈球状结构,外表面具有褶皱和空隙。由于表面褶皱的存在,好氧颗粒污泥比活性污泥具有更大的比表面积,因此更有利于与水体中有机物充分接触,从而增强了对有机污染物的去除效果。此外,好氧颗粒污泥表面的空隙是溶解氧和营养物质渗透到颗粒污泥内部的通道[19]。颗粒表面的微生物以球菌和丝状菌为主,同时还存在少量杆菌和钟虫(图3(b)~图3(e))。球菌呈密集的生长状态(图3(b)),丝状菌相互交联,形成类似网状结构(图3(c))。有研究[20]发现,丝状菌不仅能通过缠绕、连接等作用强化颗粒结构,而且可以消除细菌代谢产物在颗粒内部的积累从而可提高好氧颗粒污泥的结构稳定性。
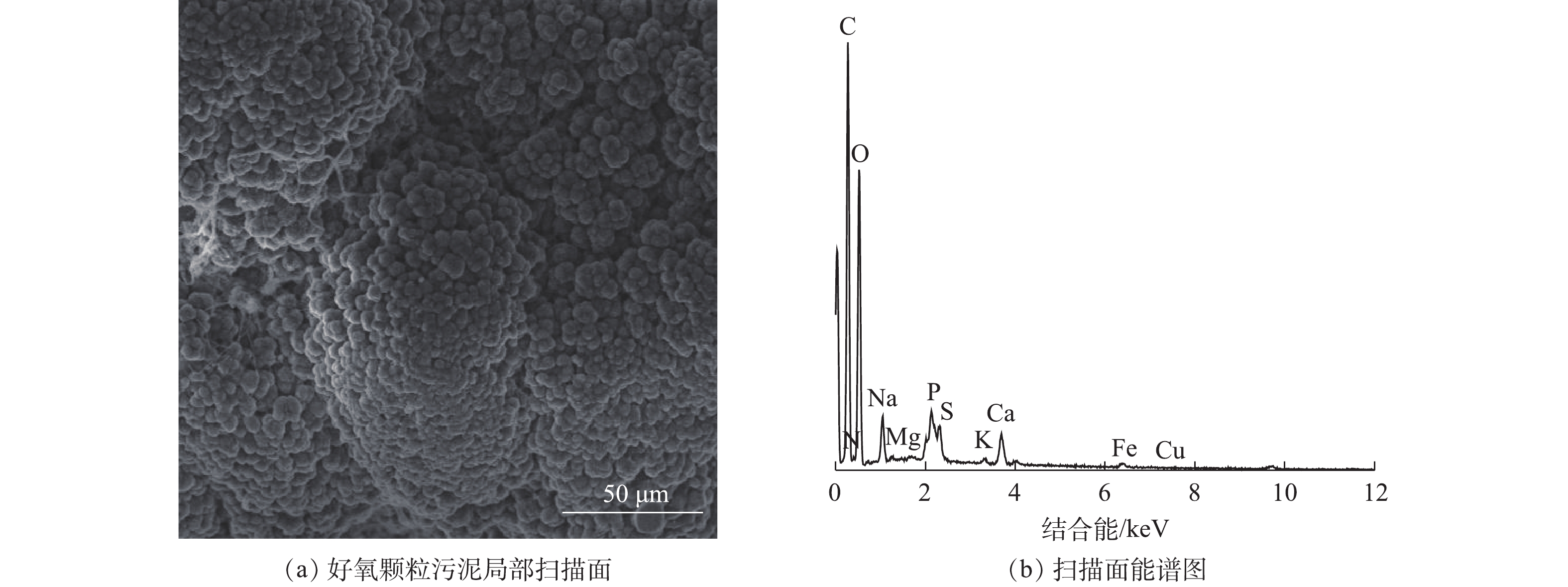
图4为好氧颗粒污泥局部扫描电镜图像及其面能谱图,扫描结果见图4(a)和图4(b)。其对应的组成元素分析结果如表2所示。由能谱分析结果发现,好氧颗粒污泥中碳元素的质量分数和原子个数比分别达到50%和60%以上,氧元素的质量分数和原子个数比分别达到39%和34%以上,说明颗粒污泥中的元素主要是碳和氧,同时好氧颗粒污泥还含有少量其他元素,如N、Na、Ca、P、S等。
-
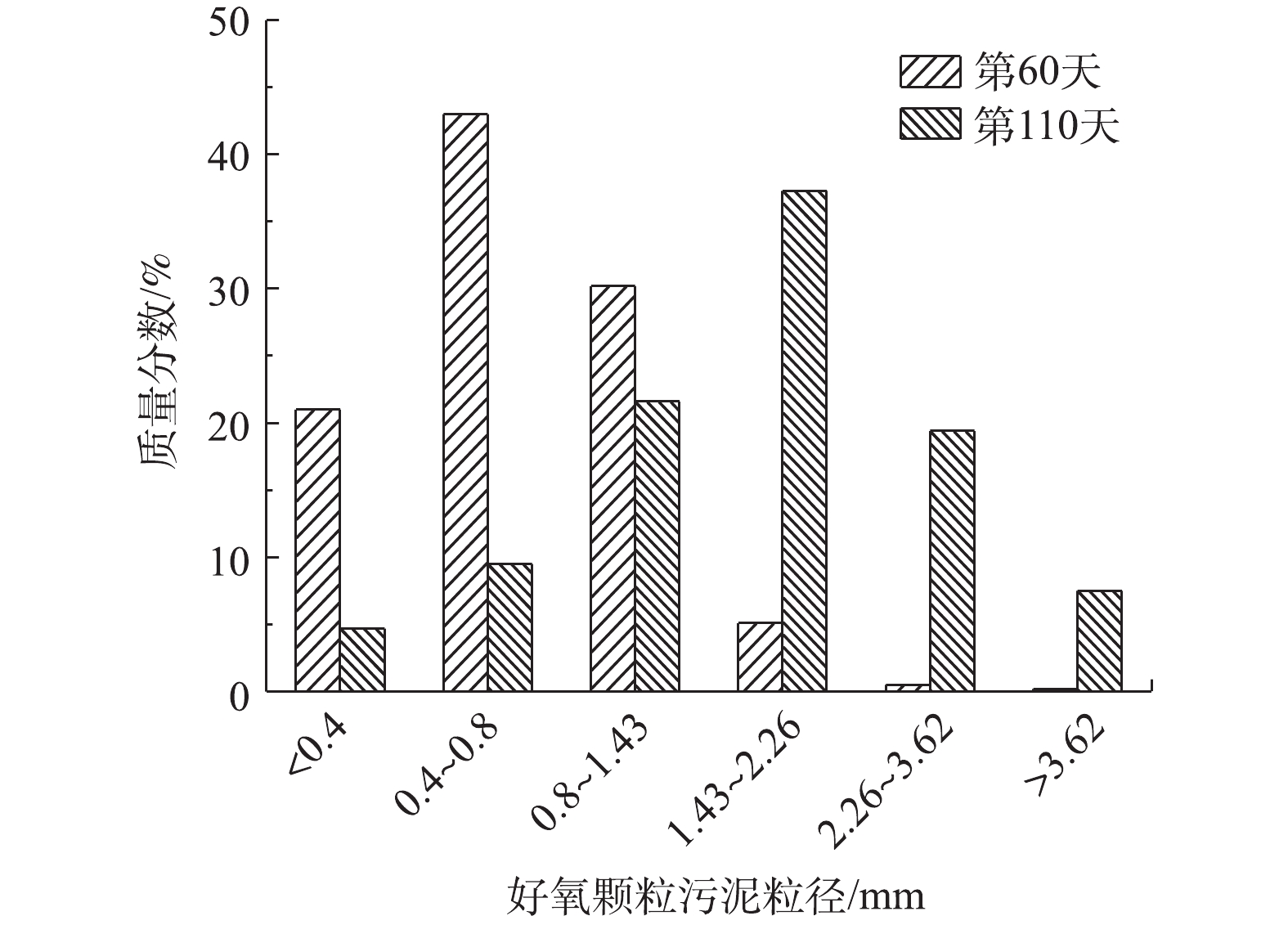
1)好氧颗粒污泥粒径分布变化。如图5所示,第60天,初期好氧颗粒污泥已经形成,其颗粒粒径主要集中在0.4~1.43 mm。随着实验不断进行,第110天,SBR中的好氧颗粒污泥粒径主要分布在1.43~2.26 mm,其质量分数为37%。粒径分布在0.8~3.62 mm的好氧颗粒污泥质量分数为88%,而粒径<0.4 mm和粒径>3.62 mm的好氧颗粒污泥质量分数均不足8%,结合图3(a)可知,SBR中的污泥呈球状立体结构,基本无絮状污泥存在,说明好氧颗粒污泥培养成功且可实现泥水分离。
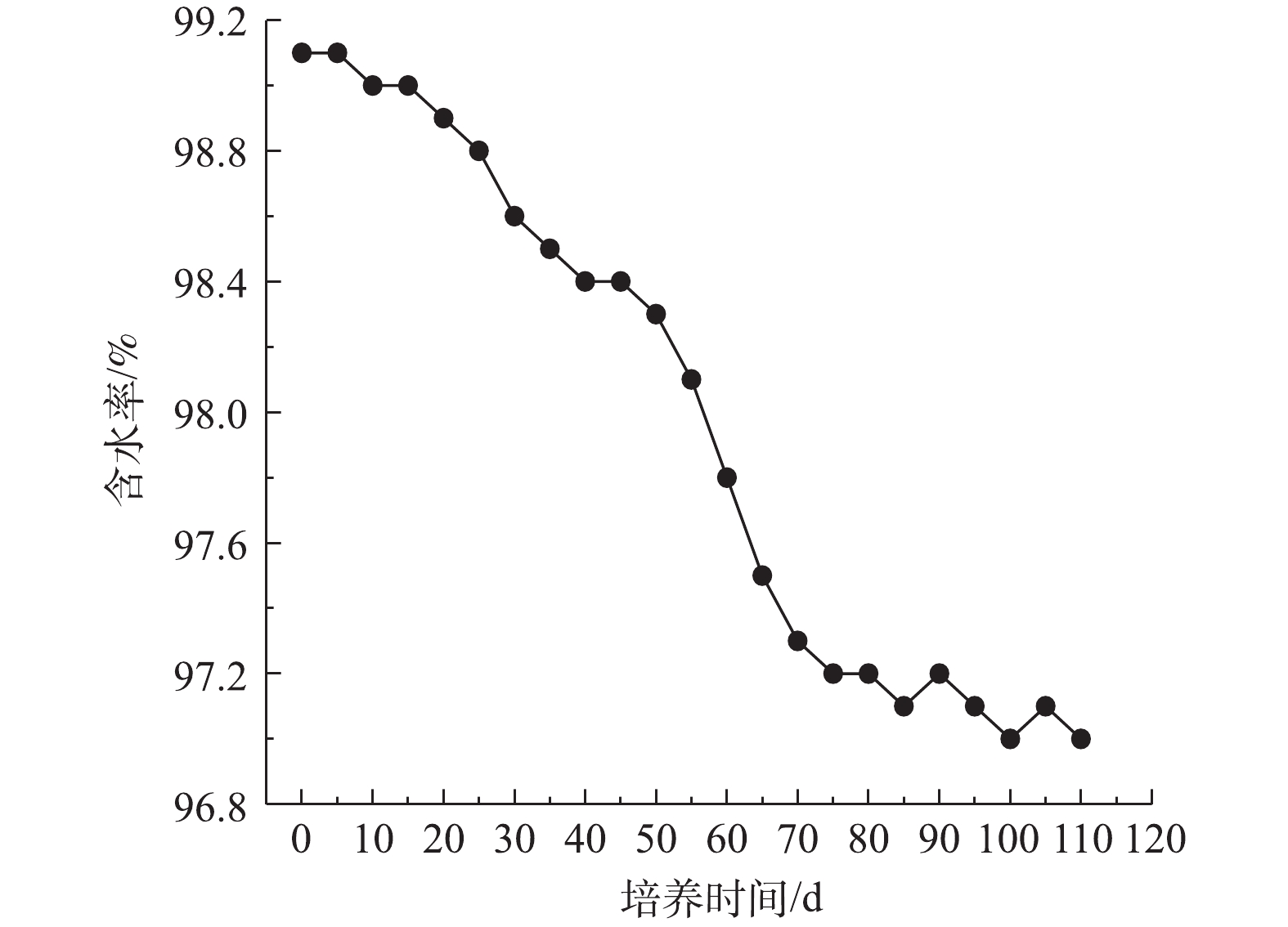
2)好氧颗粒污泥含水率变化。污泥含水率是表征污泥物理性状的一个重要参数。污泥颗粒化过程中污泥含水率随时间变化情况如图6所示。接种污泥含水率为99.14%,在SBR启动初期,因为在曝气状态下接种污泥受到剪切力的作用,污泥原始状态受破坏;此外,污泥沉降时间受到限制(沉降时间为15 min),所以大量沉降性较差的污泥被排出反应器。随着颗粒化逐渐推进,微生物细胞逐渐生长促进污泥间的凝聚,使污泥中的间隙水减少,导致含水率逐渐下降。第50天,由于初期好氧颗粒污泥形成,大量微生物菌群聚集成团,颗粒污泥密实性增加,因此颗粒污泥含水率明显下降。好氧颗粒污泥逐渐趋于成熟状态,其含水率基本维持在较稳定水平。最后培养得到的好氧颗粒污泥含水率为97%。
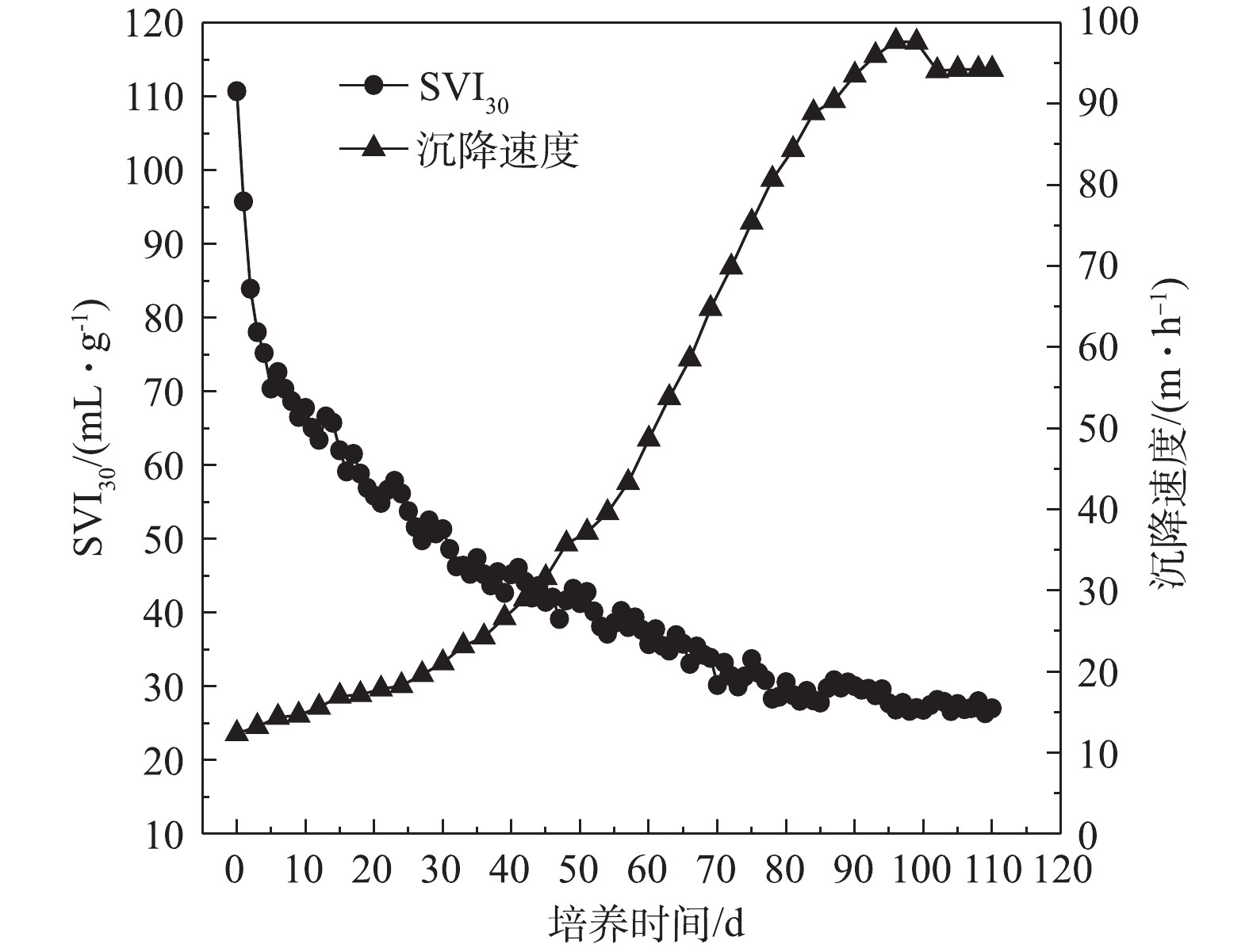
3)好氧颗粒污泥沉降性能和沉降速度变化。由图7可知,接种污泥SVI30为110.7 mL·g−1,沉降性能较差。随着反应器的运行,颗粒化程度不断增加,污泥沉降性能也在不断提升,SVI30不断下降。随着污泥颗粒化的完成,SVI30为28 mL·g−1,远低于普通絮状污泥。接种污泥沉降速度为12.36 m·h−1,好氧颗粒污泥培养初期,污泥沉降速度呈缓慢增大的趋势。第40天,好氧颗粒污泥沉降速度显著增加,最后沉降速度为94 m·h−1。以上表明培养出的好氧颗粒污泥结构密实,沉降性能良好。
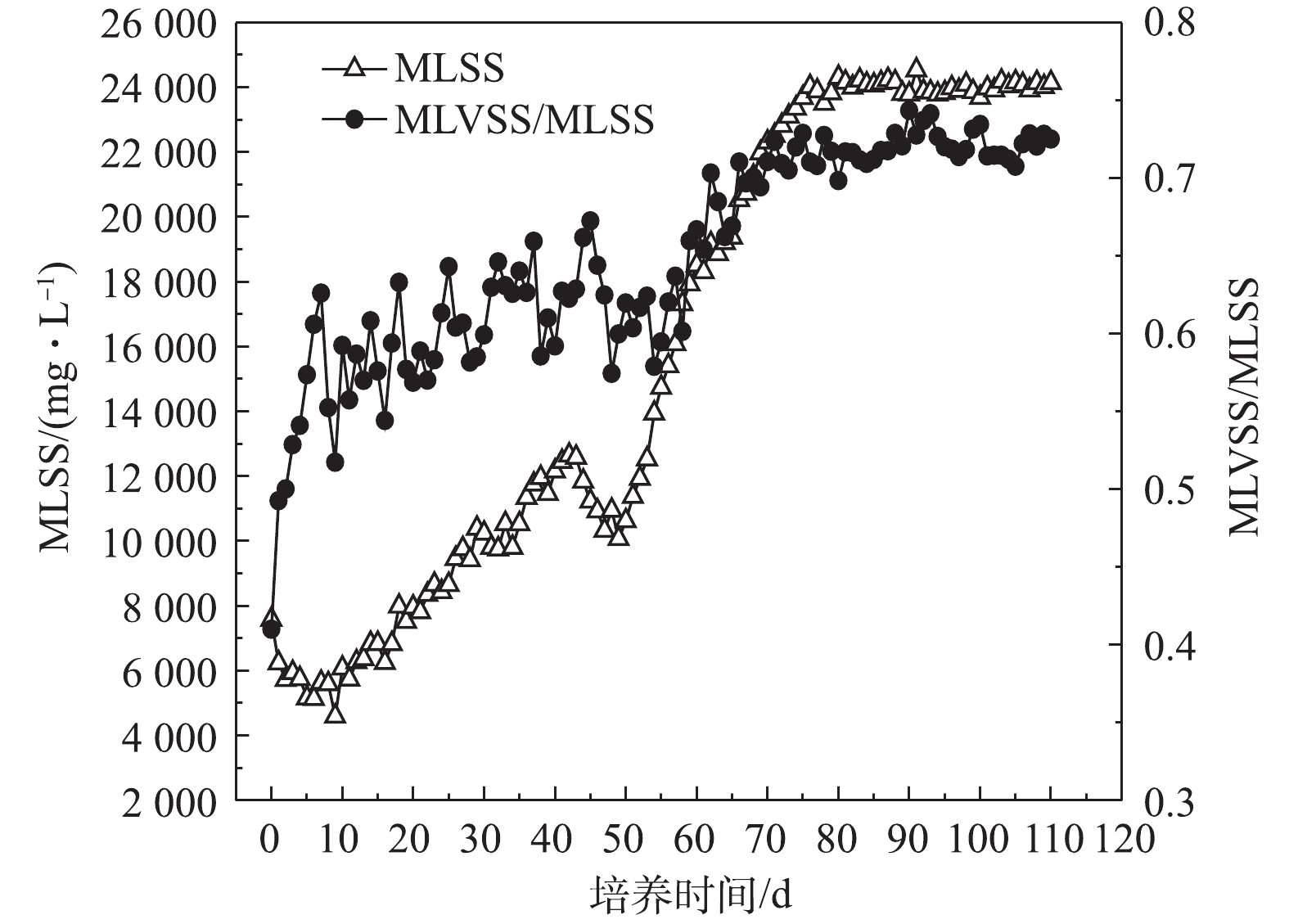
4) MLSS和MLVSS/MLSS变化。MLVSS/MLSS代表污泥中有机固体的比例,表示污泥内部活性微生物量,MLVSS/MLSS越大说明微生物量越高。污泥颗粒化过程中的MLSS和MLVSS/MLSS变化情况如图8所示,接种MLSS为7 588 mg·L−1,在SBR启动初期,污泥沉降时间突然缩短,大量松散絮状污泥被排出反应器,MLSS显著下降。随着接种污泥对进水水质和SBR运行方式的适应,污泥开始逐渐生长,在第20天达到7 990 mg·L−1,超过接种时水平。第44 天,可能是因为颗粒污泥尚未形成,表面上升气速的增加促使粘附在污泥微团表面的污泥进一步被剥落,所以MLSS呈下降趋势。随着SBR的连续运行,第50天,初期好氧颗粒污泥形成,污泥不断颗粒化,好氧颗粒污泥量开始增加,MLSS明显上升,在第87天达到24 232 mg·L−1。当好氧颗粒污泥逐渐趋向成熟,MLSS基本保持在稳定水平。经SBR运行110 d后,培养出的好氧颗粒污泥MLSS为24 140 mg·L−1,约为接种时的3.2倍,说明好氧颗粒污泥具有较高的微生物浓度。接种污泥的MLVSS/MLSS仅为0.41,反映出其内部活性微生物量很少。在整个污泥颗粒化过程中,MLVSS/MLSS整体处于缓慢上升趋势。随着好氧颗粒污泥趋向成熟,SBR运行状态稳定,MLVSS/MLSS值变化不大,基本维持在0.72,说明好氧颗粒污泥微生物量较高。
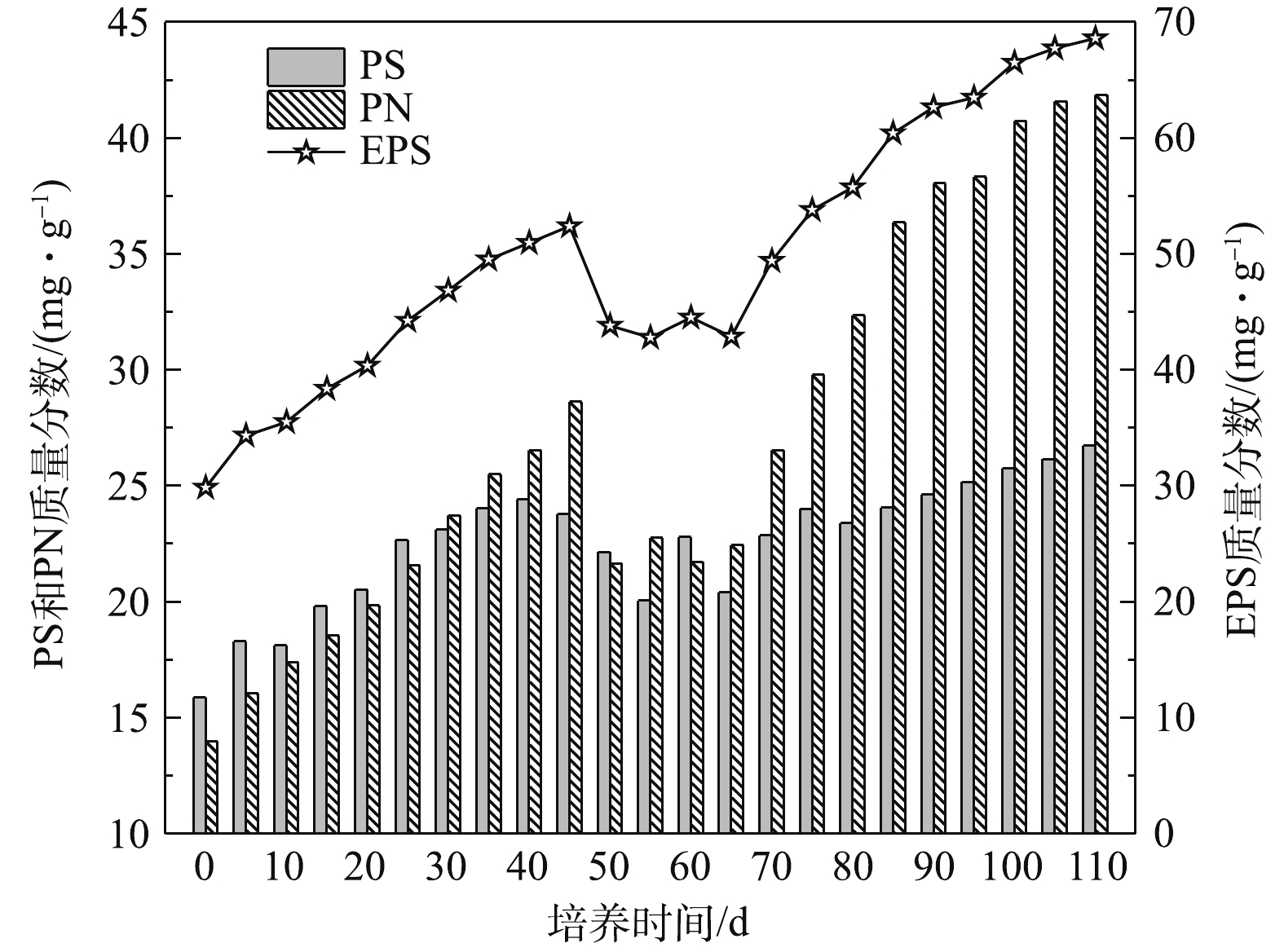
5)污泥颗粒化过程中EPS、PN和PS质量分数变化。如图9所示,接种污泥EPS质量分数为29.86 mg·g−1,其中PN和PS质量分数分别为13.98 mg·g−1和15.88 mg·g−1。在SBR运行初期,EPS、PN和PS含量均缓慢增加,但PS含量略高于PN含量,这是因为污泥内微生物在新环境刺激下需要分泌大量胞外多糖维持正常的生命活动[21]。随后由于沉降时间缩短,表面上升气速和有机污染物浓度提高,SBR内的选择压增强,打破了污泥中微生物细胞间信息交流的动态平衡,使微生物的新陈代谢活动受到抑制,因此EPS、PN和PS含量开始出现短时间的下降趋势。第70天SBR中的污泥以颗粒污泥为主,微生物量提高,EPS和PN含量开始显著增加,而PS含量没有明显波动。随着污泥颗粒化的完成,EPS、PN和PS含量逐渐趋于稳定。第110天的好氧颗粒污泥EPS和PN质量分数分别为68.6 mg·g−1和41.86 mg·g−1,PS质量分数为26.74 mg·g−1,这表明污泥颗粒化与PN含量变化密切相关,而PS含量变化对污泥颗粒化影响不大。在整个污泥颗粒化过程中,EPS含量变化趋势与PN含量变化相一致,这与CHEN等[22]的研究结果相符合。
-
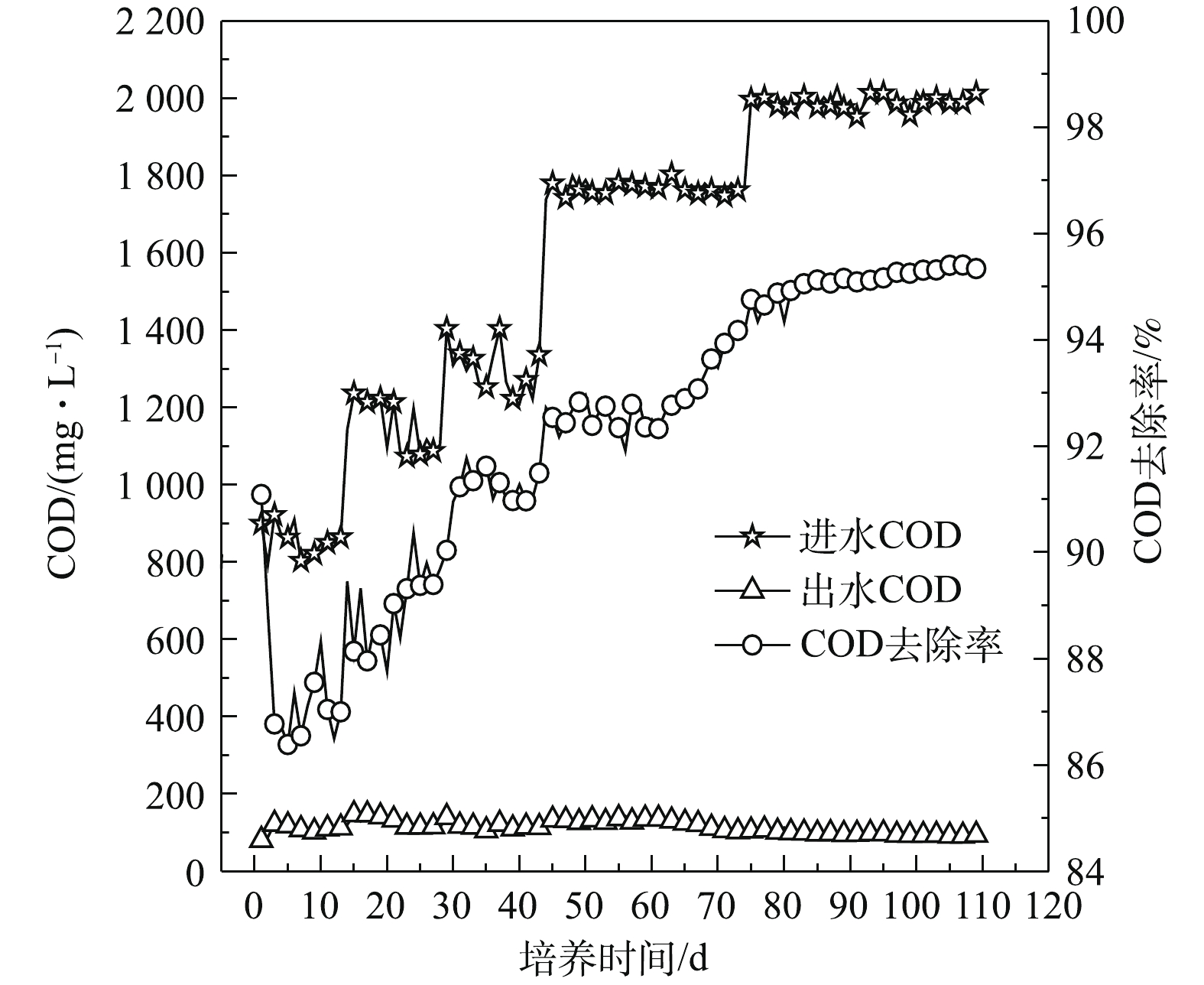
1)污泥颗粒化过程中COD去除效果。接种污泥曝气24 h 后污泥活性较大,对有机物的去除效果较好,如图10所示,第1天,反应器中的污泥对COD去除率为91.09%。随后因为接种污泥受到剪切力的作用,在沉降时间缩短的情况下,大量沉降性较差的絮状污泥被排出反应器,使MLSS和微生物量快速下降,所以在实验初期COD去除率明显下降。随着污泥内部微生物对反应器运行条件的逐渐适应,微生物量不断积累,MLSS开始增加,SBR的污泥颗粒化程度不断提高,因此,COD去除率有一定范围的波动,但整体随着进水COD值的提高在不断增大。第50天,初期好氧颗粒污泥形成,进水COD为1 764 mg·L−1,出水COD为126 mg·L−1,COD去除率达到92.83%。在好氧颗粒污泥培养后期,COD去除率逐渐趋于稳定,第110天,好氧颗粒污泥培养成功,反应器进水COD为1 989 mg·L−1,出水COD为90 mg·L−1,COD去除率为95%。
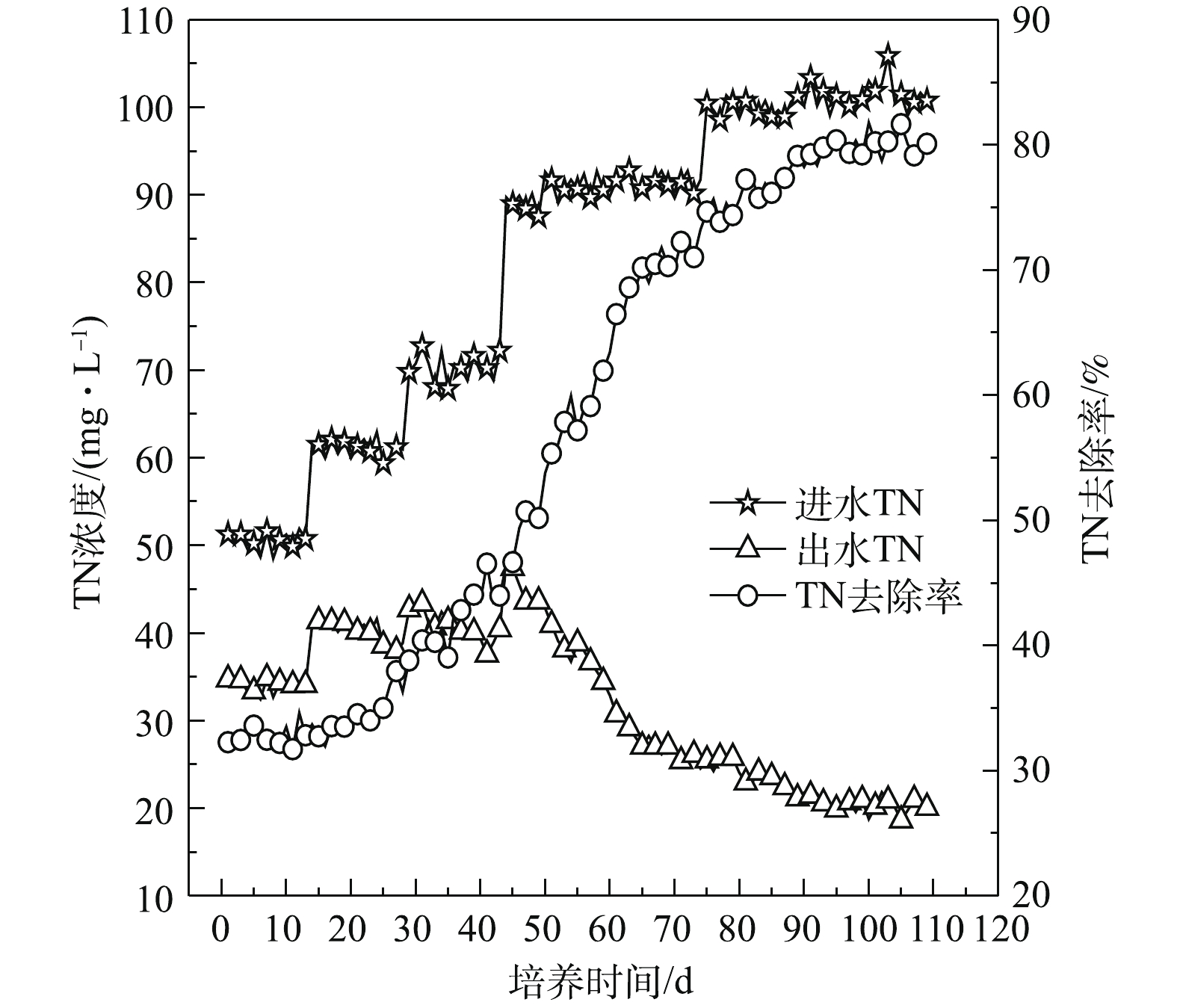
2)污泥颗粒化过程中TN去除效果。污泥颗粒化过程中TN去除效果如图11所示,SBR运行初期,进水TN浓度由最初的50 mg·L−1上升到60 mg·L−1,出水TN浓度随进水TN浓度而增加,TN去除率较低,仅为32%。一方面,因为刚接种污泥内微生物活性较低,对生存环境正处于适应阶段,仅靠微生物的同化作用将TN转化为自身细胞原生质成分;另一方面,又因为初期反应器以絮状污泥为主体,污泥颗粒化现象不明显,尚未形成同步硝化反硝化所需要的微环境[23-24],因此,TN去除率总体较低。之后TN去除率明显增加,出水TN浓度逐渐降低。随着反应器中颗粒污泥粒径不断增大,在第80天TN去除率为75%左右,出水TN浓度为25 mg·L−1。研究发现TN去除效果受颗粒污泥粒径的影响[25],这主要是因为随着颗粒污泥粒径不断增大,其内部因氧气传递的限制产生分层,分别在颗粒污泥表面和内部形成好氧环境和缺氧环境[26];硝化菌在颗粒表面发生硝化作用将
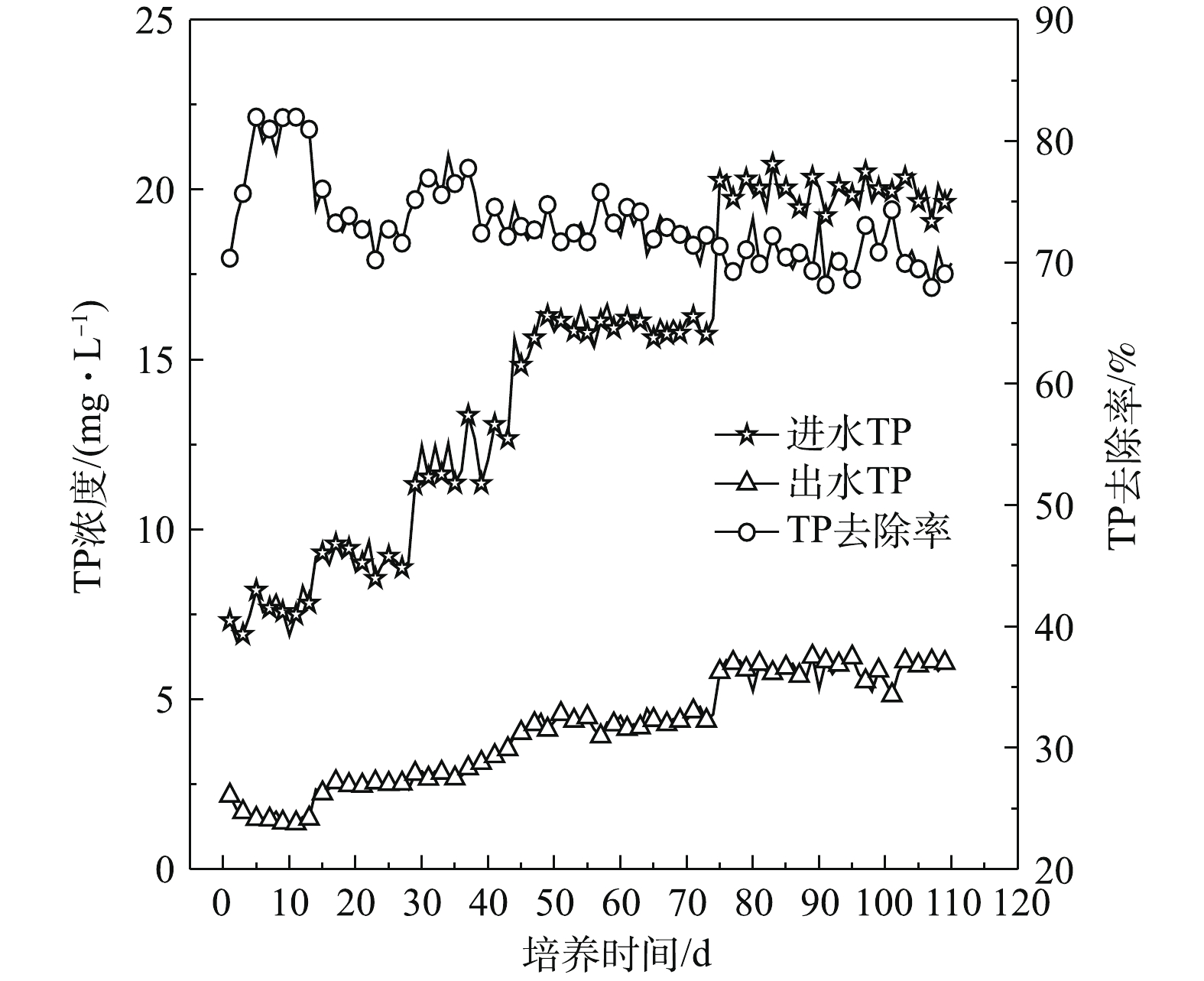
NH+4 -N氧化为硝态氮和亚硝态氮;反硝化菌在颗粒内部发生反硝化作用将进入的硝态氮和亚硝态氮还原成氮气,从而实现对N的去除[27]。当好氧颗粒污泥趋于成熟,硝化和反硝化作用逐渐稳定,出水TN浓度基本维持在20 mg·L−1,TN去除率稳定在80% 左右。王晓艳等[28]使用相同的混合碳源,通过逐步提高有机负荷和缩短沉降时间的方法培养得到的好氧颗粒污泥对TN的去除率为60%,出水TN浓度为40 mg·L−1,说明本实验的颗粒污泥对TN具有较好的去除效果。结合TN去除率整体变化规律可知,TN去除效果与污泥颗粒化程度密切相关,因此,实现更好的脱氮效果需要加快推进污泥颗粒化程度。3)污泥颗粒化过程中TP去除效果。图12为污泥颗粒化过程中TP去除效果。好氧颗粒污泥去除TP的实质是生物除磷,主要是利用污泥中聚磷菌一类的微生物从外部环境中磷的过剩摄取,并将磷以聚合的形态贮藏在微生物体内,形成高磷污泥,排出SBR,从而实现对污水中TP的去除。由于污泥接种前进行了曝气处理,聚磷菌可吸附污水中大量的磷,而且大量絮状污泥外排,所以TP去除率由最初的70.36%上升到81.99%,随后TP去除率开始下降。当反应器运行一段时间后,絮状污泥凝聚成团或细小颗粒,TP去除率又出现缓慢上升趋势。由于污泥颗粒化程度不断加大,大量沉降性能良好的颗粒污泥被截留在反应器内,污泥排出量越来越少。此阶段,由于污泥中的聚磷菌在好氧条件下,可以通过主动运输的方式将外部环境中的磷摄入体内,用于合成ATP,从而获得能量。因此在SBR实验阶段基本不排泥的情况下,由于好氧颗粒污泥量逐渐增大,对TP仍具有一定的去除效果。随着好氧污泥颗粒化的完成,TP出水浓度为5 mg·L−1, 去除率为70%。
2.1. 好氧颗粒污泥形成过程
2.2. 好氧颗粒污泥微观形貌和元素组成分析
2.3. 污泥颗粒化过程中污泥理化特性变化
2.4. 污泥颗粒化过程中污染物去除效果
-
1)在SBR中,经过110 d后,培养出致密的好氧颗粒污泥,颗粒粒径主要分布在1.43~2.26 mm,大量球菌和丝状菌附着在好氧颗粒污泥表面。好氧颗粒污泥主要是由碳和氧元素构成,此外还含有少量的金属元素。
2)好氧颗粒污泥SVI30为28 mL·g−1,沉降速度为94 m·h−1,含水率为97%,MLSS为17 400 mg·L−1,MLVSS/MLSS基本维持在0.72,具有较高的微生物量和微生物活性。
3)在污泥颗粒化过程中,PS含量没有明显波动,PN含量却明显增加,由13.98 mg·g−1增加到41.86 mg·g−1,且EPS含量的变化与PN含量变化趋势相一致,表明EPS中的PN含量在增加可促进对好氧颗粒污泥的形成。
4)好氧颗粒污泥具有较好的除污效果,对COD、TN、TP的去除率分别约为95%、80%、70%。





 下载:
下载: